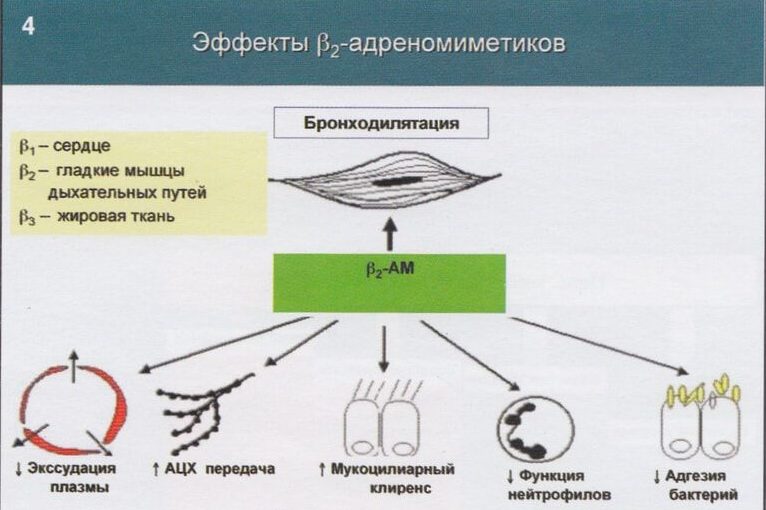
Исходя из патогенеза бронхиальной астмы, в борьбе с астматическими проявлениями применяют бронхорасширяющие средства и противовоспалительные препараты.
Адреномиметики при бронхиальной астме быстро снимают симптомы удушья. Следует помнить, что все бронхолитики обладают симптоматическим действием.
То, насколько часто они используются, будет индикатором эффективности основной, базисной терапии.
Итак, адреномиметики — обширная группа лекарственных средств, оказывающих стимулирующее воздействие на адренорецепторы. Адренорецепторы локализуются во всех тканях организма — они встроены в клеточные мембраны, представляют собой особые белковые молекулы.
Эффект адреномиметиков определяется воздействием на рецепторы, что приводит к определенным метаболическим изменениям. В итоге может возникать спазм или расширение сосудов и т. д.
Адреномиметики оказывают стимулирующее воздействие на адренорецепторы, подобное действию адреналина и норадреналина. Когда молекула агониста соединяется с рецептором на поверхности клетки, происходит взаимодействие с регуляторным белком.
Этот белок способствует активации особого фермента, стимулирующего синтез аденозинмонофосфата — вещества, участвующего в передаче сигналов в клетке. Вследствие этого в клетке происходят определенные химические процессы, в результате которых изменяется концентрация кальция.
На этот процесс реагирует гладкая мускулатура различных органов, расслабляясь или сокращаясь.
Эффект действия препаратов зависит от типа рецепторов, на которые осуществляется воздействие.
Хотя адренорецепторы бывают 5 типов, мы остановимся только на бета1- и бета2-адренорецепторах, раз речь идет об астме.
Итак, бета1-адренорецепторы локализованы в сердце, и их стимулирование приводит к увеличению ЧСС, повышению артериального давления. Также они находятся в почках.
Бета-2-адренорецепторы локализуются в бронхах, скелетной мускулатуре, сосудах, сердце и других органах. Эффектом их стимуляции будет расслабление гладкой мускулатуры бронхов, снятие спазма, расширение просвета бронхиального дерева.
При астме адреномиметики оказывают симптоматический эффект и используются для купирования и предотвращения приступов.
Адреномиметики, применяемые при бронхиальной астме, разделяются на селективные и неселективные. Первые характеризуются тем, что воздействуют только на бета2-рецепторы, а вторые и на бета1, и на бета2.
При бронхиальной астме бета-агонисты должны воздействовать именно на бронхиальные бета2-рецепторы. Бета2-адреномиметики бывают длительного и короткого действия. Первые обладают пролонгированным эффектом и помогают предупредить ночные приступы, а вторые применяют в качестве средств против обострения астмы.
Следует обратить внимание на то, что адреномиметики, будь то селективные или неселективные, используют только по назначению врача. Если речь идет о адреномиметиках короткого действия, то это экстренные средства, которые ни в коем случае не следует применять бесконтрольно.
Они дают хороший терапевтический эффект, однако могут вызывать побочные явления – аритмию, гипертонический криз или гипотонию и многое другое. Пациентам с сахарным диабетом, артериальной гипертензией, атеросклерозом сосудов головного мозга, заболеваниями щитовидной железы применять такие средства рекомендуется с осторожностью, в той дозе и с той частотой, которую определил врач.
Бета-адреномиметики при бронхиальной астме используются как селективные, так и неселективные. Назначаются селективные адреномиметики короткого действия в форме аэрозоля, что позволяет быстро снять симптомы бронхиальной астмы.
Если ребенок не может в силу возраста использовать ингалятор, применяют специальные приборы для распыления лекарственного раствора — небулайзеры. Дозы препаратов для ингаляции при помощи небулайзера выше.
В больших дозах могут активировать бета1-адренорецепторы, альфа-адренорецепторы в сосудах. Неселективные возбуждают эти рецепторы в любых дозах. С этим связаны побочные эффекты — повышение артериального давления, увеличение ЧСС.
Некоторые селективные антагонисты бета-адренорецепторов:
Как было отмечено выше, бета-адренометики при бронхиальной астме применяют в комбинации с глюкокортикоидами и другими средствами. К средствам длительного действия относят, например, формотерол.
Длительный эффект связан с накоплением вещества в мембранах гладкомышечных клеток. При комбинации с глюкокортикоидами усиливают эффект гормонов, позволяют снизить их дозировку и, соответственно, уменьшить побочные эффекты при использовании для предотвращения ночных приступов, а также проявлений астмы физического напряжения.
Эти препараты не могут использоваться для монотерапии и в качестве экстренных средств для купирования удушья. Также следует избегать резкой отмены таких препаратов.
При применении оптимальных доз адреномиметиков короткого действия бета1-адренорецепторы миокарда практически не стимулируются.
В эту группу входят следующие препараты:
При приступе удушья адреномиметики короткого действия быстро купируют обострение — при ингаляционном введении эффект наблюдается уже спустя четыре минуты и длится на протяжении нескольких часов. Также они применяются для предупреждения проявлений астмы физического усилия.
Препараты этой группы не подходят для профилактического лечения — это средства экстренной помощи, которые действуют непродолжительное время. При частом использовании их эффективность может уменьшиться. Регулярное применение сальбутамола приводит к учащению приступов астмы физического усилия и увеличивает выраженность воспаления.
Для правильного введения лекарства при помощи ингалятора необходимы соответствующие навыки. В противном случае в бронхиальное дерево попадет меньше лекарства, чем требуется.
Неселективные адреномиметики при бронхиальной астме
Стимулируют бета1-, бета2-, альфа-адренергические рецепторы. При бронхиальной астме применяют следующие неселективные адреномиметики:
Как было отмечено выше, неселективные адреномиметики оказывают активное воздействие на сердечно-сосудистую систему даже в небольших дозах, провоцируют повышение артериального давления.
Важно, что для поддержания нормального качества жизни оптимален ступенчатый подход к использованию препаратов, который предполагает повышение доз и увеличение количества приемов по мере усугубления заболевания. Главная цель — контролировать астму, принимая минимальные дозы лекарств.
Если состояние пациента ухудшается, доза и частота приема увеличивается. Если астма хорошо поддается контролю, то доза и частота приема уменьшается. Чтобы перейти с одной ступени на другую, необходимо хорошо контролировать заболевание в течение определенного времени.
Цель лечения — поддерживать нормальное качество жизни, сохранять привычную физическую активность.
Прогноз бронхиальной астмы во многом зависит от того, выполняет ли пациент все предписания, которые касаются как схемы приема препаратов, так и общих правил, знания различий между препаратами базисной и неотложной терапии, профилактических мер.
Даже в период ремиссии в дыхательных путях сохраняется воспалительный процесс, но это не означает, что достичь хорошего самочувствия невозможно. Не стоит надеяться лишь на лекарственные средства: необходимо исключать контакты с аллергенами, соблюдать элиминационные диеты и в целом бережно относиться к своему здоровью.
источник
Автор: Синицкий В.А. · Опубликовано 2018/01/13 · Обновлено 2018/01/14
Адреномиметики при бронхиальной астме разделяют на селективные (активируют исключительно бета-2 рецепторы) и неселективные (активируют бета-1 и бета-2 рецепторы). Активация бета-2 адренорецепторов способствует расслаблению гладкой мускулатуры бронхов и приводит к их расширению.
Адреномиметики при бронхиальной астме должны стимулировать именно бронхиальные бета-2-адренорецепторы, что приводит к активации аденилатциклазы и повышению уровня циклического аденозинмонофосфата (ц-АМФ) в гладкой мускулатуре бронхов. Помимо этого, адреномиметики слегка препятствуют высвобождению медиаторов бронхоспазма из тучных клеток. Что немаловажно при лечении бронхиальной астмы. Читайте подробнее на нашем сайте про другие адреномиметики.
Селективные адреномиметики в больших дозах помимо активации бета-2 рецепторов в бронхах, могут также активировать бета-1 рецепторы в сердце и альфа-адренорецепторы в сосудах. Основные побочные эффекты адреномиметиков, такие как повышение АД, тахикардия, связаны именно с этими рецепторами. Поэтому предпочтительнее принимать селективные, нежели неселективные адреномиметики при бронхиальной астме (о которых будем говорить ниже). Так как селективные возбуждают их только в больших дозах, а неселективные – в любых.
Селективные адреномиметики при бронхиальной астме назначаются в дозированных аэрозольных ингаляторах.
Небулайзеры применяются только у тех пациентов, которые не могут правильно использовать ингалятор (у детей)
Частицы адреномиметиков, которые вдыхаются через небулайзер в 3-4 раза больше, чем аэрозольные, поэтому дозы этих препаратов в небулайзерах, соответственно, в 3-4 раза в больше. Селективные адреномиметики при бронхиальной астме подразделяются на препараты длительного и короткого действия.
Основными препаратами, которые относятся к селективным адреномиметикам длительного действия (12 часов и более), являются:
Препараты характерны высокой липофильностью, что способствует их накоплению в мембранах гладкомышечных клеток. Благодаря этому обеспечивается длительность действия. Эту группу лекарственных средств чаще всего применяют при бронхиальной астме. А именно:
- в комбинациях с ингаляционными глюкокортикоидами, когда последние оказывают недостаточный эффект (например при появлении ночных приступов астмы);
- в комбинациях с глюкокортикоидами с целью снизить их дозу и этим избежать побочных эффектов;
- для профилактики приступов астмы физического усилия.
Такие ограничения в применении препаратов данной группы обоснованы повышением риска смерти от бронхиальной астмы. Селективные адреномиметики длительного действия нельзя резко отменять и использовать для монотерапии бронхиальной астмы, а также для купирования ее приступов.
Кленбутерол является препаратом допинга для спортсменов, так как обладает анаболическим эффектом.
Основные представители селективных адреномиметиков короткого действия (эффект длится 3-4 часа):
- тербуталин,
- фенотерол (беротек),
- сальбутамол (альбутерол),
- левалбутерол,
- битолтерол,
- метапротеренол (алупент),
- пирбутерол.
Препараты этой группы оказывают сильный, быстрый (в течение 5 минут) и кратковременный (3-4 часа) эффект. Селективные адреномиметики короткого действия являются самыми эффективными препаратами для купирования приступа бронхиальной астмы. Адреномиметики при бронхиальной астме применяются в форме аэрозоля, для того чтобы избежать системных побочных эффектов. При применении подкожно тербуталин может заменить эпинефрин (который относится к неселективным адреномиметикам, о нем читайте ниже) для купирования тяжелых приступов бронхиальной астмы.
Применение данной подгруппы для профилактики приступов бронхиальной астмы не рекомендовано, так как:
- они действуют кратковременно,
- при длительном применении может развиваться устойчивость к их бронхолитическому действию,
- повышается риск развития побочных эффектов.
К неселективным адреномиметикам при бронхиальной астме (активируют бета-1 и бета-2 рецепторы) относятся:
- изопреналин (изопротеренол, изадрин),
- эпинефрин (адреналин),
- эфедрин.
Препараты данной группы в настоящее время при лечении бронхиальной астмы применяются редко, так как чрезмерно сильно стимулируют сердечно-сосудистую систему посредством активации альфа и/или бета-1 адренорецепторов. Неселективные адреномиметики при бронхиальной астме оказывают следующие наиболее частые побочные эффекты:
- тахиаритмии,
- тремор,
- чувство тревоги,
- сердцебиение.
Врач общей практики. Автор 11 научных публикаций, нескольких внедрений в учебный и лечебный процессы. Призер республиканской научно-практической конференции молодых ученых.
источник
Препараты этой группы использовали при многих состояниях, но сегодня их основное применение — устранение бронхоспазма у больных с бронхиальной астмой и ХОЗЛ.
Адреналин стали впервые использовать в качестве бронходилататора в начале XX века. Эфедрин вошел в западную медицину в 1924 г., хотя в Китае он применялся до этого в течение нескольких тысяч лет (Chen and Schmidt, 1930). Следующим крупным шагом стала разработка в 1940-х гг. избирательного β-адреностимулятора изопреналина: появилась возможность применять при бронхиальной астме лекарственное средство, не обладающее а-адреностимулирущей активностью и соответствующими побочными эффектами. Наконец, были получены избирательные β2-адреностимуляторы — еще более ценные в терапевтическом отношении препараты. К их достоинствам относится высокая биодоступность при приеме внутрь, отсутствие а-адреностимулирущей активности и низкий риск побочных эффектов на сердечно-сосудистую систему.
Бета-адреностимуляторы применяют для повышения частоты и силы сердечных сокращений. Их хронотропное действие важно для экстренного купирования таких аритмий, как пируэтная тахикардия, резкая брадикардия и АВ-блокада (гл. 35), а инотропное — в ситуациях, когда важно повысить сократимость сердца. Клиническое применение препаратов этой группы рассматривается ниже.
Этот препарат (табл. 10.1) представляет собой мощный неизбирательный β-адреностимулятор с очень низким сродством к а-адренорецепторам.
Фармакологические свойства. На рис. 10.2 приведены изменения некоторых показателей гемодинамики, возникающие у человека в ответ на в/в инфузию изопреналина. ОПСС снижается, прежде всего за счет расширения мышечных сосудов, но также — почечных и брыжеечных сосудов. Диастолическое АД уменьшается, систолическое может оставаться прежним или повышаться, среднее — обычно снижается. Сердечный выброс повышается в связи с положительным инотропным и хронотропным эффектом изопреналина, с одной стороны, и со снижением посленагрузки — с другой. При введении изопреналина возможны сердцебиение, синусовая тахикардия и аритмии. У животных высокие дозы изопреналина вызывают некроз миокарда.
Изопреналин вызывает расслабление почти всех гладких мышц (особенно если они находятся в состоянии высокого тонуса), однако наиболее выражено его действие на бронхи и ЖКТ. Он предупреждает или устраняет бронхоспазм; кроме того, его эффект при бронхиальной астме может быть обусловлен и подавлением вызванного антигенами высвобождения гистамина и других медиаторов воспаления. Такое действие свойственно и избирательным β2-адреностимуляторам.
Фармакокинетика. Изопреналин легко всасывается при приеме внутрь или ингаляции в виде аэрозоля. Он инактивируется КОМТ — прежде всего в печени, но также и в других тканях. МАО на него действует слабо, а симпатическими нейронами он не захватывается в такой степени, как адреналин и норадреналин. В связи со всеми этими особенностями длительность действия изопреналина несколько больше, чем адреналина, но все равно невелика.
Побочные эффекты. Часто наблюдаются сердцебиение, тахикардия, головная боль, приливы. Возможны нарушения ритма сердца, особенно у больных ИБС.
Применение. Изопреналин применяют при экстренных состояниях для повышения ЧСС у больных с резкой брадикардию или полной АВ-блокадой — особенно как временную меру це ред установкой электрокардиостимулятора или при пируэтной тахикардии. При бронхиальной астме и шоке вместо изопреналина в настоящее время используют другие препараты (гл. 28)
По химической структуре добутамин сходен с дофамином, однако у него имеется крупный ароматический радикал при аминогруппе (табл. 10.1). Физиологические эффекты добутамина обусловлены его прямым действием на α- и β-адренорецепторы, а не повышением высвобождения норадреналина из симпатических окончаний и не влиянием на дофаминовые рецепторы. Вначале считали, что добутамин — это сравнительно избирательный β1-адреностимулятор, однако теперь доказано, что механизмы его действия сложнее. У молекулы добутамина имеется хиральный центр, и поэтому существуют его оптические изомеры. Используемый в клинике препарат представляет собой рацемическую смесь из лево- и правовращающего изомеров (Ruffolo et al., 1981): /-добутамин — мощный α1-адреностимулятор, способный вызвать резкое повышение АД (Ruffolo and Yaden, 1983V напротив, d-добутамин — мощный α1-адреноблокатор подавляющий реакцию на /-добутамин. Таким образом конечная реакция на добутамин обусловлена влиянием обоих изомеров на β-адренорецепторы; d-добутамин примерно в 10 раз более активный бета-адреностимулятор,чем /-добутамин. Бета-адреноблокирующей активностью,видимо, не обладает ни один из изомеров.
Фармакологические свойства. Сердечно-сосудистая система. Как уже говорилось, применяемый в клинике добутамин — это рацемическая смесь, и поэтому его влияния на сердечно-сосудистую систему складываются из эффектов обоих изомеров. В отличие от изопреналина, добутамин обладает более выраженным инотропным, чем хронотропным действием. Причина этого не известна. Возможно, дело в том, что ОПСС под действием добутамина не изменяется; не исключено также, что в инотропном эффекте добутамина участвуют α1-адренорецепторы. В дозах, оказывающих одинаковый инотропный эффект, добутамин меньше влияет на частоту разрядов синусового узла, чем изопреналин. На АВ- и внугрижелудочковое проведение оба препарата действуют одинаково.
Инфузия животным добутамина со скоростью 2,5— 15 мкг/кг/мин приводит к повышению сократимости миокарда и сердечного выброса. ОПСС меняется маловидимо, из-за того, что обусловленное α1-адренорецеп-торами сужение сосудов компенсируется опосредованным β2-адренорецепторами расширением (Ruffolo, 1987), При скоростях инфузии меньше 20 мкг/мг/мин ЧСС возрастает незначительно. Инфузия добутамина на фоне β-адреноблокаторов не вызывает повышения сердечного выброса, но приводит к росту ОПСС. Это еще раз подтверждает, что добутамин оказывает некоторое стимулирующее влияние на сосудистые α-адренорецепторы.
Побочные эффекты. У некоторых больных добутамин вызывает резкое повышение АД и ЧСС, требующее снижения скорости инфузии. Вероятность повышения АД выше у больных с артериальной гипертонией в анамнезе. Поскольку добутамин улучшает АВ-проведение, при мерцательной аритмии он может привести к чрезмерному повышению частоты сокращений желудочков. Для профилактики этого осложнения назначают, например, дигоксин. Иногда добутамин вызывает желудочковые экстрасистолы. Как и другие инотропные средства, он может привести к увеличению зоны инфаркта из-за повышения потребности миокарда в кислороде; это всегда надо учитывать при принятии решения о назначении добутамина. Не известно, насколько эффективно применять добутамин на протяжении более нескольких суток. Есть данные о развитии к нему устойчивости (Unverferth et al., 1980).
Показания и применение. Добутамин применяют коротким курсом при декомпенсированной сердечной недостаточности I после операций на сердце, на фоне тяжелой хронической сердечной недостаточности, при инфаркте миокарда. В таких случаях он повышает ударный объем и сердечный выброс, как правило, без выраженного увеличения ЧСС и существенных изменений АД и ОПСС (впрочем, как уже говорилось, у некоторых больных возможен резкий подъем ЧСС и АД). Данных о его влиянии на долгосрочный прогноз мало. При ИБС по строгим показаниям применяют добутаминовую стресс-ЭхоКГ (Madu et al. 1994): вызванная добутамином повышенная нагрузка на миокард позволяет выявить очаги нарушений.
Т1/2 добутамина составляет примерно 2 мин. Основные пути метаболизма — конъюгация и превращение в З-О-метилдобутамин. Эффект развивается быстро, поэтому насыщающая доза не нужна, а стационарная концентрация достигается через 10 мин после начала инфузии. Для повышения сердечного выброса обычно проводят инфузию со скоростью 2,5—10 мкг/кг/мин, хотя иногда требуется и большая скорость. В целом скорость и длительность инфузии индивидуальны и зависят от клинического состояния и параметров гемодинамики.
Некоторые из основных побочных эффектов, возникающих при назначении β-адреностимуляторов больным бронхиальной астмой, обусловлены стимуляцией β1-ад-ренорецепторов сердца. В связи с этим были разработаны препараты, действующие преимущественно на β2-адренорецепторы. Однако избирательность их не абсолютна, и в высоких дозах они действуют на оба подтипа β-адренорецепторов.
Еще один подход к повышению эффективности β2-адреностимуляторов при бронхиальной астме — это получение препаратов с меньшей скоростью метаболизма и большей биодоступностью при приеме внутрь (по сравнению с катехоламинами). Это достигается путем гидроксилирования в положениях 3 и 5 бензольного кольца или замены гидроксильной группы в положении 3 на иную группу. Так были получены орципреналин, сальбутамол и тербуталин. Все эти препараты не инактивируются КОМТ. Замены на крупные радикалы в аминогруппе катехоламинов приводят к повышению активности в отношении β-адренорецепторов, снижению активности в отношении а-адренорецепторов и уменьшению чувствительности к МАО (Nelson, 1982).
Наконец, для преимущественной стимуляции β2-адренорецепторов бронхов используют ингаляцию малых доз упомянутых препаратов в аэрозолях. Обычно это приводит к выраженному действию на данные рецепторы при очень низких сывороточных концентрациях препаратов (Newhouse and Dolovich, 1986). При этом в меньшей степени стимулируются β1-адренорецепторы сердца и β2-адренорецепторы скелетных мышц (активация последних приводит к тремору, что ограничивает прием препаратов внутрь).
Ингаляция β-адреностимуляторов обычно дает очень быстрый (в течение минут) эффект. Есть и препараты с замедленным действием, например сальметерол. При п/к введении бета-адреностимуляторов расширение бронхов также наступает быстро, но при приеме внутрь максимальный эффект может быть достигнут лишь через несколько часов. Действие ингалируемых препаратов зависит от попадания их в дистальные отделы дыхательных путей — что, в свою очередь, определяется размерами частиц и параметрами дыхания (скоростью воздушного потока на вдохе, дыхательным объемом, временем задержки дыхания, сопротивлением дыхательных путей и др.; Newhouse and Dolovich, 1986). Лишь 10% ингалируемых препаратов попадает в легкие, остальная часть заглатывается и затем всасывается из ЖКТ. Для эффективности ингаляционной терапии необходимо, чтобы больной был обучен правильно ее проводить. Многие же больные, особенно старики и дети, этого не умеют — часто из-за того, что недостаточное внимание уделяют их обучению (Kelly, 1985; Newhouse and Dolovich, 1986). В таких случаях могут помочь буферные насадки (гл. 28).
Считается, что основной механизм действия β-адреностимуляторов при бронхиальной астме — это активация бета-адренорецепторов бронхов, бронходилатация и снижение сопротивления дыхательных путей. Однако есть данные о том, что бета-адреностимуляторы подавляют также высвобождение лейкотриенов и гистамина из тучных клеток легких (Hughes et al., 1983), усиливают восходящий ток слизи, снижают проницаемость сосудов микроциркуляторного русла и, возможно, ингибируют фосфолипазу Ц (Seale, 1988). Вклад всех этих механизмов в терапевтический эффект p-адреностимуляторов уточняется, но уже сейчас ясно, что воспаление бронхов играет роль в их повышенной реактивности (гл. 28). Значит, важную роль в лечении бронхиальной астмы могут играть противовоспалительные средства (например, ингаляции глюкокортикоидов). Применение β-адреностимуляторов при этом заболевании подробнее рассматривается в гл. 28.
Орципреналин. Орципреналин, тербуталин, фенотерол — это резорцинолы, имеющие гидроксильные группы в положениях 3 и 5 бензольного кольца (катехолы — в положениях 3 и 4; см. табл. 10.1). Поэтому они устойчивы к КОМТ, и их биодоступность при приеме внутрь достаточно высока — 40%. Элиминация происходит путем конъюгирования с глюкуроновой кислотой и последующим выведением почками. Орципреналин считается избирательным β2-адреностимулятором, хотя эта избирательность у него, видимо, меньше, чем у сальбутамола и тербуталина. Эффект развивается через несколько минут и длится несколько часов после ингаляции. После приема внутрь эффект развивается медленнее, а длится 3—4 ч. Орципреналин используют при приступах бронхиальной астмы и для длительного лечения при ХОЗЛ (гл. 28).
Тербуталин. Это избирательный β2-адреностимулятор, используемый в качестве бронходилататора. Будучи производным резорцинола, он устойчив к КОМТ и поэтому эффективен при введении не только п/к и путем ингаляции, но и внутрь. После ингаляции или парентерального введения эффект развивается быстро; он длится в течение 3—6 ч после ингаляции. При приеме внутрь эффект может наступить лишь через 1—2 ч. Тербуталин используют при приступах бронхиальной астмы и для длительного лечения при ХОЗЛ. Препараты тербуталина для парентерального введения применяют в экстренных ситуациях при астматическом статусе (гл. 28).
Сальбутамол. Это также избирательный β2-адреностимулятор, по фармакологическим свойствам и показаниям сходный с тербуталином. Его вводят путем ингаляции или внутрь. При ингаляции он в пределах 15 мин вызывает значительное расширение бронхов, и его эффект длится 3—4 ч. Сальбутамол значительно меньше влияет на сердечно-сосудистую систему, чем изопреналин (при ингаляции в дозах, вызывающих одинаковое расширение бронхов).
Изоэтарин. Эго первый из бета2-адреностимуляторов, который начали широко применять при обструктивных заболеваниях легких. В то же время его избирательность меньше, чем более современных средств, и он, будучи катехоламином (табл. 10.1), метаболизируется КОМТ (хотя и устойчив к МАО). Поэтому его назначают только в ингаляциях для купирования острого бронхоспазма.
Пирбугерол. Это относительно избирательный β2-адреностимулятор, отличающийся отсальбутамола только заменой бензольного кольца на пиридиновое (Richards and Brogden, 1985). Его назначают в ингаляциях, обычно каждые 4—6 ч.
Битолтерол. Это новый β2-адреностимулятор, у которого катехоловые гидроксильные группы защищены от действия КОМТ путем этерификации с 4-метилбензоатом. Эстеразы легких и других тканей гидролизуют его до активной формы (колтерола, или тербутилнорадреналина; табл. 10.1). На животных показано, что в легких активность таких эстераз выше, чем в других тканях, например в сердце (Nelson, 1986; Friedel and Brogden, 1988). Длительность эффекта битолтерола после ингаляции составляет 3—6 ч.
Фенотерол. Эффект этого β2-адреностимулятора развивается после ингаляции быстро и длится 4—6 ч. В США он не выпускается. Данные о возможной связи приема фенотерола с повышенной смертностью от бронхиальной астмы, полученные в Новой Зеландии, противоречивы (Pearce et al., 1995; Suissa and Ernst, 1997).
Формотерол. Это препарат длительного действия: через несколько минут после ингаляции он вызывает выраженное расширение бронхов, сохраняющееся до 12 ч (Faulds et al., 1991). В этом его главное преимущество перед другими бета2 — адреностимуляторами — особенно при ночных приступах бронхиальной астмы. В США он не выпускается.
Прокатерол. Эффект этого β2-адреностимулятора развивается после ингаляции быстро и длится около 5 ч. В США он не выпускается.
Сальметерол. Это препарат длительного (около 12 ч) действия. Однако эффект его после ингаляции развивается сравнительно медленно, и поэтому для быстрого купирования приступов бронхиальной астмы он не подходит (Lotvall and Svedmyr, 1993; Brogden and Faulds, 1991).
Ритодрин. Этот избирательный β-адреностимулятор был разработан как средство для расслабления мускулатуры матки, однако по своим фармакологическим свойствам он во многом сходен с другими препаратами данной группы. При приеме внутрь он всасывается быстро, хотя и недостаточно полно (на 30%), и на 90% выводится с мочой в виде неактивных конъюгатов. При в/в введении 50% препарата выводится с мочой в неизмененном виде. Фармакокинетика его сложна и изучена недостаточно, особенно у беременных.
Применение. Ритодрин и некоторые другие β2-адреностимуляторы вводят в/в по строгим показаниям при угрозе преждевременных родов (King et al., 1988). Однако существенного снижения перинатальной смертности при их применении не выявлено, а материнская смертность может даже возрастать (The Canadian Preterm Labor Investigators Group, 1992; Higby et al., 1993; Johnson, 1993). Впрочем, учитывая современные достижения в ведении недоношенных детей, можно полагать, что имеющиеся статистические методы недостаточно чувствительны для того, чтобы выявить небольшие, но все же важные положительные эффекты. При угрозе преждевременных родов применяют и некоторые другие средства (Bossmar, 1998; Norwitz et al., 1999), например препараты магния. Есть данные о токолитическом действии индометацина, однако для него пока не установлено соотношение пользы и риска (Panter et al., 1999). Такое действие оказывают и антагонисты кальция, но их влияние на долгосрочный прогноз также не выяснено (Carret al., 1999; гл. 32). Побочные эффекты β2-адреностимуляторов. Основные из этих эффектов связаны с чрезмерной активацией β-адренорецепторов. Особенно велик их риск при сердечно-сосудистых заболеваниях, но его можно снизить путем назначения препаратов в виде ингаляций.
Сравнительно частый побочный эффект бета2-адреностимуляторов — тремор. Со временем он обычно уменьшается (то есть развивается привыкание); пока не известно, связано ли это с десенситизацией бета2-адреноре-цепторов скелетных мышц или с адаптацией на уровне ЦНС. Тремор можно облегчить, начиная прием препаратов внутрь с малых доз и постепенно увеличивая их по мере развития привыкания. Бета2-адреностимуляторы, особенно при приеме внутрь или парентеральном введении, могут вызвать тревожность и беспокойство, что ограничивает их применение.
Частый побочный эффект при системном введении β2-адреностимуляторов — тахикардия. В то же время известно, что положительный хронотропный эффект катехоламинов опосредован активацией β1-адренорецепторов, и поэтому механизм вызываемой β2-адреностимуляторами тахикардии пока не ясен. Возможно, активация сердечных β2-адренорецепторов тоже может приводить к повышению ЧСС. Не исключено также, что тахикардия обусловлена рефлексами, возникающими в ответ на опосредованное β2-адренорецепторами снижение ОПСС. При тяжелом приступе бронхиальной астмы β2-адреностимуляторы могут, напротив, вызвать снижение ЧСС -предположительно благодаря улучшению показателей дыхания и, как следствие, снижению симпатических тонических влияний на сердце. У больных без заболеваний сердца β2-адреностимуляторы редко вызывают аритмию или ишемию миокарда, однако риск этих осложнений гораздо выше у больных ИБС или с уже имеющейся аритмией. Кроме того, вероятность сердечно-сосудистых осложнений повышена у принимающих ингибиторы МАО.
При начале лечения β2-адреностимуляторами приступа бронхиальной астмы возможно снижение Ра02. Оно может быть обусловлено вызванным этими препаратами расширением сосудов легких, приводящим к еще большему нарушению вентиляционно-перфузионного отношения. Обычно этот эффект выражен незначительно и вскоре проходит, но при необходимости можно назначить ингаляцию кислорода. У женщин, получающих ритодрин или тербуталин в связи с угрозой преждевременных родов, описан тяжелый отек легких.
Данные ряда эпидемиологических исследований свидетельствуют о возможной связи между длительный приемом β-адреностимуляторов и риском смерти или критических состояний при бронхиальной астме (Suissa et al., 1994). Делать из этих исследований однозначные выводы трудно, однако вопрос о постоянном приеме β2-адреностимуляторов при бронхиальной астме явно не прост. Известно и хорошо изучено, как in vivo, так и in vitro, привыкание к адренергическим средствам (гл. 6). Длительное системное применение β-адреностимуляторов во многих органах сопровождается снижением плотности β-адренорецепторов, а следовательно, и уменьшением реакций на данные препараты. Впрочем, у большинства больных бронхиальной астмой такое привыкание не приводит к снижению терапевтического эффекта — если, конечно, они не используют чрезмерно высокие дозы β-адреностимуляторов в течение длительного времени (Jenne, 1982; Tattersfield, 1985).
Есть данные о том, что постоянное употребление β2-адреностимуляторов может еще больше повышать реактивность бронхов, тем самым затрудняя лечение бронхиальной астмы (Lipworth and McDevitt, 1992; Hancox et al., 1999). He известно, повышается ли риск такого осложнения при использовании препаратов длительного действия или высоких доз (Beasley et al., 1999). Как бы то ни было, при решении вопроса о назначении β2-адреностимуляторов на длительный срок необходимо подумать о дополнительной или иной терапии (например, об ингаляциях глюкокортикоидов).
У животных высокие дозы β-адреностимуляторов вызывают некроз миокарда. Их парентеральное введение может также приводить к повышению концентраций в плазме глюкозы, молочной кислоты и свободных жирных кислот и к понижению концентрации К+. Последний эффект очень важен при заболеваниях сердца, особенно у принимающих сердечные гликозиды и диуретики. При сахарном диабете β-адреностимуляторы могут усугублять гипергликемию, и порой бывает необходимым повышать дозу инсулина. Риск всех этих побочных эффектов гораздо ниже при ингаляциях, чем при парентеральном введении или приеме внутрь.
Бета-3 адренорецепторы локализованы в стенках мочевого пузыря, а также на адипоцитах бурой жировой ткани. В настоящее время разработан препарат мирабегрон, который является селективным стимулятором бета-3 рецепторов.
источник
Бронхорасширяющие препараты делятся на три группы: в-адреностимуляторы (АдС), антихолинергические препараты (АХП), ксантиновые препараты (КП).
В сочетании с инталом (или тайледом) и ингаляционными стероидами они составляют список жизненно необходимых антиастматических препаратов.
Бронхорасширяющее действие АдС связано с повышением внутриклеточного уровня циклического аденозинмонофосфата (цАМФ) (в связи с увеличением активности фермента аденилатциклазы) и блокадой выхода медиаторов из тучных клеток и базофилов. Длительное время для лечения бронхиальной астмы (БА) применялись неселективные АдС, лишь в последние десятилетия созданы препараты, действующие преимущественно на в2-адренорецепторы, расположенные в бронхах. В связи с этим препараты часто называют в2-агонистами (что не совсем правильно).
Консенсус рекомендует использовать для купирования приступов удушья сальбутамол и фенотерол. Сальбутамол (вентолин) чаще применяется в виде дозированного аэрозоля по 100-200 мкг (1-2 вдоха) до 3-4 раз в сутки. Несколько реже используют сальбутамол в таблетках по 2 и 4 мг (2-4 таблетки в сутки) или дисковую форму — вентодиски, содержащие мельчайший порошок сальбутамола в дозах 200 или 400 мкг для ингаляций через «Дискхалер». Фенотерол (беротек) применяют в виде дозированного аэрозоля по 0,2 мг. Он является наиболее эффективным и наименее токсичным. Перечисленные здесь АдС с коротким действием применяют при более легких формах болезни.
В последние годы консенсус в лечении БА рекомендует использовать новые ингаляционные в2-адреностимуляторы длительного действия: сальметерол и формотерол, а также таблетированный препарат сальбутамолавольмакс (по 4 и 8 мг), обеспечивающий бронходилатирующий эффект в течение суток.
в2-агонисты длительного действия (сальметерол и формотерол), благодаря улучшенному фармакологическому профилю, имеют особые преимущества при терапии больных БА. Препараты обладают бронходилатирующим и бронхопротективным эффектом продолжительностью 12 ч, что дает возможность назначать эти препараты для терапии ночной астмы.
Кроме того, пролонгированные препараты обеспечивают лучший контроль симптомов и функциональных легочных показателей у больных бронхиальной астмой по сравнению с в2-агонистами короткого действия, улучшают качество жизни больных БА, обладают выраженным протективным эффектом при астме физического усилия. Сальметерол выпускается в виде дозированного ингалятора и в виде порошковых ингаляторов, формотерол — только в форме порошковых ингаляторов.
Формотерол является полным агонистом в2-адренорецепторов и отличается быстрым началом действия (через 1-3 минуты после ингаляции) и продолжительностью действия (более 12 часов), тогда как сальметерол представляет собой частичный в2-агонист и характеризуется более медленным наступлением эффекта (через 20-30 минут после ингаляции) и также продолжительным действием (более 12 часов).
Согласно современным международным согласительным документам, в2-агонисты длительного действия относятся к классу средств длительной превентивной терапии БА и рекомендованы для терапии больных с персистирующей бронхиальной астмой (начиная с 3-й ступени по классификации GINA). Назначение пролонгированных в2-агонистов показано больным БА, течение заболевания у которых не контролируется стандартными дозами ИГКС.
К новым отечественным АдС, полученным на основе сальбутамола, относится савентол, который превосходит сальбутамол по биодоступности и пролонгированности. Разработаны две формы препарата: таблетки савентола по 4 мг, применяемые в среднем 3 раза в сутки, и таблетки сальтос по 6 мг с замедленным освобождением активного вещества, назначаемые 2 раза в сутки. Применение препаратов пролонгированного действия оказалось особенно удобным для контроля за ночной астмой. Длительность курса лечения — 1 месяц.
Действие зарубежных ингаляционных АдС основано на использовании экологически неблагоприятных фреонов. Отечественными авторами под руководством академиком А. Г. Чучалина разработаны новые оригинальные лекарственные формы сальбутамола под названием сальбен и бенакорт в виде сухих порошков для ингаляций. Эти препараты экологически безопасны и вполне конкурентоспособны с аналогичными зарубежными средствами.
Сальбен применяется в суточной дозе 800 мкг, продолжительность лечебного курса 4-5 недель. Для ингаляций используются разработанные отечественными авторами специальные ингаляторы: «Спинхалер», кисетный ингалятор «Дискхалер», дозирующий ингалятор «Турбохалер», портативный дозирующий ингалятор «Циклохалер». За рубежом также выпускаются противоастматические препараты в виде порошка для вдыхания, например вентолин и бекотид (вентодиски и бекодиски).
Из отечественных препаратов следует также назвать комбипек (в таблетке содержится 0,2 г теофиллина и совентол в дозе 8 мг в пересчете на сальбутамол; принимается 2 раза в день) и детскую пероральную лекарственную форму сальбутамола-гемисукцината-гливент.
Побочные эффекты АдС проявляются, прежде всего, кардиотоксическим действием, что объясняется наличием у всех этих препаратов в1-стимулирующего эффекта. Кардиотоксическое действие (сердцебиение, боли в области сердца), а также тремор, головная боль чаще наблюдаются при использовании сальбутамола и беротека. В связи с неблагоприятным действием на сердечно-сосудистую систему АдС с большой осторожностью используют при ишемической болезни сердца и артериальной гипертонии.
Десенситизация (снижение чувствительности) в2-адренорецепторов и снижение эффективности лечения развивается и при длительном применении АдС в лечебных дозах. В связи с этим через определенное время курсового применения АдС (примерно через каждые 4-5 недель) необходимо делать 7-10-дневные перерывы, заменяя, при необходимости, АдС на другие бронхолитики.
Антихолинергические препараты в виде атропина и атропиноподобных средств издавна применялись для лечения БА. Однако они не получили широкого применения в связи с недостаточной эффективностью и наличием серьезных побочных эффектов (сухость слизистых оболочек и затруднение отделения мокроты, тахикардия, психоэмоциональное возбуждение, нарушение аккомодации, повышение внутриглазного давления).
Интерес к АХП при бронхиальной астме возродился после получения ингаляционного антихолинергического препарата атровента (ипратропиума бромида, отечественный препарат — тровентол), который оказывает на дыхательные пути селективное действие и практически полностью лишен системных эффектов, свойственных атропину, поскольку всасывается не более 10 % введенного вещества.
Применяется по 40-60 мкг (2-3 вдоха) до 3-4 раз в сутки. При недостаточном эффекте разовую дозу можно увеличить до 80 мкг (до 4 вдохов). Специальные исследования показали, что даже увеличение однократных доз до 200 мкг (10 вдохов) при частоте применения до 14 раз в сутки не нарушало переносимость препарата и, что особенно ценно, не влияло на количество мокроты и ее вязкость.
При этом параллельно с нарастанием дозы увеличивался терапевтический эффект. Действие препарата начинается через 30-60 минут после ингаляции, эффект достигает максимума и остается на таком уровне на протяжении 3 часов после ингаляции, сохраняется, в среднем, 5-6 часов. Снижение чувствительности к препарату при длительном его применении (до года и более) не развивается.
Показанием для применения АХП является приступ удушья при любой форме БА, но преимущественно их следует назначать при наличии побочных эффектов со стороны сердечно-сосудистой системы при лечении АдС, сопутствующих сердечно-сосудистых заболеваниях (ишемическая болезнь сердца (ИБС), артериальная гипертония), у пожилых больных и особенно при вагусных формах бронхоспазма, при которых преобладает спазм относительно крупных бронхов.
Многие авторы считают, что эффективность АХП более высокая при эндогенной астме, т. е. у больных, страдающих хроническим бронхитом с повышенным отделением мокроты. К сожалению, приходится констатировать, что системные побочные эффекты, свойственные атропину, некоторые врачи необоснованно переносят на атровент (тровентол). Этим объясняется недостаточное использование АХП во врачебной практике.
Ингаляционные АХП практически не имеют противопоказаний. Известную осторожность необходимо соблюдать на протяжении первых трех месяцев беременности.
Атровент (тровентол) хорошо сочетается с в-адреностимуляторами и ксантиновыми препаратами, при этом действие АдС потенцируется. На этом основано применение беродуала — комбинированного препарата, одна ингаляция (вдох) которого содержит 50 мкг беротека (фенотерола) и 20 мкг атровента. Благодаря такому сочетанию бронходилатирующий эффект обеспечивается как стимуляцией в2-адренорецепторов, так и блокадой холинергических рецепторов.
Обычно применяют по 2 вдоха беродуала до 3-4 раз в сутки; по силе действия они не уступают, а по продолжительности действия превосходят соответствующее количество беротека, хотя в них содержится в 4 раза меньше в-адреностимулятора. Это резко уменьшает возможность побочного действия препарата на сердечно-сосудистую систему. При тяжелых приступах рекомендуется увеличить разовую дозу до 3-4 вдохов. Напомним, что в 4 вдохах беродуала содержится 200 мкг беротека (средняя рекомендуемая доза препарата) и 80 мкг атровента (выше уже говорилось, что даже увеличение разовой дозы до 200 мкг не приводило к побочным эффектам).
В целом показания для применения беродуала совпадают с таковыми атровента (тровентола), однако следует иметь в виду возможность побочных явлений, вызванных беротеком. В связи с этим следует проявлять большую осторожность при наличии у больного сопутствующих ИБС и артериальной гипертонии.
Из различных ксантиновых препаратов (кофеин, теобромин, теофиллин) для лечения бронхиальной астмы используют только теофиллин, вернее его химические комплексы с этилендиамином (для повышения растворимости), известные как эуфиллин, диафиллин и аминофиллин.
1) ингибирование фосфодиэстеразы, что приводит к накоплению в тканях цАМФ и расслаблению гладкой мускулатуры бронхов; по мнению ряда авторов, ингибирование фосфодиэстеразы не является основным в механизме действия КП, поскольку клинически значимая блокада фермента развивается лишь при таких высоких концентрациях теофиллина в крови, какие никогда не наблюдаются в клинике;
2) ингибирование аденозиновых рецепторов, что снижает высвобождение медиаторов анафилактической реакции и стимулирует высвобождение норадреналина;
3) стимуляция ресничек мерцательного эпителия, увеличение мукоцилиарного транспорта, улучшение реологических свойств бронхиальной слизи и отделения мокроты;
5) улучшение сократительной способности диафрагмы;
6) стимуляция адренорецепторов.
КП назначают в различных формах: таблетках, порошках, свечах, растворах для внутривенного (2,4 %) и внутримышечного (24 %) введения. Для купирования приступов удушья предпочтительно внутривенное капельное введение эуфиллина. Обычно всем больным вводят 10 мл 2,4 % раствора. Между тем, вводимая доза должна зависеть от массы тела больного, возраста, сопутствующих заболеваний, применения других лекарств и даже от того, является больной курильщиком или нет.
Для обеспечения лечебной концентрации теофиллина в крови (от 5 до 20 мкг/мл) необходимо сначала ввести внутривенно капельно в течение 30 мин ударную дозу эуфиллина из расчета 5,6 мг/кг (при массе 80 кг х 18 мл 2,4 % раствора), а затем вводится поддерживающая доза также внутривенно капельно из расчета 0,6 мг/кг/ч в течение 3-5 часов (в нашем случае 2 мл 2,4 % раствора в час).
Если больной уже получал эуфиллин в предшествующие сутки, то ударная доза уменьшается примерно наполовину, у курильщика поддерживающая доза увеличивается в 1,5 раза. Метаболизм теофиллина осуществляется в печени, поэтому при заболеваниях печени и недостаточности кровообращения с застойными явлениями в печени, а также при патологии почек доза уменьшается примерно в 2 (при тяжелых процессах в 3) раза.
Дозировка значительно снижается у пожилых и особенно старых лиц, при наличии дыхательной недостаточности, при приеме пищи, богатой белками и витаминами. Учитывается и взаимодействие с другими лекарствами: при одновременном приеме эритромицина, олеандомицина, линкомицина, фуросемида, аллопуринола, оральных контрацептивов доза снижается на 25-50%, при приеме фенобарбитала, рифампицина — увеличивается. Таким образом, клиническая эффективность КП зависит от многих факторов. В связи с этим для подбора лечебной дозы необходимо определение концентрации теофиллина в крови.
При приеме внутрь эуфиллин хорошо всасывается; после приема 0,3 г препарата (2 таблетки) концентрация его в плазме через 1-1,5 часа достигает 4-5 мкг/мл и сохраняется на этом уровне на протяжении 4-5 часов. Интерес к эуфиллину возрос в связи с разработкой и внедрением в практику пролонгированных препаратов теофиллина. Часть таких препаратов (теодур, теотард, дурофиллин, теобиолонг, слофиллин, слабид) обеспечивает лечебную концентрацию в крови при приеме 2 раза в сутки, другие (теодур-24, унифилл, эуфилонг) — при однократном приеме.
Необходимо подчеркнуть хорошие качества отечественных пролонгированных препаратов теопэка и теобиолонга, применяемых по 0,3 г после еды 2 раза в сутки. В частности, специально проведенные исследования показали, что по фармакодинамике и фармакокинетике теопэк не уступает теотарду и теодуру, а по некоторым параметрам превосходит их. После приема 0,3 г теопэка бронхолитическое действие развивается через 3-6 часов, постоянная концентрация сохраняется в течение 12-24 часов.
На 4-е сутки ежедневного приема теопэка в дозе 600 мг в сутки концентрация теофиллина в крови достигает 12-19 мкг/мл. Если внутривенное введение эуфиллина рекомендуется при приступах удушья и обострении заболевания, то пролонгированные препараты, благодаря круглосуточному бронхоспазмолитическому действию, — при затяжных бронхообструктивных синдромах (чаще при эндогенной астме), особенно у больных с ночными и утренними приступами удушья.
Особенностью КП является небольшой диапазон терапевтической концентрации в крови, которая непосредственно переходит в концентрацию, дающую токсические эффекты. Больше того, начальная интоксикация (сердцебиение, тремор, головная боль, головокружение, нарушение сна, тошнота) появляется уже при лечебной концентрации теофиллина в сыворотке крови (15-20 мкг/мл).
При более высокой концентрации эти явления усиливаются, развиваются выраженная тахикардия, возбуждение, бессонница, рвота, гипотония или, наоборот, гипертензия, могут развиться аритмии сердца, увеличение имеющейся коронарной и легочно-сердечной недостаточности, судорожные приступы. Помимо токсических, препараты теофиллина могут оказывать (очень редко) аллергические реакции за счет этилендиамина, который может действовать как аллерген.
В связи с этим начинают выпускаться препараты теофиллина без этилендиамина. К ним относится теотард, представляющий собой чистый безводный теофиллин и назначаемый двукратно в таблетках, в среднем по 600-800 мг/сут. Применение КП противопоказано при некоторых формах ИБС (остром инфаркте миокарда, нестабильной стенокардии, высоком (III-IV) функциональном классе стенокардии напряжения), экстрасистолии, пароксизмальной тахикардии, тиреотоксикозе, выраженной артериальной гипертензии, идиопатическом гипертрофическом субаортальном стенозе, индивидуальной непереносимости теофиллина.
Саперов В.Н., Андреева И.И., Мусалимова Г.Г.
источник
а) Адреналин обладает альфа- и бета-адренергической активностью. Его применяют для оказания неотложной помощи при приступах бронхиальной астмы, особенно если неэффективны препараты для приема внутрь. Назначают 0,2—0,5 мл (детям — 0,01 мл/кг) раствора адреналина 1:1000 п/к. Эффект обычно наступает в течение 15 мин. При необходимости адреналин вводят повторно каждые 20 мин. Отсутствие эффекта после третьей инъекции адреналина свидетельствует о высоком риске астматического статуса. Побочные действия — тахикардия, тошнота, рвота, головная боль, артериальная гипертония, боль за грудиной, раздражительность, тремор, головокружение. У пожилых, особенно страдающих сердечно-сосудистыми заболеваниями, адреналин применяют с осторожностью.
При введении адреналина в виде водной суспензии 1:200 его действие проявляется немедленно и сохраняется в течение 6—8 ч. Суспензию вводят в дозе 0,1—0,3 мл (детям — 0,005 мл/кг) п/к. При приступе бронхиальной астмы для оценки обратимости бронхоспазма рекомендуется сначала вводить раствор адреналина 1:1000, а через 20—30 мин — суспензию адреналина. Суспензию можно вводить в той же дозе каждые 8 ч. Побочные действия те же, что при применении раствора адреналина.
б) Эфедрин — природное соединение, по действию сходно с адреналином. Применяется внутрь в виде растворов или таблеток, часто в комбинации с метилксантинами. Эфедрин обладает менее выраженным бронходилатирующим действием, чем адреналин, однако эффективен при приеме внутрь. Препарат назначают в дозе 25—50 мг каждые 4—6 ч (детям — 3 мг/кг/сут в 4—6 приемов). По побочным действиям эфедрин сходен с адреналином, к наиболее серьезным относятся раздражительность, нарушения сна и тахикардия, особенно у детей. Из-за этого вместо эфедрина в настоящее время назначают селективные бета2-адреностимуляторы.
в) Этилнорэпинефрин — эффективный бронходилататор. По побочным действиям сходен с адреналином. Это препарат короткого действия, выпускается в виде раствора для инъекций. Этилнорэпинефрин назначают в дозе 0,6—2,0 мг (детям — 0,04 мг/кг) п/к или в/м. Инъекции можно повторять каждые 20 мин.
г) Изопреналин — бета1— и бета2-адреностимулятор, эффективный бронходилататор. К основным побочным эффектам относятся усиление ЧСС и силы сердечных сокращений, аритмии, сосудорасширяющее действие. Изопреналин малоэффективен при приеме внутрь. Его применяют в виде раствора 1:100 или 1:200 для ингаляций с помощью распылителя или ингалятора-дозатора. Ингаляция изопреналина вызывает быстрое — в течение нескольких секунд или минут — расширение бронхов, эффект сохраняется 1—2 ч. Слишком частое применение препарата при тяжелых приступах бронхиальной астмы может приводить к снижению его эффективности и увеличению риска побочных действий. При тяжелых приступах, сопровождающихся гипоксемией, изопреналин применяют с осторожностью, поскольку он, расширяя сосуды легких, еще больше нарушает соотношение между перфузией и вентиляцией. Больным объясняют, что злоупотребление ингаляционными адреностимуляторами недопустимо. На сегодняшний день при бронхиальной астме вместо изопреналина все чаще применяют препараты с более длительным действием на бета2-адренорецепторы.
д) Изоэтарин — производное изопреналина, действует преимущественно на бета2-адренорецепторы и поэтому обладает менее выраженными побочными действиями. Длительность действия изоэтарина незначительно превышает длительность действия изопреналина и составляет 2—3 ч. Изоэтарин обычно применяют в виде ингаляций с помощью распылителя или ингалятора-дозатора. При применении в виде дозированного аэрозоля препарат назначают по 1—2 вдоха (0,34—0,68 мг) каждые 4 ч.
е) Орципреналин по строению близок к изопреналину, однако метаболизируется более медленно и поэтому обладает более длительным действием (до 5 ч). Орципреналин выпускается в виде таблеток по 10 и 20 мг (назначают по 10—20 мг каждые 4—6 ч), дозированного аэрозоля, 0,65 мг/вдох (назначают по 1—3 вдоха каждые 4—6 ч), 5% раствора для ингаляций (0,2—0,3 мл разводят в 2,5 мл воды или физиологического раствора, ингаляции повторяют каждые 4—6 ч). Дозы для детей приведены в табл. 4.5. Хотя орципреналин менее активен, чем изопреналин, он обладает более длительным действием и его можно принимать внутрь. Наиболее частые побочные действия — раздражительность, тремор и тахикардия.
ж) Тербуталин сходен с орципреналином, однако в отличие от него, является селективным бета2-адреностимулятором и обладает более длительным действием. Тербуталин назначают внутрь по 2,5—5,0 мг каждые 8 ч, п/к по 0,25 мг или в виде дозированного аэрозоля по 1—2 вдоха (0,4 мг) каждые 4—6 ч. Выраженность и длительность бронходилатирующего действия при п/к введении тербуталина такие же, как при п/к введении адреналина. Однако тербуталин не имеет преимуществ перед адреналином для лечения приступов бронхиальной астмы, поскольку обладает такими же побочными действиями. При приеме тербуталина внутрь эффект наступает через 15—30 мин и длится 6—8 ч. Тербуталин не рекомендуется назначать детям младше 12 лет. Побочные действия — тахикардия и раздражительность. Примерно у 50% больных отмечается тремор. При регулярном применении препарата это побочное действие обычно исчезает.
з) Сальбутамол является селективным бета2-адреностимулятором, длительность действия такая же, как у тербуталина. Для приема внутрь выпускают препарат короткого действия в виде таблеток по 2 и 4 мг (назначают по 2—4 мг каждые 6—8 ч), таблеток длительного действия по 4 и 8 мг (назначают по 4—8 мг каждые 12 ч, максимальная доза 32 мг/сут) и сироп, содержащий 2 мг препарата в 5 мл. Сироп сальбутамола назначают взрослым и детям старше 14 лет по 5—10 мл 3—4 раза в сутки, детям 6—14 лет — 5 мл 3—4 раза в сутки, детям 2—6 лет — по 0,25 мл/кг 3 раза в сутки, разовая доза не должна превышать 5 мл. Для профилактики ночных приступов бронхиальной астмы назначают таблетки длительного действия. Сальбутамол также можно применять в виде дозированного аэрозоля — по 2 вдоха (180 мкг) каждые 4—6 ч — и порошка — по 200 мкг (1 капсула) каждые 4—6 ч с помощью распылителя порошков для ингаляций. Используется также 0,5% раствор для ингаляций — по 5 мл (2,5 мг) каждые 4—6 ч. Дозы для детей приведены в табл. 4.5. Побочные действия такие же, как у тербуталина, наиболее выраженное из них — тремор.
и) Битолтерол — селективный бета2-адреностимулятор, обладает длительным действием. Применяют в виде дозированного аэрозоля по 1—3 вдоха (0,37—1,11 мг) каждые 8 ч и в виде раствора для ингаляций (см. гл. 7, п. V.Б.1.а.3).
к) Пирбутерол — селективный бета2-адреностимулятор, по структуре и действию сходный с сальбутамолом. Взрослым и детям старше 12 лет его назначают в виде дозированного аэрозоля — по 2 вдоха (400 мкг) каждые 4—6 ч. Выпускаются также ингаляторы-дозаторы, подающие пирбутерол только на вдохе. Эти ингаляторы рекомендуют больным, которые не могут пользоваться обычными ингаляторами-дозаторами.
л) Сальметерол более выраженно и избирательно действует на бета2-адренорецепторы, чем другие бета2-адреностимуляторы. Действие проявляется через 15 мин и становится максимальным не ранее чем через 3 ч после применения, что делает сальметерол непригодным для лечения приступов бронхиальной астмы. Однако большая продолжительность действия (около 12 ч) позволяет применять этот препарат для профилактики приступов бронхиальной астмы физического усилия и ночных приступов бронхиальной астмы. К преимуществам сальметерола относится и то, что его применяют 2 раза в сутки. Сальметерол выпускается в виде дозированного аэрозоля (21 мкг/вдох). Обычно его назначают по 2 вдоха каждые 12 ч. Сальметерол применяют у детей старше 12 лет и взрослых. Его не используют, если эффективны ингаляционные бета2-адреностимуляторы короткого действия. При бронхиальной астме физического усилия сальметерол назначают за 30—60 мин до физической нагрузки. При развитии бронхоспазма на фоне применения сальметерола не следует увеличивать частоту ингаляций. В этом случае дополнительно назначают бета2-адреностимулятор короткого действия.
м) Фенотерол и прокатерол — селективные бета2-адреностимуляторы, сходные по действию с тербуталином, сальбутамолом и битолтеролом. По сравнению с прокатеролом фенотерол обладает менее избирательным действием на бета2-адренорецепторы, поэтому чаще вызывает тахикардию. Увеличение летальности бронхиальной астмы, наблюдавшееся в 70-х гг. в Новой Зеландии, было обусловлено широким применением фенотерола. Прокатерол выпускается в виде таблеток длительного действия. В США фенотерол и прокатерол не производятся.
б. Метилксантины. Расширение бронхов под действием метилксантинов обусловлено, по-видимому, блокадой аденозиновых рецепторов и снижением концентрации кальция в цитоплазме. Метилксантины не связываются с адренорецепторами, поэтому усиливают действие адреностимуляторов.
1) Теофиллин — основной препарат группы метилксантинов, бронходилататор. Эффективность и побочное действие теофиллина зависят от его концентрации в сыворотке. Терапевтическая концентрация в сыворотке, вызывающая минимальные побочные эффекты, составляет 8—15 мкг/мл. При концентрации теофиллина в сыворотке выше 15 мкг/мл риск побочных эффектов значительно возрастает.
а) Побочные действия — тошнота, рвота, понос, головная боль, частое мочеиспускание, раздражительность. Реже отмечаются бессонница, психические расстройства, нарушение внимания.
б) Побочные действия теофиллина обычно наблюдаются при концентрации препарата в сыворотке, превышающей 15—20 мкг/мл (см. табл. 7.3). Концентрация теофиллина в сыворотке индивидуальна и зависит от скорости его метаболизма в печени. У детей клиренс теофиллина составляет 0,6—2,2 мл/кг/мин, у взрослых — 0,37—1,57 мл/кг/мин. Он значительно снижается при печеночной и сердечной недостаточности. При употреблении марихуаны и курении клиренс теофиллина повышается. При подборе дозы теофиллина необходимо учитывать факторы, влияющие на его клиренс (см. табл. 4.6), эффективность, побочные действия и концентрацию в сыворотке. Для выбора режима применения препаратов теофиллина длительного действия определяют максимальную и минимальную концентрацию теофиллина в сыворотке. При низкой скорости метаболизма теофиллин назначают 1 раз в сутки.
в) При подборе дозы теофиллина часто ориентируются на появление первых признаков передозировки — тошноты и неприятных ощущений в животе. Однако поскольку у некоторых больных первыми признаками передозировки могут быть аритмии, судороги и кома, при подборе дозы теофиллина все же лучше ориентироваться на концентрацию препарата в сыворотке. В большинстве лабораторий ее определяют с помощью спектрофотометрии, высокоэффективной жидкостной хроматографии и твердофазного ИФА. Готовые наборы, в состав которых входят моноклональные антитела к теофиллину, позволяют быстро и точно определить концентрацию теофиллина в сыворотке. Исследование с помощью этих наборов можно проводить в амбулаторных условиях. Концентрацию теофиллина определяют не только в сыворотке, но и в слюне. Концентрация теофиллина в слюне обычно пропорциональна концентрации в сыворотке, однако соотношение между ними индивидуально и меняется в течение суток.
г) Пути введения. Теофиллин назначают внутрь, ректально и в/в. При приеме препарата внутрь в виде водного или водно-спиртового раствора и таблеток, не покрытых оболочкой, он быстро и полностью всасывается в кишечнике. Максимальная концентрация в сыворотке достигается через 30—60 мин. Высокодисперсный теофиллин всасывается еще быстрее. При приеме таблеток или капсул длительного действия максимальная концентрация в сыворотке обычно достигается через 4—6 ч, поэтому эти формы лучше назначать при продолжительном лечении теофиллином. Теофиллин в виде ректальных свечей всасывается медленно и неполно, количество всосавшегося препарата непостоянно. Всасывание теофиллина в виде раствора для ректального введения более предсказуемо. Вводить теофиллин ректально, особенно в свечах, не рекомендуется, исключение составляют случаи непереносимости препарата при приеме внутрь. Теофиллин выпускается также в виде раствора для в/в введения (в 5% растворе глюкозы).
В большинстве случаев начальная доза теофиллина для взрослых составляет: при назначении таблеток короткого действия — 150—200 мг каждые 6 ч, таблеток длительного действия — 100—200 мг каждые 12 ч. При выборе начальной дозы следует учитывать факторы, влияющие на клиренс теофиллина (см. табл. 4.6). Поддерживающая доза для взрослых обычно составляет: при назначении таблеток короткого действия — 100—400 мг каждые 6 ч, таблеток длительного действия — 200—500 мг каждые 12 ч. Препараты с продолжительностью действия 24 ч назначают по 200—1000 мг 1 раз в сутки. При высоком клиренсе суточную дозу делят на 2 части, препарат принимают каждые 12 ч. Препараты длительного действия различаются по биодоступности. На всасывание некоторых препаратов теофиллина влияет прием пищи и одновременный прием антацидных средств, поэтому при смене препарата теофиллина определяют его концентрацию в сыворотке. Начальная доза теофиллина для детей обычно составляет 12—14 мг/кг/сут внутрь (см. гл. 4, п. VIII.Г.1). При необходимости ее можно увеличивать до 24 мг/кг/сут и более. Препараты короткого действия назначают каждые 6 ч, препараты длительного действия — каждые 8—12 ч. При высоком клиренсе теофиллина препараты короткого действия приходится назначать каждые 4 ч, препараты длительного действия — каждые 8—12 ч. Подбор дозы теофиллина иногда занимает несколько недель. В сложных случаях дозу меняют каждые 2—3 сут, концентрацию теофиллина в сыворотке определяют через 2 ч после приема препаратов короткого действия и через 5 ч после приема препаратов длительного действия. До тех пор пока концентрация теофиллина в сыворотке не достигнет постоянного значения (обычно через 3 сут после применения одной и той же дозы препарата), дозу теофиллина не меняют (см. табл. 4.7).
Ректально теофиллин назначают взрослым в дозе 250—500 мг каждые 8—12 ч, детям — 7 мг/кг каждые 12 ч. Поскольку всасывание теофиллина при ректальном введении непостоянно, обязательно контролируют его концентрацию в сыворотке. В/в вводят раствор теофиллина в концентрации 1,6 мг/мл (или раствор аминофиллина в концентрации 2 мг/мл). Препарат назначают в дозе 3—5 мг/кг каждые 6 ч или, что предпочтительнее, в виде длительных инфузий. Длительные инфузии проводят по следующей схеме: 1) сначала вводят насыщающую дозу препарата, которая составляет 5 мг/кг для больных, не принимавших теофиллин в последние 12—24 ч, и 2 мг/кг для больных, принимавших теофиллин в последние 12—24 ч; 2) после введения насыщающей дозы больным моложе 50 лет теофиллин вводят со скоростью 0,6—1,0 мг/кг/ч, больным старше 50 лет — со скоростью 0,4—0,6 мг/кг/ч, больным с печеночной и сердечной недостаточностью — со скоростью 0,1—0,4 мг/кг/ч (см. табл. 7.4).
2) Аминофиллин — соль теофиллина и этилендиамина — применяется внутрь, ректально и в/в. Препарат содержит 80% теофиллина. В организме аминофиллин превращается в теофиллин. Показания к применению и побочные действия такие же, как у теофиллина. Аминофиллин лучше растворяется в воде, чем теофиллин, хотя новые препараты высокодисперсного теофиллина тоже хорошо растворимы в воде.
а) Для приема внутрь аминофиллин назначают в дозе, на 20% превышающей дозу теофиллина. Аминофиллин выпускается в виде препаратов короткого действия (растворы и таблетки) и препаратов длительного действия (таблетки). Ректально аминофиллин назначают взрослым в дозе 300 мг каждые 8 ч. При ректальном введении аминофиллина следует соблюдать такие же меры предосторожности, как при ректальном введении теофиллина.
б) В/в аминофиллин вводят в дозе 4—6 мг/кг каждые 6 ч или, что предпочтительнее, в виде длительной инфузии (см. табл. 7.4). Длительную инфузию проводят по следующей схеме: 1) в течение 20—30 мин вводят насыщающую дозу (в 50—100 мл 5% раствора глюкозы), которая составляет 6 мг/кг для больных, не принимавших теофиллин в последние 12—24 ч, и 3 мг/кг — для больных, принимавших теофиллин в последние 12—24 ч, 2) затем больным моложе 50 лет аминофиллин вводят со скоростью 0,7—1,2 мг/кг/ч, больным старше 50 лет — со скоростью 0,5—0,7 мг/кг/ч, больным с печеночной и сердечной недостаточностью — со скоростью 0,1—0,5 мг/кг/ч. Концентрацию теофиллина в сыворотке определяют через 1—2 ч после введения насыщающей дозы аминофиллина, а затем — каждые 12—24 ч. После изменения поддерживающей дозы аминофиллина концентрацию теофиллина в сыворотке определяют каждые 4—6 ч. После приема внутрь или в/в струйного введения дополнительной дозы аминофиллина концентрацию теофиллина в сыворотке определяют через 1—2 ч.
3) Холина теофиллинат — соль теофиллина и холина, которая в организме превращается в теофиллин, содержание теофиллина в препарате составляет 65%. Холина теофиллинат принимают внутрь в виде препаратов короткого (растворы и таблетки) и длительного (таблетки) действия. Он лучше всасывается и реже вызывает желудочно-кишечные нарушения, чем теофиллин, поэтому холина теофиллинат можно назначать при непереносимости других препаратов теофиллина. Дозы холина теофиллината для приема внутрь на 35—40% выше, чем дозы теофиллина.
4) Дипрофиллин — дигидроксипропилтеофиллин — алкильное производное теофиллина. Эффективный бронходилататор, содержащий 70% теофиллина. Концентрацию дипрофиллина в сыворотке нельзя определить с помощью стандартных методов, применяемых для определения концентрации теофиллина. Препарат реже вызывает побочные действия, чем теофиллин. Назначается внутрь и в/м. Начальная доза для взрослых составляет 15 мг/кг внутрь каждые 6 ч, доза для детей не установлена.
Действие препаратов теофиллина усиливается при одновременном назначении бета-адреностимуляторов. Механизм действия теофиллина и бета-адреностимуляторов различен. Длительное лечение теофиллином, в отличие от длительного лечения бета-адреностимуляторами, не приводит к снижению его эффективности. Иногда одновременное назначение теофиллина и бета-адреностимуляторов оказывается столь же эффективным, как монотерапия этими препаратами в максимальных дозах. При одновременном назначении теофиллина и бета-адреностимуляторов побочные действия наблюдаются реже, поэтому при непереносимости высоких доз этих препаратов рекомендуется назначать их одновременно в более низких дозах. Применение бета-адреностимуляторов в виде ингаляций еще больше снижает риск побочных действий. Ни теофиллин, ни бета-адреностимуляторы не обладают противовоспалительным действием.
в. M-холиноблокаторы снижают тонус и реактивность бронхов. Эти препараты показаны при непереносимости или неэффективности ингаляционных адреностимуляторов, психогенном бронхоспазме и бронхоспазме, вызванном применением бета-адреноблокаторов, а также при повышенной секреции слизи в бронхах. Среди M-холиноблокаторов, применяемых при бронхоспазме, следует отметить атропин и ипратропия бромид — производное атропина, не всасывающееся через слизистую дыхательных путей. Атропин применяют в дозе 1—2 мг в виде раствора с концентрацией 0,4—1,0 мг/мл с помощью распылителя 4—6 раз в сутки (ингаляционный путь введения атропина не одобрен FDA). Ипратропия бромид применяют в виде дозированного аэрозоля по 1—2 вдоха (18—36 мкг) 3—4 раза в сутки. Показано, что применение ипратропия бромида в виде дозированного аэрозоля по 4—6 вдохов 3—4 раза в сутки оказывает более выраженное бронходилатирующее действие в отсутствие побочного. Препарат выпускают также в виде 0,02% раствора для ингаляций во флаконах по 2,5 мл. Ингаляции проводят 3—4 раза в сутки с помощью распылителя. По сравнению с бета-адреностимуляторами нового поколения аэрозольные формы M-холиноблокаторов действуют более медленно (эффект проявляется через несколько минут, пик действия — через 60 мин), но сходны с ними по продолжительности действия — до 4—6 ч. Самый частый побочный эффект — сухость во рту. Иногда отмечается нечеткость зрения, задержка мочи и редко — тахикардия.
2. Кромолин угнетает дегрануляцию тучных клеток и высвобождение ими гистамина, лейкотриенов и других медиаторов воспаления. Показано также, что он тормозит активацию и подавляет секреторную активность нейтрофилов, эозинофилов и моноцитов, а также снижает реактивность бронхов. Кромолин не вызывает расширения бронхов. Поскольку препарат плохо всасывается в ЖКТ, его применяют ингаляционно — в виде высокодисперсного порошка в смеси с лактозой, раствора для ингаляций или дозированного аэрозоля (см. гл. 4, п. X).
а. Показания к применению. Кромолин применяют только для профилактики приступов бронхиальной астмы. Его назначают при длительном течении бронхиальной астмы, неэффективности бронходилататоров, а также в тех случаях, когда необходимо прекратить или ограничить применение бронходилататоров и кортикостероидов. Кроме того, кромолин предотвращает бронхоспазм при физической нагрузке, вдыхании пыли и паров и бронхоспазм, обусловленный поздней фазой аллергических реакций немедленного типа. Кромолин не применяют при приступах бронхиальной астмы, так как он может усилить бронхоспазм.
б. Дозы. Начальная и поддерживающая дозы — по 2 вдоха дозированного аэрозоля (1600 мкг) 4 раза в сутки. При длительном применении дозу обычно снижают. Кромолин также применяют в виде порошка — по 20 мг (1 капсула) 4 раза в сутки — и раствора для ингаляций — по 20 мг (1 ампула, 2 мл) 4 раза в сутки с помощью распылителя. Ингаляция кромолина может сопровождаться першением в горле. В этом случае рекомендуется после ингаляции полоскать рот и горло водой. Если же ингаляция кромолина вызывает бронхоспазм, за 10—20 мин до нее следует проводить ингаляцию бронходилататоров. Если в первые 4—8 нед лечения кромолином частота и тяжесть приступов бронхиальной астмы не снижаются, а уменьшение доз других препаратов приводит к ухудшению состояния, кромолин отменяют. Для предупреждения бронхоспазма препарат принимают за 10—15 мин, но не ранее чем за 60 мин, до контакта с аллергеном или физической нагрузки.
в. Побочные действия. Обычно отмечаются легкий бронхоспазм, кашель, заложенность носа и першение в горле. К редким побочным действиям относятся отек гортани, крапивница, дерматит, тошнота, кровохарканье, паротит, легочная эозинофилия.
3. Недокромил назначают ингаляционно в виде дозированного аэрозоля. По активности, показаниям к применению и побочным действиям (неприятный вкус, кашель, першение в горле) он сходен с кромолином. Детям младше 12 лет недокромил не назначают. В отличие от кромолина, недокромил угнетает дегрануляцию тучных клеток не только в соединительной ткани, но и в слизистых. Недокромил обладает более выраженным противовоспалительным действием и более эффективен для профилактики приступов бронхиальной астмы, чем кромолин. При легком и среднетяжелом течении бронхиальной астмы недокромил применяют в виде дозированного аэрозоля, по 2 вдоха (3,5 мг) 4 раза в сутки, самостоятельно или в сочетании с ингаляционными кортикостероидами. Если через несколько недель после начала лечения наступает улучшение, дозу постепенно снижают до 2 вдохов 3 раза в сутки. При поддерживающем лечении недокромил назначают по 2 вдоха 2 раза в сутки (см. гл. 4, п. XI).
4. Кортикостероиды применяют при среднетяжелом течении бронхиальной астмы (ингаляционно), а также при длительном бронхоспазме и астматическом статусе (внутрь и в/в). Кортикостероиды непосредственно не расширяют бронхи. Механизм их действия до конца не изучен, однако предполагается, что они повышают реактивность бета-адренорецепторов, а также ингибируют фосфолипазу A2. Снижение активности фосфолипазы A2 приводит к угнетению продукции метаболитов арахидоновой кислоты — лейкотриенов, тромбоксанов и простагландинов. Дозы, свойства и побочные действия разных кортикостероидов приведены в гл. 4, п. XII.
а. Показания к применению и дозы
1) При приступах бронхиальной астмы кортикостероиды применяются в тех случаях, когда неэффективны бронходилататоры. Кортикостероиды обычно назначают внутрь, например преднизон, 40—60 мг 1 раз в сутки (или в несколько приемов) в течение 3—7 сут. Доза для детей — 1—2 мг/кг/сут. Отменяют препарат постепенно, также в течение 3—7 сут. При тяжелых приступах бронхиальной астмы и астматическом статусе кортикостероиды вводят в/в. Раннее применение кортикостероидов быстро устраняет гипоксемию. Рекомендуемая доза гидрокортизона для взрослых — 200 мг в/в каждые 4—6 ч, для детей — 4—6 мг/кг в/в каждые 4—6 ч; доза метилпреднизолона для взрослых — 40—80 мг в/в каждые 6—8 ч, для детей — 1 мг/кг в/в каждые 6—8 ч. Если в течение 24 ч после начала лечения кортикостероидами улучшение не наступает, дозу увеличивают. Максимальная доза метилпреднизолона для взрослых — 250 мг в/в каждые 6 ч. Лечение высокими дозами кортикостероидов проводят под постоянным контролем основных физиологических показателей, водного и электролитного баланса.
2) Ингаляционные кортикостероиды почти не обладают системным действием, поскольку не всасываются в бронхах. Они применяются самостоятельно или в комбинации с бронходилататорами при длительном течении бронхиальной астмы. При среднетяжелом течении бронхиальной астмы ингаляционные кортикостероиды применяют в низких дозах, например беклометазон, 2—4 вдоха (84—168 мкг) 2 раза в сутки, триамцинолон, 2—4 вдоха (200—400 мкг) 2 раза в сутки, флунизолид, 2 вдоха (500 мкг) 2 раза в сутки. При тяжелой бронхиальной астме кортикостероиды назначают в более высоких дозах: беклометазон и триамцинолон, 4 вдоха 4 раза в сутки, флунизолид, 4 вдоха 2 раза в сутки. Новый кортикостероид для ингаляционного применения — будесонид — назначают взрослым в дозе 200—1600 мкг/сут, детям старше 6 лет — 200—400 мкг/сут. Будесонид оказывает побочные действия реже, чем другие кортикостероиды, однако в США он пока не разрешен к применению для лечения бронхиальной астмы. После каждого применения ингаляционных кортикостероидов во избежание першения в горле и кандидоза рта рекомендуется полоскать рот и горло водой. Риск местных побочных действий ингаляционных кортикостероидов уменьшается при применении буферных насадок (см. гл. 7, п. V.Б.7). Ингаляционные кортикостероиды в низких дозах в сочетании с ингаляционными бета2-адреностимуляторами можно применять для поддерживающего лечения бронхиальной астмы легкого течения. Это позволяет уменьшить дозы бета2-адреностимуляторов.
3) При тяжелой бронхиальной астме, которая сопровождается частыми приступами при физической нагрузке и ночью, дозу ингаляционных кортикостероидов повышают до 4—6 вдохов 2—4 раза в сутки. Ингаляционные кортикостероиды снижают потребность в кортикостероидах для системного применения. Однако при тяжелых приступах бронхиальной астмы в большинстве случаев все же приходится использовать кортикостероиды для приема внутрь. Их назначают в высоких дозах коротким курсом каждый день или через день.
б. Побочные действия. Чаще всего ингаляционные кортикостероиды вызывают першение в горле, охриплость и кандидоз рта, которые исчезают после отмены препаратов или при снижении их дозы. При кандидозе назначают суспензию нистатина для полоскания, 400 000—600 000 ед 3—4 раза в сутки. Применение буферных насадок предотвращает оседание кортикостероидов в ротоглотке и существенно уменьшает местные побочные действия (см. гл. 7, п. V.Б.7). Беклометазон, триамцинолон и флунизолид плохо всасываются в бронхах, поэтому почти не вызывают угнетения функции надпочечников. При замене кортикостероидов для системного применения на ингаляционные дозу препарата для системного применения снижают постепенно, чтобы не вызвать острую надпочечниковую недостаточность. При улучшении состояния на фоне длительного лечения ингаляционными кортикостероидами их дозу обычно уменьшают.
в. Назначение кортикостероидов для системного применения через день, в отличие от ежедневного, вызывает улучшение при менее выраженном угнетении функции надпочечников. При этом применяют препараты короткого действия в достаточно низких дозах, например преднизон в дозе не более 20 мг/сут внутрь через день. Препараты более длительного действия, например дексаметазон, вызывают угнетение функции надпочечников даже при таком режиме приема. При необходимости ежедневного применения кортикостероиды назначают в минимальных дозах, утром, 1 раз в сутки. После длительного лечения дозу кортикостероидов снижают постепенно, например если применяется преднизон, то на 1—5 мг каждые 1—4 нед. При длительном лечении кортикостероидами больных регулярно обследуют для раннего выявления осложнений (см. гл. 4, пп. XII.Г—Е).
г. Тролеандомицин, антибиотик из группы макролидов, повышает эффективность кортикостероидов для системного применения, особенно метилпреднизолона (применение тролеандомицина в сочетании с метилпреднизолоном не одобрено FDA). Хотя механизм взаимодействия тролеандомицина с кортикостероидами неизвестен, показано, что через 1 нед после начала его применения снижается скорость выведения и повышается концентрация метилпреднизолона в сыворотке. Назначение низких доз тролеандомицина внутрь при бронхиальной астме позволяет снизить дозу метилпреднизолона. Схема лечения метилпреднизолоном и тролеандомицином приведена в табл. 7.5.
Тролеандомицин обладает гепатотоксическим действием, поэтому при его назначении возможно повышение активности печеночных ферментов и желтуха. Повышение активности АсАТ и АлАТ может наблюдаться даже при назначении препарата в низких дозах, например 500 мг/сут внутрь. Ежедневное же применение препарата в дозе 1 г внутрь в течение 2 нед приводит к повышению активности печеночных ферментов более чем у 50% больных. При стойком повышении активности АсАТ и АлАТ тролеандомицин отменяют или снижают его дозу. Тролеандомицин замедляет выведение теофиллина, угнетая его деметилирование в печени. Поэтому при назначении тролеандомицина и метилпреднизолона дозу теофиллина снижают на 25—50% и регулярно определяют его уровень в сыворотке. Показания к назначению тролеандомицина и метилпреднизолона ограничены. Обычно комбинацию этих препаратов применяют при тяжелой бронхиальной астме, когда необходимо назначать кортикостероиды в дозе более 15—20 мг/сут внутрь в пересчете на преднизон. Перед назначением препаратов следует сопоставить риск осложнений лечения тролеандомицином и метилпреднизолоном и риск осложнений длительного лечения высокими дозами кортикостероидов. Больному и его родственникам необходимо сообщить о побочных эффектах тролеандомицина и метилпреднизолона и получить письменное согласие на лечение.
При применении тролеандомицина и метилпреднизолона чаще всего отмечаются тошнота и схваткообразная боль в животе. В связи с замедленным выведением метилпреднизолона его побочные эффекты сохраняются длительное время и могут даже усиливаться.
5. Метотрексат — антагонист фолиевой кислоты. Применяется обычно для лечения злокачественных новообразований. В дозе 7,5—15 мг/нед внутрь оказывает противовоспалительное действие. При назначении метотрексата снижается потребность в кортикостероидах для системного применения. Метотрексат назначают при бронхиальной астме, требующей постоянного лечения кортикостероидами в дозах, превышающих 10 мг/сут в пересчете на преднизон, а также при высоком риске тяжелых побочных действий кортикостероидов — остеопороза, катаракты, сахарного диабета. Более чем у 40% больных метотрексат вызывает тошноту, понос, головную боль и сыпь, у 5% больных развивается лекарственный гепатит, который не всегда проявляется клинически, у 3—5% — лекарственный пневмонит, который может привести к пневмосклерозу. В связи с этим метотрексат назначают лишь в крайних случаях: при неудачной попытке снизить дозу кортикостероидов для системного применения и перевести больного на ингаляционные кортикостероиды в максимальной переносимой дозе, например беклометазон по 6—8 вдохов 4 раза в сутки (1200—1600 мкг/сут). Во время лечения метотрексатом больных регулярно обследуют для ранней диагностики токсического действия препарата на печень, костный мозг и легкие. Метотрексат применяют внутрь и в/м. Внутрь препарат назначают 1 раз в сутки через 8 ч после еды или не позднее чем за 1 ч до еды. При сильной тошноте переходят на в/м введение препарата. Общая доза в первую неделю составляет 7,5 мг, при хорошей переносимости ее повышают до 15 мг/нед. Впоследствии назначают максимальную переносимую дозу. Перед началом лечения проводят общий анализ крови (обязательно определяют число тромбоцитов), биохимическое исследование крови (определяют уровень креатинина и АМК, активность АсАТ, АлАТ и щелочной фосфатазы) и общий анализ мочи. Общий анализ крови и биохимическое исследование крови проводят ежемесячно. Если общая доза метотрексата достигла 1,5 г, рекомендуется биопсия печени.
6. Препараты золота также угнетают высвобождение медиаторов тучными клетками. Показано, что эти препараты позволяют снизить дозу кортикостероидов при лечении тяжелой бронхиальной астмы. Препараты золота назначают в/м (ауротиоглюкоза) и внутрь (ауранофин). У взрослых ауротиоглюкозу применяют по следующей схеме: 10 мг/нед в течение 1-й недели, 25 мг/нед в течение 2-й и 3-й недель, 50 мг/нед начиная с 4-й недели до общей дозы 800—1000 мг. Затем, если препарат эффективен и не вызывает побочных эффектов, его продолжают применять в дозе 50 мг каждые 3—4 нед. Ауранофин взрослым назначают по 6 мг/сут в 1—2 приема. Если в этой дозе препарат неэффективен, через 6 мес ее увеличивают до 9 мг/сут в 3 приема. Если через 3 мес улучшение не наступает, препарат отменяют. Препараты золота вызывают много побочных эффектов: дерматит, тошноту, понос, стоматит, анемию, лейкопению, тромбоцитопению, протеинурию, повышение активности печеночных ферментов, интерстициальный пневмонит. В связи с этим больных, получающих эти препараты, регулярно обследуют для раннего выявления осложнений лечения.
7. Буферные насадки — это камеры разных размеров, которые надеваются на наконечники ингаляторов-дозаторов для увеличения подачи ингаляционных препаратов в бронхи и уменьшения их оседания в ротоглотке. Попадая в буферную насадку, поток аэрозоля замедляется, крупные капли оседают, а мелкие достигают бронхов, распределяясь в них более равномерно и не попадая в ротоглотку. Особенно рекомендуется использовать буферные насадки детям и пожилым, а также тем больным, у которых ингаляционные препараты вызывают першение в горле и оказывают местное раздражающее действие. Многие авторы рекомендуют буферные насадки всем больным, получающим ингаляционные кортикостероиды. Для детей младшего возраста особенно удобны насадки с односторонним клапаном, позволяющие вдохнуть одну дозу аэрозоля в несколько приемов. В настоящее время выпускаются следующие насадки: ИнспайэрИз (Шеринг-Плау), Брифэнсер (Новартис), Эллипс (Глаксо Вэллком), ОптиХэйлер (Хелфскэн Продактс, Инк.), Аэрочэмбер (Форест Фармасьютикэлс). Последняя предназначена для детей младшего возраста и имеет маску с односторонним клапаном. Больные должны соблюдать рекомендованные производителем правила пользования и ухода за насадками.
Для повышения эффективности ингаляционных препаратов больного необходимо научить правильно пользоваться ингаляторами-дозаторами. Перед использованием ингалятор встряхивают. Голова больного должна быть слегка запрокинута. Наконечник ингалятора-дозатора помещают перед открытым ртом, не далее 2,5 см от него. В начале вдоха нажимают на баллончик. Делают глубокий, медленный вдох, после чего дыхание задерживают на 10 с. При необходимости нескольких ингаляций между ними делают паузы: 3—4 мин — при применении бета-адреностимуляторов, 1 мин — при применении кортикостероидов. Для уменьшения местного раздражающего действия после ингаляции рекомендуется прополоскать рот и горло водой. Это особенно важно при применении ингаляционных кортикостероидов.
8. Отхаркивающие средства. Назначение этих средств улучшает отделение мокроты. При дегидратации для разжижения мокроты показано введение жидкости.
а. Восстановление водного баланса способствует снижению вязкости слизи, разрыхлению слизистых пробок и замедлению их образования. Взрослым рекомендуется выпивать 3—4 л жидкости в сутки. В тяжелых случаях рекомендуются ингаляции 0,45% раствора хлорида натрия в течение 20—30 мин 3—4 раза в сутки с помощью распылителя ингаляционных растворов. Поскольку капли жидкости раздражают дыхательные пути и могут вызвать бронхоспазм, перед ингаляцией солевого раствора или во время нее следует применять ингаляционные бронходилататоры.
б. Ингаляции солевых растворов и бронходилататоров рекомендуется сочетать с постуральным дренажем, перкуссионным и вибрационным массажем грудной клетки. Если бронхоспазм усиливается, ингаляцию солевых растворов прекращают.
в. Эффективность других отхаркивающих средств зависит от водного баланса. Мнения о целесообразности их применения при бронхиальной астме противоречивы.
1) Гвайфенезин стимулирует секрецию слизи и снижает ее вязкость. Этот препарат редко оказывает побочные действия, входит в состав многих средств от кашля. Обычная доза — 200 мг (для детей — 100 мг) внутрь каждые 4—6 ч. Препараты длительного действия назначают по 600—1200 мг внутрь каждые 12 ч. При применении гвайфенезина рекомендуется пить больше жидкости. Эффективность препарата при бронхиальной астме незначительна, он не может заменить бронходилататоры.
2) Препараты йода также снижают вязкость мокроты. При их применении также рекомендуется пить много жидкости. Эффективность лечения зависит от дозы, препараты можно применять внутрь и в/в, однако в/в введение препаратов йода не имеет преимуществ перед их применением внутрь. Внутрь назначают насыщенный раствор йодида калия (10—15 капель разводят водой и принимают 3 раза в сутки) и йодированный глицерин (30—60 мг 3—4 раза в сутки). В/в вводят йодид натрия, 1—2 г/сут в 5% растворе глюкозы. Этот препарат применяют только у взрослых. По эффективности препараты йода близки к гвайфенезину. Применение препаратов йода ограничено из-за большого количества побочных эффектов. Они вызывают угри, особенно у подростков, паротит, тошноту, рвоту, потерю аппетита, боль в животе и понос. Многие больные отмечают металлический вкус во рту. Иногда наблюдаются гипотиреоз и увеличение щитовидной железы. Побочные эффекты при применении йодида калия возникают чаще, чем при применении йодированного глицерина. Из-за большого количества побочных эффектов препараты йода не рекомендуется применять постоянно, кормящим и беременным они противопоказаны. При приступах бронхиальной астмы препараты йода малоэффективны.
3) Ацетилцистеин снижает вязкость мокроты за счет расщепления мукопротеидов. Действие препарата дозозависимо. Обычная доза для взрослых и детей — 1—10 мл 20% раствора или 2—20 мл 10% раствора 1—4 раза в сутки в виде аэрозоля. Сразу после применения ацетилцистеина усиливается секреция слизи, поэтому после ингаляции больным рекомендуют тщательно откашливаться или проводят постуральный дренаж. Препарат раздражает дыхательные пути, а при повышенной реактивности бронхов может вызвать бронхоспазм. В связи с этим его применяют только в сочетании с бронходилататорами, например с 0,25—0,50 мл 1% раствора изоэтарина, 0,3 мл 5% раствора орципреналина или 0,5 мл 5% раствора сальбутамола. Если бронходилататоры не устраняют бронхоспазм, вызванный ацетилцистеином, препарат отменяют. Частое побочное действие — стоматит. Поскольку ацетилцистеин нередко вызывает бронхоспазм, его применяют лишь в тех случаях, когда вязкую, густую мокроту невозможно удалить иными методами.
9. H1-блокаторы при приступах бронхиальной астмы малоэффективны. Их применение оправдано только при сочетании бронхиальной астмы с аллергическими заболеваниями верхних дыхательных путей. При этом обязательно лечение бронходилататорами. Кетотифен — препарат, сходный по строению с ципрогептадином, обладает антигистаминным, противовоспалительным и бронходилатирующим действием. В США он не производится, однако широко применяется в Европе и Японии. Кетотифен назначают внутрь в дозе 1 мг 1—2 раза в сутки. Бронходилатирующим действием обладает и цетиризин — H1-блокатор из группы пиперазинов.
10. Антимикробные средства при бронхиальной астме применяются редко, поскольку она обычно осложняется вирусными инфекциями верхних дыхательных путей.
а. Среди бактериальных инфекций, осложняющих бронхиальную астму, чаще всего встречаются синуситы, бронхит и пневмония. Возбудителями острого синусита обычно бывают Haemophilus influenzae, Streptococcus pyogenes, Streptococcus pneumoniae и Staphylococcus aureus. Хронический синусит обычно вызывают анаэробные бактерии и Haemophilus influenzae. Лечение острых и хронических синуситов подробно описано в гл. 5, п. VII.Г. При остром бронхите в мазках мокроты, окрашенных по Граму, выявляется большое количество нейтрофилов (эозинофилов обычно мало) и микроорганизмов — чаще Streptococcus pneumoniae и Haemophilus influenzae.
б. В разных возрастных группах пневмонию вызывают разные возбудители. Так, у детей младше 5 лет заболевание чаще всего обусловлено вирусной инфекцией, в этих случаях антимикробные средства не назначают. В возрасте от 5 до 30 лет обычно встречается вирусная и микоплазменная пневмония. При микоплазменной пневмонии назначают тетрациклин или эритромицин. Наиболее распространенный возбудитель пневмонии у лиц старше 30 лет — Streptococcus pneumoniae. В этом случае обычно эффективны пенициллины и цефалоспорины. При подозрении на пневмонию обязательно проводят микроскопию мазка мокроты, окрашенного по Граму, и ее посев.
VI. Принципы лечения. Основная цель лечения бронхиальной астмы — предупреждение приступов в течение как можно более длительного периода с помощью как можно меньшего количества лекарственных средств. Важнейшая роль в лечении бронхиальной астмы отводится обучению больных. Вместе с больным и его родственниками врач разрабатывает индивидуальный план лечения. Больному объясняют необходимость точного выполнения указаний врача. Профилактические мероприятия включают устранение факторов, вызывающих приступы, лечение сопутствующих аллергических и инфекционных заболеваний, а также медитацию, аутотренинг, методы релаксации и биологической обратной связи (см. гл. 7, п. V.А). Тактика лечения зависит от тяжести заболевания. Критерии оценки тяжести бронхиальной астмы приведены в табл. 7.6. Кроме того, ниже описано лечение бронхиальной астмы физического усилия, аспириновой и сульфитной бронхиальной астмы, а также бронхиальной астмы у беременных и при желудочно-пищеводном рефлюксе.
А. Лечение приступа бронхиальной астмы. Приступ бронхиальной астмы начинается внезапно или развивается постепенно во время обострения заболевания.
1. Больного успокаивают, просят его расслабиться, дышать медленно и глубоко. Рекомендуют обильное питье.
2. Если приступ возник на фоне отсутствия симптомов заболевания, эффективны дозированные аэрозоли бронходилататоров. Улучшение обычно наступает через несколько минут после 1—3 вдохов аэрозоля. Вместо ингаляций можно назначить бета2-адреностимуляторы короткого действия внутрь или препараты теофиллина — лучше в виде таблеток, содержащих высокодисперсный препарат, или раствора. Улучшение в этом случае обычно наблюдается через 30—60 мин.
3. Если бронхоспазм сохраняется или возникает вновь, а также если в анамнезе есть указания на длительные приступы, назначают поддерживающее лечение бета2-адреностимуляторами или теофиллином.
а. Лечение начинают с бета2-адреностимуляторов. Их назначают внутрь или ингаляционно. Названия препаратов и дозы приведены в табл. 4.5. Дозу бета2-адреностимуляторов для приема внутрь подбирают в зависимости от эффективности и побочных действий. Для усиления бронходилатирующего действия бета2-адреностимуляторы назначают одновременно и внутрь, и ингаляционно. При плохой переносимости бета-адреностимуляторов вместо них назначают ипратропия бромид, 1—4 вдоха дозированного аэрозоля или раствора для ингаляций 3—4 раза в сутки. Ипратропия бромид можно применять в комбинации с бета2-адреностимуляторами. Если ингаляционные бета2-адреностимуляторы или их комбинация с ипратропия бромидом неэффективны, назначают препараты теофиллина длительного (дозы приведены в гл. 7, п. V.Б.1) или короткого действия (дозы приведены в гл. 4, п. VIII.Г, биодоступность — в табл. 7.7). При плохой переносимости препаратов теофиллина их дозу снижают и дополнительно назначают бета2-адреностимуляторы внутрь. Кроме того, при непереносимости какого-либо препарата теофиллина его можно заменить на другой. Если теофиллин переносится хорошо, каждые 2—3 сут его дозу увеличивают до достижения эффективной. При этом регулярно определяют концентрацию теофиллина в сыворотке.
б. Длительность лечения. Лечение проводят до тех пор, пока не наступит стабильное улучшение. После устранения бронхоспазма препараты в минимальных эффективных дозах назначают по крайней мере еще в течение 2—3 сут.
в. Противовоспалительные и противоаллергические средства. При легкой и среднетяжелой бронхиальной астме вместо бронходилататоров для приема внутрь с успехом применяются ингаляционные кортикостероиды (по 2—4 вдоха дозированного аэрозоля 2 раза в сутки) и кромолин (по 2 вдоха 4 раза в сутки). Ингаляционные бета2-адреностимуляторы при этом назначают по 2 вдоха дозированного аэрозоля каждые 3—4 ч. Если ингаляционные бета2-адреностимуляторы в этих дозах неэффективны, увеличивают дозу кортикостероидов — до 4 вдохов 2—4 раза в сутки.
4. Кортикостероиды для приема внутрь назначают при неэффективности описанного выше лечения, а также если в анамнезе есть указания на тяжелые приступы бронхиальной астмы и лечение кортикостероидами для системного применения. Начинают с насыщающей дозы, эквивалентной 40—60 мг/сут преднизона (у детей — 1—2 мг/кг/сут). Препарат назначают внутрь в один или несколько приемов в течение 3—7 сут. Действие обычно развивается через 6—24 ч, реже через 2—3 сут после начала лечения. Если наступает улучшение, в течение последующих 3—7 сут дозу постепенно снижают до полной отмены препарата. Ингаляционные кортикостероиды и бронходилататоры для приема внутрь в поддерживающих дозах вместе или по отдельности назначают еще в течение 5—7 сут, затем дозы этих препаратов также снижают.
5. Если кортикостероиды неэффективны, больного госпитализируют (см. гл. 7, п. VII).
Б. Рекомендации больным по лечению приступов бронхиальной астмы в домашних условиях (NIH Guidelines for the Diagnosis and Management of Asthma, 1991).
1. При возникновении приступа следует сделать 2—4 вдоха дозированного аэрозоля какого-либо бета2-адреностимулятора. Ингаляции можно повторять каждые 20—60 мин. При этом лучше использовать буферную насадку.
2. Если бронхоспазм удалось устранить или значительно уменьшить его выраженность, а пиковая объемная скорость превышает 70—90% исходного значения, ингаляции адреностимуляторов проводят каждые 3—4 ч в течение 1—2 сут и продолжают проводившееся ранее поддерживающее лечение. При возобновлении приступа связываются с врачом.
3. Если симптомы сохраняются в покое и ограничивают повседневную активность, а пиковая объемная скорость составляет 50—70% исходного уровня, бета2-адреностимуляторы в виде дозированных аэрозолей или растворов для ингаляций используют каждый час и начинают прием кортикостероидов внутрь в насыщающей дозе. Если лечение кортикостероидами уже проводится, то увеличивают их дозу. Если улучшение не наступает в течение 2—6 ч и если необходимо применять ингаляционные бета2-адреностимуляторы в максимальной дозе 16 вдохов/сут, необходимо обратиться к врачу.
4. Если несмотря на лечение сохраняется выраженный бронхоспазм, из-за одышки невозможно пройти более 30 м, а пиковая объемная скорость не превышает 50% исходного значения, немедленно связываются с врачом. Применяют ингаляционные бета2-адреностимуляторы: с помощью ингалятора-дозатора, 4—6 вдохов, ингаляцию повторяют через 10 мин, или распылителя ингаляционных растворов, 4—6 вдохов однократно. Начинают применение кортикостероидов или повышают их дозу. Если через 30 мин улучшение не наступает, а пиковая объемная скорость не превышает 50% исходного значения, следует вызвать скорую помощь. В этих случаях, а также тогда, когда в течение последних 6—12 ч ингаляции бета2-адреностимуляторов проводились каждые 1—3 ч, показана госпитализация.
В. Лечение приступа бронхиальной астмы в приемном отделении (NIH Guidelines for the Diagnosis and Management of Asthma, 1991, U.S. Department of Health and Human Services Publication no. 91-3042, August 1991).
1. Для оценки тяжести приступа проводят пневмотахометрию или спирометрию. При необходимости исследуют газы артериальной крови. Больного успокаивают, для облегчения дыхания используют приемы, описанные в гл. 7, п. V.А.4.
2. С помощью пульс-оксиметрии определяют насыщение гемоглобина артериальной крови кислородом. Если оно ниже 90%, а paO2 — ниже 60—65 мм рт. ст., начинают ингаляцию кислорода со скоростью 2—4 л/мин.
3. Назначают бета2-адреностимуляторы: в виде дозированных аэрозолей с использованием буферной насадки (по 4—6 вдохов) или растворов для ингаляций, например 0,5—1,0 мл 0,5% раствора сальбутамола, или 0,2—0,3 мл 5% раствора орципреналина, или 0,25—0,5 мл 1% раствора изоэтарина с помощью распылителя каждые 20—30 мин в течение 1—1,5 ч. Детям старше 5 лет назначают дозированный аэрозоль сальбутамола по 2 вдоха каждые 5 мин, но не более 12 вдохов, или 0,5% раствор сальбутамола, 0,15 мг/кг, но не более 5 мг каждые 20 мин в течение 1—2 ч, при непрерывной ингаляции — не более 15 мг/ч. У детей ингаляции бета2-адреностимуляторов проводят с помощью буферной насадки, снабженной маской с односторонним клапаном. Вместо ингаляционных бета2-адреностимуляторов иногда назначают раствор адреналина 1:1000, 0,2—0,3 мл п/к, детям — 0,01 мл/кг п/к. При необходимости инъекции адреналина повторяют каждые 20—30 мин (не более 3 инъекций). Кортикостероиды применяют: 1) при неэффективности бета2-адреностимуляторов, 2) при лечении кортикостероидами в анамнезе, 3) при возникновении приступа на фоне лечения кортикостероидами для приема внутрь. Кортикостероиды назначают в насыщающей дозе внутрь (см. гл. 7, п. VI.A.4) или в/в. В/в вводят гидрокортизон, 5 мг/кг, или метилпреднизолон, 1—2 мг/кг.
4. При стабильном улучшении, повышении пиковой объемной скорости и ОФВ1 не менее чем до 70% исходного значения и в отсутствие одышки переходят на поддерживающее лечение. Назначают адреностимуляторы для приема внутрь, ингаляционные кортикостероиды и кромолин или недокромил в разных сочетаниях с ингаляционными бета2-адреностимуляторами. Для профилактики побочных действий адреностимуляторов соблюдают меры предосторожности, описанные в гл. 7, п. V.Б.1.a.1. Если начат прием кортикостероидов для приема внутрь, его продолжают, если не начат, решают вопрос о целесообразности назначения кортикостероидов. В дальнейшем больного наблюдают амбулаторно.
5. Если сохраняются свистящее дыхание и одышка, а пиковая объемная скорость не превышает 40—70% исходной, ингаляции бета2-адреностимуляторов проводят каждый час и назначают кортикостероиды для системного применения. При дегидратации проводят в/в инфузию жидкостей. При неэффективности бета2-адреностимуляторов вводят аминофиллин, 6 мг/кг в/в в течение 20—30 мин (см. табл. 7.4), затем 0,2—1,2 мг/кг/ч в/в (в зависимости от клиренса теофиллина, в среднем 0,5 мг/кг/ч). Если больной принимает теофиллин внутрь, аминофиллин назначают в более низкой дозе. Регулярно определяют концентрацию теофиллина в сыворотке (см. табл. 4.7). Вместо аминофиллина в/в можно назначить теофиллин (см. табл. 7.4).
6. При неэффективности перечисленных мероприятий больного госпитализируют. Лечение астматического статуса описано в гл. 7, п. VII.Г.
Г. Лечение тяжелой бронхиальной астмы. Если наблюдаются длительные обострения или ежедневные приступы бронхиальной астмы или для их предупреждения необходимо постоянное медикаментозное лечение, говорят о тяжелой бронхиальной астме. При этой форме заболевания особое значение имеет немедикаментозное лечение.
1. Дозированные аэрозоли бета2-адреностимуляторов назначают по 1—3 вдоха, при необходимости дозу увеличивают до 3—4 вдохов в сутки.
2. Если потребность в ингаляционных бета2-адреностимуляторах превышает 3—4 вдоха в сутки, дополнительно назначают ингаляционные кортикостероиды, 2—4 вдоха 2 раза в сутки (см. гл. 7, п. V.Б.4). Если ингаляции кортикостероидов вызывают бронхоспазм или их применение затруднено из-за бронхоспазма, за 5—10 мин до ингаляции назначают дозированный аэрозоль бета2-адреностимулятора, 1—3 вдоха. Чтобы обеспечить попадание кортикостероида в мелкие бронхи, после каждого вдоха рекомендуют задерживать дыхание на 10—15 с. Промежуток между вдохами ингаляционных кортикостероидов должен составлять не менее 1 мин. При местном раздражающем действии и кандидозе рта применяют буферные насадки. Они уменьшают оседание препарата в ротоглотке и особенно необходимы при назначении ингаляционных кортикостероидов в высоких дозах (в виде дозированного аэрозоля во флаконе с буферной насадкой выпускается триамцинолон). Если указанные дозы кортикостероидов неэффективны, их повышают до 4 вдохов 2—4 раза в сутки. После улучшения состояния дозы ингаляционных кортикостероидов постепенно снижают. При плохой переносимости физических нагрузок и частых приступах, в том числе по ночам, ингаляционные кортикостероиды назначают по 4—6 вдохов 2—4 раза в сутки, а при каждом приступе — кортикостероиды для приема внутрь коротким курсом. Такая схема лечения в большинстве случаев позволяет избежать постоянного назначения кортикостероидов для системного применения.
3. Кромолин, 2 вдоха (1600 мкг) дозированного аэрозоля или 20 мг порошка или раствора для ингаляций 4 раза в сутки, назначают вместо или в дополнение к ингаляционным кортикостероидам. В течение первых 4—8 нед лечения больного просят вести дневник, в котором он должен отмечать свое состояние и указывать дозы принимаемых им препаратов. Отдельно записывают дозы всех препаратов, принимавшихся до назначения кромолина. Если кромолин уменьшает симптомы заболевания и снижает потребность в других препаратах, его применяют неопределенно долго, по возможности снижая дозу, например назначают на 1 ингаляцию меньше каждые 1—2 нед. Недокромил, 2 вдоха (по 1,75 мг) 4 раза в сутки с помощью ингалятора-дозатора, можно использовать вместо кромолина. Схема лечения такая же, как при применении кромолина.
4. Препараты теофиллина длительного действия назначают вместо или в дополнение к кортикостероидам, кромолину или недокромилу. Концентрация теофиллина в сыворотке должна составлять 8—15 мкг/мл. Препараты теофиллина длительного действия назначают 2—3 раза в сутки. Для профилактики ночных и утренних приступов препараты длительного действия принимают перед сном. При появлении побочных эффектов дозу уменьшают (см. гл. 4, п. VIII.Е).
5. При плохой переносимости теофиллина или неэффективности комбинации теофиллина с ингаляционными кортикостероидами или кромолином вместо теофиллина или в дополнение к нему назначают бета2-адреностимуляторы внутрь (дозы теофиллина при этом снижают). Применение ингаляционных бета2-адреностимуляторов в этом случает продолжают (названия и дозы приведены в табл. 4.5).
6. Кортикостероиды для системного применения, чаще всего преднизон, применяют при неэффективности всех перечисленных выше схем лечения. Преднизон назначают в насыщающей дозе — 40—60 мг/сут — обычно в течение 3—4 сут (см. гл. 7, п. V.Б.4.a), затем дозу постепенно снижают сначала до 20 мг/сут (у детей — до 0,5 мг/кг/сут), а затем на 2,5—5,0 мг каждые 1—2 сут до минимальной эффективной.
7. Чтобы уменьшить осложнения длительного лечения кортикостероидами для системного применения, их назначают через день. К этой схеме лечения переходят одним из двух способов: 1) доза в 1-й день остается прежней, а дозу во 2-й день постепенно уменьшают до полного перехода на прием препарата через день, 2) суточную дозу удваивают и принимают ее через день. При возобновлении симптомов заболевания возвращаются к ежедневному применению препарата. Кортикостероиды при длительном лечении лучше назначать 1 раз в сутки, утром сразу после пробуждения. При язвенной болезни в анамнезе или диспепсии через 20—30 мин после приема кортикостероидов назначают антацидные средства. Ограничивают употребление поваренной соли, при необходимости назначают препараты калия, особенно у больных, получающих диуретики. Если кортикостероиды неэффективны, их дозу увеличивают в 3 раза и назначают ежедневно в несколько приемов в течение 2—3 сут, затем пытаются снизить дозу до исходной. Во всех случаях стремятся назначать кортикостероиды для системного применения в минимальных эффективных дозах. Больных регулярно обследуют для раннего выявления осложнений лечения (см. гл. 4, п. XII.Е). Кортикостероиды не заменяют бронходилататоры, кромолин или недокромил.
8. Триамцинолон назначают больным тяжелой бронхиальной астмой с длительными обострениями, которая сопровождается угрожающими жизни приступами и требует постоянного лечения кортикостероидами. В анамнезе у этих больных обычно имеются указания на частые госпитализации, в том числе в реанимационное отделение для проведения ИВЛ. Триамцинолон особенно показан тем больным, которые по каким-либо причинам не могут принимать кортикостероиды внутрь. Препарат назначают в дозе 120 мг/сут в/м в течение 3 сут. Это приводит к улучшению функции внешнего дыхания, уменьшению частоты обращений за неотложной помощью, госпитализаций и снижению доз назначаемых препаратов, в том числе кортикостероидов для системного применения. Однако побочные эффекты — миопатия, кровоточивость, гирсутизм — при назначении триамцинолона в высоких дозах возникают чаще и оказываются более выраженными, чем при назначении кортикостероидов внутрь. Поскольку в/м введение триамцинолона может привести к локальной атрофии мышц, препарат лучше вводить в бедро. Некоторым больным триамцинолон приходится назначать в более высоких дозах — по 360 мг в сутки в/м в течение 3 сут — и повторять курс лечения через 3—6 мес. Иногда триамцинолон назначают по 80 мг в/м 1 раз в месяц. При улучшении состояния дозу препарата снижают. При тяжелых побочных эффектах, например миопатии, препарат отменяют.
9. При тяжелой бронхиальной астме, требующей высоких доз кортикостероидов, назначают метилпреднизолон в сочетании с тролеандомицином, метотрексат или препараты золота. Однако эти схемы лечения не рекомендованы FDA для применения при бронхиальной астме (см. гл. 7, пп. V.Б.4.г и V.Б.5—6).
10. При тяжелой бронхиальной астме рекомендуется обильное питье. Отхаркивающие средства имеют ограниченное применение, однако в некоторых случаях, при обильной, густой и вязкой мокроте их назначают в сочетании с постуральным дренажем.
11. При тяжелой бронхиальной астме ингаляции бронходилататоров с помощью распылителей более эффективны, чем ингаляции дозированных аэрозолей, поскольку распылители ингаляционных растворов обеспечивают более длительное введение аэрозоля и равномерное распределение препарата в бронхах. Буферные насадки повышают эффективность ингаляторов-дозаторов.
12. Антибиотики применяются только при вторичной бактериальной инфекции (см. гл. 7, п. V.Б.10).
Д. Бронхиальная астма физического усилия. У большинства больных бронхиальной астмой и более чем у 40% больных аллергическим ринитом 10—15-минутная физическая нагрузка вызывает бронхоспазм, на что указывает существенное снижение ОФВ1. Чем тяжелее бронхиальная астма, тем более выраженный бронхоспазм вызывает физическая нагрузка. У части больных приступы бронхиальной астмы развиваются только после физической нагрузки.
1. Частота и выраженность приступов бронхиальной астмы, вызванных физической нагрузкой, зависят от характера этой нагрузки. Чаще всего бронхоспазм возникает при быстром беге, реже — при ходьбе и езде на велосипеде. Плавание обычно не вызывает бронхоспазма. Бронхоспазм обычно развивается через 5—10 мин после нагрузки и исчезает в покое, реже он сохраняется более 1 ч или усиливается после физической нагрузки. Повторная нагрузка менее чем через 2 ч обычно переносится легче, чем предшествующая.
2. Причиной бронхиальной астмы физического усилия, по-видимому, является охлаждение дыхательных путей, вызванное гипервентиляцией. Показано, что определенную роль в патогенезе заболевания играют медиаторы воспаления, однако механизм развития бронхоспазма под действием холодного воздуха пока неизвестен.
3. Лечение в основном направлено на профилактику приступов. Определяют характер и продолжительность нагрузки, приводящей к бронхоспазму. Подбирают такую нагрузку, которая хорошо переносится больным. Рекомендуют, чтобы периоды интенсивной физической нагрузки были короткими, между ними больной обязательно должен отдыхать. Если улучшение не наступает, перед физической нагрузкой рекомендуют применять бронходилататоры. Назначают бета2-адреностимуляторы в виде дозированного аэрозоля за 15—20 мин до нагрузки. Это наиболее эффективный способ лечения бронхиальной астмы физического усилия. Назначая препараты спортсменам, участвующим в соревнованиях, следует иметь в виду, что многие организационные комитеты не разрешают применение катехоламинов, например изопреналина или изоэтарина, в то время как тербуталин и сальбутамол — адреностимуляторы, не относящиеся к катехоламинам, — разрешены к применению. В некоторых случаях эффективен кромолин. Его применяют за 15—60 мин до физической нагрузки в виде дозированного аэрозоля (1600 мкг) или порошка для ингаляций (20 мг). Перед применением кромолина можно назначить ингаляцию адреностимуляторов. Кромолин применяют при непереносимости других препаратов для лечения бронхиальной астмы физического усилия. Иногда эффективен ипратропия бромид, 1—2 вдоха дозированного аэрозоля (см. гл. 7, п. V.Б.1.в) за 15—30 мин до физической нагрузки. Больным, испытывающим затруднения при пользовании ингалятором, а также дополнительно к ингаляционным препаратам назначают адреностимуляторы или теофиллин внутрь за 1—2 ч до физической нагрузки.
4. Родители больного ребенка должны сообщить о его заболевании школьным учителям и тренерам и объяснить, что перед физической нагрузкой он должен принимать бронходилататоры, а при возникновении приступа нуждается в отдыхе.
Е. Аспириновая бронхиальная астма часто сочетается с вазомоторным ринитом и полипами носа. Заболевание обычно возникает у взрослых, не страдающих аллергическими заболеваниями, на фоне длительного вазомоторного ринита (см. гл. 13, п. VI.Б.1).
1. Через несколько минут или часов (до 24 ч) после приема аспирина появляются обильное водянистое отделяемое из носа, покраснение лица и одышка. Приступы бронхиальной астмы обычно бывают тяжелыми. Возможны крапивница, отек Квинке и шок. Предполагается, что в патогенезе заболевания основную роль играет нарушение метаболизма арахидоновой кислоты. Угнетение активности циклоксигеназы приводит к снижению синтеза простагландинов, обладающих бронходилатирующим действием, а активация липоксигеназного пути сопровождается накоплением лейкотриенов, которые вызывают бронхоспазм.
2. Провокационные пробы с салицилатами не проводят. Основа лечения — профилактика, основанная на исключении приема аспирина и содержащих его препаратов. К родственным препаратам, которые могут вызвать приступ при аспириновой бронхиальной астме, относятся индометацин, мефенамовая кислота, феназон, аминофеназон, а также пищевой краситель тартразин (см. табл. 13.7 и приложение IX). Неацетилированные салицилаты и парацетамол обычно не противопоказаны. Лечение приступов бронхиальной астмы проводят по стандартной схеме. Однако поскольку приступы при аспириновой бронхиальной астме обычно тяжелые, часто бывает необходима госпитализация и лечение кортикостероидами. Лечение крапивницы, отека Квинке и шока подробно описано в гл. 10, п. VI и гл. 11, п. V.
3. Прием аспирина может вызвать бронхоспазм и у некоторых больных бронхиальной астмой в отсутствие сенсибилизации к аспирину в анамнезе. Этим больным впоследствии необходимо избегать приема аспирина. Врач должен подробно рассказать им, какие препараты и пищевые продукты содержат аспирин и сходные с ним вещества. Больные с тяжелыми реакциями на аспирин в анамнезе должны всегда иметь при себе опознавательный браслет.
Ж. Сульфитная бронхиальная астма. У некоторых больных приступы бронхиальной астмы вызывают сульфиты — метабисульфит калия, бисульфит калия, метабисульфит натрия, бисульфит натрия, сульфит натрия, двуокись серы. Эти соединения добавляют во многие продукты и лекарственные средства в качестве антиоксидантов и консервантов. Чаще всего бронхиальную астму вызывает метабисульфит калия. Реакции на сульфиты наблюдаются у 5% больных бронхиальной астмой. Чаще всего они развиваются у взрослых с тяжелой формой заболевания, требующей постоянного лечения кортикостероидами. Перекрестные реакции с другими пищевыми добавками и аспирином отсутствуют. В большинстве случаев сульфиты вызывают внезапный тяжелый бронхоспазм, который может закончиться смертью. Возможны и другие анафилактоидные реакции. Патогенез бронхоспазма, вызванного сульфитами, неизвестен. Возможно, к нему приводит прямая активация тучных клеток двуокисью серы, нарушение метаболизма арахидоновой кислоты и стимуляция холинергических рецепторов. Относительно недавно показано, что сульфиты могут стимулировать продукцию IgE. Диагноз обычно ставят на основании клинической картины. Сразу после употребления продуктов, содержащих сульфиты (салатов, вина, креветок), возникают одышка, свистящее дыхание, покраснение груди и лица. Реакций на сульфиты, содержащиеся в лекарственных средствах, включая ингаляционные бронходилататоры, и двуокись серы в смоге не отмечалось. Однако не исключено, что неэффективность лечения бронхиальной астмы у некоторых больных обусловлена постоянным контактом с этими веществами. Диагноз подтверждается при положительных провокационных пробах, которые может проводить только опытный специалист в условиях стационара. Больному рассказывают, какие лекарственные средства и продукты содержат сульфиты, подчеркивают, что он должен избегать их употребления (см. приложение IX). Согласно инструкциям FDA, запрещается обрабатывать сульфитами сырые фрукты и овощи, за исключением картофеля. Если концентрация сульфитов в продуктах превышает предельно допустимую, упаковка должна содержать специальную метку. Лекарственные средства, содержащие сульфиты, также должны быть снабжены специальной меткой (значения предельно допустимых концентраций сульфитов в продуктах и лекарственных средствах могут быть изменены только в соответствии с инструкциями FDA). Лечение приступов бронхиальной астмы, вызванных сульфитами, проводится по стандартной схеме. Больные с тяжелыми реакциями на сульфиты в анамнезе должны иметь при себе адреналин в шприце, например АНА—Кит (Холлистер-Стайэр Майлс) или ЭпиПен (Сентэ Лэборэтрис), и опознавательный браслет, особенно если они часто посещают кафе и рестораны.
источник