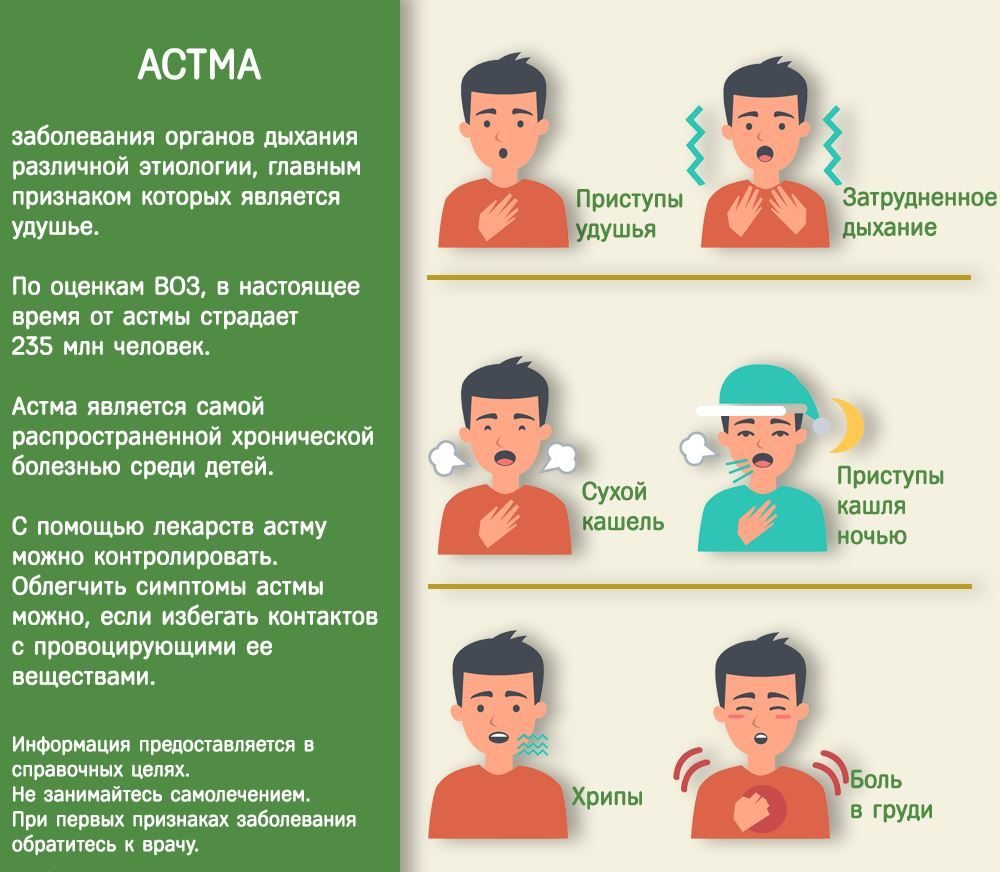
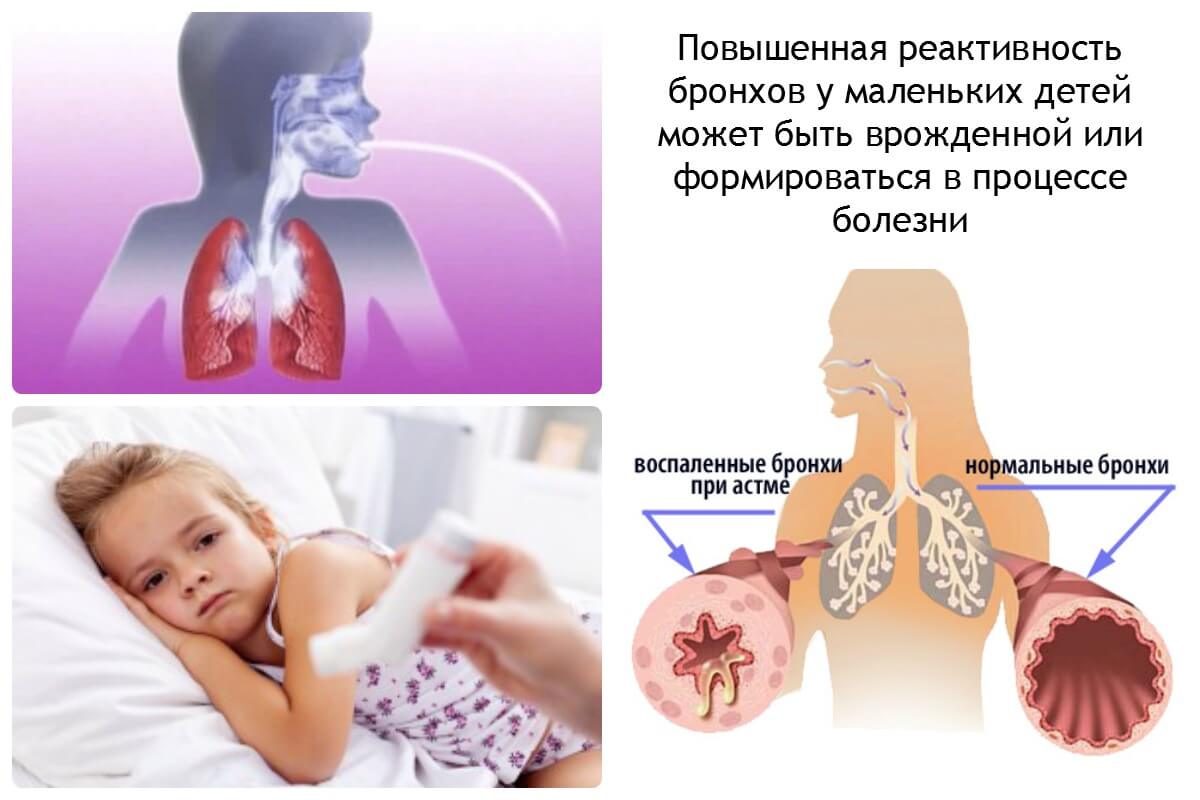
Бронхиальная астма – мультифакторальная болезнь. Это означает, что предрасположенность к ней передается по наследству, сам же недуг развивается в силу воздействия на человека целого ряда внешних факторов. Означает ли это, что у ребенка, родители которого страдают аллергическими заболеваниями, тоже будет аллергия?
Многие ошибочно считают, что бронхиальная астма – наследственная болезнь. На самом деле это не совсем так. Обусловленное генными мутациями заболевание в большинстве начинается у людей независимо от того, какие факторы окружающей среды на них воздействуют. Для того же, чтобы развилась бронхиальная астма, полигенное мультифакториальное заболевание, необходимо совпадение двух условий:
- наследственная предрасположенность к недугу;
- влияние патогенных внешних факторов.
Для определения риска развития бронхиальной астмы у детей ученые проводят генетические и статистические исследования.
Так, статистика говорит следующее:
- У ребенка, родители которого не являются астматиками или аллергиками, риск развития бронхиальной астмы – около 10%.
- Если один из родителей страдает той или иной атопией, риск увеличивается до 20%, если оба родителя – до 35%.
- Если оба родителя – аллергики, а у одного из них астма, с вероятностью 42 % ребенок унаследует предрасположенность к этому заболеванию.
- У супругов-астматиков в 75% случаев рождается ребенок, у которого астма развивается в возрасте до 7 лет.
Генетикам удалось выяснить, что за развитие атопии (атопической бронхиальной астмы) отвечают более чем 50 генов, находящихся в 5-ой и 11-ой хромосомах. Они отвечают за независимые компоненты болезни, а именно выработку специфических Е-антител, возникновения атопии, бронхиальную гиперреактивность.
Этим объясняется сложность фенотипирования заболевания:
- астма проявляется в детском или уже взрослом возрасте (если женщина или мужчина заболевают после 60-ти лет, это не означает отсутствие у них предрасположенности);
- астма может быть атопической и неатопической, то есть возникать вследствие инфекции, воздействия холодного воздуха, физического перенапряжения, ожирения, лечения ацетилсалициловой кислотой и др.;
- особенности протекания болезни, острота приступов, продолжительность ремиссии, ответ на терапию у всех больных различные.
Исследования, проводимые на однояйцевых близнецах еще в 1982 году, выявили, что в паре с высоким риском развития недуга более чем в 80% случаев заболевает только один из близнецов. Получается, что болезнь возникает из-за:
- генетической предрасположенности;
- особенностей внутриутробного развития (например, повышают риск развития бронхиальной астмы у детей вирусные болезни у их матерей незадолго до или во время беременности);
- воздействия определенных факторов окружающей среды.
Последние делятся на пять групп:
- Инфекционные (бактерии, вирусы, грибы).
- Аллергические (растения, животные, насекомые, пыль, лекарства, производственные факторы, пары кислот, дым, прочее).
- Физические (физическое перенапряжение, хроническая усталость, прочее).
- Погодные (колебания температур, влажности, атмосферного давления, прочее).
- Нервно-психологические (заболевания ЦНС, стрессы, прочее).
Родители ребенка с предрасположенностью к бронхиальной астме должны понимать, что создав определенные условия, они могут предупредить у него эту болезнь.
В первую очередь, еще на стадии планирования беременности или уже в ее период необходимо выяснить, есть ли у него в роду астматики или аллергики с одной или обеих сторон. Тогда родители смогут оценить риски и осознать, какие меры профилактики им необходимо предпринять.
Этой профилактикой является:
- Правильное питание.
Во время беременности будущая мать ребенка, у которого может развиться астма, должна придерживаться правильного диетического питания. Во-первых, из рациона должны быть исключены продукты, на которые возможна аллергическая реакция (экзотические фрукты, некоторые виды мяса, мясные бульоны, колбасы и копчености, шоколад, прочее), а также любые генетически модифицированные продукты, трансжиры, синтетические добавки. Во-вторых, свежие и натуральные продукты должны проходить щадящую термическую обработку – их нужно варить, тушить, запекать, готовить на пару, но ни в коем случае не жарить (при жарке выделяются экстрактивные вещества, способные спровоцировать аллергию и бронхиальную астму).
Подобное питание должно сохраняться и в период грудного вскармливания. В рацион кормящей материи, а после 6 месяцев и в рацион ребенка, продукты-аллергены должны вводиться с большой осторожностью и только в случае крайней необходимости.
Необходимо отметить, что правильно организованное грудное вскармливание само по себе уже является профилактикой бронхиальной астмы. Желательно сохранить его на 12-24 месяца. - Воздержание от контакта с бытовыми аллергенами.
Все в доме у ребенка, который может заболеть астмой, должно быть гипоаллергенным: постельное белье, одежда, бытовая химия, игрушки, прочее. - Чистота.
Бороться с пылью помогают регулярные уборки пылесосом и влажные уборки. В интерьере должно быть как можно меньше поглощающих пыль элементов: ковров, плотных штор, накидок на мебель, мягких игрушек. Книги должны храниться исключительно в закрытых шкафах. - Отказ от курения.
Родители должны побороть пагубную привычку, чтобы ребенок не вдыхал табачный дым пассивно. - Отсутствие домашних животных.
Не только их шерсть, но и слюна, ороговевшие частички кожи – это сильные аллергены. - Прием медикаментов только по назначению врача.
Риск возникновения аллергии и бронхиальной астмы возрастает у детей, которые в первые годы жизни часто проходили антибактериальную терапию. - Укрепление иммунитета.
Чтобы исключить инфекционный фактор развития бронхиальной астмы, необходимо увеличить сопротивляемость организма ребенка к инфекционным заболеваниям. Для этого ему необходимы правильное, витаминизированное питание, закаливание, занятия спортом.
Если ребенок с детства привыкнет жить по указанным выше правилам, они станут привычкой и сохранятся и во взрослой жизни. Возможно, это поможет ему не заболеть астмой.
источник
Опубликовано Редакция в 12/06/10 • Категории Педиатрия
Обсуждается генетический компонент развития бронхиальной астмы. Гены-кандидаты расположены на хромосомах 2, 4, 7, на кластере цитокинов, на хромосоме 5 и на хромосоме 6 в области MHC.
Authors discussed genetic component development of bronchial asthma. Candidate genes located on chromosomes 2, 4, 7, on a cluster of cytokines, on chromosome 5 and on chromosome 6 in the MHC.
Бронхиальная астма (БА) — заболевание с выраженной наследственной предрасположенностью. Дети, имеющие родственников первой линии родства с БА, имеют высокий риск развития клинических проявлений астмы [1]. Некоторые клиницисты большое внимание уделяют признакам мезенхимальной дисплазии как внешним маркерам генетических особенностей. У пациентов с БА часто встречаются множественные стигмы дисморфогенеза, патология соединительной ткани, кожные факомы. По итогам близнецовых исследований, генетический вклад в развитие БА оценивается в 30-70%.
Риск атопии у пробанда при достижении им возраста 7 лет в зависимости от наличия атопии в семейном анамнезе
| Семейный анамнез | Риск развития атопии (%) |
| Нет атопии | 10 |
| Один из родителей страдает атопией | 20 |
| Сиблинги страдают атопией | 35 |
| Оба родителя страдают атопией, но разными вариантами | 42 |
| Оба родителя страдают атопией, клиническая форма идентична | 75 |
БА — типичное заболевание мультифакториальной природы, развитие которого определяется взаимодействием наследственных факторов (мутаций или сочетаний аллелей) и факторов среды.
В последние годы генетические исследования при астме ведутся по нескольким направлениям: выявление вариантов генов, которые могут предсказать ответ на терапию, выявление вариантов генов, которые связаны с развитием болезни и играющих решающую роль в патофизиологии заболевания.
Верифицированы несколько групп генов-кандидатов, которые важны в развитии БА.
Гены атопии или гуморального иммунного ответа локализованы в участках хромосомы 5q24-33 и содержат кластер семейства генов цитокинов (IL-4, IL-5, IL-13, IL-3, GM-CSF), ответственный за развитие реакций немедленного типа (IgE-опосредованных реакций). IL-4, IL-13 экспрессируются Th-2 лимфоцитами и способствуют переключению В-клеток на синтез IgE. IL-5 и GM-CSF — цитокины, обеспечивающие созревание, выживание и хемотаксис эозинофилов. К этой группе также относят HLA-DR (гены молекул II класса МНС) — важные молекулы, участвующие в презентации антигена. Имеющиеся сегодня данные свидетельствуют, что полиморфизм генов интерлейкинов и их рецепторов является важным генетическим фактором возникновения БА и атопии [2, 3].
Гены рецепторных молекул (IL-4Rα, FcεRI β, ADRβ2). IL-4Rα — альфа цепь рецептора IL-4. Mitsuyasu et al. [4] сообщили о полиморфном варианте гена Ile50Val IL-4Rα цепи, наличие которого повышает синтез IgE и является одним из определяющих наследственных факторов возникновения атопической формы заболевания. В 17% случаев замена одного аминокислотного остатка (изолейцина лейцином в позиции 181) в гене, кодирующем β-субъединицу высокоаффинного рецептора к IgE (FcεRI β), приводит к развитию бронхиальной астмы. Однако аналогичные исследования, проведенные в Италии и Японии, такой закономерности не выявили.
Продукт ADRβ2 (гена β2-адренергического рецептора; 11q13) контролирует лабильность бронхов. Установлен полиморфизм гена ADRβ2 (Arg16Gly и Glu27Gln), определяющий повышенную вероятность развития тяжелой бронхиальной астмы. Более того, больные гомозиготные по этим вариантам гена быстро теряют чувствительность к β2-агонистам и требуют лечения гормональными препаратами [5]. Это является одним из достижений в фармакогенетике БА. Причем ген рецептора IL-4 (IL4RA) и ген, кодирующий β-субъединицу высокоаффинного рецептора к IgE (FcεRI β), могут быть отнесены к генам атопии, а ген ADRβ2 — к генам бронхиальной гиперреактивности.
Южнокорейскими учеными [6] выявлены 2 полиморфных гена CRTH2, экспрессирующихся на поверхности эозинофилов, с однонуклеотидными заменами -466T>C и -129C>A, которые тесно связаны с инфильтрацией эозинофилами дыхательных путей у больных с аспирин-индуцированной БА. Гены факторов транскрипции — STAT6, JAK1, JAK3 [7] ассоциированы с наличием БА. Последний мета-анализ объединил результаты 11 исследований [8]. Выявлены хромосомные регионы, содержащие ведущие гены восприимчивости к БА, при использовании самых строгих статистических критериев. К ним относятся 6p22.3-p21.1 (гиперактивность бронхов), 5q11.2-q14.3 и 6pter-p22.3 (концентрация общего IgE), 3p22.1-q22.1, и 17p12-q24.3 (положительный кожный тест). Однако никакой преобладающей ассоциации среди указанных регионов не обнаружено, что объясняет гетерогенность болезни и вариабельность диагноза в разных популяциях разных стран.
Признано, что многочисленные гены взаимодействуют между собой при БА и атопии, повышая или уменьшая риск развития болезни. При наличии генов, кодирующих IL-13 и IL-4RA (обе ключевые молекулы в Th-2 сигнализации), выявлен в 2,5 раза больший риск развития БА, чем у индивидуумов с наличием одного гена. Исследование четырех генов показало, что комбинация определенного однонуклеотидного полиморфизма (SNPs) в IL-13, IL-4, IL4RА, и STAT 6 сопровождается 16,8-кратным увеличением риска БА. Эти сведения указывают на значение изучения взаимодействия генов при сложных болезнях и объясняют их роль в развитии и прогрессировании болезни.
Имеется предположение, что эндогенная БА — аутоиммунное заболевание, опосредованное аутоантителами к эпителиальному антигену. Не исключено, что появление аутоантител связано с генетически обусловленным дефицитом антиоксидантной системы. Свободные радикалы способны превращать макромолекулы в аутоантигены. На их возникновение иммунная система отвечает выработкой специфических аутоантител. В организме запускается аутоиммунный процесс, который в конечном итоге и приводит к БА. В этой связи относительно недавно обнаружена субпопуляция T-хелперов, названная Th17 [9], играющая значимую роль при аутоиммунных заболеваниях.
IL-17 является эффекторным цитокином, который продуцируют Th17 клетки, и его повышенная концентрация выявлена в слюне больных БА [10]. Однако имеются исследования [11] о варианте гена IL-17, His161Arg, который ассоциирован с протективным эффектом при астме. В 2009 году обнаружены новые гены восприимчивости к БА, не связанные с иммунной системой. Полиморфизм генов хитиназы и хитиназоподобных белков CHIT1, CHIA, CHI3L1 сочетается с риском БА.
Относительно недавно был охарактеризован первый позиционно клонированный ген астмы ADAM33 [12] на хромосоме 20p13. Анализ 135 однонуклеотидных полиморфизмов в 23 из них показал наиболее существенную ассоциацию заболевания с вариантом гена ADAM33, который кодирует металлопротеазу, играющую важную роль в функционировании гладких мышц бронхов и фибробластов легкого. Эти данные свидетельствуют о важной роли ADAM33 в ремоделировании дыхательных путей. В настоящее время роль этих генетических вариаций, связанных с восприимчивостью к астме, подтверждена в Саудовской Аравии, Китае [13]. В локусе хромосомы 1q31 в 2010 году был идентифицирован ген DENND1B, который экспрессируется натуральными киллерами и дендритными клетками, кодирует белок, взаимодействующий с рецептором фактора некроза опухоли, и связан с развитием БА [14].
Гены-модификаторы (GSTM1, GSTT1, CYP2E1, NAT2, SLC11A1). На сегодняшний день известно, что в патологии БА принимают участия белковые продукты генов системы детоксикации ксенобиотиков. Недавними исследованиями Сардарян И.С. [15] изучены фенотипические особенности БА при аллельном полиморфизме генов глутатион-S-трансферазы Т1 (GSTT1), глутатион-S-трансферазы М1 (GSTM1), ангиотензин превращающего фермента (ACE), эндотелиальной синтазы оксида азота (eNOS). Выявлено, что ассоциация генотипов GSTT1-\GSTM1‑ повышает в 5 раз риск развития БА у детей по сравнению с популяцией. У детей при функционально активном генотипе GSTT1+\GSTM1+ в ассоциации с полиморфизмом I\I по гену АСЕ риск развития БА снижается в 7 раз, что позволяет считать данную ассоциацию генотипов протективной.
В заключение можно указать, что к развитию астмы причастны много генов, расположенных на разных хромосомах. Прежде всего это генный комплекс HLA на 6-й хромосоме. Кроме того, с развитием БА связаны:
- локусы 2 pter*
- 2q6 (реакция на домашних клещей)
- 2q33 (CD28; белок, связывающий инсулиноподобный фактор)
- 3p24.2-p22 (С-С рецептор хемокина)*
- 4q35 (интерферонорегулирующий фактор-2)*
- 5q15 (ген не идентифицирован)
- 5q23-q33 (IL-3; IL-4; IL-5; IL-9; IL-13; глюкокортикоидный рецептор)**
- 5q31 (гены регуляции IgE). В непосредственной близости расположены гены бронхиальной гиперреактивности и адренергических b2 рецепторов
- 6p21.1-p23 (HLA, фактор некроза опухолей α)*
- 7р15.2 (Т-клеточный рецептор G, IL-6)*
- 9q31.1 (тропомиозин связывающий белок)*
- 11р15 (ген не идентифицирован)
- 11q13 (ген b-цепи высоко аффинного IgE рецептора, триггер аллергических реакций на мастоцитах, передается по материнской линии, отцовский «импринтинг» вероятен)**
- 12q (синтаза оксида азота)
- 12q14-q24.33 (сигнальный кондуктор и активатор транскрипции 6; интерферон γ; фактор стволовых клеток; инсулин-подобный фактор роста 1; лейкотриен А4 гидролаза; β субъединица ядерного фактора Y; В-клеточный транслокационный ген 1)**
- 13q14.3-qtep (трансляционно контролируемый протеин-1 опухоли)*
- 16q22.1-q24.2 (ген не идентифицирован)
- 17p11.1-q11.2 (хемокиновый кластер)
- 19q13 (CD22)
- 21q21 (ген не идентифицирован)
- Xq28/Yq28 (рецептор IL-9)
* — общие гены с атопией; ** — общие гены с атопией и атопическим дерматитом
Данный перечень генов, ответственных за развитие БА, не полон. Не упомянуты гены, участвующие в ремоделировании дыхательных путей, гетерогенна и гиперреактивность дыхательных путей. Все это делает понятным клинический полиморфизм заболевания.
Будет ли возможно в будущем предсказать развитие БА, базируясь на генетическом тестировании? Предсказующая величина тестирования единственного гена при полигенном наследовании болезни очень ограничена как для диагностики, так и в профилактических целях. В будущем прогноз астмы, возможно, будет основываться на оценке комплекса генов, персональных факторов и факторов риска окружающей среды, вместе содействующих развитию, персистенции, прогрессированию или ремиссии БА [16, 17].
Ю.И. Будчанов, В.М. Делягин
Тверская государственная медицинская академия
Федеральный научно-клинический центр детской гематологии, онкологии и иммунологии, г. Москва
Будчанов Юрий Иванович — кандидат медицинских наук, доцент кафедры клинической иммунологии с аллергологией Тверской государственной медицинской академии.
1. Burr M., Merrett T., Dunstan F., Maguire M. The development of allergy in high-risk children // Clinical and Experimental Allergy, 1997. — v. 27. — Р. 1247-1252.
2. Фрейдин М.Б., Огородова Л.М., Пузырев В.П. Вклад полиморфизма генов интерлейкинов в изменчивость количественных факторов риска атопической бронхиальной астмы // Мед. генетика, 2003. — Т. 2. — № 3. — С. 130-135.
3. Фрейдин М.Б., Брагина Е.Ю., Огородова Л.М., Пузырев В.П. Генетика атопии: современное состояние. // Вестник ВОГиС, 2006. — Том 10. — № 3 — С. 492-503.
4. Mitsuyasu H., Izuhara K., Mao X.-Q. et al. Ile50Val variants or IL4Ra upregulates IgE synthesis and associates with atopic asthma // Nat. genet., 1998. — v. 19. — Р. 119-120.
5. Wechsler M., Lehman E., Lazarus S. et al. National Heart, Lung and Blood Institute’s Asthma Clinical Research Network. beta-Adrenergic receptor polymorphisms and response to salmeterol //American Journal Respir. Crit. Care Medicine, 2006. — v. 173. — P. 519-526.
6. Palikhe N., Kim S-H., Cho B-Y. et al. Genetic variability in CRTH2 polymorphism increases eotaxin-2 levels in patients with aspirin exacerbated respiratory disease // Allergy, 2010. — v. 65. — Р. 338-346.
7. Moller M., Gravenor M., Roberts S. et al. Genetic haplotypes of Th-2 immune signalling link allergy to enhanced protection to parasitic worms. // Human Molecular Genetics, 2007. — v. 16. — Р. 1828-1836.
8. Denham S., Koppelman G, Blakey J. et al. Meta-analysis of genome-wide linkage studies of asthma and related traits // Respir. Research, 2008. — v. 9. — р. 38.
9. Weaver C., Hatton R., Mangan P., Harrington L. IL-17 family cytokines and the expanding diversity of effector T cell lineages // Annual Revy Immunology, 2007. — 25. — Р. 821-852.
10. Bullens D., Truyen E., Coteur L. et al. IL-17 mRNA in sputum of asthmatic patients: linking T cell driven inflammation and ranulocytic influx? // Respir. Res., 2006. — v. 7. — Р. 135.
11. Kawaguchi M., Takahashi D., Hizawa N. et al. IL-17F sequence variant (His161Arg) is associated with protection against asthma and antagonizes wild-type IL-17F activity // Journal of Allergy and Clinical Immunology, 2006. — v. 117. — Р. 795-801.
12. Van Eerdewegh P., Little R., Dupuis J. et al. Association of the ADAM33 gene with asthma and bronchial hyperresponsiveness // Nature, 2002. — v. 418. — Р. 426-430.
13. Bazzi M., Al-Anazi M., Al-Tassan N.A. et al. Genetic variations of ADAM33 in normal versus asthmatic Saudi patients // http://biotechcentersa.org/asthma-genetics/.
14. Sleiman P., Flory J., Imielinski M. et al. Variants of DENND1B associated with asthma in children // New England Journal of Medicine, 2010. — v. 362. — Р. 36-44.
15. Сардарян И.С. Фенотипические особенности бронхиальной астмы у детей при различных аллельных полиморфизмах генов «предрасположенности» (GSTТ1, GSTМ1, ACE, eNOS) / Автореф. дисс. к.м.н. — СПб, 2009. — 22 с.
16. Koppelman G., te Meerman G., Postma D. Genetic testing for asthma // Eur. Respir. J., 2008. — v. 32. — Р. 775-782.
17. Postma D., Koppelman G. Genetics of asthma: where are we and where do we go? // The Proceedings of the American Thoracic Society, 2009. — v. 6. — Р. 283-287.
источник
Многих родителей, страдающих заболеваниями дыхательных путей, волнует вопрос о генетической предрасположенности детей к этим болезням. Многие не знают точно, передается астма по наследству или нет. Генетики предполагают, что есть высокая вероятность заболеть, если родитель страдает от хронического воспаления дыхательных путей.
Радует то, что с симптомами заболевания реально бороться. Но нужно быть осторожным, чтобы, например, обычная аллергия не переросла в астму. Если в семье есть аллергик или астматик, родителям стоит быть настороже и заботиться о здоровье своих детей.
Астма считается мультифакторным заболеванием. Это значит, что в ее развитии принимает участие много внешних и внутренних факторов. И в этом случае наследственность отходит на второй план.
Можно даже говорить о том, что астма по наследству не передается. По мере развития медицинской науки выявляются новые источники, которые влияют на развитие болезни. Среди них стоит выделить две основные группы:
- Внешние факторы прямого воздействия.
- Физиологическое состояние организма.
Первая группа — экзогенные факторы. К ним можно отнести провокаторы аллергической реакции. Это:
- плесневые грибы, различные продукты, пыльца растений, шерсть животных;
- бактерии и вирусы;
- вредная работа на опасных производствах, частый контакт с раздражающими веществами;
- экологическая ситуация;
- курение сигарет;
- инфекционные заболевания;
- неправильное питание.
Вторая группа — эндогенные факторы:
- ожирение разной степени тяжести;
- бронхит, который возникает чаще, чем несколько раз в год;
- наличие определенных заболеваний у матери или отца;
- гендерность. Если передача заболевания происходит на генетическом уровне, то чаще всего от матери.
Следует уточнить, что передача предрасположенности к астме со стороны женщин провоцирует более тяжелое течение заболевания. Если ген передал мужчина, то симптомы будут не такими яркими, а сама астма протекает намного легче.
Конечно, если родители страдают бронхиальной астмой, то велик риск ее появления у наследников. Но это не на 100%, потому как генетику спрогнозировать невозможно. Стоит отметить, что на развитие заболеваний дыхательных путей влияет излишняя гигиена.
Часто это происходит, пока ребенок маленький. Медики утверждают, что если мыть руки много раз в день, особенно антибактериальным мылом, нарушится естественная микрофлора. Иммунитету будет просто не с чем бороться. Для его хорошей работы нужны и болезнетворные бактерии, чтобы он активизировался.
При избыточной гигиене иммунитет начнет реагировать на любые поступающие в организм вещества и даст реакцию в виде аллергии. Многим известно, что те дети, которым дают больше самостоятельности, меньше подвержены бронхиальным заболеваниям.
Напротив, если соблюдать все меры предосторожности, постоянно мыть руки, то можно заболеть. Все хорошо в меру, о гигиене стоит беспокоиться, но растить ребенка в стерильных условиях неправильно.
Стоит сразу отметить, что сама астма не передается по наследству. А вот предрасположенность к ней переходит. Если родитель беспокоится, передается ли бронхиальная астма от родителей по наследству, то можно сказать, что на заболевание влияет не только генный фактор. Чтобы у ребенка проявились астматические симптомы, должно сойтись несколько условий:
- предрасположенность на генном уровне;
- наличие экзогенных факторов, которые оказывают воздействие на развитие бронхиальной астмы.
Чтобы понять, как гены родителей влияют на появление заболевания у детей, генетики постоянно проводят исследования, а также ведут статистический учет.
Несколько статистических данных:
- В 10% случаев дети абсолютно здоровых родителей, без признаков бронхиальной астмы, могут ею заболеть.
- Когда от недуга страдает мать или отец, болезнь может развиться в 20% случаев. Вероятность в 35% наблюдается, когда болеют оба родителя.
- Ситуация осложняется, если у родителей наблюдаются аллергические проявления, и к тому же один из них астматик. Целых 42% говорят о том, что ребенок может унаследовать болезнь.
- Когда от астмы страдают оба родителя, то в 75 случаях из 100 у детей может возникнуть астма. Болезнь заявляет о себе до семилетия ребенка.
Ученые нашли, какие гены отвечают за предрасположенность к развитию бронхиальной астмы. Их более 50. Находятся они в пятой и одиннадцатой хромосоме. Задача этих генов — вырабатывать специфические антитела.
Заболевание сложно выявить :
- Бронхиальная астма может развиться в разном возрасте. Больше вероятность того, что она проявится у детей до семи лет. Возникает также у взрослых, которые не реагировали на проявления аллергии, и она переросла в астму. Можно заболеть и в пожилом возрасте, если есть предрасположенность.
- Заболевание возникает на фоне внутренних факторов. Это может быть инфекционное заболевание, простуда, наличие лишнего веса, применение лекарственных препаратов.
- Так как реакции больных индивидуальны, то классифицировать признаки можно только приблизительно. Приступы у больных разных возрастных групп проходят по-разному, реакция организма на применяемые лекарственные препараты тоже отличается .
Стоит отметить, что проявления астматической болезни при наследственной предрасположенности можно предупредить. Для этого нужно соблюдать осторожность еще при внутриутробном развитии ребенка, а после его рождения принимать профилактические меры.
Беременность – это очень ответственное время. Каждая стадия важна для развития будущего ребенка. Например, во время эмбрионального развития закладываются зачатки будущего иммунитета.
Возможность бороться с различного рода вирусами, микробами, находится в прямой зависимости от того, какие гены в этом участвовали. Так как ДНК ребенка содержит гены отца и матери, то и проблемы он унаследует в равной степени.
Астма по наследству может передаться, если даже один из родителей болел. Эти гены уже будут в ДНК. Развитие заболевания зависит от того, сколько генов, перешедших от носителя, займут место в генной структуре эмбриона. Соответственно, чем больше количество, тем больше предрасположенность.
Родителям, конечно же, хочется знать, унаследовал ли новорожденный предрасположенность к астме. Если она есть, то у ребенка может возникнуть приступ удушья. Его появление могут спровоцировать следующие факторы:
- перевод с грудного молока на сухую смесь;
- начало прикорма;
- пыль в помещении;
- шерсть;
- цветочная пыльца.
Бывает, что астма никак не проявляет себя, вплоть до преклонного возраста человека. Это говорит о том, что хоть у него и была высокая вероятность заболеть, но при этом иммунитет был очень высоким. Поэтому болезнь долгое время себя никак не проявляла. Со временем защитная функция иммунитета ослабевает, и человек сталкивается с первым приступом астмы.
Обобщая, можно сказать, что, как и отец, мать может передать предрасположенность к заболеванию дыхательных путей. Но при этом развитие болезни можно приостановить, если соблюдать профилактические меры.
Будущие родители часто задают себе вопрос, может ли астма передаться по наследству от отца. Медициной установлено, что если болезнь идет по женской линии, то протекать у ребенка астма будет сложнее.
Генетики доказали, что отец также может передать предрасположенность к бронхиальной астме. Поэтому с определенной долей вероятности можно утверждать, что если будущий отец болен, то и ребенок попадает в группу риска. Примерно в 10% случаев виноват в развитии болезни отец.
Особенности проявления заболевания таковы:
- дети мужского пола болеют чаще, но симптомы бронхиальной астмы у них не сильно выражены;
- девочки могут болеть не так часто, но при этом астма будет тяжело протекать.
Если предрасположенность к бронхиальной астме передается со стороны матери, то автоматически повышается риск развития осложнений. Основные симптомы при этом состоянии:
- частые приступы нехватки воздуха;
- непрекращающийся кашель;
- повышенное выделение пота;
- нехватка кислорода.
Что характерно, если папа болеет астмой, то велика вероятность, что и ребенок заболеет. А вот уже родившегося ребенка заразить отец не может. Когда у отца бронхиальная астма, а у матери она отсутствует, такое сочетание порождает высокую степень сопротивляемости.
Врачами установлено, что передается предрасположенность к возникновению астмы, а не само заболевание. Поэтому, астма – это результат воздействия наследственных и внешних факторов.
Когда болеет один из родителей, то риск передачи генов заболевания ребенку очень велик. Хоть на возникновение бронхиальной астмы и влияет наследственность, но болезнь поддается корректировке, если принимать меры профилактики.
Самое первое, что могут сделать родители ребенка, — это расспросить ближайших родственников о наличии аллергических проявлений. Между бронхиальной астмой и обычной аллергией есть прямая связь. Из-за реакции на пыльцу у отца начинается насморк.
В будущем у его ребенка может появиться экзема. Если не заниматься ее лечением, то велика вероятность развития бронхиальной астмы на фоне кожной болезни. Вот так простая аллергическая реакция на цветочную пыль запускает генетический механизм развития болезни дыхательных путей.
Астма не всегда проявляется в детском возрасте. Можно спокойно прожить более половины жизни, а потом столкнуться с этим недугом. Объясняется это тем, что у человека был высокий иммунитет, а внешние факторы не имели на него влияния.
Некоторые матери подвержены приступам бронхиальной астмы во время беременности. Если они быстро проходят и их можно купировать, то опасности для ребенка нет. С ним все будет в порядке, родится он в срок, с низким риском развития патологий.
Но не всегда астма протекает легко. Если приступы тяжелые, то это состояние скажется на ребенке. Возникает большой риск преждевременных родов, ребенок может родиться с недостаточным весом . Врачи предупреждают о том, что за такими детьми нужно следить внимательнее. Вследствие того что дыхательные пути не защищены в должной степени, риск развития болезней более высокий.
Развитие астматических проявлений реально избежать, если:
- кормить ребенка грудью хотя бы один год;
- правильно вводить прикорм;
- соблюдать режим сна и питания;
- исключить внешние факторы, провоцирующие болезнь (бытовая пыль, пыльца, шерсть).
Для того чтобы болезнь не получила развития, следует принимать профилактические меры. Это гораздо легче, чем лечить бронхиальную астму. Для родителей важно заняться устранением экзогенных причин, ведь на эндогенные повлиять никак нельзя.
Если женщина раньше курила, то в период беременности сигареты должны исчезнуть из ее жизни. Курение — это один из усугубляющих факторов, который влияет на развитие заболевания дыхательных путей. Родив ребенка, к вредной привычке возвращаться не нужно, потому что предстоит грудное вскармливание.
От него нельзя отказываться ни в коем случае. С молоком матери ребенок получает антитела, способствующие развитию иммунитета . К тому же грудное вскармливание является хорошей профилактической мерой.
Нельзя недооценивать влияние на развитие болезни внешних факторов, потому что, хоть передается астма на генном уровне, но провоцируют ее развитие экзогенные факторы.
Условно существует три вида факторов:
- бытовые аллергены;
- воздействие окружающей среды;
- прочие факторы.
Для устранения провокаторов первого вида должны соблюдаться следующие рекомендации:
- В течение дня несколько раз следует проветривать комнаты, делать влажную уборку.
- Вытравить насекомых, в первую очередь тараканов.
- Побороть плесень.
- Родителям нужно отказаться от сигарет.
- Своевременно менять и чистить фильтры в кондиционерах.
- Не допускать контакт с цветочной пыльцой.
- Избегать физического переутомления в холодное время года.
- С осторожностью применять лекарственные препараты, содержащие аспирин.
- Проходить ежегодную вакцинацию от гриппа.
- Вовремя лечить сопутствующие болезни.
- Следить за весом.
- Избегать стрессов.
Если бронхиальная астма уже проявилась, задача родителей — следить за интенсивностью приступов. Нельзя допускать, чтобы острые приступы были частым явлением. Когда предрасположенность к заболеванию передается от мамы, приступы удушья случаются чаще. Чтобы снизить их проявление, следует соблюдать правила профилактики:
- В идеале вся семья должна придерживаться принципов правильного питания. На примере родителей ребенок должен видеть, что отсутствие вредных привычек – это норма.
- Нужно регулярно заниматься физическими упражнениями, а также освоить дыхательную гимнастику.
- Лекарственные препараты принимать только по рекомендации врача. Самолечение может негативно сказаться на состоянии больного.
- Не стоит приобретать продукты, в которых содержаться консерванты.
- Инфекции усугубляют протекание болезни, поэтому их надо быстро лечить.
- Каждые полгода или год следует проходить медосмотр.
- По возможности отказаться от домашних животных.
- После вирусного заболевания следует оградить ребенка от общения с другими детьми и взрослыми. Это временная мера, пока не восстановится иммунитет.
- Полезно закаляться с помощью холодной воды. Эта процедура благотворно влияет на иммунитет.
- Нужно исключить из рациона ребенка копчености, газировку, цитрусы, чересчур острые блюда.
Бронхиальная астма – это болезнь дыхательных путей, которая передается по наследству. Точнее сказать, передается предрасположенность к ней.
Ученые выявили гены, которые за это отвечают. Если носителем гена является женщина, то у ребенка бронхиальная астма может протекать довольно тяжело. У девочек зафиксированы более острые приступы, а у мальчиков они происходят чаще.
Если оба родителя являются астматиками, то им нужно очень пристально следить за развитием своего ребенка. У него болезнь может проявиться до семи лет.
Чтобы облегчить жизнь ребенка, родителям следует принимать профилактические меры. Гораздо легче предупредить развитие заболевания, чем лечить его.
источник
Роль генов интерлейкинов и их рецепторов в формировании предрасположенности к бронхиальной астме и атопии
Иммунный ответ при БА и/или атопии начинается с взаимодействия аллергена с дендритными клетками слизистой дыхательных путей. Взаимодействие посредством молекул класса II главного комплекса гистосовместимости CD1a+ дендроцитов с рецепторами Т-клеток стимулирует дифференциацию Th0-лимфоцитов в Th2-клетки, способные к секреции интерлейкина 10 (Ил-10) и цитокинов, чьи гены расположены на хромосоме 5q: Ил-3, -4, -5, -9, -13, GM-CSF, а функция тесно связана с гуморальным ответом. При действии антигенов микобактерий и некоторых вирусов CD4+ клетки превращаются в Th1-клетки, секретирующие Ил-2, интерферон-g (Ифн-g ) и лимфотоксин-? (фактор некроза опухолей-?). Поляризация в сторону Th2-ответа активируется Ил-4 и ингибируется Ифн-g и -a . Th1-ответ требует высвобождение Ил-12 макрофагами и дендритными клетками и супрессируется Ил-10 (цит. по: Holgate, 1997).
Th2-клетки высвобождают провоспалительные цитокины, главным образом Ил-4 и -13, которые, взаимодействуя со своими рецепторами на В-клетках, активируют транскрипцию генного локуса тяжелой цепи типа e иммуноглобулинов и вместе с сигналом, передаваемым молекулой CD40 В-клеток, индуцируют переключение изотипов с m на e (Stavnezer J., 1996).
IgE, высвобождаемый активированными В-клетками, связывается с высоко-аффинным (Fce R1) и низко-аффинным (Fce R2; CD23) рецепторами мастоцитов. Когда аллерген взаимодействует с IgE на мастоцитах, Fce R1 инициирует серию внутриклеточных событий, приводящих к высвобождению медиаторов воспаления и хемокинов: гистамина, простагландинов, лейкотриенов, фактора активации тромбоцитов, дегранулированных протеаз, эотаксина и др. (Galli S. J., 1993). Кроме того, эти медиаторы синтезируются эозинофилами, активированными Ил-3, -5, GM-CSF и др. (Gleich, Kita, 1997; Holgate, 1997). Действуя в совокупности, все эти факторы приводят к микроизменениям сосудов стенок воздухоносных путей, сокращениям гладкой мускулатуры бронхов, гиперсекреции слизи. Кроме того, цито- и хемокины, по крайней мере, частично ответственны за миграцию и активацию клеток воспаления и, таким образом, вносят вклад в сохранение патологического процесса (Ricci M. et al., 1997).
Приведенная схема развития воспаления при БА далеко не исчерпывающая. Однако она вполне приемлема с точки зрения поиска генетической основы БА, поскольку содержит все ключевые звенья патогенетического каскада заболевания. Учитывая значительное число агентов, участвующих в развитии воспаления, а также влияние негенетических факторов (наличие в среде аллергенов, возраст, климатические особенности и т.д.) на развитие БА, правомерна будет гипотеза о мультифакториальной природе заболевания. Это обстоятельство сильно осложняет генетический анализ БА. К настоящему моменту идентифицировано более 20 генов-кандидатов БА и атопии (Пузырев В. П. и др., 1998; табл.). Список этот отнюдь не полон и постоянно расширяется.
Гены-кандидаты бронхиальной астмы и атопии
(Пузырев и др., 1998; с дополнениями и изменениями)