Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Для лечения больных бронхиальной астмой наиболее приемлемы препараты группы преднизолона и триамцинолона.
При очень тяжелом течении бронхиальной астмы и при отсутствии эффекта от остальных методов лечения рекомендуется применять препараты короткого действия (преднизон, преднизалон, метилпреднизолон).
Системная глюкокортикоидная терапия проводится только по строгим показаниям:
- очень тяжелое течение бронхиальной астмы при отсутствии эффекта от всех остальных методов лечения;
- кортикозависимая бронхиальная астма (т.е. когда больной уже длительно лечится глюкокортикоидами и в данный момент отменить их невозможно);
- астматический статус (глюкокортикоиды применяются парентерально);
- кома при бронхиальной астме (глюкокортикоиды применяются парентерально);

Системная глюкокортикоидная терапия обладает следующими механизмами действия:
- стабилизирует тучные клетки, предупреждает ихдегрануляцию и выход медиаторов аллергии и воспаления;
- блокируют образование IgE (реагинов);
- подавляют позднюю астматическую реакцию, что обусловлено подавлением клеточной воспалительной реакции вследствие перераспределения лимфоцитов и моноцитов, угнетением способности нейтрофи-лов к миграции из сосудистого русла, перераспределением эозинофилов. Поздняя астматическая рекция начинается через 3-4 ч после воздействия аллергена, максимум ее наблюдается через 12 ч, продолжается более 12 ч; она отражает механизмы прогрессирования бронхиальной астмы. Гиперреактивность бронхов, сохраняющаяся длительно (в течение недель и месяцев), связана с поздней астматической реакцией;
- стабилизируют лизосомальные мембраны и уменьшают выход лизосомальных ферментов, повреждающих бронхопульмональную систему;
- подавляют сосудорасширяющее действие гистамина;
- увеличивают количество и чувствительность бета-адренорецепторов бронхов к бронхорасширяющим воздействиям адреномиметаков;
- уменьшают отек слизистой оболочки бронхов;
- повышают активность эндогенных катехоламинов;
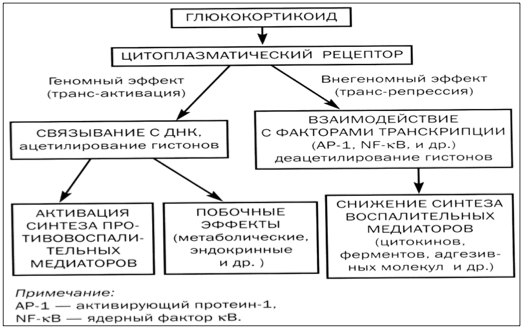
После проникновения в клетку глюкокортикоиды связываются со специфическими цитоплазматическими рецепторами, образуя комплекс гормон-рецептор, взаимодействующий в ядре клетки с хроматином. В результате активируется синтез белков, опосредующих эффекты глюкокортикоидов. Весь процесс занимает около 6 ч, поэтому глюкокортикоиды не купируют приступы удушья при обострении бронхиальной астмы, они действуют не ранее 6 ч после их введения.
Используются 3 группы глюкокортикоидов:
- группа преднизолона: преднизолон (таблетки по 0.005 г; ампулы по 1 мл с содержанием 30 мг препарата); метилпреднизолон (метипред, урбазон — таблетки по 0.004 г);
- группа триамцинолона: триамцинолон, кенакорт, полькортолон, берликорт (таблетки по 0.004 г);
- группа дексаметазона: дексаметазон, дексон, дексазон (таблетки по 0.0005 г; ампулы для внутривенного и внутримышечного введения по 1 и 2 мл 0.4%-раствора с содержанием препарата 4 и 8 мг соответственно).
Методика лечения по М. Э. Гершвину (1984):
- при обострении начинать с высоких доз (например, 40-80 мг преднизолона ежедневно);
- после уменьшения симптомов — медленно снижать дозу (в течение 5-7 дней) до поддерживающей, например, на 50% каждый день;
- для хронического (длительного) лечения применять ежедневную дозу преднизолона ниже 10 мг;
- принимать препарат в первой половине дня;
- в начале лечения дневную дозу разделить на 2-3 приема;
- если требуется прием более 7.5 мг преднизолона в день, предпринять попытку прерывистой терапии (например, 15 мг преднизолона через день вместо ежедневного приема 7.5 мг);
- для снижения суточной пероральной дозы преднизолона можно заменить часть принимаемого внутрь препарата ингаляцией бекотида, исходя из того, что 6 мг преднизолона равны по активности 400 мг бекотида.
В. И. Трофимов (1996) рекомендует начинать терапию таблетированными глюкокортиковдами с суточной дозы 20-40 мг преднизолона или 16-32 мг метипреда, триамцинолона 2/3 — 3/4 суточной дозы больной должен принимать утром после завтрака, остальную часть — после обеда (до 15.00) в соответствии с циркадными ритмами продукции глюкокортикоидов и чувствительности к ним тканей и клеток организма. После значительного улучшения состояния больного (отсутствие приступов удушья в течение 7-10 дней) можно снижать дозу глюкокортикоидов на 1/2 таблетки в 3 дня, а при достижении дозы 10 мгДуг преднизолона или эквивалентной дозы другого препарата — на 1/4 таблетки за 3 дня до полной отмены или сохранения поддерживающей дозы (обычно 1,1/2 таблетки). Если больной получал глюкокортикоиды длительно (более 6 месяцев), снижение дозы нужно производить более медленно: на 1/2 — 1/4 таблетки за 7-14 и более дней.
Рекомендуется сочетать прием глюкокортикоидов внутрь с использованием их ингаляционных форм, что позволяет значительно уменьшить лечебную и поддерживающую дозы пероральных препаратов.
При необходимости длительного применения глюкокортикоидов для контроля за астмой тяжелого течения целесообразно использование альтернирующей схемы приема (удвоенной суточной дозы через день 1 раз в сутки утром), что позволяет уменьшить риск угнетения надпочечников и развития системных побочных эффектов. Короткий период полураспада пероральных глюкокортикоидов группы преднизолона и триамцинолона позволяет применять альтернирующую схему. Следует подчеркнуть что альтернирующая схема приема глюкокортикоидов обычно приемлема тогда, когда с помощью ежедневного их приема уже удалось добиться улучшения течения астмы и снизить суточную дозу преднизолона до 5-7.5 мг/день; однако, если наступило ухудшение состояния, необходимо вернуться к ежедневному приему препарата. При очень тяжелом течении астмы альтернирующая схема неэффективна, приходится применять глюкокортикоиды ежедневно и даже 2 раза в день.
Согласно совместному докладу Национального института сердца, легких и крови (США) и ВОЗ «Бронхиальная астма. Глобальная стратегия» — короткий курс лечения пероральными глюкокортикоидами (5-7 дней) может быть использован как «максимальная терапия» для достижения контроля течения астмы у больного. Этот курс может применяться или в начале лечения больного с неконтролируемой астмой или в течение периода, когда больной отмечает постепенное ухудшение своего состояния. Побочные эффекты при коротких курсах (менее 10 дней), как правило, не наблюдаются, отменять глюкокортикоиды можно сразу после коротких курсов.
При наличии противопоказаний к приему глюкокортикоидных препаратов внутрь (эрозивный гастрит, язвенная болезнь желудка и двенадцатиперстной кишки) можно применить кенолог-40 (препарат триамцинолона продленного действия) внутримышечно в дозе 1-2 мл (40-80 мг) 1 раз в 4 недели.
Количество инъекций на курс лечения и интервалы между инъекциями определяются индивидуально, однако, к сожалению, при продолжительном лечении длительность эффекта уменьшается и возникает необходимость более частых введений. Некоторые больные, страдающие кортикозависимым вариантом бронхиальной астмы, вместо систематического перорального приема глюкокортикоидов применяют внутримышечное введение кеналога 1 раз в 3-4 недели.
При выраженных обострениях, тяжелых приступах бронхиальной астмы, угрожающих развитием астматического состояния, нередко приходится применять большие дозы глюкокортикоидов внутривенно через короткие интервалы времени. Считается, что оптимальная концентрация глюкокортикоидов в плазме достигается при введении гидрокортизона гемисукцината в дозе 4-8 мг/кг или преднизолона в дозе 1-2 мг/кг с интервалами 4-6 ч. Более эффективно внутривенное капельное введение глюкокортикоидов, которое может производиться 1-4 раза в сутки в зависимости от состояния больного. Обычно курс лечения внутривенными капельными вливаниями глюкокортикоидов до достижения оптимального эффекта составляет 3-7 дней, после чего глюкокортикоиды отменяют, постепенно снижая дозу на 1/4 начальной суточной дозы, добавляя ингаляционные глюкокортикоиды.
При глюкокортикозависимой бронхиальной астме отменить полностью глюкокортикоиды невозможно, достаточно активной оказывается суточная доза преднизолона 5-10 мг.
Большинство пульмонологов считает противопоказанной системную пероральную глюкокортакоидную терапию в первом триместре беременности из-за высокого риска развития уродств у плода. Ингаляционные глюкокортикоиды могут применяться для лечения бронхиальной астмы (в дозе не более 1000 мкг в сутки) в течение всего периода беременности, т.к. их системные побочные эффекты незначительны, а риск гибели плода вследствие гипоксии при приступах астмы велик.
Небольшие дозы глюкокортикоидов при необходимости можно назначать внутрь во II-III триместрах в комбинации с ингаляционными глюкокортикоидами. При тяжелом приступе астмы и астматическом статусе показано внутривенное введение глюкокортикоидов.
Побочные эффекты системного лечения глюкокортикоидами:
- ожирение, преимущественно в области груди, живота, шейного отдела позвоночника, появление лунообразного гиперемированного лица;
- психозы, эмоциональная лабильность;
- истончение, сухость кожи, багрово-фиолетовые стрии;
- акне, гирсутизм;
- атрофия мышц;
- остеопороз, в т.ч. позвоночника (возможны переломы позвоночника);
- гиперсекреция и повышение кислотности желудочного сока, развитие язв желудка и двенадцатиперстной кишки;
- гипергликемия (стероидный сахарный диабет);
- артериальная гипертензия;
- задержка натрия, отеки;
- задняя субкапсулярная катаракта;
- активизация туберкулезного процесса;
- угнетение функции надпочечников.
Внезапная отмена глюкокортикоидов после длительного их применения, особенно в больших дозах, приводит к быстрому появлению синдрома отмены, который проявляется:
- ухудшением течения бронхиальной астмы, возобновлением приступов удушья, возможным развитием астматического статуса;
- значительным падением артериального давления;
- резкой слабостью;
- тошнотой, рвотой;
- артралгией, миалгией;
- болями в животе;
- головной болью.
Для уменьшения развития побочных явлений глюкокортиковдной терапии и для уменьшения кортикозависимости рекомендуется:
- стараться обходиться меньшими дозами препарата;
- сочетать лечение с ингаляциями интала;
- назначать короткодействующие препараты (преднизолон, урбазон, полькортолон) и не применять длительно действующие глюкокортикоиды (кеналог, дексазон и др.);
- назначать глюкокортикоид в первой половине дня, наибольшую часть суточной дозы давать утром, чтобы концентрация препарата в крови совпадала с наибольшим выбросом эндогенного кортизола;
- поддерживающую дозу препарата (1.5-2 таблетки) целесообразно давать прерывистым способом (т.е. удвоенную поддерживающую дозу принимать однократно утром, но через день). При таком приеме уменьшается возможность угнетения надпочечников и развития побочных явлений;
- для уменьшения кортикозависимости в момент снижения дозы преднизолона и перехода на поддерживающие дозы принимать этимиол по 0.1 г 3 раза в день (под контролем артериального давления), глициррам по 0.05 г 2-3 раза в день внутрь. Эти средства стимулируют надпочечники. Для уменьшения кортикозависимости можно применять также настойку диоскореи кавказской по 30 капель 3 раза в день;
- применять РДТ с сочетании с иглорефлексотерапией;
- для предупреждения или уменьшения побочных явлений пероральной глюкокортикоидной терапии целесообразно часть дозы заменить ингаляциями глюкокортикоидов;
- применять плазмаферез, гемосорбцию.
Одним из наиболее тяжелых осложнений системной глюкокортикоидной терапии является остеопороз. Для его профилактики и лечения применяются препараты, содержащие гормон С-клеток щитовидной железы кальцитонин — кальцитрин, миакалъцик. Кальцитрин назначается по 1 ЕД подкожно или внутримышечно ежедневно в течение месяца с перерывами каждый 7-й день (курс 25 инъекций) или по 3 ЕД через день (курс 15 инъекций). Миакальцик (кальцитонин лосося) вводится подкожно или внутримышечно по 50 ЕД (курс 4 недели). Можно применять также миакальцик в виде спрея интраназально по 50 ЕД через день в течение 2 месяцев с последующим двухмесячным перерывом. Лечение препаратами кальцитонина нужно проводить в сочетании с приемом кальция глюконата внутрь по 3-4 г/сут. Препараты кальцитонина способствуют поступлению кальция в костную ткань, уменьшают явления остеопороза, обладают противовоспалительным действием, уменьшают дегрануляцию тучных клеток и кортикозависимость.

источник
Использование ингаляционных форм глюкокортикоидов для лечения бронхиальной астмы (местная глюкокортикоидная терапия)
В настоящее время бронхиальная астма рассматривается как хронический воспалительный процесс в бронхах, приводящий к гиперреактивности и обструкции бронхов. В связи с этим, основным направлением в лечении бронхиальной астмы является противовоспалительная (базисная) терапия. К противовоспалительным средствам, используемым при лечении бронхиальной астмы, относятся глюкокортикоиды (ингаляционные формы) и стабилизаторы тучных клеток (интал, ломудал, недокромил, тайлед, дитек).
Противовоспалительная терапия с использованием ингалируемых глюкокортикоидов рекомендуется как первичная ступень терапии бронхиальной астмы средней и тяжелой степени с добавлением при необходимости Рз-адреномиметиков.
При лечении больных с легким персистирующим течением бронхиальной астмы, в случае отсутствия эффекта от эпизодического использования р-адреномиметиков, рекомендуется регулярно использовать ингаляции глюкокортикоидов.
При тяжелой кортикозависимой бронхиальной астме после достижения ремиссии с помощью глюкокортикоидов, принимаемых внутрь, рекомендуется переходить на ингаляции глюкокортикоидов с использованием больших доз (Salmeron, 1989).
Прием глюкокортикоидов в ингаляциях является важнейшей ступенью лечения бронхиальной астмы, так как ингалируемые глюкокортикоиды оказывают активное местное противовоспалительное действие, при этом системные побочные эффекты практически не развиваются (Utigev, 1993).
Механизм противовоспалительного действия ингаляционных глюкокортикоидов:
• препараты имеют высокое сродство к глюкокортикоидным рецепторам клеток, участвующих в воспалении, и взаимодействуют с этими рецепторами;
• образовавшийся комплекс влияет непосредственно на транскрипцию генов через взаимодействие с молекулой ДНК. При этом угнетается функция мРНК, ответственной за синтез протеинов воспаления, и образуется новая молекула мРНК, отвечающая за синтез противовоспалительных протеинов (липокортин или липомодулин, нейтральная
пептидаза и т.д.). Вновь синтезированные пептиды непосредственно угнетают фосфолипазу Аг, ответственную за продукцию противоспалительных простагландинов, лейкотриенов, фактора агрегации тромбоцитов.
Выделяют два поколения глюкокортикоидов в ингаляциях:
• препараты I поколения: бекотид, бекломет, бекодиск;
• препараты II поколения: будезонид, флюнизолид, флютиказона дипропионат.
Ингаляционные глюкокортикоиды 1-го поколения
Беклометазона дипропионат (бекломет, бекотид) — это 9
• суспензия для использования в небулайзере (в 1 мл 50 мкг);
• дисковые формы (бекодиски по 100 и 200 мкг), ингалируемые с по
мощью дискового ингалятора «Дискхайлер».
Беклометазона дипропионат является «пропрепаратом». Он метаболизируется в более активный метаболит беклометазона монопропионат во многих тканях, в т.ч. в легких и печени.
При вдыхании беклометазона дипропионата 30% его количества попадает в легкие и в них метаболизируется, около 70% осаждается в полости рта, глотки, проглатывается и активируется в печени до беклометазона мо-нопропионата. При применении больших доз беклометазона возможны системные побочные эффекты.
Бекотид (бекломет) в виде аэрозолей для ингаляций предназначается для длительного регулярного применения. Препарат не применяется для купирования приступов бронхиальной астмы, терапевтическое действие его проявляется только через несколько дней после начала лечения. Больные, которым ранее назначалась системная кортикостероидная терапия, должны продолжать ее еще в течение 1 недели после начала применения бекотида, затем можно попытаться постепенно понижать его дозу.
Обычная терапевтическая доза бекотида составляет 400 мкг в день, ее следует разделить на 2-4 разовые дозы (2-4 вдоха). При тяжелом течении бронхиальной астмы можно повысить суточную дозу до 1000-1500 мкг и даже 2000 мкг. Эта доза эффективна и не вызывает системных побочных действий, не угнетает коры надпочечников. При необходимости применять большие дозы бекотида целесообразно воспользоваться препаратом беко-тид-250 (1-2 вдоха 2-3 раза в день).
Поддерживающая доза препарата составляет 200-400 мкг в сутки при двукратном применении (утром и вечером). Снижение дозы до поддерживающей производится постепенно (на 1 ингаляцию каждые 3-7 дней).
При лечении бекотидом (беклометом) возможно осаждение препарата на слизистой полости рта, что способствует развитию кандидомикоза и фарингита. Для профилактики кандидомикоза полости рта ингаляции бекотида производятся с использованием специального дозатора-спейсера, который надевается на ингалятор, в результате чего частицы препарата, оседавшие в полости рта, задерживаются в камере-спейсере. После ингаляции бекотида целесообразно полоскать рот. При применении дозатора-спейсера количество препарата, достигающего легких, увеличивается.
Ингаляции бекотида могут частично заменить дозу глюкокортикоидов, принимаемых внутрь, и снизить кортикозависимость (400 мкг бекотида эквивалентны 6 мг преднизолона).
Бекодиск — в одной дозе содержит 100 и 200 мкг бекотида, в виде сухого вещества ингалируется в суточной дозе 800-1200 мкг (т.е. 1-2 вдоха 4 раза в день) с помощью специального ингалятора.
Беклометазона дипропионат выпускается в виде препарата беклокорт в 2 формах: мите и форте. Беклокортмите применяется в тех же дозах, что и бекотид. Беклокорт-форте, 1 доза которого содержит 250 мкг беклометазона дипропионата, обладает более длительным действием, чем беклокортмите, его следует применять по 1-2 ингаляции 2-3 раза в день.
Беклометазона дипропионат выпускается также в виде препарата альдецин. Он показан для лечения больных, у которых бронхиальная астма сочетается с вазомоторным аллергическим ринитом, полипозом носа. В упаковке препарата имеется сменная насадка для назальных ингаляций белометазона, а также насадка для ингаляций через рот Альдецин применяют по 1 ингаляции (50 мкг) в каждый носовой ход 4 раза в день или через оральную насадку ингалируют через рот (1-2 вдоха 4 раза в день)
Вентид — комбинированный дозированный аэрозоль, содержащий глюкокортикоид и р2-адреномиметик (вентолин) Ингалируется по 1-2 вдоха 3-4 раза в день
Ингаляционные глюкокортикоиды 2-го поколения
Ингаляционные глюкокортикоиды 2-го поколения обладают более значительным сродством к глюкокортикоидным рецепторам в бронхопульмональной системе Считается, что препараты этого поколения более эффективны, чем бекотид, и действуют более длительно
Будесонид (горакорт) — аэрозоль (200 доз по 160 мкг) — препарат продленного действия в капсулах, действует около 12 ч, ингалируется 2 раза по 200 мкг, при тяжелом течении бронхиальной астмы суточная доза повышается до 1600 мкг
Флунисолид (ингакорт) выпускается в виде аэрозоля для ингаляций Одна доза аэрозоля содержит 250 мкг флунисолида Начальная доза препарата составляет 2 вдоха утром и вечером, что соответствует 1000 мкг флунисолида При необходимости дозу можно увеличить до 4 ингаляций 2 раза в день (2000 мкг в сутки)
После ингаляции флунисолида только 39% введенной дозы поступает в общий кровоток При этом более 90% препарата, подвергшегося резорбции в легких, превращается в печени в почти неактивный метаболит — 6р-гидроксифлунисолид Его активность в 100 раз ниже активности исходного препарата
В отличие от беклометазона дипропионата, флунисолид является исходно биологически активным, не подвергается метаболизму в легких, в дозе 2000 мкг в сутки не оказывает угнетающего влияния на гипоталамо-гипофизарно-надпочениковую ось и не имеет системных побочных эффектов Баллончик с флунисолидом оснащен специально разработанным спейсером, который способствует более эффективному и глубокому поступлению препарата в бронхи, уменьшает осаждение его в полости рта и, следовательно, частоту осложнений со стороны рта, глотки (кандидомикоз, охриплость голоса, горечь во рту, кашель)
Флютжазона пропионат (фликсомид) — выпускается в виде дозированного аэрозоля с содержанием в 1 дозе 25, 50, 125 или 250 мкг препарата Применяются ингаляции в дозе от 100 до 1000 мкг 2 раза в день в зависимости от тяжести состояния больного Поддерживающая доза — 100-500 мкг 2 раза в день Препарат практически не дает системных побочных явлений, является наиболее эффективным и безопасным ингаляционным глюкокортикоидом
Флютиказон обладает высокой местной активностью, его аффинность к глюкокортикоидным рецепторам в 18 раз превышает таковую дексаметазона и в 3 раза — будесонида
При ингалировании флютиказона 70-80% препарата проглатывается, но при этом абсорбируется не более 1% При первом прохождении через печень происходит почти полная биотрансформация препарата с образованием неактивного метаболита — деривата 17-карбоксиловой кислоты
Все три препарата (беклометазона дипропионат, флунисолид, флютиказона пропионат) снижают число приступов бронхиальной астмы в дневное и ночное время, потребность в симпатомиметиках и частоту рецидивов Однако названные положительные эффекты более выражены и быстрее наступают при использовании флютиказона, при этом практически отсутствует опасность развития системных побочных действий глюкокортикоидов
При легких и среднетяжелых формах бронхиальной астмы можно использовать любые ингаляционные глюкокортикоиды в дозах 400-800 мкг/сутки При более тяжелом течении заболевания, требующем применения высоких доз ингаляционных глюкокортикоидов (1500-2000 мкг/сутки и (юлее), следует предпочесть флютиказона пропионат
Побочные действия ингаляционной глюкокортикоидной терапии
1 Развитие фарингита, дисфонии вследствие атрофии мышц гортани, кандидомикоза слизистой полости рта Для профилактики этого побочного действия, обусловленного оседанием частиц глюкокортикоида на слизистой оболочке полости рта во время ингаляции, следует полоскать рот после ингаляции, а также пользоваться спейсером (см выше)
2 Системные побочные эффекты Развитие системных побочных явлений обусловлено частичным всасыванием ингалируемых глюкокортикоидов слизистой оболочкой бронхопульмональной системы, желудочно-кишечного тракта (часть препарата проглатывается больным) и поступлением его в кровоток
Всасывание ингалируемого глюкокортикоида через бронхопульмональную систему зависит от степени воспаления бронхов, интенсивности метаболизма глюкокортикоидов в дыхательных путях и количества препарата, поступающего в дыхательные пути во время ингаляции
Системные побочные явления возникают при использовании больших доз ингалируемых глюкокортикоидов (более 2000 мкг бекотида в сутки) и могут проявиться развитием кушингоидного синдрома, угнетением гипофизарно-надпочечниковой системы, снижением интенсивности процессов костеобразования, развитием остеопороза Обычные терапевтические дозы ингалируемых глюкокортикоидов системных побочных явлений не вызывают
Флунисолид (ингокорт) и флюказона дипропионат очень редко проявляют системные побочные действия по сравнению с бекотидом
Таким образом, применение ингаляционных форм глюкокортикоидов является современным и активным методом лечения бронхиальной астмы, позволяющим уменьшить потребность в пероральных глюкокортикоидах, а также р-адреномиметиках (Woolcock)
Целесообразно сочетать ингаляции глюкокортикоидов и бронхолитиков по схеме вначале ингаляция симпатомиметика (беротека, сальбутамола), а через 15-20 мин — ингаляция глюкокортикоида Сочетанное применение ингаляционного глюкокортикоида с другим ингаляционным противовоспалительным средством (интал, тайлед) позволяют у многих больных уменьшить лечебную дозу глюкокортикоидного препарата
Применение глюкокортикоидов внутрь или парентерально (системная глюкокортикоидная терапия)
Системная глюкокортикоидная терапия проводится только по строгим показаниям
· очень тяжелое течение бронхиальной астмы при отсутствии эффекта от всех остальных методов лечения,
• кортикозависимая бронхиальная астма (т.е. когда больной уже длительно лечится глюкокортикоидами и в данный момент отменить их невозможно);
• астматический статус (глюкокортикоиды применяются парентерально);
• кома при бронхиальной астме (глюкокортикоиды применяются парентерально);
Системная глюкокортикоидная терапия обладает следующими механизмами действия:
• стабилизирует тучные клетки, предупреждает их дегрануляцию и выход медиаторов аллергии и воспаления;
• блокируют образование IgE (реагинов);
• подавляют позднюю астматическую реакцию, что обусловлено подавлением клеточной воспалительной реакции вследствие перераспределения лимфоцитов и моноцитов, угнетением способности нейтрофилов к миграции из сосудистого русла, перераспределением эозинофилов. Поздняя астматическая реакция начинается через 3-4 ч после воздействия аллергена, максимум ее наблюдается через 12 ч, продолжается более 12 ч; она отражает механизмы прогрессирования бронхиальной астмы. Гиперреактивность бронхов, сохраняющаяся длительно
(в течение недель и месяцев), связана с поздней астматической реакцией;
• стабилизируют лизосомальные мембраны и уменьшают выход лизосомальных ферментов, повреждающих бронхопульмональную систему;
• подавляют сосудорасширяющее действие гистамина;
• увеличивают количество и чувствительность р-адренорецепторов бронхов к бронхорасширяющим воздействиям адреномиметиков;
• уменьшают отек слизистой оболочки бронхов; повышают активность эндогенных катехоламинов;
После проникновения в клетку глюкокортикоиды связываются со специфическими цитоплазматическими рецепторами, образуя комплекс гормон-рецептор, взаимодействующий в ядре клетки с хроматином. В результате активируется синтез белков, опосредующих эффекты глюкокортикоидов. Весь процесс занимает около 6 ч, поэтому глюкокортикоиды не купируют приступы удушья при обострении бронхиальной астмы, они действуют не ранее 6 ч после их введения
Используются 3 группы глюкокортикоидов:
• группа преднизолона: преднизолон (таблетки по 0.005 г; ампулы по 1 мл с содержанием 30 мг препарата); метилпреднизолон (метипред, урбазон — таблетки по 0.004 г);
• группа триамцинолона: триамцинолон, кенакорт, полькортолон, берликорт (таблетки по 0 004 г);
• группа дексаметазона: дексаметазон, дексон, дексазон (таблетки по
0 0005 г; ампулы для внутривенного и внутримышечного введения по
1 и 2 мл 0.4%-раствора с содержанием препарата 4 и 8 мг соответственно).
Для лечения больных бронхиальной астмой наиболее приемлемы препараты группы преднизолона и триамцинолона.
При очень тяжелом течении бронхиальной астмы и при отсутствии эффекта от остальных методов лечения рекомендуется применять препараты короткого действия (преднизолон, преднизолон, метилпреднизолон).
Методика лечения по М. Э. Гершвину (1984):
• при обострении начинать с высоких доз (например, 40-80 мг преднизолона ежедневно);
• после уменьшения симптомов — медленно снижать дозу (в течение 5-7 дней) до поддерживающей, например, на 50% каждый день;
• для хронического (длительного) лечения применять ежедневную дозу
преднизолона ниже 10 мг;
• принимать препарат в первой половине дня;
• в начале лечения дневную дозу разделить на 2-3 приема;
• если требуется прием более 7.5 мг преднизолона в день, предпринять попытку прерывистой терапии (например, 15 мг преднизолона через день вместо ежедневного приема 7.5 мг);
• для снижения суточной пероральной дозы преднизолона можно заменить часть принимаемого внутрь препарата ингаляцией бекотида, исходя из того, что 6 мг преднизолона равны по активности 400 мг бекотида.
В. И. Трофимов (1996) рекомендует начинать терапию таблетированными глюкокортикоидами с суточной дозы 20-40 мг преднизолона или 16-32 мг метипреда, триамцинолона. 2 /з- 3 /4 суточной дозы больной должен принимать утром после завтрака, остальную часть — после обеда (до 15.00) в соответствии с циркадными ритмами продукции глюкокортикоидов и чувствительности к ним тканей и клеток организма. После значительного улучшения состояния больного (отсутствие приступов удушья в течение 7-10 дней) можно снижать дозу глюкокортикоидов на ‘/2 таблетки в 3 дня, а при достижении дозы 10 мг/сут преднизолона или эквивалентной дозы другого препарата — на ‘/4 таблетки за 3 дня до полной отмены или сохранения поддерживающей дозы (обычно ‘/г»2 таблетки). Если больной получал глюкокортикоиды длительно (более 6 месяцев), снижение дозы нужно производить более медленно: на ‘/V’A таблетки за 7-14 и более дней.
Рекомендуется сочетать прием глюкокортикоидов внутрь с использованием их ингаляционных форм, что позволяет значительно уменьшить лечебную и поддерживающую дозы пероральных препаратов.
При необходимости длительного применения глюкокортикоидов для контроля за астмой тяжелого течения целесообразно использование альтернирующей схемы приема (удвоенной суточной дозы через день 1 раз в сутки утром), что позволяет уменьшить риск угнетения надпочечников и развития системных побочных эффектов. Короткий период полураспада пероральных глюкокортикоидов группы преднизолона и триамцинолона позволяет применять альтернирующую схему. Следует подчеркнуть что альтернирующая схема приема глюкокортикоидов обычно приемлема тогда, когда с помощью ежедневного их приема уже удалось добиться улучшения течения астмы и снизить суточную дозу преднизолона до 5-7.5 мг/день; однако, если наступило ухудшение состояния, необходимо вернуться к ежедневному приему препарата. При очень тяжелом течении астмы альтернирующая схема неэффективна, приходится применять глюкокортикоиды ежедневно и даже 2 раза в день.
Согласно совместному докладу Национального института сердца, легких и крови (США) и ВОЗ «Бронхиальная астма Глобальная стратегия» — короткий курс лечения пероральными глюкокортикоидами (5-7 дней) может быть использован как «максимальная терапия» для достижения контроля течения астмы у больного. Этот курс может применяться или в начале лечения больного с неконтролируемой астмой или в течение периода, когда больной отмечает постепенное ухудшение своего состояния Побочные эффекты при коротких курсах (менее 10 дней), как правило, не наблюдаются, отменять глюкокортикоиды можно сразу после коротких курсов
При наличии противопоказаний к приему глюкокортикоидных препаратов внутрь (эрозивный гастрит, язвенная болезнь желудка и двенадцатиперстной кишки) можно применить кеналог-40 (препарат триамцинолона продленного действия) внутримышечно в дозе 1-2 мл (40-80 мг) 1 раз в 4 недели.
Количество инъекций на курс лечения и интервалы между инъекциями определяются индивидуально, однако, к сожалению, при продолжительном лечении длительность эффекта уменьшается и возникает необходимость более частых введений .Некоторые больные, страдающие кортикозависимым вариантом бронхиальной астмы, вместо систематического перорального приема глюкокортикоидов применяют внутримышечное введение кеналога 1 раз в 3-4 недели
При выраженных обострениях, тяжелых приступах бронхиальной астмы, угрожающих развитием астматического состояния, нередко приходится применять большие дозы глюкокортикоидов внутривенно через короткие интервалы времени Считается, что оптимальная концентрация глюкокортикоидов в плазме достигается при введении гидрокортизона гемисукцината в дозе 4-8 мг/кг или преднизолона в дозе 1-2 мг/кг с интервалами 4-6 ч. Более эффективно внутривенное капельное введение глюкокортикоидов, которое может производиться 1-4 раза в сутки в зависимости от состояния больного. Обычно курс лечения внутривенными капельными вливаниями глюкокортикоидов до достижения оптимального эффекта составляет 3-7 дней, после чего глюкокортикоиды отменяют, постепенно снижая дозу на ‘Д начальной суточной дозы, добавляя ингаляционные глюкокортикоиды.
При глюкокортикозависимой бронхиальной астме отменить полностью глюкокортикоиды невозможно, достаточно активной оказывается суточная доза преднизолона 5-10 мг.
Побочные эффекты системного лечения глюкокортикоидами:
• ожирение, преимущественно в области груди, живота, шейного отдела позвоночника, появление лунообразного гиперемированного лица;
• психозы, эмоциональная лабильность;
• истончение, сухость кожи, багрово-фиолетовые стрии;
• остеопороз, в т.ч. позвоночника (возможны переломы позвоночника);
• гиперсекреция и повышение кислотности желудочного сока, развитие
язв желудка и двенадцатиперстной кишки;
• гипергликемия (стероидный сахарный диабет);
• задняя субкапсулярная катаракта;
• активизация туберкулезного процесса;
• угнетение функции надпочечников.
Внезапная отмена глюкокортикоидов после длительного их применения, особенно в больших дозах, приводит к быстрому появлению синдрома отмены, который проявляется:
• ухудшением течения бронхиальной астмы, возобновлением приступов
удушья, возможным развитием астматического статуса;
• значительным падением артериального давления;
Для уменьшения развития побочных явлений глюкокортикоиднои терапии и для уменьшения кортикозависимости рекомендуется:
• стараться обходиться меньшими дозами препарата;
• сочетать лечение с ингаляциями интала;
• назначать короткодействующие препараты (преднизолон, урбазон, полькортолон) и не применять длительно действующие глюкокортикоиды (кеналог, дексазон и др.);
• назначать глюкокортикоид в первой половине дня, наибольшую часть суточной дозы давать утром, чтобы концентрация препарата в крови совпадала с наибольшим выбросом эндогенного кортизола;
• поддерживающую дозу препарата (1.5-2 таблетки) целесообразно давать прерывистым способом (т.е. удвоенную поддерживающую дозу принимать однократно утром, но через день). При таком приеме уменьшается возможность угнетения надпочечников и развития побочных явлений;
· для уменьшения кортикозависимости в момент снижения дозы преднизолона и перехода на поддерживающие дозы принимать этимизол по 0.1 г 3 раза в день (под контролем артериального давления), глициррам по 0.05 г 2-3 раза в день внутрь. Эти средства стимулируют надпочечники. Для уменьшения кортикозависимости можно применять также настойку диоскореи кавказской по 30 капель 3 раза в день;
• применять РДТ с сочетании с иглорефлексотерапией;
· для предупреждения или уменьшения побочных явлений пероральной глюкокортикоиднои терапии целесообразно часть дозы заменить ингаляциями глюкокортикоидов;
· применять плазмаферез, гемосорбцию.
Одним из наиболее тяжелых осложнений системной глюкокортикоидной терапии является остеопороз. Для его профилактики и лечения применяются препараты, содержащие гормон С-клеток щитовидной железы кальцитонин — калъцитрин, миакалъцик. Калъцитрин назначается по 1 ЕД подкожно или внутримышечно ежедневно в течение месяца с перерывами каждый 7-й день (курс 25 инъекций) или по 3 ЕД через день (курс 15 инъекций). Миакальцик (кальцитонин лосося) вводится подкожно или внутримышечно по 50 ЕД (курс 4 недели). Можно применять также миакальцик в виде спрея интраназально по 50 ЕД через день в течение 2 месяцев с последующим двухмесячным перерывом. Лечение препаратами кальцитонина нужно проводить в сочетании с приемом кальция глюконата внутрь по 3-4 г/сут. Препараты кальцитонина способствуют поступлению кальция в костную ткань, уменьшают явления остеопороза, обладают противовоспалительным действием, уменьшают дегрануляцию тучных клеток и кортикозависимость.
Лечение глюкокортикоидами беременных женщин, страдающих бронхиальной астмой
Большинство пульмонологов считает противопоказанной системную пероральную глюкокортикоидную терапию в первом триместре беременности из-за высокого риска развития уродств у плода. Ингаляционные глюкокортикоиды могут применяться для лечения бронхиальной астмы (в дозе не более 1000 мкг в сутки) в течение всего периода беременности, т.к. их системные побочные эффекты незначительны, а риск гибели плода вследствие гипоксии при приступах астмы велик.
Небольшие дозы глюкокортикоидов при необходимости можно назначать внутрь во П-Ш триместрах в комбинации с ингаляционными глюкокортикоидами. При тяжелом приступе астмы и астматическом статусе показано внутривенное введение глюкокортикоидов.
Лечение цитостатиками (иммунодепрессантами)
Лечение цитостатиками в настоящее время применяется редко.
Механизм действия цитостатиков заключается в угнетении продукции реагинов и противовоспалительном эффекте. В отличие от глюкокортикоидов они не угнетают надпочечников.
• тяжелая форма атопической бронхиальной астмы, не поддающаяся
лечению обычными средствами, в т.ч. глюкокортикоидами;
• кортикозависимая кортикорезистентная бронхиальная астма — с целью уменьшения кортикозависимости;
• аутоиммунная бронхиальная астма.
Методика лечения цитостатиками изложена в разделе «Лечение аутоиммунной бронхиальной астмы».
Иммуномодулирующая терапия нормализует работу иммунной системы. Назначается при затяжном течении бронхиальной астмы, резистентной к терапии обычными средствами, особенно при сочетании атопической формы с инфекцией в бронхопульмональной системе.
Дата добавления: 2015-04-23 ; Просмотров: 1827 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
источник
Глюкокортикоиды в лечении аллергических болезней широко используются в качестве заместительной терапии (при глюкокортикоидной зависимости), как индукторы ремиссии (при сывороточной болезни, токсидермии), в качестве пульс-терапии (в больших дозах при астматическом статусе, анафилактическом шоке), в виде базовой терапии (современные ингаляционные глюкокортикоиды при бронхиальной астме).
Однако применение глюкокортикоидов — это каждый раз отчаянная, вынужденная мера, которая требует углубленного анализа заболевания, прогноза, правильной оценки реальной эффективности неглюкокортикоидной терапии и, главное, определения мер, способствующих предупреждению последствий применения гормональных препаратов.
Эта проблема широко освещена в литературе (К. Абендрот, 1988; Б.И. Шмушкович, 1997; О. А. Суточникова, 1997; Б.С. Утешев, 1997; В. Шрейбер, 1987; Borumetal., Freedman, 1986; Michel, Delooz,1989, и др.).
Глюкокортикоиды — биологически весьма активная часть гормонального гомеостаза, в продукции и саморегуляции которых главная роль отводится гипофизарно-надпочечниковой системе. В коре надпочечников синтезируется кортизон — биологически неактивное соединение, которое в печени превращается в активное — гидрокортизон (кортизол).
У взрослого человека за сутки вырабатывается 10—30 мг кортизола, в условиях стресса (различных перегрузок, травм, инфекций и др.) это количество может возрастать в 10 раз (до 250 мг). Потребность организма в кортизоле неравномерна в течение суток и зависит от активации обменно-ферментативных процессов — основная его часть реализуется в дневной (особенно утром и в середине дня) период и лишь 1/10 — в ночное время.
Назначая глюкокортикоидные препараты, необходимо каждый раз предпринимать усилия, чтобы избежать возможных нежелательных реакций (табл. 7).
Проявление нежелательных реакций связано с продолжительностью глюкокортикоидной терапии, предрасположенностью к ним, наличием факторов риска — гипертензии, язвенной болезни желудка, избыточной массы тела, остеопороза. По времени развития они могут быть ранними или поздними (табл. 8).
По времени полужизни в организме глюкокортикоиды условно делятся на короткоживущие: кортизон и гидрокортизон — 8—12 ч, преднизолон, метилпреднизолон — 12—36 ч; среднеживущие: триамицинолон, параметазон — 24—48 ч; долгоживущие: бетаметазон, дексаметазон, беклометазон—36—54 ч.
Практически в той же последовательности нарастает глюкокортикоидная активность приведенных препаратов и угнетение гипоталамо-гипофизарно-надпочечниковой системы.
В связи с этим при длительной терапии необходимо отдать предпочтение короткоживущим препаратам (преднизолону или медролу), однако они обладают и большей минералокортикоидной активностью.
- глюкокортикоиды, которые при приеме внутрь быстро всасываются в верхних отделах тонкого кишечника, создавая максимальную концентрацию в крови через 0,5—1,5 ч;
- сукцинаты, гемисукцинаты и фосфаты водорастворимых глюкокортикоидов, вводимых внутривенно, обладают быстрым и сравнительно кратковременным эффектом;
- ацетаты, ацетониды — мелкокристаллические суспензии глюкокортикоидов, нерастворимы в воде (предназначены для введения внутрь суставов, в суставные сумки, синовиальные влагалища, рубцы и реже внутримышечно), медленно всасываются с началом действия через 24—48 ч и общей продолжительностью до 4 нед.
Гидрокортизон как природный глюкокортикоид обладает в 4 раза более слабым противовоспалительным действием по сравнению с преднизолоном, как минералокортикоид превосходит его. Применяется главным образом для заместительной терапии.
— гидрокортизона ацетат, суспензия в ампулах — 25 мг/мл для внутримышечного введения, введения в суставные сумки и др.;
— гидрокортизона гемисукцинат, сухое вещество или раствор в ампулах — 100 и 500 мг (солу-кортеф, гидрокортизонтева).
Преднизолон — синтетический глюкокортикоид.
— таблетки — 5, 10, 20 и 50 мг;
— преднизолона натрия фосфат, ампулы — 30 мг/мл;
— преднизолона гемисукцинат (солюдекортин), порошок в ампулах — 25, 50 и 250 мг;
— преднизолона ацетат, суспензия в ампулах — 25 и 50 мг.
Метилпреднизолон — глюкокортикоидная активность на 20 % выше, чем у преднизолона, минимальный ульцерогенный побочный эффект. Обладает способностью подавлять перекисное окисление.
— таблетки — 4, 16, 32 и 100 мг (медрол, метипред, урбазон);
— метилпреднизолона сукцинат, сухое вещество во флаконах — 40, 125, 250, 500 и 1000 мг (метипред, солу-медрол);
— метилпреднизолона ацетат, суспензия во флаконах — 40 мг (депо-медрол, метипред).
Триамцинолон — фторированный глюкокортикоид, действие на 20 % сильнее, чем у преднизолона.
— таблетки — 2, 4, 8 мг (полькортолон, кенакорт, берликорт);
— триамцинолона ацетонид, суспензия в ампулах — 40 мг/мл (кеналог).
Дексаметазон — фторированный глюкокортикоид, обладает в 7 раз более сильным противовоспалительным действием, чем преднизалон, стимулирует синтез сурфактанта в альвеолах.
— таблетки — 0,5 и 1,5 мг (кортидекс, дексазон, даксин);
— дексаметазона фосфат натрия, ампулы — 4 мг/мл (дексазон, дексабене, сондекс).
Бетаметазон — фторированный глюкокортикоид, по силе и длительности действия близок к дексаметазону.
— таблетки — 0,5 мг (целестон);
— бетаметазона динатрия фосфат, ампулы — 3 мг/мл (целестон), может вводиться внутривенно, субконъюнктивально;
— бетаметазона ацетат, ампулы по 1 мл и флаконы по 5 мл— 3 мг/мл (целестон хронодозе);
— бетаметазона динатрия фосфат и дипропионат, ампулы по 1 мл суспензии, содержащие 7 мг бетаметазона, включающего 2 мг быстро всасывающегося фосфата и 5 мг медленно всасывающегося дипропионата (дипроспан, флостерон).
Терапия глюкокортикоидами подразделяется на заместительную и противовоспалительную.
Заместительная терапия восполняет недостающий эндогенный кортизол на фоне недостаточности коры надпочечников. Препаратом выбора при такой терапии является гидрокортизон — средство, наиболее близкое к кортизолу.
Среди перечня нежелательных реакций при долговременной терапии глюкокортикоидами заслуживает внимания вторичная недостаточность надпочечников.
1. При длительной поддерживающей терапии преднизолоном или медролом до 5 мг/сут, гидрокортизоном до 25 мг/сут угнетение гипоталамо-гипофизарно-надпочечниковой системы маловероятно.
При применении преднизолона, медрола в более высоких дозах (40 мг в сутки) более 10 дней может сформироваться недостаточность коры надпочечников, для восстановления которой требуется иногда 6 и более месяцев. Следует учитывать при этом и время приема преднизолона, медрола, например, вечерний прием в количестве 5 мг этих препаратов более опасен, чем 20 мг в утреннее время.
Можно с большой вероятностью прогнозировать наличие недостаточности надпочечников у тех лиц, которые лечились фторированными глюкокортикоидами длительное время (триам-цинолон, дексаметазон).
2. Признаки недостаточности коры надпочечников могут появиться у пациентов вскоре после отмены глюкокортикоидов — через 2—7 дней или через несколько месяцев после окончания курса лечения.
Последняя ситуация может быть спровоцирована стрессовой нагрузкой (вследствие травмы, инфекции, операции, родов и др.).
Недостаточность надпочечников (синдром отмены глюкокортикоидов) проявляется недомоганием, вялостью, быстрой утомляемостью, болью в мышцах, обострением основного заболевания. На этом фоне вероятность недостаточности надпочечников повышается при тахикардии, понижении артериального давления.
Чтобы предупредить недостаточность коры надпочечников, необходимо принять следующие меры.
Пациентам с прогнозируемой недостаточностью надпочечников во время стрессовой ситуации (травмы, операции, роды, повышение температуры тела) в профилактических целях показана заместительная терапия — внутримышечное введение гидрокортизона в дозе 25 мг/сут.
Если при этом наблюдаются клинические проявления недостаточности надпочечников, то доза гидрокортизона может повышаться до стрессовой потребности (250 мг/сут) в сочетании с капельным введением кровезаменителей до 1,5 л на фоне комплексной терапии.
Противовоспалительная терапия может проводиться в разных режимах как инициирующая (индукция ремиссии), долговременная, альтернативная, пульс-терапия, антиэметическая терапия, ингаляционная долговременная терапия.
1. Глюкокортикоиды, проникая через мембрану клеток, в цитоплазме связываются со специфическим рецептором, образуя активированные комплексы, стимулируют в ядре клетки образование информационной ДНК, обеспечивающей синтез различных регуляторных белков, включая и липокортин. Последний ингибирует фермент фосфолипазу А2, что приводит к снижению синтеза гтростагландинов, лейкотриенов, активаторов воспалительной реакции.
2. Глюкокортикоиды, стабилизируя мембраны клеток, внутриклеточных органелл, микросом, снижают проницаемость капилляров, тормозят миграцию нейтрофилов и макрофагов в очаг воспаления, угнетают пролиферацию фибробластов и синтез коллагена, снижают цитотоксическую активность Т-лимфоцитов, активацию Т-хелперов.
3. Глюкокортикоиды тормозят взаимодействие иммуноглобулинов с тучной клеткой, ингибируя высвобождение биологически активных веществ. Они также подавляют синтез «противовоспалительных» цитокинов ИЛ-1, ИЛ-6, ИЛ-8, фактора некроза опухолей.
Предлагаемые режимы противовоспалительной терапии позволяют максимально избегать побочных реакций.
Инициирующая терапия (индукция ремиссии) проводится медролом в расчете на оптимальный противовоспалительный эффект в дозе 0,8 мг метилпреднизолона на 1 кг массы тела в день, т.е. для пациента массой 60 кг потребуется прием 16 мг утром, в обед и вечером — всего 48 мг в сутки. В зависимости от клинической ситуации и предполагаемой регрессии заболевания суточная доза медрола может быть и меньшей.
В целом данный режим терапии направлен на переключение максимально выраженной воспалительной реакции на минимальную за максимально короткий период, охватывающий не более 7—10 дней, а чаще 3—4 дня. Например, подобная терапия при лечении токсидермии может быть полностью закончена в эти же дни без специального режима отмены медрола.
Если невозможно полностью отменить медрол в течение 10 дней, переходят на режим долговременной терапии, проведение которой медролом позволяет более успешно избегать нежелательных реакций, чем, например, при лечении полькортолоном, дексаметазоном.
Суточная доза медрола практически остается такой же, как и при проведении инициирующей терапии, только распределяется она на два приема — утром и в обед.
Долговременная противовоспалительная терапия как вынужденная мера проводится при развитии эозинофильных инфильтратов, после купирования астматического статуса, после купирования токсидермии, развившейся на фоне рецидивирующей крапивницы.
Долговременная терапия может осуществляться в зависимости от ситуации в течение 2 недель или больше, и практически при стабилизации заболевания она проводится в альтернативном режиме.
Сущность проводимого лечения заключается в том, что суточная доза медрола, предусмотренная при долговременной терапии, дается через день, т.е. лечение осуществляется в прерывистом режиме.
В ряде случаев при переходе на альтернативный режим суточную дозу медрола вначале назначают через день в половинной дозе. Например, в первый день 48 мг медрола, во второй — 24 мг и т.д. Затем, если ремиссия остается стойкой, половинная доза полностью снимается.
Альтернативный режим лечения предполагает наличие эндогенного кортизола, обеспечивающего компенсацию заболевания при подобном чередовании медрола через день.
Такое лечение может продолжаться до 3—4 нед. При стойкой ремиссии переходят на режим отмены медрола.
Для предупреждения недостаточности надпочечников — синдрома отмены глюкокортикоидов — в случаях проведения долговременной противовоспалительной терапии более 10 дней медролом, преднизолоном в таблетках в дозе более 20—40 мг/сут снижать дозу этих препаратов у больных с наступившим клиническим благополучием нужно поэтапно:
а) если терапия преднизолоном, медролом продолжалась до 2 нед, то доза снижается по 4 мг каждую последующую неделю;
б) если терапия преднизолоном, медролом продолжалась более 2 нед, то доза снижается по 4 мг каждые две недели.
У больных бронхиальной астмой снижение дозы пероральных глюкокортикоидов на 4 мг возможно за одну неделю на фоне перехода на режим применения ингаляционных глюкокортикоидов.
Во избежание системного действия глюкокортикоидов, где это возможно, отдается предпочтение местному их применению и препаратам, которые могут всасываться в минимальных количествах (ингаляционные глюкокортикоиды — будезонид, флутиказон; элоком при нанесении на кожные покровы).
Пульс-терапия — вынужденная мера при различных ургентных ситуациях. Может применяться в составе комплексной терапии при второй или третьей стадии астматического статуса, при выведении из анафилактического шока.
Пульс-терапия осуществляется в виде внутривенных инфузий солу-медрола, доза которого может составлять 0,5—1,0 г в сутки в течение 1—2—3 дней с последующей полной отменой препарата.
За больными при этом осуществляется постоянное наблюдение (наибольшую угрозу представляет изменение артериального давления и экстрасистолия). Пульс-терапия до 500 мг может осуществляться солу-медролом с осторожностью (при необходимости) лицам старше 50 лет.
Ингаляционные глюкокортикоиды при бронхиальной астме позволяют создать оптимальную противовоспалительную концентрацию в очаге воспаления и исключить системные нежелательные реакции при условии соблюдения правил их применения (с помощью спейсеров и полоскания полости рта после впрыскивания препарата).
Ингаляционные глюкокортикоиды не используются для купирования приступов удушья, они предназначаются для противовоспалительной, противоаллергической, антипролиферативной терапии при аллергических ринитах и бронхиальной астме (см.).
Беклометазон для ингаляций используется в дозе от 200 до 1600 мкг/сут, интраназально по 100 мкг 2 раза в день в каждую ноздрю.
— дозированные аэрозоли — в одной дозе 50, 100 (альдецин, бекотид, бекломет) и 250 мкг (беклокорт форте, беклофорт) беклометазона дипропионата;
— бекодиск — оригинальная форма выпуска беклометазона в виде пудры в разовых дозах 100 и 200 мкг, ингалируется с помощью дискхалера;
— дозированные аэрозоли для интраназального применения по 50 мкг беклометазона дипропионата (альдецин, беконазе, бекломет-назаль).
Флунизолид — фторированный глюкокортикоид, для ингаляций используется в дозе 1000 мкг/сут, интраназально — по 50 мкг в каждую ноздрю 2 раза в день.
— флунизолид в виде дозированного аэрозоля со спейсером — 250 мкг (ингакорт);
— дозированный ингалятор для интраназального применения, один вдох 25 мкг флунизолида (синтарис).
Будезонид — негалогенизированный глюкокортикоид.
— будезонид в виде дозированного аэрозоля, один вдох 50 и 100 мкг (пульмикорт) и 200 мкг (бенакорт);
— будезонид в виде дозированного интраназального ингалятора, в одной дозе 50 мкг (ринокорт).
Флутиказон — препарат, имеющий высокий аффинитет к глюкокортикоидным рецепторам, превосходит будезонид в 2 раза.
— фликсотид—дозированный аэрозоль, содержащий в одной дозе 25,50,125 и 250 мкг флутиказона;
— фликсоназе—дозированный интраназальный ингалятор, содержащий в одной дозе 50 мкг флутиказона.
Триамцинолон — фторированный глюкокортикоид.
— в виде дозированного аэрозоля со встроенным спейсером (азмакорт). Содержит в одной дозе 100 мкг триамцинолона ацетонида;
— в виде дозированного аэрозоля для интраназального применения (назакорт). В одной дозе 55 мкг триамцинолона ацетонида.
источник
Бронхиальной астмой называют хроническое заболевание дыхательной системы, при котором отмечается сильное сужение бронхов. Гормоны при астме нужны для оказания противовоспалительного и антиаллергического эффекта.
В базисную терапию астмы включены глюкокортикостероиды. Если их не применять для лечения заболевания, сильно возрастает зависимость от симптоматических бронходилататоров. Это является признаком неконтролируемого течения астмы.
Глюкокортикостероиды — это гормоны, производимые корой надпочечников. В организме человека вырабатывается кортизол, кортикостерон.
Разностороннее воздействие на организм этих биологически активных веществ позволило активно использовать их в лечении различных заболеваний, в том числе астмы.
Сейчас существует ряд фторированных и нефторированных синтетических глюкокортикоидов. В отличие от природных, они обладают большей активностью, поэтому действуют более эффективно.
Для полного понимания, почему так активно используют гормоны от астмы, важно знать их механизм действия. В клетках человеческого организма существуют специальные рецепторы, с которыми глюкокортикостероиды связываются, проникая в цитоплазму.
Полученный в результате этого взаимодействия комплекс проникает внутрь ядра, где воздействует непосредственно на ДНК. Это позволяет активировать процесс образования различных белков:
- липокортин-1. Его действие направлено на торможение продукции арахидоновой кислоты, из которой синтезируются медиаторы воспаления;
- нейтральная эндопептидаза. Нужна для разрушения кининовых комплексов, принимающих участие в развитии воспалительного процесса;
- интерлейкин-10, оказывающий противовоспалительное действие;
- ингибитор ядерного фактора. Играет важную роль в торможении воспалительного процесса бронхов.
За счет действия комплекса гормон-рецептор наблюдается выраженное торможение образования активизирующих воспалительный процесс белков.
Глюкокортикоиды благодаря своим свойствам отлично помогают при бронхиальной астме, давая выраженный противовоспалительный эффект.
Применение глюкокортикоидов при бронхиальной астме является традиционным методом лечения данного заболевания. Их использование началось еще в середине 40-х годов ХХ века, после того, как Ф. Хенч и Э. Кендэлл смогли искусственно синтезировать ГКС.
Поняв, что глюкокортикостероиды помогают в контроле воспалительного процесса при гормональной астме, они начали активно тестировать их при лечении заболевания, однако отметили большое количество побочных эффектов и временно прекратили их использование.
В современной медицине астматикам назначается два типа гормональных препаратов: ингаляционные и системные ГКС.
Главные преимущества, объясняющие широкое применение ингаляционных глюкокортикостероидов (ИГКС) для лечения бронхиальной астмы, — высокая липофильность, малый период полувыведения, а также быстрая инактивация.
В клинической практике используются следующие ИГКС:
- беклометазона дипропионат;
- будесонид;
- мометазона фуроат;
- флутиказона пропионат;
- циклесонид.
Механизм действия ИГКС при бронхиальной астме основан на их высокой липофильности. Эпителий человеческих бронхов покрыт незначительным слоем жидкости.
Поэтому не все вещества могут быстро проникнуть сквозь этот барьер. Липофильность позволяет препарату быстро достичь слизистой оболочки бронхов и проникнуть в кровеносную систему.
Эффект от применения ингаляционных глюкокортикоидов напрямую зависит от того, каким методом они были доставлены в организм.
Так, при использовании ингаляторов с аэрозолями большая часть препарата оседает в ротовой полости либо проглатывается. Лишь 10% достигает непосредственно слизистой оболочки бронха.
При вдыхании препарата через спейсер — около 5%. В системный кровоток ИГКС попадают в виде неактивных продуктов обмена, за исключением беклометазона. Также применяется введение препаратов через небулайзер для определенных групп пациентов, а именно:
- дети;
- пожилые люди;
- люди с нарушениями сознания;
- больные с сильной бронхиальной обструкцией.
Согласно ряду клинических испытаний, ингаляционные глюкокортикостероиды крайне эффективны при бронхиальной астме.
Системные глюкокортикостероиды (СГКС) не являются препаратами экстренной помощи при бронхиальной астме, однако они крайне важны для проведения терапевтических мероприятий во время обострений. В целом они нужны для повышения качества жизни пациента и не обладают быстрым эффектом.
Согласно глобальной стратегии ВОЗ, крайне важно применять СГКС при всех обострениях астмы, за исключением самых легких. Особенно это касается следующих случаев:
- после введения ИГКС не отмечается улучшения состояния пациента;
- приступ начался, несмотря на прием ИГКС;
- требуется увеличение дозы ИГКС;
- состояние пациента постоянно ухудшается;
- снижение реакции организма на действие ИГКС;
- снижение пикфлоуметрических показателей (ПСВ ниже 60%)
Отмечается, что для длительной терапии лучше применять СГКС в форме таблеток, внутривенное введение чаще используется при приступе. Основные глюкокортикостероиды, использующиеся для системной терапии при бронхиальной астме, — это преднизолон и гидрокортизон.
При пероральном приеме отмечается крайне высокая биодоступность. Максимальная концентрация препаратов в крови при внутривенном введении достигается менее чем через час после попадания в организм.
В печени данные лекарственные средства метаболизируются, а затем выводятся вместе с мочой.
При лечении больных гормонозависимой бронхиальной астмой важно помнить, что ГКС обладают рядом побочных эффектов, которые можно разделить на две группы:
- Развивающиеся во время терапии заболевания.
- Развивающиеся после прекращения лечения (синдром отмены).
К первой группе можно отнести следующие последствия:
- метаболические нарушения;
- повышение артериального давления;
- снижение иммунного статуса;
- язвенная болезнь;
- миопатия;
- расстройства психики;
- нарушения роста у детей;
- кушингоид.
Метаболические нарушения проявляются в виде гипергликемии, нарушении жирового, а также водно-электролитного обмена. Повышение уровня сахара в крови связано с тем, что на фоне приема ГКС отмечается увеличение устойчивости тканей к действию инсулина.
При этом данное состояние наблюдается достаточно редко, и к нему более склонны люди, которые, помимо гормональной астмы, болеют сахарным диабетом.
Нарушение обмена жиров проявляется в том, что на лице и туловище наблюдается чрезмерное развитие жировой ткани. Развивается так называемый кушингоидный хабитус.
Нарушения водного и минерального обмена проявляются в виде задержки воды в организме и потери кальция и калия.
Артериальная гипертензия при приеме ГКС связана с их воздействием на стенки сосудов. Развивается при длительном лечении большими дозами препаратов.
Еще реже возникает язвенная болезнь. Именно поэтому, все больные, которые применяют в лечении астмы СГКС, должны проходить обследования на предмет наличия язв в желудке.
У некоторых больных, применяющих ГКС, может возникнуть мышечная слабость, вплоть до полной атрофии. Это напрямую связано с влиянием препаратов на минеральный обмен. Также миопатия может наблюдаться при кушингоиде, поэтому ее нельзя называть специфичным побочным эффектом.
Легкие нарушения психического состояния могут наблюдаться в самом раннем начале терапии ГКС. Так, у больных отмечаются нервозность, частая смена настроения, а также нарушения сна. Стероидные психозы развиваются крайне редко.
У детей при использовании СГКС может отмечаться нарушение роста. В особенности этому подвержены мальчики. Считается, что патология связана с нарушением продукции половых гормонов.
При синдроме отмены наблюдается повышенная утомляемость, отсутствие аппетита, лихорадка, тошнота, а также сильные головные боли. В некоторых случаях может проявиться недостаточность надпочечников. Крайне редко наблюдается клиника псевдоопухоли мозга.
Первое, что должны понимать люди, больные гормонозависимой бронхиальной астмой, — нельзя самостоятельно отказываться от применения ГКС. Лечение должно быть системным и проходить под контролем специалиста.
Если говорить о лечении астмы без гормональных препаратов, то нужно вспомнить о такой группе лекарств, как кромоны. Нужно понимать, что данные лекарственные средства в большей мере обладают профилактическим, а не лечебным эффектом.
Их рекомендуется применять в период ремиссии. Существует много форм кромонов, однако лучший эффект достигается при применении при помощи ингаляторов. Они обладают рядом преимуществ:
- простота применения;
- отсутствие привыкания;
- минимальный риск побочных эффектов.
Благодаря своим свойствам препараты кромоглициевой кислоты отлично подходят для профилактики приступов астмы у детей, страдающих легкой формой заболевания. В соответствии с глобальной стратегией ВОЗ, они являются препаратом выбора.
Согласно проведенным исследованиям, если при средней тяжести и тяжелом течении астмы применение ИГКС не вызывает вопросов, то на начальных стадиях их употребление не оправдано.
Лечение астмы без гормонов у взрослого человека, который уже длительное время применял стероиды, практически невозможно.
Медикаментозные средства, такие как ИГКС и СГКС, при лечении бронхиальной астмы важно применять под контролем лечащего врача. Препараты необходимо подбирать индивидуально, а само лечение должно носить системный характер.
При обострениях БА рекомендуется использовать ИГКС для снятия приступа, а затем, при необходимости подключать СГКС. Несмотря на риск развития побочных эффектов, данные средства являются оптимальным вариантом лечения астмы.
источник