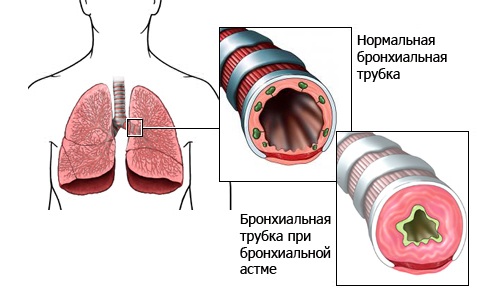
Аллергическая бронхиальная астма протекает с обструкцией просвета бронхов.
Проявляется приступами кашля и удушья. Обструкция бронхов при этом обратима либо сама по себе, либо под воздействием лечения.
Выделяют следующие виды заболевания:
- преимущественно аллергическая или экзогенная астма – приступы удушья развиваются после попадания в дыхательные пути аллергена,
- неаллергическая или эндогенная – приступы развиваются без воздействия аллергена, но под воздействием инфекции, холодного воздуха, физической или психической нагрузки.
- смешанная.
Основными факторами, приводящими к развитию заболевания, считаются:
- наследственная предрасположенность,
- длительное воздействие пыли (биологической и минеральной), испарений, вредных газов (к примеру, на производстве с профессиональной вредностью),
- негативные изменения экологии (выхлопные газы, дым, смог),
- нерациональное питание (злоупотребление животной, жирной, рафинированной, белковой пищей),
- средства бытовой химии (например, чистящие средства в аэрозолях, средства для мытья полов).
Пусковым механизмом приступа могут служить:
- различные аллергены в воздухе,
- нестероидные противовоспалительные средства,
- холодный воздух,
- резкий запах, дым,
- физическая нагрузка,
- стресс.
В течении аллергической бронхиальной астмы выделяют:
- интермиттирующую астму,
- легкую персистирующую,
- персистирующую средней степени тяжести,
- тяжелую персистирующую астму.
В течении бронхиальной астмы наиболее грозным осложнением является астматический статус. Это резкое сужение просвета бронхов, проявляющееся очень тяжелым приступом удушья, резистентным к аэрозольным бронхорасширяющим лекарственным препаратам.
Симптомами заболевания являются приступы:
- чувство заложенности в грудной клетке
- сухого кашля
- одышки
- свистящих хрипов
Приступ удушья при аллергической бронхиальной астме возникает чаще всего в ночные или ранние утренние часы. Неожиданно появляется мучительный сухой кашель. К нему быстро присоединяется одышка, при которой тяжелее всего сделать выдох. Человек дышит шумно, со свистом. Несмотря на максимум прилагаемых усилий число дыхательных движений уменьшается вдвое и менее. Грудная клетка раздута, как бочка. При этом, чтоб облегчить дыхание, человек сидит или стоит, опершись на руки. Продолжаться такой приступ может от нескольких до 30 минут. А у больных «со стажем» и того дольше, затягиваясь до суток и становясь все более тяжелыми. Заканчивается приступ отхождением с кашлем тягучей мокроты в небольшом количестве. Во время обострения также может появится цианоз кожных покровов, тахикардия, сонливость, затруднение речи.
Диагностика заключается в исследовании функции внешнего дыхания – спирометрия, пикфлуометрия.
Медикаментозная терапия состоит в применении:
- кромогликат натрия,
- глюкокортикостероидные препараты,
- антагонисты лейкотриеновых рецепторов,
- моноклональные антитела.
2. симптоматической терапии:
- бета2-адреномиметики,
- ксантины,
- отхаркивающие препараты,
- антибиотики,
- антигистаминные.
Также применяются немедикаментозные методы лечения:
- дыхательная гимнастика,
- спелеолечение,
- массаж грудной клетки,
- плаванье,
- иглорефлексотерапия,
- санаторно-курортное лечение.
Профилактика заключается в предотвращении контакта с аллергенами.
Перед использованием информации, предоставляемой сайтом medportal.org, пожалуйста, ознакомьтесь с условиями пользовательского соглашения.
Сайт medportal.org предоставляет услуги на условиях, описанных в настоящем документе. Начиная пользоваться веб-сайтом Вы подтверждаете, что ознакомились с условиями настоящего Пользовательского соглашения до начала пользования сайтом, и принимаете все условия данного Соглашения в полном объеме. Пожалуйста, не пользуйтесь веб-сайтом, если Вы не согласны с данными условиями.
Описание услуги
Вся информация, размещённая на сайте, носит справочный характер, информация взята из открытых источников является справочной и не является рекламой. Сайт medportal.org предоставляет услуги, позволяющие Пользователю производить поиск лекарственных средств в данных, полученных от аптек в рамках соглашения между аптеками и сайтом medportal.org. Для удобства пользования сайтом данные по лекарственным средствам, БАД систематизируются и приводятся к единому написанию.
Сайт medportal.org предоставляет услуги, позволяющие Пользователю производить поиск клиник и другой информации медицинского характера.
Ограничение ответственности
Размещенная в результатах поиска информация не является публичной офертой. Администрация сайта medportal.org не гарантирует точность, полноту и (или) актуальность отображаемых данных. Администрация сайта medportal.org не несет ответственности за вред или ущерб, который Вы могли понести от доступа или невозможности доступа к сайту или от использования или невозможности использования данного сайта.
Принимая условия настоящего соглашения, Вы полностью понимаете и соглашаетесь с тем, что:
Информация на сайте носит справочный характер.
Администрация сайта medportal.org не гарантирует отсутствия ошибок и расхождений относительно заявленного на сайте и фактического наличия товара и цен на товар в аптеке.
Пользователь обязуется уточнить интересующую его информацию телефонным звонком в аптеку или использовать предоставленную информацию по своему усмотрению.
Администрация сайта medportal.org не гарантирует отсутствия ошибок и расхождений относительно графика работы клиник, их контактных данных – номеров телефонов и адресов.
Ни Администрация сайта medportal.org, ни какая-либо другая сторона, вовлеченная в процесс предоставления информации, не несет ответственности за вред или ущерб, который Вы могли понести от того, что полностью положились на информацию, изложенную на этом веб-сайте.
Администрация сайта medportal.org предпринимает и обязуется предпринимать в дальнейшем все усилия для минимизации расхождений и ошибок в предоставленной информации.
Администрация сайта medportal.org не гарантирует отсутствия технических сбоев, в том числе в отношении работы программного обеспечения. Администрация сайта medportal.org обязуется в максимально короткие сроки предпринять все усилия для устранения каких-либо сбоев и ошибок в случае их возникновения.
Пользователь предупрежден о том, что Администрация сайта medportal.org не несет ответственности за посещение и использование им внешних ресурсов, ссылки на которые могут содержаться на сайте, не предоставляет одобрения их содержимого и не несет ответственности за их доступность.
Администрация сайта medportal.org оставляет за собой право приостановить действие сайта, частично или полностью изменить его содержание, внести изменения в Пользовательское соглашение. Подобные изменения осуществляются только на усмотрение Администрации без предварительного уведомления Пользователя.
Вы подтверждаете, что ознакомились с условиями настоящего Пользовательского соглашения , и принимаете все условия данного Соглашения в полном объеме.
Рекламная информация, на размещение которой на сайте имеется соответствующее соглашение с рекламодателем, имеет пометку «на правах рекламы».
источник
Специфическое лечение бронхиальной астмы может проводиться в нескольких направлениях: методы элиминации — устранение контакта с причинно-значимыми аллергенами; специфическая гипосенсибилизация или иммунотерапия, в основе которой лежит выработка у больного толерантности к специфическому аллергену.
Наиболее простым и радикальным методом лечения атопической астмы является полное прекращение контакта больного с аллергеном, ответственным за заболевание, т. е. элиминационная терапия.
Однако это не всегда возможно и зависит в основном от рода аллергена.
Элиминационная терапия возможна при пищевой и лекарственной аллергии (если речь идет о моносенсибилизации); при бытовой и эпидермальной аллергии постоянная влажная уборка квартиры, замена постельных принадлежностей, содержащих перо и пух, приводит к элиминации бытовых и пищевых аллергенов. При пыльцевой аллергии прекращение контакта с «виновным» аллергеном путем выезда в другую климато-географическую зону, где не растет аллергенная растительность.
При невозможности избежать контакта с «виновным» аллергеном показана специфическая иммунотерапия, в основе которой лежит выработка у больного толерантности к специфическому аллергену, которая достигается введением в организм возрастающих доз специфического аллергена.
При специфической иммунотерапии наиболее часто используется «классический» метод, предложенный Noon в 1911 г. При этом методе этиологический аллерген вводится подкожно в постоянно возрастающих концентрациях. Существует несколько схем лечения подкожными инъекциями — замедленная (классическая) и ускоренная схемы.
Эффективность лечения атопических заболеваний дыхательных путей составляет 60 — 80% (Ю. А. Порошина и соавторы, 1964, 1986; Л. А. Горячкина и соавторы, 1981).
Специфическая иммунотерапия больных атопической бытовой астмой с подключением аллергена клеща D.pteronyssinus позволила получить отличный и хороший эффекты в 79% случаев.
О. В. Полсачева и соавторы (1986) изучили результаты трех методов специфической иммунотерапии пыльцевой аллергии у больных, сенсибилизированных к пыльце злаковых трав водно-солевыми экстрактами по ускоренной схеме (водно-солевые экстракты, депонированные ex tempore в 0,1% геле гидрата окиси алюминия) — экспериментальными сериями очищенного пролонгированного препарата цинтала. Больным контрольной группы вводили плацебо. Лучший клинический эффект получен при проведении лечения цинтаналом, в сравнении в нативным ВСЭ.
Возникающие осложнения побуждают постоянно вести поиск новых методов специфической иммунотерапии. Среди них следует остановиться на пероральном методе СИТ. Несмотря на простоту методики проведения лечения, он не получил широкого распространения ввиду недостаточного терапевтического эффекта. У детей, однако, проводят лечение поллиноза и бронхиальной астмы пероральным методом.
Оральная специфическая иммунотерапия пыльцевыми аллергенами была несколько менее эффективной в исследованиях. J. Oppenheimer et al (1994) указывает на возможность получения (121) 67,4% отличных и хороших результатов при оральном методе СИТ, в сравнении с результатами классического инъекционного специфического лечения (76,9%).
Разработанный в Институте иммунологии новый ускоренный пероральный метод специфической иммунотерапии аллергенами «глицал» позволил получить больший процент отличных и хороших результатов, по сравнению с ускоренным парентеральным методом водно-солевыми экстрактами.
При проведении специфической иммунотерапии также используется интраназальный или ингаляционный метод введения бытовых и пыльцевых аллергенов, результаты которого оказались более эффективными, в сравнении с подкожным методом лечения. Преимуществом данного метода является нетравматичность, меньшее число осложнений и возможность проведения лечения на дому с помощью ингалятора.
Локальная интраназальная специфическая иммунотерапия аллергеном амброзии позволила улучшить состояние больных в 71,5% случаев, а в группе получавших плацебо значительно меньше (Nickelsen et al, 1981).
Специфическая иммунотерапия больных атопической бронхиальной астмой проводилась в Республиканском аллергологическом центре. Больные, прошедшие специфическую иммунотерапию, были в возрасте от 10 до 60 лет. Средний возраст — 27,5 лет. Продолжительность наблюдения составила 5 -30 лет.
При обращении превалировали пациенты со средней степенью тяжести бронхиальной астмы (69%). В период с 1971 по 1985 гг. больные получили от 1 до 10 курсов специфической иммунотерапии (всего 726 курсов).
Специфическая иммунотерапия проводилась по классической замедленной схеме водно-солевыми экстрактами бытовых, эпидермальных и пыльцевых аллергенов. Инъекции делали 1 — 2 раза в неделю с постепенным повышением концентрации аллергена. Больные получали в среднем 30 — 40 инъекций. Продолжительность курса доставляла 5-8 месяцев, с переводом их в последующем на поддерживающую дозу 1:10-0,5 один раз в неделю от 2 — 6 инъекций.
Перерывы между курсами составляли не более 3-4 месяцев. За курс лечения больной получал в среднем от 5967 до 8967 PNU. Специфическая иммунотерапия начиналась осенью, когда отцветала амброзия, и завершалась в июне. После получения хорошего терапевтического эффекта больным рекомендовалось продолжение специфической иммунотерапии для закрепления результата лечения.
Эффективность специфической иммунотерапии оценивалась по клиническим и иммунологическим показателям.
Клинические показатели оценивались следующим образом: отличный эффект, хороший, удовлетворительный, неудовлетворительный (А. Д. Адо, Н. В. Адрианова, 1976) (табл. 28):
а) отличный эффект — после лечения исчезли все проявления заболевания (приступы удушья, кашель, ринорея). Бронхолитическими и антигистаминными препаратами больной не пользовался;
б) хороший — проявления болезни стали очень редкими и легкими, т. е. выраженных приступов удушья не стало, иногда беспокоили легкие затруднения дыхания, кашель, небольшой насморк. Все симптомы легко купировались малыми дозами бронхолитиков в ингаляциях;
в) удовлетворительный — приступы удушья стали протекать легче и реже. Число необходимых лекарств значительно уменьшилось;
г) неудовлетворительный — эффекта от лечения не наступило.
Результаты специфического лечения оценивались сразу же после окончания курса лечения, а за пациентами, прошедшими специфическую иммунотерапию, наблюдения продолжались в течение длительного времени (до 30 лет). В последующем больные осматривались один раз в году — осенью, в период наиболее вероятного обострения заболевания. При нестойком терапевтическом эффекте проводились повторные курсы иммунотерапии до получения стойкой клинической ремиссии, при стойкой клинической ремиссии через каждые 3-5 лет проводились профилактические, т. е. противорецидивные курсы иммунотерапии, что обозначено нами как вторичная иммунопрофилактика астмы. Если курсы иммунотерапии не повторялись, возможными становились рецидивы астмы.
При проведении специфической иммунотерапии больные выдерживали элиминационные мероприятия, по мере необходимости принимали медикаментозное лечение (бронхолитики, антигистаминные препараты, интал, за исключением кортикостероидов).
Специфическое лечение проводили стандартными бытовыми и эпидермальными аллергенами. Получено 67,5 ± 3,7% отличных и хороших результатов, у 20,0 ± 3,16% — эффект удовлетворительный, у 8,1 ± 2,14% — эффекта от лечения не было, а у 4,4 ± 0,38% — приступы удушья возобновились вновь после длительной клинической ремиссии.
Результаты иммунотерапии не всегда были устойчивы. Из 108 больных с отличным и хорошим эффектом в период клинической ремиссии у некоторых отмечали насморк, кашель, одышку при контакте с неспецифическими раздражителями (запахом краски, при переохлаждении, респираторном заболевании). Все это расценивалось нами как нестойкий терапевтический эффект.
Последующий анализ показал, что подобные обострения чаще возникали у больных, которые нарушали последовательность и ритмичность лечения, т. е. пройдя один курс специфического лечения, почувствовав облегчение или исчезновение приступов удушья, они самовольно прекращали лечение. Через несколько лет, когда состояние их ухудшалось, они вновь являлись к аллергологу, получали следующий курс иммунотерапии и прекращали его до очередного ухудшения состояния.
70 больных имели стойкий терапевтический эффект, в связи с чем в дальнейшем специфическое лечение им было прекращено, а наблюдение за ними продолжалось. Большинство из них лечилось регулярно, подряд 2-3 курса и более с небольшими перерывами между курсами.
Больной С. М., 20 лет, обратился к аллергологу. Страдает бронхиальной астмой. Первый приступ удушья связывает с фактором переохлаждения. В последующем приступы удушья приняли характер атопической астмы, дома, в селе, приступы удушья были каждую ночь, вне дома, в стационаре был здоров. Больному провели два курса специфического лечения бытовыми аллергенами.
Состояние несколько улучшилось, но приступы удушья еще беспокоили, в связи с чем больному начали третий курс специфической иммунотерапии в условиях стационара, затем продолжили его в условиях высокогорья. После проведения еще трех курсов бытовыми аллергенами был получен отличный терапевтический эффект, стойкая клиническая ремиссия. Больной служил в рядах Советской Армии, и приступы удушья не возобновились. Отдаленные результаты лечения с отличным эффектом — 20 лет.
Из данных аллергологического анамнеза: у матери и у дяди по линии матери бронхиальная астма.
У двух сестер тоже появились приступы удушья. Обе сестры обследованы, диагноз атопической астмы подтвержден, проведено специфическое лечение. Одна из сестер провела подряд два курса специфической иммунотерапии с отличным эффектом. Отдаленные результаты с отличным эффектом — 6 лет. Другая сестра по семейным обстоятельствам сумела провести только один курс специфической иммунотерапии, чувствовала себя хорошо в течение двух лет, однако спустя год у больной — рецидив астмы, развился приступ удушья.
Таким образом, при регулярном проведении специфической иммунотерапии не менее двух курсов получена стойкая клиническая ремиссия, в то время как у одной из сестер получена нестойкая клиническая ремиссия с последующим рецидивом астмы, что явилось основанием для продолжения специфической иммунотерапии.
Возобновление приступов удушья у больной после длительной клинической ремиссии навело нас на мысль о необходимости проведения профилактических, т. е. противорецидивных курсов иммунотерапии с целью продлить клиническую ремиссию.
Поскольку результаты специфической иммунотерапии были относительно невысокими (67,5 ± 3,74% отличных и хороших результатов), специфическая иммунотерапия продолжена у части из них с целью улучшить терапевтический эффект или закрепить уже полученный хороший терапевтический эффект.
С целью улучшения терапевтического эффекта продолжено специфическое лечение краевыми аллергенами — клещом, амброзией и аллергеном домашней пыли, а при отсутствии эффекта специфическое лечение проводилось в условиях горного климата Приэльбрусья. При сочетании с пищевой аллергией назначали элиминационные диеты.
При проведении специфической иммунотерапии больным с сочетанной полиаллергией выдерживалась определенная последовательность: сначала лечение проводилось бытовыми и эпидермальными аллергенами, а затем — пыльцевыми (табл. 29).
Учитывая наличие выраженной сенсибилизации к клещу у 210 (51,4 ± 2,46%) больных, при проведении специфической иммунотерапии к смеси домашней пыли и пера подушки подключали 0,1 мл аллергена клеща Dermatophagoides pteronyssinus с содержанием 10000 PNU в 1 мл и продолжали специфическую иммунотерапию по обычной методике и схеме.
Для проведения специфической иммунотерапии были взяты больные, у которых клинически явно превалировал выраженный клещевой компонент — приступы удушья дома, ночью, четкий фактор элиминации, к тому же эффект специфической иммунотерапии, полученный от предыдущих курсов, был недостаточным. В эту группу включены больные в возрасте от 15 до 64 лет.
При проведении специфической иммунотерапии бытовыми и эпидермальными аллергенами с подключением аллергена клеща получено отличных и хороших результатов 80,0 ± 6,7%.
Проведение специфического лечения бытовыми, эпидермальными аллергенами с подключением аллергена клеща оказалось значительно эффективнее, что свидетельствует об этиологической значимости его.
Учитывая данные литературы о том, что краевые и индивидуальные аллергены являются более специфичными, были приготовлены краевые и индивидуальные аллергены в Институте иммунологии МЗ РФ.
Специфическая иммунотерапия краевым аллергеном домашней пыли проведена 73 больным, ранее у которых при использовании стандартных аллергенов не удалось достигнуть желаемого эффекта (табл. 30).
источник
Патогенез бронхиальной астмы определяется клинико-патогенетическим вариантом.
Патогенез атопической бронхиальной астмы. В иммунологической фазе под влиянием неинфекционного аллергена (пыльца растений, растительные и животные белки, лекарственные средства) в условиях врожденного или приобретенного дефицита Т-супрессорной функции В-лимфоцитами продуцируются реагиновые IgE-антитела, которые фиксируются на тучных клетках. В патохимической стадии при повторном контакте с аллергеном происходит его связывание с иммуноглобулином Е на поверхности тучных клеток слизистой оболочки бронхов, агрегация мембранных IgE-рецепторов, дегрануляция тучных клеток — активный секреторный процесс (экзоцитоз) с выделением медиаторов, не сопровождающийся повреждением и гибелью клетки. Выделяются следующие медиаторы: обладающие бронхоспастическим и вазоактивным эффектом (гистамин; лейкотриены LTA4, LTB4, LTC4, LTD4; медленно действующая субстанция, основными компонентами которой являются LTC4 и LTD4; калликреин-подобное вещество, простагландины F2a, G2, D2, тромбоксан А2); обладающие хемотаксическим действием (эозинофильный и нейтрофильные хемотаксические факторы); протеолитические ферменты; лизосомальные ферменты; фактор активации тромбоцитов. В патофизиологической стадии под влиянием медиаторов развивается гиперреактивность бронхов, что проявляется бронхоспазмом, отеком слизистой оболочки бронхов, гиперкринией и дискринией — гиперсекрецией слизи и повышением ее вязкости. Развитию гиперреактивности бронхов способствует врожденный или приобретенный недостаток в бронхах фермента аденилциклазы. В дальнейшем формируется условно-рефлекторный механизм бронхиальной астмы.
Патогенез инфекционно-зависимой бронхиальной астмы. В патогенезе инфекционно-зависимого варианта БА участвуют следующие механизмы:
гиперчувствительность замедленного типа, основная роль в развитии которой принадлежит Т-лимфоцитам. При повторных контактах с инфекционным аллергеном они гиперсенсибилизируются и приводят к выделению медиаторов замедленного действия: факторов хемотаксиса нейтрофи-лов, эозинофилов, лимфотоксина, фактора агрегации тромбоцитов. Медиаторы замедленного действия вызывают в клетках-мишенях (тучные клетки, базофилы, макрофаги) освобождение простагландинов (PgD2, F2a), лейкотриенов (LNC4, LND4, LNE4) и др., вследствие чего развивается бронхоспазм. Кроме того, вокруг бронха формируется воспалительный инфильтрат, содержащий нейтрофилы, лимфоциты, эозинофилы. Этот инфильтрат является источником медиаторов немедленного типа (лейкотриены, гистамин), вызывающих спазм бронха и его воспаление. Из гранул эозинофилов выделяются также белки, повреждающие непосредственно мерцательный эпителий бронхов, что затрудняет эвакуацию мокроты;
аллергическая реакция немедленного типа с образованием реагина IgE (аналогично атопической астме). Развивается редко, на ранних стадиях инфекционно-зависимой БА, главным образом при грибковой и нейссериальной астме;
неиммунологические реакции — повреждение токсинами надпочечников и снижение глюкокортикоиднои функции, нарушение функции мерцательного эпителия и понижение активности р2-адренорецепторов.
Патогенез дисгормонального варианта бронхиальной астмы. В патогенезе четко участвуют гормональные факторы. Наиболее изучены нарушения глюкокортикоиднои функции и функции половых желез. Глюкокортикоидная недостаточность развивается преимущественно вследствие длительного лечения глюкокортикоидами, инфекционно-токсических влияний на надпочечники и способствует формированию гиперактивности тучных клеток, повышению уровня гистамина и PgF2a в крови и развитию бронхоспазма. Дизовариальные расстройства проявляются гиперэстрогенизмом и гипопрогестеронемией. Гиперэстрогенизм повышает активность транскортина, который связывает гидрокортизон крови и усугубляет надпочечниковую недостаточность, снижает активность р2-адренорецепторов. Гипопрогестеронемия понижает активность р2-адренорецепторов и способствует бронхоспазму.
Патогенез аутоиммунного варианта бронхиальной астмы.Этот вариант является этапом дальнейшего прогрессирования и усугубления течения атопической и инфекционно-зависимой БА. К патогенетическим механизмам этих форм присоединяются аутоиммунные реакции. При атопической БА выявляются аутоантитела (антиядерные, противолегочные, к гладким мышцам бронхов, к р-адренорецепторам мышц бронхов). Формирование иммунных комплексов (аутоантиген + аутоантитело) ведет к иммунокомплексному повреждению бронхов и р-адренергической блокаде.
Патогенез нервно-психического варианта бронхиальной астмы. Этот вариант, как и другие, может быть ведущим на определенных этапах болезни. Основные патогенетические механизмы следующие. Психоэмоциональные стрессы непосредственно влияют на тонус бронхов, так как при этом развивается повышенная чувствительность бронхов к гистамину и ацетилхолину. Кроме того, эмоциональное напряжение вызывает гипервентиляцию, стимуляцию ирритативных рецепторов бронхов внезапным глубоким вдохом, кашлем, смехом, плачем, что ведет к рефлекторному спазму бронхов.
Патогенез холинергичес кого варианта бронхиальной астмы. Основной патогенетический механизм — выраженная ваготония, что приводит к возбуждению ацетилхолиновых рецепторов и спазму преимущественно крупных и средних бронхов, а также к гиперсекреции слизистых и серозных желез трахеи и бронхов.
Патогенез формы «Первично-измененная реактивность бронхов» (в том числе «аспириновой астмы» и «астмы от физического усилия»). Это неиммунологическая бронхиальная астма, она связана не с первичными иммунологическими, эндокринными, нервно-психическими нарушениями, а с врожденной гиперреактивностью бронхов. В развитии гиперреактивности бронхов имеет значение увеличение межэпителиальных промежутков (это способствует прохождению через них различных химических раздражителей из воздуха, вызывающих дегрануляцию тучных клеток) и чрезвычайно выраженная реактивность бронхиальных ирритационных рецепторов, реагирующих сокращением бронха на воздействие холодного воздуха, табачного дыма и т. д.
«Астма от физического усилия» возникает вследствие повышенной чувствительности тучных клеток, альвеолярных макрофагов, слизеобразующих желез и гладких мышц бронхов к различным воздействиям. При интенсивном физическом усилии развивается гипервентиляция, в результате чего происходит испарение влаги бронхов, их охлаждение и дегрануляция тучных клеток, выделение медиаторов аллергии и воспаления, что ведет к спазму и отеку бронхов.
В основе «аспириновой астмы» лежит нарушение метаболизма арахидоновой кислоты под влиянием аспирина и других нестероидных противовоспалительных средств. После их приема из арахидоновой кислоты мембраны клеток вследствие активации 5-липооксигеназного пути образуются лейкотриены, вызывающие бронхоспазм. Одновременно угнетается циклооксигеназный путь метаболизма арахидоновой кислоты, что ведет к уменьшению образования PgE (расширяет бронхи) и увеличению — PgF2a (суживает бронхи). «Аспириновую астму» вызывают аспирин, нестероидные противовоспалительные средства (индометацин, бруфен, вольтарен и др.), баралгин, антастман, теофедрин, а также продукты, содержащие салициловую кислоту (огурцы, цитрусовые, томаты, различные ягоды) или желтые красители (тартразин).
Основным клиническим проявлением БА типичным для данного заболевания является приступ удушья, в котором различают 3 периода: период предвестников, период разгара и период обратного развития.Клинически он проявляется –экспираторной одышкой и приступами кашля с отхождением вязкой трудноотделяемой мокротой.
Типичная поза с приподнятым верхним плечевым поясом,грудная клетка цилиндрической формы.Больной делаетт короткий вдох и без паузы продолжительный мучительный выдох,сопровождающийся сухими дистанционными хрипами.В дыхании активно учавствует вспомогательная мускулатура грудной клеттки,плечевого пояса, брюшного пресса.Межреберныепромежутки расширены и расположены горизонтально.
При перкуссии-характерный коробочный звук.Нижние границы легких смещены вниз,снижена экскурсия легочных полей. Нередко экспираторная одышка провоцируется физической нагрузкой, резкими запахами, но затруднение дыхания при этом не достигает интенсивности приступа удушья, проходит самостоятельно.
Бронхообструктивный синдром у больных проявляется сильным, приступообразным кашлем, усиливающимся от разных запахов, при снижении температуры вдыхаемого воздуха, ночью и утром при вставании с постели, при заболевании гриппом, острым катаром верхних дыхательных путей, от физической нагрузки, нервного напряжения и других причин. Кашель утихает или становится менее интенсивным после приёма внутрь или ингаляции бронхолитиков.
При аускультации-ослабленное дыхание,сухие хрипы по всей легочной поверхности.После кашля количество хрипов увеличивается.При продуктивном кашле их количество уменьшается и дыхание из ослаблленного становится жестковатым.
. Внелёгочные проявления: вазомоторный ринит, крапивница, нейродермит, вазомоторный отёк Квинке, мигрень.
При длительно протекающих приступах удушья могут появляться признаки недостаточности правого желудочка. При рентгенологическом исследовании определяется повышенная прозрачность лёгочных полей, низкое стояние диафрагмы.
источник
– это хроническое заболевание, при котором в стенке бронха развивается аллергическое воспаление. Это воспаление чаще возникает в результате действия аллергенов, других веществ.
Именно воспаление приводит к симптомам болезни – затрудненному дыханию или даже удушью, кашлю, появлению хрипов в груди, что является следствием сужения дыхательных путей из-за развития спазма мышц бронхов (бронхоспазм), отека их слизистой оболочки и появления густой, вязкой слизи в их просвете. Все это – следствие воспалительного процесса.
Приступ астмы характеризуется коротким вдохом и удлиненным выдохом. Воздух с трудом проходит при вдохе в бронхи и с трудом выходит, создавая характерное шумное, «свистящее» дыхание, нередко слышимое на расстоянии. Дыхание учащается, одышка усиливается при нагрузке или при разговоре.
Приступы бронхиальной астмы возникают как днем, так и в течение ночи. Тяжелые затяжные приступы могут перейти в астматическое состояние – один из наиболее грозных вариантов течения болезни.
Когда симптомы бронхиальной астмы отсутствуют – этот период расценивается как ремиссия. Не выздоровление от астмы, а именно ремиссия (от латинского слова remissio – уменьшение, ослабление).
Мы уже говорили, что астма – хроническое заболевание и если приступов нет даже в течение нескольких месяцев или лет, можно говорить о длительной ремиссии, а не о полном выздоровлении ребенка. Он может прекрасно себя чувствовать, вести практически нормальный образ жизни, но склонность бронхов к бронхоспазму у подавляющего большинства пациентов остается практически на всю жизнь. Как только мы с вами об этом забываем, так эта коварная болезнь норовит вернуться.
Нужно еще помнить о том, что ремиссия может быть клиническая, то есть наступившая после успешного курса лечения или благоприятного изменения образа жизни, и фармакологическая – на фоне приема лекарственных препаратов. Конечно, клиническая ремиссия лучше, чем фармакологическая.
Но запомните! Если без лечения приступы (пусть по вашему мнению и нетяжелые) повторяются вновь и вновь или острых приступ удушья нет, а малыш кашляет по ночам, врач при осмотре выслушивает у него хрипы, исследование функции дыхания подтверждает, что бронхи сужены – может развиться хроническое аллергическое воспаление слизистой бронхов.
Именно аллергическое, а не инфекционное, которое требует лечения антибиотиками. Хроническое аллергическое воспаление слизистой оболочки при бронхиальной астме приводит к необратимым изменениям в стенке бронхов, а необратимые изменения, как вы понимаете, лечить поздно!
Риск заболеть астмой существенно выше, если родственники (не только родители) страдали или страдают бронхиальной астмой. И не только астмой.
Такие заболевания как нейродермит, крапивница, сезонное воспаление слизистой носа и глаз, пищевая или лекарственная аллергия имеют прямое отношение к риску возникновения бронхиальной астмы.
К счастью, астма не относится к тем заболеваниям, которые обязательно проявятся в следующем поколении. Это объясняется тем, что наследуется не сама астма, а особенность иммунной системы. Иммунная система существует для защиты организма от воздействия чуждых для каждого конкретного человека веществ.
У больных астмой эта защитная система необоснованно бурно реагирует на контакт с веществами (аллергенами), которые у здоровых людей такой реакции не вызывают.
Наиболее распространенные аллергены — домашняя пыль, особенно клещи домашней пыли, аллергены животных, пыльца растений, плесневые и дрожжевые грибы, пищевые аллергены.
Приступ астмы может развиться при контакте с аэрозолями, красками, парфюмерией и другими резкими запахами. Физическая нагрузка, респираторные инфекции, холод, высокая влажность, колебания атмосферного давления, гроза часто влияют на самочувствие больных астмой. Эмоциональный стресс, нервные перегрузки, смех, плач, страх могут быть причиной приступа астмы.
Уточнить, какие аллергены вызывают появление аллергических реакций, возможно с помощьюаллергообследования, которое включает в себя осмотр, подробный сбор аллергологического анамнеза больного и всей семьи, постановку кожных тестов, лабораторную диагностику.
Наиболее часто применяют скарификационные и уколочные тесты (прик-тесты). Они достаточно специфичны и высоко чувствительны.
Ставятся кожные тесты только в период клинической ремиссии бронхиальной астмы и после санации очагов хронической инфекции. Не проводят кожные тесты в период обострения бронхиальной астмы, атопического дерматита и аллергического ринита, а также при лечении гормональными и антигистаминными препаратами, поскольку они искажают (снижают) кожную чувствительность.
Противопоказаниями для аллергологического обследования с помощью кожного тестирования являются также острые интеркурентные инфекционные заболевания, острые психические расстройства. В случаях тяжелого течения бронхиальной астмы, постоянного рецидивирования, при необходимости выявления причинно-значимых аллергенов для проведения соответствующих элиминационных мероприятий, показано применение современных лабораторных методов диагностики для определения специфических IgE и IgG антител в крови.
Следует иметь в виду, что даже при положительных иммунологических тестах у больных бронхиальной астмой необходимо их сопоставление с данными анамнеза и результатами других методов диагностики, т.к. они могут отражать состояние латентной сенсибилизации, быть результатом перекрестной чувствительности, либо низкого качества аллергенов.
Одним из необходимых условий успешного лечения бронхиальной астмы является объективная оценка сужения бронхов. Оценку функции легких (функцию внешнего дыхания), в особенности обратимость ее нарушений после приема бронхорасширяющего препарата, проводят с помощью компьютерной пневмотахографии в кабинете аллерголога – иммунолога.
Лечение бронхиальной астмы в первую очередь заключается в борьбе с аллергическим воспалением.
В подавляющем большинстве случаев недостаточно просто расширять бронхи – через некоторое время дыхательные пути снова сузятся. Поэтому основой лечения являются мероприятия и лекарства, направленные на подавление аллергического воспаления в стенке бронхов.
Начинать лечение бронхиальной астмы нужно всегда с мероприятий по устранению контакта с известными и подозреваемыми аллергенами. Соблюдение противоаллергического режима является одной из важнейших мер на пути преодоления болезни. Однако не всегда аллерген нам известен и, кроме того, через некоторое время простое удаление аллергена уже не приводит к исчезновению симптомов. Поэтому почти всегда больной, страдающий бронхиальной астмой, должен принимать профилактические, или базисные, противоастматические препараты.
У больных со среднетяжелой и тяжелой бронхиальной астмой врачи добиваются ремиссии с помощью терапии и для того, чтобы больной мог вести нормальный образ жизни, такой же, как все сверстники, необходим длительный прием различных препаратов, которые рекомендует опытный аллерголог – иммунолог.
Самым эффективными противовоспалительными лекарствами являются гормоны. При бронхиальной астме важны гормоны, которые вырабатываются надпочечниками, на медицинском языке – глюкокортикостероиды. Эти вещества, помимо всего прочего, регулируют состояние бронхов. Много лет назад эти гормоны были выделены из крови, а затем созданы их синтетические аналоги. Гормоны в таблетках давно используются при астме. В настоящее время существуют гормоны для вдыхания в бронхи – дозированные аэрозоли и пудры для ингаляций, а также суспензия для ингаляции с помощью небулайзера. Попадая непосредственно в орган, который болеет (то есть в бронхи), эти гормоны не оказывают действия на весь организм и поэтому могут применяться длительно в качестве базисной терапии.
До сих пор в представлении большинства людей гормоны – это зло. Причем больной, как правило, не делает разницы между таблетками и ингаляторами. Лечение при бронхиальной астме должно быть строго индивидуализировано с учетом варианта течения, фазы болезни, наличия осложнений, сопутствующих заболеваний, переносимости больным лекарственных средств и наиболее рационального их применения в течение суток. Такое лечение может назначить только опытный аллерголог-иммунолог.
источник
Бронхиальная астма — одно из самых частых хронических заболеваний легких. Оно чаще всего возникает у детей, хотя может начаться в любом возрасте. Среди детей, больных бронхиальной астмой, мальчиков на 30% больше, чем девочек, причем у мальчиков заболевание протекает более тяжело. В подростковом возрасте и у взрослых заболевание чаще встречается у женщин. Бронхиальная астма больше распространена среди городского населения с низким уровнем жизни, а также среди лиц, живущих в странах с холодным климатом и в индустриальных районах. Существует наследственная предрасположенность к бронхиальной астме. Об этом свидетельствует повышенная заболеваемость бронхиальной астмой близких родственников больных. Однако, несмотря на это, подсчитать риск этого заболевания невозможно.
Если бронхиальная астма начинается в раннем детском возрасте, то прогноз, как правило, благоприятный: к периоду полового созревания у 80% больных все проявления заболевания исчезают или становятся менее выраженными. Примерно у 20% из них после 45 лет возникает рецидив заболевания. Случаи выздоровления среди взрослых больных бронхиальной астмой отмечаются реже. У детей бронхиальная астма течет тяжелее, если она сочетается с аллергическими заболеваниями дыхательных путей или диффузным нейродермитом. Прогноз бронхиальной астмы особенно неблагоприятен у больных с аспириновой триадой. Непереносимость аспирина обычно наблюдается у взрослых, чаще у женщин, связь с аллергическими заболеваниями в анамнезе отсутствует. Летальность бронхиальной астмы увеличивается с возрастом: у детей она составляет не более 1%, у взрослых — 2—4%. К факторам риска смерти при бронхиальной астме относятся частые, длительные и плохо поддающиеся лечению, а также тяжелые приступы в анамнезе, случаи резкого ухудшения состояния в течение суток, низкий уровень знаний больного о своем заболевании, отсутствие взаимопонимания между больным и врачом, низкий уровень жизни больного, недоступность медицинской помощи, бесконтрольное применение бета-адреностимуляторов, низкая эффективность противовоспалительного лечения. В 1978—1987 гг. летальность бронхиальной астмы возросла, особенно среди детей младшего возраста и представителей цветных рас.
Разнообразие проявлений бронхиальной астмы затрудняет ее классификацию. На сегодняшний день наиболее распространена этиологическая классификация бронхиальной астмы, согласно которой выделяют три формы заболевания: экзогенную, эндогенную и смешанную. Основная причина экзогенной бронхиальной астмы — аллергены. Экзогенная бронхиальная астма возникает, как правило, у лиц младше 20 лет. При этой форме заболевания кожные и провокационные пробы с аллергенами обычно положительны. Эндогенная бронхиальная астма обусловлена не аллергенами, а инфекцией, физическим или эмоциональным перенапряжением, резкой сменой температуры, влажности воздуха и т. д. Смешанная форма заболевания сочетает в себе признаки экзо- и эндогенной бронхиальной астмы, чаще встречается у детей.
I. Патогенез. Ведущую роль в патогенезе бронхиальной астмы играет повышенная реактивность бронхов, которая приводит к их периодической обратимой обструкции. Она проявляется: 1) повышением сопротивления дыхательных путей, 2) перерастяжением легких, 3) гипоксемией, вызванной очаговой гиповентиляцией и несоответствием между вентиляцией и перфузией легких, 4) гипервентиляцией.
А. Воспаление, вегетативные и иммунные нарушения. В норме тонус гладких мышц бронхов регулируется преимущественно парасимпатическими волокнами, входящими в состав блуждающего нерва. Применение лекарственных средств, блокирующих проведение возбуждения по парасимпатическим волокнам, приводит к расширению бронхов. Стимуляция этих волокон, напротив, вызывает бронхоспазм. Тонус гладких мышц бронхов меняется и под действием афферентных волокон, идущих от рецепторов бронхов и входящих в состав блуждающего нерва. В норме симпатическая нервная система играет незначительную роль в регуляции тонуса гладких мышц бронхов. При бронхиальной астме роль симпатических влияний на бронхи возрастает. Стимуляция немиелинизированных волокон (афферентных волокон типа C, расположенных в стенке бронхов и альвеол) медиаторами воспаления приводит к высвобождению нейропептидов, например вещества P, которые вызывают сужение бронхов, отек слизистой и увеличение секреции слизи.
1. Ведущую роль в патогенезе бронхиальной астмы играет повышенная реактивность бронхов, обусловленная как нарушением вегетативной регуляции тонуса гладких мышц, так и действием медиаторов воспаления. О роли вегетативных нарушений в патогенезе бронхиальной астмы свидетельствует снижение реактивности бронхов при блокаде афферентных и эфферентных волокон блуждающего нерва.
2. На гладкомышечных клетках бронхов находятся альфа-, бета1— и бета2-адренорецепторы. Преобладают бета-адренорецепторы, причем, бета2-адренорецепторов в 3 раза больше, чем бета1-адренорецепторов. Роль бета-адренорецепторов в патогенезе бронхиальной астмы до конца не изучена. Известно, что стимуляция бета2-адренорецепторов снижает реактивность бронхов у больных бронхиальной астмой, однако блокада бета-адренорецепторов у здоровых лиц не вызывает заметного изменения реактивности бронхов. Стимуляция альфа-адренорецепторов почти не влияет на тонус гладких мышц бронхов.
3. Кальций играет важную роль в сокращении гладких мышц бронхов. АТФ-зависимый кальциевый насос, выводящий кальций из клетки, участвует в поддержании мембранного потенциала покоя гладкомышечных клеток бронхов. Повышение внутриклеточной концентрации кальция приводит к сокращению, а уменьшение — к расслаблению гладкомышечных клеток. Кроме того, повышение внутриклеточной концентрации кальция вызывает дегрануляцию тучных клеток. Предполагается, что в регуляции уровня кальция в тучных клетках участвуют адренорецепторы.
4. Циклические нуклеотиды — цАМФ и цГМФ — образуются под действием мембраносвязанных ферментов аденилатциклазы и гуанилатциклазы из АТФ и ГТФ соответственно. Циклические нуклеотиды участвуют в регуляции сокращения гладкомышечных клеток бронхов и дегрануляции тучных клеток. Выброс медиаторов тучными клетками под действием M-холиностимуляторов и простагландина F2альфа опосредован повышением уровня цГМФ. Стимуляция альфа-адренорецепторов приводит к снижению уровня цАМФ, что также вызывает дегрануляцию тучных клеток. Стимуляция бета-адренорецепторов приводит к повышению уровня цАМФ и, как следствие, к угнетению дегрануляции тучных клеток. Полагают, что блокада аденозиновых рецепторов также угнетает дегрануляцию.
5. Выброс тучными клетками медиаторов, влияющих на тонус бронхов и сосудов, играет ведущую роль в патогенезе экзогенной бронхиальной астмы. Связывание антигенов с IgE, фиксированными на поверхности тучных клеток, вызывает выброс медиаторов гранул и стимуляцию метаболизма фосфолипидов мембраны (см. гл. 2, п. I.Г.1 ). К медиаторам гранул относятся гистамин, анафилактический фактор хемотаксиса эозинофилов и анафилактический фактор хемотаксиса нейтрофилов. Из фосфолипидов мембраны образуются арахидоновая кислота и фактор активации тромбоцитов. Метаболизм арахидоновой кислоты приводит к накоплению лейкотриенов и простагландинов (см. гл. 2, п. I.Г.2.а ). Гистамин вызывает мгновенный и кратковременный бронхоспазм, тогда как лейкотриены — отсроченный и более длительный. Гистамин и лейкотриены относятся к медиаторам ранней фазы, а факторы хемотаксиса и фактор активации тромбоцитов — к медиаторам поздней фазы аллергической реакции немедленного типа. Медиаторы поздней фазы вызывают хемотаксис, активацию клеток воспаления в слизистой бронхов и стимулируют синтез лейкотриенов в этих клетках. Бронхоспазм, вызываемый факторами хемотаксиса и фактором активации тромбоцитов, возникает через 2—8 ч после начала аллергической реакции и может длиться несколько суток. Среди других медиаторов, которые участвуют в патогенезе экзогенной бронхиальной астмы, можно отметить гепарин , тромбоксаны, серотонин, свободные радикалы кислорода, кинины, нейропептиды, протеазы и цитокины (см. табл. 2.1 ).
Б. Патологические изменения, приводящие к обструкции дыхательных путей. Обструкция дыхательных путей — наиболее характерный признак бронхиальной астмы. Патологические изменения, приводящие к сужению бронхов, затрагивают слизистую оболочку, подслизистый слой и мышечную оболочку бронхиального дерева. Патологический процесс распространяется от трахеи и крупных бронхов к терминальным бронхиолам (см. рис. 7.1 ). К сужению бронхов приводит спазм гладких мышц, образование слизистых пробок, отек и воспаление слизистой. Обструкция усиливается во время выдоха, поскольку при этом происходит динамическое сужение дыхательных путей. Из-за сужения бронхов часть воздуха задерживается в альвеолах (эффект воздушной ловушки), что приводит к перерастяжению легких и удлинению выдоха. Избыточное сопротивление дыхательных путей приводит к увеличению работы дыхания, в акт дыхания включаются вспомогательные мышцы, появляется одышка (см. рис. 7.2 ).
1. Образование слизистых пробок. При бронхиальной астме в дыхательных путях образуется густая, вязкая слизь. Она содержит слущенный эпителий бронхов, эозинофилы, кристаллы Шарко—Лейдена. Слизь может частично или полностью закупоривать просвет бронхов. Чем длительнее и тяжелее приступ, тем более вязкой становится слизь из-за дегидратации.
2. Изменения стенки бронхов. При бронхиальной астме уменьшается количество клеток мерцательного эпителия, увеличивается количество и наблюдается гиперплазия бокаловидных клеток, секретирующих слизь. Кроме того, возникают эозинофильная инфильтрация, отек и утолщение базальной мембраны. В подслизистом слое также наблюдаются инфильтрация эозинофилами, нейтрофилами, лимфоцитами и макрофагами, гипертрофия желез, отек. Отмечается гипертрофия мышечной оболочки бронхов.
3. Наиболее вероятная причина острых кратковременных приступов бронхиальной астмы — бронхоспазм. Длительные и плохо поддающиеся лечению приступы бронхиальной астмы обусловлены закупоркой бронхов слизистыми пробками и отеком слизистой бронхов.
4. В патологический процесс могут быть вовлечены крупные, средние и мелкие бронхи, однако чаще всего на первый план выступает обструкция мелких бронхов. Шумное, свистящее дыхание наблюдается при обструкции крупных бронхов, а приступы одышки и кашля более характерны для обструкции мелких бронхов.
5. Обструкция бронхов во время приступа бронхиальной астмы приводит к увеличению остаточного объема, уменьшению ЖЕЛ и повышению общей емкости легких. Выраженность этих изменений зависит от тяжести приступа. Остаточный объем во время приступа может превышать значение общей емкости легких в межприступный период.
6. Обструкция бронхов во время приступа неравномерна, поэтому одни участки легких вентилируются лучше, другие — хуже. В норме перфузия плохо вентилируемых участков снижается. При бронхиальной астме это происходит далеко не всегда, равновесие между вентиляцией и перфузией нарушается, что приводит к снижению paO2. В легких случаях это может быть единственным изменением газового состава крови. Уровень paCO2 зависит от вентиляции альвеол. При легких и среднетяжелых приступах бронхиальной астмы возникает гипервентиляция, которая приводит к уменьшению paCO2 и дыхательному алкалозу. При тяжелых и длительных приступах, напротив, развивается гиповентиляция, повышается paCO2 и возникает дыхательный ацидоз.
7. Перерастяжение легких и снижение парциального давления кислорода в альвеолах вызывают сужение капилляров альвеол и повышение давления в легочной артерии. Чем тяжелее приступ бронхиальной астмы, тем более выражена легочная гипертензия.
А. Анамнез имеет огромное значение в диагностике и лечении бронхиальной астмы (см. гл. 2, п. II.А ). Бронхиальную астму исключают во всех случаях беспричинной одышки или приступообразного кашля, а также при частых бронхитах и пневмонии, особенно у детей. В большинстве случаев диагноз бронхиальной астмы поставить несложно.
1. О тяжести заболевания можно судить по частоте, длительности и тяжести приступов. При обследовании во время приступа обязательно уточняют, когда он начался и чем мог быть вызван (инфекцией, контактом с аллергеном и т. д), отличается ли этот приступ от предшествующих, не беспокоят ли больного тошнота, рвота, боль в груди, лихорадка, какие препараты принимал больной до и во время приступа, а также дозы и время их применения.
2. Уточняют состояние больного в межприступный период. Это также позволяет оценить тяжесть заболевания и выбрать схему лечения. Выясняют, наблюдаются ли в этот период одышка и кашель, в том числе ночью и после физического усилия, каковы количество и характер мокроты, отмечаются ли повышенная утомляемость и снижение работоспособности. Кроме того, уточняют, какие лекарственные средства и в каких дозах применяет больной, какие отмечаются побочные эффекты. Выясняют, какие факторы обычно вызывают приступы, как болезнь влияет на учебу и работу больного.
3. Оценка состояния окружающей среды и условий труда и быта больного позволяет определить факторы, вызывающие приступы бронхиальной астмы, — контакт с аллергенами и раздражающими веществами, курение, эмоциональное или физическое перенапряжение, инфекцию, неблагоприятные климатические и погодные условия, профессиональные вредности, лекарственные средства (например, аспирин или бета-адреноблокаторы), пищевые добавки (например, глутамат или метабисульфит натрия).
4. Семейный анамнез. У родственников больного часто отмечаются бронхиальная астма и аллергические заболевания дыхательных путей.
Б. Физикальное исследование. Выраженность изменений, выявляемых при физикальном исследовании, зависит от частоты и тяжести приступов. При неосложненной бронхиальной астме в межприступный период физикальное исследование обычно в норме. Обязательно исключают аллергический ринит и синуситы, а также полипы носа (см. гл. 5, пп. I—III и VII ). Определяют частоту дыханий, пульс, АД, а также рост и вес больного, оценивают внешний вид и позу. При исследовании грудной клетки обращают внимание на ее форму, проводят перкуссию и аускультацию легких.
1. Во время приступа бронхиальной астмы дыхание и пульс учащены (следует помнить, что тахикардия наблюдается на фоне приема бета-адреностимуляторов), нередко повышено АД. В дыхании участвуют вспомогательные мышцы (лестничные, грудино-ключично-сосцевидные), характерно втяжение податливых участков грудной клетки, выдох через сжатые губы, расширение крыльев носа, увеличение переднезаднего размера грудной клетки, коробочный перкуторный звук, уменьшение подвижности нижнего края легких и экскурсии грудной клетки. Аускультативная картина неоднородна, выявляются жесткое дыхание, разнокалиберные сухие хрипы на вдохе и выдохе.
2. Во время тяжелого приступа бронхиальной астмы помимо симптомов, перечисленных в гл. 7, п. II.Б.1 , отмечаются цианоз, парадоксальный пульс, астериксис, миоз, отек диска зрительного нерва, нарушения чувствительности. При осмотре грудной клетки определяются ее расширение и резкое уменьшение экскурсии, при аускультации — дыхание не проводится, хрипы отсутствуют (немое легкое).
В. Лабораторные и инструментальные исследования. Дополнительные исследования бывают необходимы только для оценки длительности заболевания и тяжести приступа, для дифференциальной диагностики, выбора лечения и оценки его эффективности.
1. На рентгенограммах грудной клетки в межприступный период при неосложненной бронхиальной астме какие-либо изменения отсутствуют. Во время приступа выявляются повышенная прозрачность легочных полей, расширение грудной клетки, уплощение куполов диафрагмы. Из-за закупорки бронхов слизистыми пробками могут возникнуть сегментарные и субсегментарные ателектазы. При длительном и тяжелом течении бронхиальной астмы в боковых проекциях выявляются деформация грудины, кифоз грудного отдела позвоночника, возможно усиление легочного рисунка и расширение сосудов корней легких. Для диагностики неосложненной бронхиальной астмы рентгенография грудной клетки не нужна, однако ее проводят при первичном обследовании больных, поскольку это облегчает их дальнейшее наблюдение. Рентгенография грудной клетки показана при изменении течения заболевания или состояния больного. При этом можно выявить тени, ателектазы, пневмоторакс, пневмомедиастинум, изменение структуры легочной ткани. Проводить рентгенографию грудной клетки при каждом приступе бронхиальной астмы не требуется.
2. Рентгенография или КТ придаточных пазух носа показаны в тех случаях, когда бронхиальная астма сочетается с хроническими заболеваниями верхних дыхательных путей. На рентгенограммах можно выявить утолщение слизистой придаточных пазух носа, тени, уровни жидкости, кисты, полипы носа (см. гл. 5, п. VII.В.1—2 ).
3. Туберкулиновые пробы. Выясняют, были ли в прошлом туберкулиновые пробы положительными. Это особенно важно, если планируется лечение кортикостероидами. Туберкулиновые пробы проводят лишь тем больным, у которых в прошлом они были отрицательными. Для этого внутрикожно в предплечье вводят 5 ед (0,1 мл) очищенного туберкулина . Диаметр папулы измеряют через 48—72 ч.
4. Общий анализ крови при неосложненной бронхиальной астме обычно в норме. Иногда отмечается незначительная эозинофилия (число эозинофилов 500—1000 мкл –1 ). Характерно колебание числа эозинофилов — повышение ночью и в периоды контакта с аллергеном и уменьшение во время лечения кортикостероидами. Присоединение инфекции сопровождается снижением числа эозинофилов, увеличением числа нейтрофилов и сдвигом лейкоцитарной формулы влево. СОЭ при бронхиальной астме обычно в норме, а ее повышение свидетельствует о присоединении инфекции. Для диагностики бронхиальной астмы определение лейкоцитарной формулы не нужно, оно показано только при подозрении на вторичную инфекцию.
5. Исследование мокроты. При легком и среднетяжелом течении заболевания, особенно при экзогенной бронхиальной астме, кашель сухой. Мокрота появляется при длительном течении эндогенной бронхиальной астмы, особенно при ее сочетании с хроническим бронхитом.
а. Мокрота может быть слизистой или слизисто-гнойной. Желтая или желто-зеленая мокрота появляется при распаде эозинофилов и других клеток и не обязательно свидетельствует об инфекции.
б. Исследование мазков мокроты помогает в оценке эффективности кортикостероидов и диагностике инфекции. Мокроту собирают во время кашля. Если она не отходит, проводят ингаляцию физиологического раствора и перкуссионный массаж или получают мокроту с помощью катетера, введенного в трахею. В последнем случае в трахею можно ввести 3—5 мл стерильного физиологического раствора. Следует помнить, что все манипуляции, стимулирующие отхождение мокроты, могут усилить бронхоспазм. Мазки мокроты высушивают и окрашивают по Ханселу или Райту (см. приложение II, п. II ). В мазках обычно выявляется много макрофагов, эпителиальных клеток, нейтрофилов, слизи, фибрина, иногда обнаруживаются бактерии.
1) При экзогенной бронхиальной астме в мокроте определяются клетки мерцательного эпителия (25—35%), эозинофилы (5—80%), число нейтрофилов разное. При эндогенной бронхиальной астме и хроническом бронхите в мокроте присутствуют те же клеточные элементы, однако преобладают нейтрофилы, содержание эозинофилов колеблется от 5 до 20%. При обострении эндогенной бронхиальной астмы общее число клеток в мокроте увеличивается, однако соотношение между ними остается прежним, при обострении экзогенной бронхиальной астмы в мокроте повышается число эозинофилов. При лечении кортикостероидами число эозинофилов в мокроте уменьшается, что может быть критерием их эффективности при экзогенной бронхиальной астме.
2) При присоединении инфекции повышается число нейтрофилов и соотношение между нейтрофилами и эозинофилами, в мазке могут выявляться микробы. Для выявления возбудителя и определения его чувствительности к антимикробным средствам проводят посев мокроты. Это исследование особенно важно при частых приступах бронхиальной астмы и неэффективности лечения.
6. ЭКГ при неосложненной бронхиальной астме не выявляет изменений. При тяжелых приступах и длительном течении заболевания, особенно при сочетании бронхиальной астмы с хроническим бронхитом, возможно отклонение электрической оси сердца вправо, блокада правой ножки пучка Гиса, высокий заостренный зубец P. Во время приступа часто наблюдается тахикардия, которая усиливается при приеме бета-адреностимуляторов.
7. Общий уровень IgE в сыворотке, уровень специфических IgE и кожные пробы с аллергенами. При экзогенной бронхиальной астме общий уровень IgE в сыворотке обычно повышен. Это особенно характерно для детей и больных, у которых бронхиальная астма сочетается с диффузным нейродермитом или аллергическими заболеваниями верхних дыхательных путей. Однако определение общего уровня IgE в сыворотке у больных бронхиальной астмой малоинформативно и обычно не применяется. Для выбора метода лечения экзогенной бронхиальной астмы нередко проводят кожные пробы или определяют уровень специфических IgE, например с помощью РАСТ.
8. Исследование функции внешнего дыхания
а. Нарушения дыхания при бронхиальной астме обусловлены обратимой обструкцией дыхательных путей, что проявляется в первую очередь снижением ОФВ1 и пиковой объемной скорости. Эти показатели обычно быстро нормализуются после применения бронходилататоров (см. рис. 7.3 ). Увеличение ОФВ1 после применения бронходилататоров более чем на 20% свидетельствует об обратимом бронхоспазме. При закупорке бронхов слизистыми пробками и отеке слизистой действие бронходилататоров более медленное. Следует помнить, что отсутствие существенного увеличения ОФВ1 после применения бронходилататоров не исключает диагноза бронхиальной астмы. Отсутствие реакции может быть обусловлено следующими причинами: 1) отсутствием обструкции или незначительной обструкцией дыхательных путей в межприступный период, 2) действием бронходилататоров, примененных незадолго до проведения исследования, 3) неправильным применением ингаляционных бронходилататоров, 4) бронхоспазмом, вызванным раздражающими веществами, входящими в состав ингаляционных бронходилататоров, 5) бронхоспазмом, вызванным диагностическими процедурами, в частности спирометрией.
1) В межприступный период ОФВ1 обычно в норме. Показатели ОФВ1 и пиковой объемной скорости отражают состояние крупных бронхов. При сужении мелких (менее 2—3 мм в диаметре) бронхов ОФВ1 и пиковая объемная скорость нередко в норме (ОФВ1 бывает снижен только при выраженной обструкции мелких бронхов). Для оценки состояния мелких бронхов используют другой показатель — среднюю объемную скорость середины выдоха. Для определения ее строят график зависимости потока воздуха от объема форсированного выдоха — кривую поток—объем (см. рис. 7.3 ). Следует помнить, что изолированное снижение средней объемной скорости середины выдоха может наблюдаться и в межприступный период.
2) Зависимость скорости форсированного выдоха от плотности газа позволяет более точно определить диаметр бронхов, подверженных обструкции. Для выявления этой зависимости строят две кривые поток—объем: 1-ю — при вдыхании воздуха, 2-ю — при вдыхании газовой смеси низкой плотности, состоящей из 80% гелия и 20% кислорода. Если при дыхании газовой смесью низкой плотности скорость форсированного выдоха не менее чем на 20% выше, чем при дыхании воздухом, основное ограничение потока происходит в крупных бронхах. Отсутствие зависимости скорости форсированного выдоха от плотности вдыхаемого газа свидетельствует о преимущественной обструкции мелких бронхов. При легком течении бронхиальной астмы наблюдается обструкция преимущественно крупных бронхов. При тяжелой бронхиальной астме, особенно сопровождающейся постоянным кашлем и частыми инфекциями дыхательных путей, а также у курильщиков наблюдается преимущественная обструкция мелких бронхов. Обструкция мелких бронхов обычно бывает более стойкой, чем обструкция крупных бронхов.
3) Во время приступа бронхиальной астмы ОФВ1, пиковая объемная скорость и средняя объемная скорость середины выдоха снижаются пропорционально степени обструкции бронхов. Улучшение состояния сопровождается постепенной нормализацией этих показателей (см. рис. 7.4 ). Более быстрая нормализация пиковой объемной скорости и ОФВ1 по сравнению со средней объемной скоростью середины выдоха свидетельствует о том, что обструкция крупных бронхов лучше поддается лечению, чем обструкция мелких бронхов. Обструкция мелких бронхов часто связана с отеком и закупоркой слизистыми пробками, поэтому она требует более длительного лечения.
4) ЖЕЛ снижается во время приступов, а также при длительном течении бронхиальной астмы. Снижение ЖЕЛ объясняется прежде всего увеличением остаточного объема (см. рис. 7.5 ), которое обусловлено эффектом воздушной ловушки. Эффект воздушной ловушки и увеличение сопротивления дыхательных путей приводят к повышению функциональной остаточной емкости легких и общей емкости легких, что, в свою очередь, сопровождается перерастяжением легких. Оно носит компенсаторный характер, поскольку сопровождается увеличением диаметра бронхов. Однако при возрастании объема эластическая тяга легких и подвижность диафрагмы снижаются, что приводит к повышению работы дыхания. По мере увеличения обструкции бронхов снижение ЖЕЛ, повышение остаточного объема, функциональной остаточной емкости и общей емкости легких становятся более выраженными (см. рис. 7.5 ). После длительного приступа бронхиальной астмы легочные объемы восстанавливаются медленно. В некоторых случаях лечение тяжелой бронхиальной астмы приводит к субъективному улучшению без выраженного увеличения ОФВ1. Это объясняется тем, что изначально повышенные остаточный объем, общая емкость и функциональная остаточная емкость легких в процессе лечения существенно снижаются, что приводит к уменьшению перерастяжения легких, сужению бронхов и, как следствие, к возрастанию сопротивления дыхательных путей. Уменьшение одышки в таких случаях обусловлено снижением функциональной остаточной емкости легких до нормальных значений, увеличением подвижности диафрагмы и снижением работы вдоха.
5) Диффузионная способность легких при бронхиальной астме, в отличие от таковой при эмфиземе легких, как правило, в норме, поскольку альвеолярно-капиллярная мембрана при бронхиальной астме не поражается. Измерение диффузионной способности легких проводят у больных пожилого возраста для дифференциальной диагностики бронхиальной астмы и эмфиземы легких.
б. Методы исследования функции внешнего дыхания. Нормальные показатели функции внешнего дыхания для лиц разного возраста и пола приведены в приложении VII .
1) ЖЕЛ, ОФВ1 и среднюю объемную скорость середины выдоха (см. рис. 7.3 ) обычно измеряют с помощью водяного или сухого спирографов. С помощью пневмотахографа можно построить кривую поток—объем. Однако пневмотахографы почти не имеют преимуществ перед спирографами. Пиковую объемную скорость можно определить с помощью пневмотахографа (по максимальному углу наклона кривой зависимости объема форсированного выдоха от времени) или измерить с помощью пневмотахометра. Достоверность показателей зависит от точности прибора и выполнения больным указаний врача. Во время тяжелого приступа бронхиальной астмы надежно измерить ЖЕЛ и показатели форсированного выдоха часто бывает невозможно. Чтобы избежать бронхоспазма во время исследования функции внешнего дыхания, можно попросить больного сделать неполный вдох, а затем — форсированный выдох. На основании данных, полученных таким образом, строят так называемые неполные кривые поток—объем.
2) Сопротивление дыхательных путей измеряют с помощью общей плетизмографии. Это исследование показано, если при назначении бронходилататоров ОФВ1 остается прежним или даже снижается. Последнее обусловлено тем, что максимальный вдох и форсированный выдох могут вызвать сужение бронхов. При проведении общей плетизмографии обструкции бронхов удается избежать, поскольку для этого не требуется форсированное дыхание. При бронхиальной астме сопротивление дыхательных путей повышено. После применения бронходилататоров оно обычно снижается не менее чем на 35%.
3) Остаточный объем, общую емкость и функциональную остаточную емкость легких можно измерить по разведению инертного газа, вымыванию из легких азота, а также с помощью общей плетизмографии. Эти исследования проводятся только в специализированных лабораториях.
в. Цели исследования функции внешнего дыхания: 1) выявление обратимой обструкции бронхов для подтверждения диагноза бронхиальной астмы; 2) оценка обструкции бронхов и эффективности бронходилататоров; 3) наблюдение больных тяжелой бронхиальной астмой во время лечения бронходилататорами и кортикостероидами; 4) оценка риска операции. При амбулаторном лечении бронхиальной астмы и для контроля за состоянием больного при оказании неотложной помощи достаточно измерить ОФВ1 и ЖЕЛ или только пиковую объемную скорость. Полное исследование функции внешнего дыхания, иногда с оценкой диффузионной способности легких, проводят только с диагностической целью и после оказания неотложной помощи при приступе бронхиальной астмы. Для диагностики бронхиальной астмы в межприступный период проводят провокационную пробу с метахолином (см. гл. 7, п. II.В.10.а ).
9. Исследование газов артериальной крови. Нарушение равновесия между вентиляцией и перфузией легких приводит к снижению paO2, которое может наблюдаться даже в межприступный период. Формула для расчета paO2 и кривые диссоциации гемоглобина приведены в приложении VIII, п. А . Однако даже при нормальном paO2 p(A-a)O2 может быть повышено (более 20 мм рт. ст.).
а. Для определения p(A-a)O2 сначала рассчитывают парциальное давление кислорода в альвеолах (pAO2) по следующей формуле: pAO2 = pIO2 – paCO2/R, где pIO2 = 150 мм рт. ст. (pO2 во вдыхаемом воздухе на уровне моря), R = 0,8. Из формулы видно, что при снижении paCO2 p(A-a)O2 может повышаться несмотря на нормальное paO2.
б. paO2 во время приступа бронхиальной астмы снижается пропорционально степени обструкции бронхов (см. рис. 7.6 ). paCO2 вначале тоже снижается, а затем повышается. Так, при легких приступах обычно наблюдается гипервентиляция, которая приводит к уменьшению paCO2 (см. рис. 7.6 ). При тяжелых приступах чаще развивается гиповентиляция, показателем которой служит увеличение paCO2 более 42 мм рт. ст. Нормальный или повышенный уровень paCO2 во время приступа бронхиальной астмы свидетельствует о выраженной обструкции бронхов и необходимости немедленного лечения под постоянным контролем газов артериальной крови.
в. При легких и среднетяжелых приступах бронхиальной астмы pH обычно в норме, реже наблюдается респираторный алкалоз. Он может быть компенсированным (за счет выведения бикарбоната почками) и декомпенсированным. Тяжелые приступы бронхиальной астмы, при которых ОФВ1 составляет менее 15—20% нормального, сопровождаются снижением pH. Это обусловлено накоплением лактата и метаболическим ацидозом (BE метахолина вызывает бронхоспазм у большинства больных бронхиальной астмой, лиц с бронхиальной астмой в анамнезе, а также у больных с аллергическими заболеваниями верхних дыхательных путей. Бронхоспазм при ингаляции метахолина наблюдается менее чем у 10% здоровых. Он может быть обусловлен недавно перенесенной инфекцией верхних дыхательных путей (в течение последних 6 нед), недавней вакцинацией против гриппа, контактом с аллергенами и веществами, загрязняющими воздух. Ложноотрицательные реакции на метахолин отмечаются при проведении провокационной пробы на фоне лечения бронходилататорами.
1) ОФВ1 определяют перед проведением пробы и через 2—3 мин после ингаляции физиологического раствора и разных доз метахолина . Снижение ОФВ1 после ингаляции физиологического раствора не должно превышать 10%.
2) Пробу с метахолином считают положительной, если ОФВ1 снижается более чем на 20% по сравнению с контролем (ингаляция физиологического раствора). Ингаляцию метахолина — 1—5 глубоких вдохов — начинают с концентрации 0,075 мг/мл, удваивая ее каждые 5 мин до появления положительной реакции. В отсутствие реакции на максимальную концентрацию метахолина — 25 мг/мл — пробу считают отрицательной. При бронхиальной астме бронхоспазм обычно возникает при ингаляции метахолина в концентрации 8—16 мг/мл.
3) Нередко для проведения провокационной пробы вместо метахолина используют гистамин. Проба проводится так же, как с метахолином . Начальная концентрация гистамина — 0,03 мг/мл, максимальная — 10 мг/мл.
4) Другие провокационные пробы включают физическую нагрузку, ингаляцию сухого холодного воздуха, ингаляцию гипотонического раствора хлорида натрия .
б. Если на основании данных анамнеза не удается выявить связь между приступами бронхиальной астмы и действием аллергенов, выявляемых с помощью кожных проб и при определении специфических IgE, проводят провокационные пробы с этими аллергенами. Следует отметить, что эти пробы технически сложны, требуют времени и могут спровоцировать как немедленный, так и отсроченный приступ бронхиальной астмы. Провокационные пробы с метахолином , гистамином и аллергенами должны проводиться только врачом и только в межприступный период, когда ОФВ1 составляет не менее 75% от нормального значения.
1) Провокационные пробы с аллергенами проводятся так же, как проба с метахолином .
2) Провокационную пробу начинают с 5 вдохов аллергена в разведении 1:1 000 000, затем концентрацию последовательно повышают: 1:500 000, 1:100 000, 1:50 000, 1:10 000, 1:5000, 1:1000, 1:500 и 1:100. Интервал между ингаляциями аллергена должен составлять не менее 10 мин. Пробу считают положительной, если ингаляция вызывает снижение ОФВ1 не менее чем на 20% (по отношению к исходному уровню), которое сохраняется в течение 10—20 мин. Если при ингаляции аллергена в разведении 1:100 реакция отсутствует, пробу считают отрицательной.
3) За одно исследование можно провести пробу только с одним аллергеном. Если позволяет состояние больного, за сутки до исследования отменяют бронходилататоры, кромолин и H1-блокаторы. Недокромил и астемизол следует отменять еще раньше. Наиболее выраженное угнетение реакции при проведении провокационных проб вызывают бета-адреностимуляторы. Кортикостероиды могут угнетать отсроченную реакцию на аллерген.
4) Если немедленная реакция на аллерген отсутствует, больного предупреждают о том, что через 4—12 ч после провокационной пробы может возникнуть отсроченный приступ бронхиальной астмы. При выраженной немедленной реакции за больным наблюдают не менее 12 ч.
А. Инфекции дыхательных путей — частое осложнение бронхиальной астмы. Они могут возникнуть как во время обострения, так и во время ремиссии заболевания и нередко провоцируют приступы бронхиальной астмы. Сухие хрипы, слышные на расстоянии, во время острого респираторного заболевания могут быть первым проявлением бронхиальной астмы у детей. Бронхиальную астму следует исключать у всех детей с частыми бронхитами и острыми респираторными заболеваниями.
1. Острые респираторные заболевания чаще всего вызывают приступы бронхиальной астмы. Наиболее распространены инфекции, вызванные респираторным синцитиальным вирусом, вирусами парагриппа и гриппа, рино- и аденовирусами. Предполагается, что эти вирусы непосредственно действуют на бронхи, повышая их реактивность. Возможно, возникновение приступов бронхиальной астмы во время острых респираторных заболеваний обусловлено IgE, специфичными к данному вирусу, или вызванными вирусом снижением чувствительности бета-адренорецепторов и высвобождением медиаторов воспаления.
2. Бактериальные инфекции редко провоцируют приступы бронхиальной астмы. Исключение составляют хронические синуситы и микоплазменная инфекция.
3. Пневмония обычно развивается вторично, после длительных или частых приступов бронхиальной астмы, когда в бронхах скапливается большое количество слизи. В возрасте до 5 лет чаще возникают вирусные, 5—30 лет — микоплазменные, после 30 лет — пневмококковые и другие бактериальные пневмонии.
Б. Ателектазы — долевые, сегментарные и субсегментарные — могут возникнуть во время как обострения, так и ремиссии. Обычно их появление связано с закупоркой бронхов слизистыми пробками. Для ателектаза характерны усиление кашля, постоянные хрипы, одышка, лихорадка, ослабленное везикулярное дыхание и притупление перкуторного звука в зоне ателектаза. Чаще всего наблюдаются ателектазы средней доли правого легкого. Нередко они не диагностируются. При подозрении на ателектаз показана рентгенография грудной клетки. Ателектазы характерны для детей младшего возраста, часто рецидивируют, при этом обычно поражаются одни и те же участки легкого.
В. Пневмоторакс и пневмомедиастинум
1. Пневмоторакс — редкое осложнение бронхиальной астмы. При рецидиве пневмоторакса исключают кисту, врожденную долевую эмфизему и другие заболевания легких. Пневмоторакс может возникнуть при сильном кашле и во время ИВЛ. Это осложнение следует заподозрить при внезапном появлении боли в боку, усиливающейся при дыхании и сопровождающейся одышкой, тахипноэ, иногда — кашлем. Диагноз подтверждается при рентгенографии грудной клетки. При небольшом пневмотораксе (менее 25% объема плевральной полости) в отсутствие сильной одышки и боли показан постельный режим и наблюдение. Воздух в плевральной полости рассасывается самостоятельно. В остальных случаях требуется дренирование плевральной полости.
2. Пневмомедиастинум и подкожная эмфизема наблюдаются чаще, чем пневмоторакс. Больные, как правило, не предъявляют жалоб, поэтому эти осложнения обнаруживаются случайно при рентгенографии грудной клетки, осмотре и пальпации шеи и груди. Иногда пневмомедиастинум проявляется болью за грудиной, реже — одышкой, тахипноэ, тахикардией, артериальной гипотонией и цианозом верхней половины тела. Характерный признак пневмомедиастинума — симптом Хаммана (крепитирующий шум при аускультации сердца). Пневмомедиастинум и подкожная эмфизема обычно возникают во время сильного кашля и ИВЛ. Лечение в большинстве случаев не требуется, в тяжелых случаях дренируют средостение.
Г. Бронхоэктазы — редкое осложнение бронхиальной астмы. Обычно они возникают при сочетании бронхиальной астмы с хроническим бронхитом, длительным ателектазом или аллергическим бронхолегочным аспергиллезом. При бронхоэктазах наблюдаются продолжительный кашель, гнойная мокрота, кровохарканье, симптом барабанных палочек. Следует отметить, что при неосложненной бронхиальной астме последний признак отсутствует. Иногда диагноз можно поставить на основании рентгенографии грудной клетки, однако в большинстве случаев требуется рентгеновская томография или КТ. В редких случаях проводят бронхографию.
Д. Аллергический бронхолегочный аспергиллез. Возбудитель — Aspergillus fumigatus. В патогенезе заболевания играют роль аллергические реакции, вызванные возбудителем. Наблюдается в основном у взрослых больных бронхиальной астмой (см. гл. 8, п. II ).
Е. Сердечно-сосудистые осложнения при бронхиальной астме чаще всего проявляются аритмиями — от редких желудочковых экстрасистол до фибрилляции желудочков. Аритмии чаще наблюдаются у больных сердечно-сосудистыми заболеваниями. Тяжесть аритмий возрастает при гипоксемии и злоупотреблении бета-адреностимуляторами. Во время приступа бронхиальной астмы может возникнуть перегрузка правых отделов сердца. Правожелудочковая недостаточность развивается очень редко — только в случае длительной тяжелой гипоксемии и перегрузки объемом. Во время приступа бронхиальной астмы нередко наблюдается легочная гипертензия, однако легочное сердце возникает только при сочетании бронхиальной астмы с ХОЗЛ. Для уменьшения гипоксемии назначают ингаляции кислорода. Ограничивают применение бета-адреностимуляторов (как ингаляционных, так и системных) и теофиллина . При тяжелых аритмиях и правожелудочковой недостаточности назначают сердечные гликозиды (если аритмия не вызвана этими препаратами) и другие антиаритмические средства. При этом обязательно учитывают, не вызывают ли они бронхоспазм.
Ж. Астматический статус и дыхательная недостаточность (см. гл. 7, п. VII ).
IV. Дифференциальная диагностика. Приступ бронхиальной астмы дифференцируют с другими состояниями, для которых характерно острое нарушение дыхания (см. табл. 7.1 ). При обследовании больного в межприступный период исключают хронические заболевания легких.
А. Дифференциальная диагностика приступа бронхиальной астмы
1. Инфекционные заболевания дыхательных путей. Внезапная одышка и хрипы, слышные на расстоянии, могут наблюдаться при острых бронхиолите, бронхите, ларинготрахеобронхите, эпиглоттите, ангине, тонзиллярном абсцессе. Острый бронхиолит обычно наблюдается у детей грудного возраста, инфекция верхних дыхательных путей более характерна для детей 1—12 лет. Важную роль в дифференциальной диагностике этих заболеваний и приступа бронхиальной астмы играет течение заболевания (периодическое возникновение приступов) и эффективность бронходилататоров.
2. Острая левожелудочковая недостаточность. Заболевания сердца в анамнезе, звучные влажные хрипы, а также появление III тона при аускультации сердца позволяют отличить острую левожелудочковую недостаточность от приступа бронхиальной астмы.
3. Инородное тело в главном, долевом или сегментарном бронхе может быть причиной одышки и свистящего дыхания. В отличие от приступа бронхиальной астмы, сухие хрипы при этом односторонние, а в анамнезе обычно есть указания на аспирацию инородного тела. При рентгенографии грудной клетки можно обнаружить инородное тело, сегментарный или долевой ателектаз или эмфизему на стороне поражения легкого. Для подтверждения диагноза и лечения проводят бронхоскопию.
4. Обструкция верхних дыхательных путей, в отличие от приступа бронхиальной астмы, обычно сопровождается инспираторной одышкой. Самые частые причины обструкции верхних дыхательных путей — гипертрофия небных миндалин, аденоиды, инородное тело, острый эпиглоттит, острый ларингит, паралич мышц гортани, ларингоспазм при истерии.
5. Гипервентиляционный синдром. Приступы учащенного, глубокого дыхания, сопровождающиеся страхом, чувством онемения и покалывания в конечностях, могут быть обусловлены тревожными расстройствами. Диагноз ставят на основании данных анамнеза и физикального исследования. Эффективно дыхание в бумажный пакет. Во время приступа бронхиальной астмы и при ХОЗЛ дыхание в бумажный пакет противопоказано, поскольку усиливает гипоксемию.
7. ТЭЛА обычно проявляется тахипноэ и одышкой. Иногда наблюдаются кашель, кровохарканье и боль в боку. ТЭЛА обычно развивается у больных с сердечной недостаточностью, ожирением, злокачественными новообразованиями, тромбофлебитом, а также при длительном постельном режиме и приеме пероральных контрацептивов. При ТЭЛА paO2, как правило, не превышает 60 мм рт. ст., p(A-a)O2 почти всегда увеличена. Диагноз подтверждают с помощью вентиляционно-перфузионной сцинтиграфии легких и ангиопульмонографии.
Б. Дифференциальная диагностика бронхиальной астмы в межприступный период
1. ХОЗЛ. Хронический бронхит и эмфизема легких обычно наблюдаются у курильщиков, начинаются в среднем возрасте, характеризуются постоянным кашлем и одышкой при физической нагрузке. Бронходилататоры при этих заболеваниях, как правило, неэффективны. Следует учитывать, что хронический бронхит и эмфизема легких могут быть осложнениями бронхиальной астмы. В этих случаях требуются исследование функции внешнего дыхания и рентгенография грудной клетки.
2. Аллергический бронхолегочный аспергиллез и экзогенный аллергический альвеолит (см. гл. 8, пп. I—II ).
3. Хроническая обструкция верхних дыхательных путей, вызванная инородным телом, гипертрофированными небными миндалинами, аденоидами, реже диафрагмой гортани, трахеомаляцией, опухолью или сосудистым кольцом трахеи, проявляется периодической или постоянной одышкой и стридором.
4. Карциноидный синдром. В анамнезе возможны приступы одышки, подобные приступам бронхиальной астмы. Диагноз ставят на основании анамнеза (периодические приливы и понос) и лабораторных исследований (повышение концентрации 5-гидроксииндолуксусной кислоты в моче).
5. Муковисцидоз встречается у детей. Характерны длительный кашель, свистящее дыхание, частые пневмонии, синдром нарушенного всасывания, хроническая диарея, зловонный стул, задержка развития. Диагноз подтверждается, если концентрация хлора в поте превышает 60 мэкв/л.
6. Дефицит альфа1-антитрипсина — аутосомно-рецессивное заболевание, для которого характерна прогрессирующая эмфизема легких. Начинается обычно в молодом возрасте. Заболевание развивается как у гомозигот, так и у гетерозигот. Диагноз ставят на основании определения активности и фенотипа альфа1-антитрипсина.
7. Заболевания, проявляющиеся длительным кашлем, — желудочно-пищеводный рефлюкс, стекание секрета по задней стенке глотки при хронических синуситах и круглогодичном аллергическом рините, применение ингибиторов АПФ. Следует учитывать, что длительный кашель может быть единственным проявлением бронхиальной астмы, нарушения функции внешнего дыхания при этом могут отсутствовать.
А. Немедикаментозное лечение дополняет медикаментозное при лечении приступов бронхиальной астмы и применяется для их профилактики.
1. Обучение больного. Больному рассказывают о его заболевании, объясняют необходимость тщательно выполнять все предписания врача, обучают правильно вести себя во время приступов. Обучающую литературу предоставляют Американское пульмонологическое общество, Национальный институт аллергии и инфекционных болезней, Национальный институт сердца, легких и крови, Американский фонд бронхиальной астмы и аллергии, Общество матерей больных бронхиальной астмой и другие общественные и государственные организации. С участием больного и членов его семьи разрабатывают примерный план лечения (см. табл. 7.2 ).
2. Устранение факторов, вызывающих приступы бронхиальной астмы, — наиболее важное профилактическое мероприятие. Выясняют привычки и увлечения больного, особенности его питания, климатические, производственные и бытовые условия. Уточняют, какие инфекции он перенес, с какими аллергенами контактирует и какие лекарственные средства принимает (см. гл. 2, п. II.А ). Решение о перемене места жительства или смене профессии принимается лишь в том случае, когда избежать контакта с вредными факторами не удается. Меры по борьбе с неблагоприятными факторами окружающей среды перечислены в табл. 4.1 .
3. Десенсибилизация эффективна при экзогенной бронхиальной астме (см. гл. 4, п. XIV—XXIII ). Аллергены выявляют с помощью кожных и провокационных проб, а также определения специфических IgE. Десенсибилизация не исключает необходимости устранения контакта с аллергеном.
4. Методы релаксации. Умение расслабиться и успокоиться, особенно в начале или разгаре приступа бронхиальной астмы, помогает снизить его тяжесть и предотвратить дальнейшее развитие. Поскольку паника, возникающая во время приступа, приводит к повышению частоты дыхания и усугубляет бронхоспазм, больных учат управлять своим дыханием. Методам релаксации обучают в межприступный период.
а. Для облегчения дыхания во время приступа рекомендуется: 1) принять удобную позу и расслабиться, 2) дышать медленно и глубоко, 3) положить руку на верхнюю часть живота для контроля за движением диафрагмы во время дыхания, 4) вдыхать через нос (при этом должен приподниматься живот), а выдыхать медленно, через сжатые губы (как при задувании свечи), расслабляя мышцы живота.
б. Ниже приведено описание поз, которые помогают расслабиться и поддерживать брюшное дыхание. Больной должен сам выбрать наиболее удобную для него.
а) Наклониться вперед, держа локти на коленях.
б) Наклониться над столом и положить плечи, предплечья и голову на подушку, лежащую на столе. При длительном затруднении дыхания больной может спать в таком положении.
а) Встать лицом к стене на расстоянии 30—45 см от нее, опереться о стену предплечьями. Положить голову на предплечья и поставить одну ногу вперед. Эта поза способствует расслаблению мышц живота.
б) Прислониться спиной к стене, поставив стопы на расстоянии 30 см от нее.
в. Для уменьшения тревожности и облегчения дыхания также рекомендуют медитацию, аутотренинг, методы биологической обратной связи. Выясняют, какие факторы вызывают приступ, и объясняют больному, как можно избегать их. При эмоциональных расстройствах рекомендуется консультация психиатра или психолога.
5. Обильное питье предупреждает дегидратацию, снижает вязкость слизи и улучшает отхождение мокроты. Больным рекомендуют обильное питье не только во время приступа, но и в межприступный период. Тяжелые приступы бронхиальной астмы и астматический статус сопровождаются дегидратацией, поскольку снижается потребление жидкости и возрастают ее потери, обусловленные гипервентиляцией, потоотделением и рвотой. В связи с этим неотъемлемым компонентом лечения этих состояний служит инфузионная терапия. Объем и скорость введения жидкости зависят от степени дегидратации. Следует помнить о возможности развития отека легких во время инфузионной терапии.
6. Постуральный дренаж, перкуссионный и вибрационный массаж облегчают отхождение мокроты во время приступов бронхиальной астмы, осложненной ателектазами и пневмонией. Эти процедуры также показаны при длительном течении бронхиальной астмы, когда выделяется большое количество очень густой мокроты. Постуральный дренаж и массаж обычно хорошо переносятся, улучшение наступает через 30 мин. Усиление одышки отмечается только при тяжелых приступах бронхиальной астмы, в этом случае процедуру прекращают. Постуральный дренаж лучше всего проводить утром после сна, при необходимости его можно повторять 2—3 раза в сутки. Перед процедурой назначают ингаляцию бронходилататора.
а. Больного укладывают в таком положении, которое обеспечивает отток слизи под действием силы тяжести. В течение 1—2 мин сложенными чашей руками поколачивают по грудной клетке над дренируемым участком легкого. Больного просят дышать медленно и глубоко. Положение тела выбирают индивидуально, выявляя участки скопления слизи при физикальном исследовании и рентгенографии грудной клетки. На рис. 7.7 показано, в каком положении должен находиться больной и в каких участках грудной клетки следует проводить перкуссионный массаж для дренирования разных участков легких.
б. Противопоказания — кровохарканье, пневмоторакс, эпилепсия.
7. Ингаляции кислорода показаны при выраженной гипоксемии.
а. Кислород должен быть хорошо увлажнен. Его подают через носовые канюли, лицевую маску или маску Вентури. Дети младшего возраста плохо переносят маску и канюли, поэтому ингаляции кислорода им обычно проводят в кислородной палатке.
б. Кислород подают с низкой скоростью, обычно 2—4 л/мин, поддерживая paO2 в пределах 70—100 мм рт. ст. При гиперкапнии ингаляция кислорода может усилить гиповентиляцию. Это осложнение обычно наблюдается у больных ХОЗЛ.
а. Адреностимуляторы (см. гл. 4, п. VII ). Стимуляция альфа-адренорецепторов вызывает сужение сосудов, сокращение матки, расслабление гладких мышц кишечника, сокращение мочеточников, сфинктеров кишечника и капсулы селезенки, расширение зрачков. Стимуляция бета1-адренорецепторов вызывает увеличение ЧСС и силы сердечных сокращений, расширение коронарных артерий, расслабление гладких мышц кишечника, активацию липолиза. Стимуляция бета2-адренорецепторов приводит к расслаблению гладких мышц бронхов и матки, тремору, активации гликогенолиза в печени и гликолиза в мышцах.
1) При бронхиальной астме эффективны селективные бета2-адреностимуляторы. Эти препараты выпускаются в форме растворов для инъекций и ингаляций, а также в форме таблеток для приема внутрь. Бета2-адреностимуляторы применяются как при приступах бронхиальной астмы, так и в межприступный период. При сердечно-сосудистых заболеваниях, особенно при аритмиях, бета-адреностимуляторы назначают с осторожностью. При длительном применении бета-адреностимуляторов их эффективность может снижаться, что, видимо, связано с уменьшением количества бета-адренорецепторов. Скорость снижения чувствительности гладких мышц бронхов к адреностимуляторам не установлена.
2) Бета-адреностимуляторы обычно применяют в виде дозированных аэрозолей: во время приступа — по 2 вдоха каждые 3—4 ч, в межприступный период — 3—4 раза в сутки. Ингаляторы можно снабдить приспособлениями, облегчающими их использование, например буферной насадкой или насадкой с клапаном. Во время приступов ингаляции можно делать чаще, однако для этого необходима консультация врача.
3) Если при приступе бронхиальной астмы неэффективны бета-адреностимуляторы в виде таблеток или дозированных аэрозолей, проводят ингаляцию с помощью распылителя ингаляционных растворов. Иногда вместо этого применяют ИВЛ с пассивным выдохом. Максимальное давление на вдохе при этом не должно превышать 15—20 мм рт. ст. Этот способ лечения не имеет преимуществ перед ингаляционным применением бета-адреностимуляторов, среди его недостатков следует отметить высокую стоимость и риск пневмоторакса. Ингаляцию бета-адреностимуляторов с помощью распылителя применяют вместо п/к введения адреналина или тербуталина или в сочетании с одним из этих препаратов на начальном этапе лечения приступа бронхиальной астмы. Кроме того, применение распылителя ингаляционных растворов эффективно при длительных приступах, а также в межприступный период — в комбинации с постуральным дренажем, перкуссионным и вибрационным массажем. Ниже приведены рекомендуемые дозы бета-адреностимуляторов, применяемых в виде ингаляций с помощью распылителя (все препараты разводятся в 2—3 мл физиологического раствора): сальбутамол — 2,5 мг (0,5 мл 0,5% раствора), орципреналин — 15 мг (0,3 мл 5% раствора), битолтерол — 2,5 мг (1,25 мл 0,2% раствора), изоэтарин — 5 мг (0,5 мл 1% раствора). Дозы для детей приведены в табл. 4.5 . Сальбутамол и орципреналин выпускаются во флаконах, содержащих 1 дозу препарата в физиологическом растворе. Ингаляции обычно продолжаются 5—10 мин, больному объясняют, что он должен медленно и глубоко дышать и слегка задерживать дыхание после каждого вдоха. Оборудование для ингаляций должно быть чистым и исправным.
4) Часто пользоваться распылителями не рекомендуется, их применяют только в тех случаях, когда дозированные аэрозоли неэффективны или больной не может пользоваться ингалятором-дозатором. ИВЛ с пассивным выдохом противопоказана при пневмотораксе. Если в анамнезе есть указания на пневмоторакс, ИВЛ следует проводить с осторожностью.
5) Бета-адреностимуляторы, применяемые при бронхиальной астме
а) Адреналин обладает альфа- и бета-адренергической активностью. Его применяют для оказания неотложной помощи при приступах бронхиальной астмы, особенно если неэффективны препараты для приема внутрь. Назначают 0,2—0,5 мл (детям — 0,01 мл/кг) раствора адреналина 1:1000 п/к. Эффект обычно наступает в течение 15 мин. При необходимости адреналин вводят повторно каждые 20 мин. Отсутствие эффекта после третьей инъекции адреналина свидетельствует о высоком риске астматического статуса. Побочные действия — тахикардия, тошнота, рвота, головная боль, артериальная гипертония, боль за грудиной, раздражительность, тремор, головокружение. У пожилых, особенно страдающих сердечно-сосудистыми заболеваниями, адреналин применяют с осторожностью.
При введении адреналина в виде водной суспензии 1:200 его действие проявляется немедленно и сохраняется в течение 6—8 ч. Суспензию вводят в дозе 0,1—0,3 мл (детям — 0,005 мл/кг) п/к. При приступе бронхиальной астмы для оценки обратимости бронхоспазма рекомендуется сначала вводить раствор адреналина 1:1000, а через 20—30 мин — суспензию адреналина . Суспензию можно вводить в той же дозе каждые 8 ч. Побочные действия те же, что при применении раствора адреналина .
б) Эфедрин — природное соединение, по действию сходно с адреналином. Применяется внутрь в виде растворов или таблеток, часто в комбинации с метилксантинами. Эфедрин обладает менее выраженным бронходилатирующим действием, чем адреналин , однако эффективен при приеме внутрь. Препарат назначают в дозе 25—50 мг каждые 4—6 ч (детям — 3 мг/кг/сут в 4—6 приемов). По побочным действиям эфедрин сходен с адреналином , к наиболее серьезным относятся раздражительность, нарушения сна и тахикардия, особенно у детей. Из-за этого вместо эфедрина в настоящее время назначают селективные бета2-адреностимуляторы.
в) Этилнорэпинефрин — эффективный бронходилататор. По побочным действиям сходен с адреналином . Это препарат короткого действия, выпускается в виде раствора для инъекций. Этилнорэпинефрин назначают в дозе 0,6—2,0 мг (детям — 0,04 мг/кг) п/к или в/м. Инъекции можно повторять каждые 20 мин.
г) Изопреналин — бета1— и бета2-адреностимулятор, эффективный бронходилататор. К основным побочным эффектам относятся усиление ЧСС и силы сердечных сокращений, аритмии, сосудорасширяющее действие. Изопреналин малоэффективен при приеме внутрь. Его применяют в виде раствора 1:100 или 1:200 для ингаляций с помощью распылителя или ингалятора-дозатора. Ингаляция изопреналина вызывает быстрое — в течение нескольких секунд или минут — расширение бронхов, эффект сохраняется 1—2 ч. Слишком частое применение препарата при тяжелых приступах бронхиальной астмы может приводить к снижению его эффективности и увеличению риска побочных действий. При тяжелых приступах, сопровождающихся гипоксемией, изопреналин применяют с осторожностью, поскольку он, расширяя сосуды легких, еще больше нарушает соотношение между перфузией и вентиляцией. Больным объясняют, что злоупотребление ингаляционными адреностимуляторами недопустимо. На сегодняшний день при бронхиальной астме вместо изопреналина все чаще применяют препараты с более длительным действием на бета2-адренорецепторы.
д) Изоэтарин — производное изопреналина , действует преимущественно на бета2-адренорецепторы и поэтому обладает менее выраженными побочными действиями. Длительность действия изоэтарина незначительно превышает длительность действия изопреналина и составляет 2—3 ч. Изоэтарин обычно применяют в виде ингаляций с помощью распылителя или ингалятора-дозатора. При применении в виде дозированного аэрозоля препарат назначают по 1—2 вдоха (0,34—0,68 мг) каждые 4 ч.
е) Орципреналин по строению близок к изопреналину , однако метаболизируется более медленно и поэтому обладает более длительным действием (до 5 ч). Орципреналин выпускается в виде таблеток по 10 и 20 мг (назначают по 10—20 мг каждые 4—6 ч), дозированного аэрозоля, 0,65 мг/вдох (назначают по 1—3 вдоха каждые 4—6 ч), 5% раствора для ингаляций (0,2—0,3 мл разводят в 2,5 мл воды или физиологического раствора, ингаляции повторяют каждые 4—6 ч). Дозы для детей приведены в табл. 4.5 . Хотя орципреналин менее активен, чем изопреналин , он обладает более длительным действием и его можно принимать внутрь. Наиболее частые побочные действия — раздражительность, тремор и тахикардия.
ж) Тербуталин сходен с орципреналином , однако в отличие от него, является селективным бета2-адреностимулятором и обладает более длительным действием. Тербуталин назначают внутрь по 2,5—5,0 мг каждые 8 ч, п/к по 0,25 мг или в виде дозированного аэрозоля по 1—2 вдоха (0,4 мг) каждые 4—6 ч. Выраженность и длительность бронходилатирующего действия при п/к введении тербуталина такие же, как при п/к введении адреналина . Однако тербуталин не имеет преимуществ перед адреналином для лечения приступов бронхиальной астмы, поскольку обладает такими же побочными действиями. При приеме тербуталина внутрь эффект наступает через 15—30 мин и длится 6—8 ч. Тербуталин не рекомендуется назначать детям младше 12 лет. Побочные действия — тахикардия и раздражительность. Примерно у 50% больных отмечается тремор. При регулярном применении препарата это побочное действие обычно исчезает.
з) Сальбутамол является селективным бета2-адреностимулятором, длительность действия такая же, как у тербуталина . Для приема внутрь выпускают препарат короткого действия в виде таблеток по 2 и 4 мг (назначают по 2—4 мг каждые 6—8 ч), таблеток длительного действия по 4 и 8 мг (назначают по 4—8 мг каждые 12 ч, максимальная доза 32 мг/сут) и сироп, содержащий 2 мг препарата в 5 мл. Сироп сальбутамола назначают взрослым и детям старше 14 лет по 5—10 мл 3—4 раза в сутки, детям 6—14 лет — 5 мл 3—4 раза в сутки, детям 2—6 лет — по 0,25 мл/кг 3 раза в сутки, разовая доза не должна превышать 5 мл. Для профилактики ночных приступов бронхиальной астмы назначают таблетки длительного действия. Сальбутамол также можно применять в виде дозированного аэрозоля — по 2 вдоха (180 мкг) каждые 4—6 ч — и порошка — по 200 мкг (1 капсула) каждые 4—6 ч с помощью распылителя порошков для ингаляций. Используется также 0,5% раствор для ингаляций — по 5 мл (2,5 мг) каждые 4—6 ч. Дозы для детей приведены в табл. 4.5 . Побочные действия такие же, как у тербуталина , наиболее выраженное из них — тремор.
и) Битолтерол — селективный бета2-адреностимулятор, обладает длительным действием. Применяют в виде дозированного аэрозоля по 1—3 вдоха (0,37—1,11 мг) каждые 8 ч и в виде раствора для ингаляций (см. гл. 7, п. V.Б.1.а.3 ).
к) Пирбутерол — селективный бета2-адреностимулятор, по структуре и действию сходный с сальбутамолом . Взрослым и детям старше 12 лет его назначают в виде дозированного аэрозоля — по 2 вдоха (400 мкг) каждые 4—6 ч. Выпускаются также ингаляторы-дозаторы, подающие пирбутерол только на вдохе. Эти ингаляторы рекомендуют больным, которые не могут пользоваться обычными ингаляторами-дозаторами.
л) Сальметерол более выраженно и избирательно действует на бета2-адренорецепторы, чем другие бета2-адреностимуляторы. Действие проявляется через 15 мин и становится максимальным не ранее чем через 3 ч после применения, что делает сальметерол непригодным для лечения приступов бронхиальной астмы. Однако большая продолжительность действия (около 12 ч) позволяет применять этот препарат для профилактики приступов бронхиальной астмы физического усилия и ночных приступов бронхиальной астмы. К преимуществам сальметерола относится и то, что его применяют 2 раза в сутки. Сальметерол выпускается в виде дозированного аэрозоля (21 мкг/вдох). Обычно его назначают по 2 вдоха каждые 12 ч. Сальметерол применяют у детей старше 12 лет и взрослых. Его не используют, если эффективны ингаляционные бета2-адреностимуляторы короткого действия. При бронхиальной астме физического усилия сальметерол назначают за 30—60 мин до физической нагрузки. При развитии бронхоспазма на фоне применения сальметерола не следует увеличивать частоту ингаляций. В этом случае дополнительно назначают бета2-адреностимулятор короткого действия.
м) Фенотерол и прокатерол — селективные бета2-адреностимуляторы, сходные по действию с тербуталином , сальбутамолом и битолтеролом . По сравнению с прокатеролом фенотерол обладает менее избирательным действием на бета2-адренорецепторы, поэтому чаще вызывает тахикардию. Увеличение летальности бронхиальной астмы, наблюдавшееся в 70-х гг. в Новой Зеландии, было обусловлено широким применением фенотерола . Прокатерол выпускается в виде таблеток длительного действия. В США фенотерол и прокатерол не производятся.
б. Метилксантины. Расширение бронхов под действием метилксантинов обусловлено, по-видимому, блокадой аденозиновых рецепторов и снижением концентрации кальция в цитоплазме. Метилксантины не связываются с адренорецепторами, поэтому усиливают действие адреностимуляторов.
1) Теофиллин — основной препарат группы метилксантинов, бронходилататор. Эффективность и побочное действие теофиллина зависят от его концентрации в сыворотке. Терапевтическая концентрация в сыворотке, вызывающая минимальные побочные эффекты, составляет 8—15 мкг/мл. При концентрации теофиллина в сыворотке выше 15 мкг/мл риск побочных эффектов значительно возрастает.
а) Побочные действия — тошнота, рвота, понос, головная боль, частое мочеиспускание, раздражительность. Реже отмечаются бессонница, психические расстройства, нарушение внимания.
б) Побочные действия теофиллина обычно наблюдаются при концентрации препарата в сыворотке, превышающей 15—20 мкг/мл (см. табл. 7.3 ). Концентрация теофиллина в сыворотке индивидуальна и зависит от скорости его метаболизма в печени. У детей клиренс теофиллина составляет 0,6—2,2 мл/кг/мин, у взрослых — 0,37—1,57 мл/кг/мин. Он значительно снижается при печеночной и сердечной недостаточности. При употреблении марихуаны и курении клиренс теофиллина повышается. При подборе дозы теофиллина необходимо учитывать факторы, влияющие на его клиренс (см. табл. 4.6 ), эффективность, побочные действия и концентрацию в сыворотке. Для выбора режима применения препаратов теофиллина длительного действия определяют максимальную и минимальную концентрацию теофиллина в сыворотке. При низкой скорости метаболизма теофиллин назначают 1 раз в сутки.
в) При подборе дозы теофиллина часто ориентируются на появление первых признаков передозировки — тошноты и неприятных ощущений в животе. Однако поскольку у некоторых больных первыми признаками передозировки могут быть аритмии, судороги и кома, при подборе дозы теофиллина все же лучше ориентироваться на концентрацию препарата в сыворотке. В большинстве лабораторий ее определяют с помощью спектрофотометрии, высокоэффективной жидкостной хроматографии и твердофазного ИФА. Готовые наборы, в состав которых входят моноклональные антитела к теофиллину , позволяют быстро и точно определить концентрацию теофиллина в сыворотке. Исследование с помощью этих наборов можно проводить в амбулаторных условиях. Концентрацию теофиллина определяют не только в сыворотке, но и в слюне. Концентрация теофиллина в слюне обычно пропорциональна концентрации в сыворотке, однако соотношение между ними индивидуально и меняется в течение суток.
г) Пути введения. Теофиллин назначают внутрь, ректально и в/в. При приеме препарата внутрь в виде водного или водно-спиртового раствора и таблеток, не покрытых оболочкой, он быстро и полностью всасывается в кишечнике. Максимальная концентрация в сыворотке достигается через 30—60 мин. Высокодисперсный теофиллин всасывается еще быстрее. При приеме таблеток или капсул длительного действия максимальная концентрация в сыворотке обычно достигается через 4—6 ч, поэтому эти формы лучше назначать при продолжительном лечении теофиллином . Теофиллин в виде ректальных свечей всасывается медленно и неполно, количество всосавшегося препарата непостоянно. Всасывание теофиллина в виде раствора для ректального введения более предсказуемо. Вводить теофиллин ректально, особенно в свечах, не рекомендуется, исключение составляют случаи непереносимости препарата при приеме внутрь. Теофиллин выпускается также в виде раствора для в/в введения (в 5% растворе глюкозы).
В большинстве случаев начальная доза теофиллина для взрослых составляет: при назначении таблеток короткого действия — 150—200 мг каждые 6 ч, таблеток длительного действия — 100—200 мг каждые 12 ч. При выборе начальной дозы следует учитывать факторы, влияющие на клиренс теофиллина (см. табл. 4.6 ). Поддерживающая доза для взрослых обычно составляет: при назначении таблеток короткого действия — 100—400 мг каждые 6 ч, таблеток длительного действия — 200—500 мг каждые 12 ч. Препараты с продолжительностью действия 24 ч назначают по 200—1000 мг 1 раз в сутки. При высоком клиренсе суточную дозу делят на 2 части, препарат принимают каждые 12 ч. Препараты длительного действия различаются по биодоступности. На всасывание некоторых препаратов теофиллина влияет прием пищи и одновременный прием антацидных средств, поэтому при смене препарата теофиллина определяют его концентрацию в сыворотке. Начальная доза теофиллина для детей обычно составляет 12—14 мг/кг/сут внутрь (см. гл. 4, п. VIII.Г.1 ). При необходимости ее можно увеличивать до 24 мг/кг/сут и более. Препараты короткого действия назначают каждые 6 ч, препараты длительного действия — каждые 8—12 ч. При высоком клиренсе теофиллина препараты короткого действия приходится назначать каждые 4 ч, препараты длительного действия — каждые 8—12 ч. Подбор дозы теофиллина иногда занимает несколько недель. В сложных случаях дозу меняют каждые 2—3 сут, концентрацию теофиллина в сыворотке определяют через 2 ч после приема препаратов короткого действия и через 5 ч после приема препаратов длительного действия. До тех пор пока концентрация теофиллина в сыворотке не достигнет постоянного значения (обычно через 3 сут после применения одной и той же дозы препарата), дозу теофиллина не меняют (см. табл. 4.7 ).
Ректально теофиллин назначают взрослым в дозе 250—500 мг каждые 8—12 ч, детям — 7 мг/кг каждые 12 ч. Поскольку всасывание теофиллина при ректальном введении непостоянно, обязательно контролируют его концентрацию в сыворотке. В/в вводят раствор теофиллина в концентрации 1,6 мг/мл (или раствор аминофиллина в концентрации 2 мг/мл). Препарат назначают в дозе 3—5 мг/кг каждые 6 ч или, что предпочтительнее, в виде длительных инфузий. Длительные инфузии проводят по следующей схеме: 1) сначала вводят насыщающую дозу препарата, которая составляет 5 мг/кг для больных, не принимавших теофиллин в последние 12—24 ч, и 2 мг/кг для больных, принимавших теофиллин в последние 12—24 ч; 2) после введения насыщающей дозы больным моложе 50 лет теофиллин вводят со скоростью 0,6—1,0 мг/кг/ч, больным старше 50 лет — со скоростью 0,4—0,6 мг/кг/ч, больным с печеночной и сердечной недостаточностью — со скоростью 0,1—0,4 мг/кг/ч (см. табл. 7.4 ).
2) Аминофиллин — соль теофиллина и этилендиамина — применяется внутрь, ректально и в/в. Препарат содержит 80% теофиллина . В организме аминофиллин превращается в теофиллин . Показания к применению и побочные действия такие же, как у теофиллина . Аминофиллин лучше растворяется в воде, чем теофиллин , хотя новые препараты высокодисперсного теофиллина тоже хорошо растворимы в воде.
а) Для приема внутрь аминофиллин назначают в дозе, на 20% превышающей дозу теофиллина . Аминофиллин выпускается в виде препаратов короткого действия (растворы и таблетки) и препаратов длительного действия (таблетки). Ректально аминофиллин назначают взрослым в дозе 300 мг каждые 8 ч. При ректальном введении аминофиллина следует соблюдать такие же меры предосторожности, как при ректальном введении теофиллина .
б) В/в аминофиллин вводят в дозе 4—6 мг/кг каждые 6 ч или, что предпочтительнее, в виде длительной инфузии (см. табл. 7.4 ). Длительную инфузию проводят по следующей схеме: 1) в течение 20—30 мин вводят насыщающую дозу (в 50—100 мл 5% раствора глюкозы), которая составляет 6 мг/кг для больных, не принимавших теофиллин в последние 12—24 ч, и 3 мг/кг — для больных, принимавших теофиллин в последние 12—24 ч, 2) затем больным моложе 50 лет аминофиллин вводят со скоростью 0,7—1,2 мг/кг/ч, больным старше 50 лет — со скоростью 0,5—0,7 мг/кг/ч, больным с печеночной и сердечной недостаточностью — со скоростью 0,1—0,5 мг/кг/ч. Концентрацию теофиллина в сыворотке определяют через 1—2 ч после введения насыщающей дозы аминофиллина , а затем — каждые 12—24 ч. После изменения поддерживающей дозы аминофиллина концентрацию теофиллина в сыворотке определяют каждые 4—6 ч. После приема внутрь или в/в струйного введения дополнительной дозы аминофиллина концентрацию теофиллина в сыворотке определяют через 1—2 ч.
3) Холина теофиллинат — соль теофиллина и холина, которая в организме превращается в теофиллин , содержание теофиллина в препарате составляет 65%. Холина теофиллинат принимают внутрь в виде препаратов короткого (растворы и таблетки) и длительного (таблетки) действия. Он лучше всасывается и реже вызывает желудочно-кишечные нарушения, чем теофиллин , поэтому холина теофиллинат можно назначать при непереносимости других препаратов теофиллина . Дозы холина теофиллината для приема внутрь на 35—40% выше, чем дозы теофиллина .
4) Дипрофиллин — дигидроксипропилтеофиллин — алкильное производное теофиллина . Эффективный бронходилататор, содержащий 70% теофиллина . Концентрацию дипрофиллина в сыворотке нельзя определить с помощью стандартных методов, применяемых для определения концентрации теофиллина . Препарат реже вызывает побочные действия, чем теофиллин . Назначается внутрь и в/м. Начальная доза для взрослых составляет 15 мг/кг внутрь каждые 6 ч, доза для детей не установлена.
Действие препаратов теофиллина усиливается при одновременном назначении бета-адреностимуляторов. Механизм действия теофиллина и бета-адреностимуляторов различен. Длительное лечение теофиллином , в отличие от длительного лечения бета-адреностимуляторами, не приводит к снижению его эффективности. Иногда одновременное назначение теофиллина и бета-адреностимуляторов оказывается столь же эффективным, как монотерапия этими препаратами в максимальных дозах. При одновременном назначении теофиллина и бета-адреностимуляторов побочные действия наблюдаются реже, поэтому при непереносимости высоких доз этих препаратов рекомендуется назначать их одновременно в более низких дозах. Применение бета-адреностимуляторов в виде ингаляций еще больше снижает риск побочных действий. Ни теофиллин , ни бета-адреностимуляторы не обладают противовоспалительным действием.
в. M-холиноблокаторы снижают тонус и реактивность бронхов. Эти препараты показаны при непереносимости или неэффективности ингаляционных адреностимуляторов, психогенном бронхоспазме и бронхоспазме, вызванном применением бета-адреноблокаторов, а также при повышенной секреции слизи в бронхах. Среди M-холиноблокаторов, применяемых при бронхоспазме, следует отметить атропин и ипратропия бромид — производное атропина, не всасывающееся через слизистую дыхательных путей. Атропин применяют в дозе 1—2 мг в виде раствора с концентрацией 0,4—1,0 мг/мл с помощью распылителя 4—6 раз в сутки (ингаляционный путь введения атропина не одобрен FDA). Ипратропия бромид применяют в виде дозированного аэрозоля по 1—2 вдоха (18—36 мкг) 3—4 раза в сутки. Показано, что применение ипратропия бромида в виде дозированного аэрозоля по 4—6 вдохов 3—4 раза в сутки оказывает более выраженное бронходилатирующее действие в отсутствие побочного. Препарат выпускают также в виде 0,02% раствора для ингаляций во флаконах по 2,5 мл. Ингаляции проводят 3—4 раза в сутки с помощью распылителя. По сравнению с бета-адреностимуляторами нового поколения аэрозольные формы M-холиноблокаторов действуют более медленно (эффект проявляется через несколько минут, пик действия — через 60 мин), но сходны с ними по продолжительности действия — до 4—6 ч. Самый частый побочный эффект — сухость во рту. Иногда отмечается нечеткость зрения, задержка мочи и редко — тахикардия.
2. Кромолин угнетает дегрануляцию тучных клеток и высвобождение ими гистамина, лейкотриенов и других медиаторов воспаления. Показано также, что он тормозит активацию и подавляет секреторную активность нейтрофилов, эозинофилов и моноцитов, а также снижает реактивность бронхов. Кромолин не вызывает расширения бронхов. Поскольку препарат плохо всасывается в ЖКТ, его применяют ингаляционно — в виде высокодисперсного порошка в смеси с лактозой, раствора для ингаляций или дозированного аэрозоля (см. гл. 4, п. X ).
а. Показания к применению. Кромолин применяют только для профилактики приступов бронхиальной астмы. Его назначают при длительном течении бронхиальной астмы, неэффективности бронходилататоров, а также в тех случаях, когда необходимо прекратить или ограничить применение бронходилататоров и кортикостероидов. Кроме того, кромолин предотвращает бронхоспазм при физической нагрузке, вдыхании пыли и паров и бронхоспазм, обусловленный поздней фазой аллергических реакций немедленного типа. Кромолин не применяют при приступах бронхиальной астмы, так как он может усилить бронхоспазм.
б. Дозы. Начальная и поддерживающая дозы — по 2 вдоха дозированного аэрозоля (1600 мкг) 4 раза в сутки. При длительном применении дозу обычно снижают. Кромолин также применяют в виде порошка — по 20 мг (1 капсула) 4 раза в сутки — и раствора для ингаляций — по 20 мг (1 ампула, 2 мл) 4 раза в сутки с помощью распылителя. Ингаляция кромолина может сопровождаться першением в горле. В этом случае рекомендуется после ингаляции полоскать рот и горло водой. Если же ингаляция кромолина вызывает бронхоспазм, за 10—20 мин до нее следует проводить ингаляцию бронходилататоров. Если в первые 4—8 нед лечения кромолином частота и тяжесть приступов бронхиальной астмы не снижаются, а уменьшение доз других препаратов приводит к ухудшению состояния, кромолин отменяют. Для предупреждения бронхоспазма препарат принимают за 10—15 мин, но не ранее чем за 60 мин, до контакта с аллергеном или физической нагрузки.
в. Побочные действия. Обычно отмечаются легкий бронхоспазм, кашель, заложенность носа и першение в горле. К редким побочным действиям относятся отек гортани, крапивница, дерматит, тошнота, кровохарканье, паротит, легочная эозинофилия.
3. Недокромил назначают ингаляционно в виде дозированного аэрозоля. По активности, показаниям к применению и побочным действиям (неприятный вкус, кашель, першение в горле) он сходен с кромолином . Детям младше 12 лет недокромил не назначают. В отличие от кромолина , недокромил угнетает дегрануляцию тучных клеток не только в соединительной ткани, но и в слизистых. Недокромил обладает более выраженным противовоспалительным действием и более эффективен для профилактики приступов бронхиальной астмы, чем кромолин . При легком и среднетяжелом течении бронхиальной астмы недокромил применяют в виде дозированного аэрозоля, по 2 вдоха (3,5 мг) 4 раза в сутки, самостоятельно или в сочетании с ингаляционными кортикостероидами. Если через несколько недель после начала лечения наступает улучшение, дозу постепенно снижают до 2 вдохов 3 раза в сутки. При поддерживающем лечении недокромил назначают по 2 вдоха 2 раза в сутки (см. гл. 4, п. XI ).
4. Кортикостероиды применяют при среднетяжелом течении бронхиальной астмы (ингаляционно), а также при длительном бронхоспазме и астматическом статусе (внутрь и в/в). Кортикостероиды непосредственно не расширяют бронхи. Механизм их действия до конца не изучен, однако предполагается, что они повышают реактивность бета-адренорецепторов, а также ингибируют фосфолипазу A2. Снижение активности фосфолипазы A2 приводит к угнетению продукции метаболитов арахидоновой кислоты — лейкотриенов, тромбоксанов и простагландинов. Дозы, свойства и побочные действия разных кортикостероидов приведены в гл. 4, п. XII .
а. Показания к применению и дозы
1) При приступах бронхиальной астмы кортикостероиды применяются в тех случаях, когда неэффективны бронходилататоры. Кортикостероиды обычно назначают внутрь, например преднизон , 40—60 мг 1 раз в сутки (или в несколько приемов) в течение 3—7 сут. Доза для детей — 1—2 мг/кг/сут. Отменяют препарат постепенно, также в течение 3—7 сут. При тяжелых приступах бронхиальной астмы и астматическом статусе кортикостероиды вводят в/в. Раннее применение кортикостероидов быстро устраняет гипоксемию. Рекомендуемая доза гидрокортизона для взрослых — 200 мг в/в каждые 4—6 ч, для детей — 4—6 мг/кг в/в каждые 4—6 ч; доза метилпреднизолона для взрослых — 40—80 мг в/в каждые 6—8 ч, для детей — 1 мг/кг в/в каждые 6—8 ч. Если в течение 24 ч после начала лечения кортикостероидами улучшение не наступает, дозу увеличивают. Максимальная доза метилпреднизолона для взрослых — 250 мг в/в каждые 6 ч. Лечение высокими дозами кортикостероидов проводят под постоянным контролем основных физиологических показателей, водного и электролитного баланса.
2) Ингаляционные кортикостероиды почти не обладают системным действием, поскольку не всасываются в бронхах. Они применяются самостоятельно или в комбинации с бронходилататорами при длительном течении бронхиальной астмы. При среднетяжелом течении бронхиальной астмы ингаляционные кортикостероиды применяют в низких дозах, например беклометазон , 2—4 вдоха (84—168 мкг) 2 раза в сутки, триамцинолон , 2—4 вдоха (200—400 мкг) 2 раза в сутки, флунизолид , 2 вдоха (500 мкг) 2 раза в сутки. При тяжелой бронхиальной астме кортикостероиды назначают в более высоких дозах: беклометазон и триамцинолон , 4 вдоха 4 раза в сутки, флунизолид , 4 вдоха 2 раза в сутки. Новый кортикостероид для ингаляционного применения — будесонид — назначают взрослым в дозе 200—1600 мкг/сут, детям старше 6 лет — 200—400 мкг/сут. Будесонид оказывает побочные действия реже, чем другие кортикостероиды, однако в США он пока не разрешен к применению для лечения бронхиальной астмы. После каждого применения ингаляционных кортикостероидов во избежание першения в горле и кандидоза рта рекомендуется полоскать рот и горло водой. Риск местных побочных действий ингаляционных кортикостероидов уменьшается при применении буферных насадок (см. гл. 7, п. V.Б.7 ). Ингаляционные кортикостероиды в низких дозах в сочетании с ингаляционными бета2-адреностимуляторами можно применять для поддерживающего лечения бронхиальной астмы легкого течения. Это позволяет уменьшить дозы бета2-адреностимуляторов.
3) При тяжелой бронхиальной астме, которая сопровождается частыми приступами при физической нагрузке и ночью, дозу ингаляционных кортикостероидов повышают до 4—6 вдохов 2—4 раза в сутки. Ингаляционные кортикостероиды снижают потребность в кортикостероидах для системного применения. Однако при тяжелых приступах бронхиальной астмы в большинстве случаев все же приходится использовать кортикостероиды для приема внутрь. Их назначают в высоких дозах коротким курсом каждый день или через день.
б. Побочные действия. Чаще всего ингаляционные кортикостероиды вызывают першение в горле, охриплость и кандидоз рта, которые исчезают после отмены препаратов или при снижении их дозы. При кандидозе назначают суспензию нистатина для полоскания, 400 000—600 000 ед 3—4 раза в сутки. Применение буферных насадок предотвращает оседание кортикостероидов в ротоглотке и существенно уменьшает местные побочные действия (см. гл. 7, п. V.Б.7 ). Беклометазон , триамцинолон и флунизолид плохо всасываются в бронхах, поэтому почти не вызывают угнетения функции надпочечников. При замене кортикостероидов для системного применения на ингаляционные дозу препарата для системного применения снижают постепенно, чтобы не вызвать острую надпочечниковую недостаточность. При улучшении состояния на фоне длительного лечения ингаляционными кортикостероидами их дозу обычно уменьшают.
в. Назначение кортикостероидов для системного применения через день, в отличие от ежедневного, вызывает улучшение при менее выраженном угнетении функции надпочечников. При этом применяют препараты короткого действия в достаточно низких дозах, например преднизон в дозе не более 20 мг/сут внутрь через день. Препараты более длительного действия, например дексаметазон , вызывают угнетение функции надпочечников даже при таком режиме приема. При необходимости ежедневного применения кортикостероиды назначают в минимальных дозах, утром, 1 раз в сутки. После длительного лечения дозу кортикостероидов снижают постепенно, например если применяется преднизон , то на 1—5 мг каждые 1—4 нед. При длительном лечении кортикостероидами больных регулярно обследуют для раннего выявления осложнений (см. гл. 4, пп. XII.Г—Е ).
г. Тролеандомицин , антибиотик из группы макролидов, повышает эффективность кортикостероидов для системного применения, особенно метилпреднизолона (применение тролеандомицина в сочетании с метилпреднизолоном не одобрено FDA). Хотя механизм взаимодействия тролеандомицина с кортикостероидами неизвестен, показано, что через 1 нед после начала его применения снижается скорость выведения и повышается концентрация метилпреднизолона в сыворотке. Назначение низких доз тролеандомицина внутрь при бронхиальной астме позволяет снизить дозу метилпреднизолона . Схема лечения метилпреднизолоном и тролеандомицином приведена в табл. 7.5 .
Тролеандомицин обладает гепатотоксическим действием, поэтому при его назначении возможно повышение активности печеночных ферментов и желтуха. Повышение активности АсАТ и АлАТ может наблюдаться даже при назначении препарата в низких дозах, например 500 мг/сут внутрь. Ежедневное же применение препарата в дозе 1 г внутрь в течение 2 нед приводит к повышению активности печеночных ферментов более чем у 50% больных. При стойком повышении активности АсАТ и АлАТ тролеандомицин отменяют или снижают его дозу. Тролеандомицин замедляет выведение теофиллина , угнетая его деметилирование в печени. Поэтому при назначении тролеандомицина и метилпреднизолона дозу теофиллина снижают на 25—50% и регулярно определяют его уровень в сыворотке. Показания к назначению тролеандомицина и метилпреднизолона ограничены. Обычно комбинацию этих препаратов применяют при тяжелой бронхиальной астме, когда необходимо назначать кортикостероиды в дозе более 15—20 мг/сут внутрь в пересчете на преднизон . Перед назначением препаратов следует сопоставить риск осложнений лечения тролеандомицином и метилпреднизолоном и риск осложнений длительного лечения высокими дозами кортикостероидов. Больному и его родственникам необходимо сообщить о побочных эффектах тролеандомицина и метилпреднизолона и получить письменное согласие на лечение.
При применении тролеандомицина и метилпреднизолона чаще всего отмечаются тошнота и схваткообразная боль в животе. В связи с замедленным выведением метилпреднизолона его побочные эффекты сохраняются длительное время и могут даже усиливаться.
5. Метотрексат — антагонист фолиевой кислоты. Применяется обычно для лечения злокачественных новообразований. В дозе 7,5—15 мг/нед внутрь оказывает противовоспалительное действие. При назначении метотрексата снижается потребность в кортикостероидах для системного применения. Метотрексат назначают при бронхиальной астме, требующей постоянного лечения кортикостероидами в дозах, превышающих 10 мг/сут в пересчете на преднизон , а также при высоком риске тяжелых побочных действий кортикостероидов — остеопороза, катаракты, сахарного диабета. Более чем у 40% больных метотрексат вызывает тошноту, понос, головную боль и сыпь, у 5% больных развивается лекарственный гепатит, который не всегда проявляется клинически, у 3—5% — лекарственный пневмонит, который может привести к пневмосклерозу. В связи с этим метотрексат назначают лишь в крайних случаях: при неудачной попытке снизить дозу кортикостероидов для системного применения и перевести больного на ингаляционные кортикостероиды в максимальной переносимой дозе, например беклометазон по 6—8 вдохов 4 раза в сутки (1200—1600 мкг/сут). Во время лечения метотрексатом больных регулярно обследуют для ранней диагностики токсического действия препарата на печень, костный мозг и легкие. Метотрексат применяют внутрь и в/м. Внутрь препарат назначают 1 раз в сутки через 8 ч после еды или не позднее чем за 1 ч до еды. При сильной тошноте переходят на в/м введение препарата. Общая доза в первую неделю составляет 7,5 мг, при хорошей переносимости ее повышают до 15 мг/нед. Впоследствии назначают максимальную переносимую дозу. Перед началом лечения проводят общий анализ крови (обязательно определяют число тромбоцитов), биохимическое исследование крови (определяют уровень креатинина и АМК, активность АсАТ, АлАТ и щелочной фосфатазы) и общий анализ мочи. Общий анализ крови и биохимическое исследование крови проводят ежемесячно. Если общая доза метотрексата достигла 1,5 г, рекомендуется биопсия печени.
6. Препараты золота также угнетают высвобождение медиаторов тучными клетками. Показано, что эти препараты позволяют снизить дозу кортикостероидов при лечении тяжелой бронхиальной астмы. Препараты золота назначают в/м ( ауротиоглюкоза ) и внутрь ( ауранофин ). У взрослых ауротиоглюкозу применяют по следующей схеме: 10 мг/нед в течение 1-й недели, 25 мг/нед в течение 2-й и 3-й недель, 50 мг/нед начиная с 4-й недели до общей дозы 800—1000 мг. Затем, если препарат эффективен и не вызывает побочных эффектов, его продолжают применять в дозе 50 мг каждые 3—4 нед. Ауранофин взрослым назначают по 6 мг/сут в 1—2 приема. Если в этой дозе препарат неэффективен, через 6 мес ее увеличивают до 9 мг/сут в 3 приема. Если через 3 мес улучшение не наступает, препарат отменяют. Препараты золота вызывают много побочных эффектов: дерматит, тошноту, понос, стоматит, анемию, лейкопению, тромбоцитопению, протеинурию, повышение активности печеночных ферментов, интерстициальный пневмонит. В связи с этим больных, получающих эти препараты, регулярно обследуют для раннего выявления осложнений лечения.
7. Буферные насадки — это камеры разных размеров, которые надеваются на наконечники ингаляторов-дозаторов для увеличения подачи ингаляционных препаратов в бронхи и уменьшения их оседания в ротоглотке. Попадая в буферную насадку, поток аэрозоля замедляется, крупные капли оседают, а мелкие достигают бронхов, распределяясь в них более равномерно и не попадая в ротоглотку. Особенно рекомендуется использовать буферные насадки детям и пожилым, а также тем больным, у которых ингаляционные препараты вызывают першение в горле и оказывают местное раздражающее действие. Многие авторы рекомендуют буферные насадки всем больным, получающим ингаляционные кортикостероиды. Для детей младшего возраста особенно удобны насадки с односторонним клапаном, позволяющие вдохнуть одну дозу аэрозоля в несколько приемов. В настоящее время выпускаются следующие насадки: ИнспайэрИз (Шеринг-Плау), Брифэнсер (Новартис), Эллипс (Глаксо Вэллком), ОптиХэйлер (Хелфскэн Продактс, Инк.), Аэрочэмбер (Форест Фармасьютикэлс). Последняя предназначена для детей младшего возраста и имеет маску с односторонним клапаном. Больные должны соблюдать рекомендованные производителем правила пользования и ухода за насадками.
Для повышения эффективности ингаляционных препаратов больного необходимо научить правильно пользоваться ингаляторами-дозаторами. Перед использованием ингалятор встряхивают. Голова больного должна быть слегка запрокинута. Наконечник ингалятора-дозатора помещают перед открытым ртом, не далее 2,5 см от него. В начале вдоха нажимают на баллончик. Делают глубокий, медленный вдох, после чего дыхание задерживают на 10 с. При необходимости нескольких ингаляций между ними делают паузы: 3—4 мин — при применении бета-адреностимуляторов, 1 мин — при применении кортикостероидов. Для уменьшения местного раздражающего действия после ингаляции рекомендуется прополоскать рот и горло водой. Это особенно важно при применении ингаляционных кортикостероидов.
8. Отхаркивающие средства. Назначение этих средств улучшает отделение мокроты. При дегидратации для разжижения мокроты показано введение жидкости.
а. Восстановление водного баланса способствует снижению вязкости слизи, разрыхлению слизистых пробок и замедлению их образования. Взрослым рекомендуется выпивать 3—4 л жидкости в сутки. В тяжелых случаях рекомендуются ингаляции 0,45% раствора хлорида натрия в течение 20—30 мин 3—4 раза в сутки с помощью распылителя ингаляционных растворов. Поскольку капли жидкости раздражают дыхательные пути и могут вызвать бронхоспазм, перед ингаляцией солевого раствора или во время нее следует применять ингаляционные бронходилататоры.
б. Ингаляции солевых растворов и бронходилататоров рекомендуется сочетать с постуральным дренажем, перкуссионным и вибрационным массажем грудной клетки. Если бронхоспазм усиливается, ингаляцию солевых растворов прекращают.
в. Эффективность других отхаркивающих средств зависит от водного баланса. Мнения о целесообразности их применения при бронхиальной астме противоречивы.
1) Гвайфенезин стимулирует секрецию слизи и снижает ее вязкость. Этот препарат редко оказывает побочные действия, входит в состав многих средств от кашля. Обычная доза — 200 мг (для детей — 100 мг) внутрь каждые 4—6 ч. Препараты длительного действия назначают по 600—1200 мг внутрь каждые 12 ч. При применении гвайфенезина рекомендуется пить больше жидкости. Эффективность препарата при бронхиальной астме незначительна, он не может заменить бронходилататоры.
2) Препараты йода также снижают вязкость мокроты. При их применении также рекомендуется пить много жидкости. Эффективность лечения зависит от дозы, препараты можно применять внутрь и в/в, однако в/в введение препаратов йода не имеет преимуществ перед их применением внутрь. Внутрь назначают насыщенный раствор йодида калия (10—15 капель разводят водой и принимают 3 раза в сутки) и йодированный глицерин (30—60 мг 3—4 раза в сутки). В/в вводят йодид натрия , 1—2 г/сут в 5% растворе глюкозы. Этот препарат применяют только у взрослых. По эффективности препараты йода близки к гвайфенезину . Применение препаратов йода ограничено из-за большого количества побочных эффектов. Они вызывают угри, особенно у подростков, паротит, тошноту, рвоту, потерю аппетита, боль в животе и понос. Многие больные отмечают металлический вкус во рту. Иногда наблюдаются гипотиреоз и увеличение щитовидной железы. Побочные эффекты при применении йодида калия возникают чаще, чем при применении йодированного глицерина . Из-за большого количества побочных эффектов препараты йода не рекомендуется применять постоянно, кормящим и беременным они противопоказаны. При приступах бронхиальной астмы препараты йода малоэффективны.
3) Ацетилцистеин снижает вязкость мокроты за счет расщепления мукопротеидов. Действие препарата дозозависимо. Обычная доза для взрослых и детей — 1—10 мл 20% раствора или 2—20 мл 10% раствора 1—4 раза в сутки в виде аэрозоля. Сразу после применения ацетилцистеина усиливается секреция слизи, поэтому после ингаляции больным рекомендуют тщательно откашливаться или проводят постуральный дренаж. Препарат раздражает дыхательные пути, а при повышенной реактивности бронхов может вызвать бронхоспазм. В связи с этим его применяют только в сочетании с бронходилататорами, например с 0,25—0,50 мл 1% раствора изоэтарина , 0,3 мл 5% раствора орципреналина или 0,5 мл 5% раствора сальбутамола . Если бронходилататоры не устраняют бронхоспазм, вызванный ацетилцистеином , препарат отменяют. Частое побочное действие — стоматит. Поскольку ацетилцистеин нередко вызывает бронхоспазм, его применяют лишь в тех случаях, когда вязкую, густую мокроту невозможно удалить иными методами.
9. H1-блокаторы при приступах бронхиальной астмы малоэффективны. Их применение оправдано только при сочетании бронхиальной астмы с аллергическими заболеваниями верхних дыхательных путей. При этом обязательно лечение бронходилататорами. Кетотифен — препарат, сходный по строению с ципрогептадином , обладает антигистаминным, противовоспалительным и бронходилатирующим действием. В США он не производится, однако широко применяется в Европе и Японии. Кетотифен назначают внутрь в дозе 1 мг 1—2 раза в сутки. Бронходилатирующим действием обладает и цетиризин — H1-блокатор из группы пиперазинов.
10. Антимикробные средства при бронхиальной астме применяются редко, поскольку она обычно осложняется вирусными инфекциями верхних дыхательных путей.
а. Среди бактериальных инфекций, осложняющих бронхиальную астму, чаще всего встречаются синуситы, бронхит и пневмония. Возбудителями острого синусита обычно бывают Haemophilus influenzae, Streptococcus pyogenes, Streptococcus pneumoniae и Staphylococcus aureus. Хронический синусит обычно вызывают анаэробные бактерии и Haemophilus influenzae. Лечение острых и хронических синуситов подробно описано в гл. 5, п. VII.Г . При остром бронхите в мазках мокроты, окрашенных по Граму, выявляется большое количество нейтрофилов (эозинофилов обычно мало) и микроорганизмов — чаще Streptococcus pneumoniae и Haemophilus influenzae.
б. В разных возрастных группах пневмонию вызывают разные возбудители. Так, у детей младше 5 лет заболевание чаще всего обусловлено вирусной инфекцией, в этих случаях антимикробные средства не назначают. В возрасте от 5 до 30 лет обычно встречается вирусная и микоплазменная пневмония. При микоплазменной пневмонии назначают тетрациклин или эритромицин . Наиболее распространенный возбудитель пневмонии у лиц старше 30 лет — Streptococcus pneumoniae. В этом случае обычно эффективны пенициллины и цефалоспорины. При подозрении на пневмонию обязательно проводят микроскопию мазка мокроты, окрашенного по Граму, и ее посев.
VI. Принципы лечения. Основная цель лечения бронхиальной астмы — предупреждение приступов в течение как можно более длительного периода с помощью как можно меньшего количества лекарственных средств. Важнейшая роль в лечении бронхиальной астмы отводится обучению больных. Вместе с больным и его родственниками врач разрабатывает индивидуальный план лечения. Больному объясняют необходимость точного выполнения указаний врача. Профилактические мероприятия включают устранение факторов, вызывающих приступы, лечение сопутствующих аллергических и инфекционных заболеваний, а также медитацию, аутотренинг, методы релаксации и биологической обратной связи (см. гл. 7, п. V.А ). Тактика лечения зависит от тяжести заболевания. Критерии оценки тяжести бронхиальной астмы приведены в табл. 7.6 . Кроме того, ниже описано лечение бронхиальной астмы физического усилия, аспириновой и сульфитной бронхиальной астмы, а также бронхиальной астмы у беременных и при желудочно-пищеводном рефлюксе.
А. Лечение приступа бронхиальной астмы. Приступ бронхиальной астмы начинается внезапно или развивается постепенно во время обострения заболевания.
1. Больного успокаивают, просят его расслабиться, дышать медленно и глубоко. Рекомендуют обильное питье.
2. Если приступ возник на фоне отсутствия симптомов заболевания, эффективны дозированные аэрозоли бронходилататоров. Улучшение обычно наступает через несколько минут после 1—3 вдохов аэрозоля. Вместо ингаляций можно назначить бета2-адреностимуляторы короткого действия внутрь или препараты теофиллина — лучше в виде таблеток, содержащих высокодисперсный препарат, или раствора. Улучшение в этом случае обычно наблюдается через 30—60 мин.
3. Если бронхоспазм сохраняется или возникает вновь, а также если в анамнезе есть указания на длительные приступы, назначают поддерживающее лечение бета2-адреностимуляторами или теофиллином .
а. Лечение начинают с бета2-адреностимуляторов. Их назначают внутрь или ингаляционно. Названия препаратов и дозы приведены в табл. 4.5 . Дозу бета2-адреностимуляторов для приема внутрь подбирают в зависимости от эффективности и побочных действий. Для усиления бронходилатирующего действия бета2-адреностимуляторы назначают одновременно и внутрь, и ингаляционно. При плохой переносимости бета-адреностимуляторов вместо них назначают ипратропия бромид , 1—4 вдоха дозированного аэрозоля или раствора для ингаляций 3—4 раза в сутки. Ипратропия бромид можно применять в комбинации с бета2-адреностимуляторами. Если ингаляционные бета2-адреностимуляторы или их комбинация с ипратропия бромидом неэффективны, назначают препараты теофиллина длительного (дозы приведены в гл. 7, п. V.Б.1 ) или короткого действия (дозы приведены в гл. 4, п. VIII.Г , биодоступность — в табл. 7.7 ). При плохой переносимости препаратов теофиллина их дозу снижают и дополнительно назначают бета2-адреностимуляторы внутрь. Кроме того, при непереносимости какого-либо препарата теофиллина его можно заменить на другой. Если теофиллин переносится хорошо, каждые 2—3 сут его дозу увеличивают до достижения эффективной. При этом регулярно определяют концентрацию теофиллина в сыворотке.
б. Длительность лечения. Лечение проводят до тех пор, пока не наступит стабильное улучшение. После устранения бронхоспазма препараты в минимальных эффективных дозах назначают по крайней мере еще в течение 2—3 сут.
в. Противовоспалительные и противоаллергические средства. При легкой и среднетяжелой бронхиальной астме вместо бронходилататоров для приема внутрь с успехом применяются ингаляционные кортикостероиды (по 2—4 вдоха дозированного аэрозоля 2 раза в сутки) и кромолин (по 2 вдоха 4 раза в сутки). Ингаляционные бета2-адреностимуляторы при этом назначают по 2 вдоха дозированного аэрозоля каждые 3—4 ч. Если ингаляционные бета2-адреностимуляторы в этих дозах неэффективны, увеличивают дозу кортикостероидов — до 4 вдохов 2—4 раза в сутки.
4. Кортикостероиды для приема внутрь назначают при неэффективности описанного выше лечения, а также если в анамнезе есть указания на тяжелые приступы бронхиальной астмы и лечение кортикостероидами для системного применения. Начинают с насыщающей дозы, эквивалентной 40—60 мг/сут преднизона (у детей — 1—2 мг/кг/сут). Препарат назначают внутрь в один или несколько приемов в течение 3—7 сут. Действие обычно развивается через 6—24 ч, реже через 2—3 сут после начала лечения. Если наступает улучшение, в течение последующих 3—7 сут дозу постепенно снижают до полной отмены препарата. Ингаляционные кортикостероиды и бронходилататоры для приема внутрь в поддерживающих дозах вместе или по отдельности назначают еще в течение 5—7 сут, затем дозы этих препаратов также снижают.
5. Если кортикостероиды неэффективны, больного госпитализируют (см. гл. 7, п. VII ).
Б. Рекомендации больным по лечению приступов бронхиальной астмы в домашних условиях (NIH Guidelines for the Diagnosis and Management of Asthma, 1991).
1. При возникновении приступа следует сделать 2—4 вдоха дозированного аэрозоля какого-либо бета2-адреностимулятора. Ингаляции можно повторять каждые 20—60 мин. При этом лучше использовать буферную насадку.
2. Если бронхоспазм удалось устранить или значительно уменьшить его выраженность, а пиковая объемная скорость превышает 70—90% исходного значения, ингаляции адреностимуляторов проводят каждые 3—4 ч в течение 1—2 сут и продолжают проводившееся ранее поддерживающее лечение. При возобновлении приступа связываются с врачом.
3. Если симптомы сохраняются в покое и ограничивают повседневную активность, а пиковая объемная скорость составляет 50—70% исходного уровня, бета2-адреностимуляторы в виде дозированных аэрозолей или растворов для ингаляций используют каждый час и начинают прием кортикостероидов внутрь в насыщающей дозе. Если лечение кортикостероидами уже проводится, то увеличивают их дозу. Если улучшение не наступает в течение 2—6 ч и если необходимо применять ингаляционные бета2-адреностимуляторы в максимальной дозе 16 вдохов/сут, необходимо обратиться к врачу.
4. Если несмотря на лечение сохраняется выраженный бронхоспазм, из-за одышки невозможно пройти более 30 м, а пиковая объемная скорость не превышает 50% исходного значения, немедленно связываются с врачом. Применяют ингаляционные бета2-адреностимуляторы: с помощью ингалятора-дозатора, 4—6 вдохов, ингаляцию повторяют через 10 мин, или распылителя ингаляционных растворов, 4—6 вдохов однократно. Начинают применение кортикостероидов или повышают их дозу. Если через 30 мин улучшение не наступает, а пиковая объемная скорость не превышает 50% исходного значения, следует вызвать скорую помощь. В этих случаях, а также тогда, когда в течение последних 6—12 ч ингаляции бета2-адреностимуляторов проводились каждые 1—3 ч, показана госпитализация.
В . Лечение приступа бронхиальной астмы в приемном отделении (NIH Guidelines for the Diagnosis and Management of Asthma, 1991, U.S. Department of Health and Human Services Publication no. 91-3042, August 1991).
1. Для оценки тяжести приступа проводят пневмотахометрию или спирометрию. При необходимости исследуют газы артериальной крови. Больного успокаивают, для облегчения дыхания используют приемы, описанные в гл. 7, п. V.А.4 .
2. С помощью пульс-оксиметрии определяют насыщение гемоглобина артериальной крови кислородом. Если оно ниже 90%, а paO2 — ниже 60—65 мм рт. ст., начинают ингаляцию кислорода со скоростью 2—4 л/мин.
3. Назначают бета2-адреностимуляторы: в виде дозированных аэрозолей с использованием буферной насадки (по 4—6 вдохов) или растворов для ингаляций, например 0,5—1,0 мл 0,5% раствора сальбутамола , или 0,2—0,3 мл 5% раствора орципреналина , или 0,25—0,5 мл 1% раствора изоэтарина с помощью распылителя каждые 20—30 мин в течение 1—1,5 ч. Детям старше 5 лет назначают дозированный аэрозоль сальбутамола по 2 вдоха каждые 5 мин, но не более 12 вдохов, или 0,5% раствор сальбутамола , 0,15 мг/кг, но не более 5 мг каждые 20 мин в течение 1—2 ч, при непрерывной ингаляции — не более 15 мг/ч. У детей ингаляции бета2-адреностимуляторов проводят с помощью буферной насадки, снабженной маской с односторонним клапаном. Вместо ингаляционных бета2-адреностимуляторов иногда назначают раствор адреналина 1:1000, 0,2—0,3 мл п/к, детям — 0,01 мл/кг п/к. При необходимости инъекции адреналина повторяют каждые 20—30 мин (не более 3 инъекций). Кортикостероиды применяют: 1) при неэффективности бета2-адреностимуляторов, 2) при лечении кортикостероидами в анамнезе, 3) при возникновении приступа на фоне лечения кортикостероидами для приема внутрь. Кортикостероиды назначают в насыщающей дозе внутрь (см. гл. 7, п. VI.A.4 ) или в/в. В/в вводят гидрокортизон , 5 мг/кг, или метилпреднизолон , 1—2 мг/кг.
4. При стабильном улучшении, повышении пиковой объемной скорости и ОФВ1 не менее чем до 70% исходного значения и в отсутствие одышки переходят на поддерживающее лечение. Назначают адреностимуляторы для приема внутрь, ингаляционные кортикостероиды и кромолин или недокромил в разных сочетаниях с ингаляционными бета2-адреностимуляторами. Для профилактики побочных действий адреностимуляторов соблюдают меры предосторожности, описанные в гл. 7, п. V.Б.1.a.1 . Если начат прием кортикостероидов для приема внутрь, его продолжают, если не начат, решают вопрос о целесообразности назначения кортикостероидов. В дальнейшем больного наблюдают амбулаторно.
5. Если сохраняются свистящее дыхание и одышка, а пиковая объемная скорость не превышает 40—70% исходной, ингаляции бета2-адреностимуляторов проводят каждый час и назначают кортикостероиды для системного применения. При дегидратации проводят в/в инфузию жидкостей. При неэффективности бета2-адреностимуляторов вводят аминофиллин , 6 мг/кг в/в в течение 20—30 мин (см. табл. 7.4 ), затем 0,2—1,2 мг/кг/ч в/в (в зависимости от клиренса теофиллина , в среднем 0,5 мг/кг/ч). Если больной принимает теофиллин внутрь, аминофиллин назначают в более низкой дозе. Регулярно определяют концентрацию теофиллина в сыворотке (см. табл. 4.7 ). Вместо аминофиллина в/в можно назначить теофиллин (см. табл. 7.4 ).
6. При неэффективности перечисленных мероприятий больного госпитализируют. Лечение астматического статуса описано в гл. 7, п. VII.Г .
Г. Лечение тяжелой бронхиальной астмы. Если наблюдаются длительные обострения или ежедневные приступы бронхиальной астмы или для их предупреждения необходимо постоянное медикаментозное лечение, говорят о тяжелой бронхиальной астме. При этой форме заболевания особое значение имеет немедикаментозное лечение.
1. Дозированные аэрозоли бета2-адреностимуляторов назначают по 1—3 вдоха, при необходимости дозу увеличивают до 3—4 вдохов в сутки.
2. Если потребность в ингаляционных бета2-адреностимуляторах превышает 3—4 вдоха в сутки, дополнительно назначают ингаляционные кортикостероиды, 2—4 вдоха 2 раза в сутки (см. гл. 7, п. V.Б.4 ). Если ингаляции кортикостероидов вызывают бронхоспазм или их применение затруднено из-за бронхоспазма, за 5—10 мин до ингаляции назначают дозированный аэрозоль бета2-адреностимулятора, 1—3 вдоха. Чтобы обеспечить попадание кортикостероида в мелкие бронхи, после каждого вдоха рекомендуют задерживать дыхание на 10—15 с. Промежуток между вдохами ингаляционных кортикостероидов должен составлять не менее 1 мин. При местном раздражающем действии и кандидозе рта применяют буферные насадки. Они уменьшают оседание препарата в ротоглотке и особенно необходимы при назначении ингаляционных кортикостероидов в высоких дозах (в виде дозированного аэрозоля во флаконе с буферной насадкой выпускается триамцинолон ). Если указанные дозы кортикостероидов неэффективны, их повышают до 4 вдохов 2—4 раза в сутки. После улучшения состояния дозы ингаляционных кортикостероидов постепенно снижают. При плохой переносимости физических нагрузок и частых приступах, в том числе по ночам, ингаляционные кортикостероиды назначают по 4—6 вдохов 2—4 раза в сутки, а при каждом приступе — кортикостероиды для приема внутрь коротким курсом. Такая схема лечения в большинстве случаев позволяет избежать постоянного назначения кортикостероидов для системного применения.
3. Кромолин , 2 вдоха (1600 мкг) дозированного аэрозоля или 20 мг порошка или раствора для ингаляций 4 раза в сутки, назначают вместо или в дополнение к ингаляционным кортикостероидам. В течение первых 4—8 нед лечения больного просят вести дневник, в котором он должен отмечать свое состояние и указывать дозы принимаемых им препаратов. Отдельно записывают дозы всех препаратов, принимавшихся до назначения кромолина . Если кромолин уменьшает симптомы заболевания и снижает потребность в других препаратах, его применяют неопределенно долго, по возможности снижая дозу, например назначают на 1 ингаляцию меньше каждые 1—2 нед. Недокромил , 2 вдоха (по 1,75 мг) 4 раза в сутки с помощью ингалятора-дозатора, можно использовать вместо кромолина . Схема лечения такая же, как при применении кромолина .
4. Препараты теофиллина длительного действия назначают вместо или в дополнение к кортикостероидам, кромолину или недокромилу . Концентрация теофиллина в сыворотке должна составлять 8—15 мкг/мл. Препараты теофиллина длительного действия назначают 2—3 раза в сутки. Для профилактики ночных и утренних приступов препараты длительного действия принимают перед сном. При появлении побочных эффектов дозу уменьшают (см. гл. 4, п. VIII.Е ).
5. При плохой переносимости теофиллина или неэффективности комбинации теофиллина с ингаляционными кортикостероидами или кромолином вместо теофиллина или в дополнение к нему назначают бета2-адреностимуляторы внутрь (дозы теофиллина при этом снижают). Применение ингаляционных бета2-адреностимуляторов в этом случает продолжают (названия и дозы приведены в табл. 4.5 ).
6. Кортикостероиды для системного применения, чаще всего преднизон , применяют при неэффективности всех перечисленных выше схем лечения. Преднизон назначают в насыщающей дозе — 40—60 мг/сут — обычно в течение 3—4 сут (см. гл. 7, п. V.Б.4.a ), затем дозу постепенно снижают сначала до 20 мг/сут (у детей — до 0,5 мг/кг/сут), а затем на 2,5—5,0 мг каждые 1—2 сут до минимальной эффективной.
7. Чтобы уменьшить осложнения длительного лечения кортикостероидами для системного применения, их назначают через день. К этой схеме лечения переходят одним из двух способов: 1) доза в 1-й день остается прежней, а дозу во 2-й день постепенно уменьшают до полного перехода на прием препарата через день, 2) суточную дозу удваивают и принимают ее через день. При возобновлении симптомов заболевания возвращаются к ежедневному применению препарата. Кортикостероиды при длительном лечении лучше назначать 1 раз в сутки, утром сразу после пробуждения. При язвенной болезни в анамнезе или диспепсии через 20—30 мин после приема кортикостероидов назначают антацидные средства. Ограничивают употребление поваренной соли, при необходимости назначают препараты калия, особенно у больных, получающих диуретики. Если кортикостероиды неэффективны, их дозу увеличивают в 3 раза и назначают ежедневно в несколько приемов в течение 2—3 сут, затем пытаются снизить дозу до исходной. Во всех случаях стремятся назначать кортикостероиды для системного применения в минимальных эффективных дозах. Больных регулярно обследуют для раннего выявления осложнений лечения (см. гл. 4, п. XII.Е ). Кортикостероиды не заменяют бронходилататоры, кромолин или недокромил .
8. Триамцинолон назначают больным тяжелой бронхиальной астмой с длительными обострениями, которая сопровождается угрожающими жизни приступами и требует постоянного лечения кортикостероидами. В анамнезе у этих больных обычно имеются указания на частые госпитализации, в том числе в реанимационное отделение для проведения ИВЛ. Триамцинолон особенно показан тем больным, которые по каким-либо причинам не могут принимать кортикостероиды внутрь. Препарат назначают в дозе 120 мг/сут в/м в течение 3 сут. Это приводит к улучшению функции внешнего дыхания, уменьшению частоты обращений за неотложной помощью, госпитализаций и снижению доз назначаемых препаратов, в том числе кортикостероидов для системного применения. Однако побочные эффекты — миопатия, кровоточивость, гирсутизм — при назначении триамцинолона в высоких дозах возникают чаще и оказываются более выраженными, чем при назначении кортикостероидов внутрь. Поскольку в/м введение триамцинолона может привести к локальной атрофии мышц, препарат лучше вводить в бедро. Некоторым больным триамцинолон приходится назначать в более высоких дозах — по 360 мг в сутки в/м в течение 3 сут — и повторять курс лечения через 3—6 мес. Иногда триамцинолон назначают по 80 мг в/м 1 раз в месяц. При улучшении состояния дозу препарата снижают. При тяжелых побочных эффектах, например миопатии, препарат отменяют.
9. При тяжелой бронхиальной астме, требующей высоких доз кортикостероидов, назначают метилпреднизолон в сочетании с тролеандомицином , метотрексат или препараты золота. Однако эти схемы лечения не рекомендованы FDA для применения при бронхиальной астме (см. гл. 7, пп. V.Б.4.г и V.Б.5—6 ).
10. При тяжелой бронхиальной астме рекомендуется обильное питье. Отхаркивающие средства имеют ограниченное применение, однако в некоторых случаях, при обильной, густой и вязкой мокроте их назначают в сочетании с постуральным дренажем.
11. При тяжелой бронхиальной астме ингаляции бронходилататоров с помощью распылителей более эффективны, чем ингаляции дозированных аэрозолей, поскольку распылители ингаляционных растворов обеспечивают более длительное введение аэрозоля и равномерное распределение препарата в бронхах. Буферные насадки повышают эффективность ингаляторов-дозаторов.
12. Антибиотики применяются только при вторичной бактериальной инфекции (см. гл. 7, п. V.Б.10 ).
Д. Бронхиальная астма физического усилия. У большинства больных бронхиальной астмой и более чем у 40% больных аллергическим ринитом 10—15-минутная физическая нагрузка вызывает бронхоспазм, на что указывает существенное снижение ОФВ1. Чем тяжелее бронхиальная астма, тем более выраженный бронхоспазм вызывает физическая нагрузка. У части больных приступы бронхиальной астмы развиваются только после физической нагрузки.
1. Частота и выраженность приступов бронхиальной астмы, вызванных физической нагрузкой, зависят от характера этой нагрузки. Чаще всего бронхоспазм возникает при быстром беге, реже — при ходьбе и езде на велосипеде. Плавание обычно не вызывает бронхоспазма. Бронхоспазм обычно развивается через 5—10 мин после нагрузки и исчезает в покое, реже он сохраняется более 1 ч или усиливается после физической нагрузки. Повторная нагрузка менее чем через 2 ч обычно переносится легче, чем предшествующая.
2. Причиной бронхиальной астмы физического усилия, по-видимому, является охлаждение дыхательных путей, вызванное гипервентиляцией. Показано, что определенную роль в патогенезе заболевания играют медиаторы воспаления, однако механизм развития бронхоспазма под действием холодного воздуха пока неизвестен.
3. Лечение в основном направлено на профилактику приступов. Определяют характер и продолжительность нагрузки, приводящей к бронхоспазму. Подбирают такую нагрузку, которая хорошо переносится больным. Рекомендуют, чтобы периоды интенсивной физической нагрузки были короткими, между ними больной обязательно должен отдыхать. Если улучшение не наступает, перед физической нагрузкой рекомендуют применять бронходилататоры. Назначают бета2-адреностимуляторы в виде дозированного аэрозоля за 15—20 мин до нагрузки. Это наиболее эффективный способ лечения бронхиальной астмы физического усилия. Назначая препараты спортсменам, участвующим в соревнованиях, следует иметь в виду, что многие организационные комитеты не разрешают применение катехоламинов, например изопреналина или изоэтарина , в то время как тербуталин и сальбутамол — адреностимуляторы, не относящиеся к катехоламинам, — разрешены к применению. В некоторых случаях эффективен кромолин . Его применяют за 15—60 мин до физической нагрузки в виде дозированного аэрозоля (1600 мкг) или порошка для ингаляций (20 мг). Перед применением кромолина можно назначить ингаляцию адреностимуляторов. Кромолин применяют при непереносимости других препаратов для лечения бронхиальной астмы физического усилия. Иногда эффективен ипратропия бромид , 1—2 вдоха дозированного аэрозоля (см. гл. 7, п. V.Б.1.в ) за 15—30 мин до физической нагрузки. Больным, испытывающим затруднения при пользовании ингалятором, а также дополнительно к ингаляционным препаратам назначают адреностимуляторы или теофиллин внутрь за 1—2 ч до физической нагрузки.
4. Родители больного ребенка должны сообщить о его заболевании школьным учителям и тренерам и объяснить, что перед физической нагрузкой он должен принимать бронходилататоры, а при возникновении приступа нуждается в отдыхе.
Е. Аспириновая бронхиальная астма часто сочетается с вазомоторным ринитом и полипами носа. Заболевание обычно возникает у взрослых, не страдающих аллергическими заболеваниями, на фоне длительного вазомоторного ринита (см. гл. 13, п. VI.Б.1 ).
1. Через несколько минут или часов (до 24 ч) после приема аспирина появляются обильное водянистое отделяемое из носа, покраснение лица и одышка. Приступы бронхиальной астмы обычно бывают тяжелыми. Возможны крапивница, отек Квинке и шок. Предполагается, что в патогенезе заболевания основную роль играет нарушение метаболизма арахидоновой кислоты. Угнетение активности циклоксигеназы приводит к снижению синтеза простагландинов, обладающих бронходилатирующим действием, а активация липоксигеназного пути сопровождается накоплением лейкотриенов, которые вызывают бронхоспазм.
2. Провокационные пробы с салицилатами не проводят. Основа лечения — профилактика, основанная на исключении приема аспирина и содержащих его препаратов. К родственным препаратам, которые могут вызвать приступ при аспириновой бронхиальной астме, относятся индометацин , мефенамовая кислота , феназон , аминофеназон , а также пищевой краситель тартразин (см. табл. 13.7 и приложение IX ). Неацетилированные салицилаты и парацетамол обычно не противопоказаны. Лечение приступов бронхиальной астмы проводят по стандартной схеме. Однако поскольку приступы при аспириновой бронхиальной астме обычно тяжелые, часто бывает необходима госпитализация и лечение кортикостероидами. Лечение крапивницы, отека Квинке и шока подробно описано в гл. 10, п. VI и гл. 11, п. V .
3. Прием аспирина может вызвать бронхоспазм и у некоторых больных бронхиальной астмой в отсутствие сенсибилизации к аспирину в анамнезе. Этим больным впоследствии необходимо избегать приема аспирина . Врач должен подробно рассказать им, какие препараты и пищевые продукты содержат аспирин и сходные с ним вещества. Больные с тяжелыми реакциями на аспирин в анамнезе должны всегда иметь при себе опознавательный браслет.
Ж. Сульфитная бронхиальная астма. У некоторых больных приступы бронхиальной астмы вызывают сульфиты — метабисульфит калия, бисульфит калия, метабисульфит натрия, бисульфит натрия, сульфит натрия, двуокись серы. Эти соединения добавляют во многие продукты и лекарственные средства в качестве антиоксидантов и консервантов. Чаще всего бронхиальную астму вызывает метабисульфит калия. Реакции на сульфиты наблюдаются у 5% больных бронхиальной астмой. Чаще всего они развиваются у взрослых с тяжелой формой заболевания, требующей постоянного лечения кортикостероидами. Перекрестные реакции с другими пищевыми добавками и аспирином отсутствуют. В большинстве случаев сульфиты вызывают внезапный тяжелый бронхоспазм, который может закончиться смертью. Возможны и другие анафилактоидные реакции. Патогенез бронхоспазма, вызванного сульфитами, неизвестен. Возможно, к нему приводит прямая активация тучных клеток двуокисью серы, нарушение метаболизма арахидоновой кислоты и стимуляция холинергических рецепторов. Относительно недавно показано, что сульфиты могут стимулировать продукцию IgE. Диагноз обычно ставят на основании клинической картины. Сразу после употребления продуктов, содержащих сульфиты (салатов, вина, креветок), возникают одышка, свистящее дыхание, покраснение груди и лица. Реакций на сульфиты, содержащиеся в лекарственных средствах, включая ингаляционные бронходилататоры, и двуокись серы в смоге не отмечалось. Однако не исключено, что неэффективность лечения бронхиальной астмы у некоторых больных обусловлена постоянным контактом с этими веществами. Диагноз подтверждается при положительных провокационных пробах, которые может проводить только опытный специалист в условиях стационара. Больному рассказывают, какие лекарственные средства и продукты содержат сульфиты, подчеркивают, что он должен избегать их употребления (см. приложение IX ). Согласно инструкциям FDA, запрещается обрабатывать сульфитами сырые фрукты и овощи, за исключением картофеля. Если концентрация сульфитов в продуктах превышает предельно допустимую, упаковка должна содержать специальную метку. Лекарственные средства, содержащие сульфиты, также должны быть снабжены специальной меткой (значения предельно допустимых концентраций сульфитов в продуктах и лекарственных средствах могут быть изменены только в соответствии с инструкциями FDA). Лечение приступов бронхиальной астмы, вызванных сульфитами, проводится по стандартной схеме. Больные с тяжелыми реакциями на сульфиты в анамнезе должны иметь при себе адреналин в шприце, например АНА—Кит (Холлистер-Стайэр Майлс) или ЭпиПен (Сентэ Лэборэтрис), и опознавательный браслет, особенно если они часто посещают кафе и рестораны.
З. Бронхиальная астма у беременных
1. Физиологические изменения во время беременности
а. Функция внешнего дыхания. Во время беременности увеличивается минутный объем дыхания и уменьшается функциональная остаточная емкость легких. Показатели форсированного выдоха, емкость вдоха, диффузионная способность легких и потребление кислорода не меняются. В крови плода paO2 снижено.
б. Гормональные изменения. Повышение уровня ХГ, кортизола, а также незначительное возрастание уровня цАМФ угнетают действие гистамина. Кроме того, отмечается незначительное снижения уровня IgE в сыворотке.
в. Клинические изменения. Во время беременности примерно у 30% больных бронхиальной астмой наблюдается улучшение, у 30% больных состояние не изменяется, у остальных — ухудшается. Состояние больных тяжелой бронхиальной астмой во время беременности, реже в послеродовом периоде обычно ухудшается. У беременных, больных бронхиальной астмой, несколько повышена частота преждевременных родов и самопроизвольных абортов.
2. Лечение бронхиальной астмы во время беременности проводят по стандартной схеме. Особенное внимание уделяют борьбе с неблагоприятными факторами окружающей среды и исключению контакта с аллергенами. Назначая лекарственные средства, учитывают, к какой категории по классификации FDA они относятся (см. табл. 7.8 ). Больной рассказывают, почему ей необходимо лечение и какими осложнениями оно может сопровождаться.
а. Во время беременности десенсибилизацию (см. гл. 4, п. XIX.В ) не проводят, за исключением тех случаев, когда курс был начат до беременности. Обязательно лечат инфекции дыхательных путей. Больных обучают дыхательным упражнениям, которые они должны регулярно выполнять. По показаниям проводят постуральный дренаж. Избегают применения фенилэфрина , фенилпропаноламина , гидроксизина , бромфенирамина , препаратов йода, тетрациклинов, аминогликозидов, сульфаниламидов и ципрофлоксацина . Роды желательно проводить под регионарной анестезией.
б. Во время приступов бронхиальной астмы назначают ингаляционные бета2-адреностимуляторы. Если необходимо поддерживающее лечение, рекомендуется применять ингаляционные препараты, например кромолин , недокромил или кортикостероиды, в низких дозах. Препараты для системного применения — теофиллин или бета2-адреностимуляторы для приема внутрь — назначают только при неэффективности ингаляционных. При необходимости назначают короткие курсы кортикостероидов для системного применения. Новорожденных от матерей, получавших кортикостероиды в высоких дозах, обследуют для исключения надпочечниковой недостаточности.
И. Бронхиальная астма и желудочно-пищеводный рефлюкс. Приступ бронхиальной астмы может быть вызван аспирацией желудочного содержимого. Желудочно-пищеводный рефлюкс исключают при наличии отрыжки, изжоги, грыжи пищеводного отверстия диафрагмы, а также рецидивирующей пневмонии и ограниченного затемнения, выявляемого при рентгенографии грудной клетки. Желудочно-пищеводный рефлюкс следует исключать у всех больных тяжелой бронхиальной астмой при неэффективности лечения.
1. Диагностика. Рентгенография пищевода и желудка с барием часто не позволяет выявить желудочно-пищеводный рефлюкс. Для уточнения диагноза определяют тонус нижнего пищеводного сфинктера и pH содержимого нижнего отдела пищевода в положении лежа.
2. Лечение. При подозрении на желудочно-пищеводный рефлюкс назначают щадящую диету и антацидные средства. Рекомендуется принимать пищу не менее чем за 2 ч до сна, приподнимать головной конец кровати на 15—20 см. Дополнительно можно назначить ранитидин , метоклопрамид , омепразол или цизаприд . В некоторых случаях требуется хирургическое вмешательство. Необходимо учитывать, что теофиллин и бета-адреностимуляторы расслабляют нижний пищеводный сфинктер, поэтому могут вызывать желудочно-пищеводный рефлюкс.
К. Профессиональная бронхиальная астма. Распространенность бронхиальной астмы, обусловленной действием вредных производственных факторов, составляет 5%. Факторами, провоцирующими приступ бронхиальной астмы, могут быть как аллергены, так и вещества, повышающие реактивность бронхов. У больных бронхиальной астмой действие вредных производственных факторов вызывает обострение и приводит к прогрессированию заболевания. Проявления профессиональной бронхиальной астмы разнообразны. К наиболее распространенным относятся кашель, одышка, свистящее дыхание, особенно выраженные во время работы. В выходные дни и во время отпуска обычно наступает улучшение. У некоторых больных ухудшение наступает в течение 1 ч после начала действия вредных факторов (то есть почти сразу после прибытия на работу), у других — спустя 4—12 ч. У части больных наблюдается двухфазная реакция. Ухудшение при этом наблюдается в начале и конце рабочего дня: в начале рабочего дня симптомы обычно незначительны и исчезают через 1—4 ч, в конце дня они более выражены. Иногда симптомы заболевания не исчезают даже после длительного перерыва в работе. Для ранней стадии профессиональной бронхиальной астмы характерен длительный кашель, нередко он сочетается с ринитом и частыми вирусными инфекциями верхних дыхательных путей. Известно более 100 веществ, с которыми человек контактирует на производстве и которые могут вызвать бронхиальную астму или спровоцировать ее приступ. Управление производственной безопасности и здоровья США устанавливает значения предельно допустимых концентраций этих веществ. Однако при повышенной реактивности бронхов приступы бронхиальной астмы возникают при действии даже допустимых концентраций вредных веществ. Так, у здоровых лиц двуокись серы вызывает раздражение дыхательных путей при концентрации 6,5 мг/м 3 , а у больных бронхиальной астмой — при концентрации 0,65 мг/м 3 . К наиболее распространенным веществам, вызывающим бронхиальную астму, относятся латекс, изоцианаты, ангидриды и древесная пыль (см. табл. 7.9 ). Так, в сыворотке больных профессиональной бронхиальной астмой врачей и медицинских сестер выявляются IgE, специфичные к латексу. Толуилендиизоцианаты — вещества, применяемые в производстве красок и полиуретанов, — повреждают слизистую дыхательных путей, что приводит к стойкой сенсибилизации к этим соединениям. В сыворотке некоторых больных выявляются IgE, специфичные к толуилендиизоцианатам, однако роль этих антител в развитии сенсибилизации к толуилендиизоцианатам не установлена. Ангидриды тримеллитовой и фталевой кислот применяются в производстве красок и пластмасс и вызывают реакции, сходные с реакциями на толуилендиизоцианаты. Кислота, содержащаяся в древесине туи гигантской, вызывает раздражение дыхательных путей, которое после длительного контакта с ней может сохраняться в течение нескольких лет.
1. Диагноз основан на данных анамнеза и физикального исследования. Ранняя диагностика позволяет предотвратить прогрессирование бронхиальной астмы. Повышенную реактивность бронхов выявляют с помощью спирометрии, проведенной до и после рабочего дня. С помощью индивидуального пневмотахометра больной может самостоятельно измерять пиковую объемную скорость в течение рабочего дня (измерение рекомендуется проводить каждый час). Диагноз подтверждается с помощью провокационных проб (см. гл. 7, п. II.В.10 ). Их следует проводить только в условиях стационара. Следует помнить, что при профессиональной бронхиальной астме часты поздние реакции, которые могут появиться спустя 12 ч после проведения пробы.
2. Лечение направлено на устранение действия вредных производственных факторов, что часто требует профессиональной переподготовки больного. Особое внимание следует уделять больным с тяжелой и прогрессирующей бронхиальной астмой. Лечение проводится по стандартной схеме, однако оно не может заменить мероприятия по устранению контакта с провоцирующими факторами. Ранние реакции предотвращает профилактическое применение бронходилататоров или кромолина , при поздних — эффективны кортикостероиды.
VII. Астматический статус и дыхательная недостаточность
А. Определение. Астматический статус — это тяжелый приступ бронхиальной астмы, при котором неэффективны ингаляционные бета2-адреностимуляторы, адреналин п/к, аминофиллин в/в и кортикостероиды. Астматический статус в 1—3% случаев приводит к смерти, поэтому требует оказания неотложной помощи.
Б. Провоцирующие факторы те же, что при обычном приступе бронхиальной астмы — контакт с аллергенами, действие раздражающих веществ, вирусная инфекция дыхательных путей, изменение температуры и влажности воздуха, эмоциональное перенапряжение, аспирация желудочного содержимого. Риск астматического статуса повышается при несоблюдении больным рекомендаций врача и недоступности медицинской помощи.
а. Изменение симптомов: более частые и тяжелые приступы одышки, прогрессирующее снижение переносимости физической нагрузки, усиление кашля с выделением скудной вязкой мокроты.
б. Снижение эффективности бронходилататоров. Несмотря на более частое применение бронходилататоров, продолжительность их действия и эффективность снижаются.
в. Психические нарушения: усиливающаяся тревога и раздражительность.
г. Недавние частые и тяжелые приступы бронхиальной астмы, требовавшие оказания неотложной помощи или госпитализации.
2. Физикальное исследование
а. Больной возбужден, речь и дыхание затруднены, отмечается тахипноэ.
б. Втяжение яремной ямки, участие вспомогательных мышц в акте дыхания, признаки перерастяжения легких: низкое стояние куполов диафрагмы, уменьшение экскурсии грудной клетки, усиленный перкуторный звук.
в. Жесткое дыхание, хрипы, при выраженной обструкции бронхов дыхание не проводится.
г. Парадоксальный пульс, снижение систолического АД на вдохе более чем на 10 мм рт. ст. Втяжение податливых участков грудной клетки и парадоксальный пульс наблюдаются примерно у 50% больных с астматическим статусом. У взрослых эти признаки обычно появляются, когда ОФВ1 становится менее 1 л.
д. Признаки активации симпатоадреналовой системы: тахикардия, повышение АД и потливость.
3. Дифференциальную диагностику проводят со следующими заболеваниями.
а. Обструкция верхних дыхательных путей, например острый эпиглоттит, отек, опухоль или паралич мышц гортани, острый ларинготрахеобронхит, стеноз трахеи, трахеомаляция, опухоль или сдавление трахеи, инородное тело. Для обструкции верхних дыхательных путей характерны хрипы на вдохе.
б. Острая сердечная недостаточность. Диагноз ставят на основании данных анамнеза: указаний на сердечно-сосудистые заболевания, частые ночные приступы одышки, одышку при физической нагрузке, а также физикального и инструментальных исследований, выявляющих увеличение размеров сердца, набухание шейных вен, наличие III тона сердца, мелкопузырчатые хрипы, линии Керли в реберно-диафрагмальном углу. Признаки перерастяжения легких отсутствуют.
в. ТЭЛА более чем в 80% случаев проявляется внезапной одышкой. Кроме того, возможны боль в боку, усиливающаяся при дыхании, кровохарканье, признаки сердечной недостаточности, шум трения плевры, притупление перкуторного звука. На рентгенограммах грудной клетки выявляются локальное обеднение легочного рисунка и высокое стояние левого или правого купола диафрагмы. Диагноз можно заподозрить при наличии предрасполагающих факторов: ТЭЛА в анамнезе, сердечной недостаточности, злокачественных новообразований, тромбофлебита.
г. Аспирацию желудочного содержимого можно заподозрить при нарушении глотания, у больных алкоголизмом и эпилепсией, а также при выявлении ателектазов.
д. Карциноидный синдром сопровождается приступами одышки у 20—30% больных. От бронхиальной астмы его легко отличить по следующим признакам: приливам, водянистому стулу и боли в животе.
4. Лабораторные исследования
а. Измерение ОФВ1, ЖЕЛ и пиковой объемной скорости до и после п/к или ингаляционного применения бронходилататоров. У больных с тяжелыми приступами бронхиальной астмы ОФВ1 обычно составляет не более 15—30% исходного значения (менее 0,7 л), ЖЕЛ — не более 30—50% исходного значения, а пиковая объемная скорость — менее 100 л/мин (у взрослых). Незначительное повышение ОФВ1 (менее чем на 0,3 л) и пиковой объемной скорости (менее чем на 60 л/мин) после применения бронходилататоров у этих больных свидетельствует о высоком риске повторного тяжелого приступа бронхиальной астмы. Эти больные нуждаются в госпитализации. При тяжелых приступах бронхиальной астмы лечение в стационаре продолжают до тех пор, пока ОФВ1 (у взрослых) не достигнет 2,1 л, а пиковая объемная скорость — 300 л/мин.
б. Исследование газов артериальной крови. При тяжелых приступах бронхиальной астмы paO2 может быть ниже 60 мм рт. ст., тогда как paCO2 остается нормальным (38—42 мм рт. ст.), или слегка повышается из-за гиповентиляции. При легких и среднетяжелых приступах бронхиальной астмы, напротив, наблюдается незначительное снижение paO2 и выраженное снижение paCO2, что приводит к дыхательному алкалозу, затем через некоторое время может развиться гиперхлоремический ацидоз, обусловленный компенсаторным снижением реабсорбции бикарбоната почками и повышением реабсорбции ионов водорода и хлора. При выраженной обструкции бронхов, усталости дыхательных мышц и угнетении дыхательного центра развивается гиповентиляция, которая приводит к респираторному ацидозу. При тяжелых приступах бронхиальной астмы из-за метаболического (BE 42 мм рт. ст.) ацидоза снижается pH артериальной крови. У детей риск ацидоза при тяжелом приступе бронхиальной астмы выше, чем у взрослых. При астматическом статусе наблюдается метаболический ацидоз, обусловленный накоплением лактата из-за значительного увеличения работы дыхания и уменьшения венозного возврата, сердечного выброса и перфузии тканей, вызванных перерастяжением легких.
При астматическом статусе необходимо регулярно исследовать газы артериальной крови. Если paCO2 при поступлении составляет 50—60 мм рт. ст. и через 8 ч после начала лечения не опускается ниже 50 мм рт. ст. или превышает 60 мм рт. ст. при поступлении, показаны интубация трахеи и ИВЛ. Вместо исследования газов артериальной крови можно часто измерять пиковую объемную скорость и ОФВ1, поскольку эти показатели позволяют косвенно судить о наличии респираторного ацидоза, он развивается лишь при снижении пиковой объемной скорости ниже 130 л/мин. Увеличение пиковой объемной скорости (даже при исходном уровне менее 130 л/мин) считается хорошим прогностическим признаком: гиперкапния в этом случае обычно не возникает.
в. Рентгенография грудной клетки. Обычно выявляются лишь повышенная прозрачность легочных полей и расширение грудной клетки. Иногда видны ателектазы. Основная цель рентгенографии грудной клетки при астматическом статусе — выявление осложнений: пневмоторакса, пневмомедиастинума, сегментарных и долевых ателектазов, а также исключение пневмонии, ТЭЛА, заболеваний сердца, которые могли бы привести к сердечной недостаточности.
г. Общий анализ крови. Примерно у 50% больных число лейкоцитов повышается до 15 000 мкл –1 , что может быть следствием лечения адреналином и кортикостероидами. При инфекции и выраженной дегидратации лейкоцитоз обычно более значительный. Значительное повышение числа эозинофилов (до 1000—1500 мкл –1 ) указывает на аллергическую природу обострения. При инфекции наблюдается умеренная эозинофилия. Снижение числа эозинофилов до 50—100 мкл –1 на фоне лечения кортикостероидами свидетельствует об их эффективности, при сохранении эозинофилии необходимо увеличение дозы препаратов.
д. Концентрацию теофиллина в сыворотке определяют для подбора дозы препарата.
е. Исследование мокроты. До лечения из-за большого количества слизи мокрота обычно густая, непрозрачная и вязкая. Сначала проводят микроскопию нативного мазка мокроты. Большое число эозинофилов свидетельствует о ведущей роли аллергических реакций, а нейтрофилов — о ведущей роли инфекции в развитии приступа. Для определения возбудителя производят окраску мазка мокроты по Граму и посев. Бактериальной инфекцией дыхательных путей обусловлено примерно 5% приступов бронхиальной астмы у взрослых.
ж. ЭКГ в 12 отведениях проводят пожилым больным. При тяжелой бронхиальной астме возникает легочная гипертензия, для которой характерны сдвиг электрической оси сердца вправо, гипертрофия правого желудочка и блокада правой ножки пучка Гиса. Применение бета-адреностимуляторов и теофиллина в больших дозах может сопровождаться аритмиями. Особенно высок риск аритмий при гипоксемии и нарушениях кислотно-щелочного равновесия. У пожилых больных астматический статус может осложниться ишемией и инфарктом миокарда.
5. Признаки тяжелой дыхательной недостаточности
б. Выраженная усталость дыхательных мышц.
в. Отсутствие дыхательных шумов.
е. ОФВ1 0,6 л, пиковая объемная скорость сальбутамола , 0,5 мл в 1—3 мл физиологического раствора, или 5% раствора орципреналина , 0,2—0,3 мл в 1—3 мл физиологического раствора, с помощью распылителя ингаляционных растворов. При необходимости назначают ИВЛ с пассивным выдохом, во время которой каждые 1—2 ч проводят ингаляции 100% кислорода. Если ингаляционные бронходилататоры неэффективны, вводят раствор адреналина 1:1000, 0,3 мл п/к, или тербуталин , 0,25 мг п/к, при необходимости инъекцию повторяют через 15—20 мин. При выраженной обструкции бронхов (ОФВ1 не более 35% от исходного) ингаляции бета-адреностимуляторов оказывают более выраженное бронходилатирующее действие, чем введение адреналина п/к. Для усиления эффекта ингаляционные бета-адреностимуляторы назначают в сочетании с бета-адреностимуляторами для приема внутрь, например тербуталином , 2,5—5,0 мг внутрь каждые 8 ч, сальбутамолом , 2—4 мг внутрь каждые 8 ч, или орципреналином , 10—20 мг внутрь каждые 6 ч.
3. Аминофиллин и теофиллин сначала назначают в насыщающей дозе, а затем проводят длительную инфузию в периферическую вену. Дозы указаны в гл. 7, п. V.Б.1.б и табл. 7.4 . В центральные вены теофиллин и аминофиллин не вводят. Улучшение после введения насыщающей дозы аминофиллина обычно наступает через 15 мин. Назначение аминофиллина в поддерживающей дозе без предварительного введения насыщающей вызывает улучшение только через несколько часов. Концентрацию теофиллина в сыворотке определяют в следующих случаях.
а. Перед назначением теофиллина в насыщающей дозе, если с момента последнего применения препарата прошло не более 12—24 ч.
б. Через 1—2 ч после применения теофиллина в насыщающей дозе, для оценки изменения его концентрации в сыворотке. Ожидаемый прирост концентрации составляет 2 мкг/мл на 1 мг/кг насыщающей дозы. Если концентрация теофиллина в сыворотке ниже терапевтической (8—20 мкг/мл), дополнительно вводят половину насыщающей дозы.
в. Во время длительной в/в инфузии — концентрацию теофиллина в сыворотке определяют каждые 12—24 ч.
г. Через 4—6 ч после изменения дозы или режима введения теофиллина .
д. При появлении признаков интоксикации. Зависимость токсического действия теофиллина от его концентрации в сыворотке представлена в табл. 7.3 . При повышении концентрации теофиллина в сыворотке сначала, как правило, появляются желудочно-кишечные нарушения (обычно при концентрации менее 20 мкг/мл), затем аритмии (при концентрации 20—40 мкг/кг) и только после этого эпилептические припадки (при концентрации теофиллина в сыворотке более 40 мкг/мл). Аритмии могут сопровождаться падением АД и остановкой кровообращения, эпилептические припадки, вызванные теофиллином , примерно в 50% случаев приводят к смертельному исходу. У детей летальность меньше, хотя эпилептические припадки наблюдаются чаще. Во избежание завышенных результатов кровь для исследования концентрации теофиллина забирают из вены, удаленной от места введения препарата.
е. Прием теофиллина внутрь так же эффективен, как в/в введение. Если больной уже принимает теофиллин внутрь и у него нет рвоты, то теофиллин в/в не назначают. В этом случае можно продолжить прием препарата внутрь. Для этого лучше использовать препараты теофиллина длительного действия. Дозу теофиллина для приема внутрь также подбирают под контролем его концентрации в сыворотке. Если концентрация теофиллина в сыворотке ниже терапевтической, назначают раствор теофиллина внутрь (80 мг в 15 мл 20% этанола). Для повышения концентрации теофиллина в сыворотке на 2 мкг/мл этот препарат назначают в дозе 1 мг/кг.
4. Кортикостероиды. Раннее применение кортикостероидов при тяжелом приступе бронхиальной астмы способствует быстрому его прекращению, уменьшает риск осложнений, а также снижает необходимость госпитализации. Кортикостероиды показаны в следующих случаях: 1) в отсутствие стойкого улучшения через 1—2 ч после начала интенсивной терапии; 2) при лечении кортикостероидами в течение последнего месяца; 3) при длительном (не менее 2 нед) применении кортикостероидов в течение предшествующего года. Кортикостероиды назначают в средних и высоких дозах. Так, доза гидрокортизона для взрослых колеблется от 200 мг в/в 4 раза в сутки до 4—6 мг/кг каждые 4—6 ч, доза метилпреднизолона — от 60 мг до 250 мг в/в каждые 6 ч. Доза метилпреднизолона для детей составляет 1—2 мг/кг в/в каждые 6 ч. Если через 24 ч после начала лечения существенного улучшения не наступает, дозу удваивают каждые 24 ч до максимально допустимой.
5. В/в инфузии жидкости. В среднем во время приступа бронхиальной астмы теряется около 5% общего объема жидкости. Применяют 5% раствор глюкозы и 0,22—0,45% раствор хлорида натрия . Инфузию жидкости продолжают в течение 6—12 ч, затем по возможности переходят на прием жидкости внутрь. Во избежание перегрузки объемом необходимо следить за количеством введенной жидкости и ее потерями. Особенно осторожно следует проводить инфузионную терапию при сердечно-сосудистых заболеваниях.
6. Антибиотики назначают при вторичной бактериальной инфекции (см. гл. 7, п. V.Б.10 ).
7. Бикарбонат натрия в/в назначают при ацидозе в тех случаях, когда неэффективны другие методы лечения. При ацидозе снижается чувствительность бета-адренорецепторов к эндогенным и экзогенным катехоламинам. При нормализации функции внешнего дыхания выработка молочной кислоты снижается, а накопившийся лактат быстро метаболизируется в печени, поэтому при применении бикарбоната натрия метаболический ацидоз следует компенсировать не более чем наполовину. Алкалоз, вызванный передозировкой бикарбоната натрия , проявляется аритмиями, артериальной гипотонией, угнетением дыхательного центра. Дозу бикарбоната натрия (ммоль) рассчитывают по следующей формуле: 0,3 вес тела (кг) BE (мэкв/л).
В отсутствие респираторного ацидоза или алкалоза бикарбонат натрия в этой дозе повышает, но не нормализует pH.
8. Санация бронхов. Откашливание способствует эффективному отделению мокроты при небольших затратах энергии. Для этого после неполного вдоха больной должен сделать несколько кашлевых толчков, пытаясь вытолкнуть мокроту из нижних отделов легких. Больного предупреждают, что он должен избегать перенапряжения, поскольку оно усиливает бронхоспазм и ухудшает состояние. Если мокрота при откашливании отделяется с трудом, проводят постуральный дренаж, перкуссионный и вибрационный массаж грудной клетки. Если эти процедуры усиливают бронхоспазм, их отменяют. Если мокрота очень густая, для облегчения ее отхождения проводят ингаляции теплых растворов, например 0,45% раствора хлорида натрия в течение 20—30 мин (см. гл. 7, п. V.Б.8 ). Поскольку капли аэрозоля могут вызвать рефлекторный бронхоспазм, до или во время ингаляции солевого раствора назначают ингаляционные бронходилататоры. При выраженном бронхоспазме ингаляцию солевых растворов прекращают. Ультразвуковые распылители ингаляционных растворов обычно не применяют, поскольку в них образуются мелкие капли жидкости, которые часто вызывают бронхоспазм.
9. Поддерживающее лечение в стационаре. Дозы и режим введения препаратов подбираются индивидуально, в зависимости от состояния больного. Для оценки состояния регулярно проводят: 1) исследование газов артериальной крови, особенно если исходно paCO2 превышало 40 мм рт. ст., а paO2 было менее 60 мм рт. ст., 2) измерение ОФВ1 с помощью портативного спирометра и пиковой объемной скорости с помощью индивидуального пневмотахометра до и после применения ингаляционных бронходилататоров, 3) ежедневное определение абсолютного числа эозинофилов в крови для оценки эффективности кортикостероидов. Так, если в течение 24 ч абсолютное число эозинофилов не опускается ниже 50 мкл –1 , дозу кортикостероидов увеличивают. В отсутствие быстрого и стойкого повышения пиковой объемной скорости в ответ на ингаляцию бронходилататора показаны кортикостероиды в высоких дозах, частое применение ингаляционных бета-адреностимуляторов и в/в введение аминофиллина или теофиллина .
10. Транквилизаторы обычно не назначают, особенно при нормальном или повышенном paCO2, так как они угнетают дыхательный центр. При выраженном беспокойстве применяют диазепам , 2—5 мг внутрь 4 раза в сутки, или лоразепам , 1—2 мг внутрь 3 раза в сутки, или алпразолам , 0,25—0,50 мг внутрь 3 раза в сутки, или гидроксизин , 25 мг внутрь 3 раза в сутки. Эти препараты следует назначать с крайней осторожностью.
11. Лечение дыхательной недостаточности. Если лечение астматического статуса начато своевременно, интубации трахеи и ИВЛ не требуется. Однако в некоторых случаях, несмотря на лечение, дыхательная недостаточность прогрессирует: paCO2 повышается до 50—60 мм рт. ст. и более, pH опускается ниже 7,25. При этом возникает заторможенность, которая затрудняет применение ингаляционных бронходилататоров и санацию бронхов. Избыточная работа дыхания приводит к усталости дыхательных мышц и, как следствие, к еще большему ухудшению вентиляции. Интубация трахеи и ИВЛ в этом случае снижает работу дыхания, обеспечивает эффективную вентиляцию легких и способствует постепенной нормализации paCO2 и pH. Для нормализации paCO2 обычно достаточна подача дыхательной смеси, содержащей не более 40% кислорода. Дети младшего возраста нуждаются в ИВЛ чаще, чем взрослые, так как у них чаще наблюдается тяжелая гиповентиляция (бронхи у детей уже, чем у взрослых).
а. Длительная в/в инфузия изопреналина может заменить интубацию трахеи и ИВЛ и особенно эффективна при лечении дыхательной недостаточности у детей. Изопреналин вызывает аритмии, которые чаще отмечаются у взрослых. В последнее время для длительной инфузии вместо изопреналина стали применять тербуталин . В Европе в этих случаях назначают сальбутамол (не выпускается в США в виде растворов для в/в введения). В/в введение адреностимуляторов применяется у детей. Согласно рекомендациям Национального института здоровья США по лечению тяжелых приступов бронхиальной астмы, взрослым в/в инфузии адреностимуляторов противопоказаны. В/в инфузию проводят по следующей схеме.
1) Для инфузии готовят раствор изопреналина с концентрацией 10 мкг/мл. Инфузию изопреналина с помощью инфузионного насоса начинают со скоростью 0,1 мкг/кг/мин. Дозу увеличивают постепенно — на 0,1 мкг/кг/мин каждые 10—15 мин до улучшения газового состава артериальной крови, повышения ЧСС до 200 мин –1 или развития аритмий. Инфузию изопреналина проводят в реанимационном отделении под контролем ЭКГ.
2) Каждые 15—30 мин во время увеличения дозы изопреналина измеряют paO2 и paCO2 и проводят мониторинг АД через артериальный катетер.
3) Во время инфузии изопреналина ингаляции адреностимуляторов прекращают. В/в введение аминофиллина и кортикостероидов продолжают (их вводят через отдельный венозный катетер). Следует помнить, что теофиллин может усиливать побочные действия адреностимуляторов.
4) При прогрессирующей дыхательной недостаточности показаны интубация трахеи и ИВЛ.
5) При улучшении состояния и стойком снижении paCO2 до уровня, не превышающего 45 мм рт. ст., дозу изопреналина снижают каждый час на 0,1 мкг/кг/мин. Улучшение обычно наступает после 24—48 ч инфузии изопреналина со скоростью 0,25—0,75 мкг/кг/мин (у детей — до 3,5 мкг/кг/мин). После каждой дозы измеряют paCO2. Если paCO2 повышается на 5 мм рт. ст., дозу изопреналина увеличивают.
б. Тербуталин в/в обычно назначают детям, изредка взрослым. Насыщающая доза препарата составляет 10 мкг/кг в течение 10 мин. Затем начинают длительную инфузию со скоростью 0,1 мкг/кг/мин. При необходимости скорость инфузии можно повышать на 0,1 мкг/кг/мин до максимальной — 3—6 мкг/кг/мин. При этом обязательно проводят мониторинг ЭКГ. В/в введение тербуталина можно заменить на длительную ингаляцию сальбутамола со скоростью 5 мг/ч (не более 15 мг/ч). Для этого 20 мл раствора сальбутамола для ингаляций (100 мг сальбутамола ) разводят в 480 мл физиологического раствора. Ингаляцию сальбутамола с помощью распылителя проводят в течение длительного времени через маску одновременно с ингаляцией кислорода со скоростью 5—8 л/мин. Если больной интубирован, ингаляцию сальбутамола с помощью распылителя проводят через респиратор.
в. Осложнения интубации трахеи и ИВЛ. Высокое давление на вдохе при проведении ИВЛ у больных с бронхоспазмом может стать причиной подкожной эмфиземы, пневмоторакса и пневмомедиастинума и, как следствие, нарушения гемодинамики. К осложнениям приводит и неправильная интубация трахеи. Так, при интубации правого главного бронха возможны ателектазы, при поврежденной манжетке — гиповентиляция и растяжение желудка. К осложнениям ИВЛ относятся также ателектазы, возникающие вследствие закупорки дыхательных путей слизью, подскладочный стеноз, пневмония и сепсис.
1) Для мониторинга АД и забора проб крови устанавливают постоянный артериальный катетер. Непрерывно регистрируют насыщение гемоглобина артериальной крови кислородом с помощью пульс-оксиметра.
2) При проведении ИВЛ у больных с бронхоспазмом часто требуется в/в введение морфина , а иногда и миорелаксантов, поскольку отсутствие синхронизации между самостоятельным и принудительным дыханием снижает эффективность вентиляции и усиливает ацидоз.
а) Морфина сульфат вводят в дозе 3—5 мг (детям — 0,1—0,2 мг/кг) в/в в течение 4—5 мин, одновременно регистрируя АД, при необходимости введение препарата повторяют через 5—10 мин.
б) При артериальной гипотонии, вызванной морфином , применяют налоксон , 0,1—0,2 мг (у детей — 0,01 мг/кг) в/в каждые 2—3 мин до нормализации АД.
в) Если морфин не повышает эффективность вентиляции, назначают панкуроний , 0,04 мг/кг в/в, при необходимости препарат вводят повторно через 4—5 мин. При повторном нарушении синхронизации дыхания вводят дополнительные дозы морфина или панкурония . Эти препараты могут назначаться одновременно.
г) Транквилизаторы, например диазепам , 2—5 мг в/в каждые 4—6 ч, или лоразепам , 1—2 мг в/в каждые 2 ч, также угнетают самостоятельное дыхание. Дозы транквилизаторов и морфина указаны для взрослых.
д) Если с помощью морфина и панкурония не удается добиться оптимальной вентиляции легких, в/в вводят тербуталин (см. гл. 7, п. VII.Г.11.б ).
г. ИВЛ с ограничением объема при бронхоспазме более эффективно обеспечивает вентиляцию, чем ИВЛ с ограничением давления.
1) В начале ИВЛ дыхательный объем должен составлять 8—12 мл/кг, а частота вдуваний — 10—12 мин –1 . При проведении ИВЛ у детей частоту вдуваний повышают. Ее подбирают так, чтобы установленный дыхательный объем обеспечивал максимальную вентиляцию. При выраженной обструкции бронхов, для того чтобы предупредить чрезмерное повышение давления на вдохе, снижают частоту вдуваний. Для снижения давления на вдохе можно также уменьшить дыхательный объем, одновременно слегка увеличив частоту вдуваний.
2) Перед интубацией трахеи, сразу после нее и в начале ИВЛ дают 100% кислород.
3) Исследование газов артериальной крови проводят в течение первых 30 мин после начала ИВЛ и любых изменений ее параметров. Изменение параметров ИВЛ необходимо для постепенного снижения paCO2 со скоростью 5—10 мм рт. ст./ч и поддержания paO2 на уровне 60 мм рт. ст. и выше.
4) При респираторном ацидозе следует избегать быстрого снижения paCO2, это предотвращает метаболический алкалоз.
5) Эффективность новых моделей респираторов, которые позволяют проводить ИВЛ с управляемым давлением и ИВЛ с поддерживающим давлением, при астматическом статусе не доказана. Традиционно применяемая ИВЛ с ограничением объема позволяет снизить давление на вдохе и уменьшить риск баротравмы.
д. Во время ИВЛ проводят следующие лечебные мероприятия.
1) Аспирацию слизи через эндотрахеальную трубку следует проводить с соблюдением правил асептики, быстро, с минимальной травматизацией слизистой трахеи и бронхов. Частота этой процедуры должна быть достаточна для поддержания проходимости дыхательных путей.
2) Чтобы облегчить отделение вязкой мокроты, к увлажненному газу, подаваемому респиратором, добавляют водяной пар или аэрозоль солевого раствора. При усилении бронхоспазма такие ингаляции отменяют.
3) Если дыхательные пути заполнены обильной, вязкой мокротой, назначают ингаляции ацетилцистеина , 2—3 мл 10% раствора каждые 3—4 ч, и бронходилататоров. После ингаляции ацетилцистеина проводят аспирацию слизи, постуральный дренаж и перкуссионный массаж грудной клетки. Ацетилцистеин значительно уменьшает вязкость мокроты, однако он обычно плохо переносится, поскольку раздражает дыхательные пути и вызывает бронхоспазм.
4) При тяжелых приступах бронхиальной астмы, когда неэффективны бронходилататоры, кортикостероиды и обычные мероприятия по санации бронхов и требуется длительная ИВЛ, проводят бронхоскопию и бронхоальвеолярный лаваж. Бронхоальвеолярный лаваж требует общей анестезии, не всегда эффективен и сопровождается целым рядом осложнений, поэтому его применяют лишь в крайних случаях.
е. После восстановления проходимости дыхательных путей, нормализации газового состава артериальной крови и кислотно-щелочного равновесия ИВЛ прекращают, больного как можно раньше экстубируют. Интубация трахеи делает невозможным глотание и кашель и поэтому препятствует эффективному удалению мокроты.
1) Показания к прекращению ИВЛ
а) ЖЕЛ у взрослых более 1000 мл, у детей более 15 мл/кг.
б) Восстановление нормальной оксигенации артериальной крови при концентрации кислорода во вдыхаемой смеси ниже 40%.
в) Отношение объема мертвого пространства к дыхательному объему менее 60%.
г) Максимальное отрицательное давление на вдохе не более 25 см вод. ст.
д) Минутный объем дыхания у взрослых менее 10 л/мин. У детей он должен превышать нормальное значение не более чем на 50%.
е) При переходе на самостоятельное дыхание взрослый больной способен увеличить минутный объем дыхания до 20 л/мин, ребенок — до объема, в 3 раза превышающего нормальный. Дыхательный объем у детей в норме составляет 10 мл/кг. Минутный объем дыхания у новорожденных в норме составляет 30—50 л/мин, у детей младшего и старшего возраста — 18—30 л/мин. В приложении I, п. Б приведена номограмма для определения дыхательного объема у детей и взрослых.
2) Перед экстубацией проводят санацию бронхов. Паралич дыхательных мышц устраняют введением атропина , 0,6—1,2 мг в/в (детям — 0,02 мг/кг), и неостигмина , 0,5—2,0 мг в/в (детям — 0,07 мг/кг). Препараты вводят в отдельных шприцах, неостигмин вводят медленно. Перед экстубацией через T-образный адаптер, подсоединенный к эндотрахеальной трубке, вводят увлажненный кислород со скоростью 5—10 л/мин.
12. Переход на самостоятельное дыхание нередко бывает затруднен, поскольку длительная ИВЛ приводит к психологической зависимости от респиратора и слабости дыхательных мышц. Оценить степень психологической зависимости можно по реакции больного на попытку прекращения ИВЛ, а также по изменению газового состава артериальной крови. Нарушения дыхания, вызванные слабостью дыхательных мышц, сходны с нарушениями, наблюдаемыми при тяжелых ХОЗЛ. Для облегчения перехода на самостоятельное дыхание применяют перемежающуюся принудительную ИВЛ, при которой подача газовой смеси сочетается с самостоятельным дыханием. Больные в этом случае постепенно избавляются от психологической зависимости от респиратора, обретают уверенность в способности дышать самостоятельно, имеют время для тренировки дыхательных мышц и постепенного восстановления. ИВЛ с поддерживающим давлением позволяет увеличить дыхательный объем без дополнительных усилий дыхательных мышц. Этот режим может применяться вместо перемежающейся принудительной ИВЛ или в дополнение к ней. При ИВЛ с поддерживающим давлением больные самостоятельно устанавливают частоту вдуваний, дыхательный объем, скорость воздушного потока и поэтому чувствуют себя более уверенно. При переходе на самостоятельное дыхание устанавливают такой уровень поддерживающего давления, который обеспечивает дыхательный объем 5—7 мл/кг. При хорошей переносимости частоту вдуваний при перемежающейся принудительной ИВЛ медленно снижают до 1—2 мин –1 , а поддерживающее давление — на 1—2 см вод. ст. каждые 2—4 ч. Экстубацию проводят, когда при оптимальной вентиляции и оксигенации уровень поддерживающего давления составляет 6—8 см вод. ст. Если переход на самостоятельное дыхание затруднен, переходят на ИВЛ в режиме, требующем минимальной работы дыхания.
1. При улучшении состояния, стойком увеличении ОФВ1 и пиковой объемной скорости интервалы между применением ингаляционных бронходилататоров постепенно увеличивают до 4—6 ч. Продолжают назначать адреностимуляторы для приема внутрь.
2. Дозу кортикостероидов для в/в введения постепенно снижают, ежедневно уменьшая ее вдвое до дозы, эквивалентной 40 мг метилпреднизолона . Затем назначают преднизон или метилпреднизолон внутрь и более медленно снижают их дозу.
3. В/в введение аминофиллина или теофиллина прекращают и назначают эти препараты внутрь. Первую дозу препарата для приема внутрь назначают через 3 ч после прекращения в/в инфузии. Обычно применяют препараты теофиллина длительного действия. Их дозу рассчитывают следующим образом: суточную дозу аминофиллина (или эквивалентную дозу теофиллина ) для в/в введения умножают на 0,8 и делят на 2. Полученную дозу назначают каждые 12 ч. Поскольку у детей скорость выведения теофиллина выше, чем у взрослых, препараты длительного действия им назначают каждые 8—12 ч (см. гл. 7, п. V.Б.1.б.1 ). Во время поддерживающего лечения теофиллином определяют его максимальную (примерно через 5 ч после приема препарата длительного действия) и минимальную (перед приемом следующей дозы) концентрацию в сыворотке. Во время подбора дозы концентрацию теофиллина в сыворотке определяют каждые 2—3 сут.
4. Следует помнить, что проявления приступа бронхиальной астмы могут исчезнуть даже на фоне сохраняющейся обструкции бронхов, при которой ОФВ1 на 50%, а средняя объемная скорость середины выдоха на 70% ниже нормы (см. рис. 7.4 ). В связи с этим лечение продолжают и после клинического улучшения, ориентируясь на показатели функции внешнего дыхания.
5. Во время лечения в стационаре обязательно рассказывают больному о его заболевании, основных принципах его лечения и профилактики. Для предупреждения повторных приступов бронхиальной астмы необходимо диспансерное наблюдение больных.
источник