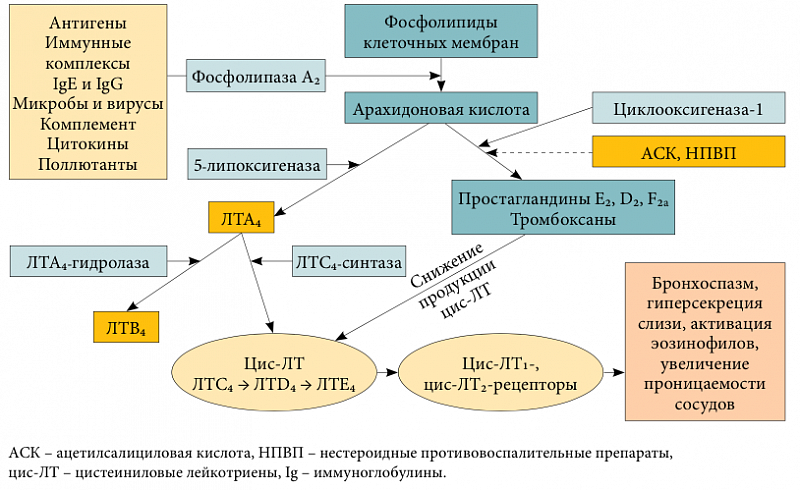
Дополнительные сведения: Лекарственные средства влияющие на бронхиальную проходимость
Для лечения бронхиальной астмы используются препараты базисной терапии, воздействующие на механизм заболевания, посредством которых пациенты контролируют астму, и симптоматические препараты, влияющие только на гладкую мускулатурубронхиального дереваи снимающие приступ.
К препаратам симптоматической терапииотносятбронходилятаторы:
К препаратам базисной терапииотносят
антагонисты лейкотриеновых рецепторов
Если не принимать базисную терапию, со временем будет расти потребность в ингаляции бронходилататоров (симптоматических средств). В этом случае и в случае недостаточности дозы базисных препаратов рост потребности в бронходилататорах является признаком неконтролируемого течения заболевания [23] .
К кромонам относят кромогликат натрия(Интал) инедокромил натрия(Тайлед). Эти средства показаны в качестве базисной терапии бронхиальной астмы интермиттирующего и лёгкого течения. Кромоны уступают по своей эффективности ИГКС [24] . Так как существуют показания для назначения ИГКС уже при лёгкой степени бронхиальной астмы [19] , кромоны постепенно вытесняются более удобными в использовании ИГКС. Не оправдан также переход на кромоны с ИГКС при условии полного контроля над симптомами минимальными дозами ИГКС [25] .
При астме применяются ингаляционные глюкокортикостероиды, которым не свойственно большинство побочных действий системных стероидов. При неэффективности ингаляционных кортикостероидов добавляют глюкокортикостероиды для системного применения.
ИГКС — основная группа препаратов для лечения бронхиальной астмы. Ниже представлена классификация ингаляционных глюкокортикостероидов в зависимости от химической структуры:
будесонид(Пульмикорт, Бенакорт, Буденит Стери-Неб)
беклометазона дипропионат(Бекотид, Беклоджет, Кленил, Беклазон Эко, Беклазон Эко Лёгкое Дыхание)
Противовоспалительный эффект ИГКС связан с подавлением деятельности клеток воспаления, уменьшением продукциицитокинов, вмешательством в метаболизмарахидоновой кислотыи синтезпростагландиновилейкотриенов, снижением проницаемости сосудов микроциркуляторного русла, предотвращением прямой миграции и активации клеток воспаления, повышением чувствительности b-рецепторов гладкой мускулатуры. ИГКС также увеличивают синтез противовоспалительного белка липокортина-1, путём ингибированияинтерлейкина-5увеличиваютапоптозэозинофилов, тем самым снижая их количество, приводят к стабилизации клеточных мембран. В отличие от системных глюкокортикостероидов, ИГКСлипофильны, имеют короткийпериод полувыведения, быстро инактивируются, обладают местным (топическим) действием, благодаря чему имеют минимальные системные проявления. Наиболее важное свойство — липофильность, благодаря которому ИГКС накапливаются в дыхательных путях, замедляется их высвобождение из тканей и увеличивается их сродство к глюкокортикоидному рецептору. Лёгочная биодоступность ИГКС зависит от процента попадания препарата в лёгкие (что определяется типом используемого ингалятора и правильностью техники ингаляции), наличия или отсутствия носителя (лучшие показатели имеют ингаляторы, не содержащие фреон) и от абсорбции препарата в дыхательных путях.
До недавнего времени главенствующией концепцией назначения ИГКС была концепция ступенчатого подхода, что означает что при более тяжёлых формах заболевания назначаются более высокие дозы ИГКС.
Основой терапии для длительного контроля воспалительного процесса являются ИГКС, которые применяются при персистирующей бронхиальной астме любой степени тяжести и по сей день остаются средствами первой линии терапии бронхиальной астмы. Согласно концепции ступенчатого подхода: «Чем выше степень тяжести течения БА, тем большие дозы ингаляционных стероидов следует применять». В ряде исследований показано, что у пациентов, начавших лечение ИГКС не позже 2 лет от начала заболевания, отмечены существенные преимущества в улучшении контроля над симптомами астмы, по сравнению с начавшими такую терапию по прошествии 5 лет и более [19] .
Существуют фиксированные комбинации ИГКС и пролонгированных β2-адреномиметиков, сочетающие в себе средство базисной терапии и симптоматическое средство. Согласно глобальной стратегии GINA, фиксированные комбинации являются наиболее эффективными средствами базисной терапии бронхиальной астмы, так как позволяют снимать приступ и одновременно являются лечебным средством [3] . ВРоссиинаибольшей популярностью пользуются две такие фиксированные комбинации:
сальметерол+флутиказон(Серетид 25/50, 25/125 и 25/250 мкг/доза, Серетид Мультидиск 50/100, 50/250 и 50/500 мкг/доза, Тевакомб 25/50, 25/125 и 25/250 мкг/доза)
формотерол+будесонид(Симбикорт Турбухалер 4,5/80 и 4,5/160 мкг/доза, В состав препарата Серетид входит салметерол в дозе 25 мкг/доза в дозированном аэрозольном ингаляторе и 50 мкг/доза в аппарате «Мультидиск». Максимально-допустимая суточная доза салметерола — 100 мкг, то есть максимальная кратность применения Серетида составляет 2 вдоха 2 раза для дозированного ингалятора и 1 вдох 2 раза для приспособления «Мультидиск». Это даёт Симбикорту преимущество в том случае, если необходимо увеличить дозу ИГКС. Симбикорт содержит формотерол,максимально-допустимая суточная дозакоторого составляет 24 мкг, делает возможным ингалироваться Симбикортом до 8 раз в сутки. В исследовании SMART выявлен риск, связанный с применением салметерола по сравнению с плацебо. Кроме того, бесспорным преимуществом формотерола является и то, что он начинает действовать сразу после ингаляции, а не через 2 часа, как салметерол [26] .
источник
Базисное лечение бронхиальной астмы необходимо для подавления воспаления в дыхательных путях, снижения бронхиальной гиперреактивности, уменьшения бронхиальной обструкции.
Терапевтический курс разрабатывается конкретно под каждого больного, с учетом тяжести болезни, возраста и иных индивидуальных особенностей. Больному астмой прописываются лекарства, необходимые для устранения воспалительного процесса, локализованного в дыхательных путях.
Лечение патологии базируется на применении средств, купирующих астматические приступы, а также препаратов базисной терапии. Вторая группа лекарств призвана оказать воздействие на патогенетический механизм болезни.
Бронхиальная астма – хроническая патология, при которой наблюдается развитие воспалительного процесса в дыхательных путях. Астматики сталкиваются с сужением бронхов, вызванным влиянием внешних и внутренних факторов. Патология проявляется в виде:
- одышки;
- головных болей;
- дыхательной недостаточности;
- свистящих хрипов;
- ощущения заложенности в области грудной клетки;
- постоянного кашля.
Всего в мире насчитывается около 230 000 000 астматиков. В развитых странах применяются схожие принципы лечения патологии, позволяющие многим пациентам достичь стадии устойчивой ремиссии при соблюдении всех врачебных рекомендаций.
Астматикам показана базисная терапия, если бронхиальная астма вызывает ухудшение общего состояния больного. Главная цель при лечении заболевания заключается в том, чтобы не допустить перехода патологии в тяжелую форму, когда она выходит из-под контроля, и развиваются осложнения.
Возможные осложнения из-за активного развития болезни: пневмоторакс, эмфизема, беттолепсия, ателектаз.
Болезнь может быть различной степени тяжести – для каждой из них существует своя схема терапии. При лечении бронхиальной астмы врачи должны решить следующие терапевтические задачи:
- оценка состояния больного и воздействие на проявляющиеся симптомы;
- сведение к минимуму количества приступов (вне зависимости от их интенсивности);
- минимизация побочных эффектов от используемых для базисного лечения лекарственных препаратов;
- обучение астматика навыкам самопомощи при развитии приступов;
- контроль реакции организма пациента на использованные препараты, корректировка назначения, если требуется.
Принято выделять 5 основных ступеней развития бронхиальной астмы, в соответствии с которыми разрабатывается схема лечения:
- На начальной стадии развития патологии больному обычно назначаются бета-адреномиметики короткого действия. Это симптоматические препараты. С их помощью расширяются бронхи, благодаря чему снимается приступ.
- На второй ступени, по решению врача, может быть использовано одно или несколько лекарственных средств. Эти лекарства астматик должен принимать систематически, чтобы остановить развитие воспалительного процесса в бронхах. Обычно назначаются глюкокортикостероиды в виде ингаляций и бета-адреномиметики. Лечение начинается с минимальных доз.
- На третьей ступени в дополнение к уже назначенным лекарствам используются бета-адреномиметики продолжительного действия. Эти препараты расширяют бронхи, поэтому больному проще дышать и говорить.
- На четвертой ступени у пациентов заболевание протекает тяжело, поэтому врачи назначают системные гормональные противовоспалительные препараты. Такие лекарства хорошо справляются с астматическими приступами, но их использование приводит к появлению различных побочных эффектов: диабет, нарушения обмена веществ, синдром отмены и т. д.
Для пятой степени характерно крайне тяжелое состояние пациента. Физическая активность больного ограничена, наблюдается сильная дыхательная недостаточность. Лечение практически всегда проводится в стационаре.
Препараты для базисной терапии бронхиальной астмы должны назначаться врачом, запрещено самостоятельно подбирать себе лекарства. Основные принципы лечения бронхиальной астмы: иммунотерапия и фармакотерапия.
Независимо от возраста и тяжести текущего состояния пациента, лечение начинается с приема небольших доз лекарств. Схема лечения обычно корректируется специалистами с учетом следующих факторов:
- наличие хронических патологий легких;
- текущее состояние астматика (на фоне приема препаратов);
- интенсивность приступов удушья ночью;
- наличие характерных астматических проявлений (одышка, хрипы, кашель);
- результаты анализов;
- продолжительность, частота, выраженность дневных приступов.
При персистирующей астме легкой, средней и тяжелой степени проводится базовая и симптоматическая терапия заболевания.
Обязательно используются бета-адреномиметики (их также называют «ингаляционные 2-агонисты») и другие средства, купирующие приступы и снижающие их число.
Базисная терапия при бронхиальной астме предполагает применение ингаляционных глюкокортикостероидов, системных глюкокортикостероидов, стабилизаторов тучных клеток, лейкотриеновых антагонистов.
Эти препараты для лечения бронхиальной астмы необходимы, чтобы контролировать заболевание, не допустить ухудшения состояния больного.
Глюкокортикостероиды крайне важны для купирования приступов. Они обладают противовоспалительным действием. Использование ингаляционных глюкокортикостероидов позволяет снять обструкцию бронхов за короткий промежуток времени.
К основным плюсам таких ингаляций можно отнести:
- устранение воспалительного процесса в бронхах;
- снижение интенсивности симптоматики заболевания;
- возможность приема сравнительно малых доз препарата;
- сведение к минимуму проникновения действующих веществ лекарства в общий кровоток;
- улучшение проходимости в бронхах.
Ингаляционные глюкокортикостероиды позволяют купировать приступы, но для базисной терапии бронхиальной астмы используются системные глюкокортикостероиды в форме таблеток.
Их назначают, если состояние больного оценивается как среднетяжелое и тяжелое. Эти препараты:
- устраняют спазмы в бронхах;
- улучшают проходимость дыхательных путей;
- устраняют воспалительный процесс;
- уменьшают секрецию мокроты.
Системные глюкокортикостероиды могут быть назначены при тяжелых стадиях заболевания, при ухудшении показателей спирометрии, при отсутствии результатов лечения ингаляционными препаратами и дальнейшем развитии проявлений бронхиальной астмы.
Запрещено самостоятельное применение таких лекарственных средств без назначения врача.
Противовоспалительная терапия бронхиальной астмы включает использование стабилизаторов тучных клеток. Эти препараты назначают больным, у которых наблюдается легкая или средняя тяжесть заболевания.
Стабилизаторы тучных клеток помогают:
- предупредить и устранить аллергию;
- предотвратить возникновение спазмов в бронхах;
- уменьшить воспалительный процесс;
- снизить гиперреактивность бронхов.
Базовая терапия бронхиальной астмы практически всегда включает в себя использование лейкотриеновых антагонистов. Их основная задача – блокирование лейкотриеновых рецепторов и угнетение активности фермента 5-липоксигеназы.
Из-за этих органических соединений происходит развитие спазмов в бронхах вследствие аллергии на различные раздражители.
Эти препараты обладает сильным противовоспалительным действием, подавляют клеточные и неклеточные компоненты воспаления в бронхах, которое вызывается воздействием антигенов. Также они оказывают следующее действие:
- устранение спазмов в бронхах;
- уменьшение образования мокроты;
- устранение инфильтрации и процесса воспаления в бронхиальных слизистых оболочках;
- увеличение проницаемости мелких сосудов в органах дыхания;
- расслабления гладких мышц в органах дыхания.
Базисная терапия при бронхиальной астме предполагает использование нескольких видов препаратов. Лечение обязательно комплексное.
Врачи, разрабатывая схему лечения, должны решить, как будут устранены у пациента проявления бронхиальной астмы. Не менее важная задача – достижение стойкой ремиссии.
Выбирая тип базисной терапии бронхиальной астмы у детей, специалисты учитывают множество факторов: возраст ребенка, давность появления первых астматических признаков, наличие иных хронических заболеваний, текущее состояние маленького пациента.
Также принимаются во внимание симптомы астмы. Они могут проявляться с разной интенсивностью. У детей, у которых диагностирована бронхиальная астма, наблюдается следующая симптоматика:
- хрипы во время дыхания;
- синюшный оттенок кожи в области носогубного треугольника (при приступе);
- ухудшение общего состояния;
- астматические приступы (при наличии внешнего раздражителя или в ночное время);
- кашель, одышка, проблемы с дыханием.
Для лечения детей используются:
- длительно действующие бронходилататоры;
- лекарственные средства с противовоспалительным эффектом.
- ингаляционные глюкокортикоиды.
Базисная терапия астмы показана всем пациентам, у которых диагностировано заболевание (за исключением больных с интермиттирующей астмой). Но некоторые больные отказываются от приема противовоспалительных средств и от любого другого традиционного лечения бронхиальной астмы, предпочитая народные средства.
Народная медицина в терапии бронхиальной астмы имеет право на существование, однако астматикам ни в коем случае нельзя отказываться от приема противовоспалительных препаратов.
Отказ от лечения и отсутствие контроля со стороны лечащего врача практически в 100% случаев приводит к ухудшению состояния пациента, усилению астматических приступов, развитию осложнений (проблемы с сердцем, головные боли и т.п.).
Поэтому между лечащим врачом и астматиком с самого начала лечения должен быть налажен прямой контакт. Важно, чтобы пациент располагал всей необходимой информацией о своем заболевании:
- Что может спровоцировать развитие астматического приступа?
- Как его можно быстро купировать?
- Какие препараты и в каких дозировках могут быть использованы?
- В каких случаях необходимо вызывать скорую помощь?
Каждый астматик должен знать ответы на эти вопросы. Если лечащий врач не провел соответствующую беседу, больной должен самостоятельно проконсультироваться со специалистом, задав ему интересующие вопросы.
Наличие прямого контакта между врачом и пациентом очень важно в случаях, когда проводится лечение маленького ребенка от бронхиальной астмы. Дети не могут сами принять решение, поэтому их родители должны располагать всей необходимой информацией о заболевании.
Лекарственные средства для лечения бронхиальной астмы, применяемые при базисной терапии, назначают врачом в зависимости от степени тяжести заболевания, частоты и выраженности симптоматики, текущего состояния больного.
Терапия в каждом случае строго индивидуальна, поэтому самолечение при развитии бронхиальной астмы, вне зависимости от ее ступени, исключено.
источник
Базисная терапия бронхиальной астмы — это основа всего лечения при этом заболевании. Бронхиальная астма характеризуется развитием хронического воспаления в бронхолегочной системе, которое вовлекает в процесс эозинофилы и тучные клетки.
В том случае, когда пациент предрасположен к негативной симптоматике, возможно развитие обструкции дыхательных путей, которая достаточно часто бывает обратимой в результате медикаментозной терапии или спонтанно. Это может сопровождаться гиперреактивностью дыхательной системы по отношению к внутренним и внешним проявлениям.
Как правило, для проведения основных терапевтических мероприятий используются препараты, которые пациенту необходимо принимать ежедневно для снятия воспалительного бронхиального процесса и расширения бронхиальных просветов.
Тактика контроля и проведение мониторинга заболевания предусматривает выполнение следующих задач, которые позволяют объективно оценить степень тяжести астмы. Наиболее важными задачами являются:
- оценка состояния бронхолегочной функциональности;
- контролирование нарастающей симптоматики;
- предотвращение возможных побочных проявлений при лечении астмы;
- снижение и предотвращение смертности от астматического приступа;
- обучение больного правилам оказания самопомощи в экстренных случаях;
- контролирование провоцирующих факторов, а также предупреждение контактов, являющихся пусковыми механизмами развития астматического приступа;
- выбор необходимой лечебной терапии во время обострения астматического приступа и в стадии ремиссии;
- кроме того, немаловажное значение отводится тщательному наблюдению за поведением пациента и его реакцией на медикаментозное лечение.
Все вышеперечисленные задачи являются основополагающими в терапии астматических заболеваний. Любая форма бронхиальной астмы, за исключением интермиттирующей легкой степени, контролируется с помощью лекарственных средств, чего невозможно добиться при остром развитии бронхоспазма и симптоматики, которая с ним связана.
Противоастматические препараты способны предотвратить воспалительные процессы в бронхах. Они эффективно борются с инфекцией с одновременным контролированием симптоматики. К ним можно отнести:
(Флутиказон, Будесонид, Беклометазон, Триамцинолон, Флунизолид и т.д.)
Терапевтическое действие этих лекарственных средств объясняется, прежде всего, возможность усиления с их помощью выработки β2-адренорецепторов, способных приостановить негативное воздействие аллергенов. Кроме того, кортикостероиды снимают воспалительный процесс и отеки слизистой бронхиальной оболочки с выработкой экссудативного секрета. Отличие этих препаратов от системных заключается в их противовоспалительном эффекте и минимальном количестве побочных проявлений. Препарат дозируется, исходя из тяжести заболевания и общего состояния пациента.
(Метилпреднизолон, Триамцинолон, Преднизолон, Бетаметазон, Дексаметазон и др.)
Эти препараты назначается перорально или инфузионно при осложненном течении заболевания в минимальной дозировке (по предусмотренной схеме), так как они обладают значительными побочными эффектами. Предпочтительно вводить эти лекарственные средства внутривенно. Системные глюкокортикостероиды назначаются при неэффективности остальных способов лечения.
(кислота Кромоглициевая, препараты Недокромил, Интал, а также сложные адреномиметики быстрого воздействия)
Эти вещества обладают специфическим свойством, предотвращающим дегрануляционные процессы тучных клеток, высвобождая гистаминовые вещества. Стабилизаторы обладают способностью к подавлению острых и пролонгированных бронхоспастических ответов на атаку аллергенов. Кроме того, эти препараты уменьшают бронхиальную активность при дыхании в холодное время года, значительно сокращая частоту и продолжительность приступа. Необходимо помнить, что лечение этими средствами должно быть кратковременным, так как они способны вызвать побочные проявления.
Такие препараты значительно снижают необходимость использования β2-адреномиметиков быстрого воздействия. Они относятся к новому поколению противоастматических и противовоспалительных препаратов, применяемых в профилактике развития бронхоспазмов.
Следует учитывать, что основной задачей терапии астмы и тактики ее лечения является контроль и подавление активности воспалительного процесса, что позволяет добиться длительной ремиссии бронхиальной астмы.
Основной целью терапии у детей с бронхиальными заболеваниями является достижение стойкой ремиссии и повышения качества жизни.
Применение базовой терапии определяется следующими критериями:
- частота бронхиальной симптоматики (менее 2 раз в течение недели);
- частота ночных приступов;
- ограничение ежедневной активности;
- необходимость в применении экстренного лечения;
- возможность обострений;
- нормализация внешней дыхательной деятельности.
Фармакотерапия является неотъемлемой частью при лечении бронхиальных заболеваний у детей. Существенного прогресса при лечении астматических заболеваний у детей достигается при использовании базисных препаратов, предназначенных для снятия воспалительного процесса в бронхолегочной системе.
Следует отметить, что противовоспалительные препараты, применяемые в рамках базисной терапии должны использоваться не только при обострении заболевания, но и во время ремиссии в качестве профилактики обострения, что доказывает необходимость длительного лечения.
Оказание неотложной помощи во время легкого астматического приступа назначаются дозирующие ингаляционные препараты (Беротек H, Сальбутамол и т.д.). Эти лекарственные средства лучше всего подходят для детей среднего и старшего возраста при неэффективности других бронхолитиков.
Для младшей возрастной группы рекомендуется применение Атровента или Беродуала. Эти аэрозоли обладают высокой степенью безопасности и могут использоваться во время ночного приступа астмы.
У детей раннего возраста рекомендуется использование дозированных ингаляторов со спейсером или небулайзера. При неэффективности подобранной дозировки лекарственного средства рекомендуется комбинировать бронхолитики с β2-агонистами, а также повысить дозу ИГКС после согласования с лечащим врачом.
В зависимости от степени тяжести астмы для детей от года может назначаться Флутиказона пропионат в ингаляциях не менее 2 раз в течение суток. При легком течении заболевания базовая терапия должна проводиться каждых 4-7 часов на протяжении 1-2 суток.
При этой степени бронхиальной астмы у детей, предпочтительно назначать комбинированные бронхоспазмолитики в аэрозолях (Беродуал). При невозможности ингаляционной терапии рекомендуется в/в введение 2,4% раствора Эуфиллина, разведенного изотоническим раствором Хлорида натрия (5 мг на 1 кг. массы тела ребенка).
Важно! Внутримышечное, ингаляционное и ректальное (свечи) введение Эуфиллина у детей при этой стадии заболевания не используется!
После оценки состояния ребенка (спустя 20 минут) принимается решение о проведении терапии стартовыми бронхоспазмолитиками через каждых 4 часа с постепенным переводом пациента на датирующиеся аэрозоли и бронхолитики пролонгированного воздействия.
Далее базисная противовоспалительная терапия у детей продолжается с использованием Ингакорта, Недокромила натрия, Беклометазона, Кромогликата натрия и Будесонида с постепенным увеличением дозировки в 2 раза в течение недели. Кроме того, рекомендуется использовать противовоспалительный бронхолитик Дитек.
При крайне тяжелой степени развития бронхиальной астмы необходима срочная госпитализация ребенка в отделение интенсивной терапии с дальнейшим проведением экстренной терапии в условиях стационара. На сегодняшний день общепринятым для лечения является «ступенчатый» подход, когда снижение или увеличение объемов терапевтического вмешательства зависит от выраженности симптоматики заболевания.
Немаловажное значение имеет непосредственный контакт с астматиком. Положительное влияние отмечено, когда помимо специфической терапии бронхиальной астмы, пациент обладает дополнительной информацией об этиологии своего заболевания, механизме ее развития и возможных осложнениях.
Для этого рекомендуется проводить небольшие беседы с пациентом, объясняя суть проводимых манипуляций и положительный эффект от их применения. Это позволяет эмоционально настроить его на позитивное отношение к лечению, что немаловажно для получения хорошего результата.
Такой подход при лечении бронхолегочных заболеваний очень важен для родителей детей, страдающих от астмы, так как малыши не могут самостоятельно принимать необходимые решения. Помочь им может только взрослый, который должен знать, как успокоить ребенка и научить его самостоятельно пользоваться ингалятором в экстренных случаях.
источник
Рациональная терапия ингаляционными кортикостероидами при бронхиальной астме у детей Текст научной статьи по специальности « Медицина и здравоохранение»
Аннотация научной статьи по медицине и здравоохранению, автор научной работы — Геппе Н.А., Колосова Н.Г., Шаталина С.И.
В настоящее время наиболее эффективными препаратами для лечения и достижения контроля над бронхиальной астмой (БА) являются ингаляционные глюкокортикостероиды (ИГКС), назначение которых, согласно международным рекомендациям, показано при персистирующей БА любой степени тяжести в качестве стартовой терапии [10].
Похожие темы научных работ по медицине и здравоохранению , автор научной работы — Геппе Н.А., Колосова Н.Г., Шаталина С.И.,
Rational therapy of asthma in children with inhaled corticostero >Currently, the most effective drugs for the treatment and management of bronchial asthma (BA) are inhaled corticosteroids (ICS) which, according to global guidelines, are indicated as initial therapy for persistent asthma of any severity.
Текст научной работы на тему «Рациональная терапия ингаляционными кортикостероидами при бронхиальной астме у детей»
Н.А. ГЕППЕ, д.м.н., профессор, Н.Г. КОЛОСОВА, к.м.н., С.И. ШАТАЛИНА, к.м.н.
Первый Московский государственный медицинский университет им. И.М. Сеченова, кафедра детских болезней
ИНГАЛЯЦИОННЫМИ КОРТИКОСТЕРОИДАМИ ПРИ БРОНХИАЛЬНОЙ АСТМЕ У ДЕТЕЙ
В настоящее время наиболее эффективными препаратами для лечения и достижения контроля над бронхиальной астмой (БА) являются ингаляционные глюкокортикостероиды (ИГКС), назначение которых, согласно международным рекомендациям, показано при персистирующей БА любой степени тяжести в качестве стартовой терапии [10].
Если при приеме ИГКС достичь стабилизации состояния и контроля над бронхиальной астмой не удается, рекомендовано добавление других препаратов, чаще всего Р2-агонистов длительного действия. Причем необходим подбор минимально возможных эффективных доз ИГКС в комбинации с другим препаратом (табл. 1) [3, 10, 13].
Противовоспалительный эффект ИГКС связан с их геномным и негеномным эффектами. ГКС чаще всего индуцируют синтез липомодулина, который блокирует активность фосфолипазы А2, влияющей на высвобождение арахидоновой кислоты из клеточных мембран, тем самым уменьшая образование метаболитов арахидоно-
вои кислоты — леикотриенов и провоспалительных про-стагландинов. Негеномный эффект реализуется путем связывания в цитоплазме активированного гормоно-рецепторного комплекса с нуклеарным фактором капа-В и другими подобными транскрипционными факторами, следствием чего является угнетение различных аспектов воспаления — образования цитокинов и хемотаксических факторов, выброс воспалительных ферментов [11].
Также ИГКС стабилизируют лизосомальные мембраны, что приводит к ограничению выхода различных про-теолитических энзимов за пределы лизосом и предупреждает деструктивные процессы в стенке бронхиального дерева. Они угнетают пролиферацию фибробластов и уменьшают синтез коллагена, что снижает темпы развития склеротического процесса в стенке бронхов, угнетают образование антител и иммунных комплексов, уменьшают чувствительность эффекторных тканей, снижают неспецифическую бронхиальную гиперреактивность. При ингаляционном введении быстро создается высокая концентрация ГКС непосредственно в трахео-бронхиальном дереве, что позволяет избежать развития системных побочных эффектов. Ингаляционные стерои-
Таблица 1. Ступенчатый подход к базисной терапии БА у детей (США-2014)[10]
Обучение пациентов. Контроль окружающей среды
Р2-агонист быстрого действия по потребности
Вариант препаратов, контролирующих течение заболевания Выберите один Выберите один Добавьте один или более Добавьте один или оба
Низкие дозы ИГКС Низкие дозы ИГКС + в2-агонист ДД Средние или высокие дозы ИГКС + в2-агонист ДД Минимальная возможная доза перорального ГКС
Антагонист лейкотриеновых рецепторов (АЛТР) Средние или высокие дозы ИГКС АЛТР Антитела к ^
Низкие дозы ИГКС + АЛТР Теофиллины замедленного высвобождения
Низкие дозы ИГКС + теофиллины замедленного высвобождения
ды в рекомендованных дозах не влияют на минеральную плотность костей и незначительно или совсем не оказывают влияния на уровень кортизола мочи и в плазме крови [3, 5, 6].
Быстрое начало действия будесонида продемонстрировано в многочисленных клинических исследованиях. Улучшение функциональных показателей легких и уменьшение количества маркеров воспаления в мокроте наблюдалось уже. через 5-6 ч после ингаляции
К хорошо изученным ИГКС относится будесонид, негалогенизированный глюкокортикостероид, оказывающий выраженное местное действие и обладающий хорошей переносимостью. Высокая местная активность и селективность действия препарата обусловлены продолжительным связыванием тканями и высокой инактивацией при первом прохождении через печень. В легких будесонид действует на глюкокортикостероидные рецепторы в течение нескольких часов. Липофильность глюкокортикостероидов является ключевым свойством, определяющим местную противовоспалительную активность, удлинение и увеличение связывания с тканями. При использовании высоких доз будесонида значительная часть препарата конъюгирует с внутриклеточным пулом коэнзима А активатора жирных кислот. Образующиеся высоколипофильные эфиры, обладающие недостаточным сродством к рецепторам, откладываются в клетке (возможно, в субклеточной мембране). При активации внутриклеточной липазы начинается медленное высвобождение свободного будесонида. Будесонид сохраняется в тканях дыхательных путей дольше, чем беклометазон дипропионат и флутиказона пропионат. Конъюгация с длинноцепочечными жирными кислотами является уникальной особенностью будесо-нида, благодаря которой создается внутриклеточное депо препарата и обеспечивается его продолжительное действие (до 24 ч). Это свойство позволяет использовать будесонид один раз в сутки без снижения эффективности [12]. Кроме того, негеномный эффект будесонида включает в себя сосудосуживающее действие, уменьшение экссудации плазмы, уменьшение продукции мокроты в дыхательных путях [7].
Быстрое начало действия будесонида продемонстрировано в многочисленных клинических исследованиях. Улучшение функциональных показателей легких и уменьшение количества маркеров воспаления в мокроте наблюдалось уже через 5-6 ч после ингаляции. Исследование, проведенное в УДКБ Первого МГМУ им. И.М. Сеченова, показало бронхорасширяющий эффект будесонида через 20-30 мин после ингаляции у детей первых пяти лет жизни. Также было показано, что улучшение по шкале дыхательных расстройств было выше у тех детей с острыми проявления бронхиальной астмы, которые получали ингаляционный будесонид, по сравнению с детьми, полу-
чавшими преднизолон per os (1,7 по сравнению с 2,5 ч соответственно; р i Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
1,06 ¿1,04_™j1_ J _ _ _■■ 106И J,04_
Пульмикорт через небулайзер
n=10976 (63% i Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
■ быстрое начало действия — при ежедневном использовании значительно снижает количество обострений астмы, требующих приема системных кортикостероидов;
■ возможность гибкого дозирования — увеличение дозы будесонида при ухудшении состояния значительно снижает риск развития тяжелого обострения;
■ возможность однократного использования — при достижении контроля над заболеванием может использоваться 1 раз в день, т. к. в организме создается депо препарата (принципиальное отличие от других ИГКС);
■ хорошая переносимость — необходима для достижения комплаенса.
Эффективность комбинированной терапии (Симбикорт® Турбухалер®) в отношении дней контроля астмы у подростков в сравнении с иГКС [15]
Симбикорт Турбухалер 80/4,5 мг, 2 ингаляции 2 раза в день иГКС (Пульмикорт Турбухалер 100 мг), 2 ингаляции 2 раза в день
Анализ большого количества исследований показал, что добавление Р2-агониста ДД к низким и средним дозам иГКС у пациентов с недостаточным контролем бронхиальной астмы способствует увеличению функции легких, пиковой скорости выдоха, снижению числа тяжелых обострений, увеличению «бессимптомных» дней и ночей, чем увеличение дозы иГКС в два раза. И что особенно важно, комбинированная терапия снижает на 60% и более общее количество принимаемых стероидов, что уменьшает риски развития побочных эффектов. Наибольшим преимуществом обладают препараты, содержащие иГКС + Р2-агонист ДД в одном ингаляторе с фиксированной комбинацией лекарственных средств, т. к. они обладают рядом дополнительных преимуществ [3,11]:
■ препараты ГКС и Р2-агонист ДД, назначенные в одном ингаляторе, обладают большей эффективностью, чем при назначении их по отдельности;
■ при назначении данных препаратов в одном ингаляторе они абсорбируются на одних и тех же участках слизистой оболочки дыхательных путей (при раздельном назначении области воздействия лекарственных средств не всегда совпадают);
■ использование комбинации препаратов в одном ингаляторе обеспечивает высокий комплаенс к лечению у пациентов, чем раздельное их использование.
В настоящее время на фармацевтическом рынке представлено несколько комбинированных препаратов: будесонид/формотерол, флутиказон/сальметерол и новые препараты беклометазон/формотерол, мометазон/ формотерол.
Значительное количество исследований показало, что добавление длительно действующих Р2-агонистов к ИГКС значительно более эффективно в контроле симптомов, улучшении функции легких, снижении количества обострений БА, чем удвоение дозы ИГКС (рис. 2). В исследовании FACET PauweLs и колл. показали, что добавление формотерола к низким или средним дозам будесонида снижает число обострений, симптомов и повышает легочную функцию.
В исследованиях эффективности комбинации будесонид/формотерол при БА у детей было показано, что добавление формотерола снижает риск тяжелых обострений и улучшает контроль над астмой более эффективно, чем удвоение дозы будесонида [15]. У детей, которые получали комбинированный препарат, значительнее увеличились утренняя и вечерняя ПСВ и ОФВ1 по сравнению с группой лиц, которые получали только ингаляции будесонида. Обе группы были схожи по количеству побочных эффектов и частоте прекращения лечения. Не было выявлено существенных различий по частоте встречаемости нежелательных явлений среди групп сравнения. Во всех терапевтических группах уровень кортизола оставался одинаковым. Таким образом, можно сделать вывод, что терапия будесонидом/формо-теролом безопасна и эффективна при терапии детей с БА; она способствует значительному улучшению показателей легочной функции по сравнению с монотерапией будесонидом.
ЛаШегБ et а1. в своем исследовании у взрослых и подростков старше 12 лет также показали высокую эффективность будесонида/формотерола для купирования бронхо-обструктивного синдрома. Они сравнили действие будесонида/формотерола 160/4,5 мкг, формотерола 4,5 мкг, сальбутамола 200 мкг и плацебо после ингаляции аденозин-5-монофосфата (АМФ), обладающего бронхо-констрикторным действием. Сочетание будесонида/формотерола оказывало выраженный защитный эффект через 3 и даже через 7 ч после ингаляции АМФ по сравнению с другими бронхолитиками. При всех трех вариантах терапии ОФВ1 повышался в одинаковой степени. Таким образом, будесонид/формотерол обладают высокой эффективностью против различных воздействий, приводящих к бронхоспазму [4].
Комбинированная терапия ингаляционными глюкокортикостероидами и в2-агонистами длительного действия у детей с умеренным и тяжелым течением БА обеспечивает высокий и постоянный уровень контроля над симптомами, эффективно защищает пациентов от развития тяжелых обострений и хорошо переносится
Наблюдательное исследование по оценке эффективности комбинированной терапии будесонидом/формоте-ролом (Симбикорт) у детей со среднетяжелой и тяжелой бронхиальной астмой с различной приверженностью к терапии, проведенное в Университетской детской клинической больнице Первого МГМУ им. И.М. Сеченова, продемонстрировало, что возможность варьирования дозы препарата базисной терапии соответственно периоду заболевания (ремиссия или обострение) позволяет адаптировать дозу препарата в соответствии с симптомами [1]. Наличие бронхообструкции у многих детей со средне-
тяжелой и тяжелой бронхиальной астмой доказывает необходимость длительного применения сочетания ингаляционного ГКС и Р2-агониста ДД с подбором индивидуальной дозы. У пациентов, требующих длительной ингаляционной базисной терапии, использование будесонида/ формотерола позволяет минимизировать дополнительное применение Р2-агониста КД, уменьшает повседневную вариабельность симптомов.
Комбинированная терапия ингаляционными глюкокортикостероидами и Р2-агонистами длительного действия у детей с умеренным и тяжелым течением БА обеспечивает высокий и постоянный уровень контроля над симптомами, эффективно защищает пациентов от развития тяжелых обострений и хорошо переносится. Эффект комбинированной терапии потенциирует на протяжении более чем 6 мес., что необходимо учитывать при оценке эффективности комбинированной терапии и при рекомендациях родителям. Применение фиксированной комбинации будесонид/формотерол позволяет добиться оптимального уровня контроля над астмой при использовании существенно более низких доз ГКС по сравнению с любым другим видом комбинированной терапии.
Современные руководства астмы рекомендуют лечение этого заболевания у детей с целью достижения и поддержания контроля и снижения риска будущих обострений астмы. Такой подход снижает вероятность заболеваемости и смертности, которые связаны с неконтролируемой астмой.
Таким образом, ингаляционный глюкокортикостероид будесонид является препаратом выбора в качестве эффективной и безопасной базисной терапии БА у детей. Многообразие различных форм будесонида (суспензия для небулайзерной терапии, дозированые порошковые ингаляторы, фиксированные комбинации с формотеро-лом) позволяет использовать его при любой тяжести БА как у взрослых, так и детей.
1. Геппе Н.А., Шаталина С.И., Колосова Н.Г., Машукова Н.П, Малышев В.С. Комбинированный препарат будесонид/формотерол в контроле обострений бронхиальной астмы у детей. Доктор.ру. 2013, 3: 16-24.
2. Геппе Н.А., Бераиа Т.Т. Ингаляционные глюко-кортикостероиды в терапии бронхиальной астмы у детей. Cons. Med. Педиатрия. 2008. 1: 50-3.
3. Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика». М., 2012, 180с.
4. AaLbers et al. Protective effect of budesonide/ formoterol compared with formoterol, salbutamol and placebo on repeated provocations with inhaled AMP in patients with asthma: a randomised, double-blind, cross-over study Respiratory Research. 2010, 11:66.
5. Agertoft L, Pedersen S. Bone mineral density in children with asthma receiving long-term
treatment with inhaled budesonide. Am J Respir Crit Care Med. 1998. Jan. 157(1):178-83.
6. Agertoft L, Pedersen S. Effect of long-term treatment with inhaled budesonide on adult height in children with asthma. N Engl J Med. 2000 Oct 12. 343(15):1064-9.
7. Brattsand R et al. The role of intracellular esterification in budesonide once-daily dosing and airway selectivity. Clin. Ther. 2003. Vol. 25 Suppl. C.P. S28-41.
8. Busse WW, Chervinsky P, Condemi J, Lumry WR, Petty TL, Rennard S, Townley RG. Budesonide delivered by Turbuhaler is effective in a dose-dependent fashion when used in the treatment of adult patients with chronic asthma. J Allergy Clin Immunol. 1998 Apr. 101(4 Pt 1):457-63.
9. Camargo CA et al. Association between common asthma therapies and recurrent asthma exacerbations in children enrolled in a state Medicaid plan. Am J Health Syst Pharm. 2007 May 15;64(10):1054-61.
10. Global Strategy for Asthma Management and Prevention. Global Initiative for Asthma (GINA); 2014. Global Initiative for Asthma.http://www. ginasthma.org
11. Horvath G, Wanner A. Inhaled corticosteroids: effects on the airway vasculature in bronchial asthma. Eur Respir J. 2006 Jan. 27(1):172-87.
12. Miller-Larsson A et al. Prolonged Airway Activity and Improved Selectivity of Budesonide Possibly Due To Esterification. Am. J. Respir. Crit. Care Med. 2000. 162: 1455-1461.
13. Papadopoulos NG. et al. International consensus on (ICON) pediatric asthma. Allergy, 2012. Vol. 67. 8: 976-997.
14. Peter G. Gibson, Nicolas Saltos, and K. Fakes Acute Anti-inflammatory Effects of Inhaled Budesonide in Asthma A Randomized Controlled Trial. Am J Respir Crit Care Med, 2001. 163: 32-36.
15. Tal A et al. Budesonide/formoterol in a single inhaler versus inhaled corticosteroids alone in the treatment of asthma. Pediatr Pulmonol. 2002 Nov. 34(5):342-50.
источник
Базисная терапия бронхиальной астмы позволяет подавить воспаление в дыхательных путях, уменьшить одышку, сократить бронхиальную гиперреактивность. Такое лечение носит подавляющий, контролирующий и профилактический характер.
Внимание! Курс разрабатывается лечащим врачом под конкретного пациента. Во внимание принимаются возраст, тяжесть протекания патологии, общее самочувствие, прочие персональные особенности.
Базисная терапия одного из самых распространённых заболеваний — бронхиальной астмы – предусматривает реализацию следующих действий.
- Обучение пациента особенностям мониторинга и оценки тяжести болезни.
- Разработка плана лечения для ситуации, если наступит обострение.
- Обеспечение систематического посещения врача для наблюдения и корректировки разработанного плана, например, при использовании ступенчатой терапии БА.
- Максимальное устранение аллергенов и опасных факторов-провокаторов (например, исключение чрезмерных физических нагрузок, которые могут привести к асфиксии).
Внимание! Четвёртый пункт имеет решающее значение. От него напрямую зависит время лечения и результат. Компетенция доктора здесь не важна, определяющее значение имеет то, насколько верно будет определён аллерген, а также то, насколько точно будет пациент придерживаться рекомендаций по недопущению контакта с таким аллергеном.
В процессе лечения важно придерживаться определённых задач:
- строгий контроль симптомов;
- поддержка на подобающем уровне функций лёгких;
- разработка персонального плана физической нагрузки;
- исключение побочных эффектов от применяемых медикаментов;
- предотвращение обострений;
- исключение прогрессирования необратимой обструкции.
Внимание! Указанные задачи помогают более детально понять особенности лечения БА.
Базисная терапия при аллергической, инфекционной и смешанной бронхиальной астме предполагает назначение базисных медикаментов (чаще принимаются пожизненно) и препаратов, которые облегчают симптоматику и помогают снять приступ (могут применяться ситуационно либо для предотвращения приступа).
Внимание! Нельзя отказываться от базисных медикаментов, даже если состояние облегчилось. Болезнь снова начнёт проявляться. Допускается только контрольная отмена.
Часто назначается физиотерапия при профессиональной, аспириновой и иной бронхиальной астме. Также применяются разные растения (наиболее востребованы чабрец, багульник, анис, подорожник, мать-и-мачеха, иссоп, фиалка, алтей). Фитотерапия рекомендована на первых трёх этапах патологии. Далее смысл в ней исчезает, т. к. растения перестают оказывать даже малейший эффект.
Внимание! Излечить БА полностью невозможно. Главная цель врача заключается в повышении качества жизни больного.
Принципы лечения дневной и ночной бронхиальной астмы таковы.
- Контролируемое течение: отсутствие ночной симптоматики, дневные симптомы возникают два и меньше раз в неделю, уходят обострения, дыхание остаётся в норме.
- Еженедельный анализ заболевания.
- Неконтролируемое течение: раз в 7 дней отмечается 3 и больше признаков.
Тактика последующих действий определяется, исходя из указанных выше принципов. Обязательно учитываются особенности лечения, проводимого в конкретный момент.
Базисное лечение бронхиальной астмы у маленьких пациентов проводится комплексно. Важно достичь устойчивой ремиссии. Большое значение имеет давность появления начальных симптомов, наличие болезней хронического характера, текущее самочувствие.
У детей симптоматика проявляется с заметно неодинаковой интенсивностью. Возникают:
- сложности с дыханием;
- хрипы;
- одышка;
- асфиксия;
- ухудшение самочувствия;
- кашель;
- посинение кожи возле носа.
Маленьким пациентам назначают глюкокортикоиды ингаляционные, препараты с противовоспалительным эффектом, бронходилататоры продолжительного действия.
Базисные препараты для лечения бронхиальной астмы позволяют не допустить ухудшения самочувствие пациента. Назначают:
- глюкокортикостероиды ингаляционные,
- глюкокортикостероиды системные,
- стабилизаторы тучных клеток,
- лейкотриеновые антагонисты.
Глюкокортикостероиды ингаляционные незаменимы для устранения приступов. Они оказывают противовоспалительный эффект, действуют в самые короткие сроки. Такие ингаляции позволяют добиться следующего:
- сократить интенсивность симптомов патологии;
- повысить проходимость в бронхах;
- устранить воспаления;
- минимизировать попадание действующих компонентов препарата в общий кровоток.
Можно принимать небольшие дозы медикамента. Это наиболее актуально для больных, которые имеют хронические болезни.
Благодаря ингаляционным средствам удаётся устранить приступ. Для базисного лечения бронхиальной астмы требуются глюкокортикостероиды таблетированной формы. Их прописывают при тяжёлом состоянии. С их помощью удаётся:
- избавиться от спазмов в бронхах;
- сократить объём выделяемой мокроты;
- устранить воспалительный процесс;
- повысить проходимость путей дыхания.
Глюкокортикостероиды системные рекомендованы при сложных ситуациях. Такие лекарства спасают, когда другие препараты оказываются неэффективными.
Внимание! Нельзя принимать данные лекарства самостоятельно. Обязательно нужно проконсультироваться с лечащим доктором.
Стабилизаторы тучных клеток снимают воспаление. Подходят людям с лёгким и средним течением болезни. Такие медикаменты позволяют эффективно:
- сократить гиперреактивность бронхов;
- ликвидировать и предупредить аллергию;
- не допустить появления спазмов.
Лейкотриеновые антагонисты блокируют лейкотриеновые рецепторы и угнетают активность ферментов 5-липоксигеназов. Если не принимать такие препараты, то организм будет неизбежно реагировать на аллергены. Они снимают даже сильные воспаления, устраняют спазмы, снижают объём мокроты, расслабляют гладкие мышцы, повышают проницаемость мелких сосудов системы дыхания.
Пожалуйста, поделитесь этим материалом в социальных сетях, чтобы ещё больше людей узнало о методах лечения бронхиальной астмы. Это поможет им контролировать проявления заболевания и вовремя предпринимать необходимые меры в целях блокирования приступа.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Кафедра пульмонологии ФУВ РГМУ
В последние годы отмечен значительный прогресс в лечении бронхиальной астмы (БА). По–видимому, это связано с определением БА, как хронического воспалительного заболевания дыхательных путей, и вследствие этого – с широким применением ингаляционных глюкокортикостероидов (ГКС) в качестве базисных противовоспалительных препаратов. Однако несмотря на достигнутые успехи, уровень контроля над течением заболевания нельзя считать удовлетворительным. Так, например, почти каждый третий больной БА, как минимум, 1 раз в месяц просыпается ночью в связи с симптомами болезни. Более половины больных имеют ограничения физической активности, более трети вынуждены пропускать занятия в школе или отсутствовать на работе. Более 40% больных вынуждены обращаться за неотложной помощью вследствие обострения заболевания. Причины подобной ситуации многообразны, и не последнюю роль в этом играет недостаточная осведомленность врача в патогенезе БА и, соответственно, выбор неправильной тактики лечения.
Определение и классификация БА
Бронхиальная астма – хроническое заболевание дыхательных путей, в котором принимают участие многие клетки: тучные клетки, эозинофилы и Т–лимфоциты. У предрасположенных лиц это воспаление приводит к повторным эпизодам хрипов, одышки, тяжести в грудной клетке и кашлю, особенно ночью и/или ранним утром. Эти симптомы сопровождаются распространенной, но вариабельной обструкцией бронхиального дерева, которая, по крайней мере, частично обратима, спонтанно или под влиянием лечения. Воспаление также вызывает увеличение ответа дыхательных путей на различные стимулы (гиперреактивность).
Ключевыми положениями определения следует считать следующие:
1. БА – хроническое персистирующее воспалительное заболевание дыхательных путей вне зависимости от тяжести течения.
2. Воспалительный процесс приводит к гиперреактивности бронхов, обструкции и появлению респираторных симптомов.
3. Обструкция дыхательных путей обратима, по крайней мере, частично.
4. Атопия – генетическая предрасположенность к продукции иммуноглобулинов класса Е (может присутствовать не всегда).
Бронхиальную астму можно классифицировать на основе этиологии, тяжести течения и особенностей проявления бронхиальной обструкции.
Однако в настоящее время бронхиальную астму в первую очередь следует классифицировать по степени тяжести, т. к. именно это отражает степень выраженности воспалительного процесса в дыхательных путях и определяет тактику противовоспалительной терапии.
Степень тяжести определяется по следующим показателям:
- Количество ночных симптомов в неделю.
- Количество дневных симптомов в день и в неделю.
- Кратность применения b 2–агонистов короткого действия.
- Выраженность нарушений физической активности и сна.
- Значения пиковой скорости выдоха (ПСВ) и ее процентное соотношение с должным или наилучшим значением.
- Суточные колебания ПСВ.
- Объем проводимой терапии.
Существует 5 степеней тяжести течения БА: легкая интермиттирующая; легкая персистирующая; средней тяжести персистирующая; тяжелая персистирующая; тяжелая персистирующая стероидозависимая (табл. 1).
БА интермиттирующего течения: симптомы астмы реже 1 раза в неделю; короткие обострения (от нескольких часов до нескольких дней). Ночные симптомы 2 раза в месяц или реже; отсутствие симптомов и нормальная функция легких между обострениями: пиковая скорость выдоха (ПСВ) > 80% от должного и колебания ПСВ менее 20%.
БА легкого персистирующего течения. Симптомы 1 раз в неделю или чаще, но реже 1 раза в день. Обострения заболевания могут нарушать активность и сон. Ночные симптомы возникают чаще 2 раз в месяц. ПСВ более 80% от должного; колебания ПСВ 20–30%.
БА средней тяжести. Ежедневные симптомы. Обострения нарушают активность и сон. Ночные симптомы возникают более 1 раза в неделю. Ежедневный прием b 2–агонистов короткого действия. ПСВ 60–80% от должного. Колебания ПСВ более 30%.
БА тяжелого течения: постоянные симптомы, частые обострения, частые ночные симптомы, физическая активность ограничена проявлениями астмы. ПСВ менее 60% от должного; колебания более 30%.
Необходимо отметить, что определение степени тяжести астмы по этим показателям возможно только перед началом лечения. Если больной уже получает необходимую терапию, то ее объем также должен учитываться. Таким образом, если у пациента по клинической картине определяется легкая персистирующая астма, но при этом он получает медикаментозное лечение, соответствующее тяжелой персистирующей астме, то у данного пациента диагностируется БА тяжелого течения.
БА тяжелого течения стероидозависимая: независимо от клинической картины пациент, получающий длительное лечение системными кортикостероидами, должен быть расценен, как страдающий БА тяжелого течения.
Рекомендован ступенчатый подход к терапии БА в зависимости от тяжести ее течения (табл. 1). Все препараты для лечения БА разделены на две основные группы: для длительного контроля воспалительного процесса и средства для купирования острых симптомов астмы. Основой терапии для длительного контроля воспалительного процесса являются ингаляционные глюкокортикостероиды (ИГКС), которые следует применять, начиная со второй ступени (легкое персистирующее течение) до пятой (тяжелое стероидозависимое течение). Поэтому в настоящее время ИГКС рассматриваются в качестве средств первой линии для терапии БА. Чем выше степень тяжести течения БА, тем большие дозы ИГКС следует применять. По данным ряда исследований, у пациентов, начавших лечение ИГКС не позже двух лет от начала заболевания, отмечены существенные преимущества в улучшении контроля над симптомами астмы по сравнению с группой, начавшей лечение ИГКС по прошествии более чем 5 лет от дебюта заболевания.
Механизмы действия и фармакокинетика
ИГКС способны связываться со специфическими рецепторами в цитоплазме, активируют их и образуют с ними комплекс, который затем димеризуется и перемещается в ядро клетки, где связывается с ДНК и взаимодействует с механизмами транскрипции ключевых ферментов, рецепторов и других сложных белков. Это приводит к проявлению фармакологического и терапевтического действия.
Противовоспалительный эффект ИГКС связан с их ингибирующим действием на клетки воспаления и их медиаторы, включая продукцию цитокинов, вмешательство в метаболизм арахидоновой кислоты и синтез лейкотриенов и простагландинов, предотвращение миграции и активации клеток воспаления. ИГКС увеличивают синтез противовоспалительных белков (липокортина–1), увеличивают апоптоз и снижают количество эозинофилов путем ингибирования интерлейкина–5. Таким образом, ИГКС приводят к стабилизации клеточных мембран, уменьшают проницаемость сосудов, улучшают функцию b –рецепторов как путем синтеза новых, так и повышая их чувствительность, стимулируют эпителиальные клетки.
ИГКС отличаются от системных глюкокортикостероидов своими фармакологическими свойствами: липофильностью, быстротой инактивации, коротким периодом полувыведения из плазмы крови. Важно учитывать, что лечение ИГКС является местным (топическим), что обеспечивает выраженные противовоспалительные эффекты непосредственно в бронхиальном дереве при минимальных системных проявлениях. Количество ИГКС, доставляемое в дыхательные пути, зависит от номинальной дозы препарата, типа ингалятора, наличия или отсутствия пропеллента, а также техники выполнения ингаляции. До 80% пациентов испытывают сложности при использовании дозированных аэрозолей.
Наиболее важной характеристикой для проявления селективности и времени задержки препарата в тканях является липофильность. Благодаря липофильности ИГКС накапливаются в дыхательных путях, замедляется их высвобождение из тканей и увеличивается их сродство к глюкокортикоидному рецептору. Высоколипофильные ИГКС быстрее и лучше захватываются из просвета бронхов и длительно задерживаются в тканях дыхательных путей. ИГКС отличает от системных препаратов их топическое (местное) действие. Поэтому бесполезно назначать ингаляции системных ГКС (гидрокортизона, преднизолона и дексаметазона): эти препараты вне зависимости от способа применения обладают только системным действием.
В многочисленных рандомизированных плацебо-контролируемых исследованиях у больных БА показана эффективность всех доз ИГКС в сравнении с плацебо.
Системная биодоступность складывается из пероральной и ингаляционной. От 20 до 40% от ингалируемой дозы препарата попадает в дыхательные пути (это величина значительно варьирует в зависимости от средства доставки и от ингаляционной техники пациента). Легочная биодоступность зависит от процента попадания препарата в легкие, наличия или отсутствия носителя (лучшие показатели имеют ингаляторы, не содержащие фреон) и от абсорбции препарата в дыхательных путях. 60–80% ингаляционной дозы оседает в ротоглотке и проглатывается, подвергаясь затем полному или частичному метаболизму в желудочно–кишечном тракте и печени. Пероральная доступность зависит от абсорбции в желудочно–кишечном тракте и от выраженности эффекта «первого прохождения» через печень, благодаря чему в системный кровоток поступают уже неактивные метаболиты (за исключением беклометазона 17–монопропионата – активного метаболита беклометазона дипропионата). Дозы ИГКС до 1000 мкг/сутки (для флютиказона до 500 мкг/сут) обладают незначительным системным действием.
Все ИГКС имеют быстрый системный клиренс, сравнимый с величиной печеночного кровотока. Это один из факторов, снижающих системное действие ИГКС.
Характеристика наиболее часто используемых препаратов
К ИГКС относятся беклометазона дипропионат, будесонид, флютиказона пропионат, флунизолид, триамсинолона ацетонид, мометазона фуроат. Они выпускаются в виде дозированных аэрозолей, порошковых ингаляторов, а также в виде растворов для ингаляции через небулайзер (будесонид).
Беклометазона дипропионат. Применяется в клинической практике более 20 лет и остается одним из самых эффективных и часто используемых препаратов. Разрешено применение препарата у беременных. Выпускается в виде дозированного аэрозольного ингалятора (Бекотид 50 мкг, Беклофорте 250 мкг, Альдецин 50 мкг, Беклокорт 50 и 250 мкг, Бекломет 50 и 250 мкг/доза), дозированного ингалятора, активируемого вдохом (Беклазон Легкое Дыхание 100 и 250 мкг/доза), порошкового ингалятора (Бекодиск 100 и 250 мкг/доза ингалятор Дискхалер; мультидозовый ингалятор Изихейлер, Бекломет 200 мкг/доза). Для ингаляторов Бекотид и Беклофорте производятся специальные спейсеры – «Волюматик» (клапанный спейсер большого объема для взрослых) и «Бэбихалер» (2–клапанный спейсер малого объема с силиконовой лицевой маской для детей раннего возраста).
Будесонид. Современный высокоактивный препарат. Используется в виде дозированного аэрозольного ингалятора (Будесонид-мите 50 мкг/доза; Будесонид–форте 200 мкг/доза), порошкового ингалятора (Пульмикорт Турбухалер 200 мкг/доза; Бенакорт Циклохалер 200 мкг/доза) и суспензии для небулайзера (Пульмикорт 0,5 и 0,25 мг/доза). Пульмикорт Турбухалер – единственная лекарственная форма ИГКС, не содержащая носителя. Для дозированных ингаляторов Будесонид мите и Будесонид форте производится спейсер. Будесонид является составной частью комбинированного препарата Симбикорт.
Будесонид имеет наиболее благоприятный терапевтический индекс, что связано с его высоким сродством к глюкокортикоидным рецепторам, и ускоренным метаболизмом после системной абсорбции в легких и кишечнике. Будесонид является единственным ИГКС, для которого доказана возможность однократного применения. Фактор, обеспечивающий эффективность применения будесонида один раз в день, – ретенция будесонида в дыхательных путях в виде внутриклеточного депо благодаря обратимой эстерификации (образованию эфиров жирных кислот). При снижении концентрации свободного будесонида в клетке активируются внутриклеточные липазы, высвобождающийся из эфиров будесонид вновь связывается с рецептором. Подобный механизм не свойственен другим ГКС и позволяет пролонгировать противовоспалительный эффект. В ряде исследований показано, что внутриклеточное депонирование может оказаться более важным в плане активности препарата, чем сродство к рецептору.
Исследования последних лет по препарату Пульмикорт Турбухалер доказали, что он не влияет на конечный рост при длительном применении у детей, на минерализацию кости, не вызывает ангиопатию и катаракту. Пульмикорт также рекомендован к применению у беременных: установлено, что его применение не вызывает увеличения числа аномалий плода. Пульмикорт Турбухалер является первым и единственным ИГКС, которому FDA (организация по контролю за лекарственными средствами в США) присвоила категорию «В» в рейтинге лекарств, назначаемых при беременности. В эту категорию включаются лекарства, прием которых в период беременности является безопасным. Остальные ИГКС относятся к категории «С» (прием их во время беременности не рекомендуется).
Флютиказона пропионат. Самый высокоактивный препарат на сегодняшний день. Обладает минимальной пероральной биодоступностью ( b 2–агонистов короткого действия по потребности или регулярно. Таким образом появилась острая потребность в новом классе препаратов, свободных от недостатков, которые присущи b 2–агонистам короткого действия, и обладающих доказанным длительным протективным и противовоспалительным действием на дыхательные пути.
Были созданы и в настоящее время широко применяются b 2–агонисты длительного действия, которые на фармацевтическом рынке представлены двумя препаратами: формотерола фумаратом и сальметерола ксинафоатом. В современных руководствах по терапии астмы рекомендовано добавление b 2–агонистов длительного действия при недостаточном контроле БА монотерапией ингаляционными ГКС (начиная со второй ступени). В ряде исследований было показано, что комбинация ингаляционного ГКС с b 2–агонистом длительного действия более эффективна, чем удвоение дозы ингаляционных ГКС, и приводит к более значимому улучшению функции легких и лучшему контролю над симптомами астмы. Было показано также снижение количества обострений и значимое улучшение качества жизни у пациентов, получающих комбинированную терапию. Таким образом, появление комбинированных препаратов, содержащих ингаляционный ГКС и b 2–агонист длительного действия, – отражение эволюции взглядов на терапию БА.
Главным преимуществом комбинированной терапии является повышение эффективности лечения при использовании более низких доз ИГКС. Кроме того, соединение двух препаратов в одном ингаляторе облегчает пациенту выполнение назначений врача и потенциально улучшает комплайнс.
Серетид Мультидиск. Составными компонентами являются сальметерола ксинафоат и флютиказона пропионат. Обеспечивает высокий уровень контроля над симптомами БА. Используется только в качестве базисной терапии, может назначаться, начиная со второй ступени. Препарат представлен в различных дозировках: 50/100, 50/250, 50/500 мкг сальметерола/флютиказона в 1 дозе. Мультидиск относится к ингаляционным устройствам малого сопротивления, что позволяет использовать его и у пациентов со сниженной скоростью вдоха.
Симбикорт Турбухалер. Составными компонентами являются будесонид и формотерола фумарат. На российском рынке представлен в дозировке 160/4,5 мкг в 1 дозе (дозы препаратов указаны как доза на выходе). Важная особенность Симбикорта – возможность использовать его как для базисной терапии (для контроля воспалительного процесса), так и для немедленного облегчения симптомов астмы. Это обусловлено прежде всего свойствами формотерола (быстрое начало действия) и способностью будесонида активно действовать в течение 24 часов на слизистую бронхиального дерева.
Симбикорт дает возможность индивидуального гибкого дозирования (1–4 ингаляционные дозы в сутки). Симбикорт можно использовать, начиная со 2 ступени, но особенно он показан пациентам с нестабильной астмой, для которой характерны внезапные тяжелые приступы затрудненного дыхания.
Системные ГКС применяются в основном для купирования обострения БА. Наиболее эффективны пероральные ГКС. Внутривенно кортикостероиды назначают при обострении БА, если более желателен внутривенный доступ, или при нарушении всасывания из желудочно–кишечного тракта, используя высокие дозы (до 1 г преднизолона, метилпреднизолона и гидрокортизона). Кортикостероиды приводят к клинически значимому улучшению спустя 4 часа после их введения.
При обострении БА показан короткий курс пероральных ГКС (7–14 дней), причем начинают с высоких доз (30–60 мг преднизолона). В последних публикациях рекомендуют следующий короткий курс системных ГКС при не угрожающих жизни обострениях: 6 таблеток преднизолона утром (30 мг) в течение 10 дней с последующим прекращением приема. Хотя схемы лечения системными ГКС могут быть различными, основополагающими принципами являются назначение их в высоких дозах для быстрого достижения эффекта и последующая быстрая отмена. Следует помнить, что как только пациент оказывается готовым к приему ингаляционных ГКС, они должны быть ему назначены с соблюдением ступенчатого подхода.
Системные глюкокортикоиды следует назначить, если:
- Обострение средней тяжести или тяжелое.
- Назначение ингаляционных b 2–агонистов короткого действия в начале лечения к улучшению не привело.
- Обострение развилось, несмотря на то, что больной находился на длительном лечении пероральными кортикостероидами.
- Для купирования предыдущих обострений требовались пероральные кортикостероиды.
- 3 и более раз в год проводились курсы глюкокортикоидов.
- Больной находится на ИВЛ.
- Ранее были угрожающие жизни обострения.
Нежелательно использование пролонгированных форм системных стероидов для купирования обострений и проведения поддерживающей терапии БА.
Для длительной терапии при тяжелом течении БА системные ГКС (метилпреднизолон, преднизолон, триамсинолон, бетаметазон) следует назначать в наименьшей эффективной дозе. При длительном лечении альтернирующая схема назначения и прием в первой половине дня (для уменьшения влияния на циркадные ритмы секреции кортизола) вызывают наименьшее количество побочных эффектов. Следует подчеркнуть, что во всех случаях назначения системных стероидов больному должны быть назначены высокие дозы ингаляционных ГКС. Из пероральных ГКС предпочтение отдается тем, у которых отмечается минимальная минералокортикоидная активность, относительно короткий период полураспада и ограниченное действие на поперечно–полосатую мускулатуру (преднизолон, метилпреднизолон).
Пациентам, которые вынуждены постоянно принимать системные ГКС, следует уделять особое внимание. Существует несколько вариантов формирования стероидозависимости у пациентов с БА и другими заболеваниями, сопровождающимися бронхообструкцией:
- Отсутствие комплайенса (взаимодействия) врача и пациента.
- Неназначение ингаляционных ГКС пациентам. Многие врачи считают, что нет необходимости назначать ингаляционные ГКС больным, получающим системные стероиды. Если пациент с БА получает системные стероиды, его следует расценивать, как больного с тяжелой формой БА, имеющего прямые показания к назначению высоких доз ингаляционных ГКС.
- У больных системными заболеваниями (включая легочные васкулиты, например, синдром Чардж–Стросса) бронхиальная обструкция может быть расценена, как БА. Отмена системных стероидов у этих больных может сопровождаться тяжелыми проявлениями системного заболевания.
- В 5% случаев встречается стероидорезистентность, для которой характерна резистентность стероидных рецепторов к стероидным препаратам. В настоящее время различают две подгруппы: больные с истинной стероидной резистентностью (тип II), не имеющие побочных эффектов при длительном приеме высоких доз системных ГКС, и пациенты с приобретенной резистентностью (тип I) – имеющие побочные эффекты системных ГКС. В последней подгруппе резистентность можно преодолеть, скорее всего, повышением дозы ГКС и назначением препаратов, имеющих аддитивный эффект.
Необходима разработка диагностических программ для пациентов, которые получают адекватную терапию, чувствительны к кортикостероидам, имеют высокий комплайнс, но несмотря на все это, испытывают симптомы астмы. Эти пациенты являются самыми «непонятными» с точки зрения терапии и с точки зрения патофизиологии. У них следует проводить тщательную дифференциальную диагностику для исключения других заболеваний, имитирующих клиническую картину БА.
1. Бронхиальная астма. Глобальная стратегия: совместный доклад Национального института Сердце, Легкие, Кровь и Всемирной организации здравоохранения. Пульмонология, 1996.
2. Бронхиальная астма. Руководство для врачей России (формулярная система). «Пульмонология», приложение–99.
3. Ведущие направления в диагностике и лечении бронхиальной астмы. Основные положения отчета группы экспертов EPR–2. National Institute of Health. National Heart, Lung and Blood Institute. NIH publication–97. Перевод под ред. Проф. Цой А.Н., М, Грантъ,1998.
4. Ильина Н.И. Ингаляционные глюкокортикоиды. Астма.ru. Аллергические и респираторные заболевания. 0*2001 (пилотный выпуск).
5. Огородова Л.М. Системы ингаляционной доставки препаратов в дыхательные пути. Пульмонология, 1999; №1, 84–87
6. Формулярная система: лечение бронхиальной астмы. Астма. ru ,0. 2001, 6–9
7. Чучалин А.Г. Бронхиальная астма. Москва, 1997.
8. Цой А.Н. Ингаляционные глюкокортикоиды: эффективность и безопасность. РМЖ 2001; 9: 182–185
9. Цой А.Н. Сравнительная фармакокинетика ингаляционных глюкокортикоидов. Аллергология 1999; 3: 25–33
10. Agertoft L., Pedersen S. Effect of long–term treatment with inhaled budesonide on adult height in children with asthma. N Engl J Med 2000; 343: 1064–9
11. Ankerst J., Persson G., Weibull E. A high dose of budesonide/formoterol in a single inhaler was well tolerated by asthmatic patients. Eur Respir J 2000; 16 (Suppl 31): 33s+poster
12. Barnes P.J. Inhaled glucocorticoides for asthma. N. Engl. Med. 1995; 332: 868–75
13. Beclomethasone Dipropionate and Budesonide. The clinical evidence Reviewed. Respir Med 1998; 92 (Suppl B)
14. The British Guidelines on Asthma Management. Thorax, 1997; 52 (Suppl. 1) 1–20.
15. Burney PGJ. Current questions in the epidemiology of asthma, in Holgate ST, et al, Asthma: Physiology. Immunology, and Treatment. London, Academic Press, 1993, pp 3–25.
16. Crisholm S et al. Once–daily budesonide in mild asthma. Respir Med 1998; 421–5
17. Kips JC, O/Connor BJ, Inman MD, Svensson K, Pauwels RA, O/Byrne PM. A long–termed study of the antiinflammatory effect of low–dosed budesonide plus formoterol versus high–dosed budesonide in asthma. Am Respir Crit Care Med 2000; 161: 996–1001
18. McFadden ER, Casale TB, Edwards TB et al. Administration of budesonide once daily by means of Turbuhaler to subjects with stable asthma. J Allergy Clin Immunol 1999; 104: 46–52
19. Miller–Larsson A., Mattsson H., Hjertberg E., Dahlback M., Tunek A., Brattsand R. Reversible fatty acid conjugation of budesonide: novel mechanism foe prolonged retention of topically applied steroid in airway tissue. Drug Metab Dispos 1998; 26: 623–30
20. Miller–Larsson A. et al. Prolonged airway activity and improved selectivity of budesonide possibly due to esterification. Am J Respir Crit Care Med 2000;162: 1455–1461
21. Pauwels RA et al. Effect of inhaled formoterol and budesonide on exacerbations of asthma. N Engl J Med 1997; 337: 1405–11
22. Pedersen S, O/Byrne P. A comparison of the efficacy and safety of inhaled corticosteroides in asthma. Allergy 1997; 52 (Suppl 39): 1–34.
источник