Диагностика бронхиальной астмы выполняется, ориентируясь на полное комплексное обследование организма пациента. От правильно проведенной диагностики зависит получение положительных результатов лечения.
Протоколы (стандарты) определения заболеваемости, а также дальнейшего лечения взрослого населения и детей учитывают различные методики: клинический осмотр, сбор анамнеза, выявление симптоматики, лабораторная диагностика.
После проведения необходимых мероприятий для каждого больного подбирается индивидуальная схема лечения, которая способствует снижению заболеваемости и облегчению состояния больного. Дифференциальная диагностика бронхиальной астмы учитывает все аспекты (анализы, симптоматику, анамнез, аллергологическое исследование и дыхательную функциональность.).
Современная диагностика при развитии бронхиальной астмы является важной задачей для врача, так как адекватное лечение способно обеспечить полный контроль над заболеванием при полной нейтрализации симптоматики у детей и взрослых. Для этого оцениваются все критерии астмы с исключением ХОБЛ и постановкой предварительного диагноза.
Протоколы диагностики проводятся в несколько этапов:
Бронхиальная астма, в зависимости от степени заболеваемости, определяется наиболее часто в детском и подростковом возрасте. Как правило, наблюдается генетическая предрасположенность к развитию астматических заболеваний. Кроме того, ее развитие возможно на фоне ХОБЛ.
Бронхиальный приступ нередко связан с воздействием определенных факторов, провоцируя характерную симптоматику (одышку, кашель, свистящее дыхание, слабость и т.д.). Приступ способен появиться внезапно. Его можно купировать при помощи ингаляционных бронхолитиков. Если после использования ингалятора приступ не снимается, необходимы дальнейшие протоколы диагностики, а также исключение ХОБЛ.
В начальной стадии заболевания профессиональная диагностика не способна определить какие-то определенные протоколы в определении бронхиальной астмы, кроме исключения ХОБЛ. Во время затяжного приступа может возникнуть симптом «бочкообразной грудной клетки», что связано с затрудненным выдохом. В результате этого возможно постепенное развитие эмфиземы, критерии и протоколы которой зависят от выраженности симптоматики и стадии заболеваемости. От результатов визуального осмотра может зависеть дальнейшее лечение.
Немаловажным способом профессиональной диагностики является перкуссия (выстукивание) и аускультация (выслушивание) легких. По мере развития приступа можно услышать свистящее дыхание и хрипы в легких. Перкуссия эффективна при длительном течении заболевания и эмфиземе.
Лабораторная диагностика предполагает назначение проведения различного вида анализов, среди которых:
- биохимический анализ крови — определяет количество эозинофилов, являющихся маркерами аллергического процесса. Кроме того, этот анализ в совокупности с аллергологической пробой, позволяет выявить конкретный аллерген, на который острее всего реагирует организм;
- общий анализ крови — позволяет выявить воспалительные процессы, ХОБЛ и интоксикацию в организме больного. Забор крови выполняется натощак;
- общий анализ мокроты — выявляет характерные астматические маркеры с характерными спиралями Куршмана и кристаллами Шарко – Лейдена. При этом определяется вязкая и густая мокрота, которая может расслаиваться двумя слоями. При микроскопическом исследовании определяются эозинофилы;
- анализ кала — способствует выявлению паразитарных инвазий, которые нередко провоцируют развитие бронхиальной астмы. Например, аскариды при своей цикличности развития способны проникнуть через легочную систему, вызывая общую интоксикацию организма, ослабление иммунной системы, повышенную аллергизацию пациента;
- аллергопроба (включая скарификационную) — критерии проведения аллергопробы позволяют уточнить наличие триггера в крови, который вызывает ответную цепь реакций в крови, приводя к бронхоспазму. При положительном ответе могут наблюдаться местные признаки воспаления (зуд, гиперемия, отек и т.д.).
Наиболее сложно диагностировать астму при наличии обструктивного бронхита (ХОБ). Этот процесс проявляется, как хроническая обструктивная болезнь легких (ХОБЛ).
Протоколы выполнения этого вида диагностики служат показателями для постановки итогового диагноза.
Профессиональная рентгенография способна выявить повышенную воздушность легочной ткани (эмфизему) и усиленный легочный рисунок за счет активного притока крови к легочной ткани. Тем не менее, следует учитывать, что иногда даже рентгенограмма не может выявить изменения. Поэтому принято считать, что методы рентгенографии глубоко неспецифичны.
Этот метод служит для определения ФВД (функций внешней дыхательной деятельности) и является достаточно эффективным. Профессиональная спирометрия способна определить ряд главных показателей дыхательной деятельности.
Диагностика спирометрии выглядит следующим образом:
- пациенту предлагается дышать через специальный прибор (спирометр), который обладает чувствительностью и фиксирует все изменения дыхания;
- анализ проведенного обследования сравнивается (врачом или пациентом) с рекомендуемыми показателями ФВД;
- на основании профессиональной сравнительной характеристики внешнего дыхания врач устанавливает предварительный диагноз (для 100% уверенности в диагнозе одной спирометрии недостаточно);
- если у больного наблюдается бронхообструктивные нарушения (исключая ХОБЛ) это может говорить о проявлении бронхиальной астмы.
Помимо этого, спирометрические данные позволяют определить тяжесть астматического приступа и эффективность проводимого лечения в том случае, когда оно использовалось.
Этот метод диагностирования относится к нововведениям для контроля и определения развития бронхиальной астмы у взрослого пациента. Мониторинговый протокол с участием пикфлоуметра обладает следующими преимуществами:
- позволяет определить обратимость бронхиальной обструкции;
- возможность оценки тяжести течения болезни;
- протоколы пикфлоуметрии позволяют спрогнозировать период, когда возникает астматический приступ, в зависимости от степени заболеваемости;
- возможность выявления профессиональной астмы;
- мониторинг эффективности проводимого лечения.
Пикфлоуметрию следует выполнять ежедневно. Это позволяет получить более точные результаты диагностики.
При помощи этого способа профессиональной диагностики определяется пиковая объемность и максимальная объемная скорость на различных уровнях, учитывая процентное соотношение ФЖЕЛ (форсированную жизненную емкость легких). Измеряют максимальную скорость на уровне в 75%, 50% и 25%.
Наиболее затруднительны протоколы определения профессиональной астмы, так как приступ могут вызвать некоторые химические соединение, присутствующие в воздухе. Для подтверждения профессиональной астмы необходимо выяснение анамнеза у взрослого пациента, а также анализ показателей внешней дыхательной деятельности. Кроме того, необходимо в обязательном порядке своевременно сдавать анализы (мокроты, мочи, крови и т.д.) и проводить необходимое лечение.
Одновременно с показателями внешнего дыхания и в зависимости от выраженности симптоматики проводятся прик-тесты (инъекционные) и скарификационная проба на выявление аллергологической этиологии. Однако следует учитывать, что клиническая картина таких обследований в некоторых случаях могут дать ложнопозитивный или ложнонегативный ответ. Именно поэтому рекомендуется проводить исследование крови на наличие специфических антител в сыворотке. В профессиональной диагностике особенно важно выяснение аллергического статуса у детей.
Диагностика бронхиальной астмы у детей нередко сопровождается большими трудностями. Это связано, прежде всего, с симптоматикой заболевания у детей, которая аналогична многим другим детским заболеваниям. Поэтому многое зависит от выяснения анамнеза со склонностью к аллергическим заболеваниям. В первую очередь необходимо опираться на повторение ночного приступа бронхиальной астмы, что подтверждает развитие заболевания.
Помимо этого, протоколы диагностики предусматривают проведение ФВД (функционального исследования внешнего дыхания) с бронходилататорами для назначения адекватной тактики лечения. Вполне естественно, что необходимо сдать анализы мокроты, крови и кала, а также провести спирометрическое тестирование и аллергообследование.
Следует отметить, что затруднительно проводить диагностику астматического приступа у лиц пожилого возраста. Это связано, прежде всего, с обилием хронических заболеваний, которые сопровождают бронхиальную астму, «стирая» ее картину. В этом случае, необходим тщательный сбор анамнеза, исследование мокроты и крови, выполнение специфических тестирований, направленных на исключение вторичных заболеваний. Прежде всего, проводится диагностика сердечной астмы, выявление ИБС, сопровождающейся симптомами недостаточности левого желудочка.
Кроме того, рекомендуется проводить функциональные методы выявления бронхиальной астмы, включающие ЭКГ, рентгенографию, пикфлоуметрию (в течение 2 недель). Только после выполнения всех диагностических мероприятий назначается симптоматическое лечение бронхиальной астмы.
источник
ГОУ ВПО Тверская ГМА Росздрава
Кафедра факультетской терапии
Под редакцией профессора В.В. Чернина
Цель занятия: Научиться ставить диагноз бронхиальной астмы с указанием степени тяжести, предполагаемого патогенетического варианта, проводить дифферинциальную диагностику и выбирать тактику лечения пациента.
В результате освоения темы студент должен знать:
Определения бронхиальной астмы;
Классификацию бронхиальной астмы;
Патогенетические механизмы развития бронхиальной астмы;
Основные клинические симптомы;
Методы лабораторной и инструментальной диагностики бронхиальной астмы;
Дифференциально-диагностические критерии бронхиальной астмы;
Принципы лечения бронхиальной астмы.
На основании полученных данных студент должен уметь:
Целенаправленно собрать жалобы и анамнез у пациента с бронхиальной астмой;
Провести клинический осмотр больного;
Составить план обследования больного с заболеванием органов дыхания;
Интерпретировать результаты дополнительных методов обследования;
Поставить диагноз бронхиальной астмы при типичном течении заболевания;
Выяснить степень тяжести бронхиальной астмы;
Провести дифференциальный диагноз с другими заболеваниями, протекающими со сходной клинической картиной;
Назначить соответствующее лечение.
Основные термины: бронхиальная астма, конрролируемая бронхиальная астма, триггеры, внутренние факторы, легкая интермитирующая бронхиальная астма, легкая персистирующая астма, персистирующая астма средней тяжести, тяжелая персистирующая астма, бронходилататоры, базисная терапия бронхиальной астмы.
Бронхиальная астма – хроническое воспалительное заболевание дыхательных путей, сопровождающееся гиперреактивностью бронхов, кашлем, одышкой и приступами удушья, вызванными нарушением бронхиальной проходимости разной степени и выраженности.
Термин происходит от греческого слова – одышка, удушье.
По данным статистики число больных бронхиальной астмой в странах Европы и США в настоящее время достигает 5-7% от общей численности населения. При этом среди детей распространенность заболевания составляет 10-15%. В последние годы наблюдается увеличение не только числа случаев астмы, но и углубляется тяжесть течения заболевания. Это связано с загрязнением окружающей среды и появлением большого числа новых негативно действующих пневмофакторов, с ослаблением иммунитета, ростом стрессовых ситуаций. Несмотря на успехи, достигнутые в лечении данного страдания, смертность от астмы не снижается. По данным профессора Rabe (U.K.) в 2004 году только 10-15 % больных имели контролируемую астму, а в 2006 г это число снизилось до 5%.
Этиологические факторы вызывающие бронхиальную астму можно разделить на две группы. Факторы риска, которые предопределяют возможность развития заболевания и состояния, реализующие эту предопределенность.
Основным фактором риска является наследственность. Наличие предрасположенности достаточно очевидно в связи с преобладанием случаев астмы среди родственников. Наследование предрасположенности к данной патологии связано с различными генами, определяющими способность к гиперпродукции IgE, склонность к развитию сенсибилизации. Первый признак связан с В-лимфоцитами и наследуется по аутосомно-рецессивному типу. Другой признак, связанный с повышенной восприимчивостью к аллергии, определяется типами генов иммунного ответа, экспрессированными на Т-лимфоцитах. Функция Т-системы лимфоцитов обусловливается соотношением ее супрессорной и хелперной активности. Именно с повышенной хелперной активностью клеток связывают участие Т-лимфоцитов в развитии аллергического воспаления. Генетически обусловлено и образование интерлейкинов, определяющих стимуляцию синтеза IgE, дифференцировку базофилов, эозинофилов из предшественников и их миграцию в ткань бронхов. Наследственная предрасположенность вызывает развитие спастической реакции в ответ на гистамин, в то время как введение гистамина здоровым людям не приводит к бронхоспазму.
Развитие бронхиальной астмы связано с разнообразными факторами внешней среды, стимулирующими иммунопатологические реакции в бронхах, изменение свойств их ткани, нервно-рефлекторное раздражение, определяющее и поддерживающее бронхоспазм. Наибольшее значение имеют соединения, поступающие в организм с вдыхаемым воздухом (пневмоаллергены), а также компоненты пищевых продуктов, приобретающих свойства аллергена в результате их расщепления и всасывания в кровь через кишечную стенку. Среди пневмоаллергенов наиболее распространенны пыльца растений и трав, домашняя пыль и ее компоненты (особенно микроскопические клещи и продукты их метаболизма), частички эпидермиса, шерсть и перья домашних животных, споры плесневых грибов. Достаточно большое значение имеют две группы факторов: связанных с содержанием в атмосфере различных загрязняющих веществ и влияющих на развитие профессиональной бронхиальной астмы в условиях производственного контакта.
Отдельная проблема связана с курением. Курение, безусловно, является фактором, стимулирующим гиперреактивность бронхов. Имеется положительная зависимость между курением и умеренным повышением уровня антител. Однозначная статистика существует для астмы в детском возрасте: частота развития заболевания в раннем детстве совпадает с курением матери в период беременности и грудного вскармливания.
В развитии бронхиальной астмы имеют значение вирусные (в большей степени), бактериальные и грибковые инфекции. Внедрение вируса в дыхательные пути закономерно вызывает транзиторную гиперреактивность бронхов, сохраняющуюся в течение нескольких недель с начала заболевания. Вирус нарушает целостность дыхательного эпителия, повышает его проницаемость, облегчает доступ различных раздражителей к ирритантным рецепторам блуждающего нерва и стимуляцию бронхоспазма. Существенное значение имеет вовлечение периферических отделов бронхиального дерева. Особенность бактериальной инфекции при астме связана с участием не только патогенных, но условно патогенных и сапрофитных микроорганизмов, преобладанием сенсибилизирующего эффекта над токсическим.
Лекарственная аллергия является распространенным фактором риска при бронхиальной астме. При этом прямым противопоказанием для больных данной патологией является назначение β-адреноблокаторов.
Бронхоспазм в ответ на вдыхание холодного воздуха и изменение его влажности представляет характерный признак астмы. Его выраженность соответствует степени гиперреактивности бронхов. Механизм спазма связан с непосредственным раздражением ирритативных рецепторов и/или набуханием слизистой оболочки бронхов в условиях повышенной влажности с последующей дегрануляцией тучных клеток и высвобождением из них медиаторов бронхоспазма. Развитие внезапного тяжелого приступа астмы возможно при резком изменении окружающей температуры.
Провокаторами, реализующими возможность развития бронхиальной астмы, являются также сопутствующие заболевания (заболевания носоглотки, тиреотоксикоз, желудочно-пищеводный рефлюкс и др.).
Выраженное проявление эмоций могут приводить к гипервентиляции и вызывать бронхоспазм.
В основе патогенеза бронхиальной астмы лежат две основные закономерности: гиперреактивность бронхиального дерева и характерная картина воспалительного процесса. При этом каждый из механизмов стимулирует и поддерживает развитие другого.
Особенности воспаления при бронхиальной астме. Пусковым механизмом заболевания является повышенная дегранулирующая активность тучных клеток бронхов. В норме количество тучных клеток возрастает по направлению от внутренней поверхности (просвета) бронхов глубину, достигая максимума в составе базальной мембраны и далее. При астме эта закономерность приобретает противоположный характер: наблюдается повышенная инфильтрация тучными клетками эпителиального слоя, при этом эти клетки обладают постоянной дегранулирующей активностью. Основным медиатором тучных клеток является гистамин. Спастическая реакция в ответ, на который — один из основных признаков гиперреактивности бронхов. Кроме того, тучные клетки продуцируют специальный фактор хемотаксиса эозинофилов, стимулирующий миграцию эозинофилов к месту дегрануляции. Во всех случаях астмы находят активированные или разрушенные эозинофилы в тканях бронхов и повышенное содержание эозинофильных белков в их промывных водах. Из эозинофилов выделяется медленно реагирующая субстанция аллергии. По сравнению с гистамином, спазмогенный эффект этого вещества выражен более чем в 1000 раз и проявляется в течение нескольких часов после действия аллергена и, наряду со спазмом мускулатуры, сопровождается расширением посткапиллярных венул, выпотом из сосудов, отеком ткани и повышенным слизеобразованием. Состав медленно реагирующий субстанции определяют лейкотриены, обладающие выраженной спазмогенной и воспалительной активностью.
Наряду с характерной для астмы кооперацией тучных клеток и эозинофилов, в процесс воспаления закономерно вовлекаются другие клетки бронхов, в частности, макрофаги, лимфоциты, нейтрофилы. Макрофаги стимулируют реакции тканевого воспаления путем синтеза простагландинов, лейкотриенов, других факторов и, в первую очередь, цитокинов, вовлекающих в дальнейший процесс различные типы клеток. Совместно с макрофагами, способностью к образованию цитокинов обладают клетки бронхиального эпителия. Они первыми вступают в контакт с пневмофакторами окружающей среды. В процессе развития бронхиальной астмы эпителий подвергается необратимому повреждению вплоть до обнажения подлежащей пластинки и массивного слущивания клеток в просвет бронхов. Кроме того, эпителиальные клетки больных астмой отвечают более выраженной продукцией цитокинов по сравнению со здоровыми людьми, и эта особенность еще больше проявляется на фоне активации воспалительного процесса. Участие цитокинов стимулирует различные этапы воспалительной реакции бронхов и создает устойчивую кооперацию клеток, поддерживающую течение воспалительного процесса. Еще одним важным фактором воспаления при астме являются нейтрофилы. Они не участвуют в немедленной бронхоспастической реакции, а вовлекаются в процесс постепенно. При дегрануляции из тучных клеток высвобождается специальный фактор хемотаксиса нейтрофилов. Стимулированные нейтрофилы мигрируют из крови в ткань и вызывают поздний и повторный бронхоспастический эффект спустя 4 часа после «немедленного» бронхоспазма. Если патологический процесс принимает устойчивый характер, нейтрофилы инфильтрируют стенку бронха, создавая лейкоцитарный вал вокруг источника воспаления, и провоцируют дальнейшие изменения в ткани за счет высвобождения собственных медиаторов: простагландинов, лейкотриенов и лизосомальных ферментов, вызывающих дезорганизацию ткани бронха и развитие устойчивого повреждения. С активностью этих реакций связан переход к хроническому течению астмы с устойчивой обструкцией дыхательных путей, постоянным отеком слизистой оболочки бронхов. У больных бронхиальной астмой по сравнению со здоровыми людьми усилена агрегация тромбоцитов, а также повышено их отложение в ткани бронхов. Тромбоциты содержат вещества, обладающие спазмогенной активностью. Источником привлечения тромбоцитов является специальный фактор их агрегации, высвобождающийся из различных клеток, участвующих в воспалении бронхов. Этот фактор обладает бронхоспастической активностью, является мощным индуктором внутрисосудистой проницаемости и отека дыхательных путей, причем способен оказывать не только быструю спастическую реакцию (подобно гистамин-индуцированному бронхоспазму), но отсроченную и замедленную (при действии медиаторов из макрофагов и нейтрофилов).
Таким образом, в воспалении при бронхиальной астме участвуют многие клеточные элементы и выделяющиеся из них биологически активные вещества.
Гиперреактивность бронхов при бронхиальной астме. Гиперреактивность представляет собой устойчивую спастическую реакцию бронхов по отношению к факторам окружающей среды и внутренним медиаторам воспаления. Изменение бронхиального тонуса подвержено закономерным колебаниям в связи с биологическими ритмами организма, возрастом, влиянием эндокринного профиля. Повышение реактивности бронхов закономерно проявляется при инфекциях дыхательных путей, в первую очередь, вирусных, и при контакте с различными неблагоприятными факторами среды. В этих случаях гиперреактивность имеет транзиторный характер, при выздоровлении постепенно нормализуется или становится устойчивой в связи с длительным попаданием раздражителя в бронхи.
Гиперреактивность связана с сочетанным проявлением нескольких признаков: активацией кашлевого рефлекса, усиленным слизеобразованием, повышением тонуса гладкой мускулатуры. Повышенная реактивность бронхов сопровождается нарушением нервной регуляции бронхиального тонуса и повышением чувствительности к тканевым факторам бронхоспазма. Развитие гиперреактивности связано с повышением тонуса блуждающего нерва. У больных бронхиальной астмой наблюдается увеличение массы мускулатуры стенки бронхов. Независимо от того, первично ли это явление (определяет склонность к бронхоспазму) или вторично (развивается как результат болезни), объем мышечной ткани влияет на спастическую активность.
В GINA 2002 г. Предусмотрено выделение четырех степеней тяжести течения БА. (4 ступени заболевания). К критериям, определяющим степень тяжести, относят количество ночных и дневных приступов затруднения дыхания, выраженность нарушения физической активности и сна, частоту применения β2— адреномиметиков короткого действия, изменение показателей ОФВ1 и ПСВ, а также суточное изменение ПСВ.
I ступень: легкая интермиттирующая астма – симптомы заболевания возникают в ночное время не чаще 2 раз в месяц, в дневное время не чаще 1 раза в неделю. ОФВ1 и ПСВ составляют 80 % от должных величин, суточное изменение ПСВ менее 20%. Качество жизни не страдает.
II ступень: легкая персистирующая астма – симптомы возникают в ночное время чаще 2 раз в месяц, в дневное время чаще 1 раза в неделю, но не ежедневно. ОФВ1 и ПСВ вне приступа составляют 80 % от должных величин, суточное изменение ПСВ 20-30%. Обострения могут нарушать нормальную активность и сон.
III ступень: персистирующая астма средней степени тяжести – симптомы заболевания возникают ежедневно, в ночное время чаще 1 раза в неделю. ОФВ1 и ПСВ составляют 60-80 % от должных величин, суточные колебания ПСВ превышают 30%. Необходим ежедневный прием β2— адреномиметиков короткого действия. Снижается качество жизни больных.
IV ступень: тяжелая персистирующая астма — симптомы заболевания возникают несколько раз а течении дня и ночью. ОФВ1 и ПСВ ниже 60 % от должных величин, суточные колебания ПСВ превышают 30%. Частый ежедневный прием β2-адреномиметиков короткого действия. Значительно изменяется качество жизни больных.
В пересмотре GINA 2006 г. Рекомендуется классификация по степени контроля (контролируемая, частично контролируемая и неконтролируемая БА), отражающая представление о том, что степень тяжести БА зависит не только от выраженности ее проявлений, но и ответа на терапию.
Контролируемая БА: дневные симптомы отсутствуют (или ≤ 2 эпизодов в неделю), ночные симптомы отсутствуют, показатели ОФВ1 и ПСВ в N, обострения отсутствуют, потребность в бронходилататорах отсутствует (или ≤ 2 эпизодов в неделю).
Частично контролируемая БА: дневные симптомы > 2 эпизодов в неделю, ночные симптомы любые, показатели ОФВ1 и ПСВ 2 эпизодов в неделю.
Неконтролируемая БА: наличие трех или более признаков частично контролируемой БА в течение любой недели, обострение 1 в течение любой недели.
Клинические проявления бронхиальной астмы.
При обострении заболевания характерны приступ удушья или экспираторная одышка (укорочения вдоха при удлинении выдоха), раздувание крыльев носа при вдохе, прерывистая речь, возбуждение, постоянный или эпизодический кашель, возможно участие в акте дыхания вспомогательной дыхательной мускулатуры, могут быть сухие, свистящие хрипы, усиливающиеся на вдохе и выслушиваемые на расстоянии (дистанционные хрипы). При тяжелом течении приступа пациент сидит, опираясь руками о колени, при легком течении заболевания больной сохраняет нормальную активность. Кашель при бронхиальной астме отличается рядом особенностей: имеет сухой приступообразный характер как ″дебют″ астматического приступа, при прогрессировании приступа исчезает, возобновляется при разрешении приступа с отхождением вязкой мокроты (″слепков бронхов″). Для больных астмой характерно скудное и трудное отделение мокроты, которая чаще имеет слизистый характер, белый цвет. При объективном обследовании во время приступа удушья нижние края легких опущены, их подвижность ограничена, при перкуссии возможен звук с коробочным оттенком, при аускультации часто выслушиваются сухие хрипы на фоне дыхания с удлиненным выдохом. Однако даже на фоне выраженного приступа удушья сухие хрипы могут отсутствовать, что предположительно связано с преобладающим вовлечением в процесс мелких бронхов. При развитии эмфиземы легких к проявлениям бронхиальной астмы присоединяются симптомы эмфиземы. Вне приступа удушья возможно отсутствие физикальных симптомов заболевания.
Лабораторная диагностика бронхиальной астмы.
Мокрота больных бронхиальной астмой содержит ряд характерных элементов:
— спирали Куршмана, представляющие собой штопорообразно извитые сгустки слизи (слепки бронхов), отделяющиеся по мере выхода больного из состояния приступа удушья,
— кристаллы Шарко-Лейдена, состоящие из продуктов разрушенных эозинофилов,
— тельца Креола, представляющие скопления эпителиальных клеток бронхов,
— метахроматические клетки (тучные клетки, базофилы).
В клиническом анализе крови пациентов с бронхиальной астмой отмечается эозинофилия. У больных с инфекционно-зависимым вариантом астмы могут регистрироваться лейкоцитоз на фоне эозинофилии крови, увеличение СОЭ.
Определение наличия характера сенсибилизации требует проведения специфической диагностики: постановки кожных проб с предполагаемыми аллергенами, определения уровня IgE в крови и антител этого класса иммуноглобулинов.
Представление о функции внешнего дыхания основано на определении ряда показателей спирографии – ОФВ1 (объем форсированного выдоха за первую секунду) и ФЖЭЛ (форсированная жизненная емкость легких). При этом в плане проведения дифференциальной диагностики с хронической обструктивной болезнью легких, хроническим обструктивным бронхитом имеет значение проведение пробы с бронходилятатором (β2— адреномиметиком короткого действия) – абсолютный прирост ОФВ1 более чем на 200 мл и прирост бронходилатационного коэффециента (ʌ ОФВ1 = ОФВ1 исх. в мл-ОФВ1 дилат. в мл/ ОФВ1 исх. в млX100%) ≥ 15% от исходных показателей свидетельствует об обратимости обструкции и характерен для бронхиальной астмы.
Однако величина ОФВ1 преимущественно отражает состояние крупных бронхов, на которые в большей степени приходится сопротивление воздушному потоку в начале выдоха. Для оценки состояния не только крупных бронхов, но и бронхов более мелкого калибра проводят плетизмографию.
С целью самоконтроля больных за своим состоянием широкое использование получило определение пиковой скорости форсированного выдоха (ПСВ) с помощью пикфлоуметра. Это исследование, проводимое ежедневно 2 раза в день, позволяет диагностировать обструкцию бронхов на ранних сроках развития бронхиальной астмы, оценить тяжесть течения заболевания, степень гиперреактивности бронхов и эффективность лечения.
Во время развития приступа бронхиальной астмы содержание кислорода в крови снижается в зависимости от выраженности спазма бронхов и объема захваченной им дыхательной поверхности. При этом участки легких с сохранившейся вентиляцией берут на себя компенсаторную функцию по удалению углекислоты, что вместе с увеличением частоты дыхания приводит к снижению ее уровня в крови. Таким образом, вслед за состоянием гипоксемии проявляется гипокапния и происходит сдвиг величины рН в щелочную сторону (состояние компенсированного алкалоза). Если степень бронхиальной обструкции продолжает нарастать, то нормально функционирующие альвеолы уже не справляются с компенсаторной функцией выведения углекислоты. Ее напряжение в крови постепенно возрастает. Гипокапния сменяется нормокапнией, а затем гиперкапнией, на фоне постоянно возрастающей гипоксемии. Состояние алкалоза сменяется ацидозом: дыхательным – за счет увеличения напряжения углекислоты и метаболическим – за счет недоокисленных продуктов.
При тяжелом течении бронхиальной астмы на ЭКГ выявляются перегрузка и/или гипертрофия правого желудочка, нарушения проводимости по правой ножке пучка Гиса. Во время приступа астмы возможна тахикардия, которая уменьшается в межприступный период.
Для бронхиальной астмы характерны скудность и отсутствие специфических рентгенологических признаков, часто обнаруживается повышенная воздушность легких.
Лечение бронхиальной астмы.
Все препараты, применяемые при лечении бронхиальной астмы, делятся на две группы:
Средства для профилактики приступов заболевания (не купируют приступ удушья!) составляют базисную терапию — стабилизаторы мембран тучных клеток, глюкокортикоиды, антагонисты лейкотриеновых рецепторов, β2-адреномиметические средства длительного действия.
Бронхорасширяющие препараты, используемые для купирования приступов астмы, дают симптоматический эффект и частота их применения служит индикатором эффективности базисной терапии — β2-адреномиметические средства короткого действия, М-холиноблокаторы, препараты теофиллина.
Глюкокортикоиды обладают широким спектром иммуномодулирующего и противовоспалительного действия: блокируют синтез простагландинов и лейкотриенов, подавляют синтез и эффекты цитокинов, стимулируют созревание β-адренергических рецепторов клеток и, тем самым, восстанавливают чувствительность клеток к действию адренергического стимула, влияют на систему иммунитета, преимущественно на Т-лимфоциты, уменьшая иммунологическое воспаление в ткани бронхов, подавляют дегрануляция тучных клеток и базофилов, угнетают активность слизеобразования, как базального, так и индуцированного медиаторами воспаления. В качестве препаратов первой линии в лечении БА рассматриваются ингаляционные глюкокортикостероиды (ИГКС), т.к. их действие является местным и, следовательно, они имеют большую безопасность при длительном применении, по сравнению с системными глюкокортикостероидами (СГКС). Побочные эффекты ИГКС: орофарингеальный кандидоз, дисфония вследствии миопатии или пареза мышц голосовых связок, раздражение слизистой глотки. Дозировка ИГКС определяется достижением контроля БА, целезообразно использовать высокие начальные дозы со снижением до поддерживающих (оптимальный срок применения до пересмотра дозы не менее 3 месяцев). Дозу распределяют на 2-3 приема, предпочтительно использовать спейсер, после ингаляции полоскать полость рта.
Будесонид (бупранал, транстек, эднок),
беклометазон (альдецин, бекотид, беклазон Эко),
флутиказон+салметерол (серетид, серетид мультидиск),
СГКС назначают тогда, когда не достигнут эффект ИГКС (как дополнение к ИГКС). После получения желаемого эффекта дозу СГКС следует постепенно снижать до минимальной, при которой сохраняется терапевтический эффект или до полной отмены. Предпочтение отдается СГКС средней продолжительности действия (преднизолон, метилпреднизолон). Назначают СГКС в виде одной утренней дозы или большую часть препарата (2/3-3/4) утром меньшую часть днем.
Механизм действия стабилизаторов мембран тучных клеток состоит в снижении чувствительности тучных клеток к дегранулирующим агентам: специфическим при действии аллергена на сенсибилизированную клетку и неспецифическим – при прямом дегранулирующем эффекте химических и физических факторов, за счет уменьшения концентрации внутриклеточного кальция, включающего механизмы дегрануляции. Предварительное введение препаратов этой группы предотвращает или уменьшает выраженность бронхоспазма в ответ на последующее поступление аллергена. При этом снижается уровень гистамина, стимулирующего бронхоспазм по немедленному типу, и факторов хемотаксиса, привлекающих эозинофилы и нейтрофилы в очаг воспаления бронхов. Кроме того, установлено непосредственное действие стабилизаторов мембран тучных клеток на активность эозинофилов, нейтрофилов, моноцитов. Таким образом, подавляется не только ранняя, но и поздняя фаза астматической реакции, спустя 3-4 часа после провоцирующего действия. Данная группа препаратов эффективно предупреждают приступы удушья, провоцируемые физической нагрузкой, а также при атопической астме, связанной с прогнозируемым повышением содержания аллергена в воздухе (в первую очередь при пыльцевой астме).
Кетотифен (кетостерил, задитен) 1мг×2 р, per os;
кромоглициевая кислота (ифирал, кромогексал) – 20 мг×4р, ингаляционно;
недокромил натрия 4 мг×2-4р, ингаляционно;
кромогликат натрия (интал, кромоген) 1-2 мг×3-4р, ингаляционно. Комбинированные препараты (стабилизаторы мембран тучных клеток + β2-адреномиметики) интал+, дитек.
Антагонисты лейкотриеновых рецепторов — фармакологическая активность препаратов проявляется на основных клетках мишенях, участвующих в патогенезе астмы (эозинофилах, нейтрофилах, моноцитах, тучных клетках): длительное использование снижает активность немедленной и замедленной фазы астматической реакции, уменьшает гиперреактивность бронхов. Эта группа препаратов является терапией выбора при аспириновой бронхиальной астме. Используются с сочетанной терапии при применении ИГКС (усиливая их действие).
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Исследование функции внешнего дыхания у больных бронхиальной астмой является обязательным и позволяет объективизировать степень бронхиальной обструкции, ее обратимость и вариабельность (суточные и недельные колебания), а также эффективность проводимого лечения.

Спипография — графическая регистрация объема легких во время дыхания Характерными спирографическими признаками нарушения бронхиальной проходимости у больных бронхиальной астмой являются следующие:
- снижение форсированной жизненной емкости легких (ФЖЕЛ) и объема форсированного выдоха за первую секунду (ОФВ1), причем ОФВ — наиболее чувствительный показатель, отражающий степень бронхиальной обструкции;
- снижение индекса Тиффно (соотношение ОФВ1/ЖЕЛ), как правило он менее 75%. При бронхиальной обструкции снижение ОФВ более выражено, чем ФЖЕЛ1, поэтому индекс Тиффно всегда снижается.
Измерение указанных подателей следует производить 2-3 раза и за истинное значение принимать наилучший показатель. Полученные абсолютные величины сопоставляют с должными, которые вычисляют по специальным номограммам с учетом роста, пола, возраста пациента. Кроме вышеназванных изменений спирограммы, при обострении бронхиальной астме значительно возрастает остаточный объем легких и функциональная остаточная емкость.
При частых обострениях заболевания и развитии эмфиземы легких выявляется снижение жизненней емкости легких (ЖЕЛ).
Пневмотахография регистрация в двухкоординатной системе петли «поток-объем» — скорости экспираторного потока воздуха на участке 25-75% ФЖЕЛ, т.е. у середине выдоха. С помощью этого метода рассчитывают пиковуно объемную скорость (ПОС), максимальные объемные скорости иа уровне 25%, 50%, 75% ФЖЕЛ (МОС25, МОС50, М0С75) и средние объемные скорости СОС25, 75.
По данным пневмотахографии (анализа петли «поток-объем») можно диагностировать нарушение бронхиальной проходимости на уровне крупных, средних или мелких бронхов. Для обструкции преимущественно на уровне центральных дыхательных путей, крупных бронхов характерно выраженное снижение объемной скорости форсированного выдоха в начальной части нисходящей ветви кривой «поток/объем» (ПОС и МОС25 в % к должным величинам снижены более значительно, чем MOC50 и МОС75). При периферической бронхиальной обструкции, наблюдающейся при бронхиальной астме, характерны вогнутый xaрактер кривой выдоха ц значительное снижение максимальной объемной скорости на уровне 50-75% ФЖЕЛ (МОС50, МОС75).
Определение ОФВ1 индекса Тиффно и пневмотахографию с построением кривой «поток-объем» целесообразно проводить до и после применения бронходилататоров, а также для оценки степени тяжести заболевания и контроля за течением бронхиальной астмы (2 раза в год).
Пикфлуометрия — метод измерения максимальной (пиковой) объемной скорости воздуха во время форсированного выдоха (пиковой скорости выдоха) после полного вдоха.
Показатель пиковой скорости выдоха (ПСВ) тесно коррелирует с ОФВ1. В настоящее время сконструированы и широко применяются портативные индивидуальные пикфлоуметры. Пикфлоуметрия проводится несколько раз в течение суток, до и после приема бронходилататоров. Обязательным является измерение ПСВ утром (сразу после подъема больного), затем через 10-12 ч (вечером). Пикфлоуметрия должна производиться врачом во время приема больного, а также ежедневно самим больным. Это позволяет сказать о стабильности и тяжести течения бронхиальной астмы, выявить факторы, вызывающие обострение заболевания, эффективность проводимых лечебных мероприятий.
Нормальные величины ПСВ у взрослых можно определить с помощью номограммы.
Для достоверной бронхиальной астмы характерны следующие изменения ПСВ:
- увеличение ПСВ более, чем на 15% через 15-20 минут после ингаляции бета2-стимуляторов короткого действия;
- суточные колебания ПСВ составляют 20% и более у больных, получающих бронхолитики, и 10% и более у пациентов без бронхолитической терапии;
Суточные колебания ПСВ определяются по следующей формуле:
Суточные колебания ПСВ в % (ПСВ сут в %) = ПСВ макс — ПСВ мин / ПСВ средн х 100%
- уменьшение ПСВ на 15% и более после физической нагрузки или после воздействия других триггеров.
Бронходилатационные пробы используются для уточнения степени обратимости бронхиальной обструкции. Определяют показатели ОФВ1, индекс Тиффно, показатели кривой «поток-объем» (пневмотахографии) и пикфлоуметрии до и после применения бронходилататора. О состоянии бронхиальной обструкции судят на основании абсолютного прироста ОФВ1 (Δ ОФВ1исх%)»
ΔОФВ1исх % = ОФВ1дилат (мл)-ОФВ1исх(мл) / ОФВ1исх(мл) х 100%
Примечания: ОФВ1дилат (мл) — объем форсированного выдоха за первую секунду после применения бронходилататоров; ОФВ1 исх (мл) — объем форсированного выдоха за первую секунду исходный, до применения бронходилататоров.
Специфических изменений при рентгенологическом исследовании легких не выявляется. Во время приступа бронхиальной астмы, а также при частых ее обострениях обнаруживаются признаки эмфиземы легких, повышенная прозрачность легких, горизонтальное положение ребер, расширение межреберных промежутков, низкое стояние диафрагмы
При инфекционно-зависимой бронхиальной астме рентгенологическое исследование может выявить признаки, характерные для хронического бронхита (см соответствующую главу), пневмосклероза.
Во время приступа бронхиальной астмы обнаруживаются признаки повышенной нагрузки на миокард правого предсердия: высокие остроконечные зубцы Р в отведениях II, III, aVF,V„ V„ возможен поворот сердца вокруг продольной оси по часовой стрелке (правым желудочком вперед), что проявляется появлением глубоких зубцов S в грудных отведениях, в том числе и в левых. После купирования приступа указанные ЭКГ-изменения исчезают. При тяжелом течении бронхиальной астмы, частых ее обострениях постепенно формируется хроническое легочное сердце, что проявляется ЭКГ-признаками гипертрофии миокарда правого предсердия и правого желудочка.

Определение газового состава артериальной крови позволяет более объективно оценить тяжесть обострения заболевания, а также является необходимым при астматическом статусе. Выраженная бронхиальная обструкция (ОФВ1 — 30-40% от должного, ПСВ

- Клиническое наблюдение и выявление глюкокортикоидной недостаточности: отсутствие эффекта при длительном лечении глюкокортикоидами, кортикозависимость, возникновение пигментации кожи, наклонность к артериальной гипотензии, ухудшение состояния (иногда развитие астматического состояния) при отмене преднизолона или уменьшении дозы.
- Снижение содержания в крови кортизола, 11-ОКС, уменьшение выделения с мочой 17-ОКС, недостаточное повышение экскреции с мочой 17-ОКС после введения адренокортикотропного гормона, уменьшение количества глюкокортикоидных рецепторов на лимфоцитах.

- Ухудшение состояния больной перед или во время менструального цикла, в связи с беременностью и во время климакса.
- Цитологическое исследование влагалищного мазка: признаки уменьшения содержания прогестерона (неполноценность второй фазы цикла или ановуляция).
- Измерение базальной (ректальной) температуры: снижение во вторую фазу менструального цикла.
- Радиоиммунологическое определение содержания эстрогенов и прогестерона в плазме крови: повышение содержания эстрогенов во вторую фазу менструального цикла, нарушение соотношения эстрогены/прогестерон.

- Тяжелое, беспрерывно рецидивирующее течение заболевания (при исключении других причин тяжести течения болезни).
- Положительная внутрикожная проба с аутолимфоцитами.
- Высокий уровень кислой фосфатазы в крови.
- Положительная РБТЛ с фитогемагглютинином.
- Снижение в крови уровня комплемента и выявление циркулирующих иммунных комплексов, противолегочных антител.
- Наличие выраженных, часто инвалидизирующих осложнений глюкокортикоидной терапии.

- Клиническое наблюдение — выявление факторов, способствующих формированию адренергического дисбаланса: чрезмерное применение симпатомиметиков, вирусная инфекция, гипоксемия, ацидоз, эндогенная гаперкатехоламинемия вследствие стрессовой ситуации, трансформация приступа бронхиальной астмы в астматический статус.
- Парадоксальное действие симпатомиметиков — усиление бронхоспазма при их использовании.
- Лабораторная и инструментальная диагностика:
- функциональное исследование проходимости бронхов до и после ингаляции селективных бета2-адреномиметиков: отсутствие возрастания или уменьшение ФЖЕЛ, скорости выдоха после ингаляции симпатомиметика;
- снижение степени гипергликемического ответа на адреналин, появление парадоксальных реакций (снижение уровня глюкозы в ответ на введение адреналина);
- эозинопенический тест с адреналином: снижение эозинопенического ответа на введение адреналина (абсолютное количество эозинофилов в 1 мм 3 крови уменьшается в ответ на введение адреналина менее чем на 50 %);
- гликогенолиз лимфоцитов: снижение степени гликогенолиза в лимфоцитах после инкубации с адреналином.

- Выявление нарушений нервно-психической сферы в преморбидном периоде, в процессе развития заболевания, по данным анамнеза — психологические особенности личности; наличие в анамнезе психических и черепно-мозговых травм, конфликтных ситуаций в семье, на работе, расстройств в сексуальной сфере, ятрогенных воздействий, диэнцефальных нарушений.
- Уточнение нервно-психических патогенетических механизмов (производится психотерапевтом) — определяются истероподобный, неврастеноподобный, психастеноподобный механизмы, которые способствуют возникновению приступов удушья.

- Нарушение бронхиальной проходимости преимущественно на уровне крупных и средних бронхов.
- Бронхорея.
- Высокая эффективность ингаляционных холинолитиков.
- Системные проявления ваготонии — частое сочетание с язвенной болезнью двенадцатиперстной кишки, гемодинамические расстройства (брадикардия, гипотензия), мраморность кожи, потливость ладоней.
- Лабораторные признаки: высокое содержание в крови ацетилхолина, значительное снижение активности сывороточной холинэстеразы, повышение содержания в крови и моче циклического гуанозинмонофосфата.
- Выявление преобладания тонуса парасимпатической нервной системы методом вариационной пульсометрии.

- Клинические наблюдения — возникновение приступов удушья после физической нагрузки, при вдыхании холодного или горячего воздуха, перемене погоды, от резких запахов, табачного дыма при отсутствии доказательств ведущей роли других патогенетических механизмов, формирующих измененную реактивность.
- Снижение показателей бронхиальной проходимости, по данным спирографии и пикфлоуметрии, пробы с вдыханием холодного воздуха, ацетилхолином, PgF2а, обзиданом.
- Положительный ацетилхолиновый тест. Непосредственно перед исследованием готовят растворы ацетилхолина в концентрациях 0.001%; 0.01%; 0.1%; 0.5% и 1% и определяют ОФВ1 и индекс Тиффно. Затем с помощью аэрозольного ингалятора больной вдыхает аэрозоль ацетилхолина в самом высоком разведении (0.001%) в течение 3 минут (если у больного начинается кашель ранее 3 минут — ингаляцию прекращают раньше).
Через 15 минут оценивают состояние больного, производят аускультацию легких и определяют ОФВ1 и индекс Тиффно. Если по клиническим и инструментальным данным нарушений бронхиальной проходимости не выявляется, повторяют исследование со следующим разведением. Тест считается положительным, если индекс Тиффно падает на 20% и более. Даже реакция на 1% раствор учитывается как положительная. Положительный ацетилхолиновый тест патогномоничен для всех форм бронхиальной астмы.
В ряде случаев для определения гиперреактивности бронхов применяется ингаляционный гистаминовыи тест. В этом случае концентрация гистамина
Портал iLive не предоставляет медицинские консультации, диагностику или лечение.
Информация, опубликованная на портале, предназначена только для ознакомления и не должна использоваться без консультации со специалистом.
Внимательно ознакомьтесь с правилами и политикой сайта. Вы также можете связаться с нами!
Copyright © 2011 — 2019 iLive. Все права защищены.
источник

Обследование, основанное на сборе анамнеза, внешнем осмотре, пальпации, прослушивании и простукивании называется физикальным. Именно с такого метода диагностики начинается определение типа болезни.

- В каком возрасте начались астматические приступы, возможно какие детские болезни привели к астме. Это может быть коклюш, корь и другие, которые могут негативно повлиять на дыхательную систему.
- Были ли среди родственников астматики, это позволяет проследить генетическую связь, возможно кто-то из близких имел сильные аллергии.
- С какими раздражителями связаны приступы. Такие раздражители называются триггерами, и среди них может быть физическая нагрузка, холодный влажный воздух, микроскопические частицы шерсти и кожи собак, кошек, пыльца цветов разных растений, запыленность в помещении пылью определенного типа, продукты питания.
- Нужно узнать, как именно проходят приступы. Ведь при астматическом кашле пациенты принимают положение, при котором вдох менее мучительный, например, опираются руками о стол, расслабляя при этом плечевой пояс.
- Есть ли звуки при кашле, ведь свист при дыхании — это признак астматического сужения бронхов. Чтобы услышать характерные звуки при дыхании и приступах, не нужно прослушивать грудь стетоскопом, их хорошо слышно и на небольшом расстоянии.
- Долго ли длится приступообразный кашель, пропадает ли он после приема бронхолитических лекарств.
- После приступа наблюдается выделения вязкой, но прозрачной, как стекло мокроты, которая освобождает бронхи, таким образом облегчается дыхание, такие особенности также нужно узнавать при опросе.
Внешний осмотр проходит следующим образом:
- Врач смотрит на грудную клетку, которая может иметь вид, похожий на бочку. Такую форму грудная клетка приобретает вследствие развития эмфиземы, расширения легких, и, как результат — увеличение размеров грудной клетки;
-
Прослушивание проходит через стетоскоп, стетофонендоскоп или фонендоскоп, причем последний наиболее подходит для изучения звуков, издаваемых грудной клеткой при астме. Если происходит обострение, свист и характерные хрипы слышны по всей легочной поверхности, но при ремиссии свистящий хрип слышен снизу от лопаток и то только при усиленном вдохе.
- Постукивание пальцами не может эффективно сообщить информацию на ранних этапах астмы. Но если болезнь длится долго, то пальпацией и постукиванием можно услышать пустоту (звук картонной коробки), которая образовалась из-за эмфиземного расширения легких.
Лабораторные исследования проводятся в следующих направлениях:
- анализ крови направлен на определение количества эозинофилов — этот вид лейкоцитов является показателем аллергических процессов в организме;
-
если в анализе крови отсутствуют признаки воспалительных процессов и токсинов, выделяемых бактериями, то при наличии астматических симптомов доктору легче отличить астму от обычного бронхита или пневмонии;
- в мокроте под микроскопом можно обнаружить эозинофилы;
- в анализе мокроты присутствуют кристаллические вкрапления — особенные кристаллы Шарко-Лейдена и спиралевидные кристаллы Куршмана;
- мокрота при астме специфическая, отличается от мокроты при бронхите, структура двухслойная, консистенция густая, по густоте вязкая;
- методом проделывания царапин на коже (скарификации) берут пробы на аллергены, по которым уточняют аллергический возбудитель (триггер) бронхоспазма, аллергены вызывают на коже покраснение и зудящие ощущения;
- кал берут для определения гельминтов, которые могут размножиться до инвазивного количества и вызвать аллергическую интоксикацию организма, что также может влиять на возникновение приступов.
С помощью специально разработанных аппаратов проводится инструментальная диагностика. На первом месте в аппаратной диагностики стоит пикфлуометрия. На пикфлоуметре, который являет собой трубочку с нанесенной шкалой, измеряется самая большая скорость потока воздуха при выдохе, сделанном с максимальным усилием (форсированный выдох). Такая пиковая скорость выдоха называется ПСВ. Этот тест доступен детям с четырех лет, также он применяется и для взрослых.
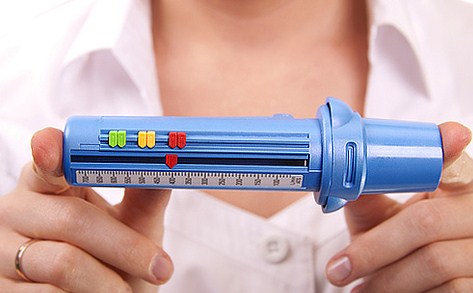
Измерительные процессы проводятся дважды в день, сутра и ближе к вечеру. Делаются три попытки, из которых выбирается та, которая сделана наиболее правильно. На трубку нанесена шкала с зеленой, желтой и красной зоной, которые обозначают степень проблемы. Но эта шкала не унифицирована, она подбираются путем индивидуальных двухнедельных исследований каждого больного. Если показатели в зеленой зоне, значит, что симптомы астмы под контролем, желтая зона — возможно обострение, при красной зоне нужно немедленно спешить человеку на помощь.
Больной должен зафиксировать лучшее значения ПСВ, и при дальнейшем использовании прибора при определении обструктивных изменений надобно соотносить с этим значениям другие показатели шкалы. Нужно правильно делать выдох форсированным способом, результаты записывать в дневник, чтобы с этими результатами ознакомить позже лечащего врача. Возможно, в вашем городе есть школа для больных астмой (где доктора рассказывают, как лечить это заболевание), поинтересуйтесь у доктора.

Спирограмма показывает форсированную жизненную емкость легких, сокращенно ФЖЕЛ, а также объем форсированного выдоха за одну секунду, сокращенно — ОФВ1, и так называемую пиковую скорость выдоха (ПСВ). Высчитывается индекс Тиффно, который составляет ОФВ1 поделить на ФЖЕЛ, у здоровых людей этот показатель выше 0,75.
Если при подозрениях на астму показатели спирографа в пределах нормы, делают медицинскую провокацию — дают больному метхолин или гистамин в виде ингаляций и сравнивают спирограмму с обычной обструкцией и под действием этих лекарств.
Но анализ дыхания может не дать четких результатов в случае, если заболевание являются профессиональным и приступ вызывает вещество, присутствующее только на работе. Чтобы диагностировать профессиональную астму, нужно кроме тестов дыхания изучить анализы и с помощью опроса выявить аллерген на рабочем месте пациента.
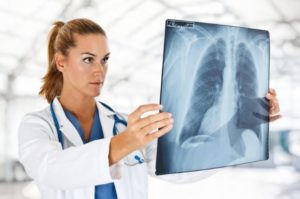
Если болезнь уже долго прогрессирует, развивается эмфизема, увеличение в объеме легких, которые на рентгенологической фотографии видимы как более прозрачные.
Томографию также назначают не во всех случаях, а только тогда, когда кашель и удушье не проходят длительное время, не смотря на лечение, и есть подозрения на наличие других болезней.
Диагностика астматических приступов у детей имеет особенности, поскольку они часто болеют респираторными и другими заболеваниями с похожими симптомами. Прежде всего у детей выясняют зависимость приступов от действий аллергенов, также возможную склонность к аллергии на генетическом уровне — есть ли близкие родственники с сильной аллергией на что-либо, это позволяет уточнить диагноз.

У детей исследуют внешнее дыхание с помощью приборов, предварительно дав бронходилататоры (препараты, расширяющие просвет в бронхах). Также сдают анализы, чтобы отследить наличие гельминтов и воспалительного процесса в организме, иногда проводят аллергологический тест. Но некоторые современные врачи отказываются от тестов на аллергены, резонно указывая на то, что в большинстве случаев аллергены вполне обычны и избежать их влияния довольно трудно.
У детей бронхиальная астма полностью излечима в большинстве случаев, однако для успешного лечения имеет большое значение своевременная диагностика бронхиальной астмы и правильное лечение, которое состоит не только в приеме медикаментов, но и в укреплении организма.
Люди пожилого возраста имеют множество заболеваний, которые могут хронически проходить долгие годы. Симптомы этих болезней могут накладываться на астматические, и клиническая картина становится нечеткой.

Кроме того, рекомендуется проводить функциональные методы выявления бронхиальной астмы, включающие ЭКГ, рентгенографию, пикфлоуметрию (это исследование нужно делать в течение 2 недель). Только после выполнения всех диагностических мероприятий назначается симптоматическое лечение бронхиальной астмы.
источник



 Прослушивание проходит через стетоскоп, стетофонендоскоп или фонендоскоп, причем последний наиболее подходит для изучения звуков, издаваемых грудной клеткой при астме. Если происходит обострение, свист и характерные хрипы слышны по всей легочной поверхности, но при ремиссии свистящий хрип слышен снизу от лопаток и то только при усиленном вдохе.
Прослушивание проходит через стетоскоп, стетофонендоскоп или фонендоскоп, причем последний наиболее подходит для изучения звуков, издаваемых грудной клеткой при астме. Если происходит обострение, свист и характерные хрипы слышны по всей легочной поверхности, но при ремиссии свистящий хрип слышен снизу от лопаток и то только при усиленном вдохе. если в анализе крови отсутствуют признаки воспалительных процессов и токсинов, выделяемых бактериями, то при наличии астматических симптомов доктору легче отличить астму от обычного бронхита или пневмонии;
если в анализе крови отсутствуют признаки воспалительных процессов и токсинов, выделяемых бактериями, то при наличии астматических симптомов доктору легче отличить астму от обычного бронхита или пневмонии;