Автореферат и диссертация по медицине (14.00.09) на тему: Клиническое значение дисбаланса минералов и микроэлементов при бронхиальной астме у детей
ГЛАВА I. СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О РОЛИ МАКРО- И МИКРОЭЛЕМЕНТОВ В РАЗВИТИИ АЛЛЕРГИИ (ОБЗОР ЛИТЕРАТУРЫ).
1.1. Макро- и микроэлементы в организме человека.
I 2. Роль отдельных элементов в развитии аллергии.
I.3. Участие минералов и микроэлементов в основных звеньях патогенеза бронхиальной астмы.
ГЛАВА II. ОБЪЕМ И МЕТОДЫ ИССЛЕДОВАНИЯ.
Н.2.1. Общеклинические методы.
11.2.2. Специальные методы исследования.
II.2.2.1. Выбор биологического субстрата.
II.2.2.2. Методика определения микроэлементов в волосах.
11.2.3. Статистические методы обработки материала исследований.
ГЛАВА III. ОБЩАЯ ХАРАКТЕРИСТИКА ГРУППЫ
III. 1. Группа детей с бронхиальной астмой.
ГЛАВА IV. ОСОБЕННОСТИ ДИСБАЛАНСА
МИНЕРАЛОВ И МИКРОЭЛЕМЕНТОВ У ДЕТЕЙ, БОЛЬНЫХ
IV. 1. Сопоставимость результатов анализа волос, полученных у обследованных детей методами АЭС-ИП и НАА.
IV.2. Характеристика макро- и микроэлементного состава волос детей, больных бронхиальной астмой.
IV.2.1. Сравнительный анализ макро- и микроэлементного состава волос у больных бронхиальной астмой, здоровых детей и выборки из общей детской популяции России.
IV.2.2. Отклонения в содержании макро- и микроэлементов в волосах у детей с бронхиальной астмой.
IV.2.3. Клинико-функциональная характеристика дисбаланса макро- и микроэлементов у детей, больных бронхиальной астмой.
1V.2.3.1. Макро- и микроэлементный состав волос больных бронхиальной астмой детей, в зависимости от тяжести заболевания, его продолжительности и степени нарушения функции внешнего дыхания.
IV.2.3.2. Макро- и микроэлементный состав волос больных бронхиальной астмой детей, получающих современную патогенетическую терапию.
IV.2.3.3. Макро- и микроэлементный состав волос детей, больных бронхиальной астмой, имеющих сопутствующую патологию органов пищеварения.
IV.2.3.4. Сравнительное исследование элементного состава волос детей разного возраста, больных бронхиальной астмой.
Глава IV.3. Взаимосвязи содержащихся в волосах элементов с некоторыми биохимическими, иммунологическими и клеточными показателями крови у детей, больных бронхиальной астмой.
Неуклонный рост распространенности бронхиальной астмы в структуре детской заболеваемости, как и его обусловленность экологическим неблагополучием представляют серьезную проблему для здравоохранения большинства стран мира. В последние годы наблюдается тенденция к раннему возникновению и более тяжелому течению заболевания, что снижает качество жизни больных детей и способствует увеличению детской инвалидности.
Согласно современной концепции, патогенетической основой бронхиальной астмы является хроническое аллергическое воспаление бронхов. Точные причины его возникновения до сих пор не установлены [14, 15, 25, 44, 70, 103, 117, 125, 164, 205], в связи с чем очевидна необходимость дальнейшего исследования патогенеза заболевания. В первую очередь, требуют изучения многие молекулярные, клеточные и иммунные механизмы, способствующие возникновению и поддержке хронического воспаления, и определяющие его интенсивность [25].
За последние сорок лет накоплены многочисленные, но разрозненные и противоречивые факты, свидетельствующие об участии минералов и микроэлементов в разных звеньях патогенеза аллергии [2, 37, 41, 45, 54, 66, 82, 85, 93, 182, 189, 202]. В то же время число клинических исследований, посвященных обмену макро- и микроэлементов при бронхиальной астме, ограничено. Как правило, такие работы были ориентированы на проблемы экологии и изучение профессиональных заболеваний. Особенно мало исследована детская астма. Поскольку большинство работ относится к 60 — 80-м годам XX века, то постановка задачи, диагностические подходы и интерпретация результатов не согласуются с современными представлениями о патогенезе бронхиальной астмы. Кроме того, в большинстве экспериментальных и клинических исследований изучались лишь эффекты одного или нескольких элементов. Все это не позволяет составить целостного
-» 6 представления об изменениях баланса макро- и микроэлементов в организме больных бронхиальной астмой, в связи с чем изучение данной проблемы, особенно у детей, остается актуальным. ЦЕПЬ Рйбдты
На основании многоэлементного анализа изучить особенности накопления минералов и микроэлементов в волосах детей, больных бронхиальной астмой и оценить роль минералов, эссенциальных, условно-эссенциальных, токсичных и некоторых малоизученных элементов в патогенезе заболевания.
1. Определить содержание минералов и микроэлементов в волосах здоровых детей современного мегаполиса.
2. Определить характер изменений минерального и микроэлементного состава волос у детей, больных бронхиальной астмой.
3. Провести анализ взаимосвязи элементов, содержащихся в волосах больных бронхиальной астмой детей, с наиболее важными маркерами аллергии (общего и эозинофилии периферической крови).
4. Охарактеризовать возрастные особенности нарушения баланса минералов и микроэлементов у детей 1—8 лет, больных бронхиальной астмой.
5. Исследовать зависимость изменений в макро- и микроэлементном составе волос больных бронхиальной астмой детей от формы и продолжительности заболевания, нарушения функции внешнего дыхания и использования в лечении основных препаратов современной патогенетической терапии.
6. Исследовать содержание минералов, эссенциальных, условно-эссенциальных и токсичных элементов в волосах больных бронхиальной астмой детей, проживающих в современном мегаполисе в районах с разной экологической обстановкой.
Впервые с позиций современной клинической медицины проведено комплексное исследование 26 химических элементов периодической системы Д.И.
Менделеева (минералов, эссенциальных, условно-эссенциальных, токсичных и некоторых малоизученных элементов) в волосах у детей, больных бронхиальной астмой. Впервые наиболее точным методом нейтронно-активационного анализа получены показатели содержания в волосах здоровых детей московской популяции 18 химических элементов: А1, Аи, Ва, Вг, Са, С1, Со, Си, Ей, Ре, I, К, Ьа, Мп, Ыа, 8е, Ъь.
При бронхиальной астме у детей современного мегаполиса установлено наличие дисбаланса в волосах преимущественно минералов и, в меньшей степени, эссенциальных и условно-эссенциальных микроэлементов. Из токсичных элементов наибольшее значение имел А1. Впервые установлено клиническое значение при данном заболевании дисбаланса редкоземельных металлов: Ьа, Ей.
Установлено сочетание эозинофилии периферической крови больных бронхиальной астмой детей со снижением в их волосах Са и Показана связь между уровнем ^Е в крови и содержанием в волосах кальция, марганца, селена и кремния.
Доказано существование значительных отличий в дисбалансе макро- и микроэлементов у больных бронхиальной астмой детей разных возрастных групп.
Проанализирована взаимосвязь основных показателей функции внешнего дыхания с содержанием макро- и микроэлементов в волосах детей, больных бронхиальной астмой. Нарушения бронхиальной проходимости на разных уровнях бронхиального дерева ассоциировались с дисбалансом Вг и Ъъ. Впервые выявлена зависимость накопления брома в волосах больных астмой детей от длительности заболевания и частоты интеркуррентных ОРВИ, провоцирующих приступы астмы. Впервые с современных клинических позиций проведено сопоставление между содержанием минералов (ионов) в волосах и плазме детей, больных бронхиальной астмой; выявлены особенности накопления калия, свидетельствующие о наличии существенных нарушений в его обмене у больных бронхиальной астмой.
Впервые проведена оценка влияния современной патогенетической терапии на содержание 26 химических элементов в волосах детей с бронхиальной астмой: при длительном применении препаратов кромонового ряда, ингаляционных глюкокортикостероидов, метилксантинов и р2
Впервые выявлено избыточное накопление токсичного металла-аллергена алюминия в волосах больных астмой детей из экологически неблагополучных районов современного мегаполиса.
Практическая значимость работы.
Получены показатели нормы содержания в волосах детей 4—7 лет 18 элементов (минералов, эссенциальных, условно-эссенциальных, некоторых токсичных и малоисследованных элементов). Установлен круг элементов, показатели обмена которых целесообразно определять при бронхиальной астме.
Обоснована возможность использования относительно дешевого метода АЭС-ИП для оценки содержания макро- и микроэлементов в волосах детей, больных бронхиальной астмой.
Обнаружено повышенное содержание токсичного металла-аллергена алюминия в волосах у детей из экологически неблагополучных районов г.Москвы, на которое следует обратить внимание при проведении экологических исследований. Данных о накоплении других токсичных элементов и металлов-аллергенов в волосах здоровых и больных детей мегаполиса не получено.
Внедрение результатов исследования в практику.
Результаты исследования внедрены в клиническую практику 5 отделения Морозовской детской городской клинической больницы, астма-школы Российского научного центра восстановительной медицины и курортологии МЗ РФ, используются в учебном процессе на кафедре детских болезней Российского университета дружбы народов.
Основные положения, выносимые на защиту.
1. У детей I — 8 лет, больных бронхиальной астмой, имеется дисбаланс макро-и микроэлементов, проявляющийся снижением в волосах содержания Са, Mg, Zn, Mn, La, Eu и повышением — К, CI, Br, Si, Au. При этом тяжесть заболевания ассоциируется с содержанием в волосах К, Zn и Au, Se, P.
2. У детей, больных бронхиальной астмой, имеется зависимость между основными маркерами аллергии и содержанием Са, Mg, Se, Мл, Si в волосах.
3. У детей, больных бронхиальной астмой, наблюдаются существенные возрастные отличия в макро- и микроэлементном составе волос.
Апробация работы. Основные положения диссертации обсуждались на конференциях: «Monitiring of Natural and Man-Made Radionuclides and Heavy Metal Waste in Environment» ( 1999, Dubna, Russia ); «Европа—наш общий дом: экологические аспекты»( 1999, Минск ); «20 th International Conference on Nuclear tracks in solid» (2000, Portoroz, Slovenia); «Monitiring of Natural and Man-Made Radionuclides and Heavy Metal Waste in Environment» (2000, Dubna, Russia); «Здоровье и образование в XXI веке» ( Москва, 2001 г.); совместной конференции кафедры детских болезней РУДН и кафедры детских болезней №3 педиатрического факультета РГМУ.
Публикации. По теме диссертации опубликовано 8 печатных работ. Объем и структура диссертации. Диссертация изложена на 188 страницах и состоит из введения, обзора литературы, материалов и методов исследования, 4 глав собственных исследований, обсуждения результатов исследования, выводов, практических рекомендаций и указателя литературы, включающего 227 источников, из них 110 на русском и 117 на иностранных языках. Работа иллюстрирована таблицами, рисунками, 3 выписками из историй болезни.
источник
В клинике госпитальной терапии Санкт-Петербургского государственного медицинского университета им. акад. И.П. Павлова проводилось комплексное исследование метаболизма магния и его антагониста кальция у 133 больных БА. У обследованных пациентов было обнаружено достоверное снижение внутриклеточной концентрации Mg и увеличение Са наряду с уменьшением суточной экскреции магния с мочой. По данным нагрузочных тестов с сульфатом магния у больных отмечалась высокая задержка этого катиона (в среднем 54% от вводимой дозы). Полученные результаты свидетельствуют о том, что дефицит магния у пациентов с бронхиальной астмой имеет место не только в форменных элементах крови, но и в клетках, принимающих участие в развитии воспаления.
Соотношение внутриклеточных концентраций кальция и магния достоверно (р
Выполненные исследования послужили основанием для назначения больным бронхиальной астмой ингаляций аэрозоля сульфата магния. Было установлено, что препарат достоверно по сравнению с плацебо снижает неспецифическую гиперреактивность бронхов и секреторную активность тучных клеток, улучшая непосредственные и отдаленные результаты лечения больных бронхиальной астмой атопического генеза и физического усилия.
Таким образом, нарушения минерального обмена, по-видимому, являются одним из механизмов формирования синдрома гиперреактивности бронхов и бронхообструктивного синдрома у пациентов с бронхиальной астмой.
Помимо ионов калия, натрия, кальция и магния, в регуляции бронхиальной проходимости и различных фаз реакций гиперчувствительности принимают, вероятно, микроэлементы (МЭ).
В исследованиях, выполненых in vitro и in vivo, установлено, что наиболее чувствительны к дефициту меди и цинка Т-киллеры и Т-хелперы, макрофаги и нейтрофилы, в меньшей степени — В-лимфоциты. У экспериментальных животных, получавших диету с низким содержанием данных МЭ, и у больных с генетически детерминированными нарушениями обмена меди и цинка наблюдалось развитие Т- и В-иммунодефицитов, проявляющихся инфекционными поражениями внутренних органов, в том числе и легких. Селективный дефицит цинка приводил к гипоплазии тимуса, снижению активности тимолина и развитию Т-клеточного иммунодефицита. Полученные данные, вероятно, можно объяснить тем, что цинк регулирует синтез нуклеиновых кислот, активной формы тимолина и стимулирует Т-лимфоциты.
При изучении показателей обмена микроэлементов у больных затяжной пневмонией найдено снижение концентрации важнейших биоэлементов, в том числе меди и цинка, в сыворотке крови, сочетающееся с Т-и В-клеточным дисбалансом и депрессией ферментов метаболизма ксенобиотиков. Коррекция содержания МЭ с помощью препаратов растительного происхождения увеличивала эффективность действия иммуномодуляторов и способствовала более быстрому восстановлению иммуноэнзиматического статуса. На основании полученных результатов сделан вывод о том, что изменение микроэлементного состава крови является одной из причин формирования вторичных иммунодефицитных состояний при заболеваниях органов дыхания.
В серии исследований продемонстрировано дозозависимое торможение физиологическими концентрациями цинка Ig Е-опосредованного освобождения гистамина и лейкотриена С4 из тучных клеток и базофилов. По мнению авторов, ионы Zn, депонированные в гранулах мастоцитов, выделяются в процессе секреции медиаторов, выполняя роль регулятора по принципу отрицательной обратной связи. Полученные результаты обусловлены мембраностабилизирующим эффектом цинка, способностью этого катиона «маскировать» рецепторы для Ig E на поверхности тучных клеток, инактивировать фосфолипазу А2, а также его конкурентный антагонизм с кальцием. Последним объясняется устранение экспериментального аллергического бронхоспазма добавками солей Zn.
Таким образом, результаты цитируемых выше исследований свидетельствуют о том, что МЭ участвуют в регуляции клеточного и гуморального звеньев иммунитета, процесса сенсибилизации, интенсивности патохимической и патофизиологической стадий аллергических реакций немедленного типа, которым принадлежит существенная роль в формировании воспалительных изменений бронхов и легких.
Заслуживают внимания данные о способности МЭ контролировать активность перекисного окисления липидов (ПОЛ) и антиоксидантной защиты. Известно, что медь, цинк и марганец входят в состав супероксиддисмутазы, селен-глютатионпероксидазы. Эти ферменты являются компонентами внутриклеточной антирадикальной системы. Церулоплазмин, один из основных внеклеточных антиоксидантов, относится к классу медьсодержащих протеинов. Цинк, образующий химические связи с сульфгидрильными группировками белков, фосфатными остатками фосфолипидов и карбоксильными группами сиаловых кислот, обладает мембраностабилизирующим действием. Избыток ионизированного железа оказывает прооксидантное действие. Дефицит меди и цинка приводит к накоплению свободных радикалов в тканях.
Таким образом, нарушение обмена МЭ является одним из факторов, способствующих избыточной активации ПОЛ, участвующей в формировании воспаления бронхов и бронхиальной обструкции у больных бронхиальной астмой и хронической обструктивной болезнью легких.
источник
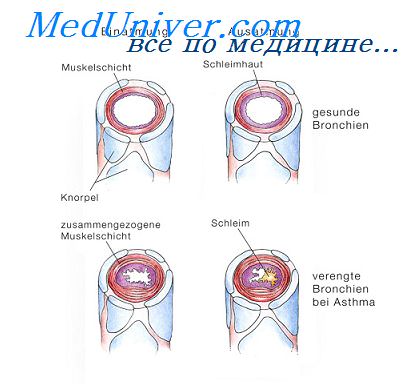
Астма – это состояние, сопровождающееся удушьем вследствие спазма мускулатуры бронхов и сужения просвета бронхиального дерева. Причинами его развития может служить непосредственное воздействие аллергена, что наблюдается наиболее часто, эндогенных провоцирующих факторов или отдельно выделяемая патология левых отделов сердца. В последнем случае состояние называется сердечной астмой. Оно встречается довольно редко и в основном астматический приступ наблюдается при бронхиальной астме.
Одним из наиболее важных факторов, определяющих правильное лечение, является этиология, то есть причина, спровоцировавшая развитие болезни.
При бронхиальной астме имеют значение как внешние, так и внутренние обстоятельства. Именно их взаимодействие часто приводит к обострению заболевания.
Однако бывают ситуации, когда приступ начинается без видимого воздействия аллергенов извне. В тех случаях, когда внешний источник, вызвавший реакцию, не обнаружен, принято говорить об астме эндогенного генеза.

- резкие перепады температур – переохлаждение;
- острый или длительный стресс;
- сильные физические нагрузки;
- инфекционные заболевания.
На последнем факторе следует остановиться подробнее, так как именно его присутствие наблюдается наиболее часто при бронхиальной астме эндогенного характера. Особенно опасны вирусные болезни дыхательных путей как состояние, напрямую влияющее на иммунные реакции в области бронхов и часто на их нервную регуляцию. В случае атопического (аллергического) происхождения болезни реактивность иммунитета также играет основополагающую роль в механизме развития приступа.
Неудивительно, что важным аспектом борьбы с астмой является нормализация работы иммунной системы и повышение сопротивляемости к инфекционным агентам. Известно, что польза витаминов при астме огромна.

- аскорбиновая кислота;
- витамины группы В;
- витамины А и Е;
- группа витамина P;
- витамин D.
В таблице подробно расписано биологическое действие этих веществ для улучшения состояниях больных бронхиальной астмой.
Таблица – Значение витаминов при лечении астмы
| Витамин | Химическое название | Действие на симптомы бронхиальной астмы |
|---|---|---|
| С | Аскорбиновая кислота | Ослабление сезонных проявлений. Снижает риск возникновения анафилактического шока и отека Квинке. Некоторые данные свидетельствуют об уменьшении под действием этого витамина содержания гистамина (основного вещества, вызывающего аллергические реакции) в крови |
| В | Никотиновая кислота (B3) | Снижение интенсивности астматических хрипов и скорости развития аллергической реакции |
| Пиридоксин (В6) | Нормализует обмен гистамина. Может быть снижен у больных, длительно принимающих брохорасширяющие препараты | |
| Цианокобаламин (В12) | Облегчение дыхательных движений во время приступа. Способствует благоприятному преодолению контакта с аллергенами и физических нагрузок. Уменьшает проявление аллергии к яичному желтку | |
| Е | Токоферол | Снижает продукцию медиаторов воспаления. Способствует уменьшению кашля, выраженности свиста, затрудненности дыхания. Улучшает функционирование сердца. Употребляется в комбинации с витамином А (ретинолом) |
| Р | Рутин | Нормализует реактивность иммунной системы |
| D | Кальциферол | Уменьшает восприимчивость дыхательных путей к аллергенам, снижает воспалительные реакции |
Прежде чем начинать употреблять какие-либо витаминные препараты или комплексы при бронхиальной астме, необходимо проконсультироваться с врачом. Аллергические реакции весьма вариабельны, поэтому назначение витаминов рассматривается в каждом отдельном случае индивидуально.
Помимо вышеуказанных полезных соединений существуют определенные микроэлементы и химические вещества, которые также показаны, когда у больного может развиться астматический приступ.
В медицине известны следующие клинические данные о влиянии различных компонентов на течение заболевания:
- Цинк (Zn) снижает восприимчивость бронхов к воздействию раздражающих веществ-аллергенов. Его дефицит обнаруживается у многих людей с нарушениями в работе дыхательной системы.
- При приеме селена (Se) по 100-200 мкг в сутки наблюдаются значимые улучшения в состоянии больных.
-
Магний (Mg) обладает некоторыми спазмолитическими свойствами, расслабляет мышцы. Снижает восприимчивость организма к аллергенам. Его в некоторых случаях при бронхиальной астме даже назначают внутривенно.
- Молибден (Mo) специфически снижает реактивность организма при аллергических реакциях на сульфиты, которые содержаться, к примеру, в яйцах или вине.
- N-ацетилцистеин разжижает мокроту.
- Теобромин (содержится в продуктах из какао) может применяться в качестве бронхорасширяющего вещества.
Отдельно стоит сказать о применении незаменимых жирных кислот ввиду их выраженной противовоспалительной активности. Они препятствуют спазмированию бронхов и их набуханию. К данной группе веществ относятся:
- Линолевая кислота;
- Гамма-линоленовая кислота.

Известно, что олеиновая кислота, та самая, что входит в состав оливкового масла, оказывает тормозное действие на высвобождение гистамина. Данный биогенный амин вырабатывается особыми высокоспециализированными элементами иммунной системы – тучными клетками. Они содержаться в тканях, в крови же их роль играют другие клетки из лейкоцитарного ростка – базофилы.
Любые синтетические микроэлементы, как и витамины при астме, назначаются лишь врачом на основе опроса и осмотра больного, тщательной проработки анамнеза его жизни и анализа лабораторных данных.
Баланс всех компонентов человеческого организма весьма важен для поддержания здоровья и любое вмешательство должно быть обдуманным, главное – обоснованным.
Прием любых лекарственных средств неизбежно сопряжен с риском возникновения различных сопутствующих нежелательных эффектов. В связи с этим к приему аптечных, а иногда и употреблению в натуральном виде некоторых витаминов следует относиться с осторожностью. Организм, который страдает какой-либо из форм аллергии, в большей мере подвержен также развитию пищевой аллергии.
К применению различных витаминов существуют следующие известные противопоказания:
- болезни, связанные с патологией крови, и особенно эритроцитов (гемохроматоз, талассемия, сидеробластная анемия);
- повышенная экскреция с мочой оксалатов;
- наличие камней в почках;
- сахарный диабет.
- повышенное содержание в крови кальция;
- атеросклероз;
- мочекаменная болезнь;
- хроническая сердечная недостаточность;
- беременность и период кормления;
- повышенное содержание фосфора в крови.

- нежелательно употреблять детям до 12 лет;
- инфаркт миокарда, острая форма.
- беременность, первый триместр;
- не следует принимать детям до 3 лет.
Также противопоказанием для приема любых витаминов можно назвать индивидуальную непереносимость какого-либо из них. Здесь перечислены и те противопоказания, при которых можно употреблять препарат, но с осторожностью.
К побочным эффектам приема большинства из витаминов можно отнести:
- тошноту;
- повышение секреции желудочного сока;
- общую слабость или наоборот повышение возбудимости центральной нервной системы;
- головокружение;
- дерматит;
- местную реакцию в виде появления боли в области введения или инфильтрата;
- гипервитаминоз.
У каждого витамина имеются свои специфические побочные эффекты при несоблюдении прописанных дозировок:
- аскорбиновая кислота может вызвать серьезные изменения в показателях крови, обмене веществ и функциях сердца;
-
пиридоксин – онемение в области конечностей, уменьшение лактации у женщин, изредка судороги;
- никотиновая кислота при передозировке ударяет по желудочно-кишечному тракту и печени;
- при повышенном содержании в организме витамина В12 страдает сердце и головной мозг, увеличивается свертываемость крови;
- очень остро проявляется гипервитаминоз кальциферола: начиная от нарушений пищеварения и функции почек, заканчивая болями в костях и воспалительными процессами в поджелудочной железе.
Повышение иммунной сопротивляемости организма является одним из главных факторов успешного преодоления заболевания. Помочь в этом может прием витаминных комплексов, однако обязательно нужно учитывать противопоказания и индивидуальные особенности организма, чтобы получить максимальную пользу и избежать побочных эффектов.
источник
Ведущее значение в этом отводится ионам кальция.
Показано, что повышение их внутриклеточной концентрации через стимуляцию кальмодулинзависимых протеинкиназ активирует сокращение гладких мышц бронхов, секрецию тучных клеток легких, образование трахеобронхиального секрета и увеличивает тонус блуждающего нерва.
Уровень свободного Са+2, являющегося универсальным внутриклеточным мессенджером, в клетках низок (10 -6 -10 -7 М) и контролируется специальными транспортными системами. Поступление этого катиона в цитоплазму осуществляется по градиенту концентрации через селективные каналы из внеклеточного пространства и внутриклеточных депо (саркоплазматического и эндоплазматического ретикулума, а также митохондрий).
В возбудимых тканях, в том числе и в гладких мышцах бронхов, транспорт кальция осуществляется через потенциалзависимые каналы, активируемые при деполяризации мембран и генерации потенциала действия. Описано 4 вида таких каналов (L, Т, N, Р), из которых в гладкомышечной ткани имеются L и Т типы. В невозбудимых клетках, в том числе мастоцитах и железах дыхательных путей, обнаружены рецепторуправляемые каналы, проницаемость которых повышается при взаимодействии рецепторов и агонистов (гормонов и биологические активные вещества (БАВ)), в том числе и медиаторов аллергических реакций (схема 1).
Схема 1. Регуляция внутриклеточного гомеостаза кальция
Механизмы сопряжения активации каналов и мобилизации внутриклеточного Са+2 изучены пока недостаточно. В настоящее время для объяснения связи деполяризации мембраны с сокращением мышц высказываются два предположения. Согласно первой, «химической» гипотезе, взаимодействие между Т-трубочками и саркоплазматическим ретикулумом осуещствляет растворимый мессенджер, открывающий кальциевый канал его терминальной цистерны.
На роль этого посредника претендуют ионы Са и инозитолтрифосфат (ИТФ), образующийся из мембранных фосфолипидов. Вторая, «электромеханическая» гипотеза предполагает прямой физический контакт между зарядом Т-трубочек и каналом выброса кальция. Следует отметить, что ни одно из этих предположений не имеет пока полного экспериментального подтверждения.
Вторичным посредником, связывающим агонистзависимые кальциевые каналы и внутриклеточные депо, считается ИТФ. Источником для его образования служит мембранный фосфолипид фосфатидилинозитол. Фактором, запускающим метаболизм последнего, является взаимодействие рецептора и агониста, активирующее фосфолипазу С. Этот фермент катализирует синтез диацилглицерола и ИТФ. Установлено, что последний гидролизуется кальмодулинзависимой киназой до инозитолтетрафосфата, который может открывать Са+2 каналы плазматических мембран.
Следует отметить, что активация потенциалзависимых каналов приводит к быстрому, но кратковременному повышению уровня ионизированного кальция в цитоплазме, а агонистзависимых — к более медленному, но длительному увеличению его содержания. Источником Са+2 в первом случае является преимущественно внеклеточное пространство, а во втором — внутриклеточные депо. Отсюда становится понятной причина недостаточной клинической эффективности при БА синтетических антагонистов кальция, блокирующих лишь потенциалзависимые кальциевые каналы.
Поддержание низкой концентрации ионизированного Са+2 в клетках осуществляется за счет специальных систем, транспортирующих этот катион из цитоплазмы во внеклеточное пространство и внутриклеточные депо против градиента концентрации. К их числу относится Са-стимулируемая, Mg-зависимая аденозинтрифосфатаза (Са-АТФаза), являющаяся интегральным белком цитоплазматической и внутриклеточной мембран.
Этот фермент обеспечивает первично активный транспорт кальция за счет энергии гидролиза аденозинтрифосфата (АТФ). Активность Са-АТФазы регулируется комплексом катьций-кальмодулин, магнием, кальцитонином и зависит от гидрофобного окружения мембранных фосфолипидов. Установлено, что Mg, АТФ-зависимый транссарколемный транспорт является лимитирующей стадией расслабления гладких мышц.
Другим путем выхода Са+2 из клетки служит Na+/Ca+2 противотранспорт, осуществляющий удаление 1 иона кальция в обмен на поступление 3 катионов натрия. Эта система может функционировать и в обратном направлении, т.е. осуществлять вход Са в цитоплазму и выход из нее натрия в той же стереохимии. В термодинамическом отношении такой транспорт является вторично активным, т.к. для его осуществления используется энергия движения Na (схема 1).
Принимая во внимание ключевую роль Са в регуляции бронхиальной проходимости, а также противоастматическую активность его синтетических антагонистов, американский исследователь Е. Middleton в начале 80-х годов сформулировал кальциевую гипотезу бронхиальной астмы (БА). Согласно последней, повышение внутриклеточной концентрации этого катиона, обусловленное активацией его транспорта в цитоплазму и снижение депонирования, является одной из причин формирования синдрома гиперреактивности бронхов. Данная гипотеза получила подтверждение в работах отечественных авторов. Вместе с тем, механизмы формирования выявленных изменений, их участие в развитии воспалительных изменений дыхательных путей и возможные пути коррекции изучены пока недостаточно.
В последние годы большой интерес исследователей вызывают натрий, калий и магний, принимающие участие в регуляции функций различных клеток, ответственных за развитие воспалительных изменений бронхов и легких.
В эксперименте показано, что контакт с аллергеном сенсибилизированных мышц дыхательных путей приводит к увеличению поступления в них натрия. При исследовании концентраций одновалентных катионов у больных БА было установлено повышение в эритроцитах уровня Na+. По мнению авторов, обнаруженный прирост натрия через активацию Na+/Ca+2 обмена может приводить к накоплению Са+2 в клетке, что подтверждает кальциевую гипотезу астмы.
Механизмы увеличения концентрации натрия в клетках изучены пока недостаточно. Активность Na-K АТФазы и Na+/K+/2Cl-KO трaнспорта в лимфоцитах и эритроцитах у больных астмой и хронической обструктивной болезнью легких не отличалась от нормальной. Недавно в крови больных БА был обнаружен сывороточный фактор, повышающий транспорт натрия в лейкоциты. Скорость поступления Na в клетки коррелировала с величиной гиперреактивности бронхов к метахолину.
У больных хронической обструктивной болезнью легких, осложненной дыхательной недостаточностью и легочным сердцем, обнаружена задержка выделения с мочой натрия и жидкости после введения нагрузочных доз поваренной соли и воды. Обнаруженные нарушения авторы связывают с повышением концентрации в сыворотке крови альдостерона и вазопрессина, а также снижением почечного кровотока и клубочковой фильтрации.
Примером заболевания, при котором биохимический дефект обусловлен генетически детерминированным нарушением транспорта ионов в эпителии дыхательных путей, является муковисцидоз. Считается, что эта болезнь обусловлена мутацией гена, ответственного за синтез специфического белка (transmembrane regulator, CFTR). Последний регулирует движение С1- и Na+ через апикальную мембрану эпителиальных клеток. При снижении синтеза CFTR уменьшается секреция хлора, повышается абсорбция натрия и воды, в результате чего увеличивается вязкость трахеобронхиального секрета и нарушается его клиренс. Это, в свою очередь, способствует развитию инфекционного воспаления дыхательных путей.
Существенную роль в регуляции бронхиальной проходимости, повидимому, играют К+ каналы. Через последние осуществляется выход калия из клеток, приводящий к гиперполяризации их мембран. К+ каналы обнаружены в гладкомышечных и секреторных клетках, окончаниях блуждающего нерва и эфферентных волокон, а также в эпителии дыхательных путей. Они найдены в Т-лимфоцитах, базофилах и макрофагах, участвующих в развитии воспаления при астме.
Описано более 10 разновидностей калиевых каналов, из которых 4 типа (потенциалзависимые, агонистзависимые, Са-активируемые и АТФ-чувствительные) представлены в бронхах. Наибольшее значение, по-видимому, имеют Са-активируемые каналы большой проводимости, обнаруженные в дыхательных путях в значительном количестве. Установлено, что стимуляция выхода К+ из клетки через них является одним из механизмов бронходилятирующего действия в2-агонистов и метилксантинов. Это обусловлено фосфорилированием каналов цАМФ-зависимой протеинкиназой. Кроме того, в-адренорецепторы непосредственно активируют их через G-протеин.
В настоящее время известны специфические активаторы АТФ-чувствительных и Са-зависимых К+ каналов (кромокалим, никорандил, пинацидил). В экспериментальных и клинических исследованиях установлено, что они оказывают бронхорасширяющее действие и эффективны для предупреждения приступов ночной астмы. Вероятно, это обусловлено их непосредственным влиянием на гладкие мышцы бронхов, а также способностью уменьшать секрецию АЦХ и нейропептидов. Не исключено, что данные препараты обладают и противовоспалительным действием.
Таким образом, активаторы К-каналов представляют собой новый класс противоастматических соединений, терапевтические возможности которых нуждаются в дальнейшем изучении.
В рамках обсуждаемой проблемы особого внимания заслуживают данные о влиянии факторов питания на особенности течения БА. Впервые связь между тяжестью симптомов астмы и потреблением поваренной соли отметили A.V. Stoesser и М.М. Cock в 1938 году. В последующем у больных БА была обнаружена положительная связь между суточной экскрецией натрия и калия с мочой, с одной стороны, и величиной бронхиальной гиперреактивности бронхов к гистамину и метахолину, с другой.
Пищевые добавки поваренной соли приводили к увеличению частоты обострений астмы, ухудшению бронхиальной проходимости, повышению неспецифической гиперреактивности бронхов и потребности больных в ингаляционных стероидах. В эпидемиологических исследованиях, выполненных в Великобритании, была обнаружена связь между потреблением хлорида натрия и смертностью от БА. Тем не менее, эти данные не нашли своего подтверждения в работах других авторов.
Таким образом, несмотря на противоречивость полученных данных, можно предположить, что ио крайней мере часть больных БА является калий- и соль-чувствительными. Не исключено, что нарушения обмена Na и К+ имеют определенное значение в развитии воспаления дыхательных путей. Вместе с тем, этот вопрос требует дальнейшего изучения.
Существенный интерес исследователей вызывает магний, являющийся функциональным антагонистом кальция (схема 1). Установлено, что Mg блокирует потенциал- и агонистзависимые кальциевые каналы, мобилизацию кальция из внутриклеточных депо под влиянием ИТФ, а также активирует Са-АТФазу, удаляющую избыток этого катиона из цитоплазмы клеток. Другой внутриклеточной мишенью для магния являются циклические нуклеотиды. Известно, что этот катион активирует аденилатциклазу, катализирующую образование циклического аденозинмонофосфата (цАМФ). Последний, в отличие от кальция, ингибирует дегрануляцию тучных клеток и обеспечивает расслабление гладких мышц бронхов.
У больных гипомагниемией были обнаружены обструктивные нарушения функции внешнего дыхания и гиперреактивность бронхов к гистамину, которые полностью или частично коррегировались назначением препаратов Mg. Соли магния при внутривенном введении оказывали бронхолитическое действие, купируя легкие и тяжелые приступы удушья, а также астматический статус, увеличивали силу сокращения дыхательных мышц, снижали легочную гипертензию у пациентов с БА и другими обструктивными заболеваниями легких.
Ингаляции сульфата магния достоверно уменьшали гиперреактивность бронхов к гистамину, метахолину и физической нагрузке, а также усиливали профилактический эффект сальбутамола в отношении постнагрузочного бронхоспазма. В эпидемиологических исследованиях, выполненных в различных районах Великобритании, у взрослого населения была установлена достоверная связь между потреблением магния с пищей, величиной объем форсированного выдоха за секунду (ОФВ4) и выраженностью бронхиальной гиперреактивности к метахолину [Britton Y. et al., 1964; Soutar A. et al., 1997).
Экспериментальные исследования последних лет существенно расширили прежние представления о патофизиологических механизмах дефицита магния. У грызунов, получавших диету с низким содержанием катиона, на 5-й день опыта было обнаружено повышение уровня субстанции Р в сыворотке крови с последующим увеличением концентрации интерлейкинов 1, 6 и гистамина.
На основании полученных данных, а также результатов других экспериментов была сформулирована оригинальная концепция нейрогенного воспаления, приводящего к повреждению тканей при дефиците магния. Согласно этой гипотезе, генерализованное провоспалительное состояние у опытных животных обусловлено избыточной секрецией афферентными С-волокнами нейропептида Р, активирующего продукцию свободных радикалов, выделение цитокинов, гистамина, арахидоновой кислоты и ее метаболитов, повышающего сосудистую проницаемость, миграцию нейтрофилов, макрофагов и дегрануляцию эозинофилов в различных тканях.
Считая избыток продуктов перекисного окисления липидов (ПОЛ) основным повреждающим фактором, исследователи с успехом использовали антиоксиданты в лечении экспериментальных крыс. Механизм активации данного процесса при дефиците магния не имеет общепризнанного объяснения. Предполагается, что этому способствуют изменения липидного матрикса мембран и нарушения синтеза глютатиона, одного из основных факторов антиоксидантной защиты.
Результаты обсуждаемых выше работ подтверждают полученные ранее данные об увеличении активности фосфолипазы А, и концентрации продуктов метаболизма арахидоновой кислоты в тканях у магний-дефицитных животных. Исследования, выполненные Tapia D.P. et al., показали, что сульфат магния блокирует выделение фактора активации тромбоцитов из альвеолярных макрофагов морской свинки. Следует отметить, что внутриклеточный избыток кальция, подобно дефициту магния, усиливает секрецию медиаторов тучными клетками, фактора активации тромбоцитов макрофагами, стимулирует миграционную способность нейтрофилов и повышает продукцию свободных радикалов.
В концентрации 10 -4 -10 -5 М ионы Са+2 оказывают прооксидантное действие, вероятно, обусловленное увеличением содержания в клетках ионизированного железа и модификацией фосфолипидного состава мембран. Более высокие, нефизиологичные, уровни кальция (10 -3 и выше) в биологических системах обладают антиоксидантным эффектом. Избыток свободных радикалов увеличивает концентрацию свободного кальция за счет повышения пассивной ионной проницаемости и инактивации Са-АТФаз.
Таким образом, клинические и экспериментальные наблюдения свидетельствуют об участии ионов Mg+2 в регуляции бронхиальной проходимости, давления в легочной артерии, сократимости дыхательных мышц, свободно-радикального окисления липидов, нейрогенного воспаления. Это позволило предположить, что нарушения его гомеостаза могут иметь существенное значение в патогенезе обструктивных заболеваний легких, в том числе и БА. Важно отметить, что изменения электролитного обмена являются одним из побочных эффектов противоастматических лекарственных препаратов (в2-адреномиметиков и глюкокортикоидов), что увеличивает риск их развития при данном заболевании.
В клинике госпитальной терапии Санкт-Петербургского государственного медицинского университета им. акад. И.П. Павлова проводилось комплексное исследование метаболизма магния и его антагониста кальция у 133 больных БА. У обследованных пациентов было обнаружено достоверное снижение внутриклеточной концентрации Mg и увеличение Са наряду с уменьшением суточной экскреции магния с мочой. По данным нагрузочных тестов с сульфатом магния у больных отмечалась высокая задержка этого катиона (в среднем 54% от вводимой дозы). Полученные результаты свидетельствуют о том, что дефицит магния у пациентов с БА имеет место не только в форменных элементах крови, но и в клетках, принимающих участие в развитии воспаления.
Соотношение внутриклеточных концентраций изучаемых катионов достоверно (р
источник
Клиническое значение дисбаланса минералов и микроэлементов при бронхиальной астме у детей Алексеева Ольга Владимировна
Данный автореферат диссертации должен поступить в библиотеки в ближайшее время
Уведомить о поступлении
480 руб. | 150 грн. | 7,5 долл. ‘, MOUSEOFF, FGCOLOR, ‘#FFFFCC’,BGCOLOR, ‘#393939’);» onMouseOut=»return nd();»> Диссертация — 480 руб., доставка 10 минут , круглосуточно, без выходных и праздников
240 руб. | 75 грн. | 3,75 долл. ‘, MOUSEOFF, FGCOLOR, ‘#FFFFCC’,BGCOLOR, ‘#393939’);» onMouseOut=»return nd();»> Автореферат — 240 руб., доставка 1-3 часа, с 10-19 (Московское время), кроме воскресенья
Алексеева Ольга Владимировна. Клиническое значение дисбаланса минералов и микроэлементов при бронхиальной астме у детей : диссертация . кандидата медицинских наук : 14.00.09 / Алексеева Ольга Владимировна; [Место защиты: Российский университет дружбы народов].- Москва, 2003.- 192 с.: ил.
Глава I. Современные представления о роли макро- и микроэлементов в развитии аллергии (обзор литературы) 10
1.1. Макро- и микроэлементы в организме человека 10
I 2. Роль отдельных элементов в развитии аллергии 12
1.3. Участие минералов и микроэлементов в основных звеньях патогенеза бронхиальной астмы 39
Глава II. Объем и методы исследования 42
II. 1. Объект исследования 42
ІІ.2. Методы исследования 44
IІ.2.1. Общеклинические методы 44
II.2.2. Специальные методы исследования 46
II.2.2.1. Выбор биологического субстрата 46
II.2.2.2.. Методика определения микроэлементов в волосах 48
II.2.3. Статистические методы обработки материала исследований 53
Глава III. Общая характеристика группы наблюдавшихся детей 55
III.1. Группа детей с бронхиальной астмой 55
Глава IV. Особенности дисбаланса минералов и микроэлементов у детей, больных бронхиальной астмой 68
IV.1. Сопоставимость результатов анализа волос, полученных у обследованных детей методами АЭС-ИП и НАА 68
IV.2. Характеристика макро- и микроэлементного состава волос детей, больных бронхиальной астмой 72
IV.2.1. Сравнительный анализ макро- и микроэлементного состава волос у больных бронхиальной астмой, здоровых детей и выборки из общей детской популяции России 72
IV.2.2. Отклонения в содержании макро- и микроэлементов в волосах у детей с бронхиальной астмой 79
IV.2.3. Клинико-функциональная характеристика дисбаланса макро- и микроэлементов у детей, больных бронхиальной астмой 86
1V.2.3.1. Макро- и микроэлементный состав волос больных бронхиальной астмой детей, в зависимости от тяжести заболевания, его продолжительности и степени нарушения функции внешнего дыхания 86
IV.2.3.2. Макро- и микроэлементный состав волос больных бронхиальной астмой детей, получающих современную патогенетическую терапию 97
IV.2.3.3. Макро- и микроэлементный состав волос детей, больных бронхиальной астмой, имеющих сопутствующую патологию органов пищеварения 102
IV.2.3.4. Сравнительное исследование элементного состава волос детей разного возраста, больных бронхиальной астмой 106
IV.3. Взаимосвязи содержащихся в волосах элементов с некоторыми биохимическими, иммунологическими и клеточными показателями крови у детей, больных бронхиальной астмой 123
Глава V. Обсуждение полученных результатов 137
Практические рекомендации 158
В настоящее время принята «кальциевая» гипотеза формирования синдрома гипереактивности бронхов при бронхиальной астме [178]. По этой гипотезе, ключевое значение отводится повышению концентрации кальция в цитоплазме иммунокопетентных, эпителиальных и мышечных клеток. Вход иона кальция внутрь клетки через специальные кальциевые каналы и выход его из клеточного депо, вызванные воздействием антигена, приводят к активации внутриклеточных систем и выбросу в межклеточное пространство медиаторов аллергии. Кальций-опосредованными процессами являются большинство известных сегодня механизмов, имеющих патогенетическое значение при бронхиальной астме: секреция слизистых желез, сокращение гладкой мускулатуры бронхов, передача нервных импульсов, изменение внутриклеточной концентрации цАМФ, некоторые гормональные воздействия [1, 3,18, 37, 75, 76,104, 178,222]. Однако значение многих из внутриклеточных событий, связанных с изменением внутрицеллюлярной концентрации кальция, остается неясным, в связи с чем «кальциевая» гипотеза бронхиальной астмы требует дальнейшего подтверждения.
Среди других макро- и микроэлементов при бронхиальной астме наиболее изучена патогенетическая роль магния. В первую очередь, она состоит в регуляции концентрации внутриклеточного кальция посредством воздействия на Са-АТФазу, удаляющую избыток кальция из цитозоля как во внутриклеточные депо, так и во внеклеточное пространство. Активность этого фермента снижается при недостатке в среде ионов магния [192]. Магний также вмешивается в метаболизм цАМФ, обеспечивает стабильность мембран. При недостатке минерала в организме создаются условия для избыточной активации перикисного окисления липидов ( ПОЛ) [39].
Существует достаточно тесная связь Mg с функционированием нервной системы. Стимуляция гидролиза ацетилхолина посредством воздействия на холинэстеразу лежит в основе снижения его соединениями гиперреактивности бронхов у больных бронхиальной астмой [37, 144]. Показано влияние Mg и на функционирование «третьего» звена вегетативной нервной системы, с нарушениями в котором связывают наличие нейрогенного воспаления тканей при аллергических заболеваниях: при недостатке минерала в организме у лабораторных животных было отмечено повышение субстанции Р в сыворотке крови [217].
Не вызывает сомнения участие Mg в различных иммунных процессах. Ингибирующее влияние минерала на процесс высвобождения гистамина и стимулирующее — на гистаминопексию, подтверждается во многих работах [141, 150, 217, 218]. Кроме того, экспериментально доказано существование связи между обменом Mg и синтезом IgE , активностью эозинофилов [144, 161]. Это свидетельствует о важном месте метаболизма минерала в основных звеньях патогенеза бронхиальной астмы.
Обнаруженное снижение кортизолпоглощения лимфоцитов у больных бронхиальной астмой при недостатке магния [33] может быть одним из механизмов развития недостаточной чувствительности к кортизолу иммуннокмпетентных клеток.
Степень влияния минерала на тонус мускулатуры и бронхов, как и на их гиперреактивность до конца не ясна, поскольку не выявлено зависимости большинства показателей гомеостаза магния в организме от выраженности бронхообструктивного синдрома [37] и снижения форсированного выдоха за первую секунду в тесте с метахолином у лиц с экзогенным дефицитом минерала в организме [202]. Однако об активном участии магния в нарушении секреторной и экскреторной функции эпителия бронхов свидетельствует наличие достоверной связи между снижением бронхиальной проходимости и недостатком магния в конденсате выдыхаемого воздуха у больных хроническими обстуктивными заболеваниями легких [5]. Сульфат магния оказывает бронхорасширяющее действие, хотя и значительно уступает по клиническому эффекту другим препаратам, в связи с чем его применение в клинической практике не рекомендуется [14]. Более перспективным оказалось свойство сульфата магния снижать гиперреактивность бронхов к ацетилхолину и физической нагрузке при введении ингаляционным способом [37].
На примере взрослых больных подтверждено значение недостатка магния для формирования бронхиальной астмы. Оказалось, что нарушения клеточного гомеостаза магния, как и кальция, проявляющиеся внутриклеточным дефицитом магния и избытком кальция, а также снижением концентрации магния в суточной моче и конденсате выдыхаемого воздуха, выявляются не только у больных, но и у их практически здоровых кровных родственников [37].
Ниже представлена схема участия магния в патогенезе бронхиальной астмы, предложенная автором. Дефицит магния сопровождает бронхиальную астму и у детей [3], однако эта возрастная группа исследована меньше.
Следует заметить, что наличие магнийдефицитного состояния в организме наблюдается при многих заболеваниях: сердечно-сосудистой, нервной и эндокринной систем, вследствие чего указанные выше изменения магния нельзя считать патогмоничными для бронхиальной астмы. Магнийдефицитные состояния широко распространены в популяции [27, 54, 89]. Однако, среди больных бронхиальной астмой они встречаются, вероятно, более часто, чем в общей популяции. Так, при исследовании гомеостаза магния недостаток минерала был выявлен у 40% больных бронхиальной астмой и только у 11 % клинически здоровых лиц [ 157].
Таким образом, результаты исследований доказывают, что нарушению обмена магния принадлежит значительная роль в патогенезе бронхиальной астмы. Тем не менее клинические проявления таких нарушений у детей остаются не изученными.
Широкая распространенность цинкдефицитных состояний у населения позволяет считать их «общественной проблемой» современности [2, 29, 54, 89,190, 196]. Необходимость разработки путей профилактики и лечения таких состояний, а также определения надежных критериев их диагностики неоднократно подчеркивалась в докладах ВОЗ [208].
Как установлено в настоящее время, причины дефицита Zn не имеют исключительной связи с неполноценным питанием. Недостаток микроэлемента в организме сопровождает развитие многих заболеваний (онкологических, аллергических, аутоиммунных, инфекционных) и патологических состояний (нарушении всасывания, разнообразные иммунодефициты). Достаточно часто цинкдефицитное состояние является следствием избыточного поступления ксенобиотков (Cd, Pb), чем обусловлено его широкое распространение среди населения в экологически неблагополучных регионах. Среди других причин можно выделить природный недостаток цинка в определенных географических местностях, например, в странах Средиземноморья. Низкое содержание этого элемента имеет место и в большинстве регионов России [2, 47,54, 89, 208].
Разнообразные проявления недостатка микроэлемента в организме обусловлены многогранностью эссенциальной роли цинка. Установлено, что цинк влияет на разные виды обмена веществ: белкового, углеводного, жирового, минерального, гормонального, нуклеинового. Он необходим для нормального функционирования иммунной системы, большинства ферментов, способен изменять генетический аппарат клетки, оказывать влияние на чувствительность рецепторов к гормонам и цитокинам. Однако, несмотря на кофакторную роль этого микроэлемента более, чем для 300 ферментов, его точные функции в организме до сих пор неизвестны [54, 190, 208].
Имеющиеся на сегодняшний день результаты экспериментальных и клинических исследований свидетельствуют об участии цинка в процессах, имеющих существенное значение в патогенезе аллергических заболеваний.
На уровне клетки цинк проявляет себя конкурентным антагонистом Са, взаимодействуя с белком кальмодулином, осуществляющим контроль за содержанием кальция в клетке [79, 122, 189, 193]. Посредством участия в регуляции циклазных систем [122] цинк способен влиять на активность клетки, антиоксидантную защиту, проницаемость мембран, состояние их рецепции, передачу генетической информации. Все это обеспечивает определенную роль цинка в стабилизации мембран и предотвращении программированной гибели клетки — апоптоза [54, 110,122, 208].
В результате проведения анализа семейного и личного анамнеза наблюдавшихся детей было установлено следующее.
В семейном анамнезе 79 больных детей ( 73,1% ) имелись указания на существование у близких родственников пробанда аллергических заболеваний. При этом по линии матери в 28 ( 25,93%) семьях, только по линии отца — в 13 (12,04%) семьях, по линии матери и отца — в 38 ( 35,2%) семьях. В структуре заболеваний преобладала бронхиальная астма ( 37,95% ), несколько реже имелись указания на кожные проявления аллергии ( 35,19%) и еще реже — полли-ноз (21,30%).
Наследственная отягощенность неаллергическими заболеваниями включала эндокринную патологию ( сахарный диабет II типа, нарушение функции щитовидной железы и дисфункции репродуктивной сферы у родственников женского пола ) в семьях 48 детей ( 44,4%). Несколько реже имелись указания на хронические заболевания органов пищеварения ( в семьях 32 детей, 29,63% ), заболевания ЛОР- органов ( в семьях 20 детей , 18,52 % ), онкологические заболевания ( в семьях 18 детей, 16,7 %).
Антенатальное развитие 77 ( 71,3%) наблюдавшихся детей протекало в неблагоприятных условиях. Сведения об особенностях течения беременности у матерей этих детей представлены в табл. 3. Настоящая беременность у большинства матерей наблюдавшихся детей чаще всего осложнялась поздним гес-тозом и/или угрозой прерывания беременности. Однако, несмотря на значительную частоту осложненного течения данной беременности у матери, 104 из 108 детей родились на сроке 38 — 40 недель гестации, недоношенными родились только 4 ребенка ( 3,7%). Средний гестационный возраст недоношенных детей был равен 36,88 ± 0,43 недели. Пятеро из наблюдавшихся детей родились в состоянии асфиксии. У всех остальных детей в раннем неонаталыюм периоде осложнений не отмечалось. Путем кесарева сечения родились 25 детей (23,15 % ). С применением акушерских пособий родился один ребенок ( 0,9% ). Таким образом, 26 детей ( 24 %) родились с помощью оперативного вмешательства.
У 74 (68,5%) из наблюдавшихся нами детей, больных бронхиальной астмой, помимо основного заболевания, были сопутствующие заболеваниями других органов и систем (табл. 4).
Результаты исследования свидетельствуют, что у детей 2-й подгруппы чаще, чем у детей 1-й группы встречались хронический гастрит и хронический гастродуоденит (р 0,01), хронический пиелонефрит (р 0,02) и была тенденция к уменьшению частоты возникновения эпизодов ОРВИ, что в целом сопоставимо с распространенностью этих заболеваний в популяции московских детей в возрасте 4 лет и старше.
Отсутствие органической патологии сердечно-сосудистой системы (за исключением вегетососудистой дистонии, наблюдавшейся у большинства детей) обусловлено специальной направленностью отбора больных. Помимо этого, нами был проведен анализ проявлений аллергии у наблюдавшихся детей (табл. 5).
Результаты исследования, приведенные в табл.5, свидетельствуют о значительной частоте внелегочных проявлений аллергии у детей с бронхиальной астмой. Последняя выявлялась у 3/4 наблюдавшихся пациентов. Статистически значимое различие, за исключением пищевой аллергии, у детей двух сравниваемых подгрупп отсутствовало.
В табл.6 представлены сведения об особенностях экологии жилища и других факторов, способствующих формированию бронхиальной астмы у наблюдавшихся детей.
Результаты анамнеза, представленные в табл.10, свидетельствуют, что 3/4 наблюдавшихся детей проживали в неблагоприятной обстановке ( нарушение микроэкологии жилища), 1/3 детей были пассивными курильщиками. У 18 детей ( 16,7 %) бронхиальная астма развилась на фоне перенесенной пневмонии, либо пневмония возникла на фоне бронхиальной астмы.
Обращает на себя внимание и тот факт, что у 19 детей (17,6%) до дебюта бронхиальной астмы были указания на возникновение осложнений вакцинации в виде повышения температуры, местных реакций в месте введения вакцин, преходящие неврологические расстройства. Если учесть, что вакцинация проводилась не всем наблюдающимся больным, а только 72 из них, то частота реакций на вакцинацию зарегистрированы у 1/4 детей с бронхиальной астмой.
Маловероятно, что во всех этих случаях причиной побочных реакций на вакцинацию явились качество вакцин или технические погрешности процедуры вакцинации. Скорее всего, возникновение осложнений обусловлено особенностями организма детей основной группы. На это могут указывать и данные анамнеза о высокой отягощенности семей наблюдавшихся нами детей аллергическими заболеваниями, и высокая частота внелегочных проявлений аллергии у самих пациентов. С учетом частоты возникновения пневмонии и побочных реакций на вакцинацию, можно полагать, что у детей наблюдавшейся группы имел место эндогенный неблагоприятный преморбидный фон, способствующий возникновению данного иммунологического состояния.
Распределение обследованных больных детей в зависимости от тяжести бронхиальной астмы представлено в табл. 7.
В данном исследовании у детей раннего возраста на момент обследования доля тяжелой формы бронхиальной астмы оказалась значительно выше, чем у более старших. Эта особенность учитывалась при проведении дальнейшего анализа.
Исследование волос детей проводилось двумя методами — АЭС-ИП и НАА. Данные об общем количестве обследованных этими методами детей и распределение детей основной группы по форме бронхиальной астмы представлено в табл. 8.
В табл.9, представлены сведения о возрасте начала и продолжительности заболевания у обследованных нами детей, больных бронхиальной астмой. С учетом средней арифметической и ее ошибки, можно констатировать, что большинство обследованных нами детей имели относительно непродолжительный «стаж» заболевания, что согласуется с их возрастом.
В приведенной ниже табл. 10 представлены сведения о факторах, которые провоцировали у наблюдавшихся больных приступы бронхиальной астмы. Приступы бронхиальной астмы провоцировались разными факторами, как причинно-значимыми, так и триггерами (в первую очередь, ОРВИ). У значительной части детей приступы бронхиальной астмы возникали после вдыхания измененного воздуха ( влажного, холодного ), эмоционального стресса, физической нагрузки, что свидетельствует о гиперчувствительности бронхов.
Состояние макро- и микроэлементного обмена в организме зависит от многообразных факторов, часть из которых до сих пор не определена. Помимо изменений, обусловленных развитием хронического заболевания, имеют значение особенности питания и бытовое микроокружение человека, биогеохмические особенности и индустриальное загрязнение местности его проживания. Вследствие вышеперечисленных причин, дисбаланс макро- и микроэлементного часто встречается у самых разных слоев населения современных городов [2, 27, 54, 74, 89, 196, 208]. Все это диктует необходимость сопоставления результатов исследования волос детей, больных бронхиальной астмой, с данными о частоте отклонений в макро- и микроэлементном составе волос среди детской популяции в целом с целью оценки специфичности обнаруженных изменений для бронхиальной астмы.
Мы сравнили имеющиеся показатели детской популяции 1 — 8 лет, проживающей в экологически благополучном административном округе г. Москвы [ 98 ], с данными больных астмой детей, обследованных нами методом АЭС-ИП. Отклонения в элементном составе волос и обеих группах были рассчитаны по одним и тем же нормативам. Результаты сравнения представлены в табл.7.
Мы также провели сопоставление результатов обследования детей, больных бронхиальной астмой с имеющимися данными Центра биотической медицины о распространенности накопления и недостатка отдельных элементов в детской популяции [89]. Результаты исследования представлены в табл. 8.
Исследование показало, что в отличие от детской популяиии г. Москвы, среди больных бронхиальной астмой был более широко распространен дисбаланс Zn, К, Si. В то же время, отклонения в содержании Са, Си, Fe чаще встречались в детской популяции в возрасте от 1 до 8 лет, что может быть обусловлено повышенным расходом указанных элементов в период роста ребенка и становления у него иммунной и кроветворной систем. Изменения в содержании Сг и Ni, способствующих развитию детской астмы [66], носили единичный характер (рис.2).
Обращало на себя внимание, что отклонений в минеральном и микроэлементном статусе волос не было выявлено только у двух 73 ( 2,7 % ) детей, обследованных нами методом АЭИ-ИП. Редко встречался и изолированный дефицит или избыток какого-либо элемента ( 3 ребенка, 4,2%). Подавляющее большинство больных детей имели отклонения в содержании от двух до десяти элементов (табл.8).
Данные о распространенности отклонений Au, Br, С1, Ей, La волосах детской популяции России в настоящее время отсутствуют, что не позволило провести сравнительный анализ по этим элементам.
Наиболее часто встречавшиеся сочетанные отклонения, иллюстрирующие характер минерального и микроэлементного статуса больных бронхиальной астмой, представлены ниже в табл. 9. и на рис. 3.
У детей раннего возраста, помимо представленных в табл.9 отклонений, отмечалась высокая частота сочетанного дисбаланса таких элементов, как марганца и магния (4- Mg— 4- Мп), достигающая 85%.
Сравнительное исследование элементного состава волос детей разного возраста, больных бронхиальной астмой
В литературе мы не обнаружили сведений об особенностях накопления макро- и микроэлементов в волосах детей разного возраста, больных бронхиальной астмой. Обнаруженные нами выше отличия в элементом составе волос больных детей 1—3 лет и 4 — 8 лет послужили предпосылкой для исследования возрастных особенностей макро- и микроэлементного дисбаланса при бронхиальной астме.
Поскольку группа детей первых трех лет жизни по тяжести бронхиальной астмы была однородной, а более старших — нет, мы сформировали из детей 4 — 8 лет новую подгруппу, сопоставимую с первой по клинической картине заболевания. Бронхиальная астма у детей обеих групп была среднетяжелой и тяжелой. Длительность заболевания составила в группе детей 1 — Зх лет 0,95 ± 0,21 лет, 4 — 8 лет — 2,78 ± 0,22 года. Все дети в последние 5 месяцев (среднее время роста пробы) проходили курсы стационарного лечения по экстренным показаниям в связи с приступом астмы.
Результаты сравнительного анализа элементных профилей при бронхиальной астме у детей разных возрастных групп представлены в табл.16.
Результаты исследования, представленные в табл.16, свидетельствуют, что у больных астмой детей в возрасте 1 — 3 лет, по сравнению с детьми 4 — 7 лет, достоверно чаще в волосах встречался недостаток Mg, Со, Fe, Мп и Si. Аналогичные результаты были получены и при сравнении частоты отклонений в макро- и микроэлементном составе волос у больных детей разных возрастных групп (рис. 8 ).
Проведенный анализ выявил существенное различие в макро- и микроэлементном профиле волос у детей разного возраста, больных бронхиальной астмы. У детей первых трех лет жизни наблюдался значительное снижение содержания в волосах Mn, Со, Fe, Mg при отсутствии различий с возрастной нормой в содержании Si. В то же время у детей старше 4х лет был выявлено существенное повышение Si в волосах. Следует заметить, что в норме у здоровых детей первых трех лет жизни, по сравнению с детьми более старшего возраста, содержание в волосах Со и Mg более высокое [89]. Таким образом, выявленное нами у детей младшей возрастной группы, по сравнению с детьми 4 — 7 — летнего возраста, сниженное содержание Со и Mg свидетельствует о более глубоком недостатке этих элементов у больных бронхиальной астмой в первые три года жизни.
Изменения макро- и микроэлементного состава волос при бронхиальной астме у детей разного возраста можно проиллюстрировать следующими тремя примерами.
Больная Маша С, 2,5 года, история болезни № 22305/ 99.
Клинический диагноз: Бронхиальная астма, средней тяжести, период обострения. Атопический дерматит, распространенная форма, непрерывно-рецидивирующее течение, круглогодичный аллергичекий ринит.Поливалентная аллергия.
Жалобы при поступлении: слизистое отделяемое из носа, высыпания на коже (в области щек, ягодиц), затруднение дыхания. Указанные явления появились за неделю до поступления.
Анамнез жизни. Ребенок из семьи с наследственной предрасположенностью к аллергии ( мать страдает с детства аллергодерматозом, у деда по линии отца бронхиальная астма).
Бытовые условия удовлетворительные.
Девочка от первой беременности, осложненной на всем протяжении угрозой прерывания , в конце данной беременности мать перенесла ОРВИ. Родилась в срок, роды протекали без осложнений.
Период новорожденности протекал без особенностей. Грудное вскармливание до 9 месяцев. В возрасте одного месяца впервые появились высыпания , сопровождающиеся мокнутием, сначала на лице, затем распространились по всему телу. Обострения экссудативно-катарального диатеза на первом году наступало после введения большинства новых продуктов. В дальнейшем периодически отмечались обострения заболевания , главным образом, в летнее время . Болела ОРВИ до 5 раз в год . Полного курса вакцинации провести не удалось После введения вакцин наблюдалось обострение экссудату то-катарального диатеза.
После года возникали проявления пищевой (после приема в пищу цитрусовых, орехов, любых продуктов с красителями, сладкой и жареной пищи), эпи-дермальной (на шерсть кошки ), пыльцевой ( преимущественно на луговые травы) и бытовой (на домашнюю пыль ) аллергии . Контакт с аллергеном вызывал обострение атопического дерматита, риноконъюнктивального синдрома и приступы бронхиальной астмы. Наиболее выраженные проявления аллергии отмечались в летний период, значительно реже — осенью.
Анамнез заболевания. Впервые приступ затрудненного дыхания возник в 2 года, на фоне ОРВИ. В дальнейшем частота приступов была около 2 раз в неделю, по экстренным показаниям госпитализировалась в стационар, во время первой из них был установлен диагноз: «Бронхиальная астма». На фоне лечения эуфиллином и ингаляционных бронхоспазмолитиков отмечался положительный эффект. Течение заболевания сопровождалось ночными обострениями, не нарушающими сна. Приступы возникают на фоне ОРВИ, после вдыхания влажного воздуха, нарушения диеты, контакта с шерстью кошки и или бытовой пылью, с пыльцой луговых трав. По продолжительности отмечаются как короткие, так и длительные (до 2 дней на фоне ОРВИ) обострения. За год до проведения исследования волос девочка получала кетотифен, на фоне которого не было отмечено сухцественных изменений в клинической картине болезни. Базисной терапии в течение этого времени не было ( из-за нежелания родителей ). В качестве бронхорасширяющей терапии применялся сальбу-тамол и эуфиллин.
При поступлении: состояние удовлетворительное, сознание ясное. Одышки, втяжения уступчивых мест, катаральных явлений в носоглотке не отмечено. Тахипное, тахикардия отсутствовала. В легких выслуишвачись единичные сухие хрипы с обеих сторон. Печень выступала из-под края реберной дуги на 1 см, болезненности при пальпации не отмечалось, все физиологические отправления были нормальными.
Данные лабораторных исследований. В общем анализе крови: НЬ 119 г /л, лейкоциты 13 xlO9 /л; и/я нейтрофилы 1% 109 /л , с/я 54% 109 /л, лимфоциты 29%- 109/л, моноциты б%- 109/л, СОЭ 3 мм/ ч. Эозинофилы 10 % 109 /л. Биохимический анализ крови: общий белок 70 г/л , серомукоид 0,140 ед., ЩФ — 276Ед/л , определялся СРВ, холестерин 4,7ммоль/л; АЛТ68 Ед/л, ACT66 Ед/л, ЛДГ 480 Ед/л; К 4,0 ммоль/л, Na 140 ммоль/л, Р 1,14 ммоль/л . Уровень иммуноглобулина класса А- 60, G — 895, М-106 мг %, что находится в пределах возрастной нормы.
В посеве со слизистых ротовой полости патогенной и кандидозной флоры не обнаружено.
При исследовании общего и специфических Ig Е выявлена сенсибилизация к пыльцевым аллергенам: тимофеевки, ежи, овсянннице, амброзии, домашней пыли (+ +); сенсибилизации к другим неинфекционным аллергенам не обнаружено. Из группы инфекционных аллергенов выявлена слабая сенсибилизация к грибковым аллергенам рода Penicillium и Altemarium ( ). Уровень общего иммуноглобулина Е в крови был повышен: 135 кЕд/л (при норме до 24 кЕд/л) .
При рентгенологическом исследовании органов грудной клетки выявлено усиление сосудистого рисунка в медиальных отделах легких при отсутствии очаговых и инфильтративных изменений.
При ультразвуковом исследовании органов брюшной полости обнаружены признаки реактивного изменения поджелудочной железы и уплотнение пе-рипортального тракта.
На элетрокардиограмме выявлялась выраженная синусовая тахикардия, вертикальное положение электрической оси сердца, высота и длительность интервалов зубцов соответствовала норме (РО — 0,14 ; QRS — 0,08 ; QRST -0,30%
Проба волос для исследования содержания макро и микроэлементного состава была взята спустя месяц после последнего обострения бронхиальной астмы. Результаты анализа методом АЭС-ИП в сравнение с данными исследования популяции г. Москвы в возрасте 1-3 лет и группы здоровых детей аналогичного возраста приведены в табл.17.
В волосах девочки было выявлено повышение содержания калия, умеренное снижение цинка, селена, железа, магния и значительное — марганца.
Таким образом, изменения макро- и микроэлементного профиля волос девочки характерны для выявленных нами особенностей элементного профиля волос детей раннего возраста, больных бронхиальной астмой.
Ниже приведены истории болезни и результаты исследования волос ( методы АЭС-ИП и НАЛ) двух детей 4 и 8 лет, больных бронхиальной астмой.
источник
 Магний (Mg) обладает некоторыми спазмолитическими свойствами, расслабляет мышцы. Снижает восприимчивость организма к аллергенам. Его в некоторых случаях при бронхиальной астме даже назначают внутривенно.
Магний (Mg) обладает некоторыми спазмолитическими свойствами, расслабляет мышцы. Снижает восприимчивость организма к аллергенам. Его в некоторых случаях при бронхиальной астме даже назначают внутривенно. пиридоксин – онемение в области конечностей, уменьшение лактации у женщин, изредка судороги;
пиридоксин – онемение в области конечностей, уменьшение лактации у женщин, изредка судороги;