Анкета для опроса пациентов с бронхиальной астмой позволяет эффективно, дешево, а главное, быстро собрать и адекватно оценить информацию, особенно это важно для врача, когда речь идет о приеме больных в поликлинике.
Времени, чтобы определить тяжесть болезни и внести поправки в лечение, мало, а человек с этим заболеванием требует особого внимания для предотвращения опасных осложнений и даже инвалидизации и смерти.
По данным эпидемиологических исследований, количество больных с диагностированной бронхиальной астмой растет год от года. Современная медицина достигла больших успехов в изучении процессов возникновения этого заболевания, в раннем выявлении первых симптомов, в применении современных эффективных лекарственных средств и профилактических методов, но смертность от него увеличивается. Это связано со следующими причинами:
- неадекватная оценка пациентами тяжести своего заболевания;
- нерегулярность приема препаратов;
- частичное или полное невыполнение рекомендаций лечащего врача;
- неправильная техника использования ингаляционных лекарств.
Но астму можно успешно лечить и полностью контролировать, т.е. практически не испытывать неприятные симптомы ни днем, ни ночью, не принимать быстродействующие препараты для снятия приступа и даже жить полноценно, без ограничений, как люди со здоровой дыхательной системой.
Другими словами, контроль – это конечная цель терапии, когда в результате кропотливого труда врача и пациента удается достичь хорошего самочувствия при минимальном количестве препаратов.
На протяжении жизни одного человека симптомы астмы могут исчезать и появляться снова, поэтому разработан ступенчатый подход к лечению, при котором по мере нарастания тяжести заболевания увеличивается интенсивность приема лекарств.
Астматик должен всегда принимать базисный препарат, как правило, это гормональные препараты с противовоспалительным действием (ингаляционные глюкокортикостероиды). При ухудшении дозу лекарств увеличивают, добавляют препараты с другим механизмом действия, при улучшении – убирают. Цель лечения – достижение контроля течения бронхиальной астмы.
Но понятие контроля многоплановое, и долгое время не было единого объективного метода его оценки. Это привело к разработке множества диагностических систем, которые учитывают симптомы бронхиальной астмы, ночные приступы и их количество, историю развития заболевания (анкеты, вопросники), оценку результатов лабораторных исследований и показателей функции дыхания, полученных при пикфлоуметрии, спирометрии.
Аппаратными методами оценки функционирования дыхательной системы пользуются преимущественно для диагностики астмы, для ежедневного контроля они не подходят, так как сложны в исполнении, недоступны для детей до 5 лет. Их показатели могут искажаться на фоне приема бронхорасширяющих лекарств.
Анкета по бронхиальной астме стала более перспективным вариантом, и с 2008 г. публиковалось их большое количество. Наибольшее применение получили тест по контролю АСТ (Astma Control Test) и вопросник ACQ-5 (Asthma Control Questionnaire). Они имеют небольшие различия.
ACQ-5 не содержит вопросов о применении быстродействующих препаратов, снимающих спазм бронхов, поэтому его результаты могут быть несколько завышены. Его преимуществом над АСТ является возможность предсказать количество обострений у пациента в ближайший год и изменить лечение заранее.
Для оценки уровня контроля удобен простой тест АСТ, который больной может пройти сам и адекватно оценить свой статус. Его удобно проводить в любое время суток, на работе, дома или в поликлинике. Он представлен двумя формами: для взрослых и для детей. Ведущие пульмонологические центры одобрили АСТ для использования в медицинской практике.
Анкета по бронхиальной астме доказала свою достоверность: результаты теста совпадают с оцененным специалистом-пульмонологом состоянием пациента и с данными спирометрии. И если она покажет, что состояние пациента неудовлетворительное, то необходима консультация доктора для своевременной коррекции терапии.
С диагностическими целями врачом могут быть заданы дополнительные вопросы. Так в докладе рабочей группой GINA (Глобальная инициатива по бронхиальной астме) было предложено простое исследование. Необходимо задать вопросы больному астмой о состоянии его здоровья в течение последнего месяца:
- Дневные приступы астмы чаще, чем 2 раза в неделю?
- Были ли ночные приступы астмы?
- Принимали ли вы препараты быстрого действия чаще двух раз в неделю?
- Испытываете ли вы ограничение физической активности?
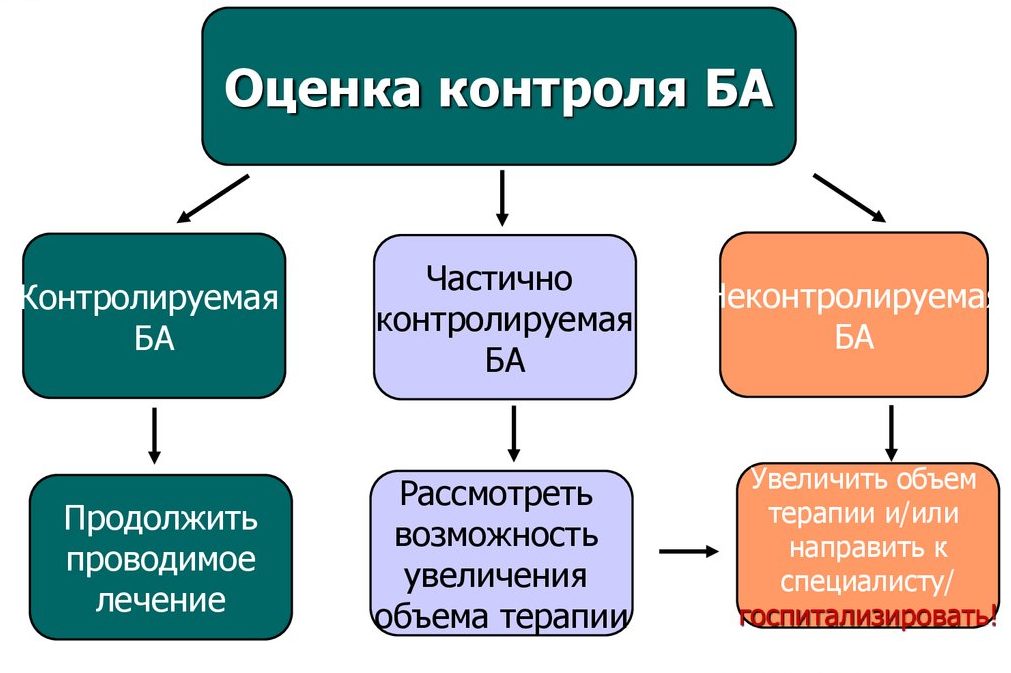
Результаты трактуются так:
- контролируемая бронхиальная астма, если ответ «нет» на все вопросы. Лечение остается прежним;
- частично контролируемая, если ответ «да» на 1-2 вопроса. Возможно внесение некоторых изменений в схему приема или дозировку лекарственных препаратов;
- неконтролируемая, если положительные ответы на 3-4 вопроса. Требуется срочная коррекция базисной терапии, возможна госпитализация пациента.
Если вы сомневаетесь, под контролем ли ваша бронхиальная астма, ответьте на вопросы анкеты АСТ самостоятельно. Тест легко можно найти в Интернете или получить у лечащего врача. Есть отдельные варианты для детей и для взрослых. Методика проведения теста проста и понятна.
Опросник состоит из 5 вопросов, на каждый из которых нужно выбрать один из предложенных вариантов ответа. За ответы начисляются баллы от 1 до 5, которые в итоге суммируются. По набранному количеству баллов можно оценить данные о течении заболевания за последние 4 недели.
- 25 баллов – астма полностью контролируется.
- 20-24 балла – хорошо контролируется.
- Менее 20 баллов – астма контролируется неудовлетворительно, надо обратиться к медицинскому специалисту для изменения схемы лечения и предотвращения развития возможных осложнений.
Бронхиальная астма неизлечима, но с ней можно жить полноценно, без приступов удушья и затруднения дыхания, если контролировать свою болезнь. Анкетирование астматиков позволяет своевременно выявить обострение бронхиальной астмы, предотвратить развитие опасных осложнений.
Успех лечения будет зависеть не только от выполнения врачебных рекомендаций и приема препаратов, но и от уровня осведомленности об особенностях болезни. Получать полезную информацию нужно из надежных источников (медицинская литература, специализированные веб-сайты).
источник
Бронхиальная астма (БА) является одним из самых распространенных заболеваний на всех континентах. По оценке экспертов, уже около 235 млн. человек страдает от этого заболевания. А к 2025 г., учитывая стремительно нарастающую урбанизацию, количество больных БА может увеличиться еще на 100 млн.
Ежегодная смертность от бронхиальной астмы (БА) составляет около 250 000 человек, при этом отсутствует четкая корреляция между распространенностью и смертностью от заболевания. В Российской Федерации, согласно официальной статистике, довольно низкая заболеваемость БА — в диапазоне 0-2,5% от общей популяции. В то же время отмечается высокая смертность от БА — 28,6 случая на 100 000 населения.
Долгое время тяжесть заболевания была определяющим фактором в тактике ведения и принятии решения об объеме необходимой ингаляционной терапии у больных бронхиальной астмой (БА). Были выработаны различные критерии легкой, среднетяжелой и тяжелой БА, в соответствии с которыми предлагалось вести пациентов. Одним из основных критериев тяжести был объем форсированного выдоха за 1-ю секунду.
Однако исследования, проведенные в конце ХХ века, убедительно доказали, что степень тяжести бронхиальной астмы (БА) не всегда объективно отражает состояние пациента и его прогноз. Выявлено, что смертность от БА слабо коррелирует с тяжестью заболевания и с одинаковой частотой присутствует как у пациентов с легкой формой БА, так и у тяжелых больных.
Контроль астмы с точки зрения современной медицины подразумевает отсутствие симптомов заболевания, в настоящее время это основной ориентир клиницистов при лечении БА. Стоит отметить, что говорить о контроле заболевания начали задолго до XXI века. Первые статьи о попытках контроля бронхиальной астмы (БА) появились одновременно с применением системных глюкокортикостероидов. Так, в 1954 г. в журнале Lancet опубликована статья под названием «Длительный контроль тяжелой бронхиальной астмы с помощью перорального кортизона», где впервые говорится о попытке контролировать заболевание.
В начале 2000-х годов формируется парадигма контроля бронхиальной астмы (БА), где основными ориентирами служат клинические симптомы, потребность в короткодействующих B2-агонистах (КДБА), ночные приступы и ограничение физической или повседневной активности, связанные с БА. Этот подход получил широкое распространение во второй половине 2000-х годов.
Было доказано, что ориентация клинициста на контроль бронхиальной астмы (БА) позволяет существенно улучшить указанные выше параметры в сравнении с подходом, основанным на тяжести болезни. При этом смертность от БА также начала снижаться.
Уже в 2008 г. в международном документе Глобальная инициатива по бронхиальной астме (GINA) предлагается подходить к тактике ведения больных бронхиальной астмой (БА) с позиции контроля. А в редакции 2010 г. уходит понятие тяжести, которое рекомендуется использовать больше в научных целях, чем в ежедневной практике.
Для оценки уровня контроля бронхиальной астмы предложены удобные в использовании вопросники, у каждого из которых есть свои преимущества. На территории Российской Федерации наибольшее распространение получили тест по контролю над бронхиальной астмой (Asthma Control Test — ACT) и вопросник по контролю над бронхиальной астмой (Asthma Control Questionnaire, 5-я версия — ACQ-5). Оба теста валидизированы и рекомендованы к применению в общей рутинной практике.
Астма контроль тест (АСТ) — это вопросник, состоящий из 5 шкал, которые заполняются пациентом, этот тест продемонстрировал хорошую надежность и высокий уровень корреляции со степенью контроля над БА. Тем не менее при сумме баллов >20 достоверность наличия контролируемой БА составила только 51%. Использование этого теста затрудняет дифференцировку между контролируемой и частично контролируемой БА и может привести к тому, что пациенты, нуждающиеся в увеличении объема терапии, будут отнесены в группу контролируемой БА.
Вопросник по контролю над бронхиальной астмой (БА) АCQ-5 является производным от теста ACQ, который в изначальной редакции состоял из 7 вопросов. Из первоначального теста были изъяты вопросы об использовании короткодействующих B2-агонистов (КДБА) в течение недели и показателях функции внешнего дыхания. Это может несколько завышать уровень контроля, поскольку потребность в КДБА является одним из основных показателей в его оценке.
В то же время доказано, что вопросник ACQ-5 хорошо коррелирует с критериями контроля БА по GINA и Gaining Optimal Asthma Control (GOAL). Число баллов по ACQ-5 менее 1 позволяет выявлять пациентов с контролируемым течением БА сопоставимо с оценкой контроля по критериям GINA и GOAL. Положительным отличием ACQ-5 от АСТ является возможность прогнозирования количества обострений у больного в течение следующего года, что позволяет выявить пациентов из групп риска и заранее скорректировать терапию.
В исследовании НИКА (2012) продемонстрировано, что ACQ-5 не имел статистически значимых отклонений от оценки контроля бронхиальной астмы (БА) по критериям GINA. Вопросник ACQ-5 оценивал удовлетворительный уровень контроля у 39% больных, тогда как согласно критериям GINA симптомы контролировались у 43% пациентов. Шкала ACT позволила выявить 33% случаев контроля бронхиальной астмы, что статистически значимо отличалось от результатов полученных при использовании критериев GINA.
К положительным аспектам применения АСТ можно отнести простоту арифметических расчетов, в то время как на тест ACQ-5 может уйти несколько больше времени. Учитывая большой поток пациентов на приеме у терапевтов, пульмонологов, аллергологов, это может оказаться немаловажным.
Проведенные исследования доказывают, что оба теста могут использоваться в качестве конечных точек клинических исследований. Однако до конца их взаимозаменяемость оставляет ряд вопросов. Следует отметить, что в последней редакции GINA предложено исходить из оценки параметров в течение 1 месяца, в то время как ACQ-5 в отличие от АСТ предлагает оценку в течение 1 недели.
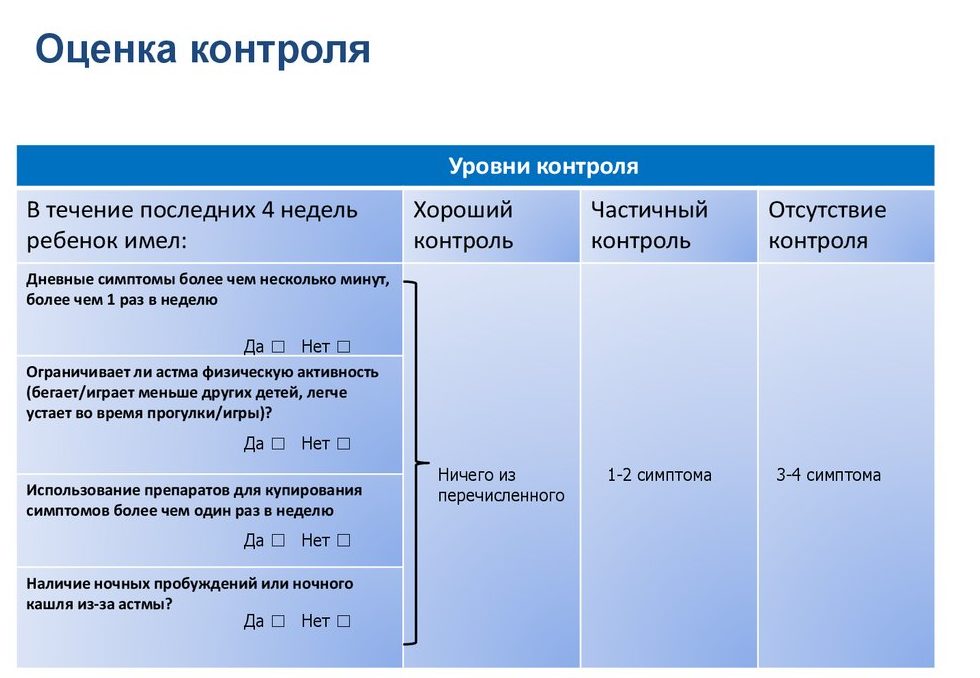
Последняя редакция GINA предельно упростила понимание оценки контроля заболевания и предлагает клиницисту задать пациенту следующие вопросы о его самочувствии в течение последних 4 недель:
- Дневные симптомы более чем 2 раза в неделю?
- Ночные пробуждения из-за симптомов астмы?
- Потребность в препаратах скорой помощи более 2 раз в неделю?
- Ограничение активности?
Если на все вопросы ответ отрицательный — это контролируемое течение бронхиальной астмы (БА); при положительном ответе на 1-2 вопроса — частично контролируемое; при положительном ответе на 3-4 вопроса симптомы бронхиальной астмы у пациента не контролируются и требуется серьезно пересмотреть базисную терапию.
© Аспирант Д.А. Нагаткин, Врач-пульмонолог О.В. Нагаткина, Д.м.н., профессор А.В. Жестков.
источник
Топографическая анатомия легких
Нормальная рентгенограмма легких




Рис. Нормальная рентгенограмма легких (вид спереди) Рис. Средостение
Граница правого предсердия
10. Тень верхней полой вены
12. Правая легочная артерия
10.Правая легочная артерия
Рис. Нормальная рентгенограмма
Рис. Топография сегментов легких
Средняя доля правого легкого:
Рис. Доли легких (вид спереди)
Рис. Доли легких (вид сзади)
А — горизонтальная (малая) щель В — правая большая щель С — левая большая щель


Рис. Сегменты легких (вид сзади)
























Рис. Доли легких (правая боковая проекция)



Наиболее распространенные заболевания органов дыхания
Дифференциальная диагностика бронхообструктивных заболеваний
источник
В современной медицине классификация все больше становится прикладным инструментом, позволяющим достичь главной цели – избавить пациента от болезни или как можно сильнее уменьшить ее проявления с помощью лечения. Таким образом, деление заболевания на варианты, формы, степени во многом становится условным. В ходе лечения нередко один вариант заболевания сменяется другим, отличие которого заключается прежде всего в ином лечении.
Бронхиальная астма не стала исключением. Если в прежние годы врачи выделяли степени тяжести болезни, то в последней редакции всех отечественных и зарубежных руководств внимание переместилось на степень контроля заболевания, то есть на интенсивность и эффект лечения.
Классификация по степени тяжести сохраняет свое значение при первом визите пациента к врачу, когда он еще не получает никакого лечения, особенно ингаляционных глюкокортикоидов и других средств базисной терапии.
Классификация по степени тяжести определяет, насколько поражено бронхиальное дерево. Она помогает определить, какие препараты следует назначить и в какой дозировке, чтобы в дальнейшем добиться устранения симптомов болезни. Это деление проводится исключительно до начала лечения.
Тяжесть течения оценивается по наличию клинических проявлений в сочетании с показателями функции внешнего дыхания (ФВД), прежде всего объема форсированного выдоха за 1 секунду (ОФВ1) и пиковой скорости выдоха (ПСВ).
- Интермиттирующее течение, или I ступень, характеризуется нечастыми признаками (кашель, одышка), беспокоящими больного реже 1 раза в 7 дней и до 2 раз в месяц ночью; данные ФВД близки к нормальным.
- Астма легкой степени, или II ступени, сопровождается более частым появлением клинических признаков: днем чаще раза в 7 дней, но не ежедневно, ночью – чаще 2 раз в месяц. При обострении болезни может быть нарушен сон и снижена активность больного. Данные ФВД при этом остаются близкими к нормальным.
- Средняя степень (III ступень) сопровождается ежедневными проявлениями, ночью симптомы возникают раз в 7 дней и чаще. Пациент вынужден ежедневно пользоваться препаратами «скорой помощи» (сальбутамол) для устранения кашля или удушья. Функция внешнего дыхания ухудшается.
- Тяжелое течение (IV ступень) сопровождается ежедневными приступами и частыми симптомами в ночные часы. Заболевание протекает с частыми обострениями, во время которых ограничивается физическая активность пациента. Показатели ФВД меньше 60% от должных величин.
Если клиническая картина и данные спирометрии не совпадают, степень тяжести устанавливают согласно более тяжелым признакам.
Тяжесть заболевания можно охарактеризовать и у больных, уже получающих лечение. В этом случае легким считается течение болезни, которое можно контролировать с помощью небольшого количества лекарств и низких дозировок. Тяжелая астма в этом случае – состояние, требующее назначения комплексной терапии в больших дозах. Плюсом этой классификации является учет получаемой больным терапии, дающей представление об истинной тяжести болезни.
Таким образом, у больного с исходной IV степенью тяжести болезни на фоне лечения мы можем добиться такого контроля над астмой, что у него вообще не будет приступов ночью, а днем он лишь иногда будет пользоваться, например, сальбутамолом. Однако получится это у врача только при назначении соответствующей комбинированной базисной терапии, что соответствует астме тяжелого течения.
Задача врача при бронхиальной астме у пациента – добиться контроля заболевания, то есть предотвращения ее проявлений. Полное излечение при этом заболевании считается невозможным. Оценив на первом приеме тяжесть состояния пациента, врач назначает ему лекарственную терапию. В процессе дальнейшего наблюдения он оценивает уже не степень тяжести, а уровень контроля над заболеванием, при необходимости изменяя лечение.
Для оценки уровня контроля используются разнообразные опросники. Их можно применять начиная с возраста пациента 4 года. Для взрослых наиболее распространен «Тест контроля над астмой». Если при ответе на все вопросы сумма составила 25 баллов – контроль хороший;20 – 24 балла – недостаточный; менее 20 баллов – результат плохой, нужно срочно обратиться к врачу. Для детей создан детский вариант теста: если ребенок набрал 19 баллов и меньше – это говорит о плохом контроле над заболеванием.
На необходимость усиления терапии указывает частое использование средств «скорой помощи» (например, сальбутамола). При этом следует увеличить объем терапии до достижения контроля над признаками болезни. Если состояние полного контроля сохраняется более 3 месяцев, можно попробовать уменьшить интенсивность лечения до минимальных поддерживающих доз.
Различают три уровня контроля над болезнью:
- контролируемая астма;
- частично контролируемая;
- неконтролируемая.
При полностью контролируемой патологии в течение как минимум месяца:
- регистрируется меньше двух эпизодов ухудшения в неделю;
- ночные пробуждения из-за симптомов болезни отсутствуют;
- физическая активность не ограничена;
- необходимость пользоваться препаратами «скорой помощи» отсутствует или есть, но не чаще двух раз в неделю;
- ФВД в пределах нормы (для детей старше 5 лет).
При частично контролируемом течении болезни хотя бы один из перечисленных показателей наблюдается чаще или выражен сильнее. Показатели ФВД меньше 80% от нормы или наилучшего известного для данного пациента показателя.
При неконтролируемой патологии могут наблюдаться три и более из следующих признаков:
- более двух эпизодов ухудшения самочувствия в неделю;
- любые ночные симптомы;
- любое ограничение активности;
- потребность в препаратах «скорой помощи» чаще 2 раз в неделю;
- ФВД менее 80% от нормы.
Кроме того, учитывается риск осложнений. Он увеличивается при плохом контроле, частые обострения, госпитализация в отделение интенсивной терапии по поводу этой патологии, низкий показатель ОФВ1, курение, необходимость приема лекарств в большой дозировке.
Под обострением понимается 7 и более дней неконтролируемого течения болезни.
Некоторые пациенты считают, что частые приступы удушья, ежедневная потребность в ингаляциях сальбутамола, одышка – признаки тяжелого течения патологии. Однако такое мнение не совсем верно. Это признаки неконтролируемого течения заболевания, которое может быть как при тяжелой, так и при легкой астме.
С чем может быть связана невозможность полного контроля над болезнью? Прежде всего, необходимо узнать, насколько пациент выполняет требования по элиминации аллергенов, правильно ли он проводит ингаляции, выполняет ли все назначения врача. Затем нужно устранить провоцирующие факторы – гастроэзофагеально-рефлюксную болезнь, синуситы, хронический ринит. Примерно у четверти больных безуспешность терапии связана с неправильно поставленным диагнозом, когда за астму принимается другое заболевание. Если же все эти факторы устранены, нужно усилить терапию.
Однако у части пациентов, несмотря на интенсивное лечение, добиться полной ремиссии не удается. Чаще всего это связано с генетическими и анатомическими особенностями – изменчивостью рецепторов к интерлейкинам, смешанным типом воспаления, наличием внутриклеточных возбудителей, более толстой стенкой бронхов и другими особенностями. Изучение таких вариантов продолжается, оно позволит в будущем создать новые препараты для помощи людям с тяжелой неконтролируемой бронхиальной астмой.
источник
1. Можете ли вы «выпустить пар» при гневе или «кому-нибудь что-нибудь насвистеть»? Можете ли вы вспомнить еще какие-либо пословицы и поговорки относительно вашего заболевания? Что это за пословицы?
2. Кто и когда сообщил вам о вашем заболевании?
3. Регулярно ли вы принимаете предписанные вам лекарства? Знаете ли вы, как они действуют, что вы можете от них ожидать и какие возможны побочные эффекты?
4. Сдерживаете ли вы себя, потому что для вас важно, «что подумают люди»?
5. Можете ли вы сказать о своей работе, что вы чувствуете себя ограничиваемым, задавленным, перегруженным?
6. Какие особенности поведения (актуальные способности) коллег, сотрудников, шефа действуют вам «на нервы»? Как вы реагируете? Можете ли вы открыто говорить об этом? Или вы «задерживаете дыхание»?
7. Характеризуются ли ваши отношения с окружающими «плохой атмосферой», «спертым» или «напряженным» воздухом, что «затрудняет ваше дыхание»? Являются ли определенные люди «отдушиной» для вас?
8. Можете ли вы вывести кого-либо «на чистую воду»?
9. Знаете ли вы или можете вспомнить такие желания, может быть, детские мечты, которые вы никогда не могли воплотить в жизнь? Что препятствует их реализации? Что бы вы стали делать и как бы стали жить, если бы у вас не стало проблем?
10. Что для вас является смыслом жизни (стимул, цель, мотивация, жизненный план, смысл болезни и смерти, жизнь после смерти)?
11. Можете ли вы воспринимать свое страдание как шанс познать неведомые до сих пор сферы?
СЕРДЕЧНО-СОСУДИСТЫЕ ЗАБОЛЕВАНИЯ
Заболевания сердца и сосудов в экономически развитых странах являются самой частой причиной смерти. В последние годы кардиологи все большее значение придают психосоциальным факторам риска и их связи с соматическими факторами (Burns, Katkin, 1993; Burns et al., 1993; Cohen et al., 1994; Contrada, 1994; Dembroski, MacDougall, 1983; Miller et al., 1996). Образ жизни, установки личности и положение человека в его профессиональном и семейном окружении важны для кровообращения и его физиологической регуляции. Издавна известны такие соматические факторы риска, как неправильное питание, ожирение, курение и злоупотребление алкоголем, в которых отражаются особенности личности (Бройтигам и др., 1999).
Психосоматический компонент в первую очередь характерен для следующих заболеваний сердечно-сосудистой системы:
• эссенциальная артериальная гипертония;
• ишемическая болезнь сердца;
• нарушения сердечного ритма;
Сердце и сосуды участвуют во всех формах жизнедеятельности, хотя в норме человек этого не осознает. При физических и психических нагрузках работа сердца начинает восприниматься в виде усиленного сердцебиения или тахикардии. В отличие от моторики или дыхания, деятельность сердца и сосудов исключена из непосредственного человеческого восприятия. И только при определенных пограничных состояниях и нарушениях сердце воспринимается осознанно. Даже в случаях тяжелых нарушений, например при врожденном пороке сердца, сердечные феномены субъективно воспринимаются лишь на поздних стадиях декомпенсации. Однако и в этих случаях возникает своеобразная неопределенность: «сердце
Сердечно-сосудистые заболевания
хотя и мое, но оно какое-то неопределенное и не поддающееся управлению, как, например, конечность». Это чувство неопределенности уже содержит в себе зародыш страха. На этом основывается предположение о возможности фобического развития личности.
Психическая сфера так же определяет функции сердца и сосудов, как и соматическая. Активность и покой, сон или бодрствование, душевная живость и возбуждение, выраженные внешне или подавленные чувства связаны с различными состояниями системы кровообращения. Связь деятельности сердца с эмоциями отражена во множестве идиом и поговорок.
Несмотря на то что изменения работы сердца в равной степени проявляются и при положительных, и при отрицательных чувствах, патологические нарушения в сердечно-сосудистой системе связаны со страхом, гневом, яростью, тоской и другими отрицательными эмоциями, которые приводят к тому что, например, при страхе одиночества, при опасности нападения возникает ощущение, будто сердце начинает стучать в горле и в области головы. Происходящий при этом выброс адреналина вызывает сужение сосудов, учащение пульса и усиление сокращения миокарда, что, в свою очередь, приводит к состоянию беспокойства и страха.
Если из-за внешних задержек или внутреннего торможения уже подготовленная активизация кровообращения не реализуется, в ряде случаев при этом в течение длительного времени может сохраняться возбуждение в ожидании выполнения действия. Возможна и обратная ситуация: вытесненная из сознания установка на действие приводит к замещающему ее напряжению в системе кровообращения.
Сердце обычно связывают с любовью. Возникает вопрос: почему разрыв отношений, потеря близкого человека нередко приводят к сердечным заболеваниям? Если мать не дает своему ребенку достаточно тепла, он проявляет к своей кукле чувства, которые хотел бы ощутить в своей матери. Кукла становится заменой близкого человека.
Некоторые кардиологи предполагают, что иногда сердце превращается в символ близкого человека и на него переносятся все те чувства, которые по каким-то причинам не могут быть выражены открыто. Человек боится показать другим свое недовольство. Женщина не решается возражать любимому человеку и для того, чтобы уменьшить тоску и избежать де-
прессии, тиранит собственное сердце, вымещая на нем свое раздражение.
Главную роль в патогенезе сердечно-сосудистых заболеваний играют подавляемая враждебность (Barefoot et al., 1996; Barefoot et al., 1994; Benotsch et al., 1997; Siegman, Smith, 1994; Siegman et al., 1992) и поведение типа А (Booth-Kewley, Friedman, 1987).
2.1. ЭССЕНЦИАЛЬНАЯ ГИПЕРТОНИЯ
Картина личности
Поскольку в большинстве случаев четко датировать начало заболевания не представляется возможным, трудно говорить и о вызывающей ее ситуации. Однако в качестве причинных ситуаций описаны определенные внутренние конфликты (Gentry, et al., 1982; Irvine, et al., 1991; Saab, Schneiderman, 1993). Артериальная гипертония часто начинается тогда, когда человек пребывает в ситуации хронического напряженного ожидания (Grace, Graham, 1952). Типичные высказывания гипертоников: «я должен быть готов ко всему», «я такой, что принимаю на себя все трудности», «никто меня не удержит, я готов на все». Провоцирующими ситуациями часто бывают длительные состояния страха, нехватка времени и нарастающее напряжение. Кроме того, описываются ситуации, в которых имеется возможность разрядки враждебности и агрессивности, но этого не происходит в силу торможения или щепетильности.
Многочисленные эксперименты как с животными, так и с людьми показали, что при страхе, гневе и озлобленности повышается давление и что хроническое эмоциональное перенапряжение может приводить к стойкой гипертонии (Coeher, 1971, Groen et al.,1971, Angermeier, Peters, 1973; Cannon, 1953; Reindell et al., 1971). Общепринято мнение, что у гипертоников существует связанная со страхом хронически подавляемая агрессия.
Для больных гипертонией описывают типичную невротическую личностную структуру с преобладанием навязчивых состояний, в результате чего часто возникают внутренние и внешние конфликты, что затрудняет эмоциональную разрядку (Groen et al.,1971).
Тот факт, что эссенциальная гипертония часто встречается у членов одной семьи, может интерпретироваться в смысле «психологического наследования» (Hermann et al.,1989). Экспериментальные исследования показывают, что больные гипертонией склонны к повышению давления даже в тех ситуациях, которые у нормотоников не вызывают никаких изменений давления (Hodapp, Weyer, 1982).
По данным Александера (2002), центральным пунктом психодинамики пациента с эссенциальной гипертонией является постоянная борьба с нарастающим враждебно-агрессивным чувством. В то же время существуют трудности самоутверждения. Пациенты боятся потерять благосклонность других людей и поэтому контролируют проявления своей враждебности. В детстве они обычно склонны к приступам ярости и агрессии. Бывший прежде агрессивным ребенком, взрослый человек становится подчеркнуто уступчивым, не может за себя постоять. Понимание возможности потерять из-за своей агрессивности расположение родных и близких заставляет ребенка контролировать свою враждебность и скрывать ее. Больные артериальной гипертонией постоянно проявляют раздражительность, если сталкиваются с непреодолимым сопротивлением. Их жизнь навязывает им роль «ломовой лошади». Они застревают на многие годы на одной работе и редко меняют фирму, даже если им недоплачивают. Если они добиваются начальственного положения, им трудно стать авторитетом для других. Они выполняют работу за других, вместо того чтобы наладить дисциплину. Из этого сверхсовестливого и доводящего до крайностей поведения с излишним чувством ответственности рождаются усиленные чувства гнева, неприязни и агрессивности, со временем требующие все больших усилий для их сдерживания. Так развивается порочный круг, который приводит к хроническому состоянию напряжения. Характерная ситуация, провоцирующая заболевание, представляет собой жизненные конфликты, которые мобилизуют враждебность и стремление к самоутверждению и одновременно создают невозможность их свободного выражения.
Первоначально эти черты были обнаружены в наблюдавшемся поведении больных. В дальнейших исследованиях показано, что в сравнении с нормотониками у них изменено восприятие конфликта и стресса. Например, летные диспетчеры подвергаются угрозе повышения давления не только то-
гда, когда идентифицируют себя со своей профессией и являются адаптивными и обходительными с сослуживцами, но и когда они не воспринимают и отрицают производственный стресс (Rose et al.. 1978).
В формировании гипертонии играет роль и непосредственное взаимодействие в семье, что показано в исследованиях конфликтного поведения в семьях с отцом-гипертоником, в которых изучалась семья как клиническое единство, исходя из системного видения симптомов (Ваег et al., 1959, 1933; Ва-ег, 1983).
Структура личности члена семьи — например, конфликтно-агрессивный импульс гипертоника — затрагивает поведение взаимодействия семьи в целом («семейное накопление» эссенциальной гипертонии). В каждой семье между родителями и детьми формируются правила, по которым регулируются конфликты; в семьях с отцом-гипертоником дети имеют менее эффективные возможности для перенесения и решения конфликтов, о чем свидетельствует преобладание в этих семьях негативно-невербальной коммуникации (например, не давать ответ, отворачивать голову, избегать контакта взглядами). Разнообразные исследования указывают на то, что ограниченное восприятие конфликта и стресса и избегание конфликта коррелирует с появлением повышенного давления крови, т. е. это типы поведения, которые дети в процессе социализации в семье приобретают от гипертоника-отца. Эта точка зрения могла бы наряду с генетическим компонентом открыть дополняющий аспект возможного воспроизведения эссенциальной гипертонии (Theorell, 1990; Любан-Плоцца и др., 2000).
Семейное взаимодействие характеризуется своего рода запретом на речь или коммуникацию, затрагивающим также и невербальную сферу, вследствие чего преобладают понимающие, наблюдающие, контролирующие, сдерживающие активности, в то время как отдающие, сообщающие, участвующие выражения появляются редко (Kroger, Petzold, 1985).
Единой личностной структуры для всех больных артериальной гипертонией не установлено. Впрочем, при широком распространении и большом разнообразии форм болезни этого и не следует ожидать.
И все же среди психосоматически обследованных предварительно отобранных пациентов постоянно повторяются определенные личностные черты. Гипертоники описываются
_______________________Сердечно-сосудистые заболевания
как люди трудолюбивые, приверженные долгу, общительные, с большим чувством ответственности. В связи с этим у них возникают внутренние и внешние конфликты, от которых они не могут эмоционально отстраниться. В своей специфической установке на скромность они отказываются от своих потребностей в пользу других, желая получить от них одобрение и не провоцировать агрессию или неприязнь. Именно эти признаки, описываемые независимо друг от друга разными исследователями как готовность помочь, стеснительность, хронически подавляемая агрессивность, и составляют манифестные свойства личности, которые имеют большое значение для формирования характерных реакций подавления потребностей, воспринимаемых как опасные. Манифестные особенности восприятия окружающего и поведения у многих гипертоников представляет собой форму защиты от собственных агрессивных побуждений (Cottingtonetal., 1986; Diamond, 1982).
У большинства пациентов с эссенциальной гипертонией обычно нет должного осознания своей болезни. С психоаналитических позиций внешне неправильное невротическое поведение идеологически оправдывается стремлением к активности и помощи людям. Но и при этой неблагоприятной исходной ситуации в отдельных случаях можно добиться изменений, если благодаря дозреванию личности устраняется ее односторонняя направленность и человек в целом начинает ориентироваться в жизни по-новому.
Манифестные черты личности больного с артериальной гипертонией, его трудолюбие и упорядоченное поведение, контактность, аккуратность и добросовестность импонируют, делают его, казалось бы, приятным, уступчивым пациентом. Однако следует помнить, что гипертоник в большинстве случаев не вербализует свою агрессивность, честолюбие и стремление к соперничеству, которые часто остаются латентными. Это можно почувствовать, если пытаться оказывать длительное влияние на образ жизни больного. Его малая податливость при необходимой длительной терапевтической программе, в процессе которой пациент обычно не может реализовать свои потребности и даже не может выразить свои суждения и отношение, противоречащие терапевтической программе, часто осложняет отношения психотерапевта и больного. В трудовых и семейных кризисных ситуациях, и прежде всего при латентных конфликтах в отношениях с психотерапевтом, больные
легкоранимы, но не могут словесно выразить свою агрессивность. Они просто уходят от лечения, не появляются к назначенному сроку. Это, казалось бы, немотивированное прерывание лечения приводит к развитию у них чувства вины и его проекции. Для контрперенесения психотерапевта важно, чтобы он знал об оппозиционных тенденциях своего пациента и вызывал его на разговор, помогая ему справиться с чувством вины или с напряжением во время лечения. Благожелательное отношение, при котором терапевт и сам не чувствует себя ущемленным, и не делает ненужных упреков, определяет возможность продолжения терапии.
Для взаимоотношений психотерапевта и больного важно вовремя заметить, что пациент склонен подавлять собственные критические потребности и выявлять их лишь косвенно, например, в форме немотивированного прерывания лечения.
Психотерапия
Ситуация отношений психотерапевта и больного часто характеризуется конфликтом агрессивности/зависимости со стороны больного.
Условия для лечения гипертоника характеризуются:
• низкой мотивацией, поскольку жалобы поступают в основном на незначительные субъективные симптомы;
• хорошими возможностями лекарственной терапии;
• личностными факторами, характеризующимися конфликтом агрессивности/зависимости, что может приводить к напряжениям в отношениях психотерапевта и больного и выражаться в ненадежности взаимодействия.
Для поддерживающего лечения рекомендуется раннее вовлечение социального поля, недирективное отношение психотерапевта к больному, не активирующее конфликт агрессивности/зависимости, активное сообщение психотерапевтом информации, усиление собственной ответственности и самостоятельности, а также самовосприятия (например, за счет самостоятельного измерения давления).
Психотерапевтическое лечение представляется целесообразным и показанным лишь тогда, когда больной имеет соответствующее давление страдания. Релаксация и поведенческие методы хорошо зарекомендовали себя как средство под-
_______________________Сердечно-сосудистые заболевания
держки медикаментозной терапии, поскольку таким образом удается существенно снижать дозы лекарств.
В рамках программы поведенческой терапии следует добиваться собственной ответственности пациента при использовании метода биологической обратной связи и применении методик снятия напряжения. Пациенты должны понять, какие ситуации, трудности, конфликты приводят к повышению артериального давления, научиться контролировать свои успехи и неудачи. Необходимо уточнить, соответствуют ли эти успехи канонам классической рефлекторной теории и идет ли речь о прямом образовании условных связей, а не просто о научении больных общим успокаивающим приемам.
Могут успешно использоваться методы терапии, фокусированной на решении, символдрамы, арт-терапии, креативной визуализации, транзактного анализа, семейной психотерапии.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Для цитирования. Лещенко И.В., Эсаулова Н.А. Бронхиальная астма: современные вопросы базисной терапии (в помощь практическому врачу) // РМЖ. 2015. № 18. С. 1074–1079.
В настоящее время имеются многочисленные отечественные и зарубежные публикации, посвященные бронхиальной астме (БА), оценке тяжести заболевания и медикаментозной терапии.
БА можно успешно лечить, поэтому почти все больные могут:
– предотвратить беспокоящие симптомы заболевания;
– предотвратить серьезные обострения;
– использовать редко или совсем не использовать средства скорой медицинской помощи;
– вести полноценную, физически активную жизнь;
– иметь нормальную (или почти нормальную) функцию легких.
Основополагающими документами, в которых изложено, как проводить диагностику, лечение и профилактику заболевания, являются современные международные руководства и Федеральные клинические рекомендации по диагностике и лечению БА [1, 2]. В соответствии с рекомендациями Global Initiative for Asthma (GINA) [1], объем базисной терапии БА зависит прежде всего от уровня контроля заболевания. Критерии контроля БА довольно просты для понимания и врачом, и пациентом и включают:
– выраженность хронических симптомов, в т. ч. ночных минимальных (в идеале – симптомы отсутствуют);
– обострения минимальны (редки);
– потребность в неотложной помощи отсутствует;
– использование b2-агонистов короткого действия «по потребности» – минимальное (в идеале – отсутствует);
– ограничения активности, в т. ч. физической, нет.
Даже одного признака степени тяжести достаточно для того, чтобы отнести пациента с БА к группе с частичным контролем или его отсутствием (табл. 1).
Опрос с использованием балльной оценки симптомов по опросникам Asthma Control Test (ACT) и Asthma Control Questionnaire (ACQ) является более чувствительным при оценке изменения уровня контроля симптомов БА [3, 4]. Весьма полезным для практического врача является опросник по контролю симптомов БА и риска обострений (ACQ), который представлен в таблицах 2 и 3 [4].
Цели лечения БА заключаются в достижении контроля заболевания, предотвращении обострений и побочных эффектов действия лекарственной терапии, улучшении качества жизни.
Факторы риска (триггеры) обострений или приступов БА:
– аллергены;
– табачный дым;
– вирусные инфекции;
– поллютанты;
– пищевые добавки;
– профессиональные вредности;
– физическая нагрузка;
– смех;
– холодный воздух;
– лекарственные препараты.
К независимым от триггерных влияний факторам риска обострений БА относятся анамнестические данные о госпитализации в отделение реанимации и интенсивной терапии или интубация в связи с острой дыхательной недостаточностью на фоне обострения БА, а также одно или в более тяжелой форме обострение за 12 мес. [5, 6].
С целью предотвращения обострений БА особое внимание следует обратить на факторы риска, влияние которых можно уменьшить в результате врачебного вмешательства. К ним относят:
– неконтролируемые симптомы БА [7];
– прием более 200 доз (один ингалятор) короткодействующего бронходилататора (КДБД) в месяц, т. е. частое использование средств скорой помощи [8];
– применение неадекватных доз ингаляционных глюкокортикоидов (ИГК), например, в случае если пациенту они ранее не назначались или были рекомендованы в необоснованно низких дозах [9];
– недостаточный объем терапии ИГК из-за низкой приверженности к лечению [9];
– нарушение техники ингаляций [10];
– уменьшение объема форсированного выдоха в 1 с (ОФВ1), особенно до 60% от должных показателей [11];
– серьезные психологические или социально-экономические проблемы [11];
– воздействие внешних факторов (например, табачный дым [11]);
– контакт с аллергенами при наличии сенсибилизации [11];
– сопутствующие заболевания, такие как ожирение, риносинусит, подтвержденная непереносимость компонентов пищи;
– эозинофилия в крови или мокроте [9, 12];
– беременность [13].
При неправильном выборе терапии или недостаточной комплаентности больного возможно развитие побочных местных и системных эффектов от приема следующих препаратов [14], таких как:
– бронходилататоры, которые при бесконтрольном использовании могут вызывать тремор, тахикардию [15]. Их применение в превышенных дозах, особенно при гипоксемии, приводит к риску аритмических осложнений, нарушению обмена глюкозы, снижению уровня калия в сыворотке крови [15, 16], десенситизации b2–рецепторов, повышению риска внезапной смерти [1];
– ИГК, применение которых в высокой суточной дозе, а также неправильная техника ингаляций могут привести к локальным нежелательным явлениям (НЯ);
– системные глюкокортикоиды (СГК), которые при частом применении (один и более курсов в течение года) увеличивают риск формирования остеопороза [5], генерализации вирусных инфекций, асептического некроза головки бедренной кости, приводят к нарушению обмена глюкозы, повышают вероятность увеличения массы тела (ожирения) и образования пептических язв [5].
Назначение базисной терапии в соответствии с уровнем контроля БА способствует:
– уменьшению частоты обострений этого заболевания;
– минимизации побочных эффектов действия лекарств;
– сокращению потребности пациентов с БА в экстренной помощи;
– числа обращений к врачу и госпитализаций;
– прямых расходов на БА.
Выбор препаратов для базисной терапии БА осуществляется на основании доказательных данных об эффективности и безопасности препаратов, а также с учетом доступности и стоимости лечения. При недостаточном контроле БА необходимо выявить причины, из-за которых он отсутствует, и, при необходимости, изменить базисную терапию (ступень вверх) с учетом индивидуальных потребностей пациента.
Одной из важнейших задач, которая стоит перед врачом, является определение объема стартовой базисной терапии и объема лекарственной терапии у больных БА, получающих базисную терапию.
При назначении стартовой базисной терапии больным БА рекомендуется руководствоваться следующими принципами:
• Пациент не нуждается в базисной терапии, если он отмечает симптомы БА или потребность в КДБД реже 2 р./мес., у него отсутствуют факторы риска обострений заболевания или само обострение БА в течение последнего года (уровень доказательности D).
• Низкие дозы ИГК показаны пациентам с нечастыми симптомами БА (реже 2 р./мес.) при наличии одного или более факторов риска обострений БА (уровень доказательности D).
• Низкие дозы ИГК назначаются, если симптомы астмы или потребность в КДБД возникают реже 2 р./нед., но чаще 2 р./мес. или если пациент просыпается в ночные часы более 1 р./мес. из-за симптомов астмы (уровень доказательности B).
• Средние или высокие дозы ИГК либо комбинация низких доз ИГК с длительно действующими бронходилататорами (ДДБД) рекомендуются пациентам с симптомами астмы (которые беспокоят их большую часть недели) или с частыми пробуждениями ночью из-за астмы (1 и более р./нед.), особенно при наличии факторов риска обострений (уровень доказательности А).
Объем лекарственной терапии у больных БА, получающих базисную терапию, определяется в зависимости от уровня контроля заболевания. При этом следует руководствоваться следующими принципами:
• Ретроспективно (в течение последних 3–6 мес.) оценивается тяжесть БА в зависимости от объема базисной терапии, которая требуется для полного контроля заболевания и предотвращения его обострений [17–19]. Степень тяжести астмы не является постоянной характеристикой и может измениться через несколько месяцев или лет.
• Определяются показатели функции внешнего дыхания (ФВД), в частности, величина ОФВ1. Установлено, что показатели ФВД не имеют сильной корреляционной связи с симптомами БА у взрослых, они не всегда имеют решающее значение, однако низкая величина ОФВ1 является независимым предиктором риска обострений БА, даже при нечастых симптомах заболевания [20, 21].
Оценку эффективности базисной терапии и показатели ФВД, в частности уровень ОФВ1, целесообразно оценивать при определении объема стартовой терапии через 3–6 мес. после начала лечения пациента. При наличии полного контроля заболевания в это время необходимо сделать попытку уменьшить объем базисной терапии на одну ступень для определения минимально эффективного объема принимаемых лекарственных средств.
Безусловно, первоочередными препаратами для базисной терапии БА являются ИГК. При выборе ИГК важно учесть эффективность и безопасность препарата.
Пациенты с респираторной патологией относятся к группе повышенного риска развития активного туберкулеза, и данный риск увеличивается при использовании высоких доз ИГК. Несмотря на низкую системную биодоступность, ИГК все же обладают системными эффектами, и одним из них является повышенный риск развития сахарного диабета или его прогрессирования, особенно при использовании высоких доз ИГК [22]. Говоря о безопасности ИГК, необходимо подчеркнуть, что при анализе случаев глаукомы, требующей терапии, не было отмечено повышенного риска развития и прогрессирования данного заболевания на фоне терапии ИГК даже в случае длительного применения препаратов в высоких дозах [22]. При применении ИГК даже в высоких дозах во время беременности, по данным публикаций, не было продемонстрировано нарушения функции надпочечников у плода [23].
Заслуживают внимания предпочтения пациента в выборе лекарственного препарата для базисной терапии, который обладает максимальным эффектом. Поскольку в настоящее время существует множество ингаляционных устройств для базисной терапии, действенность лечения зависит от технических характеристик ингалятора и способности пациента правильно пользоваться ингаляционными устройствами. Кроме того, следует убедиться, что пациент ориентирован на регулярный прием базисных препаратов, особенно при недостаточном уровне контроля заболевания. Эквипотентные суточные дозы ИГК для взрослых и детей старше 12 лет приведены в таблице 4.
ИГК применяются в качестве монотерапии в низких дозах при лечении больных с легкой персистирующей астмой (2-я ступень) и в средних/высоких дозах при лечении больных со среднетяжелой БА (3-я ступень) [1, 2]. В таблице 5 представлена схема базисной терапии БА в соответствии с уровнями доказательств, отражающая ступенчатый подход [1].
В тех случаях, когда речь идет о монотерапии ИГК больных БА, одна из задач, стоящих перед лечащим врачом, заключается в выборе ИГК в качестве монотерапии или в сочетании ИГК с ДДБД.
Изучение эффективности и безопасности различных ИГК проведено в многочисленных клинических многоцентровых плацебо-контролируемых исследованиях на большой популяции больных БА легкой и средней тяжести.
Так, например, ретроспективная оценка эффективности предотвращения обострений, требующих госпитализации, у 1273 больных с персистирующей БА легкой степени показала достоверное преимущество мометазона фуроата (МФ) по сравнению с беклометазоном дипропионатом (БДП) (отношение шансов 0,51; р=0,0191) [24].
Сравнение эффективности и безопасности МФ дозированного порошкового ингалятора (МФ-ДПИ) и будесонида в 12-недельном многоцентровом слепом исследовании (57 клинических центров, 17 стран) с участием 730 больных со среднетяжелой БА показало [25]:
• МФ-ДПИ (200 мкг 2 р./сут и 400 мкг 2 р./сут) достоверно улучшал показатели ОФВ1 по сравнению с будесонидом (400 мкг 2 р./сут) начиная со 2-й нед. терапии.
• Различие в эффективности нарастало по мере продолжения лечения вплоть до 12-й нед., и в целом увеличение значений ОФВ1 со временем при приеме будесонида 400 мкг 2 р./сут было менее выражено, чем для всех режимов лечения МФ-ДПИ.
• Дополнительно терапия МФ-ДПИ (400 мкг/сут) приводила к достоверно более выраженному снижению ежедневной потребности в КДБА по сравнению с будесонидом.
• Отмечена хорошая переносимость терапии сравниваемыми препаратами; серьезных НЯ, связанных с лечением, не было ни в одной группе; влияния на уровень кортизола не наблюдалось; НЯ, такие как головная боль (4–8%), фарингит (4–5%), дисфония (2–5%), зарегистрированы с одинаковой частотой в обеих группах.
Авторы делают вывод о том, что МФ-ДПИ в средней суточной дозе 400 мкг/сут обеспечивает значимо большее улучшение показателей ФВД по сравнению с таковым при применении будесонида 800 мкг/сут у пациентов со среднетяжелой БА и хорошо переносится [25].
В метаанализе 6 рандомизированных контролируемых клинических исследований представлена сравнительная оценка эффективности и безопасности МФ и других ИГК в эквипотентных дозах при лечении 1354 пациентов со среднетяжелой/тяжелой БА, получавших прежде терапию каким-либо ИГК [26]. Продолжительность исследований составляла 4 нед. и более.
Результаты исследований показали превосходство МФ по сравнению с другими ИГК в отношении следующих показателей ФВД:
– ОФВ1;
– пиковая скорость выдоха;
– форсированная жизненная емкость легких;
– мгновенная объемная скорость выдоха на уровне 25–75%.
МФ оказался эффективнее других ИГК в отношении уменьшения потребления короткодействующих и b2-агонистов (КДБА) и утренних симптомов астмы. Частота НЯ, в т. ч. серьезных, была сопоставима во всех группах больных, в т. ч. лечившихся МФ.
Высокая эффективность МФ связана с его более высокой аффинностью к глюкокортикостероидному рецептору, чем у наиболее часто применяемых ИГК (рис. 1) [27, 28]. Кроме того, МФ характеризуется наименьшей системной биодоступностью среди сравниваемых ИГК, обеспечивая его высокую безопасность (рис. 2) [28].
Рекомендованные дозы МФ-ДПИ для лечения больных БА взрослых и подростков от 12 лет и старше представлены в таблице 6 [29].
Конечно, основная роль в базисной терапии в достижении контролируемого течения БА принадлежит комбинированной терапии ИГК и длительно действующим b2-агонистам (ДДБА). Комбинированные препараты назначаются больным БА в соответствии с необходимой суточной дозой ИГК для достижения контролируемого течения этой болезни. В таблице 7 даны схемы лечения ингаляционными комбинированными лекарственными средствами, назначаемыми в качестве базисной терапии больным БА средней и тяжелой степени в зависимости от необходимой суточной дозы ИГК для достижения контролируемого течения БА. Все препараты, названные в таблице 7, зарегистрированы в РФ.
Представленные в таблице 7 схемы лечения ИГК и ДДБА дают возможность лечащему врачу назначить различные комбинированные препараты в соответствии с эквипотентной дозой ИГК и в зависимости от уровня контроля астмы, т. е. выраженности симптомов БА и частоты обострений.
Одной из задач, стоящих перед практикующим врачом, является выбор ингаляционного комбинированного лекарственного препарата для базисной терапии. Одним из них является МФ/формотерола фумарат (МФ/Ф). Рекомендуемые дозы МФ/Ф приведены в таблице 8.
В ряде публикаций, в т. ч. в отечественной литературе, ранее представлены материалы, посвященные фармакологическим свойствам МФ/Ф, входящим в состав комбинированного препарата МФ и Ф, сравнительным клиническим исследованиям, в которых изучались эффективность МФ/Ф в отношении уменьшения частоты тяжелых обострений, увеличения ОФВ1 и безопасность по сравнению с монотерапией составляющих его лекарственных средств и плацебо [30, 31]. Сравнение показателей ФВД в рандомизированном многоцентровом исследовании в параллельных группах у больных БА при назначении МФ/Ф 100 мкг / 5 мкг – 2 дозы 2 р./сут (n=141) и 250 мкг / 25 мкг флутиказона/салметерола (ФЛ/САЛ) – 1 доза 2 р./сут (n=68) показало более быстрое начало действия (через 5 мин) при применении МФ/Ф по сравнению с ФЛ/САЛ, выражающееся в приросте ОФВ1 (8,5% против 4,3% соответственно, р
источник