
Основной принцип данного функционального исследования заключается в проведении измерениz скорости прохождения воздуха через дыхательные пути во время вдоха и выдоха. Измерение выполняется при помощи пневмотахометра, имеющего специальную трубку с одноразовым сменным мундштуком, через которую делается максимальный вдох или выдох несколько раз.
Основным медицинским показанием к проведению пневмотахометрии является оценка функционального состояния, а именно проходимости, дыхательных путей. Данное исследование позволяет диагностировать патологию, сопровождающуюся ухудшением прохождения воздуха через бронхи различного калибра, к ней относится:
- Бронхиальная астма – специфическое воспалительное поражение бронхов, которое имеет аллергическое происхождение. Она сопровождается периодическим развитием приступов одышки, кашля с отхождением вязкой мокроты. Механизм развития патологического процесса связан с сужением просвета бронхов (бронхоспазм), вызванным повышением тонуса гладких мышц их стенок на фоне развития аллергической реакции, которую провоцирует контакт организма с аллергеном (чужеродные соединения, чаще белковой природы).
- Атопический бронхит – также аллергическое поражение легких, сопровождающееся более легким течением с развитием бронхоспазма и воспалительного процесса в бронхах различного калибра.
- Хроническая обструктивная патология легких – длительное воспаление бронхиального дерева, которое может быть вызвано различными провоцирующими факторами (инфекции, систематическое вдыхание пыли или паров различных химических соединений, курение) и сопровождается ухудшением проходимости бронхов.
- Пневмосклероз – тяжелое поражение легких, характеризующееся замещением легочной ткани соединительной тканью, она сдавливает бронхи, из-за чего сужается их просвет. Данное патологическое состояние является следствием длительного течения различной патологии органов системы дыхания, а также поступления пыли.
Проведение пневмотахометрии при данных заболеваниях дает возможность врачу оценить функциональное состояние структур дыхательной системы и подобрать наиболее оптимальную терапию.
Выделяют несколько патологических и физиологических состояний организма пациента, при которых проведение 
- Перенесенный в недавнем времени (не менее 3-х месяцев назад) геморрагический или ишемический инсульт головного мозга.
- Артериальная гипертония (повышенный уровень системного артериального давления), которая часто сопровождает гипертоническую болезнь.
- Перенесенный инфаркт (гибель участка сердечной мышцы) миокарда.
- Аневризма артерий головного мозга, а также грудного отдела аорты.
- Острый инфекционный процесс в органах системы дыхания.
- Дыхательная недостаточность, сопровождающаяся выраженным снижением функциональной активности.
- Эпилепсия (патологическое развитие приступов судорог).
- Беременность на любом сроке течения.
Перед назначением проведения пневмотахометрии врач обязательно убеждается в отсутствии противопоказаний у пациента.
Пневмотахометрия проводится в условиях процедурного кабинета медицинского учреждения. Пациент располагается на кушетке. Врач дает ему трубку пневмотахографа с одетым на нее стерильным мундштуком, на нос одевается специальный зажим. После этого он делает в трубку несколько спокойных вдохов и выдохов, затем максимально вдыхает и выдыхает воздух несколько раз (обычно 2 раза), а врач в это времени фиксирует показания пневмотахографа.
Для получения максимально достоверных результатов пневмотахометрии пациент перед его проведением должен соблюдать несколько несложных подготовительных рекомендаций, которые включают:
- Отказ от курения и употребления алкоголя за сутки до исследования.
- Отмена применения некоторых лекарственных средств, в частности фармакологической группы бронхолитики (препараты, улучшающие проходимость дыхательных путей) за 4 часа.
- Одежда не должна стеснять дыхательных движений.
- Не рекомендуется в день проведения пневмотахометрии подвергаться повышенным эмоциональным или физическим нагрузкам.
- Исследование должно проводиться натощак или не ранее, чем за 2 часа после еды. Обычно оно проводится утром, пациент при этом не завтракает.
Более подробные рекомендации врач дает во время приема. Также обязательно проводится измерение антропометрических показателей (рост, масса тела, объем грудной клетки), которые позволят специалисту правильно определить состояние структур системы дыхания.
На основании измерения скорости прохождения воздуха во время интенсивного вдоха и выдоха врач формирует несколько показателей функционального состояния органов системы дыхания, к которым относятся:
- Индекс Тиффно – рассчитывается на основании скорости прохождения воздуха во время выдоха, в норме
составляет 70%.
- Пиковая скорость – нормальный показатель составляет 0,5-1,5 л/сек.
- Максимальная скорость воздуха во время вдоха и выдоха – не должна быть меньше 70% от показателя жизненного объема легких (вычисляется во время проведения спирографии).
- Скорость выдоха – нормальный показатель колеблется от 4 до 8 л/сек и зависит от пола и возраста пациента.
При нарушении проходимости дыхательных путей все показатели снижаются, причем их уменьшение имеет прямую зависимость от выраженности ухудшения прохождения воздуха в бронхах.
Для более точного выяснения степени и характера функциональных нарушений в легочной системе врач обязательно назначает и другие методы функциональной диагностики.
источник
При подозрении на некоторые заболевания пациентам предлагают пройти определенную медицинскую процедуру. Пневмотахометрия — это исследование проходимости дыхательных путей и бронхов, подразумевающее определение скорости воздушного потока при вдохе и выдохе.
Исследование методом пневмотахометрии позволяет на ранней стадии выявить нарушенную проходимость в бронхах — как мелких, так и крупных, а также диагностировать бронхиальную астму. Сама процедура напоминает спирограмму выдоха.
Для исследования применяют специальный прибор, называемый пневмотахометром или спирометром. Пациенту предстоит сделать через него с максимальным усилием два вдоха и выдоха. Результат позволяет установить максимальную скорость движения воздуха, а также проходимость бронхов.
При вынесении заключения врач ориентируется на следующие показатели:
- Индекс Тиффно — тест, позволяющий выявить нарушение проходимости. Оптимальный показатель должен составлять как минимум 70%.
- Жизненная емкость легких — объем воздуха, который попадает в легкие при максимальном вдохе и выходит из них при максимальном выдохе. Его получают, суммируя резервный объем вдоха и выдоха и дыхательный объем. В норме ЖЕЛ составляет около 3700 мл.
- Пиковая скорость выдоха, норма — 0,5-1,5 л/с.
- Средняя скорость выдоха в интервале 25-70% от жизненной емкости легких.
- Максимальная скорость воздуха (МОС — 25, 50, 70% жизненной емкости легких).
Все показатели анализируются с учетом индивидуальных особенностей пациента: его возраст, рост и физическая подготовка. Полученные результаты имеют большое значение для диагностики обструкции дыхательных путей.
Процедура получения данных проходит следующим образом:
- Пациент удобно усаживается в кресле, руки складывает на подлокотники.
- Подготавливается к исследованию прибор, на него надевают мундштук. Нос пациента закрывают носовым зажимом.
- После этого пациент должен сделать несколько спокойных вдохов и выдохов, подготовиться к исследованию. Затем он делает форсированный вдох и такой же выдох, без задержки дыхания.
- Затем форсированные вдохи и выдохи повторяются несколько раз.
- Врач анализирует скорость форсированного выдоха по шкале, которая соответствует диаметру пневмотахометра.
Нормальные показатели скорости выдоха составляют 5-8 л/с у мужчин, у женщин — от 4 до 6 л/с. Для детей старше 7 лет разработаны особые показатели, в зависимости от возраста ребенка. У детей от 7 до 9 лет нормальный показатель скорости движения воздуха при форсированном выдохе составляет 3,3 л/с у мальчиков, и 3,1 л/с у девочек. У детей 10-12 лет показатель возрастает до 3,7 и 3,8 л/с соответственно, 13-14 лет — 4,3 и 4,8 л/с соответственно.
После определения скорости выдоха по формуле Бадаляна вычисляется должная объемная скорость выдоха. Для этого фактическая емкость легких умножают на 1,2%. Если полученный результат будет составлять менее 85%, врач дает заключение о нарушении проходимости.
Возникновение и развитие хронических нарушений выражается снижением показателя скорости. В первую очередь начинают сужаться дистальные, то есть мелкие, бронхи, что проявляется как снижение максимальной объемной скорости воздуха в интервале 50, 75 и 25-75.
При бронхиальной обструкции снижается жизненная емкость легких.
Показанием к назначению пневмотахометрии считаются любые заболевания дыхательной системы. Процедура необходима для определения патологий, которые сопровождаются появлением некоторых симптомов: одышкаи или долгого кашля.
Тахометрия нужна для контроля пациентов с хронической обструктивной болезнью легких (ХОБЛ) или бронхиальной астмой, особенно в период лечения. Пневмотахометрия — необходимое исследование при определении трудоспособности человека и при подготовке к хирургической операции.
Противопоказаниями к назначению процедуры считают:
- беременность;
- эпилепсию;
- перенесенный менее чем за три месяца до исследования инсульт (геморрагический, ишемический);
- перенесенные менее чем за две недели до тахометрии инфекции дыхательных путей;
- тяжелые нарушения работы дыхательных путей;
- если незадолго до даты процедуры больной перенес инфаркт миокарда;
- гипертонический криз;
- аневризма артерий.
Во время пневмотахометрии может появляться дискомфорт. Если процедура вызывает кашель, ее на некоторое время прерывают и повторяют через несколько минут. Боль в груди, отхаркивание крови служат сигналами к немедленному прекращению тахометрии.
Минимум за сутки до проведения процедуры больному предстоит отказаться от курения и спиртных напитков, так как они могут негативно повлиять на конечный результат. Если пациенту прописан прием бронхолитиков короткого действия, это нужно сообщить врачу. По согласованию с ним за 4 часа до пневмотахометрии прием этих лекарств может быть отменен. Если пациент вынужден периодически пользоваться ингалятором, его можно взять с собой.
За несколько часов до процедуры рекомендуют успокоиться и побыть немного в спокойной атмосфере. Интенсивные физические упражнения, нагрузки, даже ходьба быстрым шагом могут «сбить» дыхание, что приведет к получению неточных результатов.
Запрещается приходить на процедуру в тесной или некомфортной одежде, так как она будет ограничивать движения грудной клетки.
Как минимум за 2 часа до пневмотахометрии рекомендуется прекратить прием пищи, лучше проходить исследование натощак. С собой пациенту необходимо иметь тканевый или бумажный платочек.
Пневмотахометрия не имеет каких-либо ограничений, ее можно проводить и у детей, и у взрослых. Но чтобы получить точные результаты, важно сообщить основные показатели: вес, рост и возраст. Согласно этим данным, врач подберет показатели нормы и по отклонениям от них выявит нарушения.
источник
Спирография — метод графической регистрации изменений легочных объемов при выполнении естественных дыхательных движений и волевых форсированных дыхательных маневров. Спирография позволяет получить ряд показателей, которые описывают вентиляцию легких. В первую очередь, это статические объемы и емкости, которые характеризуют упругие свойства легких и грудной стенки, а также динамические показатели, которые определяют количество воздуха, вентилируемого через дыхательные пути во время вдоха и выдоха за единицу времени. Показатели определяют в режиме спокойного дыхания, а некоторые — при проведении форсированных дыхательных маневров.
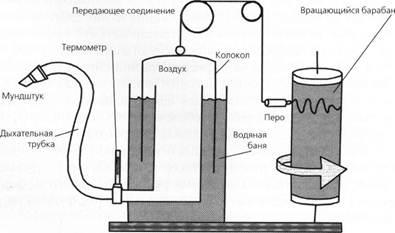
В техническом выполнении все спирографы делятся на приборы открытого и закрытого типа .В аппаратах открытого типа больной через клапанную коробку вдыхает атмосферный воздух, а выдыхаемый воздух поступает в мешок Дугласа или в спирометр Тисо (емкостью 100—200 л), иногда — к газовому счетчику, который непрерывно определяет его объем. Собранный таким образом воздух анализируют: в нем определяют величины поглощения кислорода и выделения углекислого газа за единицу времени. В аппаратах закрытого типа используется воздух колокола аппарата, циркулирующий в закрытом контуре без сообщения с атмосферой. Выдыхаемый углекислый газ поглощается специальным поглотителем.
Показания к проведению спирографии следующие:
1.Определение типа и степени легочной недостаточности.
2.Мониторинг показателей легочной вентиляции в цельях определения степени и быстроты прогрессирования заболевания.
3.Оценка эффективности курсового лечения заболеваний с бронхиальной обструкцией бронходилататорами β2-агонистами короткого и пролонгированного действия, холинолитиками), ингаляционными ГКС и мембраностабилизирующими препаратами.
4.Проведение дифференциальной диагностики между легочной и сердечной недостаточностью в комплексе с другими методами исследования.
5.Выявление начальных признаков вентиляционной недостаточности у лиц, подверженных риску легочных заболеваний, или у лиц, работающих в условиях влияния вредных производственных факторов.
6.Экспертиза работоспособности и военная экспертиза на основе оценки функции легочной вентиляции в комплексе с клиническими показателями.
7.Проведение бронходилатационных тестов в целях выявления обратимости бронхиальной обструкции, а также провокационных ингаляционных тестов для выявления гиперреактивности бронхов.
Несмотря на широкое клиническое применение, спирография противопоказана при следующих заболеваниях и патологических состояниях:
тяжелое общее состояние больного, не дающее возможности провести исследование;
прогрессирующая стенокардия, инфаркт миокарда, острое нарушение мозгового кровообращения;
злокачественная артериальная гипертензия, гипертонический криз;
токсикозы беременности, вторая половина беременности;
недостаточность кровообращения III стадии;
тяжелая легочная недостаточность, не позволяющая провести дыхательные маневры.
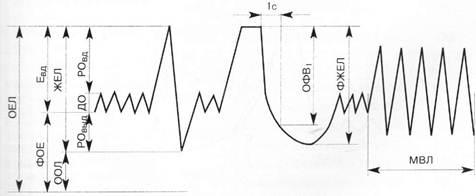
Техника проведения спирографии. Исследование проводят утром натощак. Перед исследованием пациенту рекомендуется находиться в спокойном состоянии на протяжении 30 мин, а также прекратить прием бронхолитиков не позже чем за 12 часов до начала исследования. Спирографическая кривая и показатели легочной вентиляции приведены на рис. 2. Статические показатели определяют во время спокойного дыхания. Измеряют дыхательный объем (ДО) — средний объем воздуха, который больной вдыхает и выдыхает во время обычного дыхания в состоянии покоя. В норме он составляет 500—800 мл. Часть ДО, которая принимает участие в газообмене, называется альвеолярным объемом (АО) и в среднем равняется 2/3 величины ДО. Остаток (1/3 величины ДО) составляет объем функционального мертвого пространства (ФМП). После спокойного выдоха пациент максимально глубоко выдыхает — измеряется резервный объем выдоха (РОВыд), который в норме составляет IООО—1500 мл. После спокойного вдоха делается максимально глубокий вдох — измеряется резервный объем вдоха (РОвд). При анализе статических показателей рассчитывается емкость вдоха (Евд) — сумма ДО и РОвд, которая характеризует способность легочной ткани к растяжению, а также жизненная емкость легких (ЖЕЛ) — максимальный объем, который можно вдохнуть после максимально глубокого выдоха (сумма ДО, РОВД и РОвыд в норме составляет от 3000 до 5000 мл). После обычного спокойного дыхания проводится дыхательный маневр: делается максимально глубокий вдох, а затем — максимально глубокий, самый резкий и длительный (не менее 6 с) выдох. Так определяется форсированная жизненная емкость легких (ФЖЕЛ) — объем воздуха, который можно выдохнуть при форсированном выдохе после максимального вдоха (в норме составляет 70—80 % ЖЕЛ). Как заключительный этап исследования проводится запись максимальной вентиляции легких (МВЛ) — максимального объема воздуха, который может быть провентилирован легкими за I мин. МВЛ характеризует функциональную способность аппарата внешнего дыхания и в норме составляет 50—180 л. Снижение МВЛ наблюдается при уменьшении легочных объемов вследствие рестриктивных (ограничительных) и обструктивных нарушений легочной вентиляции.
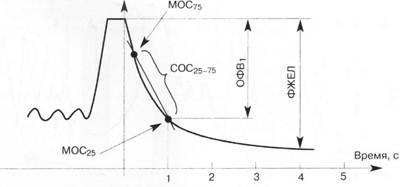
При анализе спирографической кривой, полученной в маневре с форсированным выдохом, измеряют определенные скоростные показатели (рис. 3): 1) объем форсированного выдоха за первую секунду (ОФВ1) — объем воздуха, который выдыхается за первую секунду при максимально быстром выдохе; он измеряется в мл и высчитывается в процентах к ФЖЕЛ; здоровые люди за первую секунду выдыхают не менее 70 % ФЖЕЛ; 2) проба или индекс Тиффно — соотношение ОФВ1 (мл)/ЖЕЛ (мл), умноженное на 100 %; в норме составляет не менее 70—75 %; 3) максимальная объемная скорость воздуха на уровне выдоха 75 % ФЖЕЛ (МОС75), оставшейся в легких; 4) максимальная объемная скорость воздуха на уровне выдоха 50 % ФЖЕЛ (МОС50), оставшейся в легких; 5) максимальная объемная скорость воздуха на уровне выдоха 25 % ФЖЕЛ (МОС25), оставшейся в легких; 6) средняя объемная скорость форсированного выдоха, вычисленная в интервале измерения от 25 до 75 % ФЖЕЛ (СОС25-75).
Вычисление скоростных показателей имеет большое значение в выявлении признаков бронхиальной обструкции. Уменьшение индекса Тиффно и ОФВ1 является характерным признаком заболеваний, которые сопровождаются снижением бронхиальной проходимости — бронхиальной астмы, хронического обструктивного заболевания легких, бронхоэктатической болезни и пр. Показатели МОС имеют наибольшую ценность в диагностике начальных проявлений бронхиальной обструкции. СОС25-75 отображает состояние проходимости мелких бронхов и бронхиол. Последний показатель является более информативным, чем ОФВ1, для выявления ранних обструктивных нарушений.
Все показатели легочной вентиляции изменчивы. Они зависят от пола, возраста, веса, роста, положения тела, состояния нервной системы больного и прочих факторов. Поэтому для правильной оценки функционального состояния легочной вентиляции абсолютное значение того или иного показателя является недостаточным. Необходимо сопоставлять полученные абсолютные показатели с соответствующими величинами у здорового человека того же возраста, роста, веса и пола — так называемыми должными показателями. Такое сопоставление выражается в процентах по отношению к должному показателю. Патологическими считаются отклонения, превышающие 15—20 % от величины должного показателя.
СПИРОГРАФИЯ С РЕГИСТРАЦИЕЙ ПЕТЛИ «ПОТОК-ОБЪЁМ»
Спирография с регистрацией петли «поток-объем» — современный метод исследования легочной вентиляции, который заключается в определении объемной скорости движения потока воздуха вдыхательных путях и его графическом отображением в виде петли «поток—объем» при спокойном дыхании пациента и при выполнении им определенных дыхательных маневров. За рубежом этот метод называют спирометрией. Целью исследования является диагностика вида и степени нарушений легочной вентиляции на основании анализа количественных и качественных изменений спирографических показателей.
Показания и противопоказания к применению сприрометрии аналогичны таковым для классической спирографии.
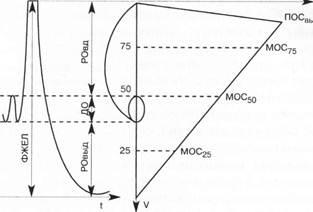
Методика проведения. Исследование проводят в первой половине дня, независимо от приема еды. Пациенту предлагают закрыть оба носовых хода специальным зажимом, взять индивидуальную простерилизованную насадку-мундштук в рот и плотно обхватить ее губами. Пациент в положении сидя дышит через трубку по открытому контуру, практически не испытывая сопротивления дыханию Процедура выполнения дыхательных маневров с регистрацией кривой «поток—объем» форсированного дыхания идентична той, которая выполняется при записи ФЖЕЛ во время проведения классической спирографии. Больному надлежит объяснить, что в пробе с форсированным дыханием выдохнуть в прибор следует так, будто нужно погасить свечи на праздничном торте. После некоторого периода спокойного дыхания пациент делает максимально глубокий вдох, в результате чего регистрируется кривая эллиптической формы (кривая АЕВ). Затем больной делает максимально быстрый и интенсивный форсированный выдох. При этом регистрируется кривая характерной формы, которая у здоровых людей напоминает треугольник (рис. 4).
Рис. 4. Нормальная петля (кривая) соотношения объемной скорости потока и объема воздуха при проведении дыхательных маневров. Вдох начинается в точке А, выдох — в точке В. ПОСвыд регистрируется в точке С. Максимальный экспираторный поток в середине ФЖЕЛ соответствует точке D, максимальный инспираторный поток — точке Е
Максимальная экспираторная объемная скорость потока воздуха отображается начальной частью кривой (точка С, где регистрируется пиковая объемная скорость выдоха — ПОСВЫД)- После этого объемная скорость потока уменьшается (точка D, где регистрируется МОС50), и кривая возвращается к изначальной позиции (точка А). При этом кривая «поток—объем» описывает соотношение между объемной скоростью воздушного потока и легочным объемом (емкостью легких) во время дыхательных движений. Данные скоростей и объемов потока воздуха обрабатываются персональным компьютером благодаря адаптированному программному обеспечению. Кривая «поток—объем» при этом отображается на экране монитора и может быть распечатана на бумаге, сохранена на магнитном носителе или в памяти персонального компьютера. Современные аппараты работают со спирографическими датчиками в открытой системе с последующей интеграцией сигнала потока воздуха для получения синхронных значений объемов легких. Рассчитанные компьютером результаты исследования печатаются вместе с кривой «поток—объем» на бумаге в абсолютных значениях и в процентах к должным величинам. При этом на оси абсцисс откладывается ФЖЕЛ (объем воздуха), а на оси ординат — поток воздуха, измеряемый в литрах в секунду (л/с)

Петля «поток—объем» представляет собой первую производную классической спирограммы. Хотя кривая «поток—объем» содержит в основном ту же информацию, что и классическая спирограмма, наглядность соотношения между потоком и объемом позволяет более глубоко проникнуть в функциональные характеристики как верхних, так и нижних дыхательных путей (рис. 6). Расчет по классической спирограмме высокоинформативных показателей МОС25, МОС50, МОС75 имеет ряд технических трудностей при выполнении графических изображений. Поэтому его результаты не обладают высокой точностью В связи с этим лучше определять указанные показатели по кривой «поток—объем». Оценка изменений скоростных спирографических показателей осуществляется по степени их отклонения от должной величины. Как правило, за нижнюю границу нормы принимается значение показателя потока, что составляет 60 % от должного уровня
Пневмотахометрия – это метод скоростей воздушного потока при форсированном вдохе и выдохе.
Пневмотахометрия является важным методом при определении состояния бронхиальной проходимости. У здоровых лиц показатель тахометрии колеблется от 4 до 8 л/с. Должная величина определяется по формуле ЖЕЛ X 1,2. Снижение этого показателя ниже 85 % считается нарушением бронхиальной проходимости.
Для того чтобы выявить скрытые бронхоспазмы, необходимо вычислить отношение пневмотахометрии на вдохе и выдохе. Если показатель ниже 0,9 — то это ранний признак бронхоспастического состояния. Нормальная проходимость бронхов у мужчин мощность выдоха и вдоха составляет — 3,5–5,5 л/с, у женщин — 3–3,8 л/с.
Как правило, фактический пневмотахометрический показатель по себе не характеризует состояния бронхиальной проходимости, его необходимо сопоставлять с должными величинами.
Наиболее эффективным является применение пневмотахографии в целях определения клапанного механизма нарушений бронхиальной проходимости, так как позволяет регистрировать скорость воздушного потока более длительно, чем при пневмотахометрии.
Пневмотахография (греч. pneuma воздух + tachos скорость + graphō писать, изображать) — непрерывная регистрация объемной скорости потока вдыхаемого и выдыхаемого воздуха при спокойном и форсированном дыхании. Самостоятельно применяется редко, чаще в сочетании с определением объема вдоха и выдоха (кривые «поток — объем»), альвеолярного и транспульмонального давления. Наиболее часто в клинической практике используется регистрация кривой «поток — объем форсированного выдоха», документирующей скорость воздушного потока на различных этапах форсированного выдоха. При правильном выполнении обследуемым форсированного выдоха кривая «поток — объем» позволяет объективно оценить состояние бронхиальной проходимости, диагностировать бронхиальную обструкцию, в т.ч. ее начальные проявления, что дает возможность выявить бронхолегочные заболевания на доклинической стадии развития Существенную роль кривая «поток — объем форсированного выдоха» играет в распознавании бронхоспазма при проведении фармакологических проб с бронхолитиками, изучении реактивности бронхов методами специфической и неспецифической бронхопровокации, оценке функциональной эффективности лечения бронхолегочной патологии в стационаре и амбулаторных условиях, определении выраженности и уровня бронхиальной обструкции. Особенно велико значение кривой «поток — объем форсированного выдоха» в изучении неблагоприятного влияния курения, загрязнения окружающей среды и профессиональных вредностей на функцию легких.
источник
Пневмотахометрия – метод измерения максимальной скорости потока воздуха, которая достигается при форсированном вдохе и выдохе.
В практической медицине большее значение имеет оценка параметров форсированного выдоха, они являются высокоинформативными для дифференциальной диагностики различных видов обструкции бронхов.
Диагностика заболеваний дыхательной системы при наличии характерных признаков – длительного кашля, одышки.
Наблюдение пациентов с заболеваниями дыхательной системы в динамике.
Подготовка пациентов с заболеваниями бронхолёгочной системы к оперативному вмешательству.
Контроль проводимого лечения у пациентов с бронхиальной астмой, хронической обструктивной болезнью лёгких.
Экспертная оценка функции внешнего дыхания при определении трудоспособности пациента.
Обструкция дыхательных путей тяжёлой степени (ОФВ1 менее1,2 л у взрослых).
Инфаркт миокарда, перенесённый менее 3 месяцев назад.
Инсульт ишемический или геморрагический, перенесённый менее 3 месяцев назад.
Аневризма аорты или артерий.
Состояние после перенесённой менее 2 недель назад инфекции верхних дыхательных путей.
Исследование проводят натощак либо спустя 2 часа после еды.
Пациента просят не курить за 24 часа до спирографии, не употреблять алкоголь.
За 30 минут до исследования необходимо исключить активные физические упражнения, посидеть в спокойной обстановке.
Одежда на обследуемом должна быть комфортной и свободной, чтобы не стеснять движений грудной клетки.
Отменить бронхолитики короткого действия за 4 часа до исследования после согласования с лечащим врачом.
Если пациент пользуется ингалятором, следует взять его с собой.
Иметь при себе носовой платок.
Пациент сидит прямо в кресле, руки расположены на подлокотниках. Исследование выполняется с помощью спирометра, который предназначен как для выполнения спирографии, так и пневмотахометрии. На спирометр надевают одноразовый мундштук для каждого пациента, а на нос пациента — носовой зажим.
После нескольких спокойных дыхательных циклов (вдох-выдох) пациент выполняет форсированный вдох и сразу же, не задерживая дыхание, форсированный выдох.
При возникновении кашля исследование приостанавливают и продолжают через несколько минут.
Появление кровохарканья или боли в грудной клетке требует прекращения пневмотахометрии.
Процедуру повторяют несколько раз для получения нескольких результатов. Затем врач оценивает графическое изображение, полученные показатели и формулирует заключение.
При пневмотахометрии оцениваются следующие параметры.
Форсированная жизненная ёмкость лёгких (ФЖЕЛ): 70 – 80%.
Объём форсированного выдоха за первую секунду (ОФВ1): не менее 70 % ФЖЕЛ.
Индекс Тиффно: не менее 70—75 %.
Максимальная объемная скорость воздуха на уровне выдоха 25% ФЖЕЛ (МОС25): не менее 60%.
Максимальная объемная скорость воздуха на уровне выдоха 50% ФЖЕЛ (МОС50): не менее 60%.
Максимальная объемная скорость воздуха на уровне выдоха 75% ФЖЕЛ (МОС75): не менее 60%.
Средняя объемная скорость форсированного выдоха, вычисленная в интервале измерения от 25 до 75 % ФЖЕЛ (СОС25-75).
ПОСвыд – пиковая объёмная скорость форсированного выдоха: 0,5 – 15 л/с.
При возникновении и прогрессировании хронической обструктивной болезни лёгких происходит постепенное снижение объёмно-скоростных показателей. Сначала поражаются мелкие бронхи (дистальные), что проявляется снижением МОС50, МОС75 и СОС25-75.
Снижение показателя МОС25 указывает на прогрессирование обструкции и поражение проксимальных отделов дыхательных путей.
Прогрессирующая обструкция бронхов проявляется снижением ОФВ1 и ФЖЕЛ.
При выраженной бронхиальной обструкции снижается и ЖЕЛ.
Выберите беспокоящие вас симптомы, ответьте на вопросы. Выясните, насколько серьезна ваша проблема и нужно ли обращаться к врачу.
Перед использованием информации, предоставляемой сайтом medportal.org, пожалуйста, ознакомьтесь с условиями пользовательского соглашения.
Сайт medportal.org предоставляет услуги на условиях, описанных в настоящем документе. Начиная пользоваться веб-сайтом Вы подтверждаете, что ознакомились с условиями настоящего Пользовательского соглашения до начала пользования сайтом, и принимаете все условия данного Соглашения в полном объеме. Пожалуйста, не пользуйтесь веб-сайтом, если Вы не согласны с данными условиями.
Описание услуги
Вся информация, размещённая на сайте, носит справочный характер, информация взята из открытых источников является справочной и не является рекламой. Сайт medportal.org предоставляет услуги, позволяющие Пользователю производить поиск лекарственных средств в данных, полученных от аптек в рамках соглашения между аптеками и сайтом medportal.org. Для удобства пользования сайтом данные по лекарственным средствам, БАД систематизируются и приводятся к единому написанию.
Сайт medportal.org предоставляет услуги, позволяющие Пользователю производить поиск клиник и другой информации медицинского характера.
Ограничение ответственности
Размещенная в результатах поиска информация не является публичной офертой. Администрация сайта medportal.org не гарантирует точность, полноту и (или) актуальность отображаемых данных. Администрация сайта medportal.org не несет ответственности за вред или ущерб, который Вы могли понести от доступа или невозможности доступа к сайту или от использования или невозможности использования данного сайта.
Принимая условия настоящего соглашения, Вы полностью понимаете и соглашаетесь с тем, что:
Информация на сайте носит справочный характер.
Администрация сайта medportal.org не гарантирует отсутствия ошибок и расхождений относительно заявленного на сайте и фактического наличия товара и цен на товар в аптеке.
Пользователь обязуется уточнить интересующую его информацию телефонным звонком в аптеку или использовать предоставленную информацию по своему усмотрению.
Администрация сайта medportal.org не гарантирует отсутствия ошибок и расхождений относительно графика работы клиник, их контактных данных – номеров телефонов и адресов.
Ни Администрация сайта medportal.org, ни какая-либо другая сторона, вовлеченная в процесс предоставления информации, не несет ответственности за вред или ущерб, который Вы могли понести от того, что полностью положились на информацию, изложенную на этом веб-сайте.
Администрация сайта medportal.org предпринимает и обязуется предпринимать в дальнейшем все усилия для минимизации расхождений и ошибок в предоставленной информации.
Администрация сайта medportal.org не гарантирует отсутствия технических сбоев, в том числе в отношении работы программного обеспечения. Администрация сайта medportal.org обязуется в максимально короткие сроки предпринять все усилия для устранения каких-либо сбоев и ошибок в случае их возникновения.
Пользователь предупрежден о том, что Администрация сайта medportal.org не несет ответственности за посещение и использование им внешних ресурсов, ссылки на которые могут содержаться на сайте, не предоставляет одобрения их содержимого и не несет ответственности за их доступность.
Администрация сайта medportal.org оставляет за собой право приостановить действие сайта, частично или полностью изменить его содержание, внести изменения в Пользовательское соглашение. Подобные изменения осуществляются только на усмотрение Администрации без предварительного уведомления Пользователя.
Вы подтверждаете, что ознакомились с условиями настоящего Пользовательского соглашения , и принимаете все условия данного Соглашения в полном объеме.
Рекламная информация, на размещение которой на сайте имеется соответствующее соглашение с рекламодателем, имеет пометку «на правах рекламы».
источник

Для проведения исследования требуется пневмотахограф или спирограф. Самый простой из них состоит из аппарата-преобразователя параметров вдоха-выдоха и графического регистратора. Принцип метода заключается в графической фиксации показателей давления, которые оказывают потоки воздуха на бронхолегочные структуры в зависимости от фазы дыхания.
Первым показателем, который определяется с помощью пневмотахографии, является максимальная скорость движения воздуха (МОС). В норме у среднестатистического взрослого здорового мужчины он колеблется от 5 до 8 л/сек, а у женщины — от 4 до 6 л/сек.
Чтобы учесть индивидуальные особенности пациента, при проведении процедуры высчитывают его личную МОС по формуле — ФЖЕЛ×1,25, где ФЖЕЛ — это форсированная жизненная емкость легких.
Полученный показатель МОС сравнивают с фактической скоростью движения воздуха, которая определена с помощью пневмотахографа. В норме фактическая МОС должна быть равна расчетной (с отклонением в 10-15%).
Метод позволяет оценить сопротивление воздушных путей потоку воздуха. Для оценки сопротивления бронхов используют методику прерывания потока воздуха. Эта методика основана на периодическом перекрытии трубки аппарата специальной заслонкой в то время, когда больной в нее дышит.
В моменты перекрытия потока воздуха давление в альвеолах легких и дыхательной трубке аппарата на короткое время выравнивается. На пневмотахограмме регистрируются выбросы, которые соответствуют альвеолярному дыханию.
На основании данных пневмотахограммы рассчитывают альвеолярное сопротивление по формуле: R = (PA – P1) / V, где R — сопротивление, PA — альвеолярное давление, P1 — давление, которое нужно для преодоления сопротивления, V — скорость движения воздушного потока.

Пневмотахография показана для установления причины частой одышки или мучительного кашля у больных, определения степени бронхообструкции при заболеваниях органов дыхательной системы (бронхиальной астме, атопическом бронхите, хронических обструктивных патологиях, пневмосклерозе).
Метод также используют перед оперативными вмешательствами на легких и бронхах, для оценки эффективности проводимой терапии, проведения экспертизы степени трудоспособности пациентов с тяжелыми заболеваниями органов дыхания.
Пневмотахография является также ценным диагностическим методом для установления причины бронхиальной обструкции у пациентов с клапанным механизмом. Процедура пневмотахографии противопоказана во время беременности, при тяжелых дыхательных нарушениях, эпилепсии, аневризме церебральных сосудов, кровохарканьи, после перенесенных пульмональных инфекций, инсультов, инфаркта миокарда, гипертонического криза.
С помощью этого диагностического метода определяют множество показателей, характеризующих функцию внешнего дыхания и степень проходимости дыхательных путей. К основным показателям, определяемым при исследовании, являются:
- форсированная жизненная емкость легких (ФЖЕЛ) — это объем выдыхаемого воздуха, максимально возможный после форсированного вдоха (в норме — 3500-3700 мл);
- объем форсированного выдоха за первую секунду (ОФВ1) — это объем воздуха за первую секунду усиленного выдоха (в норме — не менее 70%);
- индекс Тиффно — это процентное соотношение ОФВ1 и ФЖЕЛ (в норме — минимум 70%);
- максимальная скорость движения воздуха (МОС) — это максимальная скорость, с которой воздух проходит через воздухоносные пути при усиленном выдохе после полного вдоха (в норме — от 4 до 8 л/сек);
- сопротивление воздушных путей (в норме — от 2 до 8 см вод.ст.), растяжимость легочной ткани (в норме — от 0,15 до 0,35 л/см вод.ст.), работа дыхания в покое (в норме — до 0,5 кгм/мин).
Сравнение полученных результатов с нормативными показателями позволяет обнаружить обструктивную патологию дыхательных органов и определить ее степень.

Метод неинвазивный, поэтому абсолютно безболезненный для больного. Длительность исследования не дольше 10-15 минут, процедуру можно проводить амбулаторно, в поликлинических условиях.
Пневмотахография подходит для диагностики большого количества людей, не требует особой подготовки и имеет невысокую стоимость процедуры.
К недостаткам этой диагностической методики следует отнести сложность интерпретации результатов. Во время процедуры пациент вынужден усиленно дышать, что грозит обмороком от гипервентиляции.
Чтобы правильно подготовиться к процедуре, нужно минимум за сутки до нее отказаться от курения и приема спиртных напитков. В случае приема бронхолитических средств короткого действия, по согласованию с врачом, назначившим их, желательно отменить их прием минимум за 4 часа до манипуляции. Пациенты, применяющие ингаляторы, должны обязательно взять его с собой.
Одежда на обследуемом человеке должна быть просторной, чтобы не стесняла движений грудной клетки. Пояс также нужно снять или расстегнуть. На исследование необходимо прийти заранее, чтобы отдышаться, успокоиться, привести дыхание в спокойное состояние.
В день проведения процедуры запрещены любые физические нагрузки: они сбивают ритм дыхания и могут исказить результат.
Пневмотахография проводится натощак. Перед проведением процедуры фиксируют антропометрические данные пациента (рост, вес, уровень физической подготовки), которые влияют на интерпретацию результатов исследования.
Для проведения обследования пациента усаживают в кресло, на трубку аппарата надевают одноразовый мундштук, а нос закрывают специальным зажимом.
Обследуемый делает несколько спокойных вдохов-выдохов. После этого, не задерживая дыхания, пациент последовательно делает несколько усиленных вдохов и выдохов.
Если форсированные вдохи-выдохи провоцируют у больного кашель, нужно прервать обследование на несколько минут, после чего попробовать еще раз.
В случае, если после повторной попытки кашель появился опять, исследование откладывают на несколько дней. При появлении боли в грудной клетке или кровохарканья, исследование необходимо немедленно остановить, а обследуемому — оказать необходимую помощь.
Пневмотахография как метод функционального исследования проходимости бронхов и величины сопротивления воздухоносных путей потоку воздуха самостоятельно на практике практически не используется.
Современное пневмотахографическое оборудование обычно совмещают со спирографом, чтобы объединить максимальное количество возможных исследований функций дыхания в одной диагностической процедуре.
источник
При некоторых заболеваниях, связанными с бронхами и дыхательными путями, необходима пневмотахометрия. С помощью этой процедуры измеряется проходимость органов, определяется скорость и объемы воздуха при выдохе и вдохе. В каких случаях рекомендуется исследование и как оно проводится?
Пневмотахометрия рекомендуется людям, страдающими заболеваниями бронхов и верхних дыхательных путей, особенно если имеют хроническую форму. Именно благодаря этому методу диагностировать ряд патологий можно на самых ранних стадиях.
Для исследования используется пневмотахометр (спирометр). Через него пациент делает несколько вдохов и выдохов, а прибор устанавливает уровень проходимости бронхов и максимальную скорость движения воздуха.
Итоговое заключение врача зависит от:
- максимальной скорости воздуха;
- средней скорости выдоха;
- пиковой скорости выдоха;
- индекса Тиффно;
- жизненной емкости легких.
При анализе показателей учитываются индивидуальные особенности организма пациента, рост, возраст и уровень физической подготовки.
С помощью регулярной пневмотахометрии ведется мониторинг состояний и оценивается прогресс заболевания. Это необходимо при активном лечении и позволяет оценить его эффективность.
К однозначным показаниям относятся:
- бронхиальная астма;
- пневмосклероз;
- атопический бронхит;
- хроническая обструктивная патология.
При этих патологиях пневмотахометрия проводится в обязательном порядке и, как правило, неоднократно. Только таким образом специалист может оценить состояние дыхательной системы и подобрать подходящее лечение.
Дополнительно для подтверждения диагноза может быть назначена спирография – метод измерения объема легких, проводимый с учетом показателей форсированного и естественного дыхания. Во время процедуры пациенту необходимо вдыхать атмосферный воздух или чистый кислород.
Во время процедуры пациент может сидеть или стоять, тело должно быть достаточно расслаблено. На прибор надевается специальный стерильный мундштук, на нос пациента надевается зажим: во время исследования дышать можно только ртом.
Для подготовки к получению данных делаются несколько спокойных выдохов и вдохов. Без задержки дыхания выполняются глубокие форсированные вдохи и выдохи, повторяются они несколько раз. По шкале пневмотахотра специалист анализирует скорость форсированного выдоха.
У взрослых мужчин скорость выдоха должна составлять от 5 до 8 л/с, у женщин -4-6 л/с. По формуле Бадаляна вычисляется объемная скорость. Фактическая емкость легких умножается на 1,2%. Полученный результат должен составлять более 85%, в противном случае диагностируется нарушение проходимости. При наличии хронического нарушения показатели скорости заметно снижаются.
Пневмотахометрия абсолютно безболезненна и не причиняет испытуемому никакого дискомфорта. В некоторых случаях процедуру рекомендуют перенести на неопределенный срок или отменить вовсе. К ним относятся:
- артериальная аневризма;
- беременность;
- гипертонический криз;
- эпилепсия;
- тяжелые нарушения дыхательных путей.
Также отказаться от исследования придется в том случае, если пациент в течение трех месяцев до даты пневмотахометрии столкнулся с инсультом, инфарктом миокарда или инфекцией дыхательных путей.
В течение суток перед исследованием пациенту необходимо полностью отказаться от курения и употребления алкогольных напитков: все это может негативно повлиять на результат, исказив его. При необходимости с собой нужно взять ингалятор. Если больной принимает бронхолитики короткого действия, заранее нужно сказать об этом врачу.
Одежда пациента должна быть свободной, не ограничивающей движения грудной клетки, не давящей на горло. Необходимо находиться в максимально спокойном состоянии. Повлиять на конечный результат исследования могут быстрая ходьба, физические упражнения или даже чрезмерное волнение.
Последний прием пищи разрешается за два часа до исследования, проводить его желательно натощак. Перед процедурой специалисту нужно сообщить рост, возраст и вес. Если исследование проводится повторно, пациент должен находиться в таком же положении, в каком получались первоначальные данные.
источник
Пневмотахометрия — это обследование, в ходе которого измеряется проходимость дыхательных путей.
При проведении процедуры с помощью специального аппарата определяется скорость прохождения воздуха во время вдоха и выдоха.
Пневмотахометрия проводится при заболеваниях бронхов и верхних дыхательных путей. Она чаще используется для диагностики пациентов с хроническими заболеваниями.
К числу таких патологий относятся:
- Бронхиальная астма;
- Атопический бронхит;
- Пневмосклероз;
- Хроническая обструктивная патология.
Регулярное проведение пневмотахометрии позволяет определять прогресс заболевания и оценивать эффективность лечения.
Также обследование проводится:
- У пациентов с повышенным риском заболеваний легких;
- При отягощенной наследственности — у лиц, родственники которых страдают бронхолегочными и аллергическими заболеваниями;
- У военных и спортсменов для оценки функциональной активности легких.
В некоторых ситуациях пневмотахометрия противопоказана или требуется осторожность при ее проведении.
К таким случаям относятся:
- Повышенное артериальное давление;
- Выраженная недостаточность кровообращения;
- Ишемический или геморрагический инсульт, перенесенный не более трех месяцев назад;
- Перенесенный ранее инфаркт;
- Аневризма аорты или артерий головного мозга;
- Тяжелая обструкция дыхательных путей;
- Выраженное снижение функции легких, которое привело к дыхательной недостаточности;
- Общее тяжелое состояние больного, которое не позволяет провести пневмотахометрию;
- Острая инфекция органов дыхания;
- Эпилепсия;
- Беременность.
Чтобы результаты обследования были максимально достоверны, стоит пройти несложную подготовку к пневмотахометрии.
Для этого надо:
- Отказаться от курения и употребления алкоголя в течение суток перед исследованием;
- Отменить прием лекарственных препаратов, которые влияют на показатели дыхания, увеличивая проходимость дыхательных путей (таких, как бронхолитики);
- Избегать в день обследования физических и эмоциональных нагрузок;
- Надеть перед прохождением пневмотахометрии свободную одежду, которая не стесняет грудную клетку.
Обследование рекомендуется проходить не раньше, чем спустя 2 часа после еды. Если процедура проводится утром, нужно воздержаться от завтрака.
Пневмотахометрию проводят в процедурном кабинете, при этом используется специальный прибор — пневмотахометр.
Пациент может располагаться в положении сидя или стоя, на его носу располагается зажим, благодаря которому возможно только ротовое дыхание. На трубку пневмотахометра надевается стерильный мундштук.
Пациент производит несколько вдохов и выдохов в спокойном режиме, затем набирает в легкие максимальное количество воздуха и с силой выдыхает его, затем повторяет эту операцию.
Пневмотахография переносится пациентами легко, но в некоторых случаях возможно развитие осложнений:
- Потемнения в глазах;
- Головокружения;
- Обморока.
По своей сути эта диагностическая методика близка к спирограмме форсированного выдоха.
Для получения дополнительной информации при проведении пневмотахометрии могут проводиться бронходилатационные пробы. В этом случае пациент принимает препараты, расширяющие бронхи, и полученные после этого показатели сравниваются с исходными.
Основные преимущества пневмотахометрии:
- Этот метод обследования не предполагает вмешательства в организм пациента, то есть не является инвазивным;
- Прохождение пневмотахометрии не отнимает много времени;
- Метод хорошо подходит для проведения массовых обследований;
- Пневмотахометрия — это хорошо изученный и проверенный способ диагностики;
- Не требуется сложной подготовки к прохождению обследования.
К недостаткам можно отнести то, что точность диагностики сильно зависит от соблюдения методики процедуры и от квалификации врача, который проводит обследование и расшифровывает результаты.
В ходе исследования оцениваются:
- Жизненная емкость легких;
- Максимальная скорость прохождения воздуха;
- Пиковая скорость выдоха;
- Средняя скорость выдоха;
- Индекс Тиффно.
Жизненная емкость легких — это максимальный объем воздуха, который может в них попасть во время вдоха и выйти на выдохе. Индекс Тиффно позволяет оценить нарушение проходимости дыхательных путей.
Полученные в ходе обследования данные сравнивают с нормой. Низкий показатель максимальной скорости выдоха свидетельствует об ухудшении функции мышечного аппарата или снижении проходимости дыхательных путей.
При более подробном анализе кривых потока воздуха можно установить, имеет ли место нарушение его прохождения в мелких, средних и крупных бронхах и в трахее. Пневмотахометрия позволяет выявить нарушения прохождения воздуха через бронхи на ранней стадии, когда патология еще никак себя не проявляет.
Полученные в ходе обследования результаты анализируются с учетом возраста, роста, веса, уровня физической подготовки и других индивидуальных особенностей организма. Для этого перед проведением процедуры врач замеряет антропометрические параметры пациента.
Каждому, кто входит в группу риска или уже страдает от болезни дыхательных путей, необходимо знать, что такое пневмотахометрия и как к ней подготовиться. Это простое в проведении исследование, которое не занимает много времени и почти не требует подготовки.
Данная диагностическая методика может использоваться для выявления нарушений проходимости бронхов, в том числе и на ранней стадии. Она позволяет оценить динамику течения бронхолегочных заболеваний и эффективность назначенного лечения.
источник
Бронхиальная астма (БА) — «хроническое заболевание, основой которого является воспалительный процесс в дыхательных путях с участием разнообразных клеточных элементов, включая тучные клетки, эозинофилы и Т-лимфоциты. У предрасположенных лиц этот процесс приводит к развитию генерализованной бронхиальной обструкции разной степени выраженности, полностью или частично обратимой спонтанно или под влиянием лечения. Воспалительный процесс вызывает также содружественное усиление ответа дыхательных путей в виде бронхиальной обструкции на различные внешние и внутренние стимулы» (определение экспертов ВОЗ, 1993).
Появление этого определения Б А стало возможным в связи с тем, что за последние 10 лет существенно изменилось представление о Б А, ее этиологии, патогенезе, клинике, лечении и профилактике. Таким образом, в’ основе БА (независимо от степени ее тяжести) лежит хронический неинфекционный воспалительный процесс в дыхательных путях. Гиперактивность бронхов, изменяющаяся со временем бронхиальная обструкция и тесно связанные с ними клинические симптомы БА являются следствием персистирующего воспаления в бронхах.
Этиология.За последние 30 — 40 лет БА стала очень распространенным заболеванием и занимает видное место в общей структуре заболеваемости. Распространенность Б А колеблется от 3 до 8 %.
В возникновении БА имеет значение наследственная предрасположенность. Выявлена связь некоторых антигенов гистосовместимости (HLA) с тяжестью течения БА; нарастание тяжести заболевания особенно часто отмечается у носителей антигенов А2, В7, В12, В13, В27, В35, DR2, DR5 и их комбинации.
В развитии болезни играют роль внутренние и внешние факторы. Внутренние факторы — это биологические дефекты иммунной, эндокринной систем, вегетативной нервной системы, чувствительности и реактивности бронхов, мукоцилиарного клиренса, эндотелия сосудов легких, системы быстрого реагирования (тучные клетки и др.), метаболизма арахидоновой кислоты и т.д.
Внешние факторы, способствующие клинической реализации биологических дефектов, включают: 1) аллергены (пыльцевые, пылевые, пищевые, лекарственные, производственные, аллергены клещей, насекомых, животных и пр.); 2) инфекцию (вирусы, грибы; некоторые виды бактерий); 3) механические и химические раздражители (металлическая, древесная, силикатная, хлопковая пыль; пары кислот, щелочей; дымы и пр.); 4) метеорологические и физико-химические факторы (изменение температуры и влажности воздуха, колебания барометрического давления, магнитного поля земли, физические усилия и пр.); 5) стрессовые нервно-психические воздействия и физическую нагрузку; 6) фармакологические воздействия (р-адреноблокаторы, нестероидные противовоспалительные препараты и т.д.).
Инфекционные агенты, помимо их аллергизирующего действия, могут играть также иную роль: а) снижать порог чувствительности организма к неинфекционным (атопическим) аллергенам, повышать проницаемость для них слизистой оболочки органов дыхания; б) формировать неиммунологическим путем изменение реактивности клеток-мишеней (туч-
ные клетки, базофилы, моноциты и др.) и эффекторных систем. Известно, что некоторые вирусы и бактерии оказывают р-адреноблокирующее действие и способны воздействовать на эфферентные зоны вагусного бронхоконстриктивного механизма.
Как правило, при Б А у одного и того же больного можно заподозрить или выявить сочетание нескольких этиологических факторов.
Чем продолжительнее течение болезни, тем большее значение приобретают различные неспецифические раздражения и психогенные факторы. Первоначально вызвавший бронхиальную астму аллерген может со временем утратить свое значение, исчезнув из зоны окружения больного, а обострения болезни обусловливаются иными причинами.
Патогенез.Центральным звеном патогенеза Б А является неинфекционный воспалительный процесс в бронхах, который вызывается воздействием различных воспалительных клеток и выделяемых ими биологически активных веществ — медиаторов. В свою очередь воспаление бронхов ведет к развитию их гиперчувствительности и гиперреактивности, предрасполагая таким образом бронхиальное дерево к сужению в ответ на различные стимулы (схема 7).
В большинстве случаев Б А является аллергической болезнью, поэтому главным механизмом формирования патологического процесса является иммунный. У значительной части больных БА нарушения иммуноком-петентной системы протекают по I, III и IV типам реакций гиперчувствительности (по классификации, разработанной R.Coombs и P.Gell). Развитие реакций II (цитотоксического) типа при БА пока не описано.
Схема 7. Патогенез бронхиальной астмы
Чаще других главную роль играют механизмы гиперчувствительности I (анафилактического, или атопического) типа. К этому типу аллергии относят немедленные реакции, развивающиеся вследствие взаимодействия аллергена (антигена) со специфическим IgE. Реакция антигена с IgE происходит преимущественно на поверхности субмукозных тучных клеток дыхательных путей и циркулирующих в крови базофилов. В результате наблюдается их дегрануляция с высвобождением биологически активных молекул, среди которых преобладают медиаторы воспаления. Уже через несколько секунд после реакции клетки секретируют ранее синтезированные вазоактивные амины: гистамин, серотонин. Более отдаленным последствием активизации тучных клеток является запуск продукции метаболитов арахи-доновой кислоты (простагландинов, лейкотриенов), тромбоксанов и цито-кинов, которые также секретируются тучными клетками и участвуют в поддержании воспалительной реакции в тканях (интерлейкины 3, 4, 5, 8; ней-трофильный хемотаксический фактор, фактор агрегации тромбоцитов, грану лоцитарно-макрофагальный колониестимулирующий фактор и др.).
Секретируемые тучными клетками медиаторы и цитокины вызывают интенсивный приток эозинофилов и других клеток воспаления (грануло-цитов, моноцитов, Т-лимфоцитов) к месту проникновения аллергена. Через 6— 12 ч развивается поздняя стадия аллергической реакции, при которой доминирует клеточная инфильтрация. Эозинофил рассматривается как «ключевая» клетка в повреждении эпителия дыхательных путей вследствие продукции и секреции им эозинофильного катионного белка, а также выделения фактора активации тромбоцитов и так называемого «большого основного протеина». В свою очередь повреждение эпителия бронхов эозинофильным «большим основным протеином» приводит к развитию неспецифической гиперреактивности и гиперчувствительности.
Медиаторы тучных клеток привлекают в зону воспаления нейтрофилы и способствуют выделению ими активных форм кислорода. Активированные нейтрофилы в свою очередь стимулируют дегрануляцию тучных клеток, что замыкает «порочный круг».
В развитии хронического воспаления в бронхах велика роль лимфоцитов, выделяющих интерлейкины с последующей активацией тучных клеток и эозинофилов. Кроме того, вещества, обладающие мощным брон-хоспастическим действием и потенцирующие воспаление, вырабатываются макрофагами и моноцитами.
Под влиянием всех вышеописанных изменений повышается проницаемость микроциркуляторного русла, развиваются отек, гипер- и дискриния, бронхоспазм и прочие проявления неинфекционного воспаления дыхательных путей. Клинически это выражается острым нарушением проходимости бронхов и развитием приступа Б А.
В возникновении реакции I типа большая роль отводится избыточному синтезу реагинов, дефициту секреторного IgA и, главное, снижению Т-супрессорной функции лимфоцитов.
Реакция III типа (иммунокомплексный тип, или феномен Артюса) происходит в зоне избытка антигена с участием преципитирующих антител. Реакция развивается под воздействием экзоаллергенов (микроорганизмы, ферменты, пыль, антибиотики и др.) и эндоаллергенов [инфекционное и(или) аллергическое воспаление, различные раздражители и другие факторы могут приводить к денатурации белков бронхиол и альвеол с последующим формированием эндоаллергенов —аутоаллергенов].
При иммунокомплексных реакциях III типа образуются антитела, принадлежащие преимущественно к иммуноглобулинам классов G и М. Повреждающее действие образованного комплекса антиген — антитело реализуется главным образом через активацию комплемента, освобождение лизосомных ферментов. Происходят повреждение базальных мембран, спазм гладких мышц бронхов, расширение сосудов, повышается проницаемость микроциркуляторного русла.
Тип IV (клеточный), при котором повреждающее действие оказывают сенсибилизированные лимфоциты, относится к гиперчувствительности замедленного типа (ГЗТ).
Основными медиаторами аллергической реакции IV типа являются интерлейкины — лимфокины (действуют на макрофаги, эпителиальные клетки) и лизосомные ферменты; возможна роль активации кининовой системы. Под влиянием этих веществ происходят развитие отека, набухание слизистой оболочки, бронхоспазм, гиперпродукция вязкого бронхиального секрета. Выделяющиеся лимфоцитами интерлейкины способствуют также привлечению к месту аллергической реакции других клеток воспаления с развитием персистирующей воспалительной реакции. Все это приводит к длительному нарушению бронхиальной проходимости.
В патогенезе БА определенная роль принадлежит местной «поломке» иммунной защиты: отмечается уменьшение секреторного IgA, нарушается система фагоцитоза, которая в органах дыхания обеспечивается в основном альвеолярными макрофагами. При нарушении их функции (воздействие лимфокинов и др.) резко снижается противовирусная защита организма (вследствие снижения продукции интерферона). Воспаление приобретает персистирующий характер.
Неиммунные механизмы. Известно, что, помимо антиген-зависимой дегрануляции тучных клеток, существует большое количество неспецифических факторов (токсины, ферменты, лекарства, различные макромолекулы и др.), вызывающих дегрануляцию тучных клеток неиммунным путем. Различные физические, механические и химические раздражители (например, дым, двуокись серы, пыль, холодный воздух и др.), инфекционные агенты (без сенсибилизации и аллергизации) провоцируют рефлекторный бронхоспазм путем стимуляции рецепторов в дыхательных путях. Ранее считалось, что такая реакция осуществляется путем повышенной активности парасимпатической нервной системы. Однако в настоящее время этот механизм не считается основным. Обнаружена распространенная сеть нервных волокон неадренергической нехолинергичес-кой регуляции бронхов, содержащих мощные нейропептиды (нейрокин А и В, субстанцию Р, вазоактивный интенстинальный пептид и др.), которые имеют отношение к развитию большинства признаков обострения бронхиальной астмы.
Предполагают участие глюкокортикоидной недостаточности, дизова-риальных расстройств (гиперэстрогенемия и гипопрогестеронемия) и нервно-психических нарушений в формировании «нестабильного метаболизма» тучных клеток.
Недостаточность глюкокортикостероидов способствует развитию гиперреактивности тучных клеток, снижению синтеза катехоламинов, активации простагландинов F2a и др., а также нарушению иммунокомпетент-ной системы (комплексное участие в патогенезе БА и иммунологических и неиммунологических механизмов).
Гиперэстрогенемия и гипопрогестеронемия воздействуют главным образом на а- и р-адренорецепторы, повышая активность ос-рецепторов и снижая активность р-рецепторов.
При нарушении бронхиальной проходимости, обусловленной любыми другими механизмами, также отмечается адренергический дисбаланс, выражающийся в преобладании системы гуанилатциклазы над системой аде-нилатциклазы. Кроме того, изменяется содержание внутриклеточного фермента фосфодиэстеразы, усиливается поступление ионов кальция в клетку, нарушается обмен простагландинов.
Преобладание того или иного механизма в патогенезе БА позволяет выделить ее различные патогенетические варианты [Федосеев Г.Б., 1982; Чучалин А.Г., 1985].
Классификация.В последние годы в нашей стране с учетом принятого определения БА используется классификация, предложенная Г.Б. Федосеевым (1982). Она не отменяет классификацию, разработанную А.Д. Адо и П.К. Булатовым (1969), но развивает ее с учетом результатов новых исследований.
Классификация бронхиальной астмы [по Федосееву Г.Б., 1982]
• Этапы развития Б А: 1) состояние предастмы, 2) клинически офор
мленная БА.
К предастме относят все состояния, представляющие угрозу возникновения БА (острый и хронический бронхит, а также острая и хроническая пневмония с элементами бронхоспазма, в сочетании с вазомоторным ринитом, крапивницей и другими состояниями, при которых выявляются эозинофилия крови и увеличенное содержание эозинофилов в мокроте). После первого приступа или сразу возникшего астматического статуса БА считается клинически оформленной.
• Формы Б А: 1) иммунологическая, 2) неиммунологическая (в фор
мулировку клинического диагноза на включается).
• Патогенетические механизмы (клинико-патогенетические вариан
ты) БА: 1) атопический, 2) инфекционнозависимый, 3) аутоиммун
ный, 4) дисгормональный, 5) нервно-психический дисбаланс, 6) ад
ренергический дисбаланс, 7) первично измененная реактивность
бронхов.
Разделение БА по патогенетическим механизмам и выделение основного из них представляют трудную и часто неразрешимую задачу, особенно для врачей поликлиник. Однако во всех случаях такая попытка оправдана, так как каждый из патогенетических механизмов предполагает определенный, свойственный только ему характер лекарственной терапии.
У одного больного возможно сочетание нескольких клинико-патогене-тических вариантов. В такой ситуации необходимо на момент обследования выделить основной для данного больного, так как это важно для проведения адекватной терапии. В процессе длительного течения Б А возможна смена патогенетического механизма.
• Тяжесть течения БА: 1) легкое течение, 2) течение средней тяжес
ти, 3) тяжелое течение.
При легком течении Б А обострения не длительные, возникают 2 — 3 раза в год. Приступы удушья купируются, как правило, приемом различных бронхолитических препаратов внутрь. В межприступный период признаки бронхоспазма, как правило, не выявляются.
Среднетяжелое течение характеризуется более частыми обострениями 3 — 4 раза в год. Приступы удушья протекают тяжелее и купируются инъекциями лекарственных препаратов.
При тяжелом течении Б А обострения возникают часто (5 раз и более раз в год), отличаются длительностью. Приступы тяжелые, нередко переходят в астматическое состояние.
В ряде случаев разделение Б А по тяжести течения бывает условным. Так, при легком течении Б А больной может погибнуть от внезапно развившегося астматического статуса. В то же время возможна «спонтанная» ремиссия при довольно тяжелом течении болезни.
• Фазы течения Б А: 1) обострение, 2) стихающее обострение, 3) ре
миссия.
Фаза обострения характеризуется наличием выраженных признаков заболевания, прежде всего повторно возникающих приступов Б А или астматического состояния.
В фазе стихающего обострения приступы становятся более редкими и нетяжелыми. Физикальные и функциональные признаки заболевания выражены меньше, чем в фазу обострения.
В фазу ремиссии исчезают типичные проявления БА: приступы удушья не возникают; полностью или частично восстанавливается проходимость бронхов.
• Осложнения: 1) легочные: эмфизема легких, легочная недостаточ
ность, ателектаз, пневмоторакс, астматический статус и пр.; 2) вне-
легочные: легочное сердце (компенсированное и декомпенсирован-
ное с развитием правосердечной недостаточности), дистрофия мио
карда и др.
Примечания к классификации:
1. Первично измененная реактивность бронхов может быть врожденной и при
обретенной, проявляется приступами удушья при физической нагрузке, воздействии
холодного воздуха, медикаментов, инфекции и др.
2. При инфекционнозависимом варианте БА необходимо указывать характер
инфекционной зависимости: стимуляция атопической реакции; инфекционная ал
лергия; формирование первично измененной реактивности бронхов. В тех случаях,
когда инфекция является аллергеном, Б А определяется как инфекционно-аллерги-
ческая.
Предлагаемая классификация, как и все остальные, не лишена недостатков, но более прогрессивна по сравнению с существующей. Настоящая классификация еще не утверждена, но позволяет более эффективно проводить патогенетическую терапию больных Б А.
Экспертами ВОЗ (1993) даны новые критерии тяжести БА, определяемой выраженностью клинических симптомов, объемом форсированного выдоха за первую секунду (ОФВь л/с) и пиковой скоростью выдоха (ПСВ, л/мин) — наиболее значимыми показателями выраженности обструкции дыхательных путей. Оценка по этим степеням тяжести Б А по-
зволяет осуществить так называемый ступенчатый подход к лечению больных: объем терапии должен повышаться при увеличении степени тяжести болезни.
Классификация БА, основанная на степени тяжести, наиболее важна, когда нужно принять решение о выборе терапии. Кроме того, предложение экспертов ВОЗ классифицировать БА по степени тяжести базируется на том, что нередко другие рубрики вышеприведенной классификации невозможно с достоверностью определить у всех больных.
Классификация бронхиальной астмы по тяжести течения
• Легкое эпизодическое (интермиттирующее).
Кратковременные симптомы реже 1 раза в неделю.
Короткие обострения (от нескольких часов до нескольких дней).
Ночные симптомы 2 раз в месяц.
ПСВ и OOBi: £ 80 % от должных.
Разброс показателей 20 — 30 %.
• Среднетяжелое.
Ежедневные симптомы.
Обострения могут приводить к ограничению физической активности и сна.
Ночные симптомы > 1 раза в неделю. ПСВ и ОФВ1 : 60-80 % от должных. Суточный разброс показателей > 30 %.
Постоянное наличие симптомов.
Ограничение физической активности из-за симптомов астмы.
Клиническая картина.Наиболее характерный признак БА — наличие приступов удушья. Однако клинический диагноз БА может быть поставлен с учетом оценки результатов всех трех этапов диагностического поиска, так как удушье встречается как симптом и при других заболеваниях. В связи с этим возникает на каждом из трех этапов необходимость ее дифференциации от заболеваний, составной частью которых является бронхоспастический синдром с развитием приступов удушья.
На I этапе диагностического поиска устанавливают: а) наличие приступов удушья, их особенности и связь с определенными факторами; б) аллергический анамнез (наследственную предрасположенность, непереносимость пищевых и лекарственных веществ); в) наличие предшествую-
щих заболеваний легких; г) влияние метеорологических факторов, физических усилий, дизовариальных расстройств и других причин на возникновение приступов удушья; д) эффективность проводимой ранее терапии; е) течение болезни, появление осложнений.
Больные жалуются на приступы удушья (затрудненное дыхание, преимущественно на выдохе), одышку и кашель. Характер кашля может быть разнообразным: чаще кашель сухой, надсадный, приступообразный или с выделением вязкой, трудноотделяемой мокроты. При развитии легочной недостаточности одышка беспокоит и в межприсгупный период. Повышение температуры тела может свидетельствовать об активности бронхоле-гочной инфекции. Затрудненное носовое дыхание, как правило, служит проявлением аллергической риносинусопатии (вазомоторный ринит, полипоз) — частого спутника или предшественника Б А (предастма). При расспросе больного необходимо уточнить частоту возникновения симптомов Б А в неделю, обратив особое внимание на ночные симптомы. Эти данные особенно важны для оценки тяжести течения болезни на момент обследования больного.
Данные анамнеза помогают установить связь развития приступов с воздействием определенных аллергенов и других факторов. Наиболее частой причиной обострения и развития БА является инфекция дыхательных путей; особенно велика ее роль в обострении болезни. Из анамнеза узнают о влиянии физического усилия (быстрая ходьба, смех и пр.), изменений метеорологических факторов (холод, повышенная влажность и др.), дизовариальных расстройств на возникновение приступов удушья. Знакомство с условиями труда помогает обнаружить профессиональную астму.
Изучение аллергологического анамнеза способствует диагностике ато-пического варианта БА. В подобных случаях можно получить сведения о поллинозе: обострения болезни имеют сезонный характер (чаще весной и летом), сопровождаются ринитом, конъюнктивитом. У таких больных бывают крапивница, отек Квинке; выявляется непереносимость пищевых продуктов, ряда лекарственных веществ; отмечается наследственная предрасположенность к аллергическим заболеваниям.
Ориентируясь на данные анамнеза, можно предположительно, а в ряде случаев и с уверенностью высказаться о так называемой аспириновой астме. Эти больные не страдают наследственной формой аллергических заболеваний. Их беспокоит нарушенное носовое дыхание (полипозные разрастания). Наиболее характерный симптом у таких больных — непереносимость нестероидных противовоспалительных препаратов (ацетилсалициловая кислота, индометацин и пр.), вызывающих астматические приступы. На этом этапе уже можно предположить простагландиновый механизм БА.
Указание в анамнезе на прием кортикостероидных препаратов свидетельствует о тяжести болезни, а эффективность приема — об иммунной форме Б А или кортикостероидозависимом ее варианте. Отсутствие эффекта от приема кортикоидных препаратов, особенно у больных с тяжелым течением Б А, делает предположение об аллергическом генезе Б А менее достоверным и практически исключает наличие у больного глюкокортикоид-ной недостаточности. Глюкокортикоиды неэффективны также при астме физического усилия.
Данные о развитии в прошлом астматического статуса свидетельствуют о тяжести течения заболевания и указывают на необходимость проведения терапии кортикостероидами. Наличие предшествующих заболеваний
органов дыхания (ХБ, ХП) предопределяет обычно тяжесть течения БА, отсутствие «светлых» промежутков.
Б А может протекать монотонно, с постоянно нарушенным дыханием и потребностью принимать ежедневно противоастматические средства.
Другой тип течения БА характеризуется периодическими обострениями с заметно усиливающимися признаками бронхиальной обструкции и ремиссиями, когда нарушения бронхиальной проходимости резко уменьшаются или исчезают. Такое течение БА наиболее характерно для атопи-ческого варианта заболевания.
Значение I этапа диагностического поиска особенно велико для диагностики Б А в начальном периоде заболевания, когда все проявления астмы имеют эпизодический характер, а физикальное исследование не дает достаточной информации для постановки диагноза.
На II этапе диагностического поиска в развернутой стадии болезни выявляют: а) внелегочные проявления аллергии; б) признаки бронхо-обструктивного синдрома; в) осложнения БА; г) другие заболевания, сопровождающиеся приступами бронхоспазма.
При обследовании кожных покровов иногда можно выявить изменения, характерные для аллергических проявлений: крапивницу, папулезные и эритематозные высыпания. Эти изменения могут свидетельствовать об иммунологическом варианте БА. При аллергических формах БА могут быть конъюнктивиты (особенно часто у больных поллинозами). Сочетание Б А с экземой, нейродермитом, псориазом предрасполагает к тяжелому течению астмы. Грибковое поражение кожи, ногтевых лож может сопровождаться гиперчувствительностью к грибковым аллергенам.
Часто можно выявить нарушение носового дыхания. Риниты и поли-поз рассматриваются как предастма. Гаймориты и другие синуситы служат очагом инфекции, который может провоцировать удушье.
При физикальном исследовании легких могут быть выявлены признаки эмфиземы. Появлению эмфиземы легких, а затем хронической дыхательной недостаточности и легочного сердца часто способствует хронический бронхит. Он может присоединиться к БА, если она затяжная, а также может служить фоном, на котором развивается инфекционнозависимая Б А.
Аускультация легких помогает обнаружить признаки бронхиальной обструкции, для которой характерны изменение дыхания (удлиненный выдох), сухие, преимущественно свистящие, хрипы. Иногда при обследовании вне приступа удушья сухих хрипов может быть немного или они не прослушиваются. Форсированный выдох позволяет выявить скрытый бронхоспазм (появление или нарастание сухих хрипов).
Обязательно проводят аускультацию легких в положении больного лежа: количество сухих хрипов увеличивается при «вагусном» их механизме.
Постоянно выслушиваемые на определенном участке влажные звонкие («трескучие») мелкопузырчатые хрипы могут свидетельствовать о развившемся пневмосклерозе.
В случае астматического статуса отмечается уменьшение количества сухих хрипов при аускультации вплоть до развития «немого» легкого, несмотря на резкое нарастание удушья и одышки.
Объективное обследование больного помогает выявить симптомы других заболеваний («бабочка» на коже лица, лимфоаденопатия в сочетании с увеличением печени и селезенки, стойкое повышение артериального дав-
ления, упорная лихорадка и пр.), при которых возникают приступы брон-хоспазма, проявляющиеся удушьем (системная красная волчанка, узелковый периартериит, реже другие диффузные заболевания соединительной ткани). В таких случаях предполагаемый диагноз Б А становится маловероятным.
На III этапе диагностического поиска выявляют:
а) нарушение бронхиальной проходимости;
б) измененную реактивность бронхов;
в) характерные изменения при проведении аллергологического обсле
дования;
г) наличие очагов инфекции и признаков воспаления;
Спирография выявляет снижение объема форсированного выдоха за первую секунду (OOBi), уменьшение коэффициента Тиффно (соотношения ОФВ] к ЖЕЛ в процентах) и процентного отношения OOBi к ФЖЕЛ — характерные признаки нарушения бронхиальной проходимости по обструктивному типу. При обострении БА значительно возрастают (на 100 % и более превышают исходный уровень) остаточный объем легких (ООЛ) и функциональная остаточная емкость (ФОЕ). Анализ спирограм-мы позволяет обнаружить признаки трахеобронхиальной дискинезии по наличию зазубрины в верхней части нисходящего колена спирограммы (симптом Колбета— Висса). Эта дискинезия также способствует нарушению бронхиальной проходимости.
Пикфлоуметрия — определение пиковой объемной скорости выдоха — является непременным условием контроля за состоянием больного. Ее проводят утром (до приема лекарств) и вечером с помощью индивидуального карманного прибора — пикфлоуметра. Желательно, чтобы разброс утренних и вечерних значений ПСВ не превышал 20 %.
Пневмотахометрия выявляет преобладание мощности вдоха над мощностью выдоха, что служит ранним признаком бронхиальной обструкции.
Пневмотахография с построением кривой «поток —объем» позволяет диагностировать нарушение бронхиальной проходимости раздельно на уровне крупных, средних и мелких бронхов по данным экспираторного потока при легочном объеме, равном 75, 50, 35 % ФЖЕЛ. Для периферической обструкции характерно значительное снижение кривой «поток — объем» на участке 50 — 75 % ФЖЕЛ, т.е. снижение максимальной объемной скорости на уровне 50-75 % ФЖЕЛ (МОС50, МОС75).
По увеличению мощности выдоха при проведении пневмотахометрии и приросту показателей МОС75, MOCso, МОС25 по данным пневмотахометрии, проводимым после предварительного вдыхания больным бронхоли-тических (симпатомиметических и/или холинолитических) веществ определяют роль бронхоспазма в нарушении бронхиальной проходимости и степень его выраженности.
С помощью этих же методов подбирают наиболее активный для данного больного ингаляционный бронхолитический (симпатомиметический или холинолитический) препарат.
Появление повышенного бронхиального сопротивления, зарегистрированного с помощью спирографии, пневмотахометрии и пневмотахогра-фии в ответ на физическую нагрузку, вдыхание холодного воздуха, раз-
дражающих газов, пылей и ацетилхолина, свидетельствует об измененной реактивности бронхов.
Аллергологическое тестирование осуществляется только вне обострения заболевания и проводится с помощью набора разнообразных неинфекционных и инфекционных аллергенов.
Проводят кожные аллергические пробы (аппликационный, скарифи-кационный и внутрикожный способы нанесения аллергена). Выявленный аллерген можно наносить на конъюнктиву глаза, слизистую оболочку носа для оценки его провоцирующего действия. Наиболее достоверным методом специфической диагностики БА считают выявление специфической гиперреактивности бронхов с помощью ингаляционных провокационных тестов. Ингаляционно аллерген вводят с большой осторожностью, так как такой путь введения может спровоцировать тяжелый приступ БА или развитие астматического статуса. Установление аллергена и уточнение его провоцирующего действия — прямое доказательство аллергической природы БА.
Для специфической диагностики БА применяют также радиоиммуно-сорбентный тест, позволяющий количественно оценить IgE-антитела. Повышение уровня общего IgE подтверждает при соответствующих данных анамнеза атопический механизм развития БА (этот тест применяют при невозможности проведения аллергологического тестирования).
Лабораторные исследования помогают подтвердить предполагаемый диагноз, оценить эволюцию заболевания и эффективность проводимого лечения.
Появление эозинофилов в мокроте является одним из основных диагностических критериев Б А. Кроме того, диагностическое значение имеет обнаружение в мокроте спиралей Куршмана и кристаллов Шарко —Лейдена. Эозинофильный лейкоцитоз представляет собой неспецифический признак и может служить проявлением общей аллергической реакции организма.
Лабораторные исследования помогают решать вопрос о наличии активного воспалительного процесса и степени его выраженности (увеличение острофазовых показателей).
При обострении БА и астматическом статусе особое значение имеет исследование кислотно-основного состояния и газового состава крови (изменяющихся при увеличении дыхательной недостаточности).
Рентгенологическое исследование помогает выявить очаги инфекции (в придаточных пазухах, зубах, желчном пузыре) и установить наличие острого (пневмония) или обострения хронического воспалительного процесса в легких, эмфиземы легких и пневмосклероза.
По данным ЭКГ обнаруживают признаки развития компенсированного легочного сердца — гипертрофию правых отделов сердца (подробнее см. «Легочное сердце»). При подозрении на симптоматический характер бронхоспазма проводят дополнительное обследование по программе, определяемой предполагаемым заболеванием.
Астматический статус. Факторы, предрасполагающие к его развитию, почти всегда являются результатом неадекватной терапии. Чаще всего причинами его служат:
1) бесконтрольный прием симпатомиметических и кортикостероид-ных препаратов;
2) резкое прерывание длительно проводимой кортикостероидной те
рапии;
3) обострение хронического или возникновение острого воспалитель
ного процесса в бронхолегочном аппарате неэффективно леченного;
4) неудачно проведенная специфическая гипосенсибилизация;
5) злоупотребление снотворными и седативными средствами.
Критерии астматического (метаболического) статуса:
1) прогрессирующее нарушение дренажной функции бронхов;
2) развернутая клиническая картина удушья, которая может ослож
няться легочной обструкцией, гипоксемической комой, острым легочным
сердцем;
3) резистентность к симпатомиметическим и бронхолитическим пре
паратам;
4)гиперкапния; 5) гипоксия тканей.
Классификация астматического статуса: I стадия — затянувшийся приступ удушья, сформировавшаяся резистентность к симпатомиметикам; II стадия — нарастание дыхательной недостаточности по обструктивному типу, III стадия — гипоксемическая, гиперкапническая кома.
Стадия I клинически характеризуется затянувшимся приступом удушья, вынужденным положением больного, учащенным дыханием, приступообразным кашлем со скудной, трудноотделяемой мокротой, тахикардией, часто повышением АД.
Из физикальных симптомов отмечают несоответствие между интенсивностью дыхательных шумов, выслушиваемых дистанционно, и данными непосредственной аускультации легких (скудность хрипов, участки ослабленного дыхания).
Стадия I характеризуется умеренной артериальной гипоксемией (РОг составляет 60 — 70 мм рт.ст.) и нормо- или гипокапнией (показатели РСо2 нормальные или уменьшены в результате гипервентиляции и составляют менее 35 мм рт.ст).
Для II стадии характерно очень тяжелое состояние больного: бледно-серые влажные кожные покровы, учащенное поверхностное дыхание, при аускультации — «немое легкое» (хрипы почти не слышны), частый пульс малого наполнения, аритмия, снижение АД. Периоды безразличия у больного сменяются возбуждением.
Стадия II характеризуется более выраженной гипоксемией (Ро2 50 — 60 мм рт.ст.) и нарастающей гиперкапнией вследствие снижения эффективной (альвеолярной) вентиляции (Рсо2 50 — 70 мм рт.ст. и даже несколько выше).
В III стадии сознание отсутствует, тахипноэ, часто разлитой «красный» цианоз, нередко коллапс. Летальность на высоте астматического статуса достигает 5 — 20 %. Наиболее частые причины смерти — асфиксия вследствие позднего проведения реанимационных мероприятий, невозможность восстановления эффективной вентиляции легких.
Стадия III характеризуется тяжелой артериальной гипоксемией (РОг 40 — 55 мм рт.ст.) и резко выраженной гиперкапнией (РСог на уровне 80 — 90 мм рт.ст. и выше) с некомпенсированным респираторным ацидозом.
При своевременно начатой интенсивной терапии прогноз астматического статуса может быть благоприятным.
Все вышеизложенное касалось так называемого метаболического (медленно развивающегося) астматического статуса. Кроме этого, существует немедленно развивающийся (анафилактический) астматический статус, обусловленный развитием гиперергической анафилактической реакции немедленного типа с мгновенным высвобождением медиаторов аллергии и воспаления, что приводит к тотальному бронхоспазму и асфиксии в момент контакта с аллергеном.
Диагностика.Диагностика БА осуществляется на основании выявления определенных признаков.
Основные признаки: 1) наличие приступа удушья или его эквивалентов; 2) генерализованная обратимая бронхиальная обструкция; 3) эозинофилия в мокроте; 4) отсутствие заболеваний, сопровождающихся бронхоспастическим или бронхообструктивным синдромом (данный синдром — одно из проявлений болезни).
Дополнительные признаки: 1) клинико-аллергологи-ческий анамнез; 2) результаты аллергологического тестирования: а) для выявления аллергена — кожные пробы (аппликационные, внутрикож-ные, скарификационные); б) для уточнения специфичности аллергена — назальные, ингаляционные, конъюнктивальные (проводятся в стадии стойкой ремиссии); радиоаллергосорбентный тест; в) провокационные пробы (с ацетилхолином, гистамином) — при сомнительном диагнозе; 3) повышение содержания IgE в сыворотке крови; 4) эозинофилия крови.
Формулировка развернутого клинического диагноза БА учитывает:
1) основной клинико-патогенетический вариант БА (наиболее часто
встречаются инфекционнозависимый и атопический);
2) тяжесть течения (легкое, среднетяжелое, тяжелое);
3) фазу течения (обострение, стихающее обострение, ремиссия);
4) осложнения: а) легочная недостаточность (степень); б) легочно-
сердечная недостаточность (степень); в) астматический статус (стадия);
г) другие осложнения.
Примечание. При инфекционной зависимости Б А рекомендуется указывать: 1) характер хронического поражения легких, на фоне которого развилась БА или которое сопутствует Б А; 2) характер инфекционной зависимости — инфекция, играющая роль аллергена, способствующая проявлению атопических реакций или же формирующая первично измененную реактивность бронхов.
Лечение.1. Неотложная терапия приступа БА; интенсивная терапия — при развитии астматического статуса.
2. Лечение в фазу обострения.
3. Лечение в фазу ремиссии.
Лечение приступа БА проводят с учетом возраста пациента и тяжести приступа.
Легкий приступ больные, как правило, купируют самостоятельно. Используются лекарственные вещества в таблетках (эуфиллин) или в ингаляторах (сальбутамол, вентолин, фенотерол или беротек — Рг-адренос-тимуляторы; беродуал, сочетающий Рг-адреностимулирующий эффект с холинолитическим). При отсутствии ингаляторов приступ купируют подкожными инъекциями адреналина (0,3 мл 0,1 % раствора; рекомендуется молодым пациентам) или эфедрина (0,5 мл 5 % раствора) в сочетании с
папаверином (1 мл 2 % раствора) и антигистаминным препаратом (1 мл димедрола или супрастина).
Приступы средней тяжести у молодых пациентов с немедленным анамнезом купируют ингаляциями симпатомиметических средств или подкожным введением адреналина; при отсутствии эффекта внутривенно вводят эу-филлин. В случае сочетания приступа Б А с повышением АД молодым пациентам одновременно с эуфиллином можно вводить ганглиоблокаторы (пен-тамин, бензогексоний), пожилым — дроперидол. Иногда приступ проходит только после внутривенного введения преднизолона (60 мг).
Пожилым больным при среднетяжелом и тяжелом приступе, особенно при длительном анамнезе, внутривенно вводят эуфиллин, а при отсутствии эффекта — преднизолон.
При тяжелых приступах, помимо внутривенного введения преднизолона, существенное значение имеет выравнивание измененного кислотно-основного состояния; проводится инфузионная терапия натрия гидрокарбонатом, изотоническим раствором хлорида натрия, особенно в тех случаях, когда приступ затягивается и очень плохо отходит мокрота. Прибегают к повторному введению эуфиллина и преднизолона. Больного обязательно госпитализируют.
При затянувшихся тяжелых приступах БА резко возрастает угроза развития астматического статуса.
Лечение астматического статуса заключается в проведении интенсивной терапии, которую необходимо начинать в максимально ранние сроки. Она включает:
а) оксигенотерапию, терапию в виде непрерывной подачи кислородно-
воздушной смеси с относительно небольшим содержанием Ог(35 —40 %);
б) инфузионную терапию, при которой внутривенно вводят декстра-
ны, глюкозу, инсулин, 20 000 ЕД гепарина, натрия гидрокарбонат (под
контролем показателей кислотно-основного состояния) в общем количест
ве не менее 3 — 3,5 л в первые сутки с целью восполнения дефицита жид
кости, устранения гемоконцентрации, разжижения бронхиального содер
жимого;
в) обязательное внутривенное введение кортикостероидов: гидрокор
тизона по 1 мг/ч на 1 кг массы тела, преднизолона по 60 — 90 мг каждые
2 — 4 ч при I стадии статуса; во II стадии суточную дозу преднизолона до
водят до 1000 — 1500 мг. После выведения из астматического статуса дозу
стероидов ежесуточно уменьшают на 25 % до минимальной. Лечение аст
матического статуса исключает использование средств симпатомиметичес-
кого действия, если он развился в результате их передозировки.
В качестве бронхорасширяющего средства используют эуфиллин; показанием для его отмены является развитие частой экстрасистолии.
Для разжижения мокроты используют щелочное питье, паро-кисло-родные ингаляции. Мочегонные средства показаны лишь при возрастании центрального венозного давления до 150 мм вод.ст. и выше. При сопутствующей гипертензии в небольших дозах назначают ганглиоблокаторы (пентамин, бензогексоний), они же улучшают легочное кровообращение.
Активно используют перкуссионный и вибрационный массаж грудной клетки для улучшения выделения содержимого бронхов.
Прогрессирующее нарушение легочной вентиляции, не поддающееся консервативной терапии, является показанием для применения искусст-
венной вентиляции легких, лечебной бронхоскопии и проведения бронхо-альвеолярного лаважа с «отмыванием» и удалением бронхиального содержимого.
Лечение анафилактического варианта астматического статуса требует проведения немедленной парентеральной лекарственной терапии: внутривенного введения 0,3 — 0,5 мл 0,1 % раствора адреналина на 20 мл изотонического раствора хлорида натрия и струйно внутривенно 120 мг преднизолона (200 — 400 мг гидрокортизона) с последующим переходом на внутривенное капельное введение этих же препаратов. Одновременно можно добавить 0,5—1 мл 0,1 % раствора атропина, вводя его струйно на 10 мл изотонического раствора.
При отсутствии эффекта от перечисленных мероприятий проводят фторотановый наркоз и переводят больного на ИВЛ.
После купирования приступа Б А проводят плановую терапию, основные направления которой сформулированы ниже.
• Обучение пациента для создания более тесного сотрудничества с
врачом при лечении Б А.
• Повторный контроль за функциональным состоянием органов ды
хания и оценка в динамике полученных данных.
• Выявление и устранение причинно-значимых факторов внешней
среды.
• Разработка плана долгосрочного лечения больного с учетом его ин
дивидуальных особенностей.
• Разработка плана лечения обострений БА.
• Обеспечение систематического наблюдения за состоянием больного
с корректировкой при необходимости плана лечения.
Лечебные мероприятия, осуществляемые в период обострения заболевания и в период ремиссии, имеют свои особенности.
Лечение больного БА в период обострения, помимо купирования приступа, включает ряд различных мероприятий.
▲ Устранение контакта с выявленным аллергеном. А Лекарственная противовоспалительная терапия.
Глюкокортикоидные препараты в настоящее время являются наиболее эффективными противовоспалительными средствами при лечении Б А. Их можно применять местно (ингаляционно) или системно (внутрь или парентерально). Способ введения во многом определяется особенностью течения заболевания.
Ингаляционное введение кортикостероидных препаратов оказывает местный эффект и дает минимум побочных эффектов. К числу короткодействующих препаратов относятся бекотид и бекломет (беклометазон дипропионат); их следует применять 4 раза в день. Такие препараты, как ингакорт (флунисолид), фликсотид (флютиказон пропионат) и пульми-корт турбухалер (будезонид), характеризуются большей продолжительностью действия, что позволяет использовать их для надежного контроля за течением БА 2 раза в сутки. Ингакорт выпускают в комплектации вместе со специальной пространственной насадкой (спейсером), что облегчает больному пользование аэрозолем, увеличивает его поступление в нижние дыхательные пути, а также дополнительно снижает риск местных и системных побочных эффектов.
В настоящее время считается желательным применение всех дозированных ингаляторов вместе со спейсером.
Если высокие дозы ингалируемых кортикостероидных препаратов (более 1000 мкг/сут) не обеспечивают надежный контроль за течением БА, добавляют кортикостероиды внутрь. При выраженной эозинофилии крови местное введение кортикостероидов сочетается с приемом гормональных препаратов внутрь в виде так называемых толчков: 3 дня по 20 — 25 мг преднизолона (или другого глюкокортикоида в адекватной дозе). Большую часть суточной дозы рекомендуется принимать в утренние часы, заканчивать прием не позднее 5 —6 ч вечера.
При тяжелом течении Б А кортикостероиды назначают постоянно, начиная с максимальной для больного дозы (30 — 40 мг преднизолона), затем постепенно дозу снижают и переходят на поддерживающую терапию.
Противовоспалительным эффектом обладает также натрия хромогли-кат (интал, ломудал, кромолин), который эффективен при лечении большинства больных атопической (аллергической) Б А и, кроме того, иногда дает положительный эффект у больных «аспириновой» астмой и астмой физического усилия. Препарат вводят ингаляционно в виде сухого порошка (с использованием спинхайлера) или в виде распыляемого раствора (с помощью дозированного ингалятора). Лечение следует начинать с двух ингаляций препарата 4 раза в сутки; при достижении эффекта переходят на поддерживающую терапию.
В последние годы появился новый противовоспалительный препарат, также вводимый ингаляционно, — тайлед (натрия недокромил). Назначаемый по 2 —4 ингаляции в сутки, он дает возможность контролировать легкое персистирующее течение БА. У части больных средиетяжелым и иногда тяжелым течением БА его назначение позволяет уменьшить дозу применяемых кортикостероидов.
При затрудненном дыхании за 15 мин до ингаляции противовоспалительного препарата больной должен сделать 1 — 2 вдоха бронхолитика. Комбинированным препаратом, содержащим в одном аэрозоле полную дозу интал а и уменьшающую дозу бронхолитического препарата (50 мкг беротека), является дитек.
▲ Бронхолитическая терапия: 1) бронхолитические препараты парентерально, в свечах или перорально. Препаратом выбора остается эуфиллин (10 мл 2,4 % раствора внутривенно струйно или капель-но) или теофиллин (по 0,3 г в свечах предпочтительнее на ночь), эуфиллин по 0,15 г в таблетках после еды 3 — 4 раза в день. Применяют препараты эуфиллина пролонгированного действия (теопек, теодур и др.). Эти препараты являются базисными и назначаются всем больным (при условии хорошей переносимости); 2) симпато-миметические и(или) холинолитические препараты назначаются в дозированном аэрозоле, как правило, при появлении предвестников приступа удушья. Постоянное применение этих препаратов в ингаляторах не рекомендуется во избежание побочных эффектов (тахикардия, повышение АД, нарушения ритма сердца); р2-адреностиму-ляторы эффективны при Б А, вызываемой физической нагрузкой, точно так же как и блокаторы медленных кальциевых каналов [Чу-чалин А.Г., 1985].
В настоящее время наряду с ингаляционными р2-агонистами короткого действия — фенотеролом (беротек), сальбутамолом (вентолин), тербутали-ном (бриканил) и др., длительность бронхолитического действия которых составляет 4 —6 ч, применяют пролонгированные р2-агонисты с продолжительностью действия более 12 ч, в частности сальметерол (серевент).
Применяют симпатомиметики длительного действия также в форме таблеток (вольмакс и др.). Они показаны для приема внутрь на ночь при ночных приступах Б А.
Ингаляционные холинолитики — ипратропиум бромид (атровент) — имеют определенные преимущества перед р2-агонистами у лиц пожилого возраста. Применяют атровент также в комбинации с фенотеролом (беро-теком) под названием беродуал.
С учетом тяжести течения БА предлагается ступенчатая схема лечения заболевания с применением вышеописанных средств.
Ступенчатый подход к лечению бронхиальной астмы
• I ступень (лечение легкой персистирующей БА): ингаляцион
ные Рг-агонисты короткого действия применяют «по требованию»
не более 3 раз в неделю; игаляционное введение хромогликата на
трия (интала), или хромогликата натрия недокромила (тайледа),
или рг-агониста короткого действия рекомендуется перед предпола
гаемым контактом с аллергеном или перед физической нагрузкой.
• II ступень (лечение Б А средней тяжести): ежедневная ингаля
ционная противовоспалительная терапия — хромогликат натрия
(интал) или кортикостероидные препараты в дозе 200 — 500 мкг.
При необходимости увеличивают дозу кортикостероидов до 400 —
700 мкг (или при ночных приступах добавляют пролонгированные
бронходилататоры). Ингаляционные р2-агонисты короткого дейст
вия (используют не чаще 3 — 4 раз в день).
• III ступень (лечение Б А средней тяжести): ингаляционные
кортикостероидные препараты по 800 — 1000 мкг ежедневно; приме
няют пролонгированные теофиллины или пероральные рг-агонис
ты, или ингаляционные р2-агонисты пролонгированного действия
(особенно при ночных приступах); можно назначать антихолинер-
гические препараты; в случае необходимости применяют ингаляци
онные рг-агонисты короткого действия, но не чаще 3 — 4 раз в день.
• IV ступень (лечение БА тяжелого течения): ингаляционные
кортикостероидные препараты по 800—1000 мкг в день; пролонги
рованные теофиллины и/или пероральные или пролонгированные
Рг-агонисты; при необходимости назначают р2-агонисты короткого
действия (как правило, утром) ингаляционно, но не чаще 3 — 4 раз
в день. Можно применять антихолинергические препараты. В тера
пию включаются кортикостероидные препараты (перорально еже
дневно или по альтернирующей схеме).
а Дополнительная патогенетическая терапия:
1) муколитические препараты в виде ингаляции (ацетилцистеин) или таблеток (мукалтин, лазолван), настои и отвары термопсиса назначают при вязкой, трудноотделяемой мокроте. Хорошее секретолитическое действие оказывают горячее щелочное питье и йодистые препараты (3 % раствор йодида калия по 1 столовой ложке 3 — 4 раза в день; следует помнить о возмож-
ной непереносимости препарата: слезотечение, ринорея, усиление бронхоспазма);
2) антибактериальную терапию проводят при обострении воспа
лительного процесса в бронхолегочной системе у больных с
инфекционнозависимой БА;
3) лечебная бронхоскопия под наркозом проводится в случае
отсутствия эффекта от лекарственной терапии у больных при
сопутствующем катарально-гнойном и гнойном эндобронхите
(местно вводят антибактериальные средства, предпочтение
оказывается 1 % раствору диоксидина). При необходимости
эндобронхиально вводят кортикостероиды (гидрокортизон);
4) антагонисты кальция (нифедипин, изоптин, финоптин) инги-
бируют трансмембранный поток кальция, что ведет к уменьше
нию выхода медиаторных веществ из тучных клеток. Препара
ты показаны больным при сочетании БА с ишемической болез
нью сердца и при астме «физического усилия»;
5) антимедиаторы имеют небольшое значение в лечении Б А:
а) антигистаминные препараты блокируют Нгрецепторы,
уменьшая действие гистамина на гладкую мускулатуру брон
хов; б) антисеротониновые препараты (циннаризин) применя
ют лишь при лечении больных БА с четкими клиническими
признаками гиперсеротонинемии (тахикардия, наклонность к
поносам, гиперемия лица), в) ингибиторы калликреина — тра-
силол, контрикал (по 10 000 ЕД) — вводят внутривенно ка-
пельно при затянувшихся приступах Б А. Используют также
гепарин, улучшающий микроциркуляцию. В настоящее время
применяют две генерации антагонистов Hi-рецепторов. Пре
параты первого поколения (димедрол, тавегил, супрастин,
пипольфен, диазолин) оказывают ряд нежелательных воздей
ствий (снотворное, вызывает сухость во рту, тахикардию,
задержку мочи и т.д.), что резко ограничивает их применение.
Препараты второго поколения — астемизол, кларитин и др. —
лишены этих недостатков. Кроме того, помимо блокады Нгре-
цепторов, в высоких дозах они уменьшают выделение медиато
ров из тучных клеток и базофилов. Комбинацию сосудосужи
вающего средства с лоратадином (псевдоэфедрин сульфат 120 мг
и лоратадин 5 мг) — клариназе — с успехом применяют (по 1
таблетке 2 раза в день) для лечения аллергических ринитов;
6) новое направление в лечении Б А — применение антагонистов
лейкотриеновых рецепторов — препарата аколата (зафиру-
лакста) по 20 мг внутрь 2 раза в день;
7) физиотерапевтические методы воздействия (массаж грудной
клетки, специальный комплекс дыхательной гимнастики). Иг-
лорефлексотерапия оказывает благоприятный эффект в ком
плексной терапии БА.
▲ Симптоматическая терапия. При лечении Б А применяют: 1) корректоры иммунных нарушений — тималин, рибомунил, бронхомунал — назначают больным со склонностью к рецидивирующим инфекционным процессам органов дыхания, трудно поддающимся антибактериальной терапии;
2) экстракорпоральные методы — плазмаферез и гемосорбция,
эффективные у больных атопической формой БА с широким
спектром аллергенов при аутоиммунной Б А;
3) психотропные и седативные средства (седуксен, реланиум и
пр.), психотерапия — при выраженных невротических реак
циях у больных БА;
4) противокашлевые препараты (тусупрекс, бромгексин, либек-
син) — при упорном кашле; при сухом надсадном кашле реко
мендуются кодеин, дионин, стоптуссин.
Лечение больного БА в фазу ремиссии включает:
устранение контакта с аллергеном, исключение воздействия раздражителей слизистой оболочки бронхов;
специфическую гипосенсибилизацию (проводится при установленном аллергене);
неспецифическую гипосенсибилизацию (лечение гистаглобулином);
санацию очагов инфекции (как правило, оперативную);
бронхолитические препараты в подобранных ранее дозах;
поддерживающие дозы интала (при его эффективности) или кетоти-фена;
кортикостероиды в аэрозоле;
постоянные занятия ЛФК и другие физиотерапевтические процедуры;
санаторно-курортное лечение (Южный берег Крыма, курорты с горным морским воздухом).
Обучение пациентов в программе лечения БА является одной из главных задач. Цель его — научить больного жить с бронхиальной астмой, широко используя «партнерство» врача и больного в лечении заболевания. Пациенты, проходя занятия в «астмашколе», увеличивают объем знаний о сущности патологии, принципах лечения и самоконтроля. Закрепляются знания в процессе индивидуального общения врача и больного.
Прогноз.Прогноз при БА различный в зависимости от клинико-пато-генетического варианта (при атопической БА он более благоприятный, чем при инфекционнозависимой), тяжести и характера течения, эффективности терапии.
Все больные БА должны постоянно находиться под наблюдением как терапевта, так и врача-аллерголога.
Профилактика.Первичная профилактика БА состоит как в лечении больных в состоянии предастмы, так и в выявлении у практически здоровых лиц с отягощенной наследственностью биологических дефектов, представляющих угрозу возникновения Б А (повышенная чувствительность к ацетилхолину и др.).
Методы первичной профилактики должны включать устранение из окружающей больных среды потенциально опасных аллергенов, ирритан-тов и других факторов, которые могут привести к развитию болезни (ги-поаллергенная диета, запрещение курения, прекращение контакта с производственными вредностями, занятия физкультурой и пр.).
При лечении больных в состоянии предастмы необходимо санировать очаги инфекции, проводить терапию аллергической риносинусопатии,
применять различные методы немедикаментозного лечения, включая игло-и психотерапию, ЛФК, баротерапию, санаторно-курортное лечение. Показано проведение специфической (при выявлении аллергена) и неспецифической гипосенсибилизации.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Да какие ж вы математики, если запаролиться нормально не можете. 8224 — 

195.133.146.119 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
 составляет 70%.
составляет 70%.
