ГИПОСЕНСИБИЛИЗАЦИЯ (греч, hypo- + сенсибилизация) — 1) снижение чувствительности организма к аллергену; 2) комплекс профилактических мероприятий, понижающих чувствительность организма к аллергену путем предупреждения развития или торможения иммунол, механизмов сенсибилизации.
В зависимости от применяемых средств различают специфическую и неспецифическую Г. Термин «десенсибилизация (специфическая и неспецифическая)» употреблять не рекомендуется, т. к. полного исчезновения чувствительности организма к аллергену практически не наступает.
Специфическая гипосенсибилизация — снижение чувствительности организма к аллергену путем введения больному экстракта того аллергена, к к-рому имеется повышенная чувствительность. Специфическую Г. проводят при бронхиальной астме, крапивнице, поллинозе, аллергической риносинусопатии и других аллергических реакциях. Этот метод был впервые предложен Нуном (L. Noon) в 1911 г. для лечения поллиноза, а 10 лет спустя впервые применен Каулфилдом (V. Caulfield) при бронхиальной астме.
Механизм специфической Г. лучше всего изучен при поллинозе (см.). Большинство исследователей считает, что при парентеральном введении аллергенов в организме больного образуются блокирующие (защитные) антитела, открытые Р. Куком в 30-х гг. Эти антитела обладают большим сродством к специфическим аллергенам, чем реагины — кожносенсибилизирующие антитела, ответственные за развитие аллергической реакции немедленного типа (см. Антитела, аллергические антитела).
При попадании специфических аллергенов в организм через дыхательные пути (напр., при поллинозе, бронхиальной астме) антитела «блокируют» их, и т. о. предотвращается развитие аллергической реакции. Снижение же титров реагинов наступает только после длительной (в течение нескольких лет) специфической Г. Ю. А. Самушия и С. А. Дахиль (1971) при специфической Г., проведенной 102 больным поллинозом, выявили блокирующие антитела при отличном клин, эффекте в 80% случаев, при хорошем — в 76%, удовлетворительном — в 33% и при отсутствии клин, эффекта — только в 25 %. Они отметили также четкую зависимость между степенью снижения титра реагинов и длительностью специфической Г. Такие же закономерности в отношении титров общих и специфических IgE отметили с помощью радиоаллергосорбентного метода (см.) Анфоссо-Капра, Вервлоэ (F. Anfosso-Capra, D. Vervloet, 1974) и др.
Т. о., специфической Г. при аллергических заболеваниях можно достигнуть только полного или частичного клин, эффекта, а прямые и непрямые тесты со специфическим аллергеном остаются положительными, но в меньших титрах. Механизм специфической Г. при атопической форме бронхиальной астмы и других атопических болезнях (см. Атопия), по-видимому, тот же, что и при поллинозе; механизм специфической Г. бактериальными аллергенами еще недостаточно изучен.
Специфическая Г. проводится только врачами-аллергологами после тщательной специфической диагностики аллергического заболевания (аллергологический анамнез, кожные, провокационные тесты и тесты in vitro с неинфекционными и инфекционными аллергенами). Она показана во всех случаях, когда невозможно прекратить контакт с выявленным аллергеном: при аллергии к домашней пыли, пыльце растений, бактериальной аллергии; больным , имеющим в анамнезе анафилактические реакции на укусы пчел и ос,— как единственный эффективный метод профилактики анафилактического шока; при лекарственной аллергии — только в тех сравнительно редких случаях, когда препарат, вызывающий аллергию, жизненно необходим больному (напр., инсулин при сахарном диабете); при пищевой аллергии — когда исключение пищевого аллергена (напр., коровьего молока у детей) крайне затруднительно. При эпидермальной аллергии специфическая Г. показана только в тех случаях, когда прекращение контакта с животными связано со сменой профессии больного (зоотехникам, ветеринарам, лаборантам с большим стажем работы).
Специфическую Г. можно сочетать с применением антигистаминных препаратов, динатрия хромогликата (интал), бронхолитиков, седативных средств. При этом не рекомендуется применение препаратов глюкокортикоидных гормонов, а проведение профилактических прививок против инфекционных заболеваний возможно только в исключительных случаях.
Специфическую Г. при атопических заболеваниях (поллинозе, атопической бронхиальной астме, аллергической риносинусопатии и крапивнице) проводят в нашей стране отечественными стандартными пыльцевыми, эпидермальными, пылевыми и пищевыми аллергенами (серийного производства), содержащими от 10 000 до 20 000 PNU аллергена в 1 мл препарата. Больным с анафилактическими реакциями на укусы насекомых лечение проводят аллергенами, приготовленными из ос и пчел по специальной методике (см. Аллергены, как препараты). При аллергии к инсулину специфическую Г. проводят подкожными инъекциями разведений этого препарата. Аллергены вводят, как правило, подкожно в возрастающих дозах и концентрациях. Начальную концентрацию аллергена при поллинозе и других атопических болезнях определяют путем внутрикожного аллергометрического титрования (см.) ряда десятикратных его разведений (10 -7 , 10 -6 и т. д.). Начать лечение следует с той концентрации аллергена, к-рая первая вызвала слабоположительную (+) внутрикожную реакцию немедленного типа.
В зависимости от этиологии атопического заболевания проводят предсезонную, круглогодичную и сезонную специфическую Г. перечисленными выше аллергенами.
Предсезонную Г. часто применяют при поллинозе и всегда при аллергических реакциях на укусы насекомых. Г. можно начинать сразу после исчезновения из окружающей среды специфических аллергенов (напр., пыльцы растений), но не позже чем за 2 мес. до периода их появления. Иногда предсезонную Г. поллиноза проводят путем эндоназального введения специфического аллергена в возрастающих концентрациях. Вортманн (F. Wortmann, 1969) при поллинозе у детей получил хороший эффект при назначении per os пчелиного меда и различных ароматических сахаров, содержащих 10% сухой пыльцы.
Круглогодичную специфическую Г. применяют часто при пылевой бронхиальной астме. Дважды в неделю делают инъекцию пылевых аллергенов до достижения наиболее оптимальной для каждого больного дозы, а затем переходят на поддерживающую терапию, при к-рой эту дозу аллергена вводят 1 раз в 1—2 нед. в течение 3—5 лет. Иногда круглогодичную специфическую Г. проводят при поллинозе, причем специфический пыльцевой аллерген вводят и в период цветения растений, но в меньшей дозе.
Реже при пылевой бронхиальной астме и поллинозе проводят лечение в аллергологическом стационаре ускоренным методом, когда инъекции пылевых или пыльцевых аллергенов делают ежедневно (или дважды в день) до достижения наиболее оптимальной и хорошо переносимой для каждого больного дозы (в течение 3—4 нед.) с перерывом в 5—6 мес.
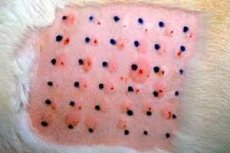
Сезонную Г. иногда проводят при поллинозе в период цветения растений и клин, проявлений болезни. Специфический пыльцевой аллерген в небольших концентрациях и дозах вводят больному, напр, методом «кожных квадратов», предложенным в 1959 г. Бламутье и Гибером (Р. Blamoutier, L. Guibert): на коже внутренней поверхности предплечья делают скарификационную сетку длиной 10 см и шириной 5 см, интервал между скарификационными линиями 5 мм; на эту сетку наносят 0,2 мл специфического аллергена. Сезонная Г. менее эффективна, чем предсезонная и круглогодичная.
Метод специфической Г. стандартными аллергенами при поллинозе, атопической бронхиальной астме и анафилактических реакциях на укусы насекомых дает высокий клин, эффект (75—90%), однако недостатком его является длительность лечения и большое число инъекций. Для сокращения числа инъекций аллергенов при специфической Г. Вольфромм (R. Wolfromm, 1959) с соавт, предложил одновременно со специфическим стандартным аллергеном вводить 0,1 мл 0,2% геля гидрата окиси алюминия с целью создания в организме депо аллергена. Инъекций делают 1 раз в неделю по укороченной схеме (0,2—0,8 мл аллергена в каждом разведении вместо 0,1—0,2—0,4—0,8 мл). Число инъекций при специфической Г. можно уменьшить также путем применения пиридиново-гидрокарбонатных аллергенов, адсорбированных гидратом окиси алюминия. Этот препарат под названием аллпирал предложен Фуксом и Страуссом (A. Fuchs, М. В. Strauss) в 1959 г. Для сокращения числа инъекций аллергенов при поллинозе за рубежом используют также аллергены, депонированные при помощи тирозина.
Специфическую Г. при инфекционно-аллергической форме бронхиальной астмы, предастме и крапивнице (бактериального происхождения) проводят в нашей стране при помощи стандартных микробных аллергенов.
При инфекционно-аллергической бронхиальной астме и предастме применяют также препараты, содержащие не только микробные клетки, но и их экзопродукты — токсины, ферменты. В Научно-исследовательской аллергологической лаборатории (НИАЛ) АМН СССР разработаны методы специфической диагностики и специфической Г. при инфекционно-аллергической форме бронхиальной астмы и предастме микробными вакцинами, приготовленными на кровяных пластинках, покрытых целлофановыми дисками (аутомоно- и гетеромоновакцины). У больного берут мазки со слизистой оболочки носа, зева, бронхов (при бронхоскопии). Из каждого высеянного от больного микробного штамма (патогенного, условно патогенного, сапрофитного) готовят аутомоновакцину, содержащую 1 млрд. микробных тел в 1 мл. Для специфической Г. используют набор аутомоно- или гетеромоновакцин, вызвавших положительную реакцию на внутрикожные и ингаляционные провокационные тесты (обычно замедленного типа). Начальную концентрацию стандартных микробных аллергенов определяют путем аллергометрического внутрикожного титрования специфического аллергена, начальную концентрацию микробных ауто- и гетеровакцин, приготовленных на целлофановых дисках, определяют путем внутрикожного титрования моновакцин, содержащих различные количества микробных тел (1000, 10 000, 100 000 и т. д.) в 1 мл препарата. Начинают лечение с введения 0,1 мл препарата той концентрации, к-рая вызвала слабоположительную (+) или сомнительную (+) реакцию замедленного типа при внутрикожном введении. Стандартные микробные аллергены и вакцины чаще вводят подкожно, реже внутрикожно. Инъекции делают дважды в неделю в возрастающих дозах и концентрациях до достижения оптимальной для каждого больного дозы, после чего переходят на поддерживающую терапию, при к-рой одну и ту же дозу препарата вводят еженедельно (или 1 раз в 10 дней) на протяжении 3—5 лет.
Осложнения. На месте введения аллергена или вакцины может возникнуть местная реакция в виде зудящего болезненного инфильтрата. В таких случаях интервал между инъекциями удлиняют и повторно несколько раз вводят ту дозу аллергена (или вакцины), к-рая не вызывала выраженной местной реакции.
При быстром повышении дозы аллергена (или вакцины), сокращении интервала между инъекциями, а также введении большей дозы аллергена возможны системные реакции (крапивница, аллергический конъюнктивит, ринит, приступ бронхиальной астмы). По данным НИАЛ АМН СССР, при специфической Г. микробными вакцинами больных инфекционно-аллергической формой бронхиальной астмы системные реакции (чаще всего приступы удушья различной степени) отмечены у 38% больных. Иногда возникают обострения в очагах хрон, инфекции. В этих случаях следует прекратить вакцинотерапию и провести соответствующее лечение (антибактериальную терапию). Системные реакции при лечении атопических заболеваний развиваются обычно в течение 40 мин. после инъекции аллергена и быстро проходят после применения антигистаминных препаратов или подкожной инъекции 0,1% р-ра адреналина. Если больному своевременно не оказана помощь, у него может развиться анафилактический шок (см.). Поэтому в течение 40 мин. после инъекции специфического аллергена больной должен находиться под наблюдением врача. Причинами анафилактического шока могут быть также введение аллергена в дозе и концентрации, превышающих предписанные врачом; попадание аллергена непосредственно в сосуд (необходимо после введения иглы под кожу потянуть поршень шприца на себя; если в шприце появится кровь, нужно вынуть иглу и сделать инъекцию в другое место); повышение дозы аллергена больному, у к-рого после введения предыдущей, меньшей, дозы отмечалась крапивница, зуд век, кашель, насморк.
При первых же симптомах анафилактического шока больному необходимо срочно ввести подкожно адреналин, кордиамин, кофеин, антигистаминные препараты, глюкокортикоидные гормоны, сердечные гликозиды, эуфиллин (внутривенно), кислород; при показаниях проводят реанимационные мероприятия (см. Реанимация). После выведения из анафилактического шока каждый больной подлежит госпитализации для наблюдения, обследования и соответствующей терапии (сердечно-сосудистыми, антигистаминными и глюкокортикоидными препаратами с целью профилактики поздних осложнений анафилактического шока — аллергического миокардита, нефрита, гепатита и др.).
При специфической Г. микробными вакцинами и бактериальными аллергенами анафилактический шок не наблюдается.
Противопоказания: обострение основного заболевания, тяжелые органические изменения легких при бронхиальной астме с хрон, легочной и легочно-сердечной недостаточностью, длительное лечение глюкокортикоидными препаратами, беременность, а также следующие заболевания; ревматизм в активной фазе, туберкулез любой локализации в активной фазе и другие хрон, инфекционные заболевания в стадии обострения, злокачественные новообразования , декомпенсированные сердечно-сосудистые заболевания, заболевания крови, декомпенсированный сахарный диабет и другие заболевания эндокринной системы (за исключением больных с аллергией к инсулину), коллагенозы, психические заболевания в фазе обострения, язвенная болезнь желудка и двенадцатиперстной кишки в фазе обострения, острые инфекционные заболевания.
Неспецифическая гипосенсибилизация — снижение чувствительности организма к аллергену под влиянием некоторых лекарственных препаратов, отдельных видов физиотерапевтического и курортного лечения. Применяют ее в тех случаях, когда специфическая Г. невозможна или недостаточно эффективна, а также при сенсибилизации к веществам невыясненной природы. Нередко неспецифическую Г. применяют в сочетании со специфической. Неспецифическая Г. — один из видов лечения аллергических заболеваний, направленный на предупреждение развития или торможение иммунол, механизмов сенсибилизации (поэтому применение антигистаминных препаратов, динатрия хромогликата, стимуляторов бета-адренергических рецепторов и др. не является неспецифической Г.).
Курортные факторы оказывают выраженное гипосенсибилизирующее действие. Под их влиянием снижается степень специфической чувствительности к аллергену (по результатам аллергометрического титрования после пребывания больных на Кисловодском курорте); сочетание курортных факторов со специфической Г. дает более выраженный клинический эффект.
Гипосенсибилизирующим действием обладает переменное и постоянное магнитное поле строго определенных параметров. Препараты глюкокортикоидных гормонов в небольших дозах повышают пороговую дозу аллергена, к-рая может «запустить» иммунол, механизмы сенсибилизации. В больших дозах они подавляют развитие иммунной фазы, тормозя фагоцитоз и переваривание аллергена в фагоцитах, разрушая малые лимфоциты и угнетая синтез антител. Глюкокортикоиды участвуют также в торможении патохим. и патофизиол, фаз аллергического процесса.
К группе гипосенсибилизирующих средств можно отнести иммунодепрессанты (см. Иммунодепрессивные вещества), однако применение их ограничено строго определенными рамками. Гипосенсибилизирующим эффектом обладает также ряд других лечебных средств — плазма крови, препараты кальция, гипосульфит натрия и др., но точный механизм их действия остается еще недостаточно ясным.
Библиография: Аллергические заболевания У детей, под ред. М. Я. Студеникина и Т. С. Соколовой, с. 331, М., 1971; Арто-масова А. В. Клиника, диагностика и терапия аллергических реакций на ужа-ления пчел и ос, Клин, мед., т. 51, № 5, с. 61, 1973, библиогр.; Беклемишев Н. Д. идр. Поллинозы (сенные катары), с. 142, Алма-Ата, 1974; Гудкова Р. Г. О специфической десенсибилизирующей терапии бронхиальной астмы, Клин, мед., т. 45, № 5, с. 55, 1967, библиогр.; С а м у ш и я Ю. А. и Д а-х и л ь С. А. О роли блокирующих антител при специфической гипосенсибилизации поллинозов, в кн.: Пробл, аллергол., под ред. А. Д. Адо и А. А. Подколзина, с. 184, М., 1971; Сидоренко Б. Н. Специфическая десенсибилизация при бронхиальной астме инфекционной природы, в кн.: Бронхиальная астма, под ред. А. Д. Адо и П. К. Булатова, с. 274, М., 1969; A n f о s s о-С a p r a F. а. о. Evolution of reaginic antibodies in specific hyposensitization, Acta allerg. (Kbh.), v. 29r p. 79, 1974; Blamoutier P., Blamoutier J. et Guibert L. Traitement de la pollinose avec extraits de pollens par la m£thode des quadrillages cutanes, Presse m6d., t. 67, p. 2299, 1959; Fuchs A. M. a. Strauss М. B. The clinical evaluation and the preparation and standartization of suspensions of a new water-insoluble whole ragweed pollen complex, J. Allergy, v. 30, p. 66, 1959; M i 1-ler А. С. M. a. Tees E. C. A metabolizable adjuvant, clinical trial of grass pollen-tyrosine adsorbate, Clin. Allergy, v. 4, p. 49, 1974; W o 1 f r o m m R. e. a. D6sen-sibilisation par association extemporan£e d’hydroxyde d’alumine aux allerg£nes (allergfcnes h action retard), Acta allerg. 6sensibilisation sp6cifique des pollinoses par voie orale chez les enfants k 1’aide de pollen en poudre, Rev. franc. Allerg., JMs 3, p. 195, 1969.
Ю. А. Порошина, А. И. Остроумов; B. И. Пыцкий (гипосенсибилизация неспецифическая).
источник
Сегодня одним из наиболее распространенных заболеваний являются различного рода аллергии. Для примера, аллергическим ринитом страдает примерно 10-25% населения, а с аллергическими заболевания глаз сталкивается 22% населения.
Сложность этой проблемы значительна, так людям, страдающим аллергией, нередко приходится мириться со значительным уменьшением комфорта жизни. На помощь пришла иммунотерапия, благодаря которой борьба с аллергией стала более эффективной.
Согласно недавно опубликованным данных, более 35% населения европейских стран имеют симптомы аллергических заболеваний. Результаты эпидемиологических исследований показали, что аллергические болезни различных клинических проявлений возникают у 30-40% населения России.
Аллергический ринит, в настоящее время, принадлежит к числу самых распространенных групп заболеваний среди указанных в исследовании (около 24% населения в возрасте от 6 до 44 лет).
Большинство аллергических заболеваний имеют хронический характер, что требует систематичности и последовательности в лечении.
Иммунная система, в первую очередь, нужна для сохранения целостности организма путем его защиты от негативного воздействия внешней среды, т.е. от бактерий, вирусов, грибов, токсинов и многих других факторов.
Несмотря на то, что путей проникновения чужеродных элементов в организм много, основное значение имеют: оральные, дыхание и кожа, потому что здесь имеет место наибольшее взаимодействие с различными патогенами.
Первая линия обороны – это элементы неспецифического иммунного ответа, такие как ферменты желудочно-кишечного тракта и дыхательных путей, желудочная кислота, кислые выделения из влагалища, комменсал бактерий желудочно-кишечного тракта и другие.
Среди механизмов неспецифического иммунитета активностью отличается фагоцитоз. Клетки фагоциты (макрофаги и нейтрофилы) в качестве первого примитивного удара поглощают проникающих внутрь организма бактерий и вирусов.
Вторую, основную часть иммунной системы, составляют элементы, ответственные за специфический ответ, направленный конкретно против данного антигена. Клетки фагоциты передают накопленную информацию о структуре антигена Т-лимфоцитам, которые имеют способность распознавать и различать собственные антигены и чужие.
Затем идет передача информации об антигене в В-лимфоциты. Эти клетки ответственны за гуморальный и клеточный иммунитет, способность к выработке антител, направленных против распознанного антигена. Произведенные антитела обладают способностью связывать чужеродный антиген и выводить его из кровообращения.
Гиперчувствительность является понятием более широким, чем аллергия, это означает, что теоретически у здоровых людей с повышенной чувствительностью могут возникнуть клинические проявления.
Повышенная чувствительность может иметь аллергический и неаллергический характер. Аллергией называется альтернативная, неправильная реакция, в результате которой происходит выработка антител класса IgE.
Это полигенное явление обусловленное генетическим дефектом. По наследству передается склонность к чрезмерной выработке IgE. Наследуется, прежде всего, предрасположенность к аллергии, а воздействия окружающей среды имеют решающее значение в запуске развития болезни.
К IgE-зависимой аллергии относят: нейродермит, (астма, аллергический ринит и конъюнктивит, атопический дерматит, некоторые крапивницы и отек Квинке) и обобщенная анафилактическая реакция при укусе насекомого и после инъекции пенициллина.
Первый контакт с аллергеном, которым может быть практически любое вещество (например, пыльца растений, пылевых клещей, шерсть домашних животных, плесень) приводит к выработке антител класса IgE, которые производят тучные клетки (мастоциты). Таким образом, развивается аллергия организма на определенный аллерген, что при повторной с ним встрече приведет каскадной реакции.
Происходит передача сигнала внутрь мастоцитов и высвобождение медиаторов аллергии, прежде всего, гистамина, лейкотриенов и простагландинов, которые стимулируют сокращение гладких мышц бронхов, приводят к набуханию слизистой оболочки и повышению проницаемости клеток сосудов.
К месту аллергической реакции начинают поступать эозинофилы, которые представляют собой основу хронического аллергического воспаления. Именно они обуславливают тяжесть течения заболевания и появление осложнений.
Постановка врачом диагноза аллергия всегда должно повлечь за собой соответствующие последствия. Прежде всего, речь идет о необходимости изменения стиля жизни, а также применение терапевтической процедуры.
Первой и основной стратегией поведения является, по мере возможности, избегание контакта с аллергеном. Это, конечно, не всегда возможно. В этом случае медикаментозное лечение, заключающееся в облегчении боли, связанной, например, с ринитом, воспалением конъюнктивы или бронхиальной астмой.
Существует также и третий вариант, но его использование возможно не в каждом случае аллергии. Это специфическая иммунотерапия, то есть десенсибилизация.
Специфическая иммунотерапия, называемая в просторечии десенсибилизацией аллергии, – это метод, заключающийся в многократном приеме постепенно увеличивающихся доз вакцины для стимуляции иммунной толерантности и облегчения симптомов, связанных с естественной экспозицией к аллергенам. Чтобы понять это явление, нужно ознакомиться с основами иммунологии и механизмами возникновения аллергии.
Основы иммунотерапии и десенсибилизации были созданы на основании работ британских ученых: Леонардо Ноона (1877-1913) и Джона Фримана (1877-1962) в 1911-1914 годах.
Считается, что первые попытки иммунотерапии были проведены в 1911 году и касались аллергического ринита. Они состояли из инъекций небольших, постепенно возрастающих объемов вещества, на которые у пациента была аллергия. Предложенные тогда методы актуальны и применяются до сих пор.
Механизм десенсибилизации до сих пор до конца не понятен. Факт состоит в том, что при иммунотерапии происходит уменьшение концентрации специфических антител IgE, ответственных за аллергическую реакцию.
Это подтверждается путем проведения кожных тестов. Особенно важны регуляторные изменения, T-лимфоциты (CD4+ CD25+), которые уменьшают распространение и производство цитокинов, изменяют функцию клеток, производящих антиген и специфически подавляют выработку IgE.
Кроме того, возникает изменение профиля цитокинов. Результатом является снижение активности эффекторных клеток и уменьшение воспаления. Подводя итоги, можно сказать, что десенсибилизация моделирует аллергическое воспаление, вынуждая организм адаптироваться, результатом этого является улучшение клинического состояния больного.
При десенсибилизации вакцину могут вводить разными путями: внутрикожные инъекции, пероральный прием, подъязычный и в форме ингаляций.
Было показано, что эффективность вакцины варьируется в зависимости от пути введения. Предпочтительна подача вакцины в виде инъекций, но и другие пути введения, особенно в педиатрии, где преобладает пероральная форма, также широко используется.
Несмотря на то, что метод специфической иммунотерапии имеет много преимуществ, он связан с рисками, поэтому его выполнению должно предшествовать тщательный анализ клинической ситуации, изучение медицинской документации и проведение кожных тестов.
Безопасность десенсибилизации зависит от правильного подбора вакцины и ее правильного использования. Ввод аллергена происходит в условиях, позволяющих получить срочную медицинскую помощь в случае возникновения анафилактической реакции.
Проведение десенсибилизации при астме возможно не у всех пациентов, особенно если одновременно существуют определенные заболевания или одновременно принимаются некоторые лекарства. У больных с повышенным риском, т. е. с сугубо положительный кожными тестами, подтвержденных высоким содержанием IgE, необходимо соблюдать особую осторожность.
В таких случаях вы должны также принимать во внимание отказ от проведения иммунотерапии. Кроме того, повышенный риск развития системной реакции происходит в случае ввода слишком большой дозы аллергена или слишком короткого периода времени между дозами, использования ускоренной схемы иммунотерапии, введения вакцины из новой упаковки и слишком часто во время периода пыльцеобразования растений.
В случае подкожного введения, аллерген может привести к местной реакции: отек, покраснение, боль и зуд в месте введения. Такие симптомы, не требуют конкретного поведения, кроме, чтобы рассмотреть уменьшение дозы аллергена.
Осложнение, которого больше всего боятся врачи – системная реакция на указанный аллерген. Ее форма характеризуется появлением следующих заболеваний: ринит, крапивница, отек Квинке, обострение симптомов астмы. В половине случаев эта реакция происходит в течение первых 30 минут, в остальных случаях – в течение суток после введения. Осуществляется медикаментозное лечение, специфическое для такого типа реакции.
Симптомы опасные для жизни, это: отек гортани, тяжелый приступ астмы не реагирующей на лечение и анафилактический шок. Такие состояния случаются примерно один сразу на 3000 инъекций и почти всегда проявляются в течение 30 минут после введения аллергена. Разработан подробный алгоритм проведения терапии в таких случаях. Риск смерти при иммунотерапии является крайне низким и составляет примерно 1 на 2,5 миллиона инъекций.
Правильное применение специфической иммунотерапии и соблюдение правил её проведения, несомненно, защитит от большинства угроз десенсибилизации.
Десенсибилизация астмы является наиболее отработанной процедурой лечения аллергических заболеваний. Эта терапия направлена на выработку толерантности в отношении наиболее распространенных аллергенов, ответственных за возникновение симптомов.
Кроме того, происходит восстановление нормального отношения между лимфоцитами Th1, которые работают провоспалительно, и Th2 работающих проаллергично. Благодаря этим механизмам не только происходит облегчения симптомов, но также замедляется прогрессирование заболевания. Специфическая иммунотерапия, таким образом, является эффективным способ лечения аллергии.
Эффективность специфической иммунотерапии зависит от выполнения условий, квалификации, соответствующего подбора вакцины, а также правильного применения схемы в ходе всей иммунотерапии.
Имейте в виду, что проведение десенсибилизации возможно не у всех пациентов, особенно если одновременно у них существуют определенные заболевания или они принимают некоторые лекарства.
источник
Иммунотерапия (специфическая гипосенсибилизация)
Иммунотерапия – введение аллергенов (аллергена) больному аллергией путем инъекции с целью снижения гиперчувствительности организма к этому виду аллергена. При данном методе лечения причиннозначимый аллерген вводится сначала в очень малых дозах, а затем вводимые дозы постепенно повышаются. В результате к концу курса лечения отмечается уменьшение проявлений аллергии у больного при встрече с аллергенами. Таким образом, заболевание протекает легче. Иногда наступает выздоровление, но чаще все-таки полной десенсибилизации не происходит.
Из практики известно, что наиболее эффективен этот метод при аллергии к пыльце растений, к домашней пыли, к шерсти животных и ужалению пчелами и осами. Лечение специфической гипосенсибилизацией больных с аллергией проводят в тех случаях, когда невозможно полностью исключить причиннозначимый аллерген из окружающей среды и контакт больного с ним неизбежен (пыльца растений, домашняя пыль и так далее). Если же удалить аллерген из окружения больного возможно (например, пищевые продукты, домашние животные и т. д.), то наилучший лечебный эффект дает именно метод исключения аллергена. Специальные исследования показали, что в случаях дыхательной аллергии метод иммунотерапии эффективен в среднем у 30% пациентов.
Но, несмотря на эти оптимистичные цифры, курс иммунотерапии все-таки имеет ряд негативных моментов. Во-первых, он является достаточно дорогостоящим, во-вторых, растянут во времени, а самое главное – чреват местными или общими осложнениями (крапивница, приступ астмы, анафилактический шок и т. д.). Поэтому метод специфической гипосенсибилизации рекомендуется лишь при тяжелых формах аллергии.
К таковым можно отнести затяжные (от нескольких недель до нескольких месяцев) приступы аллергии; солидный «стаж» аллергического заболевания (не менее 2 лет); неэффективность всех остальных методов лечения. Таким образом, и показания, и схемы проведения иммунотерапии являются строго индивидуальными.
Иммунотерапия противопоказана в следующих случаях:
– при обострении основного заболевания;
– при активном туберкулезном процессе;
– при коллагенозах (заболевания соединительной ткани), заболеваниях печени, почек и других органов;
– при ОРВИ и других острых заболеваниях;
– при психических заболеваниях;
– при одновременном проведении профилактических прививок;
– при ревматизме, беременности, язвенной болезни желудка и двенадцатиперстной кишки, онкологических заболеваниях.
Важна выраженность местной кожной реакции: покраснение и припухлость кожи диаметром более 2—3 см являются сигналом возможного развития общей реакции. В соответствии с этим лечащим врачом назначается лечение. Иммунотерапия может проводиться круглогодично (например, при повышенной чувствительности к домашней пыли) или предсезонно (например, зимой и осенью, перед периодом цветения соответствующих растений). При наличии положительного эффекта лечение проводят на протяжении не менее 2—4 лет (сроки, в течение которых наблюдаются явные признаки выздоровления). При невыдерживании данных сроков человек вновь рискует столкнуться с проявлениями аллергии. Кроме вышеописанного классического применения инъекций водных растворов аллергенов, в последнее время стали применяться и более удобные методы. Их смысл заключается в использовании препаратов длительного действия (алпирал, цинтанал), а кратность инъекций составляет 1 раз в неделю и 1 раз в месяц. Как правило, эти методы применяют при пыльцевой аллергии у взрослых. Наряду с этим методом используется ингаляционный метод иммунотерапии, а также метод чрескожного электрофореза. Как правило, при разумной оценке показаний и противопоказаний специфическая гипосенсибилизация протекает без осложнений. Но иногда возникают местные и общие реакции, требующие соответствующих лечебных мероприятий. Именно поэтому человек, получивший инъекцию аллергена, должен в течение 1 ч наблюдаться медицинским персоналом. Сам больной должен быть хорошо информирован о возможных последствиях. Всем людям, получающим иммунотерапию, на руки выдается специальная памятка.
Во время проведения данного вида лечения нельзя проводить профилактические прививки, необходимо исключить физические и эмоциональные перегрузки, переохлаждения и перегревания.
Физиотерапевтическое и климатическое лечение
В лечении аллергических заболеваний широко используют и физиотерапевтические, и климатические методы лечения. Это аэрозольтерапия, электрофорез лекарственных веществ, ультрафиолетовое облучение, ультразвук и т. д. Применяются эти методы повсеместно: в стационарах, на дому, в поликлиниках, в санаториях, но всегда по назначению врача. Аэрозольтерапию применяют, в частности, при лечении бронхиальной астмы в приступном и межприступном периодах. Осуществляют распыление соответствующих лекарственных средств при помощи различных ингаляторов. Преимуществом аэрозольтерапии является то, что лекарственные препараты вводятся непосредственно в органы дыхания. В результате человек получает нужную концентрацию их в дыхательных путях. В комплексной терапии бронхиальной астмы широко применяют электрофорез кальция, гистамина, адреналина, эуфиллина и других лекарственных препаратов. В комплексе лечения приступа бронхиальной астмы, особенно в домашних условиях, могут быть применены горячие ручные и ножные ванны, вызывающие спазмолитическое действие. Температура воды при этой процедуре постепенно повышается с 38 °С до 40—42 °С. Сама процедура длится от 7 до 15 мин в зависимости от возраста и индивидуальной чувствительности. Индуктотермия надпочечников (метод электротерапии) показана для стимуляции ослабленной функции коры надпочечников, особенно в результате длительной гормональной терапии. В осенне-зимнее время, как правило, проводят общее ультрафиолетовое облучение с целью повышения защитных сил организма.
При лечении аллергодерматозов ультрафиолетовое облучение используют наиболее часто, поскольку оно оказывает благотворное влияние на состояние многих систем, в том числе нервной и иммунной. Нормализующим влиянием на центральную нервную систему обладает электросон (воздействие на головной мозг слабого электрического тока). Используется он при лечении экземы, нейродермитов.
При той же патологии успешно применяют и ультразвуковую терапию. Противозудным действием, успокаивающим влиянием на центральную нервную систему, местным противовоспалительным действием обладают теплые ванны (при нейродермите, экземе) с добавлением крахмала, танина, отвара дубовой коры, ромашки, череды, зверобоя. Температура воды – около 37—38 °С, продолжительность – 8—10 мин, на курс – 10—12 ванн, ежедневно или через день.
Широко применяются при лечении нейродермита озокеритовые и парафиновые аппликации. В комплексе оздоравливающего лечения хронических очагов инфекции, при аллергии успешно применяют УВЧ или аппарат «Луч-2» на область придаточных пазух. На курс назначают 8—10 процедур ежедневно или через день. Также применяют УВЧ, СВЧ, ультразвук. В комплексе лечебных мероприятий аллергических заболеваний важна роль климатических и курортных факторов. Огромный оздоравливающий эффект дают прогулки на свежем воздухе, особенно в загородной зоне (но не в сезон цветения «аллергенных» растений). Одновременно прогулки выполняют и роль закаливающих мероприятий, что особенно важно для детей. Прогулки в прохладную и холодную погоду необходимо начинать с нескольких раз в день по 30 мин, постепенно доводя их продолжительность до нескольких часов. Полезно организовать детям с аллергией дневной и даже ночной сон на воздухе (например, на веранде).
Необходимо помнить, что у больных аллергией повышена чувствительность к охлаждению, поэтому любые закаливающие процедуры надо проводить осторожно. Чтобы закаливание было эффективным, его надо проводить постоянно. Наиболее эффективными закаливающими процедурами являются водные (обтирания, обливания, ножные ванны). Сначала температура воды не должна быть ниже 34—33 °С, а продолжительность процедуры не должна превышать 2—3 мин. Через каждые 3—4 дня температуру воды снижают на 1 °С, но не ниже 22 °С. После водной процедуры соответствующую кожную зону насухо растирают полотенцем. Купание в море или реке является еще более активным методом закаливания, так как при этом сочетается действие температуры воды, воздуха, солнечных лучей, активных движений. Лучшее время для купания на юге —с 9 до 11 ч, а в средней полосе – с 10 до 12 ч.
Процедура купания для больных с аллергией весьма индивидуальна, так как необходимо избегать переохлаждения с его нежелательными последствиями. С осторожностью должны применяться больными аллергией и солнечные ванны, чтобы избежать перегревания и вредного действия солнечной радиации. Солнечные ванны противопоказаны при повышенной нервной возбудимости, обострении кожного процесса, при фотосенсибилизации (повышенной чувствительности к солнечному облучению). Большинству страдающих аллергией рекомендуется пребывание в местной климатической зоне, в местных санаториях, где имеется должное медицинское наблюдение, рациональное питание (гипоаллергенная диета), комплексы лечебной физкультуры и физиотерапии. Но бывают ситуации, когда суровый местный климат необходимо сменить на другой, более подходящий для данного заболевания (например, Крым, Кавказ или Средняя Азия – для больного бронхиальной астмой).
Положительно влияет на здоровье больных аллергией дыхательных путей горный климат с его чистым воздухом, пониженными влажностью и давлением. Дыхание становится более продуктивным, улучшаются функции надпочечников и обмен веществ. Горные условия с успехом можно воссоздать в барокамере. Но не всегда привыкание к новым климатическим условиям протекает легко: возможно появление головных болей, нарушение сна, обострение аллергических заболеваний. Эти индивидуальные особенности необходимо учитывать при назначении курортного лечения.
На многих курортах для лечения аллергических заболеваний используют минеральные воды, различные по своему составу: морские, рапные, сероводородные, углекислые, кислородные и т. д. Применяют и грязелечение в виде местных аппликаций (щадящая методика). В Закарпатье, Грузии и Киргизии в санаториях используют метод спелеотерапии, т. е. лечение заболеваний органов дыхания, в том числе и аллергического происхождения, в бывших соляных шахтах. Оздоровительный эффект здесь оказывают аэрозоли солей, содержащиеся в воздухе данных шахт, постоянство температуры и влажности, отсутствие аллергенов. Общим противопоказанием к направлению на санаторно-курортное лечение является обострение заболевания. Санаторное лечение возможно лишь в период прекращения заболевания.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Специфическая гипосенсибилизация (или специфическая иммунотерапия) — создание устойчивости к действию аллергена, ответственного за гиперсенсибилизацию, путем профилактического введения этого аллергена в постепенно и строго индивидуально повышаемых дозах, начиная с субпороговых.

Метод специфической гипосенсибилизации (иммунотерапии) применяется при невозможности полного прекращения контакта с этиологически значимым аллергеном (например, у больных с сенсибилизацией к домашней пыли, пыльце растений, плесневым грибам, бактериальным аллергенам и т.д.).

Начинают введение аллергена с очень малой дозы (1: 1.000.000 — 0.1 мл), в дальнейшем дозу постепенно увеличивают.
- образование блокирующих антител IgG;
- уменьшение синтеза IgЕ;
- индукция Т-супрессоров;
- активация полиморфно-ядерных лейкоцитов;
- усиление фагоцитоза;
- снижение чувствительности клеток-мишеней аллергических реакций к аллергенам и медиаторам аллергии;
- развитие иммунологической толерантности;
- повышение уровня IgA в бронхиальной слизи;
- стабилизация мембран тучных клеток.
Используемые для специфической иммунотерапии аллергены бывают различного вида (водно-солевые, очищенные аллергены, активные фракции аллергенов, химические модифицированные аллергены, обладающие усиленными иммуногенными и ослабленными аллергенными свойствами, пролонгированные аллергены).
Специфическая иммунотерапия дает положительный терапевтический эффект при пыльцевой бронхиальной астме — у 70% больных, при бытовой бронхиальной астме — у 80-95% при длительности болезни менее 8 лет.
У больных пыльцевой бронхиальной астмой проводят предсезонный курс лечения.
А. Остроумов (1979) показал высокую эффективность специфической иммунотерапии с использованием очищенного аллергена из пыльцы амброзии. Очищенные аллергены лучше переносятся. С. Титова разработала технологию производства цинтанала — очищенного сорбированного пролонгированного препарата. Побочных действий у него нет, что связано с отсутствием балластных веществ.
В последние годы создаются направленные химически модифицированные лечебные аллергены:
- аллергоиды форматированные аллергены;
- толерогены — аллергены, денатурированные мочевиной.
Эти препараты вызывают стойкую супрессию IgE-антител, стимулируют образование IgG-антител. Они обладают низкой аллергогенностью и высокой иммуногенностью.
Завершается также экспериментальное изучение аллерговакцин. Аллерговакцины — это комплексы очищенных аллергенов с синтетическими полимерами носителями. Такие препараты угнетают образование аллергических реагинов (IgE-антител), но усиливают синтез блокирующих IgG-антител. (Получен комплекс из аллергена пыльцы тимофеевки и синтетического полимера полиоксидония).
В последние годы применяется новое направление специфической иммунотерапии — использование для лечения иммунных комплексов, состоящих из аллергенов (клещевых и пыльцевых) и специфических аутологичных антител. В процессе лечения происходит нарастание титра антиидиотипических иммуноглобулинов. Метод является безопасным, возможно снижение дозы вводимого аллергена.
Противопоказания к специфической иммунотерапии:
- обострение бронхиальной астмы и хронических очагов инфекции;
- обострение сопутствующих заболеваний — сахарного диабета, заболеваний почек, печени, гипертонической болезни, ИБС, токсического зоба, заболеваний крови, системных заболеваний соединительной ткани, других аллергических заболеваний;
- наличие необратимых изменений легочной ткани (эмфиземы, пневмосклероза), дыхательной или сердечной недостаточности;
- длительная терапия глюкокортикоидами;
- психические заболевания;
- онкологические заболевания;
- беременность и лактация;
- активная фаза ревматизма.

источник
Патогенетическое обоснование принципов гипосенсибилизации свидетельствует о целесообразности использования селективных методов медикаментозной и немедикаментозной коррекции, адаптированных к стадии развития аллергического процесса, т.е. к периоду обострения или ремиссии. Если организм сенсибилизирован, то встает вопрос о снятии гиперчувствительности. ГНТ и ГЗТ снимаются за счет подавления выработки иммуноглобулинов (антител) и активности сенсибилизированных лимфоцитов.
Гипосенсибилизация проводится в стадии ремиссии (латентный период сенсибилизации, который относится к иммунологической стадии). Под гипосенсибилизацией подразумевают комплекс мероприятий, направленных на снижение чувствительности к аллергену. Различают специфическую и неспецифическую гипосенсибилизацию. Специфическая гипосенсибилизация (СГ) – это снятие гиперчувствительности к определенному антигену. Неспецифическая гипосенсибилизация – это снижение чувствительности к различны антигенам-аллергенам. СГ возможна при аллергических реакциях немедленного типа, неспецифическая гипосенсибилизация проводится как при ГНТ, так и при ГЗТ. Термином гипосенсибилизация называют также состояния сниженной чувствительности организма к аллергену.
Принципы гипосенсибилизации при ГНТ. СГ возможна при устранении контакта с определенным аллергеном, так как АТ к нему постепенно элиминируются из организма. Она может также осуществляться путем преднамеренного введения экстракта того аллергена, к которому имеется повышенная чувствительность (синонимы: «иммунотерапия аллергенами», «специфическая вакцинация аллергии», «специфическая аллерговакцинация»). Существуют круглогодичные, предсезонные и сезонные варианты гипосенсибилизации.
Наилучшие результаты СГ достигаются при лечении ГНТ, в основе которых лежит IgE-опосредованная аллергическая реакция (поллиноз, крапивница, атопическая бронхиальная астма, риносинусит и др.). Механизм лечебного эффекта изучен недостаточно – его связывают с образованием блокирующих антител (IgG), которые воссоединяются с поступающим в организм аллергеном и предупреждают его контакт с IgE. Вполне вероятно также, что в результате проведения СГ изменяется характер иммунологической стадии аллергической реакции первого типа, что выражается в переключении иммунного ответа с Th2-зависимого типа на Th1 зависимый (уменьшается образование IgE и увеличивается синтез IgG). СГ проводится в тех случаях, когда невозможно устранить контакт больного с аллергеном (пыльца растений, домашняя пыль, бактерии, грибы), когда нельзя прервать лечение (инсулином при сахарном диабете), если нельзя исключить из рациона питания тот или иной продукт (коровье молоко у детей), если нет возможности сменить работу (ветеринары и зоотехники при аллергии к шерсти, компонентам эпидермиса животных). При инсектной аллергии – это единственный эффективный способ лечения и профилактики анафилактического шока. Возможно появление осложнений СГ в виде местных аллергических реакций в шоковом органе, или системных реакций (т.е. анафилактического шока). В таких случаях необходимо прервать СГ, затем начать с меньшей дозы аллергена и использовать щадящую (пролонгированную) схему СГ.
Противопоказаниями к проведению СГ являются обострение основного заболевания, длительное лечение глюкокортикоидами, органические изменения в легких при бронхиальной астме, осложнение основного заболевания инфекционным процессом с гнойным воспалением (ринит, бронхит, синусит, бронхоэктазы), ревматизм и туберкулез в активной фазе, злокачественные новообразования, недостаточность кровообращения II-III стадии, язвенная болезнь желудка и двенадцатиперстной кишки.
Снижение чувствительности к БАВ можно достичь введением гистамина в малых дозах или либераторов гистамина.
Частным примером СГ является дробное введение антитоксических сывороток (по Безредке) того аллергена, который вызвал сенсибилизацию. Оно рассчитано на постепенное снижение титра иммуноглобулинов или выработку блокирующих антител, когда используется дробное введение установленного аллергена, начиная с минимальных доз (например, 0,01 мл, через 2 часа 0,02 мл и т.д.).
Неспецифическая гипосенсибилизация – это снижение чувствительности к различным аллергенам, вызываемое изменением условий жизни индивидуума, действием некоторых лекарственных препаратов, отдельных видов физиотерапевтического и курортного лечения. Ее применение основано на принципах, предотвращающих развитие аллергической реакции на разных ее стадиях. Она применяется в тех случаях, когда СГ невозможна, либо тогда, когда не удается выявить природу аллергена. Неспецифическую гипосенсибилизацию часто применяют в сочетании с СГ.
Иногда можно добиться угнетения активности ИКС применением глюкокортикоидов и рентгеновского облучения по ходу развития иммунологической стадии. Глюкокортикоиды блокируют макрофагальную реакцию, образование суперантигена и синтез интерлейкинов и реакцию кооперации. В случаях формирования иммунокомплексной патологии применяют гемосорбцию, а при анафилаксии – препаратов Fc-фрагментов Ig E. Перспективным направлением в неспецифической гипосенсибилизации является использование принципов регуляция соотношения ИЛ-4 и -ИНФ, определяющие синтез в организме Ig E-класса.
Неспецифическая гипосенсибилизация направлена на изменение реактивности организма, нормализацию нарушенного равновесия между симпатическим и парасимпатическим отделами вегетативной нервной системой, что, в свою очередь, оказывает влияние на развитие всех трех стадий аллергического процесса. Соответствующие условия труда, отдыха и питания (гипоаллергенная диета), а также закаливание нормализуют функцию нейроэндокринной системы.
Подавление патохимической и патофизиологической стадий ГНТ достигается использованием комплекса лекарственных средств с различной направленностью действия. Выбор препаратов определяется типом реакции и присущим им характером образующихся медиаторов и метаболитов. В целях купирования симптомов атопических проявлений применяют стабилизаторы мембран клеток-мишеней I и II порядков – источников медиаторов ГНТ I типа, блокаторов их медиаторных рецепторов, а также инактиваторы медиаторов или ингибиторы их биосинтеза. К стабилизаторам мембран клеток-мишеней относятся хромогликан натрия, кетотифен, недокромил натрия. Хромогликан (интал) угнетает активность фосфодиэстеразы, что ведет к накоплению в тучных клетках цАМФ и поступлению в цитоплазму Ca 2+ , и, стало быть, блокируется высвобождение медиаторов и их вазоконстрикторное действие. Кетотифен (задитен) имеет сходное с инталом действие. Кроме того, кетотифен неконкурентно блокирует H1-гистаминовые рецепторы. Недокромил (тайлед) подавляет активность эозинофилов, нейтрофилов, макрофагов/моноцитов, тромбоцитов, тучных клеток и блокирует высвобождение из них предсуществующих и заново синтезируемых медиаторов воспаления.
Блокаторами рецепторов медиаторов на клетках-мишенях являются антигистаминовые препараты. Антигистаминовые препараты, блокирующие H1-гистаминовые рецепторы, широко используются в лечении ГНТ I типа. К настоящему времени известны препараты I и II поколения. К препаратам I поколения относятся димедрол, супрастин, диазолин, дипразин, фенкарон, бикарфен, которые являются конкурентными блокаторами H1-гистаминовых рецепторов, поэтому их связывание с рецепторами быстрое, обратимое и кратковременное. Препараты I поколения обладают ограниченной избирательностью действия на рецепторы, так как блокируют также холинергические мускариновые рецепторы. Препаратами II поколения являются акривастин, астемизол, левокабастин, лоратадин, терфенадин, цетиризин, эбастин. Это неконкурентные блокаторы H1-гистаминовых рецепторов, причем с рецептором связывается не сам вводимый препарат, а образующийся из него метаболит, за исключением акривастина и цетиризина, поскольку они сами являются метаболитами. Образующиеся продукты-метаболиты избирательно и прочно связываются с H1-гистаминовыми рецепторами.
К препаратам, инактивирующим медиаторы или их биосинтез, относят:
антагонисты серотонина (дигидроэрготамин, дигидроэрготоксин), которые используются преимущественно при атопическом зудящем дерматите и мигренях,
ингибиторы калликреин-кининовой системы (пармедин, или продектин),
ингибиторы липооксигеназного пути окисления арахидоновой кислоты, подавляющих образование лейкотриенов (цилейтон) и селективные блокаторы рецепторов для лейкотриенов (аколат),
ингибиторы протеолитических ферментов (апротинин, контрикал),
препараты, снижающие интенсивность свободнорадикального окисления – антиоксиданты (альфа-токоферол и другие),
Целесообразно применение фармакологических препаратов, обладающих широким сектором действия – стугерона, или циннаризина, обладающего антикининовым, антисеротониновым и антигистаминовым действиями; препарат является также антагонистом ионов кальция. Возможно использование гепарина как ингибитора комплемента, антагониста серотонина и гистамина, обладающего к тому же блокирующим эффектом в отношении серотонина и гистамина. Следует, правда, иметь в виду, что гепарин обладает способностью вызывать аллергическую реакцию, получившую наименование «гепарининдуцированная тромбоцитопения», о которой речь шла выше.
Целесообразно использовать также защиту клеток от действия БАВ, а также коррекцию функциональных нарушений в органах и системах органов (наркоз, спазмолитики и другие фармакологические препараты).
Механизмы неспецифической гипосенсибилизации весьма сложны. Например, иммунодепрессивное действие глюкокортикоидов заключается в подавлении фагоцитоза, торможении синтеза ДНК и РНК в ИКС, атрофии лимфоидной ткани, торможении образования АТ, подавлении высвобождения гистамина из лаброцитов, уменьшении содержания компонентов комплемента С3-С5 и т.д.
II. Принципы гипосенсибилизации при ГЗТ. При развитии ГЗТ используют, в первую очередь, методы неспецифической гипосенсибилизации, направленные на подавление афферентного звена, центральной фазы и эфферентного звена ГЗТ, включающие механизмы кооперации, т.е. на взаимодействие между собой регуляторных лимфоцитов (хелперов, супрессоров и т.п.), а также их цитокинов, в частности интерлейкинов. В абсолютном большинстве случаев аллергические реакции имеют сложный патогенез, включая, наряду с доминирующими механизмами реакций ГЗТ (клеточного типа) вспомогательные механизмы реакций ГНТ (гуморального типа). В связи с этим подавление патохимической и патофизиологической фаз аллергических реакций целесообразно сочетание принципов гипосенсибилизации, используемых при аллергиях гуморального и клеточного типов.
Афферентное звено реакций клеточного типа обеспечивается тканевыми макрофагами – А-клетками. Для подавления активности А-клеток, запускающих механизмы презентации АГ лимфоцитам, используют различные ингибиторы – циклофосфамид, азотистый иприт, соли золота. Для угнетения механизмов кооперации, пролиферации и дифференцировки антиген-реактивных лимфоидных клеток применяют различные иммунодепрессанты – кортикостероиды, антиметаболиты (аналоги пуринов и пиримидинов, например меркаптопурин, азатиоприн), антагонисты фолиевой кислоты (аметоптерин), цитотоксические вещества (актиномицин C и D, колхицин, циклофосфамид).
Специфическое действие иммунодепрессантов направлено на подавление активности митотического деления, дифференцировки клеток лимфоидной ткани (Т- и В-лимфоцитов), а также моноцитов, макрофагов и остальных клеток костного мозга и других короткоживущих быстро регенерирующих и интенсивно размножающихся клеток организма. Поэтому угнетающий эффект иммунодепрессантов считается неспецифическим, а гипосенсибилизация, вызванная иммунодепрессантами, стала называться неспецифической.
В целом ряде случаев в качестве неспецифической гипосенсибилизации применяют антилимфоцитарные сыворотки (АЛС). АЛС оказывают супрессивное влияние главным образом на иммунопатологические (аллергические) реакции клеточного типа: тормозят развитие ГЗТ, замедляют первичное отторжение трансплантата, лизируют клетки тимуса. Механизм иммунодепрессивного действия АЛС заключается в снижении количества лимфоцитов в периферической крови (лимфоцитопения) и лимфоидной ткани (в лимфатических узлах и т.п.). АЛС, помимо влияния на тимусзависимые лимфоциты, проявляют свой эффект опосредованно через гипоталамо-гипофизарную систему, что приводит к угнетению выработки макрофагов и подавлению функции тимуса и лимфоцитов. Применение АЛС ограничено вследствие токсичности последней, снижения эффективности при повторном использовании, способности вызвать аллергические реакции и неопластические процессы.
Следует отметить, что большинство используемых иммунодепрессантов не вызывают селективного ингибирующего воздействия лишь на афферентную, центральную или эфферентную фазы ГЗТ. Блокируя ключевые этапы биосинтеза нуклеиновых кислот и белков, они приводят к поражению пролиферирующих клеток в центральной фазе иммуногенеза, и, соответственно, к ослаблению эфферентного звена ГЗТ.
Препаратами выбора в патофизиологической стадии ГЗТ являются глюкокортикоиды. Механизм их действия до сих пор не выяснен. Известно, что глюкокортикоидные гормоны могут оказывать влияние на развитие всех трех стадий аллергических реакций. В иммунологическую стадию они подавляют макрофагальную реакцию и изменяют пролиферацию лимфоцитов – малые дозы стимулируют пролиферацию лимфоцитов и антителообразование, а большие дозы – угнетают. Глюкокортикоиды обладают также лимфолитическим действием – способны инициировать апоптоз. Их влияние на патохимическую стадию связано с ограничением высвобождения гистамина, ИЛ-1, ИЛ-2, а также с увеличением продукции липокортина (липомодулина), угнетающего активность фосфолипаз и, соответственно, образование продуктов липооксигеназного и циклооксигеназного путей превращения арахидоновой кислоты. Липокортин угнетает также эфферентные функции NK-клеток и других киллерных клеток. Однако наибольший эффект липокортина имеет место в патофизиологической стадии в виде воспаления. Глюкокортикоиды не применяют при атопических формах аллергии, когда обострение можно купировать применением других препаратов. Гораздо шире глюкокортикоиды применяются при аллергических реакциях III и IV типов.
Для подавления эфферентного звена ГЗТ, включающего повреждающее действие на клетки-мишени сенсибилизированных Т-лимфоцитов, а также медиаторов аллергии замедленного типа (лимфокинов), используют противовоспалительные средства – антибиотики цитостатического действия (актиномицин С, рубомицин), салицилаты, гормональные препараты (глюкокортикоиды, прогестерон) и биологически активные вещества (простагландины, антисыворотки).
В редких случаях в качестве средств неспецифической гипосенсибилизации используют гемосорбцию, плазмаферез (последовательную замену 75-95 % плазмы), циклоспорин А – низкомолекулярный пептид, подавляющий активность Т-хелперов. В исключительных случаях применяют ионизирующее излучение.
Отрицательные последствия использования ряда средств неспецифической гипосенсибилизации. В связи с отсутствием селективного воздействия иммунодепрессантов (цитостатиков, антиметаболитов, глюкокортикоидов АЛС) на определенный клон лимфоцитов при той или иной форме аллергии клеточного типа возникает универсальный лизис лимфоидной ткани, развитие вторичного иммунодефицита и инфекционных заболеваний. Цитостатики вызывают аплазию костного мозга и развитие гипопластической анемии, тромбоцитопении и лейкопении, подавляют процессы пролиферации эпителия слизистой желудочно-кишечного тракта, и, следовательно, ее репарации, что ведет к развитию язвенного поражения стенки желудка и кишечника и кровотечения. Подавление Т-системы лимфоцитов под действием иммунодепрессантов создает опасность онкологических заболеваний в связи с угнетением иммунологического надзора за генетическим постоянством соматических клеток. Наконец, в целом ряде случаев химические и физические иммунордепрессивные воздействия приводят к нарушениям репродуктивных возможностей организма, появлению тератогенных эффектов, а некоторые депрессанты сами обладают выраженной аллергенностью.
В заключении следует еще раз обратить внимание на то, что практически во всех случаях аллергических реакций их патогенез намного сложнее, чем представлено выше. В любой форме аллергии можно распознать участие механизмов и ГНТ (гуморального, В-опосредованного типа), и ГЗТ (клеточного, опосредуемого Т-лимфоцитами). Отсюда понятно, что для подавления цитохимической и патофизиологической стадий аллергической реакции целесообразно сочетание принципов гипосенсибилизации, используемых при ГНТ и ГЗТ. Например, при инфекционно-аллергической бронхиальной астме необходимы не только вышеперечисленные способы неспецифической гипосенсибилизации, но и антибактериальные препараты в сочетании с бронхолитиками – β2-адреномиметиками, теофиллинами, холинолитиками, антигистаминными и антипротеазными препаратами, антагонистами серотонина, ингибиторами калликреин-кининовой системы.
Так, механизм действия β2-адреномиметиков включает расслабление гладкой мускулатуры бронхов, улучшение мукоцилиарного клиренса, стабилизации проницаемости сосудов, различная степень угнетения высвобождения медиаторов из тучных клеток и базофилов. К этой же группе препаратов относятся сальбутамол, тербуталин, формотерол, сальметерол, сальметер, беротек, астмопент и их аналоги. Теофиллин и родственные метилксантины используются как препараты, расслабляющие гладкую мускулатуру бронхов, что связано с блокадой аденозиновых рецепторов А1 и А2. Кроме того, теофиллин является мощным ингибитором фосфодиэстеразы, которая катализирует гидролиз цАМФ. Накопление в клетке цАМФ тормозит соединение актина и миозина, и тем самым угнетает сократительную способность гладкомышечных клеток, а также блокирует кальциевые каналы мембран. К числу холинолитиков, оказывающих выраженное периферическое холинолитическое действие, относятся атровент, вагос, вентилат, тровентол. Однако, учитывая, что холинергический бронхоспазм локализуется главным образом в крупных бронхах, а при бронхиальной астме он выявляется и в мелких бронхах, желательно применять комбинированные препараты, объединяющие – β2-стимуляторы и холинолитики (например, беродуал) или сочетанное применение двух препаратов из указанных групп.
Указанные лекарственные средства могут быть использованы в качестве вспомогательных средств гипосенсибилизации и для преодоления трансплантационного иммунитета (например, при аллогенной пересадке органов и тканей).
источник