Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Иммунологическое бесплодие — нарушение репродуктивной функции, обусловленное поражением сперматозоидов антиспермальными антителами (АСАТ) в репродуктивной системе мужчины или женщины.
Распространённость иммунологического бесплодия составляет 5-15% из числа бесплодных супружеских пар. Частота выявления АСАТ у пациентов, состоящих в бесплодном браке, значительно варьирует в зависимости от многих причин, составляя в среднем для мужчин 15%, а для женщин вдвое выше — 32%.


Степень повреждения сперматозоидов зависит от:
• Класса антител
• Количеством выработанных иммунной системой антител АСАТ, их концентрацией
• Плотности покрытия антителами поверхности сперматозоидов
• От того, какие структуры сперматозоидов повреждаются антителами.
В зависимости от сочетания этих повреждающих факторов на репродуктивную систему выявляются следующие патологии:
• Нарушение формирования сперматозиодов, приводящее к олигоспермии, тератотоспермии и азооспермии.
• Снижение и/или подавление подвижности сперматозоидов.
• Подавление процесса взаимодействия половых клеток на этапе зачатия.
• Нарушения проходимости половых путей женщины и семявыводящих путей мужчины.
• Блокирование процесса имплантации эмбриона.
Существуют предрасполагающие факторы, обусловливающие нарушение барьера между кровью и функциональным эпителием яичек и способствующие формированию иммунного ответа на сперматозоиды у мужчин.
Причины развития иммунологического бесплодия у мужчин:
• инфекции передающиеся половым путем (гонорея, хламидиоз и т.п.);
• хронические воспалительные заболевания (простатит, эпидидимит, орхит);
• перенесённые травмы и операции на органах малого таза, мошонки.
• анатомические нарушения (паховая грыжа, варикоцеле, обструкция семявыносяших путей, крипторхизм, перекрут яичка, агенезия семявыносящих протоков).
Причины развития иммунологического бесплодия у женщин:
Причины нарушения иммуносупрессии женщины по отношению к сперматозоидам:
• Инфекции передаваемые половым путём (генитальный герпес, гонорея, хламидиоз, уреаплазмоз и т.д.)
• Хронические воспалительные заболевания женских половых органов
• Генитальный эндометриоз
• Аллергические заболевания
В большинстве случаев АСАТ, образованные в женском организме вызывают локальный иммунный ответ. Наиболее часто иммунная реакция проявляется на уровне шейки матки; в меньшей степени в иммунном ответе принимают участие эндометрий, маточные трубы и влагалище. Это обусловлено тем, что в слизистой оболочке канала шейки матки содержится большое количество плазматических клеток, способных синтезировать компоненты секреторного IgA. Вместе с тем в цервикальной слизи возможно выявление и других иммуноглобулинов, в частности IgG, имеющих значение для развития иммунологического бесплодия.

Исследования производимые при данном виде бесплодия весьма многообразны, единых стандартов диагностики и интерпретации результатов на данный момент не разработано.
1. Коррекция иммунологического статуса мужчины и женщины. Производится с целью снижения числа антиспермальных антител.
2. Применение андрогенов для лечения мужского бесплодия. Дело в том, что при выявлении в организме мужчины АСАТ часто поражается и та часть ткани яичек, которая вырабатывает тестостерон, от которого напрямую зависит активность формирования сперматозиодов.
3. Инсеминация женщины спермой мужа. Производится эндоскопическим способом.
4. Применение вспомогательных репродуктивных технологий (ВРТ).
Автор: Ткач И.С. врач, хирург офтальмолог
источник
Девочки, кому интересно, выкладываю, мнение одного репродуктолога из США по поводу иммунологических проблем бесплодия и их решения. Как сказала мне недавно одна наша гематолог, 30% репродуктивных потерь связаны с тромбофилией, 20%- с ауто-и алло-имунным бесплодием (вот о нем-то и пойдет речь), и только оставшиеся 50% приходятся суммарно на роль недостаточного качества эмбриона или неидеального состояния эндометрия. Большинство репродуктологов, при разборе причин неудач, в основном фокусируются на вот этих вторых 50%, и усиленно пытаются получить лучшие по качеству яйцеклетки/эмбрионы, либо «нарастить» тонкий эндометрий, либо провести гистероскопию, чтобы посмотреть, как там вообще дела в матке. И мало тех, кто обращает внимание на тромбофилию, а еще меньше тех, кто обращает внимание на имунные факторы. Такая ситуация не только в нашей стране, в Штатах похожая ситуация, и как написал доктор, чьи статьи буду цитировать- очень жаль, что это так, потому что многих проблем и неудач можно было бы избежать, если бы врачи больше обращали внимание и на эту сторону вопроса. Имунные факторы наши врачи чаще всего предлагают корректировать 2 способами- ЛИТы или биовен. Ниже хочу рассказать о третьем способе, который у нас менее распространен, хотя есть хочушки, которые его уже испробовали, это препарат интралипид . (он в 2 раза дешевле ЛИТов, и гоаздо дешевле биовена). Интересно будет тем, у кого, к сожалению, было несколько биохимических Б., потерь Б. на ранних сроках (до 9 нед), у кого есть АФА, СКВ, аутоимунный тиреоидит (гипотиреоз), эндометриоз.
Печальная действительность состоит в том, что во многих программах ЭКО не придается особого значения факторам, которые влияют на имплантацию эмбриона в целом и иммунологическую имплантационную дисфункцию (дальше в тексте ИИД) в частности. Возможно, отсутствие должного внимания, уделяемого оценке этих факторов у ЭКО-пациентов, связано с тем, что для организма человека, ЭКО-неудачи и невынашивание беременности в 4 раза чаще происходят по причине «некомпетентности» эмбриона (т.е. «некачественного» эмбриона), чем по причине дисфункции имплантации. Tаким образом, приемлемая успешность IVF может быть в достаточной мере достигнута, даже несмотря на игнорирование менее распространенных (и более сложных) факторов, таких как ИИД. Но для тех 20% пациентов ЭКО, у которых проблемы связаны с именно с иммунологическим фактором, это приобретает большое значение. Для них эмоциональные, физические и финансовые «американские горки» продолжаются и продолжаются. Часто потерпев неоднократные неудачи ЭКО, многие из них получают совет перейти на донорские яйцеклетки… только и в этом случае их ожидает провал. Процесс иммунологического принятия имплантирующегося эмбриона маткой матери является одновременно очень сложным и загадочным. В то время, как иммунная система организма обычно идет в атаку на все чужеродные белки (бактерии, вирусы, трансплантаты ), эмбрион, который является производным от белков, пришедших от другого индивида (отцовской спермы), как правило, благополучно имплантируется в слизистую оболочку матки, а затем вырастает в здорового ребенка.Это явление стало принято называть «иммунологической загадкой» беременности. Однако утверждать, что такой сложный процесс никогда не может потерпеть неудачу, было бы неправильно. Что-то может «пойти не так» примерно у 15-20% женщин с репродуктивными потерями. Это может проявляться как отсутствие/неудача имплантации (пациентка думает, что у нее бесплодие), как выкидыш/ невынашивание или, гораздо реже, как плацентарная недостаточность, угроза развития или внутриутробная смерть плода. Все зависит от сроков, характера и тяжести иммунной агрессии. Дальше идет сильно заумный текст, объясняющий этот сложный механизм изнутри, я его порядком сократила, оставив более-менее понятный кусочек (ну может кто и осилит:) Два типа лимфоцитов- а) маточные клетки-киллеры (NK) и б) цитотоксические лимфоциты (дальше в тексте ЦТЛ) играют жизненно важную роль в регуляции нормального процесса имплантации, контролируя проникновение и функционирование трофобласта. Есть 3 разновидности цитокинов, два из которых играть определяющую роль в поддержании имплантации: первыми являются TH-2 цитокины, которые стимулируют рост и расширение трофобласта и способствуют распространению кровеносных сосудов (ангиогенезу). TH-1 цитокины содействуют разрушению (цитолизу) клеток трофобласта, а также содействуют свертыванию крови (прокоагулянтной эффект).Баланс между TH-1 и TH-2 цитокинами необходим для нормального имплантации и развития плаценты. Чрезмерная активность (доминирования) ТН-1, являющаяся отличительной чертой активации NK-клеток и ЦТЛ, приводит к повреждению трофобласта, имплантационной дисфункции и репродуктивным потерям. Иммунологическая имплантационная дисфункция может быть по своей природе аллоимунной (по причине совпадения материнских и отцовских DQ-альфа генов — те самые HLA) или аутоиммунной (являющейся гораздо более распространенной, и составляющей 85% ИИД). Наиболее часто аутоиммунная имплантационная дисфункция связана с наличием следующих антител: 1)АФА 2)анти-тиреоидные антитела (АТ-ТПО и АТ-ТГ) 3)антиовариальные антитела. Часто аутоиммунная ИД встречается у женщин с уже имеющимися аутоиммунными заболеваниями, такими как аутоиммунный тиреоидит (он же тиреоидит Хашимото и субклинический/клинический гипотиреоз), системная красная волчанка, склеродермия, ревматоидный артрит. Одним из реакционных (вторичных) аутоимунных состояний является эндометриоз (. ) Аутоиммунная имплантационная дисфункция, как правило, сразу же становится фатальным препятствием для имплантации эмбриона и, соответственно, наиболее часто проявляется в виде «необъяснимого» бесплодия и / или «необъяснимых» неудач ЭКО, а не в виде выкидышей. Это происходит потому что активация NK / ЦТЛ произошла до момента имплантации и «корневая система» эмбриона сильно повреждена изначально. Аутоиммунная имплантационная дисфункция поддается коррекции посредством своевременного и адекватно проводимого лечения, селективной иммунотерапии — ЛИТы, ввунтривенные иммуноглобулины или терапия интралипидом. С учетом того, что терапия иммуноглобулинам является дорогостоящей, и имеет достаточное количество возможных побочных эффектов, а ЛИТы запрещены в США, автор предлагает терапию интралипидом, как наиболее безопасную из указанных и наиболее оптимальную по цене. Эффективность этой терапии доказывается проведенными клиническим исследованиями и собственным опытом автора, основанном более чем на 400 клинических случаях. Чтобы понять как влияет терапия иммуноглобулинами/интралипидом, необходимо сначала понять как возникают и действуют клетки-киллеры (вот тут для меня было очень интересное открытие): Так называемые «предшественники» клеток-киллеров (NK) появляются в матке в начале менструального цикла, где, под действием эстрогена, они подвергаются пролиферации. Эти «предшественники» — еще не те NK-клетки, которые влияют на имплантацию. Эта роль осуществляется через их «потомков», то есть, «функциональных киллеров», которые они распространяют под влиянием прогестерона. Это происходит после естественной или индуцированной овуляции, или после гормональной терапии прогестероном. Таким образом, клеткам-«предшественникам» клеток киллеров нужно около 5-7 дней на производство достаточного количества «функциональных киллеров» в месте имплантации чтобы повлиять на готовящуюся имплантацию. Это не случайно, что это совпадает по времени с моментом, когда эмбрион обычно имплантируется в слизистую оболочку матки (эндометрия) (как мы знаем, бластоциста имплантируется обычно на второй день после переноса, т.е. как раз на 7 день от овуляции/ пункции) Ни иммуноглобулины, ни интралипид не способны значительно подавить уже активированные «функциональные клетки-киллеры.» Для того чтобы это произошло, интралипид / внутривенный иммуноглобулин должны подавить активность еще «предшественников» NK клеток. Таким образом, интралипид/ иммуноглобулины должны быть введены за несколько дней до овуляции или введения прогестерона (или другими словами, за 14-7 дней до эмбриотрансфера ). Т.е. капать иммуноглобулины в день переноса, как это часто происходит, уже поздно! Но, с другой стороны, и капать их в цикле, предшествующем IVF- получается еще рано, исходя из вышесказанного, что клетки-киллеры эволюционируют в течение каждого цикла, т.е. в новом цикле начнут развиваться из „предшественников“ новые клетки-киллеры В следующий раз интралипид вводится после того, как хгч начнет показывать рост. Рекомендуемая доза- 100мл 20% интралипида на 400-500 мл хлорида натрия, капельно в течение 3-5 ч.
и вообще на этом сайте очень много подобных статей, в том числе реальных историй успеха после многих неудач, можно найти для себя много чего интересного, также можно задать автору вопросы
источник
Если вы столкнулись с диагнозом «иммунологическое бесплодие у мужчин или женщин», то у вас, наверняка, возникло немало вопросов.
На самом деле, репродуктивная активность у семейной пары снижена или зачатие невозможно без веских на то причин. Если супруги не имеют в физическом плане патологического изменения, и при этом не получается оплодотворение, может быть поставлен такой диагноз. Он характерен для 6-10% бездетных пар.
Это — выработка против сперматозоидов (АСАТ) антител. Такое патологическое состояние может наблюдаться как в организме любого полового партнера.
Иммунологическое бесплодие у женщин локализуется в цервикальном канале.
В организме мужчины антитела вырабатываются непосредственно сперме, снижая тем самым активность сперматозоидов.
Самые распространенные факторы этого вида бесплодия могут быть вызваны различными причинами. Самые распространенные у мужчин.
- Урогенитальные болезни инфекционного характера (ВИЧ, сифилис, герпес и другие).
- Приобретенные или врожденные дефекты половых органов.
- Онкологическое заболевание (необязательно органа репродуктивной функции).
- Оперативное вмешательство на мошонке или полученные травмы.
У женщины такое бесплодие возникает при:
- Генетических предрасположенностях организма.
- Хирургическом вмешательстве на половые органы, матку, яичники.
- Различных заболеваниях репродуктивной системы.
Вышеперечисленные факторы могут приводить к тому, что иммунная система воспринимает сперматозоиды как что-то ненужное, «чужое» и попросту отвергает их. Тем самым сводя шансы на успешное оплодотворение яйцеклеток к минимуму.
Для подтверждения диагноза понадобится пройти несколько специальных исследований.
Для мужчин – анализ сперматозоидов на наличие антитела в эякуляте, а также анализ крови, подсчет количества сперматозоидов, которые покрыты антиспермальными антителами.
Для женщин – специальный анализ крови и цервикальной слизи на наличие в эякуляте антител.
Обоим партнерам назначают посткоитальную пробу (тест), обследование на совместимость.
Когда диагноз подвержен, и вы точно знаете, что у вас иммунологический фактор, не стоит отчаиваться. Достаточно набрать в интернете «мужское иммунологическое бесплодие форум», чтобы понять, что патология лечится успешно на 100%.
Антитела против сперматозоидов бывают трех видов – IgM, IgА, IgG.
Независимо от класса они могут встретиться как в организме женщины, так и у мужчины (в слизи матки, половых органах, сыворотке крови).
В зависимости от вида АСАТ влияет на взаимодействие в момент оплодотворения половых клеток, нарушая проходимость половых путей, подавляя активность сперматозоидов, блокируя имплантацию эмбриона. Различные факторы вызывают бесплодие.
Причины иммунологического бесплодия различные:
- У мужчин антитела могут начать образовываться при поражении семенных каналов, травмах яичка, разрыве капиллярной системы.
- Причины иммунологического бесплодия у женщин – болезни матки, яичников, генетическая склонность, операции на репродуктивных органах.
- У обоих партнеров – при урологических инфекционных заболеваниях, передающихся половым путем.
Преимущественно такая форма бесплодия характерна для женщин. Риск увеличивается при избыточной массе тела, климаксе, анорексии, частых стрессах, хронических формах соматических заболеваний.
Как лечить иммунологическое бесплодие? Этот вопрос задают многие семейные пары, столкнувшиеся с такой проблемой.
Иммунологическое бесплодие у женщин: лечение
Для устранения причин, вызвавших бесплодие, назначаются антигистаминные препараты с высокими дозами препаратов антибактериального действия, что позволяет повысить иммунитет.
Введение гепарина под кожу и применение аспирина помогают бороться с аутоиммунными процессами.
Во время лечения важно предохраняться во время половой близости на протяжении шести-восьми месяцев (в зависимости от назначенного курса). Так как полноценное оплодотворение яйцеклетки невозможно при пониженном иммунитете.
Для стабилизации защитных систем организма женщины показан ввод смешанной группы белков перед зачатием или использование лимфоцитов от донора.
Изначально требуется устранить патологическую причину, которая вызвала возникновение антител (АСАТ), препятствующих зачатию.
Лечение может состоять из:
- Восстановления репродуктивных функций с помощью хирургических операций.
- Коррекцию кровообращения.
- Назначение лекарственных препаратов в случае необходимости: и цитостатиков или протеолитического характера.
- Оперативного вмешательства на яичке, мошонке.
Кроме этого имеются репродуктивные вспомогательные технологии, которые искореняют причины бесплодия. Однако, такие технологии требуют более тщательной подготовки и дополнительной диагностики.
- ИКСИ (интрацитоплазматические инъекции) – внедрение полноценных жизнеспособных сперматозоидов прямым путем в яйцеклетки, с дальнейшим вводов эмбрионов в матку.
- Инсеминация – введение в маточную полость женщин мужских сперматозоидов, при котором канал матки обходится.
- Искусственное оплодотворение – показано, если имеются функциональные сперматозоиды.
В практически безнадежной ситуации иммунологического бесплодия и неэффективности лечения у мужчин, рекомендуется использовать донорскую сперму.
При проведении искусственного оплодотворения важным фактором являются показания АСАТ. При повышенной концентрации процедура противопоказана, так как она не даст положительного результата. Изначально требуется устранить проблему с помощью продолжительной терапии – до полного восстановления нормальных показателей уровня аспартата.
В успешном зачатии яйцеклетки немаловажным фактором является использование наиболее активных, подвижных, качественных, полноценных, перспективных сперматозоидов. Эмбриональное консервирование с использованием предварительной заморозки или ассистированный хэтчинг гарантирует еще большие вероятности и шанс того, что будет положительный результат после лечения бесплодия.
Выход найти можно из любой ситуации, Важно, чтобы решение было принято совместно супружеской парой.
- АСАТ (оксалоацетат трансаминаза) воспроизводится только в отношении половых клеток каждого конкретного мужчины. Если причина бесплодия не подается лечения, выходом для женщины может стать замена сексуального партнера. В большинстве случаем происходит полноценное зачатие.
- ВРТ (вспомогательные репродуктивные технологии) эффективны в лечении. С их помощью успешно лечится как легкая степень заболевания, так и средней тяжести. Единственное условие – своевременное обращение за оказанием медицинской помощи и выявление причины.
Однозначно, проблема решаема. В любом случае не стоит отчаиваться и опускать руки. Если вы начнете искать в интернете «иммунологическое бесплодие у женщин, форум, кто лечил», и какие результаты дало лечение, то воспрянете духом. На самом деле патология излечивается в 100% случаев. При условии, если вы будете выполнять все рекомендации. Путь непростой, но он дарит шансы на то, что вы станете счастливыми родителями! Можно ли вылечить иммунологическое бесплодие? Ответ очевиден – да.
источник
Еще один вид бесплодия это иммунологическое бесплодие. Такое бесплодие связано с выработкой, как у мужчин, так и у женщин, антиспермальных антител. Так иммунная система человека влияет на работу репродуктивной функции. Заболевание это никак не проявляется и не имеет симптомов, кроме отсутствия возможности зачать ребенка.
Иммунологическое бесплодие – это заболевание при котором у пары отсутствуют заболевания мочеполовой системы а забеременеть не получается. Точно установить причину патологии проблематично.
Еще недавно ученые были уверены, что такое бесплодие может быть только у женщины. Проявляется это заболевание у женщины так, иммунные клетки которые должны отвечать за овуляцию просто не воспринимают сперматозоиды определенного мужчины. Иммунитет женщины принимает сперматозоиды как инородный объект и отторгает их. Поэтому оплодотворение яйцеклетки не происходит.
На сегодняшний день, в результате исследований, удалось доказать, что и иммунитет мужчины способен вырабатывать антиспермальные антитела. Таким образом, яички мужчины могут просто не воспринимать женскую фолликулярную жидкость, и даже собственные биологические компоненты. Такой процесс называется аутоиммунизацией.
При аутоиммунизации у мужчины, в организме происходит сопротивление между собственными биологическими материалами и антителами. Иммунные клетки, которые находятся в яичках, производят антитела. Антитела воспринимают биологический материал как инородный объект. В результате сопротивления с собственными антителами сперматозоиды просто склеиваются между собой, значительно снижая качество спермы. Способность мужчины к оплодотворению, в этом случае, также существенно снижается.
Самым основным признаком иммунологического бесплодия является отсутствие наступления беременности при нормальном качестве спермы у мужчины и нормальной работы репродуктивных органов у женщины.
Главная причина такого бесплодия на сегодняшний день неизвестна. Врачи говорят о наследственности и индивидуальной особенности человека, как об основной причине иммунологического бесплодия.
Особенности иммунного фактора бесплодия:
- Аутоиммунизация.
- Антитела.
- Сильная чувствительность женской иммунной системы к сперме конкретного мужчины. В этом случае, женские антитела уничтожают сперматозоиды, воспринимая их, как инородный объект.
По статистике, чаще такое бесплодие встречается у мужчин при наличии заболеваний и травм органов мошонки. Например: орхит, водянка, травмы яичек, варикоцеле, застой спермы или киста семенного канатика.

Определить степень иммунологического бесплодия можно с помощью спермограммы с MAR тестом (анализа спермы). В анализе будут приведены показатели титра АСАТ и класса IgG, IgA, IgM. Также в анализе будет показан уровень возникновения иммунной реакции и места фиксации сперматозоидов. Подробнее о том, как сдавать и расшифровывать результаты этого анализа читайте в этой статье.
Видео из лаборатории о спермограмме с MAR тестом:
По причине иммунологического бесплодия от 6 до 22% пар не могут зачать ребенка. Если в течение года попыток забеременеть результата нет, то одной из возможных причин бесплодия может быть именно нарушения связанные с иммунитетом родителей, одного или двух. Бывает, что при таком бесплодии беременность наступает, но очень высока вероятность выкидыша на ранних сроках.

Одним из методов выявления этого заболевания является посткоитальный тест. Пред сдачей этого теста нужно чтобы мужчина уже прошел свое тестирование (спермограмму). Если по результатам спермограммы будет понятно, что мужчина здоров, то назначается посткоитальный тест.
Его сдает женщина на 14 день начала цикла менструации. Для теста на исследование берут цервикальную жидкость. Перед сдачей теста пара должна воздерживаться три дня от половой близости. Сам тест сдается спустя 10 часов после полового акта, но не дольше одних суток (24 часа). По результату исследований будет ясно, есть ли в фолликулярной слизи сперматозоиды. Если они присутствуют, будет определена их активность.

Помимо посткоитального теста иммунологическое бесплодие можно определить дополнительными исследованиями, которые в себя включают:
- метод латексной агглютинации;
- смешанный антиглобулиновый тест;
- с помощью иммуноферментного анализа;
- при помощи пенетрационного теста.
Также для установления диагноза и определения уровня АСАТ (антиспермальных антител) нужно дополнительно сдать фолликулярную жидкость и кровь.
Полезное и интересное видео:
В связи со сложностью определения точных причин такого бесплодия назначение лечения очень проблематично. Лечение включает в себя несколько способов: хирургическое вмешательство, иммуностимулирующие и андрогенные препараты.
Помимо вышеперечисленных способов лечения, дополнительно назначаются антибиотики, антигистаминные препараты и противовоспалительные средства. Чтобы исключить случайное зачатие в период действия сильнодействующих препаратов пара во время полового акта обязана использовать презерватив для контрацепции.
Время курса лечения иммунологического бесплодия составляет от полугода до 8 месяцев. В результате лечения чувствительность организма к спермальным антигенам снижается, вероятность зачатия увеличивается.
За три дня до овуляции женщине назначаются препараты для повышения уровня эстрогена. Иногда назначается курс гормональных препаратов а также кортикостероиды.
Иммунологическое бесплодие поддается лечению при помощи инсеминации (исскуственного ввода спермы в женский организм). ЭКО (экстракорпоральное оплодотворение) – это еще один действенный метод зачатия ребенка при иммунологическом бесплодии. В этом случае оплодотворение яйцеклетки происходит в специальной среде вне женского организма. После оплодотворения производится подсадка змбриона в полость матки.
Многие семейные пары пытаются лечить иммунологическое бесплодие способами и рецептами народной медицины. Обязательно проконсультируйтесь у врача, не стоит заниматься самолечением.
Если у семейной пары не получается зачать ребенка в течение года это серьезная проблема, возможно это иммунологическое бесплодие. Чтобы добиться появления ребенка на свет не стоит пускать ситуацию на самотек, нужно обязательно обратиться к врачу.
Не забывайте писать комментарии и ставить оценку статье звездочками. Спасибо за посещение сайта, надеемся мы смогли вам помочь.
источник
Иммунологическое бесплодие обуславливает расстройство репродуктивной функции в 20% случаев. Иммунологическим или аутоиммунным бесплодием называют расстройство репродуктивной функции у мужчин и женщин на фоне поражения сперматозоидов АСАТ (антиспермальными антителами). Обнаружение АСАТ считается одной из основных причин бесплодия. Частота встречаемости патологии составляет 32% и 15% у женщин и мужчин соответственно.
Процессы, протекающие в организме, происходят при прямом и опосредованном участии иммунной системы. Нарушения функционирования иммунной системы провоцируют:
- воспаление хронического характера;
- расстройства созревания мужских и женских половых клеток, что приводит к бесплодию;
- невынашивание и осложнения беременности.
Если конкретизировать, что такое иммунологическое бесплодие, это состояние организма мужчины и женщины гипериммунного характера, при котором отмечается секреция антиспермальных антител. Иммунологическое бесплодие специалисты условно подразделяют на женское и мужское. Иммунное бесплодие у женщин встречается чаще приблизительно в 2 раза. Лечением занимаются гинекологи, андрологи и репродуктологи.
Примечательно, что АСАТ иногда присутствуют у фертильных женщин и мужчин в незначительном количестве. Однако при фиксации АСАТ на мужских половых клетках снижает вероятность возникновения беременности.
Аутоиммунный фактор бесплодия встречается как у женщин, так и у мужчин. Иммунологическое бесплодие зачастую подразумевает повреждение половых клеток так называемыми антиспермальными антителами. Иногда иммунологическое бесплодие обусловлено целой системой генов (HLA), отвечающих за тканевую совместимость. Гены, представленные группой связанных с иммунитетом антигенов, располагаются в шестой хромосоме человека.
Сперматозоиды содержат белок, являющийся чужеродным для иммунной системы. Таким образом, белковые структуры мужских половых клеток считаются аутоантигенами.
В норме сперматозоиды защищены специфическими механизмами, подразумевающими супрессию иммунного ответа:
- ГТБ или гемато-тестикулярный барьер яичка и придатка, способность к мимикрии, подразумевающую сорбцию и десорбцию поверхностных антигенов, иммунопрессивный фактор спермоплазмы – у мужчин;
- Снижение уровня Т-хелперов, C3 и Ig-компонента, возрастание численности Т-супрессоров при овуляции – у женщин.
Антиспермальные антитела вырабатываются у женщин и мужчин. Это иммунные комплексы следующих классов:
- IgA – прикрепляются к хвосту или головке сперматозоидов;
- IgG – локализуются в хвосте и головке;
- IgM – фиксируются в области хвоста.
АСАТ обнаруживают в крови, внутрибрюшной жидкости, цервикальном секрете и семенной жидкости. Норма содержания АСАТ в крови составляет 0-60 Ед/мл.
Повреждение сперматозоидов может иметь различную степень, которая зависит от следующих факторов:
- класс антител;
- численность и концентрация АСАТ;
- плотность покрытия сперматозоидов антителами;
- влияние на конкретные структуры мужских половых клеток.
АСАТ имеют следующие разновидности:
- спермоиммобилизирующая;
- спермоагглютинирующая;
- спермолизирующая.
Прикреплённые к хвосту, АСАТ негативно влияют только на миграцию сперматозоида через секрет цервикального канала. Существенного влияния на оплодотворение не наблюдается. Если антитела фиксируются к головке, способность к миграции не нарушается. Негативное воздействие обусловлено подавлением способности, заключающейся в растворении капсулы готовой к оплодотворению яйцеклетки. Таким образом, оплодотворение сперматозоидом становится невозможным.
У женщин с одинаковой частотой выявляются все классы иммуноглобулинов. Для мужчин характерно обнаружение антител IgG, IgA.
Специалисты называют несколько причин, приводящих к иммунологическому бесплодию вследствие разрушения барьерных факторов:
- половые инфекции и туберкулёз кожи в области гениталий;
- воспалительные болезни у мужчин, протекающие в хронической форме – простатит, орхоэпидидимит;
- повышение количества лимфоцитов в семенной жидкости;
- сальпингит, оофорит, аднексит и другие воспалительные хронические патологии у женщин;
- эндокринная дисфункция, сопровождающаяся нарушением продукции гормонов;
- аллергия на сперму, являющаяся следствием несовместимости иммунологического характера;
- травмы тканей половых органов, возникшие вследствие различных манипуляций;
- эрозия на шейке матки и её последующее лечение;
- обструкция семявыводящих путей, водянка яичка, варикоцеле, крипторхизм, пахово-мошоночная грыжа и другие анатомические нарушения;
- редкая интимная жизнь, что способствует развитию аномалий сперматозоидов;
- использование контрацепции химического воздействия;
- половые контакты с несколькими партнёрами, что провоцирует воздействие на организм разных белковых антигенов;
- проникновение в желудок и кишечник значительного количества спермы при оральном и анальном сексе, в брюшную полость при нарушении техники внутриматочной инсеминации;
- неудачный протокол ЭКО.
Аутоиммунное бесплодие может возникать вследствие комплекса неблагоприятных факторов.
Специалисты подчёркивают, что аутоиммунное бесплодие у женщин изучено недостаточно. В результате полового акта в женский организм попадает значительное число сперматозоидов, являющихся чужеродными. Мужские половые клетки отличаются разными антигенами. Определённое воздействие также оказывает составляющая спермы жидкостного характера.
Природой предусмотрена особая система иммуноподавления, чтобы предотвратить реакцию на сперматозоиды, являющиеся чужеродным объектом. Однако под воздействием некоторых факторов и причин система иммуноподавления оказывается несостоятельной. В таких случаях отмечается борьба иммунной системы женщины против сперматозоидов.
Антитела обнаруживаются у женщин в секрете цервикального канала. Их выработка способствует снижению проходимости половых путей. Избыточная продукция антиспермальных антител приводит к нарушению механизма имплантации. Примечательно, что при удалении одних антигенов на поверхности половых путей происходит накапливание других.
Под воздействием антител в балансе Т-лимфоцитов наблюдаются патологические изменения. Погибшие сперматозоиды отличаются от выбранных организмом генетически с целью проникновения в трубу и последующего оплодотворения яйцеклетки. Они создают блокаду местного иммунитета.
Зачастую образованные АСАТ способствуют появлению местного иммунного ответа. Реакция со стороны иммунитета наблюдается зачастую со стороны шейки матки. В этой области содержатся плазматические клетки, синтезирующие компоненты IgA, IgG. Иногда наблюдается вовлечение внутреннего слоя матки, труб и влагалища.
Антитела выявляют у 22% мужчин с бесплодием в анамнезе. В 10% случаев антиспермальные антитела обнаруживают у здоровых мужчин. Высокая концентрация антител наблюдается у 7% мужчин.
При созревании сперматозоидов, которые являются спермацитами первого порядка, отмечается выработка антиспермальных антител, которые имеют вид иммуноглобулинов. Действие антиспермальных антител проявляется в снижении подвижности, иммобилизации, склеивании или агглютинации сперматозоидов. Повреждающие эффекты включают:
- нарушение подвижности половых клеток у мужчин;
- угнетение взаимодействия яйцеклеток и сперматозоидов;
- снижение проходимости семявыводящих путей;
- ухудшение капацитации, которая подразумевает подготовку сперматозоида к последующему проникновению внутрь яйцеклетки.
Повреждающий эффект находится в зависимости от вида антител. Существенное значение имеет также их концентрация. Выделяют следующие барьерные факторы, которые препятствуют повреждению сперматозоидов антиспермальными антителами:
- гематотестикулярный барьер образован располагающимися между кровеносными сосудами и семенными канальцами клетками Сертоли;
- в семенной жидкости содержатся местные факторы, обеспечивающие регуляцию.
Единственным признаком аутоиммунного бесплодия является нарушение репродуктивной функции, что проявляется бесплодием в течение года и более, самопроизвольным прерыванием беременности преимущественно на ранних сроках. Других признаков иммунологического бесплодия не отмечается.
Мужчины, имеющие иммунологическое бесплодие, отличаются активным сперматогенезом, сохранением эректильной функции. На фоне аутоиммунного бесплодия у женщин могут не выявляться патологии матки, труб, эндокринной системы, что свидетельствует в пользу наличия АСАТ.
Аутоиммунное бесплодие можно предположить при отсутствии беременности при имеющихся факторах риска. На иммунологическое бесплодие указывают нарушения эндокринного характера и склонность к аллергии у партнёров.
Отсутствие беременности в течение года может говорить о наличии бесплодия, например, иммунологического плана. Диагностика подразумевает проведение обследования с целью исключения различных факторов бесплодия:
- трубно-перитонеального;
- шеечного;
- маточного;
- генетического;
- эндокринного.
Для диагностики иммунологического бесплодия используют пробы: анализы крови, спермы, выделений из половых путей с целью обнаружения АСАТ. Более чем в 40% случаев бесплодие связано с наличием патологии у мужчины. Именно поэтому обследование проходит как женщина, так и мужчина.
Диагностика аутоиммунного бесплодия включает выполнение посткоитального теста после исключения других возможных факторов. Посткоитальное тестирование подразумевает исследование слизи цервикального канала и обычно рекомендуется на 12-14 сутки цикла. За 3 дня до исследования необходим половой покой. Исследование также выполняется через 9-24 часа после полового контакта. В процессе диагностики при помощи микроскопа определяется подвижность сперматозоидов.
Результат посткоитального тестирования может быть:
- положительным при наличии 5-10 подвижных и активных сперматозоидов и отсутствии лейкоцитов в слизи;
- отрицательным в случае отсутствия мужских половых клеток;
- сомнительным , если движения сперматозоидов являются маятникообразными.
При получении сомнительного результата необходимо проведение повторного обследования. Посткоитальный тест также оценивает численность сперматозоидов, характеристику совершаемых ими движений:
- неподвижность;
- феномен качания;
- активное поступательное.
Результат тестирования предусматривает одну из пяти оценок:
- отличная или норма;
- удовлетворительная;
- плохая;
- сомнительная;
- отрицательная при отсутствии сперматозоидов.
Дополнительная диагностика иммунологического бесплодия включает:
- MAR-тест . Это смешанный антиглобулиновый тест, позволяющий определить численность мужских половых клеток, которые покрыты антителами. Тест был рекомендован ВОЗ с целью обычного скрининга спермы. Говорить об аутоиммунном бесплодии можно при получении теста, если его показатель соответствует 51%.
- Метод латексной агглютинации . Данная методика является альтернативой MAR-тесту и считается высокочувствительной при снижении подвижности мужских половых клеток. Диагностику можно применять для выявления антител в секрете цервикального канала, семенной жидкости, плазме крови. С помощью метода латексной агглютинации определить количество покрытых антиспермальными антителами клеток не представляется возможным.
- Иммуноферментный анализ (непрямой) . Посредством диагностики можно определить количество антиспермальных антител. Нормальный показатель составляет до 60 Ед/мл. Повышенная концентрация отмечается при 100 Ед/мл, а промежуточное значение от 61 до 99 Ед/мл.
- Пенетрационный тест . Диагностику целесообразно использовать при отрицательном результате посткоитального теста.
Гинекологи могут назначить следующие исследования для подтверждения или исключения аутоиммунного бесплодия:
- мазок на флору, онкоцитологию, бакпосев;
- ПЦР-диагностика половых инфекций;
- гормональный статус;
- УЗИ внутренних половых органов;
- кольпоскопия;
- выскабливание;
- гистероскопия;
- лапароскопия.
Мужчины в обязательном порядке сдают спермограмму, позволяющую определить тип движения, строение, численность и концентрацию сперматозоидов, признаки воспаления. В некоторых случаях может потребоваться консультация узких специалистов, например, генетика.
Гинекологи отвечают утвердительно на вопрос, лечится ли иммунологическое бесплодие. Лечебные мероприятия при иммунологическом бесплодии у мужчин включает устранение факторов риска, операции при водянке яичка, варикоцеле, пахово-мошоночной грыже. При необходимости назначаются иммуностимуляторы и андрогенные препараты.
Лечение аутоиммунного бесплодия у женщин предусматривает приём следующих медикаментозных средств:
- антибактериальные и противовоспалительные;
- иммуноглобулины;
- иммуномодуляторы;
- антигистаминные.
Важной составляющей лечения является использование презерватива в течение 6-8 месяцев. При отсутствии контакта женского организма и сперматозоидов можно добиться ослабления сенсибилизации иммунной системы.
За несколько дней до овуляции рекомендован приём препаратов, содержащих эстроген. Иногда назначается гормонотерапия, включающая малые дозы кортикостероидов. Гормональное лечение проводится в течение трёх месяцев. При выявлении аутоиммунного процесса, например, антифосфолипидного синдрома, терапия дополняется гепарином или аспирином в минимальных дозах.
Целесообразным считается коррекция иммунологического статуса как у женщин, так и у мужчин. Это позволяет снизить количество АСАТ. Возможно подкожное введение до зачатия аллогенных лимфоцитов. Иногда рекомендуется также внутривенное введение смеси белков плазмы (от разных доноров).
Для лечения аутоиммунного бесплодия у мужчин назначаются андрогены. При наличии фоновой патологии целесообразно проведение хирургического и медикаментозного лечения (цитостатики, протеолитические ферменты). При наличии АСАТ возможно поражение области яичек, отвечающей за продукцию тестостерона. Гормон обуславливает активность формирования мужских половых клеток.
Адекватное медикаментозное лечение иммунологического бесплодия позволяет реализовать репродуктивную функцию. При отсутствии эффекта проводимого лечения, направленного на коррекцию аутоиммунного бесплодия, женщине предлагается внутриматочная инсеминация.
Эффективность внутриматочной инсеминации, проводимой при иммунологическом бесплодии, составляет до 20%. Перед выполнением процедуры осуществляется предварительная подготовка спермы партнёра, которая включает отбор подвижных сперматозоидов. Материал вводится в область дна матки в непосредственной близости к устью труб.
Внутриматочная инсеминация позволяет сократить расстояние, которое проходят малоподвижные сперматозоиды для последующего слияния с яйцеклеткой. С целью достижения эффекта при иммунологическом бесплодии выполняют 2-3 внутриматочные инсеминации. Методику целесообразно использовать до и после овуляции.
При неполноценности спермы партнёра вследствие иммунологического фактора бесплодия также рекомендуют ЭКО. Эффективность метода составляет до 50%. В пробирку помещаются яйцеклетки и отобранные сперматозоиды. Полученные эмбрионы выращивают, а затем подсаживают в маточную полость.
Наличие антител в крови и секрете цервикального канала значительно снижает эффективность искусственного оплодотворения. Антитела оказывают неблагоприятное влияние на процессы оплодотворения, имплантации и последующее развитие, течение беременности. Высокий титр АСАТ является противопоказанием к проведению ЭКО. Необходимо продолжительное лечение до нормализации показателей.
При аутоиммунном бесплодии рекомендуют использовать ICSI. Это техника ЭКО, в рамках которой осуществляется искусственное внедрение заранее отобранного сперматозоида в цитоплазму яйцеклетки. Метод позволяет получить беременность в 60% случаев.
Вспомогательные методики эффективны исключительно при снижении подвижности, а также неподвижности мужских половых клеток. Оплодотворение и развитие беременности возможно при наличии способности сперматозоидов к оплодотворению.
Специалисты подчёркивают, что иммунологическое бесплодие является следствием различных патологий врождённого, воспалительного характера. Половые инфекции, беспорядочная интимная жизнь, травмы, аномалии гениталий могут привести к развитию аутоиммунного бесплодия.
Профилактика иммунологического бесплодия включает:
- моногамные интимные отношения;
- своевременное выявление и адекватное лечение дефектов, инфекций и воспалительных процессов внутренних половых органов;
- коррекцию нарушений гормонального фона;
- отказ от необоснованных хирургических вмешательств в области малого таза.
Существенное значение имеет соблюдение здорового образа жизни.
Иммунологическое бесплодие является одним из факторов нарушения репродуктивной функции как у мужчин, так и у женщин. Аутоиммунное бесплодие не имеет клинической картины и отличается специфическим характером. АСАТ вырабатываются исключительно на половые клетки конкретного мужчины. Смена полового партнёра может обеспечить наступление беременности. Современные вспомогательные репродуктивные технологии позволяют преодолеть тяжёлые случаи иммунологического бесплодия.
источник
Иммунологическое бесплодие – гипериммунное состояние женского или мужского организма, сопровождающееся секрецией специфических антиспермальных антител. Иммунологическое бесплодие проявляется несостоятельностью зачатия и наступления беременности при регулярной половой жизни без контрацепции при отсутствии других женских и мужских факторов инфертильности. Диагностика иммунологического бесплодия включает исследование спермограммы, антиспермальных антител плазмы, проведение посткоитального теста, MAR-теста и других исследований. При иммунологическом бесплодии применяются кортикостероиды, методы иммунизации и вспомогательные репродуктивные технологии.
Иммунологическое бесплодие — наличие патологического антиспермального иммунитета, препятствующего процессу оплодотворения яйцеклетки и имплантации эмбриона. При иммунологическом бесплодии антитела к сперматозоидам – антиспермальные антитела (АСАТ) могут синтезироваться как женским, так и мужским организмом и присутствовать в цервикальной и внутриматочной слизи, сыворотке крови, семенной плазме, семявыводящих протоках. Иммунологический фактор оказывается причиной бесплодия у 5-20% семейных пар в возрасте до 40 лет, при этом АСАТ могут выявляться только у одного супруга или сразу у обоих. Изучением проблемы иммунологического бесплодия занимаются специалисты в области репродуктивной медицины (гинекологи — репродуктологи, андрологи).
В минимальном количестве АСАТ могут присутствовать у фертильных мужчин и женщин, но их фиксация на мембранах большинства сперматозоидов резко ухудшает прогноз на беременность. Это связано с нарушением качества и фертильности спермы — повреждением структуры и резким спадом подвижности сперматозоидов, снижением их способности проникать в цервикальную слизь, блокадой подготовительных стадий (капацитации и акросомальной реакции) и самого процесса оплодотворения яйцеклетки. При наличии АСАТ существенно снижается качество эмбрионов, нарушаются процессы их имплантации в матку, формирования плодных оболочек и развития, что приводит к гибели зародыша и прерыванию беременности на самых ранних сроках.
По своей антигенной структуре сперматозоиды являются чужеродными для женского и для мужского организма. В норме они защищены механизмами супрессии иммунного ответа: у мужчин — гемато-тестикулярным барьером (ГТБ) в яичке и его придатке, иммуносупрессивным фактором спермоплазмы и способностью сперматозоидов к мимикрии (к сорбции и десоробции поверхностных антигенов); у женщин — уменьшением уровня Т-хелперов, Ig и С3-компонента системы комплемента, повышением числа Т-супрессоров во время овуляции.
Под действием определенных неблагоприятных факторов нарушение защитных механизмов делает возможным контактирование спермальных антигенов с иммунной системой и приводит к развитию иммунологического бесплодия. Причинами выработки аутоантител на сперматозоиды и клетки сперматогенеза у мужчин могут выступать острые и тупые травмы мошонки и операции на яичках, инфекции и воспалительные процессы урогенитального тракта (гонорея, хламидиоз, герпес, ВПЧ, орхит, эпидидимит, простатит), врожденные или приобретенные дефекты половых органов (крипторхизм, перекрут яичка, варикоцеле, фуникулоцеле и др.), онкопатология.
Сбой внутриматочной иммунной толерантности и появление АСАТ у женщин в предимплантационный период могут быть спровоцированы инфекционно-воспалительными заболеваниями репродуктивного тракта, повышенным уровнем лейкоцитов в эякуляте партнера (при неспецифическом бактериальном простатите), контактом с иммуногенными сперматозоидами партнера, уже связанными с его аутоантителами.
Формированию АСАТ у женщин также могут способствовать попадание спермы в ЖКТ при оральном/анальном сексе, применение химических средств контрацепции, коагуляция эрозии шейки матки в анамнезе, нарушения при внутриматочной инсеминации, гормональный «удар» при попытке ЭКО, травма при заборе яйцеклеток. Опосредованно стимулировать выработку АСАТ в женском организме могут другие изоантигены, содержащиеся в эякуляте партнера — ферменты и внутриклеточные антигены сперматозоидов, HLA антигены; несовместимость в системах ABO, Rh-Hr, MNSs.
Степень поражения сперматозоидов зависит от класса (IgG, IgA, IgM) и титра АСАТ, места их фиксации, уровня возникновения иммунной реакции. АСАТ, соединяющиеся с хвостовой частью сперматозоидов, затрудняют их движение, а фиксирующиеся к головке — блокируют слияние с ооцитом.
Иммунологическое бесплодие внешне протекает бессимптомно, не имея видимых проявлений у обоих партнеров. У мужчин с аутоиммунным бесплодием обычно сохраняется активный сперматогенез, эректильная функция и полноценность полового акта. При гинекологическом обследовании женщины не обнаруживаются маточные, трубно-перитонеальные, эндокринные и иные факторы, препятствующие зачатию.
При этом у супружеской пары детородного возраста при условии нормального менструального цикла женщины и регулярной половой жизни без предохранения имеет место отсутствие беременности в течение года и более. При АСАТ у женщин из-за дефекта имплантации и нарушения развития эмбриона наблюдается его гибель и отторжение, прерывание беременности на очень ранних сроках, обычно до того, как женщина может ее обнаружить.
При бесплодии комплексное обследование необходимо пройти и женщине, и мужчине — у гинеколога и уролога-андролога соответственно. Иммунологический характер бесплодия диагностируют по результатам лабораторных исследований: анализа эякулята, специальных биологических проб — посткоитального теста (Шуварского– унера in vivo и Курцрока–Миллера in vitro), MAR-теста; 1ВТ-теста, ПЦМ. определения антиспермальных антител плазмы. На время проведения диагностических испытаний прием гормональных и других лекарственных препаратов прерывают.
Наличие мужского фактора иммунологического бесплодия можно предположить при нарушении спермограммы (резком падении количества, искажении формы, агглютинации и слабой активности сперматозоидов, низкой выживаемости спермы, полном отсутствии живых спермиев). Данные основного посткоитального теста помогают выявить АСАТ в цервикальной слизи по ее воздействию на подвижность и жизнеспособность сперматозоидов в содержимом шеечного канала. Для соединенных с АСАТ сперматозоидов характерна низкая мобильность и адинамия, маятникообразные движения и феномен «дрожания на месте».
Одновременно со спермограммой выполняется MAR-тест, определяющий количество АСАТ-позитивных подвижных сперматозоидов (при MAR IgG >50% очевиден диагноз «мужское иммунное бесплодие»). 1ВТ-тест устанавливают локализацию АСАТ на поверхности сперматозоида и процент АСАТ-связанных спермиев. Методом проточной цитофлуорометрии (ПЦМ) оценивают концентрацию АСАТ на одном сперматозоиде, спонтанную и индуцированную акросомальную реакцию. При выявлении отклонений в спермограмме и посткоитальном тесте показано проведение ИФА с целью определения спектра АСАТ в сыворотке крови. Дополнительно может проводиться ПЦР-исследование на урогенитальные инфекции (хламидии, микоплазмы, ВПГ, ВПЧ, и др.), определение аутоантител к фосфолипидам, ДНК, кардиолипину, тиреоидным гормонам, HLA-типирование. Иммунологическое бесплодие необходимо дифференцировать от женского и мужского бесплодия другого генеза.
При иммунологическом бесплодии проводят коррекцию иммунного статуса женщины длительными курсами или ударными дозами кортикостероидов, назначают антигистаминные и антибактериальные препараты. В случае аутоиммунных процессов (антифосфолипидный синдром) лечение дополняют низкими дозами аспирина или гепарина. Использование барьерного способа контрацепции (презервативов) в течение 6-8 месяцев с исключением контакта сперматозоидов с иммунными клетками половых органов женщины позволяет уменьшить сенсибилизацию ее организма. Подавление иммунитета повышает шансы зачатия в 50% случаев. Для нормализации иммунных механизмов в женском организме предлагается подкожное введение аллогенных лимфоцитов (мужа/донора) до зачатия или внутривенное введение γ-глобулина — смеси белков плазмы от разных доноров.
Устранение мужского компонента иммунологического бесплодия основано на лечении фоновой патологии, приведшей к образованию АСАТ, и может включать оперативные вмешательства, корригирующие аномалии репродуктивного тракта и кровообращения. Возможно назначение приема протеолитических ферментов, цитостатиков и кортикостероидов.
Основными в лечении иммунологического бесплодия выступают вспомогательные репродуктивные технологии, которые требуют тщательного обследования и подготовки супругов. При искусственной инсеминации осуществляется введение спермы мужа непосредственно в полость матки, минуя шеечный канал, в овуляторном периоде женщины. При наличии способных к оплодотворению, но не достигающих яйцеклетку сперматозоидов, применяется метод искусственного оплодотворения. При низком оплодотворяющем потенциале более высокая частота наступления беременности достигается методом ИКСИ — интрацитоплазматической инъекцией одного качественного сперматозоида в цитоплазму яйцеклетки с последующей подсадкой эмбрионов в полость матки.
Для выхода полноценной яйцеклетки проводится гормональная стимуляция суперовуляции. Получение сперматозоидов у мужчин производят путем эякуляции, забором из яичка (TESA, TESE, Micro-TESE) или придатка яичка (PESA, MESA). В тяжелых случаях мужского иммунологического бесплодия используется донорская сперма. Наличие высокого титра АСАТ в крови женщины является противопоказанием для инсеминации, ИКСИ и ЭКО и требует продолжительного лечения до нормализации их уровня. Перспективно при лечении иммунологического бесплодия использование более качественных морфологически селекционных или генетически здоровых и функционально активных сперматозоидов (ИМСИ и ПИКСИ) и предимплантационной выбраковки или обработки эмбрионов (ассистированный хэтчинг). Для повышения вероятности наступления беременности производится предимплантационная криоконсервация эмбрионов.
Иммунологическое бесплодие имеет достаточно специфический характер: АСАТ вырабатываются на сперматозоиды конкретного мужчины, и при смене партнера появляется возможность беременности. При полноценном лечении с использованием современных ВРТ иммунологическое бесплодие удается преодолеть в большинстве нетяжелых случаев. Вероятность беременности в естественном цикле в отсутствие лечения мужчины с MAR IgG > 50% составляет
источник


Иммунологическим бесплодием принято называть наличие в организме мужчины или женщины реакции, которая агрессивно относится к наличию спермальных антиген. Бесплодие такого типа возникает только тогда, когда при попадании в матку мужской спермы, она воспринимается, как чужеродное тело и начинается активное отторжение. Это говорит о том, что между генами мужчины и женщины возникает конфликт. В таких ситуациях в женском организме спермальные тела вырабатываются самостоятельно и полностью уничтожают мужские половые клетки. Ну и конечно же беременность при таком поведении матки наступать не будет.
У бесплодия такого типа может быть разный механизм. Это будет зависеть от того, где происходят активные иммунные реакции. Если антитело будет вырабатываться в слизи в матки, то тогда сперматозоид полностью обездвиживается и не может попасть в матку. Если же антитела появляются в материнской крови, то воздействие будет идти уже на оплодотворенную яйцеклетку — зиготу.
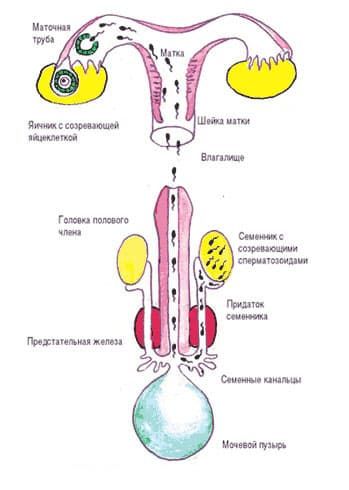
К большому счастью такой тип бесплодия встречается очень редко — только у 7% официально зарегистрированных семей. В большинстве случаев иммунологическое бесплодие возникает, как уже осложнения после заражения болезнями, которые передаются половым путем. При этом антитела которые появляются в организме всячески пытаются прервать беременность или даже не дать ей наступить. Это может вызвать у женщины большие проблемы со здоровьем в то время, когда она будет проходить ЗППП.
Для того же чтобы быть точно уверенным, что у вас есть иммунологическое бесплодие, надо сдать очень много анализов, которые помогут выявить в организме наличие антител. Если есть подозрение на данной бесплодие то вместе с диагностикой данного заболевания стоит проверить свой организм на существование и ЗППП.
На сегодняшний день еще не известно ни одного способа, который бы мог гарантировать 100% лечение данного типа бесплодия. После того, как будет пройдено полное обследование, врачи могут приступить к выявлению иммунных реакций и попытаются уничтожить факторы, которые способствуют их появлению в организме женщины, кроме избавления от антител одновременно проводится и терапия.
Конечно, любой тип бесплодия, в том числе и иммунологического, довольно сложный, но все же выход в такой ситуации есть. Для того, чтобы перебороть такую проблему стоит доложить максимум усилий и обратиться к специалисту, который подскажет все возможные варианты и выберет именно тот способ, который необходим в вашем случае. Для профилактики же данного заболевания нужно практиковать исключительно защищенный секс, который предотвратит появление венерических болезней. Также не стоит забывать о правильном и здоровом образе жизни, наличии в вашем рационе достаточного количества витаминов и полезных веществ. Ну и конечно минимум стресса, максимум положительных эмоций!
источник