Иммунологическое бесплодие – гипериммунное состояние женского или мужского организма, сопровождающееся секрецией специфических антиспермальных антител. Иммунологическое бесплодие проявляется несостоятельностью зачатия и наступления беременности при регулярной половой жизни без контрацепции при отсутствии других женских и мужских факторов инфертильности. Диагностика иммунологического бесплодия включает исследование спермограммы, антиспермальных антител плазмы, проведение посткоитального теста, MAR-теста и других исследований. При иммунологическом бесплодии применяются кортикостероиды, методы иммунизации и вспомогательные репродуктивные технологии.
Иммунологическое бесплодие — наличие патологического антиспермального иммунитета, препятствующего процессу оплодотворения яйцеклетки и имплантации эмбриона. При иммунологическом бесплодии антитела к сперматозоидам – антиспермальные антитела (АСАТ) могут синтезироваться как женским, так и мужским организмом и присутствовать в цервикальной и внутриматочной слизи, сыворотке крови, семенной плазме, семявыводящих протоках. Иммунологический фактор оказывается причиной бесплодия у 5-20% семейных пар в возрасте до 40 лет, при этом АСАТ могут выявляться только у одного супруга или сразу у обоих. Изучением проблемы иммунологического бесплодия занимаются специалисты в области репродуктивной медицины (гинекологи — репродуктологи, андрологи).
В минимальном количестве АСАТ могут присутствовать у фертильных мужчин и женщин, но их фиксация на мембранах большинства сперматозоидов резко ухудшает прогноз на беременность. Это связано с нарушением качества и фертильности спермы — повреждением структуры и резким спадом подвижности сперматозоидов, снижением их способности проникать в цервикальную слизь, блокадой подготовительных стадий (капацитации и акросомальной реакции) и самого процесса оплодотворения яйцеклетки. При наличии АСАТ существенно снижается качество эмбрионов, нарушаются процессы их имплантации в матку, формирования плодных оболочек и развития, что приводит к гибели зародыша и прерыванию беременности на самых ранних сроках.
По своей антигенной структуре сперматозоиды являются чужеродными для женского и для мужского организма. В норме они защищены механизмами супрессии иммунного ответа: у мужчин — гемато-тестикулярным барьером (ГТБ) в яичке и его придатке, иммуносупрессивным фактором спермоплазмы и способностью сперматозоидов к мимикрии (к сорбции и десоробции поверхностных антигенов); у женщин — уменьшением уровня Т-хелперов, Ig и С3-компонента системы комплемента, повышением числа Т-супрессоров во время овуляции.
Под действием определенных неблагоприятных факторов нарушение защитных механизмов делает возможным контактирование спермальных антигенов с иммунной системой и приводит к развитию иммунологического бесплодия. Причинами выработки аутоантител на сперматозоиды и клетки сперматогенеза у мужчин могут выступать острые и тупые травмы мошонки и операции на яичках, инфекции и воспалительные процессы урогенитального тракта (гонорея, хламидиоз, герпес, ВПЧ, орхит, эпидидимит, простатит), врожденные или приобретенные дефекты половых органов (крипторхизм, перекрут яичка, варикоцеле, фуникулоцеле и др.), онкопатология.
Сбой внутриматочной иммунной толерантности и появление АСАТ у женщин в предимплантационный период могут быть спровоцированы инфекционно-воспалительными заболеваниями репродуктивного тракта, повышенным уровнем лейкоцитов в эякуляте партнера (при неспецифическом бактериальном простатите), контактом с иммуногенными сперматозоидами партнера, уже связанными с его аутоантителами.
Формированию АСАТ у женщин также могут способствовать попадание спермы в ЖКТ при оральном/анальном сексе, применение химических средств контрацепции, коагуляция эрозии шейки матки в анамнезе, нарушения при внутриматочной инсеминации, гормональный «удар» при попытке ЭКО, травма при заборе яйцеклеток. Опосредованно стимулировать выработку АСАТ в женском организме могут другие изоантигены, содержащиеся в эякуляте партнера — ферменты и внутриклеточные антигены сперматозоидов, HLA антигены; несовместимость в системах ABO, Rh-Hr, MNSs.
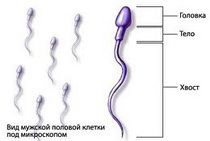
Степень поражения сперматозоидов зависит от класса (IgG, IgA, IgM) и титра АСАТ, места их фиксации, уровня возникновения иммунной реакции. АСАТ, соединяющиеся с хвостовой частью сперматозоидов, затрудняют их движение, а фиксирующиеся к головке — блокируют слияние с ооцитом.
Иммунологическое бесплодие внешне протекает бессимптомно, не имея видимых проявлений у обоих партнеров. У мужчин с аутоиммунным бесплодием обычно сохраняется активный сперматогенез, эректильная функция и полноценность полового акта. При гинекологическом обследовании женщины не обнаруживаются маточные, трубно-перитонеальные, эндокринные и иные факторы, препятствующие зачатию.
При этом у супружеской пары детородного возраста при условии нормального менструального цикла женщины и регулярной половой жизни без предохранения имеет место отсутствие беременности в течение года и более. При АСАТ у женщин из-за дефекта имплантации и нарушения развития эмбриона наблюдается его гибель и отторжение, прерывание беременности на очень ранних сроках, обычно до того, как женщина может ее обнаружить.
При бесплодии комплексное обследование необходимо пройти и женщине, и мужчине — у гинеколога и уролога-андролога соответственно. Иммунологический характер бесплодия диагностируют по результатам лабораторных исследований: анализа эякулята, специальных биологических проб — посткоитального теста (Шуварского– унера in vivo и Курцрока–Миллера in vitro), MAR-теста; 1ВТ-теста, ПЦМ. определения антиспермальных антител плазмы. На время проведения диагностических испытаний прием гормональных и других лекарственных препаратов прерывают.
Наличие мужского фактора иммунологического бесплодия можно предположить при нарушении спермограммы (резком падении количества, искажении формы, агглютинации и слабой активности сперматозоидов, низкой выживаемости спермы, полном отсутствии живых спермиев). Данные основного посткоитального теста помогают выявить АСАТ в цервикальной слизи по ее воздействию на подвижность и жизнеспособность сперматозоидов в содержимом шеечного канала. Для соединенных с АСАТ сперматозоидов характерна низкая мобильность и адинамия, маятникообразные движения и феномен «дрожания на месте».
Одновременно со спермограммой выполняется MAR-тест, определяющий количество АСАТ-позитивных подвижных сперматозоидов (при MAR IgG >50% очевиден диагноз «мужское иммунное бесплодие»). 1ВТ-тест устанавливают локализацию АСАТ на поверхности сперматозоида и процент АСАТ-связанных спермиев. Методом проточной цитофлуорометрии (ПЦМ) оценивают концентрацию АСАТ на одном сперматозоиде, спонтанную и индуцированную акросомальную реакцию. При выявлении отклонений в спермограмме и посткоитальном тесте показано проведение ИФА с целью определения спектра АСАТ в сыворотке крови. Дополнительно может проводиться ПЦР-исследование на урогенитальные инфекции (хламидии, микоплазмы, ВПГ, ВПЧ, и др.), определение аутоантител к фосфолипидам, ДНК, кардиолипину, тиреоидным гормонам, HLA-типирование. Иммунологическое бесплодие необходимо дифференцировать от женского и мужского бесплодия другого генеза.
При иммунологическом бесплодии проводят коррекцию иммунного статуса женщины длительными курсами или ударными дозами кортикостероидов, назначают антигистаминные и антибактериальные препараты. В случае аутоиммунных процессов (антифосфолипидный синдром) лечение дополняют низкими дозами аспирина или гепарина. Использование барьерного способа контрацепции (презервативов) в течение 6-8 месяцев с исключением контакта сперматозоидов с иммунными клетками половых органов женщины позволяет уменьшить сенсибилизацию ее организма. Подавление иммунитета повышает шансы зачатия в 50% случаев. Для нормализации иммунных механизмов в женском организме предлагается подкожное введение аллогенных лимфоцитов (мужа/донора) до зачатия или внутривенное введение γ-глобулина — смеси белков плазмы от разных доноров.
Устранение мужского компонента иммунологического бесплодия основано на лечении фоновой патологии, приведшей к образованию АСАТ, и может включать оперативные вмешательства, корригирующие аномалии репродуктивного тракта и кровообращения. Возможно назначение приема протеолитических ферментов, цитостатиков и кортикостероидов.
Основными в лечении иммунологического бесплодия выступают вспомогательные репродуктивные технологии, которые требуют тщательного обследования и подготовки супругов. При искусственной инсеминации осуществляется введение спермы мужа непосредственно в полость матки, минуя шеечный канал, в овуляторном периоде женщины. При наличии способных к оплодотворению, но не достигающих яйцеклетку сперматозоидов, применяется метод искусственного оплодотворения. При низком оплодотворяющем потенциале более высокая частота наступления беременности достигается методом ИКСИ — интрацитоплазматической инъекцией одного качественного сперматозоида в цитоплазму яйцеклетки с последующей подсадкой эмбрионов в полость матки.
Для выхода полноценной яйцеклетки проводится гормональная стимуляция суперовуляции. Получение сперматозоидов у мужчин производят путем эякуляции, забором из яичка (TESA, TESE, Micro-TESE) или придатка яичка (PESA, MESA). В тяжелых случаях мужского иммунологического бесплодия используется донорская сперма. Наличие высокого титра АСАТ в крови женщины является противопоказанием для инсеминации, ИКСИ и ЭКО и требует продолжительного лечения до нормализации их уровня. Перспективно при лечении иммунологического бесплодия использование более качественных морфологически селекционных или генетически здоровых и функционально активных сперматозоидов (ИМСИ и ПИКСИ) и предимплантационной выбраковки или обработки эмбрионов (ассистированный хэтчинг). Для повышения вероятности наступления беременности производится предимплантационная криоконсервация эмбрионов.
Иммунологическое бесплодие имеет достаточно специфический характер: АСАТ вырабатываются на сперматозоиды конкретного мужчины, и при смене партнера появляется возможность беременности. При полноценном лечении с использованием современных ВРТ иммунологическое бесплодие удается преодолеть в большинстве нетяжелых случаев. Вероятность беременности в естественном цикле в отсутствие лечения мужчины с MAR IgG > 50% составляет
источник
Если вы столкнулись с диагнозом «иммунологическое бесплодие у мужчин или женщин», то у вас, наверняка, возникло немало вопросов.
На самом деле, репродуктивная активность у семейной пары снижена или зачатие невозможно без веских на то причин. Если супруги не имеют в физическом плане патологического изменения, и при этом не получается оплодотворение, может быть поставлен такой диагноз. Он характерен для 6-10% бездетных пар.
Это — выработка против сперматозоидов (АСАТ) антител. Такое патологическое состояние может наблюдаться как в организме любого полового партнера.
Иммунологическое бесплодие у женщин локализуется в цервикальном канале.
В организме мужчины антитела вырабатываются непосредственно сперме, снижая тем самым активность сперматозоидов.
Самые распространенные факторы этого вида бесплодия могут быть вызваны различными причинами. Самые распространенные у мужчин.
- Урогенитальные болезни инфекционного характера (ВИЧ, сифилис, герпес и другие).
- Приобретенные или врожденные дефекты половых органов.
- Онкологическое заболевание (необязательно органа репродуктивной функции).
- Оперативное вмешательство на мошонке или полученные травмы.
У женщины такое бесплодие возникает при:
- Генетических предрасположенностях организма.
- Хирургическом вмешательстве на половые органы, матку, яичники.
- Различных заболеваниях репродуктивной системы.
Вышеперечисленные факторы могут приводить к тому, что иммунная система воспринимает сперматозоиды как что-то ненужное, «чужое» и попросту отвергает их. Тем самым сводя шансы на успешное оплодотворение яйцеклеток к минимуму.
Для подтверждения диагноза понадобится пройти несколько специальных исследований.
Для мужчин – анализ сперматозоидов на наличие антитела в эякуляте, а также анализ крови, подсчет количества сперматозоидов, которые покрыты антиспермальными антителами.
Для женщин – специальный анализ крови и цервикальной слизи на наличие в эякуляте антител.
Обоим партнерам назначают посткоитальную пробу (тест), обследование на совместимость.
Когда диагноз подвержен, и вы точно знаете, что у вас иммунологический фактор, не стоит отчаиваться. Достаточно набрать в интернете «мужское иммунологическое бесплодие форум», чтобы понять, что патология лечится успешно на 100%.
Антитела против сперматозоидов бывают трех видов – IgM, IgА, IgG.
Независимо от класса они могут встретиться как в организме женщины, так и у мужчины (в слизи матки, половых органах, сыворотке крови).
В зависимости от вида АСАТ влияет на взаимодействие в момент оплодотворения половых клеток, нарушая проходимость половых путей, подавляя активность сперматозоидов, блокируя имплантацию эмбриона. Различные факторы вызывают бесплодие.
Причины иммунологического бесплодия различные:
- У мужчин антитела могут начать образовываться при поражении семенных каналов, травмах яичка, разрыве капиллярной системы.
- Причины иммунологического бесплодия у женщин – болезни матки, яичников, генетическая склонность, операции на репродуктивных органах.
- У обоих партнеров – при урологических инфекционных заболеваниях, передающихся половым путем.
Преимущественно такая форма бесплодия характерна для женщин. Риск увеличивается при избыточной массе тела, климаксе, анорексии, частых стрессах, хронических формах соматических заболеваний.
Как лечить иммунологическое бесплодие? Этот вопрос задают многие семейные пары, столкнувшиеся с такой проблемой.
Иммунологическое бесплодие у женщин: лечение
Для устранения причин, вызвавших бесплодие, назначаются антигистаминные препараты с высокими дозами препаратов антибактериального действия, что позволяет повысить иммунитет.
Введение гепарина под кожу и применение аспирина помогают бороться с аутоиммунными процессами.
Во время лечения важно предохраняться во время половой близости на протяжении шести-восьми месяцев (в зависимости от назначенного курса). Так как полноценное оплодотворение яйцеклетки невозможно при пониженном иммунитете.
Для стабилизации защитных систем организма женщины показан ввод смешанной группы белков перед зачатием или использование лимфоцитов от донора.
Изначально требуется устранить патологическую причину, которая вызвала возникновение антител (АСАТ), препятствующих зачатию.
Лечение может состоять из:
- Восстановления репродуктивных функций с помощью хирургических операций.
- Коррекцию кровообращения.
- Назначение лекарственных препаратов в случае необходимости: и цитостатиков или протеолитического характера.
- Оперативного вмешательства на яичке, мошонке.
Кроме этого имеются репродуктивные вспомогательные технологии, которые искореняют причины бесплодия. Однако, такие технологии требуют более тщательной подготовки и дополнительной диагностики.
- ИКСИ (интрацитоплазматические инъекции) – внедрение полноценных жизнеспособных сперматозоидов прямым путем в яйцеклетки, с дальнейшим вводов эмбрионов в матку.
- Инсеминация – введение в маточную полость женщин мужских сперматозоидов, при котором канал матки обходится.
- Искусственное оплодотворение – показано, если имеются функциональные сперматозоиды.
В практически безнадежной ситуации иммунологического бесплодия и неэффективности лечения у мужчин, рекомендуется использовать донорскую сперму.
При проведении искусственного оплодотворения важным фактором являются показания АСАТ. При повышенной концентрации процедура противопоказана, так как она не даст положительного результата. Изначально требуется устранить проблему с помощью продолжительной терапии – до полного восстановления нормальных показателей уровня аспартата.
В успешном зачатии яйцеклетки немаловажным фактором является использование наиболее активных, подвижных, качественных, полноценных, перспективных сперматозоидов. Эмбриональное консервирование с использованием предварительной заморозки или ассистированный хэтчинг гарантирует еще большие вероятности и шанс того, что будет положительный результат после лечения бесплодия.
Выход найти можно из любой ситуации, Важно, чтобы решение было принято совместно супружеской парой.
- АСАТ (оксалоацетат трансаминаза) воспроизводится только в отношении половых клеток каждого конкретного мужчины. Если причина бесплодия не подается лечения, выходом для женщины может стать замена сексуального партнера. В большинстве случаем происходит полноценное зачатие.
- ВРТ (вспомогательные репродуктивные технологии) эффективны в лечении. С их помощью успешно лечится как легкая степень заболевания, так и средней тяжести. Единственное условие – своевременное обращение за оказанием медицинской помощи и выявление причины.
Однозначно, проблема решаема. В любом случае не стоит отчаиваться и опускать руки. Если вы начнете искать в интернете «иммунологическое бесплодие у женщин, форум, кто лечил», и какие результаты дало лечение, то воспрянете духом. На самом деле патология излечивается в 100% случаев. При условии, если вы будете выполнять все рекомендации. Путь непростой, но он дарит шансы на то, что вы станете счастливыми родителями! Можно ли вылечить иммунологическое бесплодие? Ответ очевиден – да.
источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Иммунологическое бесплодие — нарушение репродуктивной функции, обусловленное поражением сперматозоидов антиспермальными антителами (АСАТ) в репродуктивной системе мужчины или женщины.
Распространённость иммунологического бесплодия составляет 5-15% из числа бесплодных супружеских пар. Частота выявления АСАТ у пациентов, состоящих в бесплодном браке, значительно варьирует в зависимости от многих причин, составляя в среднем для мужчин 15%, а для женщин вдвое выше — 32%.


Степень повреждения сперматозоидов зависит от:
• Класса антител
• Количеством выработанных иммунной системой антител АСАТ, их концентрацией
• Плотности покрытия антителами поверхности сперматозоидов
• От того, какие структуры сперматозоидов повреждаются антителами.
В зависимости от сочетания этих повреждающих факторов на репродуктивную систему выявляются следующие патологии:
• Нарушение формирования сперматозиодов, приводящее к олигоспермии, тератотоспермии и азооспермии.
• Снижение и/или подавление подвижности сперматозоидов.
• Подавление процесса взаимодействия половых клеток на этапе зачатия.
• Нарушения проходимости половых путей женщины и семявыводящих путей мужчины.
• Блокирование процесса имплантации эмбриона.
Существуют предрасполагающие факторы, обусловливающие нарушение барьера между кровью и функциональным эпителием яичек и способствующие формированию иммунного ответа на сперматозоиды у мужчин.
Причины развития иммунологического бесплодия у мужчин:
• инфекции передающиеся половым путем (гонорея, хламидиоз и т.п.);
• хронические воспалительные заболевания (простатит, эпидидимит, орхит);
• перенесённые травмы и операции на органах малого таза, мошонки.
• анатомические нарушения (паховая грыжа, варикоцеле, обструкция семявыносяших путей, крипторхизм, перекрут яичка, агенезия семявыносящих протоков).
Причины развития иммунологического бесплодия у женщин:
Причины нарушения иммуносупрессии женщины по отношению к сперматозоидам:
• Инфекции передаваемые половым путём (генитальный герпес, гонорея, хламидиоз, уреаплазмоз и т.д.)
• Хронические воспалительные заболевания женских половых органов
• Генитальный эндометриоз
• Аллергические заболевания
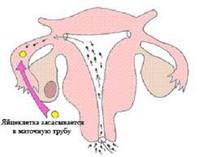
В большинстве случаев АСАТ, образованные в женском организме вызывают локальный иммунный ответ. Наиболее часто иммунная реакция проявляется на уровне шейки матки; в меньшей степени в иммунном ответе принимают участие эндометрий, маточные трубы и влагалище. Это обусловлено тем, что в слизистой оболочке канала шейки матки содержится большое количество плазматических клеток, способных синтезировать компоненты секреторного IgA. Вместе с тем в цервикальной слизи возможно выявление и других иммуноглобулинов, в частности IgG, имеющих значение для развития иммунологического бесплодия.

Исследования производимые при данном виде бесплодия весьма многообразны, единых стандартов диагностики и интерпретации результатов на данный момент не разработано.
1. Коррекция иммунологического статуса мужчины и женщины. Производится с целью снижения числа антиспермальных антител.
2. Применение андрогенов для лечения мужского бесплодия. Дело в том, что при выявлении в организме мужчины АСАТ часто поражается и та часть ткани яичек, которая вырабатывает тестостерон, от которого напрямую зависит активность формирования сперматозиодов.
3. Инсеминация женщины спермой мужа. Производится эндоскопическим способом.
4. Применение вспомогательных репродуктивных технологий (ВРТ).
Автор: Ткач И.С. врач, хирург офтальмолог
источник
Иммунологический фактор бесплодия: причины, последствия, лечение — вот тема сегодняшнего разговора с Викторией Викторовной Залетовой, главным врачом Клиники МАМА.
Иммунологический фактор бесплодия является ключевой причиной отсутствия беременности в случаев бесплодия в паре. При этом частота выявления иммунологического фактора бесплодия у мужчин составляет до 15%, у женщин — до 32%, в связи с чем иммунологическое бесплодие условно разделяют на два вида: мужское и женское.
Что такое «иммунологический фактор бесплодия», кто «виноват» и что делать в данной ситуации.
Иммунологическое бесплодие — нарушение репродуктивных способностей пары в результате поражения мужских половых клеток — сперматозоидов антиспермальными антителами (АСАТ).
АСАТ — иммуноглобулины, белки, которые может вырабатывать наша иммунная система. Антиспермальные антитела могут образовываться как в мужском организме — в крови и/или эякуляте, и приводить к нарушению сперматогенеза и снижению подвижности сперматозоидов; так и в женском — в крови, среде цервикального канала, они обездвиживают сперматозоиды, тем самым препятствуя процессу оплодотворения. В медицинской практике зафиксированы случаи, когда АСАТ выявляют и у мужчины, и у женщины в паре. В чем причины?
Образование антиспермальных тел (АСАТ) у мужчины начинается в момент образования спермы — на этапе полового созревания. Антигены спермы — «новички» в мужском организме и — по идее — должны вызывать защитную реакцию у иммунной системы. Так и было бы, если бы сперматозоиды попадали в кровь, но они находятся в некой «изоляции» и могут «вырваться» только в «экстренных случаях»:
- анатомические нарушения (паховая грыжа, варикоцеле, обструкция семявыносяших путей, крипторхизм, перекрут яичка, агенезия семявыносящих протоков);
- инфекции, передающиеся половым путем;
- травмы и операции на органах малого таза, мошонки;
- хронические воспалительные заболевания (простатит, эпидидимит, орхит);
В перечисленных ситуациях биологический барьер между кровеносными сосудами и семенными канальцами разрушается, «новички» попадают в кровь — организм воспринимает незнакомые клетки как враждебные и защищается.
Специалисты выделяют несколько видов мужских антиспермальных антител, в зависимости от их действия:
спермоиммобилизирующие — частично или полностью обездвиживающие сперматозоиды;
спермоагглютинирующие — «склеивающие» сперматозоиды друг с другом, эпителиальными клетками, макрофагами, фрагментами разрушенных клеток или комками слизи.
Оба вида могут препятствовать оплодотворению и, в ряде случаев, приводят к бесплодию.
Сперматозоиды — «чужаки» для организма женщины, и, по идее, должны вызывать защитную реакцию у иммунной системы. Но если бы так происходило — женщины не беременели бы вовсе. Защитная реакция не происходит, потому что клетки влагалища препятствуют проникновению «чужаков» в иммунную систему.
Исключение могут составлять следующие случаи:
- инфекции, передаваемые половым путём,
- хронические воспалительные заболевания половых органов,
- генитальный эндометриоз,
- аллергические заболевания.
При перечисленных заболеваниях женский организм может начать бороться со сперматозоидами — возникает иммунологический фактор бесплодия.
Подтверждение диагноза «иммунологический фактор бесплодия» включает несколько этапов: обследование мужчины — анализ крови и спермограмма на наличие антиспермальных антител в эякуляте; обследование женщины — исследование цервикальной слизи и анализ крови на антиспермальные антитела; обследование на совместимость партнеров:
- посткоитальный тест, или проба Шуварского: определение совместимости сперматозоидов и шеечной слизи.
- MAR-тест: определение количества сперматозоидов, покрытых антиспермальными антителами. Если более 50% подвижных сперматозоидов покрыты АСАТ — диагностируется иммунологический фактор бесплодия.
- проба Курцрока—Миллера (пенетрационный тест): определение проникающей способности сперматозоидов.
- тест Буво—Пальмера (перекрестный пенетрационный тест): подтверждение пробы Курцрока—Миллера. Обследование предполагает исследование спермы будущего отца и спермы мужчины-донора.
Мужской иммунологический фактор бесплодия преодолевают с помощью вспомогательных репродуктивных технологий (ВРТ), в частности — ICSI-MAQS (микроскопический анализ качества сперматозоидов для интрацитоплазматической инъекции в яйцеклетку) или PICSI (физиологический выбор лучшего сперматозоида для интрацитоплазматической инъекции в яйцеклетку) в рамках программы экстракорпорального оплодотворения (ЭКО).
Женский иммунологический фактор бесплодия может быть излечен консервативным способом — рекомендуют кондом-терапию или медикаментозное лечение, направленное на подавление продукции АСАТ у партнеров. Если лечение неэффективно, целесообразнее планировать беременность с помощью вспомогательных репродуктивных технологий — программы внутриматочной инсеминации (ВМИ). При отсутствии эффекта от инсеминации рекомендуют ЭКО с применением ICSI-MAQS (микроскопический анализ качества сперматозоидов для интрацитоплазматической инъекции в яйцеклетку) или PICSI (физиологический выбор лучшего сперматозоида для интрацитоплазматической инъекции в яйцеклетку).
В случае сочетанного иммунологического бесплодия в паре также помогают вспомогательные репродуктивные технологии.
источник
Теоретически иммунологические факторы могут действовать на любом этапе репродуктивного процесса, ведущего к имплантации, так как герминативные клетки, оплодотворенная яйцеклетка так же, как и гормоны, ткани и другие секреты, могут •быть потенциальными антигенами и способны вызывать иммунные реакции. Клетки и белки чужеродного генетического происхождения (в данном контексте мужского) могут быть причиной изоиммунизации у женщин. Кроме того, как у женщин, так и у мужчин может наблюдаться аутоиммунизация против компонентов половых путей («собственные» антигены).
В этой главе рассматриваются вопросы иммунологии бесплодия у мужчин и женщин, и освещается современный уровень знаний относительно проблем, имеющих непосредственное отношение к клинике. В тех вопросах, где явно недостаточно сведений относительно функционирования определенных механизмов у человека привлекаются обобщенные экспериментальные данные, определяя тем самым области потенциально интересные для клинициста. Читатель, желающий ознакомиться с этой проблематикой более подробно, может обратиться к представительным обзорам Katsh (1959), Menge (1970), Shul-man (1972), Behrman, Menge (1973), Behrman (1975), Rumke, Hekman (1975) и к соответствующим разделам монографий Diczfalusy (1974), Hafez (1976), Scott, Jones (1976), Boettcher (1977), Edidin, Johnson (1977), Insler, Bettendorf (1977).
Действие потенциально иммуногенных компонентов может проявляться у мужчин, вызывая аутоиммунизащда, и у женщин, вызывая изоиммунизацию. Прежде чем описывать иммунологические механизмы и клинические проявления таких ситуаций следует рассмотреть природу антигенов.
Сперма человека содержит свыше 30 антигенов; способных вызвать сильную активность антител при введении экспериментальным животным. Некоторые из этих антигенов строго-специфичны для сперматозоидов или семенной плазмы (тканевая специфичность), тогда как другие могут распределяться в сперме человека, молоке, слюне, носовой слизи, желудочном соке, моче, цервикальной слизи, шейке матки 1 , эндометрии, Mat-точных трубах, яичках, почках и печени, так же как и в алкогольных вытяжках яичек, желтого тела, мозга и определенных,, широко распространенных микроорганизмах. Специфические спермантигены могут проявлять генетический полиморфизм (вариабельность) в пределах одного организма, а некоторые могут быть идентичны спермантигенам других видов.
Так как теоретически они имеют отношение к бесплодию; основные усилия следует направить на характеристику антигенов, специфичных для самих сперматозоидов (клеточно-специфические антигены). Используя методику фиксации антител, можно показать наличие собственных антигенов в акросоме,. срединном сегменте и хвосте сперматозоида. Некоторые из них могут вызывать иммунологическое бесплодие. Антигены семенной плазмы могут покрывать поверхность сперматозоида в пре>-делах половых путей мужчины (даже в пределах придатка яичка) и их неполное удаление, путем отмывания сперматозоидов, может быть причиной ошибочной характеристики антигенов,, присущих самой зародышевой клетке. Биологическая роль антигенов, исходящих из семенной плазмы и покрывающих сперматозоид может заключаться в маскировании наиболее важных собственных антигенов сперматозоида. Вместе с тем антигены семенной плазмы могут быть модифицированы бактериями in vitro и in vivo и вызывать иммунный ответ, в результате которого возникает бесплодие.
Существуют некоторые данные о том, что в организации антигенного профиля сперматозоида; принимают участие антигены системы гистосовместимости (группы крови по системе АВО и лейкоцитарные антигены по системе HLA) и дифференцированные аллоантигены. Следует заметить, что последние являются скорее индивидуально специфическими; чем клеточно-специфическими и поэтому не могут принимать участия в аутоиммунных реакциях. Ферменты сперматозоидов также участвуют в формировании антигенных свойств. Гиалуронидаза, акросин и лактат дегидрогеназа-Х (.ЛДГ-Х) интенсивно исследовались, но из них только ЛДГ-Х является спермоспецифической и дает основание предполагать наличие связи: с иммунояогическим бесплодием.
ИЗОИММУНИЗАЦИЯ ЖЕНЩИН СПЕРМАНТИГЕНАМИ
Естественное введение спермы в половые пути женщины может вызвать иммунный ответ, афферентная и эфферентная ветви которого изображены на; рис. 32.
Рис. 32. Иммунологические механизмы, включающиеся в процесс изоиммунизации на спермантигены. Антигены обрабатываются макрофагами и информация о них доставляется в ретикулоэндотелиальную систему по афферентной ветви. Эфферентная ветвь включает как локальный, так и системный эффекты, реализующиеся путем формирования антител и клеточно-опосредованных иммунных реакций (с разрешения J. S. Scott a. Acad. Press).
1 — спермантигены; 2 — иммуногенный стимул; 3 — афферентная ветвь; 4 — обработка макрофагами; 5 — ретикуло-эндотелиальная система; 6 — изоиммунизация; 7 — эфферентная ветвь; 8 — клеточный иммунитет; 9 — локальный секреторный иммунитет; 10 — системный иммунитет; II — гуморальный (антиспермантитела); 12 — клеточный (? включающий запоминание и трансплантационный иммунитет).
источник
Еще один вид бесплодия это иммунологическое бесплодие. Такое бесплодие связано с выработкой, как у мужчин, так и у женщин, антиспермальных антител. Так иммунная система человека влияет на работу репродуктивной функции. Заболевание это никак не проявляется и не имеет симптомов, кроме отсутствия возможности зачать ребенка.
Иммунологическое бесплодие – это заболевание при котором у пары отсутствуют заболевания мочеполовой системы а забеременеть не получается. Точно установить причину патологии проблематично.
Еще недавно ученые были уверены, что такое бесплодие может быть только у женщины. Проявляется это заболевание у женщины так, иммунные клетки которые должны отвечать за овуляцию просто не воспринимают сперматозоиды определенного мужчины. Иммунитет женщины принимает сперматозоиды как инородный объект и отторгает их. Поэтому оплодотворение яйцеклетки не происходит.
На сегодняшний день, в результате исследований, удалось доказать, что и иммунитет мужчины способен вырабатывать антиспермальные антитела. Таким образом, яички мужчины могут просто не воспринимать женскую фолликулярную жидкость, и даже собственные биологические компоненты. Такой процесс называется аутоиммунизацией.
При аутоиммунизации у мужчины, в организме происходит сопротивление между собственными биологическими материалами и антителами. Иммунные клетки, которые находятся в яичках, производят антитела. Антитела воспринимают биологический материал как инородный объект. В результате сопротивления с собственными антителами сперматозоиды просто склеиваются между собой, значительно снижая качество спермы. Способность мужчины к оплодотворению, в этом случае, также существенно снижается.
Самым основным признаком иммунологического бесплодия является отсутствие наступления беременности при нормальном качестве спермы у мужчины и нормальной работы репродуктивных органов у женщины.
Главная причина такого бесплодия на сегодняшний день неизвестна. Врачи говорят о наследственности и индивидуальной особенности человека, как об основной причине иммунологического бесплодия.
Особенности иммунного фактора бесплодия:
- Аутоиммунизация.
- Антитела.
- Сильная чувствительность женской иммунной системы к сперме конкретного мужчины. В этом случае, женские антитела уничтожают сперматозоиды, воспринимая их, как инородный объект.
По статистике, чаще такое бесплодие встречается у мужчин при наличии заболеваний и травм органов мошонки. Например: орхит, водянка, травмы яичек, варикоцеле, застой спермы или киста семенного канатика.

Определить степень иммунологического бесплодия можно с помощью спермограммы с MAR тестом (анализа спермы). В анализе будут приведены показатели титра АСАТ и класса IgG, IgA, IgM. Также в анализе будет показан уровень возникновения иммунной реакции и места фиксации сперматозоидов. Подробнее о том, как сдавать и расшифровывать результаты этого анализа читайте в этой статье.
Видео из лаборатории о спермограмме с MAR тестом:
По причине иммунологического бесплодия от 6 до 22% пар не могут зачать ребенка. Если в течение года попыток забеременеть результата нет, то одной из возможных причин бесплодия может быть именно нарушения связанные с иммунитетом родителей, одного или двух. Бывает, что при таком бесплодии беременность наступает, но очень высока вероятность выкидыша на ранних сроках.

Одним из методов выявления этого заболевания является посткоитальный тест. Пред сдачей этого теста нужно чтобы мужчина уже прошел свое тестирование (спермограмму). Если по результатам спермограммы будет понятно, что мужчина здоров, то назначается посткоитальный тест.
Его сдает женщина на 14 день начала цикла менструации. Для теста на исследование берут цервикальную жидкость. Перед сдачей теста пара должна воздерживаться три дня от половой близости. Сам тест сдается спустя 10 часов после полового акта, но не дольше одних суток (24 часа). По результату исследований будет ясно, есть ли в фолликулярной слизи сперматозоиды. Если они присутствуют, будет определена их активность.

Помимо посткоитального теста иммунологическое бесплодие можно определить дополнительными исследованиями, которые в себя включают:
- метод латексной агглютинации;
- смешанный антиглобулиновый тест;
- с помощью иммуноферментного анализа;
- при помощи пенетрационного теста.
Также для установления диагноза и определения уровня АСАТ (антиспермальных антител) нужно дополнительно сдать фолликулярную жидкость и кровь.
Полезное и интересное видео:
В связи со сложностью определения точных причин такого бесплодия назначение лечения очень проблематично. Лечение включает в себя несколько способов: хирургическое вмешательство, иммуностимулирующие и андрогенные препараты.
Помимо вышеперечисленных способов лечения, дополнительно назначаются антибиотики, антигистаминные препараты и противовоспалительные средства. Чтобы исключить случайное зачатие в период действия сильнодействующих препаратов пара во время полового акта обязана использовать презерватив для контрацепции.
Время курса лечения иммунологического бесплодия составляет от полугода до 8 месяцев. В результате лечения чувствительность организма к спермальным антигенам снижается, вероятность зачатия увеличивается.
За три дня до овуляции женщине назначаются препараты для повышения уровня эстрогена. Иногда назначается курс гормональных препаратов а также кортикостероиды.
Иммунологическое бесплодие поддается лечению при помощи инсеминации (исскуственного ввода спермы в женский организм). ЭКО (экстракорпоральное оплодотворение) – это еще один действенный метод зачатия ребенка при иммунологическом бесплодии. В этом случае оплодотворение яйцеклетки происходит в специальной среде вне женского организма. После оплодотворения производится подсадка змбриона в полость матки.
Многие семейные пары пытаются лечить иммунологическое бесплодие способами и рецептами народной медицины. Обязательно проконсультируйтесь у врача, не стоит заниматься самолечением.
Если у семейной пары не получается зачать ребенка в течение года это серьезная проблема, возможно это иммунологическое бесплодие. Чтобы добиться появления ребенка на свет не стоит пускать ситуацию на самотек, нужно обязательно обратиться к врачу.
Не забывайте писать комментарии и ставить оценку статье звездочками. Спасибо за посещение сайта, надеемся мы смогли вам помочь.
источник
Бесплодие — это серьезная проблема, с которой сталкивается немало семей. Причины его могут быть разнообразными. В этой статье речь пойдет об одной из наиболее «загадочных», связанной с «поведением» иммунитета.
Бесплодие — это серьезная проблема, с которой сталкивается немало семей. Причины его могут быть разнообразными. В этой статье речь пойдет об одной из наиболее «загадочных», связанной с «поведением» иммунитета.
Существование сложных многоклеточных организмов, в том числе человека, невозможно без нормальной работы иммунной системы. Она защищает нас и от микроорганизмов, паразитирующих внутри нашего тела, и от собственных клеток, которые перестали выполнять свои функции и стали бесконтрольно размножаться (такие клетки называют «раковыми»).
Чтобы обеспечить выполнение этих задач, в иммунной системе существуют специальные клетки. Они способны распознавать «чужаков» и убивать их. В борьбе с инфекциями участвуют также иммуноглобулины (антитела). Они образуются после контакта иммунных клеток с микроорганизмом-паразитом и являются строго специфичными: например, антитела против возбудителя ветряной оспы способны бороться только с этим возбудителем, но не с возбудителем кори, краснухи и т.п.
Чтобы уничтожить «чужих», иммунные клетки должны уметь отличать их от «своих». В основе такого распознавания лежат различия в структуре антигенов — специальных биологических молекул, которые могут вызвать в организме иммунный ответ клеток. Наиболее важным для такого распознавания являются антигены так называемого главного комплекса гистосовместимости (совместимости тканей), которые у человека названы лейкоцитарными, или HLA.
Каждый человек имеет уникальный набор HLA-антигенов. Все типы клеток организма, которые имеются у младенца на момент рождения, считаются «своими»: иммунные клетки на них в норме не реагируют. Все, что от них отличается, становится «чужим». Так, «чужими» являются проникшие в организм бактерии и глисты; «чужими» становятся и свои клетки, если в них проникли вирус или бактерия с внутриклеточным циклом развития (например, хламидия), или произошла их злокачественная трансформация. «Чужими» для мужчин иногда оказываются их собственные сперматозоиды, для женщин — сперматозоиды, проникшие в половые пути, и даже развивающийся внутри материнского организма плод.
Не все клетки организма доступны иммунным клеткам, циркулирующим в крови. Некоторые отделены специальными барьерами: например, нейроны головного мозга — гемато-энцефалическим; клетки сперматогенеза, обеспечивающие образование сперматозоидов в яичках, — гемато-тестикулярным (в первом случае барьеры существуют между кровью и тканью головного мозга, во втором — между кровью и тканью яичка). Это связано с тем, что в процессе развития у некоторых клеток появляются белковые структуры (антигены), отсутствовавшие на момент рождения и в первые дни жизни. Например, сперматозоиды появляются у мальчиков в 11-13 лет и содержат элементы, необходимые для оплодотворения и ранее не контактировавшие с иммунными клетками. Поэтому на них может развиться иммунный ответ, то есть начнут вырабатываться антитела. Чтобы этого избежать, сперматозоиды развиваются в специальных трубочках — сперматогенных канальцах, стенки которых пропускают кислород, гормоны, питательные вещества, но не позволяют контактировать с циркулирующими в крови иммунными клетками. На развивающихся сперматогенных клетках и зрелых сперматозоидах отсутствуют антигены HLA-комплекса. Кроме того, специальные клетки яичка вырабатывают особое вещество — Fas — которое вызывает быструю смерть лимфоцитов, проникших в ткани яичка. В снижении активности иммунных реакций участвуют и клетки яичка, вырабатывающие мужской половой гормон тестостерон (известно, что андрогены — мужские половые гормоны, как и другие стероидные гормоны, способны ослаблять иммунный ответ).
Беременность на первый взгляд напоминает в иммунологическом плане ситуацию, возникающую при трансплантации органа, поскольку плод содержит как антигены матери, так и «чужие» антигены отца. Однако иммунологическое распознавание чужеродного плода при нормально протекающей беременности обычно не приводит к его отторжению.
В чем причины иммунологической привилегированности плода?
Во-первых, эмбрион и образующийся после внедрения в матку трофобласт 1 не имеет на своей поверхности высокоиммуногенных антигенов HLA. Кроме того, поверхность зародыша покрыта специальным слоем, защищающим его от иммунного распознавания.
Во-вторых, во время беременности в организме женщины происходят сложные перестройки, в результате которых иммунная система начинает вырабатывать меньше тех клеток, которые способны убивать «чужие» клетки, в том числе клетки плода. Многие из этих антител не только не повреждают развивающийся зародыш, но даже защищают его, предотвращая распознавание клетками-киллерами тканей плода.
Клетки плаценты выполняют функцию «универсальной карты идентичности», позволяя клетке плода быть распознанной как не чужеродной и избежать атаки специальных НК-лимфоцитов, которые убивают клетки, лишенные HLA. Одновременно трофобласт и печень плода производят вещества, также угнетающие активность иммунно-активных клеток. Как и клетки яичка, клетки плаценты вырабатывают фактор, приводящий к гибели лейкоцитов. Клетки материнской части трофобласта вырабатывают вещество, подавляющее работу клеток, убивающих чужеродные. Эти и ряд других механизмов обеспечивают подавление иммунологической реактивности материнского организма по отношению к развивающемуся плоду. Система антибактериального иммунитета (защита от бактерий) во время беременности, наоборот, активируется: увеличивается количество клеток-пожирателей (гранулоцитов и моноцитов) в крови матери, наблюдаются признаки их активации. Это обеспечивает надежную защиту от микроорганизмов-паразитов в условиях снижения активности специфического клеточного иммунитета.
1 Трофобласт — часть зародыша, контактирующая с маткой и обеспечивающая обмен веществ с материнским организмом.
Несмотря на надежную защиту развивающихся половых клеток, иногда возникают ситуации, когда они подвергаются иммунной атаке.
У мужчин наиболее частой причиной этого являются острые и тупые травмы яичек, сопровождающиеся разрывом семенных канальцев и капилляров. При этом антигены попадают в кровь и вызывают иммунный ответ. Если травма была сильной, воспалительный процесс в яичке — орхит — обычно захватывает весь орган, при этом функциональная ткань, которая обеспечивает выработку сперматозоидов, замещается на соединительную ткань. Если повреждение не сопровождалось ярко выраженными болезненными ощущениями, то за счет естественных восстановительных процессов целостность гематотестикулярного барьера восстанавливается и выработка спермы продолжается. Но специфические антиспермальные антитела (АСАТ), которые начали образовываться после травмы, продолжают циркулировать в сперме и крови и нарушают образование сперматозоидов. При этом объектом иммунной атаки оказываются все сперматозоиды, образовавшиеся как в травмированном, так и в здоровом яичке. В присутствии АСАТ снижается подвижность сперматозоидов, происходит их агглютинация (склеивание между собой), оказывается практически невозможным прохождение через цервикальный канал в матку, нарушается акросомальная реакция 2 , без чего невозможно оплодотворение яйцеклетки даже «в пробирке». Такая ситуация получила название «аутоиммунное мужское бесплодие». По различным данным, от 5 до 40% мужчин из бесплодных пар имеют АСАТ; по результатам наших исследований, более чем у 20% мужчин причиной бесплодия являются аутоиммунные реакции против сперматозоидов. При этом некоторые врожденные особенности строения половых органов, например варикоцеле 3 , в несколько раз повышают риск развития иммунного бесплодия и орхита после субклинической травмы мошонки.
2 Акросомальная реакция — выброс специальных ферментов при контакте сперматозоида с яйцеклеткой.
3 Варикоцеле — расширение вен семенного канатика у мужчин. Семенной канатик — это анатомическая структура, в которую среди прочих входит семявыносящий проток, артерии, вены, лимфатические сосуды.
Другой причиной развития антиспермального иммунитета являются урогенитальные инфекции. Принято считать, что одной из причин образования АСАТ на фоне инфекций является способность многих бактериальных, вирусных и грибковых организмов прикрепляться к мембране сперматозоидов и вызывать перекрестные реакции (в этом случае антитела вырабатываются не только к возбудителям инфекции, но и к сперматозоидам). Среди наиболее значимых следует назвать хламидии, микоплазмы, вирусы герпеса и папилломавируса. Следует подчеркнуть, что не все антитела, вырабатывающиеся против антигенов сперматозоидов, представляют угрозу для их функционирования. Из более чем 40 антигенов сперматозоидов и семенной плазмы лишь несколько связаны с нарушением оплодотворяющей способности.
АСАТ в слизи, вырабатываемой в канале шейки матки (цервикальной слизи), у женщин встречаются в несколько раз чаще (30-40%), чем у мужчин. Имеются некоторые количества АСАТ и у женщин, способных к зачатию. Возможно, они участвуют в устранении неполноценных сперматозоидов. Когда АСАТ у женщин становится слишком много, эти антитела мешают оплодотворению. В половине случаев выработка у женщины собственных АСАТ является реакцией на попадание в половые пути спермы партнера, содержащей антитела, что делает сперму более иммуногенной. Кроме присутствия мужских АСАТ, антитела против сперматозоидов могут вырабатываться у женщин под действием различных факторов, например при наличии урогенитальных инфекций, при увеличенном содержании лейкоцитов в сперме мужчин с неспецифическим бактериальным простатитом (воспалением предстательной железы), при повышенном количестве сперматозоидов в сперме и т.д. Но в случае наличия АСАТ в сперме у постоянного партнера, особенно класса IgA, антиспермальные антитела в слизи шейки матки у женщин вырабатываются практически всегда, и это резко уменьшает вероятность беременности.
Проявлением действия женских АСАТ является неспособность сперматозоидов проникать в слизь шейки матки. Это можно обнаружить при специальных лабораторных тестах, оценивающих взаимодействие сперматозоидов с цервикальной слизью.
Имеются многочисленные данные о снижении успеха ЭКО и ПЭ 4 в тех случаях, когда АСАТ имеются не только в цервикальной слизи, но и в сыворотке крови женщин. По некоторым данным, АСАТ у женщин могут также оказывать вредное влияние на раннее развитие эмбриона, имплантацию и течение беременности. При наличии антиспермальных антител часто наблюдается невынашивание беременности.
Длительное присутствие в матке вирусов и условно-патогенных микроорганизмов также может приводить к иммунологическому бесплодию. Такие микробы являются препятствием для создания в предымплантационный период местного угнетения иммунитета внутри матки. Это угнетение необходимо для формирования барьера, который защищает зародыш от антител, способных его атаковать. Поэтому инфекцию рассматривают как один из основных факторов развития привычного выкидыша: женщины, страдающие невынашиванием беременности, в 60-75% случаев страдают хроническим воспалением эндометрия (внутреннего слоя матки).
Антифосфолипидный синдром (АФС) также является одной из причин привычного выкидыша. Зачастую единственным проявлением антифосфолипидного синдрома является именно невынашивание беременности. Фосфолипиды являются важной составляющей всех биологических мембран (к биологическим мембранам относятся стенки клеток), поэтому появление антифосфолипидных антител может стать причиной воспаления, вызвать нарушения свертывания крови, следствием чего являются недостаточность кровообращения в плаценте, тромбозы кровеносных сосудов, инфаркты (не снабжающиеся кровью участки) в плаценте. АФС обнаруживают у 27-31 % женщин с привычным выкидышем. Полагают, что у женщин с АФС образование тромбов в плаценте обусловливает потерю плода в основном после 10 недель беременности. Частота АФС повышается на 15% с каждым следующим выкидышем. Таким образом, АФС является не только причиной, но и осложнением привычного невынашивания беременности.
При выявлении аутоиммунного бесплодия и причин невынашивания беременности имеет значение обнаружение аутоантител к гормонам, то есть антител к своим гормонам (наиболее изучен гормон ХГЧ), а также антитела против ДНК.
4 ЭКО и ПЭ — экстракорпоральное оплодотворение и перенос эмбриона, метод оплодотворения яйцеклетки «в пробирке» с последующим переносом зародыша в матку.
Проявлением иммунологического конфликта матери и плода является гемолитическая болезнь плода. Она возникает, когда на эритроцитах плода имеется специфический антиген, полученный от отца и называемый резус-фактором, а у матери такой белок отсутствует (резус-отрицательная кровь). В результате у женщины могут начать вырабатываться антитела против эритроцитов плода, которые приводят к разрушению его эритроцитов. Поскольку в норме плод достаточно эффективно изолирован от иммунных клеток матери, такая реакция обычно развивается уже перед самыми родами или в момент родов, и плод не успевает пострадать. Но эти антитела будут представлять опасность для следующего резус-положительного плода.
Еще одним иммунологическим осложнением является тромбоцитопения — повреждение под действием материнских антител тромбоцитов плода. Обычно при этом снижены вес плода, содержание в крови лейкоцитов и лимфоцитов. Установлено, что в 3 из 4 случаев тромбоцитопения сопровождается наличием антител против отцовских HLA-антигенов плода.
Все описанные синдромы являются отражением гипериммунных состояний, то есть таких состояний, при которых система иммунитета работает слишком активно. Но в последние годы появились данные, что причиной патологии беременности может явиться и отсутствие иммунологического распознавания матерью плода. Было показано, что женщины, близкие с мужем по HLA-антигенам, например родственники, часто страдают привычным выкидышем. Исследования HLA-антигенов матери и плода при невынашивании беременности показали, что совпадающие с матерью по HLA-антигенам II класса плоды отторгаются чаще всего. Оказалось, что развитие «терпимости» иммунной системы матери к плоду при беременности является разновидностью активного иммунного ответа, предполагающего на начальном этапе распознавание и активную переработку чужеродных антигенов. Трофобласт, распознанный организмом матери, обусловливает не реакцию отторжения, а реакцию наибольшего иммунологического благоприятствования.
Диагностика иммунологического бесплодия должна быть комплексной, причем к специалистам — андрологу и гинекологу — должны обратиться обязательно оба супруга.
Мужчинам. Первым и обязательным этапом обследования является комплексное исследование спермы. Обнаружение АСАТ любым из лабораторных методов (MAR-тест, 1ВТ-тест, ИФА/ELISA И др.) позволяет установить существование аутоиммунных реакций против сперматозоидов. Если АСАТ покрыты более 50% подвижных сперматозоидов, ставится диагноз «мужское иммунное бесплодие». Поскольку нередко причиной развития антиспермального иммунитета являются уро-генитальные инфекции, обязательно надо обследоваться на хламидии, микоплазмы, герпес и другие возбудители. При этом нужно помнить, что выявляемость этих микроорганизмов у мужчин даже при использовании современных методов диагностики, таких как, полимеразная цепная реакция (метод обнаружения микроорганизмов по их специфическим ДНК и РНК), далеко не 100%.
Лечение мужского иммунного бесплодия базируется на данных об установленных причинах формирования данного состояния и может включать оперативные вмешательства, направленные на устранение непроходимости семявыносящего тракта и нарушений кровообращения, назначение различных гормональных и негормональных лекарственных препаратов, применение методов отмывки спермы для удаления антител с поверхности сперматозоидов с сохранением их функции. Нужно быть готовым к тому, что лечение может быть длительным. При отсутствии эффекта лечения в течение года может быть рекомендовано ЭКО и ПЭ с применением инъекции сперматозоидов непосредственно внутрь яйцеклетки (ИКСИ).
Женщинам. К развитию иммунологических нарушений часто приводят хронические воспалительные заболевания и генитальные инфекции, нередко у женщины обнаруживается эндометриоз (разрастание эндометрия — клеток внутреннего слоя матки в нетипичных местах).
Для обнаружения АСАТ у женщин применяются посткоитальный тест (ПКТ), тест взаимодействия сперматозоидов с ЦС «на стекле» (проба Курцрока-Мюллера) и непосредственное определение АСАТ. Привычный выкидыш, определяемый как две и более клинически обнаруженных потерь беременности на сроке до 20 недель, требует кариотипирования — определения числа и целостности хромосом в клетках трофобраста: в основе 60-70% ранних самопроизвольных выкидышей лежит изгнание генетически неполноценного эмбриона; полезно также определение динамики бета-ХГЧ и прогестерона.
При обследовании пациенток с невынашиванием беременности в обязательном порядке проводят исследование крови на аутоантитела.
Обычно проводится определение антител к фосфолипидам, к ДНК и к факторам щитовидной железы. Важное диагностическое значение для распознавания иммунных форм невынашивания беременности имеет определение генотипа супругов по HLA-антигенам II класса. Желательно проведение определения HLA-DR и -DQ антигенов.
Методы лечебных воздействий при иммунологических нарушениях репродуктивной функции у женщин зависят от характера нарушений, степени нарушений и общего состояния пациентки. Обычно лечение включает три этапа:
- общая иммунокоррекция и лечение сопутствующих заболеваний;
- подготовка к беременности;
- лечение во время беременности.
Обнаружение АСАТ в цервикальной слизи требует регулярного применения презервативов для исключения попадания спермы в половые пути и уточнения причин иммунных реакций против сперматозоидов: АСАТ у мужа, инфекции, гормональные нарушения и др. Лечение включает меры специфического и неспецифического характера, в качестве дополнительного способа лечения может быть рекомендована внутриматочная инсеминация спермой мужа. При обнаружении значимых количеств АСАТ в сыворотке крови лечение может потребовать продолжительно периода. Инсеминации и ЭКО до нормализации количества АСАТ в крови не рекомендуются.
Общая иммунокоррекция и лечение сопутствующих заболеваний направлено на устранение иммунодефицитного состояния, выявленного при обследовании пациентки, лечение воспалительных заболеваний половых органов и генитальных инфекций, устранение дисбактериоза кишечника и влагалища, проведение общеукрепляющего лечения и психологической реабилитации. При этом нужно иметь в виду, что в настоящее время, несмотря на довольно значительное количество препаратов, обладающих иммуномодулирующими свойствами, их применение при лечении беременных резко ограничено. По-прежнему активно применяется иммуноцитотерапия — введение женщине лимфоцитов мужа или донора. Метод может успешно применяться как при избыточных реакциях иммунной системы матери против плода, так и при совпадении генотипа супругов по HLA.
Наиболее успешным лечение невынашивания беременности бывает тогда, когда иммунологическая подготовка к беременности начинается как минимум за месяц до прекращения предохранения. Конкретные лечебные мероприятия определяет врач-гинеколог. Независимо от исходных нарушений, после наступления беременности большое значение имеет периодическое исследование показателей гемостаза и анализа крови на аутоантитела с проведением адекватной коррекции в случае обнаружения отклонений.
Собственный опыт и данные научной литературы свидетельствуют, что бесплодие и осложнения беременности, связанные с нарушением регулирующей функции иммунной системы, в настоящее время в большинстве случаев излечимы.
источник


