В рамках генетического тестирования болезней органов дыхания мы предлагаем анализ генетической предрасположенности к бронхиальной астме и хронической обструктивной болезни легких.
Бронхиальная астма – хроническое воспалительное заболевание бронхов аллергической природы. Эта болезнь приводит к повышению чувствительности дыхательных путей к аллергенам и различным вредным веществам (бытовая химия, табачный дым и другие), контакт с которыми провоцирует приступы удушья.
Изменения в бронхах при бронхиальной астме можно поделить на обратимые и необратимые. К обратимым изменениям относят:
— отек бронхов, ведущий к сужению просвета в них,
— гиперсекрецию – повышенное выделение вязкого секрета, еще больше сужающего просвет бронхов,
— гиперреактивность – очень высокая чувствительность к раздражителям окружающей среды.
Эти изменения приводят к острым приступам удушья, отдышки, кашля. Однако обратимые изменения можно практически полностью вылечить при своевременно начатом адекватном лечении. При отсутствии правильного лечения органы дыхания претерпевают необратимые изменения, такие как:
— эмфизема легких
— утолщение стенки бронхов
— склероз легочной ткани.
Бронхиальная астма чаще проявляется в детском возрасте. По различным данным в нашей стране этим заболеванием страдают 5-10% детей. Однако при правильном лечении дети достаточно часто полностью излечиваются от бронхиальной астмы, «перерастая» заболевание к подростковому возрасту.
Бронхиальную астму относят к мультифакториальным заболеваниям, причиной которых могут быть внутренние и внешние факторы. К внутренним факторам относят наследственную предрасположенность и нарушение иммунного ответа. Причем риск бронхиальной астмы выше не только у тех, чьи родители болели астмой, но и у тех, чьи родители страдали различными аллергиями. К внешним факторам этого заболевания относят разнообразные аллергены: домашняя пыль, пыльца, бытовая химия, пищевые аллергены. А так же табачный дым, профессиональные вредности, сопутствующие вирусные и бактериальные инфекции, высокая влажность воздуха, колебания температуры, физическая нагрузка, аспирин, при повышенной к нему чувствительности.
Для анализа наследственной предрасположенности к бронхиальной астме мы исследуем следующие гены:
— гены, участвующие в выведении вредных веществ из организма — GSTM1, GSTT1, GSTP1, NAT2;
— ген, кодирующий основной компонент бронхиальной жидкости – CC16;
— гены, участвующие в воспалительных процессах – IL4, IL4R, TNFA;
— ген, продукт которого, участвует во многих физиологических процессах организма, таких как расширение сосудов, проведение нервных импульсов, реакции иммунной системы – NOS3.
Анализ на генетическую предрасположенность к бронхиальной астме входит в исследование для составления генетического паспорта. Так же можно провести такой анализ отдельно. Особенно мы рекомендуем провести исследование на предрасположенность к бронхиальной астме детям, чьи родственники болеют астмой или аллергическими заболеваниями, а так же людям подверженным воздействию вредных веществ (газы и пары серы, аммиака, кислот и щелочей, минеральная и биологическая пыль), часто страдающими острыми респираторными заболеваниями, курильщикам.
Хроническая обструктивная болезнь легких (ХОБЛ) – болезнь легких, приводящая к устойчивому нарушению движения воздушного потока из легких. (Слово обструктивная происходит от латинского «obstructio» — помеха, преграда.) Обструкция дыхательных путей — нарушение проходимости дыхательных путей. В случае ХОБЛ обструкция дыхательных путей обычно является следствием необычного воспалительного процесса в ответ на воздействие патогенных газов или частиц. Основными симптомами ХОБЛ являются отдышка, патологическая отдышка (смесь слюны и мокроты в дыхательных путях), кашель. По данным ВОЗ в 2005 году от ХОБЛ умерло более трех миллионов человек, что составило 5% всех случаев смерти во всем мире за этот год. Причем по прогнозам общая смертность от ХОБЛ в ближайшие 10 лет возрастет на 30%.
Основной причиной ХОБЛ является пассивное и активное курение, кроме этого к внешним факторам риска ХОБЛ можно отнести:
— загрязненный воздух внутри помещений
— плохую экологическую обстановку
— профессиональные вредности
— частые инфекции нижних дыхательных путей в детстве
источник
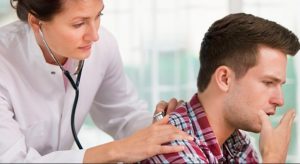

Обследование, основанное на сборе анамнеза, внешнем осмотре, пальпации, прослушивании и простукивании называется физикальным. Именно с такого метода диагностики начинается определение типа болезни.

- В каком возрасте начались астматические приступы, возможно какие детские болезни привели к астме. Это может быть коклюш, корь и другие, которые могут негативно повлиять на дыхательную систему.
- Были ли среди родственников астматики, это позволяет проследить генетическую связь, возможно кто-то из близких имел сильные аллергии.
- С какими раздражителями связаны приступы. Такие раздражители называются триггерами, и среди них может быть физическая нагрузка, холодный влажный воздух, микроскопические частицы шерсти и кожи собак, кошек, пыльца цветов разных растений, запыленность в помещении пылью определенного типа, продукты питания.
- Нужно узнать, как именно проходят приступы. Ведь при астматическом кашле пациенты принимают положение, при котором вдох менее мучительный, например, опираются руками о стол, расслабляя при этом плечевой пояс.
- Есть ли звуки при кашле, ведь свист при дыхании — это признак астматического сужения бронхов. Чтобы услышать характерные звуки при дыхании и приступах, не нужно прослушивать грудь стетоскопом, их хорошо слышно и на небольшом расстоянии.
- Долго ли длится приступообразный кашель, пропадает ли он после приема бронхолитических лекарств.
- После приступа наблюдается выделения вязкой, но прозрачной, как стекло мокроты, которая освобождает бронхи, таким образом облегчается дыхание, такие особенности также нужно узнавать при опросе.
Внешний осмотр проходит следующим образом:
- Врач смотрит на грудную клетку, которая может иметь вид, похожий на бочку. Такую форму грудная клетка приобретает вследствие развития эмфиземы, расширения легких, и, как результат — увеличение размеров грудной клетки;
-
Прослушивание проходит через стетоскоп, стетофонендоскоп или фонендоскоп, причем последний наиболее подходит для изучения звуков, издаваемых грудной клеткой при астме. Если происходит обострение, свист и характерные хрипы слышны по всей легочной поверхности, но при ремиссии свистящий хрип слышен снизу от лопаток и то только при усиленном вдохе.
- Постукивание пальцами не может эффективно сообщить информацию на ранних этапах астмы. Но если болезнь длится долго, то пальпацией и постукиванием можно услышать пустоту (звук картонной коробки), которая образовалась из-за эмфиземного расширения легких.
Лабораторные исследования проводятся в следующих направлениях:
- анализ крови направлен на определение количества эозинофилов — этот вид лейкоцитов является показателем аллергических процессов в организме;
-
если в анализе крови отсутствуют признаки воспалительных процессов и токсинов, выделяемых бактериями, то при наличии астматических симптомов доктору легче отличить астму от обычного бронхита или пневмонии;
- в мокроте под микроскопом можно обнаружить эозинофилы;
- в анализе мокроты присутствуют кристаллические вкрапления — особенные кристаллы Шарко-Лейдена и спиралевидные кристаллы Куршмана;
- мокрота при астме специфическая, отличается от мокроты при бронхите, структура двухслойная, консистенция густая, по густоте вязкая;
- методом проделывания царапин на коже (скарификации) берут пробы на аллергены, по которым уточняют аллергический возбудитель (триггер) бронхоспазма, аллергены вызывают на коже покраснение и зудящие ощущения;
- кал берут для определения гельминтов, которые могут размножиться до инвазивного количества и вызвать аллергическую интоксикацию организма, что также может влиять на возникновение приступов.
С помощью специально разработанных аппаратов проводится инструментальная диагностика. На первом месте в аппаратной диагностики стоит пикфлуометрия. На пикфлоуметре, который являет собой трубочку с нанесенной шкалой, измеряется самая большая скорость потока воздуха при выдохе, сделанном с максимальным усилием (форсированный выдох). Такая пиковая скорость выдоха называется ПСВ. Этот тест доступен детям с четырех лет, также он применяется и для взрослых.
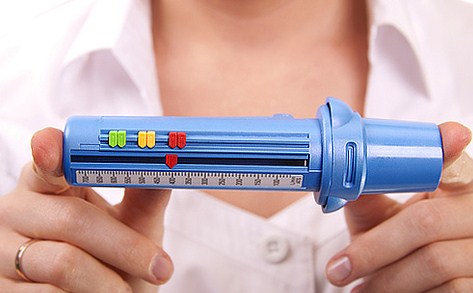
Измерительные процессы проводятся дважды в день, сутра и ближе к вечеру. Делаются три попытки, из которых выбирается та, которая сделана наиболее правильно. На трубку нанесена шкала с зеленой, желтой и красной зоной, которые обозначают степень проблемы. Но эта шкала не унифицирована, она подбираются путем индивидуальных двухнедельных исследований каждого больного. Если показатели в зеленой зоне, значит, что симптомы астмы под контролем, желтая зона — возможно обострение, при красной зоне нужно немедленно спешить человеку на помощь.
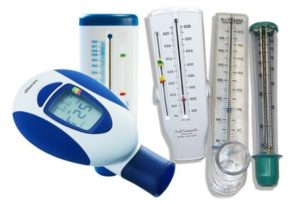
Больной должен зафиксировать лучшее значения ПСВ, и при дальнейшем использовании прибора при определении обструктивных изменений надобно соотносить с этим значениям другие показатели шкалы. Нужно правильно делать выдох форсированным способом, результаты записывать в дневник, чтобы с этими результатами ознакомить позже лечащего врача. Возможно, в вашем городе есть школа для больных астмой (где доктора рассказывают, как лечить это заболевание), поинтересуйтесь у доктора.

Спирограмма показывает форсированную жизненную емкость легких, сокращенно ФЖЕЛ, а также объем форсированного выдоха за одну секунду, сокращенно — ОФВ1, и так называемую пиковую скорость выдоха (ПСВ). Высчитывается индекс Тиффно, который составляет ОФВ1 поделить на ФЖЕЛ, у здоровых людей этот показатель выше 0,75.
Если при подозрениях на астму показатели спирографа в пределах нормы, делают медицинскую провокацию — дают больному метхолин или гистамин в виде ингаляций и сравнивают спирограмму с обычной обструкцией и под действием этих лекарств.
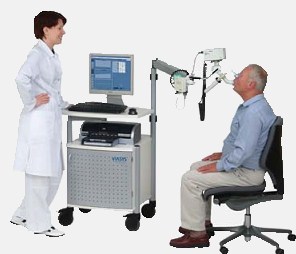
Но анализ дыхания может не дать четких результатов в случае, если заболевание являются профессиональным и приступ вызывает вещество, присутствующее только на работе. Чтобы диагностировать профессиональную астму, нужно кроме тестов дыхания изучить анализы и с помощью опроса выявить аллерген на рабочем месте пациента.
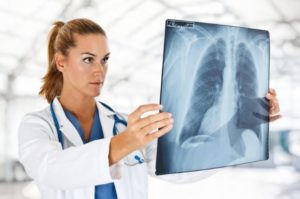
Если болезнь уже долго прогрессирует, развивается эмфизема, увеличение в объеме легких, которые на рентгенологической фотографии видимы как более прозрачные.
Томографию также назначают не во всех случаях, а только тогда, когда кашель и удушье не проходят длительное время, не смотря на лечение, и есть подозрения на наличие других болезней.
Диагностика астматических приступов у детей имеет особенности, поскольку они часто болеют респираторными и другими заболеваниями с похожими симптомами. Прежде всего у детей выясняют зависимость приступов от действий аллергенов, также возможную склонность к аллергии на генетическом уровне — есть ли близкие родственники с сильной аллергией на что-либо, это позволяет уточнить диагноз.

У детей исследуют внешнее дыхание с помощью приборов, предварительно дав бронходилататоры (препараты, расширяющие просвет в бронхах). Также сдают анализы, чтобы отследить наличие гельминтов и воспалительного процесса в организме, иногда проводят аллергологический тест. Но некоторые современные врачи отказываются от тестов на аллергены, резонно указывая на то, что в большинстве случаев аллергены вполне обычны и избежать их влияния довольно трудно.
У детей бронхиальная астма полностью излечима в большинстве случаев, однако для успешного лечения имеет большое значение своевременная диагностика бронхиальной астмы и правильное лечение, которое состоит не только в приеме медикаментов, но и в укреплении организма.
Люди пожилого возраста имеют множество заболеваний, которые могут хронически проходить долгие годы. Симптомы этих болезней могут накладываться на астматические, и клиническая картина становится нечеткой.

Кроме того, рекомендуется проводить функциональные методы выявления бронхиальной астмы, включающие ЭКГ, рентгенографию, пикфлоуметрию (это исследование нужно делать в течение 2 недель). Только после выполнения всех диагностических мероприятий назначается симптоматическое лечение бронхиальной астмы.
источник
Среди заболеваний дыхательной системы бронхиальная астма занимает особое место. Специфические симптомы болезни позволяют поставить диагноз лишь на основании клинических данных, но с помощью современных методов обследования есть возможность установить точную причину недуга. Диагностика астмы начинается со сбора подробного анамнеза, после чего врач составляет подробный план исследования, включающий лабораторные и инструментальные тесты.

- В детском возрасте чаще встречается атопический или аллергический вариант астмы. В результате продолжительного и регулярного воздействия аллергена организм ребенка подвергается повышенной нагрузке, а иммунная система формирует патологическую ответную реакцию.
- У людей с сердечными заболеваниями, а также пожилых пациентов, врачи чаще выявляют аспириновую форму болезни. Длительное воздействие ацетилсалициловой кислоты или индивидуальная непереносимость этого вещества может привести к негативным изменениям и спровоцировать начало заболевания.
- У взрослых нередко диагностируют инфекционно-зависимую форму болезни. В результате хронических инфекций дыхательных путей формируются условия для развития обструкции бронхов.
- У беременных развитие недуга может быть вызвано конфликтом резус-фактора крови или неблагоприятными условиями работы и жизни. Диагностировать болезнь нужно как можно раньше, чтобы предупредить патологию у ребенка.
- Выявлять бронхиальную астму помогает набор типичных симптомов, которые характеризуются периодами обострения и ремиссии. Обнаружение на догоспитальном этапе признаков, являющихся специфическими маркерами, служит поводом для подозрения. Сухой приступообразный кашель, свистящее дыхание (особенно ночью), тяжесть в грудной клетке, одышка, не вызванная физическими нагрузками, аллергические реакции – перечисленные симптомы служат основанием для проведения обследования. Методом исключения, а также с помощью проведения современных лабораторных и инструментальных тестов, врачам удается определить диагноз, разобраться в этиологии болезни и назначить нужное лечение.
Показаниями для проведения дифференциальной диагностики бронхиальной астмы с заболеваниями со схожей клинической картиной являются:
- Генетическая предрасположенность.
- Хронические обструктивные заболевания органов дыхания.
- Аллергические реакции по типу обструкции.
- Наличие вредных привычек или профессиональных вредностей.
- Усиление симптомов при повторяющихся обстоятельствах.
Эти и ряд других признаков говорят о необходимости проведения расширенной диагностики с целью выявления астмы на ранней стадии.
Сложность установления диагноза связана с тем, что бронхиальная астма редко протекает в форме самостоятельной патологии и сопровождается системными изменениями, характерными для заболеваний органов сердца и дыхания. Лабораторные тесты позволяют выявить отклонения, а инструментальные методы обследования подтверждают наличие патологии.

- Общий анализ крови. Базовый тест для определения уровня здоровья и основных показателей работы внутренних органов человека. Позволяет найти признаки острого или хронического воспаления и степень компенсации за счет резервных возможностей организма.
- Биохимический анализ крови. Дополнительное исследование лейкоцитарной формулы, в особенности процентное соотношение эозинофилов, важно для последующей оценки аллергопроб. Брать кровь лучше натощак, с целью исключить естественное искажение данных в результате физиологических реакций.
- Иммунологический анализ. Специфический тест на наличие в крови иммуноглобулина IgE, повышение которого типично для аллергических заболеваний.
- Анализ мокроты. Наряду с биохимией крови, является маркером при аллергических заболеваниях. Физические и биохимические показатели анализа мокроты при бронхиальной астме отличаются от результатов анализа при бронхите, поэтому важно для дифференциации.
- Анализ кала. Паразитарные заболевания нередко являются причиной аллергической реакции организма, а определение признаков глистной инвазии служит основой для построения следующих этапов диагностики.
- Анализ мочи. Рекомендуется сдавать с целью проведения дифференциальной диагностики с воспалительными заболеваниями органов дыхания.
- Аллергопроба. Играет ключевую роль в постановке диагноза. Критериями оценки является наличие реакции на контролируемое введение аллергена, что проявляется кожным зудом, покраснением, возникновением одышки и прочими типичными признаками.

Результаты лабораторных тестов заносят в таблицу, которая впоследствии дополняется данными инструментальных обследований.
Методы функциональной диагностики с применением специального оборудования показывают изменения со стороны органов дыхания, вызванные бронхиальной астмой. Прямые или косвенные подтверждения диагноза могут быть получены с помощью следующих исследований:
- Рентгенография легких. Метод не считается специфичным, но позволяет выявить изменения легочного рисунка, характерного для эмфиземы, одного из осложнений астмы на поздней стадии.
- Спирометрия. Ценный метод диагностики бронхиальной астмы, основанный на определении функции внешнего дыхания. Прибор фиксирует отклонения от нормы, которые подвергаются дальнейшей расшифровке в комплексе в другими данными.
- Пикфлоуметрия. Инструментальный метод тестирования скорости выдоха необходим для установления диагноза в больнице и для контроля состояния больного в домашних условиях. С помощью прибора, который называется пикфлоуметр, происходит измерение бронхиальной проходимости и степени обструкции бронхов.
Диагностический комплекс процедур при астме является наглядным примером того, как полноценное обследование с применением современного оборудования помогает в установлении диагноза и для осуществления контроля в период лечения.
Оценка данных исследования позволяет установить точный диагноз в максимально сжатые сроки. Увеличение процентного соотношения эозинофилов в крови, определение специфического иммуноглобулина IgE, положительные результаты аллергопробы наряду с увеличением сопротивления при выдохе с фиксированным усилием для достижения нужной вентиляции легких – эти и другие признаки в комплексе подтверждают диагноз. Дальнейшая тактика ведения зависит от многих факторов и определяется индивидуально для каждого пациента.
источник
РОССИЙСКАЯ АКАДЕМИЯ МЕДИЦИНСКИХ НАУК
1 МЕДИКО-ГЕНЕТИЧЕСКИИ НАУЧНЫЙ ЦЕНТР
На правах рукописи УДК 575.599.9
Украинцева Светлана Викторовна
ГЕНЕТИКО-ЭПИДЕМИОЛОГИЧЕСКИЙ АНАЛИЗ ПРЕДРАСПОЛОЖЕННОСТИ К БРОНХИАЛЬНОЙ АСТМЕ
АВТОРЕФЕРАТ диссертации на соискание ученой степени кандидата биологических наук
Работа выполнена в лаборатории генетической эпидемиологии Медико-генетического научного центра РАМН
кандидат медицинских наук А. С. Сергеев
Офацаальвые оппоненты: доктор медицинских наук, профессор Н.И. Капранов
доктор биологических наук, профессор М.М. Асланяи
Ведущее научное учреждение: Научный центр здоровья детей РАМН
Защита диссертации состоится «___»_ 1998 г. в_на
заседании Диссертационного Совета Д.001.16.01 при Медико-генетическом научном центре РАМН (115478 Москве, ул. Москворечье,!)
С диссертацией можно ознакомиться в библиотеке Медико-генетического научного центра РАМН.
Автореферат разослан « »_1998г.
Ученый секретарь Диссертационного совета доктор биологических наук, профессор
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Бронхиальная астма (БА) — хроническое воспалительное заболевание дыхательных путей, приводящее к гиперреактивности бронхов и приступам обратимого удушья . Природа этой патологии на сегодняшний день до конца не выяснена. Концепция патогенеза БА претерпевает постоянные изменения. Так, вплоть до начала 90-х годов ведущим в картине БА считался собственно приступ удушья. Теперь же в основу патогенеза БА положен хронический аллергический воспалительный процесс (ВОЗ, 1995).
Распространенность и заболеваемость БА сильно варьируют в зависимости от популяции и диагностических критериев — от долей до десятков процентов (Адо 1978; Чучалин 1985; Peat 1996; Shifer 1996; Vollmer 1998; ISAAC 1998). Поэтому сравнивать эпидемиологические данные, полученные в разных странах сложно.
Исследования по генетике БА пока не привели к однозначным выводам о ее генетической природе. Семейное накопление при БА наблюдалось давно. Предлагались различные генетические модели: аутосомно-рецессивная, аутосомно-доминантная с неполной пенетрантностыо, мультифакториальная. Сегрегационный анализ давал равные доказательства в пользу как главного гена, так и полигенной модели (Lubs 1972; Lawrence 1994; Martinez 1997; Bleecker 1997; Kim 1998). Сейчас большинство генетиков относят БА к мультифакториальным заболеваниям, предрасположенность к которым формируется совокупностью генетических и средовых факторов. Не исключено, что диагноз БА объединяет несколько генетически отличающихся форм патологии. Поэтому исследование генетической гетерогенности БА имеет большое теоретическое и прикладное значение. Последние годы множество работ было посвящено поиску
конкретных генов, участвующих в развитии БА (WIkinson 1996; Daniels 1996; Marshl997; CSGA 1997). Широко используется анализ сцепления. Обнаружены ассоциации ряда генетических маркеров на 5 и 11 хромосомах с БА, бронхиальной гиперреактивностью и атопией. Большая часть этих маркеров связана либо с геном рецептора IgE, либо с IL-4 (Herwerden 1995; Postma 1995; Doull 1996; Мао 1998; Mensur 1998). Однако до полного понимания генетических основ БА еще далеко. Поэтому изучение генетики предрасположенности к БА остается на сегодняшний день актуальным.
2. ЦЕЛИ И ЗАДАЧИ ИССЛЕДОВАНИЯ
Целью исследования явилось изучение генетики предрасположенности к бронхиальной астме. В задачи исследования входило:
1. Изучить эпидемиологию БА. Для этого получить повозрастные оценки распространенности, заболеваемости и популяционного риска БА в Москве.
2. Изучить накопление БА в семьях. Дня этого получить эмпирические оценки риска развития БА среда родственников пробандов.
3. Провести анализ генетической гетерогенности Б А по возрасту начала заболевания. Для этого изучить и сравнить динамику возрастных распределений заболеваемости БА в популяции и сешях больных.
4. Сопоставить генетическую отягощенность больных с разным возрастом начала БА. Для этого сравнить эмпирические риски развития БА среди родственников пробандов с БА разного возраста начала.
5. Разработать таблицы повторного риска БА среди родственников для медико-генетического консультирования (прогноза заболеваемости в семьях).
6. Изучить фенотипическую ассоциацию БА с атопическим дерматитом (АД) — распространенным кожным аллергическим заболеванием, которое, по наблюдениям клиницистов, часто встречается среди пациентов с БА. Для этого оценить эмпирический риск развития БА среди больных АД и риск развития АД среди больных БА. Рассчитать коэффициент фенотипической корреляции двух патологий.
Впервые получены оценки популяционного риска развития БА в течение жизни для Москвы. Показано наличие двух пиков заболеваемости БА в популяции, лежащих в возрастных интервалах (0-24) и (25-89) лет, с достоверным минимумом заболеваемости БА между ними.
Проведен анализ генетической гетерогенности БА по возрасту качала заболевания. Показано, что БА с возрастом начала до 25 лет и после 25 лет не являются генетически самостоятельными формами заболевания.
Показано, что больные БА с возрастом начала до 25 лет более генетически отягощены, чем больные БА с возрастом начала после 25 лег.
Получена количественная оценка фенотипической ассоциации БА и АД. Показано, что примерно 60% всех факторов (генетических и средовых), вызывающих БА и АД, являются общими.
4. ПРАКТИЧЕСКАЯ ЗНАЧИМОСТЬ РАБОТЫ
Разработанные нами таблицы повторного риска развития БА в семьях с различным семейным анамнезом могут быть использованы в медико-генетическом консультировании для прогноза заболеваемости среди родственников.
Созданные нами компьютерные программы: SAN, система управления базой данных для семейного анализа мультифакгориальных заболеваний, и ЕРЮ, программа анализа популяционного риска для заболеваний с варьирующим возрастом начала, — имеют практическое применение и используются в ряде институтов.
5. ПОЛОЖЕНИЯ, ВЫНОСИМЫЕ НА ЗАЩИТУ
1. Динамика заболеваемости БА в популяции г.Москвы имеет два пика, связанных с возрастом начала заболевания (до и после 25 лет). Между этими пиками лежит достоверный минимум заболеваемости БА в возрастном интервале 15-35 лет.
2. Заболеваемость БА в популяции имеет половые различия. В возрастном интервале 0-9 лет мальчики заболевают достоверно чаще, чем девочки (0,7% против 0,3 %). Кривая заболеваемости взрослых мужчин сдвинута относительно женщин в сторону более старших возрастов примерно на 10 лет.
3. Популяционный риск Б А, как поликлинического диагноза, составляет 2,2% для мужчин и 1,9% для женщин от рождения до 90 лет (различия недостоверны). Средний по полу риск развития БА в течение жизни равен 2%.
4. Динамика показателей заболеваемости БА среди родственников пробандов имеет два пика, как в популяции. Причем оба пика наблюдаются и при раннем, и при позднем возрасте начала БА у пробанда. Этот факт говорит против генетической гетерогенности БА по возрасту начала заболевания. Коэффициент генотипической корреляции БА с разным возрастом начала в семьях достоверно не отличается от единицы. Таким образом, БА с ранним и поздним возрастом начала не являются генетически самостоятельными «формами» заболевания.
5. Риск развития Б А среди родственников пробандов с ранним возрастом начала БА (до 25 лет) достоверно выше. чем среди родственников пробандов с поздним возрастом начала БА (после 25 лет): 11,3% против 7,3%. Этот факт говорит о более высокой генетической отягощенности больных БА с ранним возрастом начала по сравнению с больными с поздним возрастом начала БА.
6. Показатель наследуемости для БА в целом составляет h2 = 0,70. На его основе разработаны таблицы повторного риска БА с учетом семейного анамнеза для прогноза заболеваемости БА в семьях.
7. Изучена динамика заболеваемости БА среди больных атопическим дерматитом (АД) и АД среди больных БА. Показано достоверное увеличение частоты одной патологии в присутствии другой. Коэффициент фенотипической корреляции БА и АД равен г = +0,59 . Это означает, что примерно 60% всех факторов (генетических и средовых), вызывающих БА и АД, являются общими.
Результаты исследования были представлены на Всемирном конгрессе легочного здоровья (Майнц, 1994), на Европейской школе медицинской генетики (Сестри Леванте, 1996), на Международной конференции биомедицинских аспектов исследования старения (Венеция, 1997), на первом Европейском конгрессе биогеронтологии (Эльсинор, 1998).
По теме диссертации опубликовано 6 работ.
Работа изложена на ¿8Pлистах машинописного текста; состоит из введения, обзора литературы, глав «Материалы и методы,» «Результаты и обсуждение», выводов, приложения и списка литературы (йсработ). В тексте диссертации рисунков и таблиц.
Материалом для получения популяционных оценок распространенности и заболеваемости БА послужили сведения о 1221 больных БА всех возрастов, состоявших к моменту исследования на диспансерном учете в районных поликлиниках г.Москвы. Сведения о количестве взрослого населения в исследуемых районах были получены в районных управлениях здравоохранения. Численность этого населения была скорректирована на долю людей, вообще не посещающих районные поликлиники. Итоговая численность составила 259677 человек, которые были распределены по полу и возрасту в соответствии с данными о поло-возрастной структуре населения Москвы. В районных кожных диспансерах (КВД) нами были собраны сведения о 372 больных атопическим дерматитом (АД). Пробандам с БА и их родственникам, а также пробандам с АД, по почте рассылали анкеты с вопросами о ходе заболевания, возрасте его начала (ВИЗ) и сопутствующей патологии. Критерий диагноза БА в популяции и семьях больных был одинаковым: постановка на диспансерный учет в поликлинике. Несмотря на значительную вариабельность диагностических критериев БА в разных странах (и, соответственно, относительную ценность количественных оценок заболеваемости БА), сравнить заболеваемость в популяции и семьях можно было вполне корректно.
Распространенность БА в популяции, Р, считали как долю больных БА на момент исследования в соответствующей возрастной группе населения: Р=пь/ЫР (1)
Заболеваемость я в возрасте I рассчитывали по аналогии с вероятностью смерти в демографии (Сергеев, 1991):
где гге — коэффициент заболеваемости в возрасте г, который считали по формуле:
) — возраст на момент исследования (ВМИ); та- число новых случаев Б А, впервые возникших в возрасте ¡, непосредственно предшествующем j; пг- число больных возраста Г / Л>/ />/ 2
п — число больных; N — число здоровых в данном возрасте; I — расчетный ВНЗ; > — ВМИ; £ — ВНЗ больше расчетного.
Коэффициент фенотипической корреляции между родственниками, И, рассчитывали согласно пороговой модели подверженности к мультифакториальному заболеванию (Фолконер, 1985):
a + J Украинцева, Светлана Викторовна
источник
Диагностика бронхиальной астмы выполняется, ориентируясь на полное комплексное обследование организма пациента. От правильно проведенной диагностики зависит получение положительных результатов лечения.
Протоколы (стандарты) определения заболеваемости, а также дальнейшего лечения взрослого населения и детей учитывают различные методики: клинический осмотр, сбор анамнеза, выявление симптоматики, лабораторная диагностика.
После проведения необходимых мероприятий для каждого больного подбирается индивидуальная схема лечения, которая способствует снижению заболеваемости и облегчению состояния больного. Дифференциальная диагностика бронхиальной астмы учитывает все аспекты (анализы, симптоматику, анамнез, аллергологическое исследование и дыхательную функциональность.).
Современная диагностика при развитии бронхиальной астмы является важной задачей для врача, так как адекватное лечение способно обеспечить полный контроль над заболеванием при полной нейтрализации симптоматики у детей и взрослых. Для этого оцениваются все критерии астмы с исключением ХОБЛ и постановкой предварительного диагноза.
Протоколы диагностики проводятся в несколько этапов:
Бронхиальная астма, в зависимости от степени заболеваемости, определяется наиболее часто в детском и подростковом возрасте. Как правило, наблюдается генетическая предрасположенность к развитию астматических заболеваний. Кроме того, ее развитие возможно на фоне ХОБЛ.
Бронхиальный приступ нередко связан с воздействием определенных факторов, провоцируя характерную симптоматику (одышку, кашель, свистящее дыхание, слабость и т.д.). Приступ способен появиться внезапно. Его можно купировать при помощи ингаляционных бронхолитиков. Если после использования ингалятора приступ не снимается, необходимы дальнейшие протоколы диагностики, а также исключение ХОБЛ.
В начальной стадии заболевания профессиональная диагностика не способна определить какие-то определенные протоколы в определении бронхиальной астмы, кроме исключения ХОБЛ. Во время затяжного приступа может возникнуть симптом «бочкообразной грудной клетки», что связано с затрудненным выдохом. В результате этого возможно постепенное развитие эмфиземы, критерии и протоколы которой зависят от выраженности симптоматики и стадии заболеваемости. От результатов визуального осмотра может зависеть дальнейшее лечение.
Немаловажным способом профессиональной диагностики является перкуссия (выстукивание) и аускультация (выслушивание) легких. По мере развития приступа можно услышать свистящее дыхание и хрипы в легких. Перкуссия эффективна при длительном течении заболевания и эмфиземе.
Лабораторная диагностика предполагает назначение проведения различного вида анализов, среди которых:
- биохимический анализ крови — определяет количество эозинофилов, являющихся маркерами аллергического процесса. Кроме того, этот анализ в совокупности с аллергологической пробой, позволяет выявить конкретный аллерген, на который острее всего реагирует организм;
- общий анализ крови — позволяет выявить воспалительные процессы, ХОБЛ и интоксикацию в организме больного. Забор крови выполняется натощак;
- общий анализ мокроты — выявляет характерные астматические маркеры с характерными спиралями Куршмана и кристаллами Шарко – Лейдена. При этом определяется вязкая и густая мокрота, которая может расслаиваться двумя слоями. При микроскопическом исследовании определяются эозинофилы;
- анализ кала — способствует выявлению паразитарных инвазий, которые нередко провоцируют развитие бронхиальной астмы. Например, аскариды при своей цикличности развития способны проникнуть через легочную систему, вызывая общую интоксикацию организма, ослабление иммунной системы, повышенную аллергизацию пациента;
- аллергопроба (включая скарификационную) — критерии проведения аллергопробы позволяют уточнить наличие триггера в крови, который вызывает ответную цепь реакций в крови, приводя к бронхоспазму. При положительном ответе могут наблюдаться местные признаки воспаления (зуд, гиперемия, отек и т.д.).
Наиболее сложно диагностировать астму при наличии обструктивного бронхита (ХОБ). Этот процесс проявляется, как хроническая обструктивная болезнь легких (ХОБЛ).
Протоколы выполнения этого вида диагностики служат показателями для постановки итогового диагноза.
Профессиональная рентгенография способна выявить повышенную воздушность легочной ткани (эмфизему) и усиленный легочный рисунок за счет активного притока крови к легочной ткани. Тем не менее, следует учитывать, что иногда даже рентгенограмма не может выявить изменения. Поэтому принято считать, что методы рентгенографии глубоко неспецифичны.
Этот метод служит для определения ФВД (функций внешней дыхательной деятельности) и является достаточно эффективным. Профессиональная спирометрия способна определить ряд главных показателей дыхательной деятельности.
Диагностика спирометрии выглядит следующим образом:
- пациенту предлагается дышать через специальный прибор (спирометр), который обладает чувствительностью и фиксирует все изменения дыхания;
- анализ проведенного обследования сравнивается (врачом или пациентом) с рекомендуемыми показателями ФВД;
- на основании профессиональной сравнительной характеристики внешнего дыхания врач устанавливает предварительный диагноз (для 100% уверенности в диагнозе одной спирометрии недостаточно);
- если у больного наблюдается бронхообструктивные нарушения (исключая ХОБЛ) это может говорить о проявлении бронхиальной астмы.
Помимо этого, спирометрические данные позволяют определить тяжесть астматического приступа и эффективность проводимого лечения в том случае, когда оно использовалось.
Этот метод диагностирования относится к нововведениям для контроля и определения развития бронхиальной астмы у взрослого пациента. Мониторинговый протокол с участием пикфлоуметра обладает следующими преимуществами:
- позволяет определить обратимость бронхиальной обструкции;
- возможность оценки тяжести течения болезни;
- протоколы пикфлоуметрии позволяют спрогнозировать период, когда возникает астматический приступ, в зависимости от степени заболеваемости;
- возможность выявления профессиональной астмы;
- мониторинг эффективности проводимого лечения.
Пикфлоуметрию следует выполнять ежедневно. Это позволяет получить более точные результаты диагностики.
При помощи этого способа профессиональной диагностики определяется пиковая объемность и максимальная объемная скорость на различных уровнях, учитывая процентное соотношение ФЖЕЛ (форсированную жизненную емкость легких). Измеряют максимальную скорость на уровне в 75%, 50% и 25%.
Наиболее затруднительны протоколы определения профессиональной астмы, так как приступ могут вызвать некоторые химические соединение, присутствующие в воздухе. Для подтверждения профессиональной астмы необходимо выяснение анамнеза у взрослого пациента, а также анализ показателей внешней дыхательной деятельности. Кроме того, необходимо в обязательном порядке своевременно сдавать анализы (мокроты, мочи, крови и т.д.) и проводить необходимое лечение.
Одновременно с показателями внешнего дыхания и в зависимости от выраженности симптоматики проводятся прик-тесты (инъекционные) и скарификационная проба на выявление аллергологической этиологии. Однако следует учитывать, что клиническая картина таких обследований в некоторых случаях могут дать ложнопозитивный или ложнонегативный ответ. Именно поэтому рекомендуется проводить исследование крови на наличие специфических антител в сыворотке. В профессиональной диагностике особенно важно выяснение аллергического статуса у детей.
Диагностика бронхиальной астмы у детей нередко сопровождается большими трудностями. Это связано, прежде всего, с симптоматикой заболевания у детей, которая аналогична многим другим детским заболеваниям. Поэтому многое зависит от выяснения анамнеза со склонностью к аллергическим заболеваниям. В первую очередь необходимо опираться на повторение ночного приступа бронхиальной астмы, что подтверждает развитие заболевания.
Помимо этого, протоколы диагностики предусматривают проведение ФВД (функционального исследования внешнего дыхания) с бронходилататорами для назначения адекватной тактики лечения. Вполне естественно, что необходимо сдать анализы мокроты, крови и кала, а также провести спирометрическое тестирование и аллергообследование.
Следует отметить, что затруднительно проводить диагностику астматического приступа у лиц пожилого возраста. Это связано, прежде всего, с обилием хронических заболеваний, которые сопровождают бронхиальную астму, «стирая» ее картину. В этом случае, необходим тщательный сбор анамнеза, исследование мокроты и крови, выполнение специфических тестирований, направленных на исключение вторичных заболеваний. Прежде всего, проводится диагностика сердечной астмы, выявление ИБС, сопровождающейся симптомами недостаточности левого желудочка.
Кроме того, рекомендуется проводить функциональные методы выявления бронхиальной астмы, включающие ЭКГ, рентгенографию, пикфлоуметрию (в течение 2 недель). Только после выполнения всех диагностических мероприятий назначается симптоматическое лечение бронхиальной астмы.
источник
Бронхиальная астма – диагноз клинический, то есть врач ставит его на основании прежде всего жалоб, истории заболевания и данных осмотра и внешнего исследования (пальпации, перкуссии, аускультации). Однако дополнительные методы исследования дают ценную, а в некоторых случаях определяющую диагностическую информацию, поэтому они широко применяются на практике.
Диагностика бронхиальной астмы с помощью дополнительных методов включает проведение лабораторных анализов и инструментальных исследований.
Пациенту с астмой могут быть назначены следующие анализы:
- общий анализ крови;
- биохимический анализ крови;
- общий анализ мокроты;
- анализ крови для выявления общего IgE;
- кожные пробы;
- определение в крови аллергенспецифических IgE;
- пульсоксиметрия;
- анализ крови на газы и кислотность;
- определение оксида азота в выдыхаемом воздухе.
Разумеется, не все эти тесты выполняются у каждого больного. Некоторые из них рекомендуются лишь при тяжелом состоянии, другие – при выявлении значимого аллергена и так далее.
Общий анализ крови выполняется у всех пациентов. При бронхиальной астме, как и при любом другом аллергическом заболевании, в крови отмечается увеличение количества эозинофилов (EOS) более 5% от общего количества лейкоцитов. Эозинофилия в периферической крови может возникать не только при астме. Однако определение этого показателя в динамике (повторно) помогает оценить интенсивность аллергической реакции, определить начало обострения, эффективность лечения. В крови может определяться незначительный лейкоцитоз и увеличение скорости оседания эритроцитов, однако это необязательные признаки.
Биохимический анализ крови у больного с астмой часто никаких отклонений не выявляет. У некоторых пациентов отмечается увеличение уровня α2- и γ-глобулинов, серомукоида, сиаловых кислот, то есть неспецифических признаков воспаления.
Обязательно проводится анализ мокроты. В ней находят большое количество эозинофилов – клеток, участвующих в аллергической реакции. В норме их меньше 2% от всех обнаруженных клеток. Чувствительность этого признака высокая, то есть он обнаруживается у большинства больных с астмой, а специфичность средняя, то есть, помимо астмы, эозинофилы в мокроте встречаются и при других заболеваниях.
В мокроте нередко определяются спирали Куршмана – извитые трубочки, образующиеся из бронхиальной слизи при спазме бронхов. В них вкраплены кристаллы Шарко-Лейдена – образования, которые состоят из белка, образующегося при распаде эозинофилов. Таким образом, два этих признака говорят о снижении бронхиальной проходимости, вызванном аллергической реакцией, что часто и наблюдается при астме.
Кроме того, в мокроте оценивается наличие атипичных клеток, характерных для рака, и микобактерий туберкулеза.
Анализ крови на общий IgE показывает уровень в крови этого иммуноглобулина, который вырабатывается в ходе аллергической реакции. Он может быть повышен при многих аллергических заболеваниях, но и нормальное его количество не исключает бронхиальную астму и другие атопические процессы. Поэтому гораздо более информативным является определение в крови специфических IgE – антител к конкретным аллергенам.
Для анализа на специфические IgE используются так называемые панели – наборы аллергенов, с которыми реагирует кровь больного. Тот образец, в котором содержание иммуноглобулина будет выше нормы (у взрослых это 100 ед/мл), и покажет причинно-значимый аллерген. Используются панели шерсти и эпителия разных животных, бытовые, грибковые, пыльцевые аллергены, в некоторых случаях – аллергены лекарств и пищевые.
Для выявления аллергенов применяются и кожные пробы. Их можно проводить у детей любого возраста и у взрослых, они не менее информативны, чем определение IgE в крови. Кожные пробы хорошо себя зарекомендовали в диагностике профессиональной астмы. Однако при этом существует риск внезапной тяжелой аллергической реакции (анафилаксии). Результаты проб могут меняться под действием антигистаминных препаратов. Их нельзя проводить при кожной аллергии (атопическом дерматите, экземе).
Пульсоксиметрия – исследование, проводимое с помощью небольшого прибора – пульсоксиметра, который обычно надевается на палец пациента. Он определяет насыщение артериальной крови кислородом (SpO2). При снижении этого показателя менее 92% следует выполнить исследование газового состава и кислотности (рН) крови. Снижение уровня насыщения крови кислородом свидетельствует о тяжелой дыхательной недостаточности и угрозе для жизни больного. Определяемое при исследовании газового состава снижение парциального давления кислорода и увеличение парциального давления углекислого газа свидетельствует о необходимости искусственной вентиляции легких.
Наконец, определение оксида азота в выдыхаемом воздухе (FENO) у многих больных с астмой выявляет увеличение этого показателя выше нормы (25 ppb). Чем сильнее воспаление в дыхательных путях и больше доза аллергена, тем показатель выше. Однако такая же ситуация бывает и при других болезнях легких.
Таким образом, специальные лабораторные методы диагностики астмы – кожные пробы с аллергенами и определение в крови уровня специфических IgE.
Методы функциональной диагностики бронхиальной астмы включают:
- исследование вентиляционной функции легких, то есть способности этого органа доставлять необходимое количество воздуха для газообмена;
- определение обратимости бронхиальной обструкции, то есть снижения проходимости бронхов;
- выявление гиперреактивности бронхов, то есть их склонности к спазму под действием вдыхаемых раздражителей.
Основной метод исследования при бронхиальной астме – спирометрия, или измерение дыхательных объемов и скоростей воздушных потоков. С него обычно начинается диагностический поиск еще до начала лечения больного.
Главный анализируемый показатель – ОФВ1, то есть объем форсированного выдоха за секунду. Проще говоря, это количество воздуха, которое человек способен быстро выдохнуть в течение 1 секунды. При спазме бронхов воздух выходит из дыхательных путей медленнее, чем у здорового человека, показатель ОФВ1 снижается.
Если при первичной диагностике уровень ОФВ1 составляет 80% и больше от нормальных показателей, это говорит о легком течении астмы. Показатель, равный 60 – 80% от нормы, появляется при астме средней тяжести, менее 60% – при тяжелом течении. Все эти данные применимы только к ситуации первичной диагностики до начала терапии. В дальнейшем они отражают не тяжесть астмы, а уровень ее контроля. У людей с контролируемой астмой показатели спирометрии в пределах нормы.
Таким образом, нормальные показатели функции внешнего дыхания не исключают диагноз «бронхиальная астма». С другой стороны, снижение бронхиальной проходимости обнаруживается, например, при хронической обструктивной болезни легких (ХОБЛ).
Если обнаружено снижение бронхиальной проходимости, то важно выяснить, насколько оно обратимо. Временный характер бронхоспазма – важное отличие астмы от того же хронического бронхита и ХОБЛ.
Итак, при снижении ОФВ1 для выявления обратимости бронхиальной обструкции проводятся фармакологические тесты. Пациенту дают препарат посредством дозированного аэрозольного ингалятора, чаще всего 400 мкг сальбутамола, и через определенное время снова проводят спирометрию. Если показатель ОФВ1 увеличился после использования бронхолитика на 12% и больше (в абсолютных цифрах на 200 мл и больше), говорят о положительной пробе с бронходилататором. Это означает, что сальбутамол эффективно снимает спазм бронхов у данного пациента, то есть бронхиальная обструкция у него непостоянна. Если показатель ОФВ1 увеличивается менее чем на 12%, это признак необратимого сужения бронхиального просвета, а если он уменьшается, это говорит о парадоксальном спазме бронхов в ответ на использование ингалятора.
Прирост ОФВ1 после ингаляции сальбутамола на 400 мл и больше дает практически полную уверенность в диагнозе «бронхиальная астма». В сомнительных случаях может быть назначена пробная терапия ингаляционными глюкокортикоидами (беклометазон по 200 мкг 2 раза в день) в течение 2 месяцев или даже таблетками преднизолона (30 мг/сут) в течение 2 недель. Если показатели бронхиальной проходимости после этого улучшаются – это говорит в пользу диагноза «бронхиальная астма».
В некоторых случаях даже при нормальных показателях ОФВ1 применение сальбутамола сопровождается приростом его величины на 12% и больше. Это говорит о скрытой бронхиальной обструкции.
В других случаях нормальной величины ОФВ1 для подтверждения гиперреактивности бронхов применяют ингаляционную пробу с метахолином. Если она будет отрицательной, это может служить причиной для исключения диагноза астмы. Во время исследования пациент вдыхает возрастающие дозы вещества, и определяется минимальная концентрация, которая вызывает снижение ОФВ1 на 20%.
Применяются и другие пробы для выявления гиперреактивности бронхов, например, с маннитолом или физической нагрузкой. Падение ОФВ1 в результате использования этих проб на 15% и более с высокой степенью достоверности указывает на бронхиальную астму. Проба с физической нагрузкой (бег в течение 5 – 7 минут) широко применяется для диагностики астмы у детей. Применение ингаляционных провокационных проб у них ограничено.
Еще один важнейший метод инструментальной диагностики астмы и контроля за ее лечением – пикфлоуметрия. Пикфлоуметр должен быть у каждого пациента с этим заболеванием, ведь самоконтроль – основа эффективной терапии. С помощью этого небольшого аппарата определяют пиковую скорость выдоха (ПСВ) – максимальную скорость, с которой пациент может выдохнуть воздух. Этот показатель, так же как и ОФВ1, прямо отражает бронхиальную проходимость.
ПСВ можно определять у больных начиная с 5-летнего возраста. При определении ПСВ делается три попытки, записывается лучший показатель. Измеряют величину показателя утром и вечером каждого дня, а также оценивают его вариабельность – разницу между минимальным и максимальным значениями, полученными в течение дня, выраженную в процентах от максимальной величины за день и усредненную за 2 недели регулярных наблюдений. Для людей с бронхиальной астмой характерна повышенная вариабельность показателей ПСВ – более 20% при четырех измерениях в течение дня.
Показатель ПСВ используется преимущественно у людей с уже установленным диагнозом. Он помогает держать астму под контролем. В течение наблюдений определяют максимальный лучший показатель для данного больного. Если отмечается снижение до 50 – 75% от наилучшего результата – это говорит о развивающемся обострении и необходимости усилить интенсивность лечения. При снижении ПСВ до 33 – 50% от лучшего для пациента результата диагностируют тяжелое обострение, а при более значительном уменьшении показателя возникает угроза жизни больного.
Определяемый дважды в день показатель ПСВ нужно записывать в дневник, который приносят на каждый прием к врачу.
В некоторых случаях проводятся дополнительные инструментальные обследования. Рентгенография легких выполняется в таких ситуациях:
- наличие эмфиземы легких или пневмоторакса;
- вероятность воспаления легких;
- обострение, несущее угрозу жизни больного;
- неэффективность лечения;
- необходимость искусственной вентиляции легких;
- неясный диагноз.
У детей младше 5 лет используется компьютерная бронхофонография – метод исследования, основанный на оценке дыхательных шумов, и позволяющий выявить снижение бронхиальной проходимости.
При необходимости дифференциальной диагностики с другими заболеваниями выполняют бронхоскопию (осмотр бронхиального дерева с помощью эндоскопа при подозрении на рак бронхов, инородное тело дыхательных путей) и компьютерную томографию органов грудной клетки.
О том, как проводится исследование функции внешнего дыхания:
источник
 Прослушивание проходит через стетоскоп, стетофонендоскоп или фонендоскоп, причем последний наиболее подходит для изучения звуков, издаваемых грудной клеткой при астме. Если происходит обострение, свист и характерные хрипы слышны по всей легочной поверхности, но при ремиссии свистящий хрип слышен снизу от лопаток и то только при усиленном вдохе.
Прослушивание проходит через стетоскоп, стетофонендоскоп или фонендоскоп, причем последний наиболее подходит для изучения звуков, издаваемых грудной клеткой при астме. Если происходит обострение, свист и характерные хрипы слышны по всей легочной поверхности, но при ремиссии свистящий хрип слышен снизу от лопаток и то только при усиленном вдохе. если в анализе крови отсутствуют признаки воспалительных процессов и токсинов, выделяемых бактериями, то при наличии астматических симптомов доктору легче отличить астму от обычного бронхита или пневмонии;
если в анализе крови отсутствуют признаки воспалительных процессов и токсинов, выделяемых бактериями, то при наличии астматических симптомов доктору легче отличить астму от обычного бронхита или пневмонии;
