Прокол легкого — медицинская манипуляция, которая выполняется с диагностической и в некоторых случаях с лечебной целью. Она часто проводится при острых состояниях в качестве неотложной помощи. Также подобная процедура назначается при подозрении на серьезные патологии, такие как злокачественные новообразования, в таком случае она носит название «биопсия».
Первым этапом диагностики заболеваний дыхательной системы являются флюорография и рентген. В случае если на этапе скрининга было обнаружена очаговая или диффузная патология легочной ткани, пациенту назначаются дополнительные методы диагностики с целью дообследования. К ним относят КТ или МРТ, бронхоскопию и биопсию легких.
Под биопсией специалисты подразумевают взятие кусочка ткани с дальнейшим гистологическим исследованием и установлением окончательного правильного диагноза. По способу изъятия образца для микроскопии различают следующие виды обследования:
Выбор методики проведения биопсии легочной ткани осуществляет лечащий врач в зависимости от локализации патологического очага и предполагаемой природы заболевания, тяжести состояния больного, сопутствующих патологий, а также наличия необходимых для манипуляции медицинских инструментов.
Биопсия необходима при подозрении на инфекционные процессы, новообразования и кисты в ткани легкого. Методика проведения диагностической процедуры зависит от того, в каком участке локализуется обнаруженный ранее патологический процесс. Наиболее часто применяются:
- Трансбронхильная биопсия. Забор биоматериала осуществляется специальными хирургическими щипцами, вводимыми в просвет дыхательных путей одновременно с бронхоспокопом. Под контролем получаемого во время манипуляции изображения, а также рентгенологических снимков, врач прокалывает стенку подозрительного участка бронха и забирает небольшой фрагмент тканей для дальнейшего гистологического исследования. Чаще всего процедура показана при центральном раке, кистах.
В современных клиниках возможно проведение видеоторакоскопической манипуляции. При этом в области локализации подозрительного участка производится несколько небольших разрезов на коже, через них вводится игла для биопсии и камера, под контролем которой происходит забор патологической ткани. Процедура отличается коротким восстановительным периодом, однако, вследствие своей высокой цены не получила широкого распространения.
Как и любая медицинская манипуляция, процедура биопсии легких требует специализированной подготовки. Она включает в себя следующие этапы:
Перед процедурой доктор информирует больного о показаниях к ее проведению и возможных рисках, а также собирает аллергологический анамнез, поскольку во время биопсии легкого применяются местные анестетики и препараты для наркоза.
К показаниям для проведения биопсии относят подозрение на опухоли легкого, саркоидоз, туберкулез, пневмофиброз, гистиоцитоз и альвеолит. С диагностической целью процедура проводится при обнаружении любых подозрительных образований на рентгене.
Также пункцию легкого используют в качестве неотложной помощи при пневмотораксе — скоплении газа между листками плевры вследствие травмы или на фоне сопутствующего туберкулеза, бронхоэктатической болезни. При этом прокол делают во 2 межреберье по среднеключичной линии без применения обезболивающих препаратов.
Запрещена манипуляция при следующих состояниях:
- Гипоксия.
- Астматический приступ.
- Тяжелое общее состояние пациента.
- Легочное кровотечение, кровохарканье.
- Злокачественное нарушение сердечного ритма.
К относительным противопоказаниям относятся тромбоцитопения, нарушения свертываемости крови и хроническая почечная недостаточность, поскольку данные состояния могут приводить к повышенному риску кровотечений. Кроме этого с осторожностью биопсия легких назначается при легочной гипертензии и аритмиях.
Под проколом лёгкого нередко подразумевают плевральную пункцию, т. е. лечебно-диагностическую процедуру, суть которой состоит в заборе с последующим анализом или удалением излишнего объема патологической жидкости, скопившейся между листками плевры. Для ее выполнения:
- Больному предлагается принять сидячее положение с небольшим наклоном вперед. Для удобства можно упереться в спинку стула, кровати.
Полученную жидкость отправляют на гистологическое и биохимическое исследование.
Плевральная пункция показана пациентам с гемотораксом, выпотом жидкости на фоне инфекционных заболеваний и при раке легкого. После манипуляции необходимо обязательно пройти рентген легких для исключения осложнений.
К неблагоприятным последствиям пункции относят пневмоторакс, кровохарканье (вследствие повреждения сосудов), воздушную эмболию.
источник
Бронхиальная астма — хроническое воспалительное заболевание дыхательных путей, в котором принимают участие тучные клетки (ТК), эозинофилы и Т-лимфоциты; это заболевание характеризуется повторяющимися эпизодами хрипов, одышки, тяжести в грудной клетке, кашлем, особенно ночью и/или ранним утром; такие симптомы сопровождаются распространенной вариабельной обратимой обструкцией бронхиального дерева, разрешающейся спонтанно или под влиянием лечения.
Наиболее полные морфологические данные о состоянии бронхов и легочной ткани были получены при аутопсиях больных, умерших на высоте астматического приступа. При этом макроскопически выявляется острое вздутие легких, часто сочетающееся с эмфиземой, легкие выполняют всю грудную полость, очень часто на поверхности легких видны отпечатки ребер. Высота стояния диафрагмы определяется, как правило, на уровне 6-го ребра.
Поверхность легких обычно бледно-розового цвета, на разрезе — темно- или серо-красные. Пневмосклероз, как правило, бывает выражен умеренно. Выявляется утолщение выступающих над поверхностью разрезов стенок бронхов, практически все генерации бронхов вплоть до респираторных бронхиол заполнены густыми серовато-желтыми стекловидными слепками мокроты (бронхиального секрета), которые выдавливаются в виде тонких «червячков».
Слизистая оболочка бронхов почти на всем протяжении гиперемирована. Как правило, выражен отек легких, иногда встречается тромбоэмболия легочной артерии и/или ее ветвей. При гистологическом исследовании в расширенных просветах бронхов определяются слизистые пробки, пласты слущенного эпителия с примесью нейтрофилов, эозинофилов, лимфоцитов, почти полное оголение базальной мембраны, иногда встречаются кристаллы Шарко-Лейдена. В сохраненном эпителии увеличенное число бокаловидных клеток.
Инфильтраты в стенках бронхов состоят преимущественно из эозинофилов. Обнаруживают расширение и резкое полнокровие капилляров слизистой оболочки и подслизистого слоя. Базаль-ная мембрана обычно неравномерно толщена до 5 мкм, часто видны отдельные проходы в ней, перпендикулярные к просвету бронха, очаговая резорбция отдельных участков базальной мембраны. В настоящее время считают, что это следствие действия эозинофильного каионного и основного щелочного белков! эозинофилов.
По данным иммуноморфологии в утолщенных участках базальной мембраны повышена концентрация глобулинов, коллагенов II, III, IV типов, фибронектина, продуцируемого пролиферирующими фибробластами. Кроме того, в базальной мембране наблюдали диффузное расположение сывороточного альбумина и фибриногена. Электронномикроскопически было показано, что базальная мембрана состоит из двух компонентов: собственно базальной мембраны толщиной 0,8 мкм, которая отделена от эпителия светлой зоной толщиной 0,6 мкм, и широкой зоны, прилежащей к строме, состоящей из коллагеновых и тонких параллельных волокон. Большинство исследователей считаем что утолщение базальной мембраны связано с отложением иммунных комплексов.
Подслизистый слой почти на всем протяжении густо инфильтрирован полинуклеарами и эозинофилами. Наблюдается выраженный отек стромы полнокровие расширенных капилляров. Выявляется гиперплазия желез и перепол нение их ШИК-положительным материалом. Относительно состояния мышечной оболочки данные противоречивы. Часть авторов сообщает о гипертрофии и дистрофии миоцитов, однако при морфометрическом исследовании объемная плотность зачастую не отличается от контрольных значений, что связано с выраженным отеком стенки.
В периферической легочной ткани имеет место выраженное расширение респираторных бронхиол, альвеолярных ходов и альвеол, определяется внутриальвеолярный и интерстициальный отек, в просветах альвеол обнаруживается небольшое число альвеолярных макрофагов и эозинофилов. Описанные выше изменения встречаются, как правило, у умерших с анамнезом бронхиальной астмы не более 5 лет. У больных с длительным анамнезом БА к изменениям в бронхах и легочной ткани примешиваются элементы хронического продуктивного воспаления.
На основании изучения бронхобиопсий ряд исследований последних лет позволил оценить состояние бронхиальной стенки в межприступный период. Эти изменения схожи с изменениями бронхов при экспериментальных моделях в межприступный период. В настоящее время имеются данные о том, что при анализе материала бронхобиопсий возможна оценка фазы заболевания. Было показано, что в просвете бронха обнаруживаются клетки десквамированного эпителия, тельца Креолы, ассоциации нейтрофилов, лимфоцитов и эозинофилов. Увеличено число бокаловидных клеток, утолщена базальная мембрана , выявляется гиперплазия желез, расширение и полнокровие сосудов подслизистого слоя, в толще стенки увеличено число эозинофилов, лимфоцитов, нейтрофилов и ТК, единичные эозинофилы в эпителии.
Состояние мышечной оболочки не всегда одинаковое. Часто наблюдают гипертрофию и контрактуры мышечных клеток, однако это непостоянный признак, иногда встречаются мышечные клетки в состоянии зернистой или жировой дистрофии.
Остаются некоторые спорные вопросы морфологии отдельных элементов стенки. До сих пор существует лишь один критерий бронхоспазма — обнаружение в просветах бронхов не заполненных слизью пластов десквамированного эпителия. В эксперименте обнаружен еще один признак бронхоспазма — циркулярное смещение хрящевых пластинок и захождение их одна за другую. В более ранних публикациях за критерий бронхоспазма принимали гофрирован ность эпителиального пласта в виде «звездочки» и перпендикулярное расположение округлых пучков мышечных волокон, однако эти изменения встречаются и у других умерших при отсутствии клиники бронхоспазма.
Поскольку бронхоспазм является одним из пусковых механизмов БА и повторно возникает в поздней стадии приступа при наличии уже в просвете слизистых пробок, то на секции, которая, как правило, проводится спустя 6 ч после наступления смерти, когда уже начинает разрешаться трупное окоченение, достоверных признаков бронхоспазма обнаружить практически невозможно. Вероятно, ранние вскрытия в пределах первых 2 ч после смерти позволят обнаружить достоверные критерии бронхоспазма.
— Вернуться в оглавление раздела «Пульмонология.»
источник
Автор: Аверина Олеся Валерьевна, к.м.н., врач-патолог, преподаватель кафедры паталогической анатомии и патологической физиологии
Биопсия легкого – это процедура взятия образца легочной ткани для исследования и уточнения окончательного диагноза.
Первый этап диагностики заболеваний бронхов и легких, – это обычно скрининговое рентгенологическое исследование (флюорография). Но рентген может выявить только наличие очаговой или диффузной патологии в легких, примерно определить его локализацию. При выявлении патологии пациент направляется на дообследование (КТ, МРТ, эндобронхоскопию, биопсию).
Многие диффузные и очаговые патологии легких имеют схожую клиническую и рентгенологическую картину. Дифференциальный диагноз заболеваний легких очень сложен, без гистологического исследования зачастую невозможен.
Биопсия легкого до 60-х годов прошлого века проводилась только открытым хирургическим методом. В 1963 г. Андерсон впервые провел бронхоскопическую биопсию с помощью жесткого бронхоскопа. В 1974 г. Левин опубликовал опыт биопсии с помощью гибкого бронхоскопа.
По способу доступа к легочной ткани в настоящее время выделяют 4 основных вида биопсии:
-
Эндоскопическая трансбронхиальная биопсия. Проводится во время процедуры бронхоскопии.
- Чрескожная трансторакальная биопсия. Выполняется длинной толстой иглой путем прокола грудной стенки под ультразвуковым или рентгенологическим контролем.
- Открытая трансторакальная биопсия. Выполняется открытый хирургический доступ через разрез в межреберье.
- Эндоторакоскопическая биопсия. Наиболее современный метод, доступ к легкому осуществляется через торакоскоп (эндоскоп для исследования плевральной полости).
Выбор метода биопсии зависит прежде всего от локализации патологического участка, наличия необходимого оборудования, состояния пациента, наличия сопутствующей патологии, а также от согласия самого больного на тот или иной вид вмешательства.
Наиболее информативна биопсия легкого для выявления:
- Доброкачественной или злокачественной опухоли.
- Саркоидоз.
- Аллергический пневмонит.
- Легочных инфекций.
- Пылевые пневмониты.
- Поражения легких при системных заболеваниях, васкулитах.
Абсолютные противопоказания:
- Тяжелое состояние пациента.
- Тяжелая гипоксия.
- Астматический приступ.
- Несогласие пациента.
- Злокачественная аритмия.
- Массивное кровохарканье.
- Геморрагический диатез, тяжело поддающийся лечению.
Относительные противопоказания:
- Тромбоцитопения менее 50 тыс тромбоцитов в мкл.
- Хроническая почечная недостаточность (повышается риск кровотечений).
- Искусственная вентиляция легких.
- Аритмии.
- Легочная гипертензия.
Перед проведением биопсии обычно используются все возможные методы визуализационной диагностики (рентгенография, компьютерная томография, магнитно-резонансная томография). Это необходимо для максимально точного определения локализации патологии, особенно при очаговых образованиях в легких.
От этого зависит выбор метода биопсии.
Иногда патологический очаг не виден на рентгеновских и компьютерных снимках (например, на начальной стадии эндобронхиальной опухоли). Тогда биопсию выполняют сразу во время диагностической бронхоскопии из подозрительных участков.
Независимо от выбранного метода необходимо:
- Отмена лекарственных препаратов, вызывающих разжижение крови (аспирин, варфарин, плавикс, индометацин, ибупрофен и др.) за 3-4 дня до назначенной процедуры.
- Отказ от пищи за 8 часов до начала процедуры.
Такая биопсия проводится при глубоком расположении патологического очага и наличии его связи с главными, долевыми, сегментарными и субсегментарными бронхами.
Эндобронхиальная биопсия выполняется амбулаторно, под местной анестезией. Возможна предварительная премедикация с транквилизатором и атропином.
Бронхоскоп вводится через нос (реже – через рот). Слизистая предварительно орошается раствором лидокаина. Положение пациента обычно – лежа на спине.
Врач последовательно осматривает все отделы бронхиального дерева. Взятие биопсии осуществляется специальными щипцами, вводимыми через инструментальный канал бронхоскопа. Щипцы «выкусывают» кусочек ткани из патологического очага (при узловых образованиях) или из разных мест (при диффузных заболеваниях).
С помощью бронхоскопии иногда производят и трансбронхиальную пункцию лимфоузлов средостения.
Вся процедура занимает 30-50 минут.
Сама процедура неприятна, но не болезненна. Небольшое кровохарканье после проведения бронхоскопической биопсии возможно, оно быстро проходит.
Очень редко возможны осложнения:
- Легочное кровотечение.
- Повреждение висцеральной плевры с развитием пневмоторакса.
Другие названия: трансторакальная, игловая биопсия.
чрескожная пункционная биопсия
Такая биопсия назначается при расположении очага ближе к периферии легкого, вдали от крупных сосудов и нервных пучков, а также для исследовании плевры при неясных ее поражениях.
Проводится такая процедура также амбулаторно и в основном под местной анестезией. Общий наркоз возможен у детей, а также возбудимых лиц.
Место вкола пункционной иглы выбирается после рентгенологического многоосевого или КТ контроля по принципу кратчайшего расстояния до места взятия биопсии.
Производится анестезия кожи, подкожной клетчатки местным анестетиком, затем осуществляется прокол всех слоев грудной стенки и висцеральной плевры с помощью специальной биопсийной иглы. Игла может быть:
- Тонкой (как в обычном шприце) – для проведения аспирационной биопсии и цитологического исследования.
- Толстой (с вакуумным устройством для забора полноценного образца ткани) – для трепанационной биопсии.
Игла продвигается под контролем УЗИ, флюороскопии, или КТ. При этом главная задача пациента – находиться неподвижно в течение 20-30 минут, не кашлять. Несколько раз потребуется задержка дыхания. Положение – сидя или лежа (при КТ контроле).
После того, как игла достигла нужного участка, включается вакуумный механизм и осуществляется забор ткани для исследования. Необходимо взять образцы из нескольких различных мест.
После извлечения иглы на место прокола накладывается повязка.
Около часа пациент будет находиться под наблюдением. После этого при необходимости осуществляется рентгенологический контроль для исключения осложнений.
Возможные осложнения:
- Пневмоторакс (попадание большого количества воздуха в плевральную полость).
- Кровотечение.
- Ателектаз (спадение части легкого с нарушением дыхательной функции).
- Более поздние осложнения при присоединении инфекции – гнойный плеврит, флегмона грудной стенки.
- Развитие имплантационных метастазов по ходу пункционного канала.
- Подкожная эмфизема.
- Обострение специфического воспаления.
С развитием эндоскопической техники показания к чрескожной биопсии все более сужаются, так как она является более травматичным методом по сравнению с остальными.
Открытая биопсия легкого назначается в некоторых случаях, когда малоинвазивные методы неосуществимы (патологический участок находится в труднодоступном месте, высок риск осложнений, для исследования необходим достаточно большой образец ткани, при отсутствии результата от других видов биопсий). Основное показание для открытой биопсии – это диффузные интерстициальные заболевания легких с нарастающей дыхательной недостаточностью неясной природы (а таких заболеваний насчитывается около 100).
Открытая биопсия проводится под общим эндотрахеальным наркозом в условиях стационара. Осуществляется разрез в области наиболее подходящего межреберья.
Классическая малая торакотомия – это разрез длиной 8 см в 3-4 межреберье кпереди от передней подмышечной линии. С помощью наркозного аппарата легкое раздувается, часть его выпячивается в рану. На эту клиновидно выбухающую часть накладывается аппарат, который прошивает легкое и плевру скобами.
Таким образом сразу проводится герметизация плевральной полости. Прошитая часть отсекается и направляется на исследование. Это называется краевой резекцией легкого.
После изъятия в плевральной полости оставляется дренаж. На кожу накладываются швы. Пациент выписывается из стационара через несколько дней.
Торакоскопическая биопсия ценна в тех случаях, когда патологический процесс затронул плевру, или в случаях диссеминированного поражения легких (милиарный туберкулез, канцероматоз, множественные метастазы).
Обследование проводится под общим эндотрахеальным наркозом с раздельной интубацией бронхов. Исследуемое легкое выключается из вентиляции.
В грудной стенке делается несколько проколов: для торакоскопа и для инструментов. Изображение с окуляра торакоскопа выводится на монитор в многократно увеличенном виде.
После тщательной ревизии плевральной полости выбирают метод биопсии.
При поверхностно расположенных очагах производится щипцовая биопсия. Специальными щипцами производится взятие образцов тканей из нескольких разных участков. Это наиболее простой и эффективный способ.
При глубоко расположенных очагах или диссеминированном процессе в легких производится краевая резекция с помощью эндо-степлера.
Продолжительность процедуры – около 30- 40 минут. После выхода из наркоза пациент может быть отпущен домой.
Кусочки тканей для исследования берут из центра патологического участка, а также с его периферии. Количество отобранных образцов должно быть не менее пяти.
Отобранные образцы помещаются в специальный контейнер с консервирующей средой (формалин), подписывается и отправляется в гистологическую лабораторию. Если применялась тонкоигольная аспирационная биопсия (ТАБ), полученный пунктат помещают сразу на предметное стекло.
Если предполагается бактериологическое исследование, несколько образцов помещают в специальную питательную среду или просто в стерильный контейнер.
Исследование отобранных образцов выполняют врачи- патологоанатомы. Образец помещается в специальный раствор, затем в парафин для уплотнения. Из плотного кусочка готовят микросрезы специальным ножом (микротомом) для исследования под микроскопом. Готовые образцы окрашиваются и помещаются на предметное стекло.
Весь этот процесс подготовки образцов занимает время (около недели), поэтому так долго приходится ждать ответов из лаборатории (в среднем – две недели, учитывая загруженность врачей).
При биопсии легкого можно выявить следующие заболевания:
-
Рак легкого. Рак легкого может развиваться из эпителия (эпидермоидный рак) и железистых клеток (аденокарцинома, железисто-плоскоклеточный рак). Он может быть дифференцированным, низкодифференцированным и недифференцированным. Морфологическая картина рака – это наличие клеток, отличающихся по строению от нормальных тканей, различных по форме и размеру, с нарушенным клеточным строением и большим количеством делений. Чем менее клетки похожи на соседнюю здоровую ткань, тем менее дифференцированный тип опухоли, и тем она более злокачественна.
- Саркоидоз. При саркоидозе поражаются мелкие лимфатические сосуды легкого: образуются гранулемы в них рядом с ними.
- Хронический бронхит. В препаратах выявляется клеточная воспалительная инфильтрация, атрофия или гиперплазия железистых клеток, развитие грануляционной ткани, деструкция стенок бронхиол, потеря эластина.
- Фиброзирующий альвеолит. Гиперплазия пневмоцитов IIтипа, развитие в легких воздушных полостей по типу «медовых сот».
- Туберкулез легких. В препаратах выявляются гранулемы с очагами казеозного некроза. Уточнить диагноз позволяет проведение бактериологического исследования.
- Аллергический альвеолит. Картина хронического воспаления в ответ на попадание в легкие пылевого аллергена.
- Гистиоцитоз Х. Заболевание неизвестной природы. В биоптатах выявляется инфильтрация эозинофилами, макрофагами и клетками Лангерганса.
- Пневмофиброз. Это сборное понятие, являющееся результатом разрешения различных процессов. Морфологическая картина характеризуется разрастанием в легком соединительной ткани.
- Если предложена биопсия легкого, значит другие методы диагностики недостаточны для постановки правильного диагноза.
- Существует около сотни различных заболеваний, при котором поражается ткань легкого, окончательный ответ может дать только биопсия.
- Биопсия легкого – процедура, проводимая в основном амбулаторно и под местным обезболиванием. Сильной боли при этом не бывает, необходимо настроиться только на 40-50 минут почти неподвижного положения.
- Не стоит заранее паниковать. Большая часть узловых образований в легких оказываются доброкачественными опухолями.
- Следует настроиться на ожидание ответа из лаборатории, подготовка препарата и очередь на исследование занимают около 2-х недель времени.
- Необходимо знать, что результат из лаборатории может быть предположительным или сомнительным. В таких случаях требуется повторная биопсия сразу или через какой-то промежуток времени.
источник
Разрез кожи длиной до 5 см производят вдоль внутреннего края груднинноключично-осцевидной мышцы или по ее ходу. С косметической целью производят разрез кожи по ходу складки шеи. Середина разреза должна соответствовать месту наибольшей пульсации сонной артерии, определяемой пальпаторно перед операцией.
После рассечения кожи и подкожной мышцы до четвертой фасции шеи мягкие ткани с помощью двух диссекторов (с длинными и короткими брапшами) раздвигают без особого затруднения вдоль внутреннего края m. sternocleidomastoideus. Влагалище мышцы не вскрывают. Четвертую фасцию, окутывающую сосудисто-нервный пучок, рассекают под общей сонной артерией. При рассечении фасции следует избегать повреждения «исходящей ветви подъязычного нерва, идущей по переднему краю общей сонной артерии к прямым мышцам шеи.
После рассечения четвертой фасции шеи диссектором выделяют санные артерии. До выделения сонных артерий необходимо тупым крючком сместить кнаружи внутреннюю яремную вену, чтобы не поранить ее. Иногда вена располагается над сонными артериями и значительно затрудняет операцию. В таких случаях целесообразно пересечь между лигатурами общую лицевую вену, после чего внутренняя яремная вена свободно смещается в сторону.
Необходимо также учитывать варианты отхождения верхней щитовидной артерии. Иногда она пересекает развилку сонных артерий и затрудняет выделение каротидного тельца. В таких случаях ее необходимо пересечь между лигатурами.
Учитывая анатомические особенности сонных артерий, каротидное тельце выделяют, начиная с У-образного рассечения адвентиции cocудов. В начале адвентицию рассекают по переднему краю общей сонной артерии на 1 см ниже развилки, затем линию разреза продолжают на 2—2,5 см вдоль передне-наружного края наружной сонной артерии и передне-внутреннего края внутренней сонной артерии. Для того чтобы не повредить мышечный слой сосуда, адвентицию следует рассекать длинными сосудистыми ножницами, приподнимая ее анатомичэским пинцетом.
После рассечения адвентиции диссектором с короткими брашнами, скользя по краю наружной и внутренней сонных артерий, делают отверстие в адвентиции соответственно на задне-ннаружной и задне-внутренней поверхностях сонных артерий. Для профилактики кровотечения и удобства выделения каротидного азльца под общую сонную артерию и ее наружную ветвь подводит резиновые держаки. Приподнимая сонные артерии резиновыми держалками, диссектором с длинными браншами мобилизуют их заднюю стенку.
Образованный между внутренней и наружной сонно-артерией тяж берут на кетгутовую держалку. Осторожно у луковицы сонной apтерии максимально выделяют каротидное тельце. Кровотечение, возникающее из vasa pasorum, останавливают непродолжительным прижатием марлевым шариком. Артерию каротидного тельца перевязывают кетгутовой и шелковой лигатурами (на случай соскальзывания одной из них при отсечении тельца).
Межкаротидный тяж перевязывают кетгутовой лигатурой ниже подъязычного нерва. Между верхней лигатурой и каротидным тельцем тяж пересекают под диссектором. Каротидное тельце приподнимают анатомическим пинцетом и отсекают выше второй лигатуры. Рану зашивают наглухо. Если во время операции наблюдалась повышенная кровоточивость, для профилактики образования гематомы к сонным артериям подводят резиновую полоску из перчатки (Е. С. Карашуров, 1971).
По мнению Nakayama (1961), Phyllips (1966) и Е. С. Карашуровэ (1969), основным вмешательством на синокаротидной зоне следует считать удаление каротидного тельца. Различные методы денервации синокаротидной зоны вряд ли целесообразны, так как впоследствии иннервация восстанавливается. Е. М. Рутковский (1967), напротив, видит успех операции в денервации синокаротидной зоны.
После обнажения бифуркации общей сонной артерии и каротидного синуса автор иссекает сначала все рецепторные поля хемо- и барорецепторов в sinus caroticus (denervatio simplex sinus carotid), а затем, отделив нервный пучок между наружной и внутренней сонной артериями, содержащий симпатические и парасимпатические волокна и нерв Геринга, отсекает его периферическую часть (denervatio radicalis sinuus oarotici).
При операциях на синокаротидной зоне возможны такие осложнения, как повреждение купола плевры с последующим пневмотораксом у больных с короткой шеей, кровотечение из артерии каротидного тельца, остановка сердечной деятельности, аневризма и разрыв денервировашюго синуса, отрыв верхней щитовидной артерии от наружной сонной артерии, кровотечение из внутренней яремной вены и общей вены лица, моно- и гемипарез, гемиплегия, парез языкоглоточного и возвратного нервов, ларингоспазм, моторная афазия, повышение артериального давления с явлениями коллапса.
У ряда больных в отдаленные сроки после операции наблюдается гипертонический синдром (О. М. Тевит, 1968; М. И. Кузин и др., 1968). Наибольшим количеством наблюдений (более 2000) по оперативному лечению бронхиальной астмы на синокаротидной зоне располагает Nakayama. Непосредственно после операции хорошие результаты получены в 25,6%, улучшение — в 63,8%, ухудшение — в 2,2%, не отмечено изменений — в 6,4% случаев. Умерло 2,1% больных. Спустя. 5 лет после операции выздоровление констатировано в 16%, улучшение — в 42%, ухудшение — в 7,1%, смерть — в 4,5% случаев. Прооперировав свыше 800 больных бронхиальной астмой и изучив их состояние в отдаленные сроки, Е. М. Рутковский сообщает об излечении 70—80% больных.
В нашей стране к началу 1969 г., по сводным данным литературы (Е. С. Карашуров), на синокаротидной зоне произведено 1345 операций у больных бронхиальной астмой. По данным отечественных авторов, непосредственные хорошие и удовлетворительные результаты могут быть достигнуты у 60—80% оперированных. В отдаленные сроки результаты оперативного лечения бронхиальной астмы благоприятны. Положительный эффект операции сохраняется лишь в 14—40% наблюдений (С. И. Бабичев, Г. Н. Акжигатав, 1968; В. М. Грубиик, В. В. Тринчук, 1968; Е. С. Карашуров, 1969; И. Э. Велик, 1969; М. И. Кузин, В. Г. Рябцев, Т. Н. Дремина, 1968; Н. Б. Васильев, А. Т. Лидский, , Н. П. Макаров, В. А. Бабаев, 3. С. Симонова, 1971).
Отдельные авторы сообщают о полном отсутствии эффекта при гломэктомии у больных бронхиальной астмой (Pfarscher, Stresemann, 1965; Swedlund, Henderson, Payne, Fowler, 1965).
Некоторые авторы изучали непосредственные и ближайшие результаты гломэктомии у больных бронхиальной астмой методом плацебо (Gain, Tulloch, 1964; Q. Rourke, 1964; Segal, 1965). В 138 наблюдениях произведена гломэктомия; у 68 больных сделан лишь кожный разрез в области синокаротидной зоны. Несмотря на незначительную операционную травму (кожный разрез), после операции умерло 4 больных контрольной группы. У больных, перенесших гломэктомию, и у больных контрольной группы (кожный разрез) результаты были одинаковы.
Таким образом, по мнению ряда исследователей, при дисфункции каротидного тельца и неэффективности медикаментозного лечения возникают показания к хирургическому вмешательству на сипокаротидной зоне. Для выявления повышенной активности каротидного тельца Takino (1968) предлагает проводить пробы с 1% раствором цианистого натрия, который вводится внутривенно в количестве 0,3 мл, и исследовать функцию внешнего дыхания.
Для этих же целей Nakayama рекомендует пробу с вдыханием слабого раствора соляной кислоты. Для правильного обоснования показаний к операции на синокаротидной зоне при бронхиальной астме Е. М. Рутковский использует новокаиновую блокаду синокаротидной зоны на высоте приступа. Эффективность блокады служит критерием для отбора больных. Однако многие вопросы, связанные с оперативными вмешательствами на синокаротидной зоне, остаются неизученными.
Так, не решен вопрос относительно левосторонней или правосторонней гломэктомии. Е. С. Рутковский, И. Э. Велик, И. А. Коршинов применяют левосторонний доступ, Overholt и Planger — правосторонний. Е. С. Карашуров производит гломэктомию на стороне с большими изменениями функции внешнего дыхания. Нет единого мнения о том, выполнять ли одностороннюю или двустороннюю гломэктомию. Например, Nakayama, полагает, что если одностороннее вмешательство не приносит успеха, операция с другой стороны бессмысленна.
Однако по данным И. Э. Велик (1969) и Е. С. Карашурова (1969), удаление второго каротидного гломуса при неэффективности односторонней гломэктомии оказывает дополнительный эффект. Вместе с тем необходимо учесть, что при двустороннем вмешательстве создается большая возможность для тяжелых гемодинамических расстройств.
Противопоказанием к операции на синокаротидной зоне являются выраженные вторичные изменения в легких, туберкулез, гипертоническая болезнь, декомпенсированный порок сердца, печеночная и почечная недостаточность. Некоторые же авторы полагают, что сердечная декомпенсация и легочная недостаточность служат прямым показанием к операции (Phyllips, 1966).
Детский возраст, по мнению отдельных авторов, не является противопоказанием к гломэктомии. Ставя показания к хирургическому лечению бронхиальной астмы у детей, Е. С. Карашуров учитывал особенности этого возраста и возможность самоизлечения при достижении совершеннолетия. Однако в ряде наблюдений автор был убежден в целесообразности хирургического вмешательства у детей.
Исследовав больных, заболевших бронхиальной астмой 20 лет назад в детском возрасте, Buffum и Jettipone (1966) установили, что заболевание развилось у лиц, в процессе лечения которых не отмечено положительной динамики. Этот факт свидетельствует в пользу оперативного лечения бронхиальной астмы в детском возрасте, на ранних стадиях заболевания. Trajan (1967) оперировал по методу Рутковского 8 детей. Рецидив заболевания возник только у одного ребенка после гриппа.
Итак, хирургическое лечение больных бронхиальной астмой возможно при неэффективности комплексных консервативных мероприятий. Наиболее патогенетически обоснованными методами следует считать оперативные вмешательства на синокаротидной зоне и денервацию корня легкого. Показание к тому или иному вмешательству должно вытекать из генеза заболевания. При атонической форме бронхиальной астмы целесообразно вмешательство на синокаротидной зоне, так как оно менее травматично и опасно.
При инфекционно-аллергической форме бронхиальной астмы необходимо ликвидировать инфекционный очаг. Нередко при этой форме бронхиальной астмы у больных наблюдается деструктивный процесс в легких (Е. Н. Мешалкин, В. С. Сергиевский, Л. Я. Альперин, 1966; И. Е. Бе-лик, 1969; Abbot, Hopkins, Giulfail, Walner, 1950; Overholt e. a., 1952; Д. Димитров-Сокоди, 1961). Резекция патологически измененных отделов легочной ткани с денервацией корня легкого относится к числу патогенетических методов лечения этой группы больных.
При установлении обоснованных показаний хирургическое лечение бронхиальной астмы возможно и в детском возрасте.
источник
Диагностика бронхиальной астмы выполняется, ориентируясь на полное комплексное обследование организма пациента. От правильно проведенной диагностики зависит получение положительных результатов лечения.
Протоколы (стандарты) определения заболеваемости, а также дальнейшего лечения взрослого населения и детей учитывают различные методики: клинический осмотр, сбор анамнеза, выявление симптоматики, лабораторная диагностика.
После проведения необходимых мероприятий для каждого больного подбирается индивидуальная схема лечения, которая способствует снижению заболеваемости и облегчению состояния больного. Дифференциальная диагностика бронхиальной астмы учитывает все аспекты (анализы, симптоматику, анамнез, аллергологическое исследование и дыхательную функциональность.).
Современная диагностика при развитии бронхиальной астмы является важной задачей для врача, так как адекватное лечение способно обеспечить полный контроль над заболеванием при полной нейтрализации симптоматики у детей и взрослых. Для этого оцениваются все критерии астмы с исключением ХОБЛ и постановкой предварительного диагноза.
Протоколы диагностики проводятся в несколько этапов:
Бронхиальная астма, в зависимости от степени заболеваемости, определяется наиболее часто в детском и подростковом возрасте. Как правило, наблюдается генетическая предрасположенность к развитию астматических заболеваний. Кроме того, ее развитие возможно на фоне ХОБЛ.
Бронхиальный приступ нередко связан с воздействием определенных факторов, провоцируя характерную симптоматику (одышку, кашель, свистящее дыхание, слабость и т.д.). Приступ способен появиться внезапно. Его можно купировать при помощи ингаляционных бронхолитиков. Если после использования ингалятора приступ не снимается, необходимы дальнейшие протоколы диагностики, а также исключение ХОБЛ.
В начальной стадии заболевания профессиональная диагностика не способна определить какие-то определенные протоколы в определении бронхиальной астмы, кроме исключения ХОБЛ. Во время затяжного приступа может возникнуть симптом «бочкообразной грудной клетки», что связано с затрудненным выдохом. В результате этого возможно постепенное развитие эмфиземы, критерии и протоколы которой зависят от выраженности симптоматики и стадии заболеваемости. От результатов визуального осмотра может зависеть дальнейшее лечение.
Немаловажным способом профессиональной диагностики является перкуссия (выстукивание) и аускультация (выслушивание) легких. По мере развития приступа можно услышать свистящее дыхание и хрипы в легких. Перкуссия эффективна при длительном течении заболевания и эмфиземе.
Лабораторная диагностика предполагает назначение проведения различного вида анализов, среди которых:
- биохимический анализ крови — определяет количество эозинофилов, являющихся маркерами аллергического процесса. Кроме того, этот анализ в совокупности с аллергологической пробой, позволяет выявить конкретный аллерген, на который острее всего реагирует организм;
- общий анализ крови — позволяет выявить воспалительные процессы, ХОБЛ и интоксикацию в организме больного. Забор крови выполняется натощак;
- общий анализ мокроты — выявляет характерные астматические маркеры с характерными спиралями Куршмана и кристаллами Шарко – Лейдена. При этом определяется вязкая и густая мокрота, которая может расслаиваться двумя слоями. При микроскопическом исследовании определяются эозинофилы;
- анализ кала — способствует выявлению паразитарных инвазий, которые нередко провоцируют развитие бронхиальной астмы. Например, аскариды при своей цикличности развития способны проникнуть через легочную систему, вызывая общую интоксикацию организма, ослабление иммунной системы, повышенную аллергизацию пациента;
- аллергопроба (включая скарификационную) — критерии проведения аллергопробы позволяют уточнить наличие триггера в крови, который вызывает ответную цепь реакций в крови, приводя к бронхоспазму. При положительном ответе могут наблюдаться местные признаки воспаления (зуд, гиперемия, отек и т.д.).
Наиболее сложно диагностировать астму при наличии обструктивного бронхита (ХОБ). Этот процесс проявляется, как хроническая обструктивная болезнь легких (ХОБЛ).
Протоколы выполнения этого вида диагностики служат показателями для постановки итогового диагноза.
Профессиональная рентгенография способна выявить повышенную воздушность легочной ткани (эмфизему) и усиленный легочный рисунок за счет активного притока крови к легочной ткани. Тем не менее, следует учитывать, что иногда даже рентгенограмма не может выявить изменения. Поэтому принято считать, что методы рентгенографии глубоко неспецифичны.
Этот метод служит для определения ФВД (функций внешней дыхательной деятельности) и является достаточно эффективным. Профессиональная спирометрия способна определить ряд главных показателей дыхательной деятельности.
Диагностика спирометрии выглядит следующим образом:
- пациенту предлагается дышать через специальный прибор (спирометр), который обладает чувствительностью и фиксирует все изменения дыхания;
- анализ проведенного обследования сравнивается (врачом или пациентом) с рекомендуемыми показателями ФВД;
- на основании профессиональной сравнительной характеристики внешнего дыхания врач устанавливает предварительный диагноз (для 100% уверенности в диагнозе одной спирометрии недостаточно);
- если у больного наблюдается бронхообструктивные нарушения (исключая ХОБЛ) это может говорить о проявлении бронхиальной астмы.
Помимо этого, спирометрические данные позволяют определить тяжесть астматического приступа и эффективность проводимого лечения в том случае, когда оно использовалось.
Этот метод диагностирования относится к нововведениям для контроля и определения развития бронхиальной астмы у взрослого пациента. Мониторинговый протокол с участием пикфлоуметра обладает следующими преимуществами:
- позволяет определить обратимость бронхиальной обструкции;
- возможность оценки тяжести течения болезни;
- протоколы пикфлоуметрии позволяют спрогнозировать период, когда возникает астматический приступ, в зависимости от степени заболеваемости;
- возможность выявления профессиональной астмы;
- мониторинг эффективности проводимого лечения.
Пикфлоуметрию следует выполнять ежедневно. Это позволяет получить более точные результаты диагностики.
При помощи этого способа профессиональной диагностики определяется пиковая объемность и максимальная объемная скорость на различных уровнях, учитывая процентное соотношение ФЖЕЛ (форсированную жизненную емкость легких). Измеряют максимальную скорость на уровне в 75%, 50% и 25%.
Наиболее затруднительны протоколы определения профессиональной астмы, так как приступ могут вызвать некоторые химические соединение, присутствующие в воздухе. Для подтверждения профессиональной астмы необходимо выяснение анамнеза у взрослого пациента, а также анализ показателей внешней дыхательной деятельности. Кроме того, необходимо в обязательном порядке своевременно сдавать анализы (мокроты, мочи, крови и т.д.) и проводить необходимое лечение.
Одновременно с показателями внешнего дыхания и в зависимости от выраженности симптоматики проводятся прик-тесты (инъекционные) и скарификационная проба на выявление аллергологической этиологии. Однако следует учитывать, что клиническая картина таких обследований в некоторых случаях могут дать ложнопозитивный или ложнонегативный ответ. Именно поэтому рекомендуется проводить исследование крови на наличие специфических антител в сыворотке. В профессиональной диагностике особенно важно выяснение аллергического статуса у детей.
Диагностика бронхиальной астмы у детей нередко сопровождается большими трудностями. Это связано, прежде всего, с симптоматикой заболевания у детей, которая аналогична многим другим детским заболеваниям. Поэтому многое зависит от выяснения анамнеза со склонностью к аллергическим заболеваниям. В первую очередь необходимо опираться на повторение ночного приступа бронхиальной астмы, что подтверждает развитие заболевания.
Помимо этого, протоколы диагностики предусматривают проведение ФВД (функционального исследования внешнего дыхания) с бронходилататорами для назначения адекватной тактики лечения. Вполне естественно, что необходимо сдать анализы мокроты, крови и кала, а также провести спирометрическое тестирование и аллергообследование.
Следует отметить, что затруднительно проводить диагностику астматического приступа у лиц пожилого возраста. Это связано, прежде всего, с обилием хронических заболеваний, которые сопровождают бронхиальную астму, «стирая» ее картину. В этом случае, необходим тщательный сбор анамнеза, исследование мокроты и крови, выполнение специфических тестирований, направленных на исключение вторичных заболеваний. Прежде всего, проводится диагностика сердечной астмы, выявление ИБС, сопровождающейся симптомами недостаточности левого желудочка.
Кроме того, рекомендуется проводить функциональные методы выявления бронхиальной астмы, включающие ЭКГ, рентгенографию, пикфлоуметрию (в течение 2 недель). Только после выполнения всех диагностических мероприятий назначается симптоматическое лечение бронхиальной астмы.
источник
Бронхиальная астма – диагноз клинический, то есть врач ставит его на основании прежде всего жалоб, истории заболевания и данных осмотра и внешнего исследования (пальпации, перкуссии, аускультации). Однако дополнительные методы исследования дают ценную, а в некоторых случаях определяющую диагностическую информацию, поэтому они широко применяются на практике.
Диагностика бронхиальной астмы с помощью дополнительных методов включает проведение лабораторных анализов и инструментальных исследований.
Пациенту с астмой могут быть назначены следующие анализы:
- общий анализ крови;
- биохимический анализ крови;
- общий анализ мокроты;
- анализ крови для выявления общего IgE;
- кожные пробы;
- определение в крови аллергенспецифических IgE;
- пульсоксиметрия;
- анализ крови на газы и кислотность;
- определение оксида азота в выдыхаемом воздухе.
Разумеется, не все эти тесты выполняются у каждого больного. Некоторые из них рекомендуются лишь при тяжелом состоянии, другие – при выявлении значимого аллергена и так далее.
Общий анализ крови выполняется у всех пациентов. При бронхиальной астме, как и при любом другом аллергическом заболевании, в крови отмечается увеличение количества эозинофилов (EOS) более 5% от общего количества лейкоцитов. Эозинофилия в периферической крови может возникать не только при астме. Однако определение этого показателя в динамике (повторно) помогает оценить интенсивность аллергической реакции, определить начало обострения, эффективность лечения. В крови может определяться незначительный лейкоцитоз и увеличение скорости оседания эритроцитов, однако это необязательные признаки.
Биохимический анализ крови у больного с астмой часто никаких отклонений не выявляет. У некоторых пациентов отмечается увеличение уровня α2- и γ-глобулинов, серомукоида, сиаловых кислот, то есть неспецифических признаков воспаления.
Обязательно проводится анализ мокроты. В ней находят большое количество эозинофилов – клеток, участвующих в аллергической реакции. В норме их меньше 2% от всех обнаруженных клеток. Чувствительность этого признака высокая, то есть он обнаруживается у большинства больных с астмой, а специфичность средняя, то есть, помимо астмы, эозинофилы в мокроте встречаются и при других заболеваниях.
В мокроте нередко определяются спирали Куршмана – извитые трубочки, образующиеся из бронхиальной слизи при спазме бронхов. В них вкраплены кристаллы Шарко-Лейдена – образования, которые состоят из белка, образующегося при распаде эозинофилов. Таким образом, два этих признака говорят о снижении бронхиальной проходимости, вызванном аллергической реакцией, что часто и наблюдается при астме.
Кроме того, в мокроте оценивается наличие атипичных клеток, характерных для рака, и микобактерий туберкулеза.
Анализ крови на общий IgE показывает уровень в крови этого иммуноглобулина, который вырабатывается в ходе аллергической реакции. Он может быть повышен при многих аллергических заболеваниях, но и нормальное его количество не исключает бронхиальную астму и другие атопические процессы. Поэтому гораздо более информативным является определение в крови специфических IgE – антител к конкретным аллергенам.
Для анализа на специфические IgE используются так называемые панели – наборы аллергенов, с которыми реагирует кровь больного. Тот образец, в котором содержание иммуноглобулина будет выше нормы (у взрослых это 100 ед/мл), и покажет причинно-значимый аллерген. Используются панели шерсти и эпителия разных животных, бытовые, грибковые, пыльцевые аллергены, в некоторых случаях – аллергены лекарств и пищевые.
Для выявления аллергенов применяются и кожные пробы. Их можно проводить у детей любого возраста и у взрослых, они не менее информативны, чем определение IgE в крови. Кожные пробы хорошо себя зарекомендовали в диагностике профессиональной астмы. Однако при этом существует риск внезапной тяжелой аллергической реакции (анафилаксии). Результаты проб могут меняться под действием антигистаминных препаратов. Их нельзя проводить при кожной аллергии (атопическом дерматите, экземе).
Пульсоксиметрия – исследование, проводимое с помощью небольшого прибора – пульсоксиметра, который обычно надевается на палец пациента. Он определяет насыщение артериальной крови кислородом (SpO2). При снижении этого показателя менее 92% следует выполнить исследование газового состава и кислотности (рН) крови. Снижение уровня насыщения крови кислородом свидетельствует о тяжелой дыхательной недостаточности и угрозе для жизни больного. Определяемое при исследовании газового состава снижение парциального давления кислорода и увеличение парциального давления углекислого газа свидетельствует о необходимости искусственной вентиляции легких.
Наконец, определение оксида азота в выдыхаемом воздухе (FENO) у многих больных с астмой выявляет увеличение этого показателя выше нормы (25 ppb). Чем сильнее воспаление в дыхательных путях и больше доза аллергена, тем показатель выше. Однако такая же ситуация бывает и при других болезнях легких.
Таким образом, специальные лабораторные методы диагностики астмы – кожные пробы с аллергенами и определение в крови уровня специфических IgE.
Методы функциональной диагностики бронхиальной астмы включают:
- исследование вентиляционной функции легких, то есть способности этого органа доставлять необходимое количество воздуха для газообмена;
- определение обратимости бронхиальной обструкции, то есть снижения проходимости бронхов;
- выявление гиперреактивности бронхов, то есть их склонности к спазму под действием вдыхаемых раздражителей.
Основной метод исследования при бронхиальной астме – спирометрия, или измерение дыхательных объемов и скоростей воздушных потоков. С него обычно начинается диагностический поиск еще до начала лечения больного.
Главный анализируемый показатель – ОФВ1, то есть объем форсированного выдоха за секунду. Проще говоря, это количество воздуха, которое человек способен быстро выдохнуть в течение 1 секунды. При спазме бронхов воздух выходит из дыхательных путей медленнее, чем у здорового человека, показатель ОФВ1 снижается.
Если при первичной диагностике уровень ОФВ1 составляет 80% и больше от нормальных показателей, это говорит о легком течении астмы. Показатель, равный 60 – 80% от нормы, появляется при астме средней тяжести, менее 60% – при тяжелом течении. Все эти данные применимы только к ситуации первичной диагностики до начала терапии. В дальнейшем они отражают не тяжесть астмы, а уровень ее контроля. У людей с контролируемой астмой показатели спирометрии в пределах нормы.
Таким образом, нормальные показатели функции внешнего дыхания не исключают диагноз «бронхиальная астма». С другой стороны, снижение бронхиальной проходимости обнаруживается, например, при хронической обструктивной болезни легких (ХОБЛ).
Если обнаружено снижение бронхиальной проходимости, то важно выяснить, насколько оно обратимо. Временный характер бронхоспазма – важное отличие астмы от того же хронического бронхита и ХОБЛ.
Итак, при снижении ОФВ1 для выявления обратимости бронхиальной обструкции проводятся фармакологические тесты. Пациенту дают препарат посредством дозированного аэрозольного ингалятора, чаще всего 400 мкг сальбутамола, и через определенное время снова проводят спирометрию. Если показатель ОФВ1 увеличился после использования бронхолитика на 12% и больше (в абсолютных цифрах на 200 мл и больше), говорят о положительной пробе с бронходилататором. Это означает, что сальбутамол эффективно снимает спазм бронхов у данного пациента, то есть бронхиальная обструкция у него непостоянна. Если показатель ОФВ1 увеличивается менее чем на 12%, это признак необратимого сужения бронхиального просвета, а если он уменьшается, это говорит о парадоксальном спазме бронхов в ответ на использование ингалятора.
Прирост ОФВ1 после ингаляции сальбутамола на 400 мл и больше дает практически полную уверенность в диагнозе «бронхиальная астма». В сомнительных случаях может быть назначена пробная терапия ингаляционными глюкокортикоидами (беклометазон по 200 мкг 2 раза в день) в течение 2 месяцев или даже таблетками преднизолона (30 мг/сут) в течение 2 недель. Если показатели бронхиальной проходимости после этого улучшаются – это говорит в пользу диагноза «бронхиальная астма».
В некоторых случаях даже при нормальных показателях ОФВ1 применение сальбутамола сопровождается приростом его величины на 12% и больше. Это говорит о скрытой бронхиальной обструкции.
В других случаях нормальной величины ОФВ1 для подтверждения гиперреактивности бронхов применяют ингаляционную пробу с метахолином. Если она будет отрицательной, это может служить причиной для исключения диагноза астмы. Во время исследования пациент вдыхает возрастающие дозы вещества, и определяется минимальная концентрация, которая вызывает снижение ОФВ1 на 20%.
Применяются и другие пробы для выявления гиперреактивности бронхов, например, с маннитолом или физической нагрузкой. Падение ОФВ1 в результате использования этих проб на 15% и более с высокой степенью достоверности указывает на бронхиальную астму. Проба с физической нагрузкой (бег в течение 5 – 7 минут) широко применяется для диагностики астмы у детей. Применение ингаляционных провокационных проб у них ограничено.
Еще один важнейший метод инструментальной диагностики астмы и контроля за ее лечением – пикфлоуметрия. Пикфлоуметр должен быть у каждого пациента с этим заболеванием, ведь самоконтроль – основа эффективной терапии. С помощью этого небольшого аппарата определяют пиковую скорость выдоха (ПСВ) – максимальную скорость, с которой пациент может выдохнуть воздух. Этот показатель, так же как и ОФВ1, прямо отражает бронхиальную проходимость.
ПСВ можно определять у больных начиная с 5-летнего возраста. При определении ПСВ делается три попытки, записывается лучший показатель. Измеряют величину показателя утром и вечером каждого дня, а также оценивают его вариабельность – разницу между минимальным и максимальным значениями, полученными в течение дня, выраженную в процентах от максимальной величины за день и усредненную за 2 недели регулярных наблюдений. Для людей с бронхиальной астмой характерна повышенная вариабельность показателей ПСВ – более 20% при четырех измерениях в течение дня.
Показатель ПСВ используется преимущественно у людей с уже установленным диагнозом. Он помогает держать астму под контролем. В течение наблюдений определяют максимальный лучший показатель для данного больного. Если отмечается снижение до 50 – 75% от наилучшего результата – это говорит о развивающемся обострении и необходимости усилить интенсивность лечения. При снижении ПСВ до 33 – 50% от лучшего для пациента результата диагностируют тяжелое обострение, а при более значительном уменьшении показателя возникает угроза жизни больного.
Определяемый дважды в день показатель ПСВ нужно записывать в дневник, который приносят на каждый прием к врачу.
В некоторых случаях проводятся дополнительные инструментальные обследования. Рентгенография легких выполняется в таких ситуациях:
- наличие эмфиземы легких или пневмоторакса;
- вероятность воспаления легких;
- обострение, несущее угрозу жизни больного;
- неэффективность лечения;
- необходимость искусственной вентиляции легких;
- неясный диагноз.
У детей младше 5 лет используется компьютерная бронхофонография – метод исследования, основанный на оценке дыхательных шумов, и позволяющий выявить снижение бронхиальной проходимости.
При необходимости дифференциальной диагностики с другими заболеваниями выполняют бронхоскопию (осмотр бронхиального дерева с помощью эндоскопа при подозрении на рак бронхов, инородное тело дыхательных путей) и компьютерную томографию органов грудной клетки.
О том, как проводится исследование функции внешнего дыхания:
источник
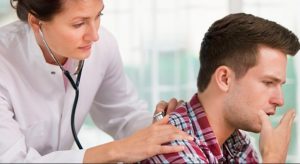

Обследование, основанное на сборе анамнеза, внешнем осмотре, пальпации, прослушивании и простукивании называется физикальным. Именно с такого метода диагностики начинается определение типа болезни.

- В каком возрасте начались астматические приступы, возможно какие детские болезни привели к астме. Это может быть коклюш, корь и другие, которые могут негативно повлиять на дыхательную систему.
- Были ли среди родственников астматики, это позволяет проследить генетическую связь, возможно кто-то из близких имел сильные аллергии.
- С какими раздражителями связаны приступы. Такие раздражители называются триггерами, и среди них может быть физическая нагрузка, холодный влажный воздух, микроскопические частицы шерсти и кожи собак, кошек, пыльца цветов разных растений, запыленность в помещении пылью определенного типа, продукты питания.
- Нужно узнать, как именно проходят приступы. Ведь при астматическом кашле пациенты принимают положение, при котором вдох менее мучительный, например, опираются руками о стол, расслабляя при этом плечевой пояс.
- Есть ли звуки при кашле, ведь свист при дыхании — это признак астматического сужения бронхов. Чтобы услышать характерные звуки при дыхании и приступах, не нужно прослушивать грудь стетоскопом, их хорошо слышно и на небольшом расстоянии.
- Долго ли длится приступообразный кашель, пропадает ли он после приема бронхолитических лекарств.
- После приступа наблюдается выделения вязкой, но прозрачной, как стекло мокроты, которая освобождает бронхи, таким образом облегчается дыхание, такие особенности также нужно узнавать при опросе.
Внешний осмотр проходит следующим образом:
- Врач смотрит на грудную клетку, которая может иметь вид, похожий на бочку. Такую форму грудная клетка приобретает вследствие развития эмфиземы, расширения легких, и, как результат — увеличение размеров грудной клетки;
-
Прослушивание проходит через стетоскоп, стетофонендоскоп или фонендоскоп, причем последний наиболее подходит для изучения звуков, издаваемых грудной клеткой при астме. Если происходит обострение, свист и характерные хрипы слышны по всей легочной поверхности, но при ремиссии свистящий хрип слышен снизу от лопаток и то только при усиленном вдохе.
- Постукивание пальцами не может эффективно сообщить информацию на ранних этапах астмы. Но если болезнь длится долго, то пальпацией и постукиванием можно услышать пустоту (звук картонной коробки), которая образовалась из-за эмфиземного расширения легких.
Лабораторные исследования проводятся в следующих направлениях:
- анализ крови направлен на определение количества эозинофилов — этот вид лейкоцитов является показателем аллергических процессов в организме;
-
если в анализе крови отсутствуют признаки воспалительных процессов и токсинов, выделяемых бактериями, то при наличии астматических симптомов доктору легче отличить астму от обычного бронхита или пневмонии;
- в мокроте под микроскопом можно обнаружить эозинофилы;
- в анализе мокроты присутствуют кристаллические вкрапления — особенные кристаллы Шарко-Лейдена и спиралевидные кристаллы Куршмана;
- мокрота при астме специфическая, отличается от мокроты при бронхите, структура двухслойная, консистенция густая, по густоте вязкая;
- методом проделывания царапин на коже (скарификации) берут пробы на аллергены, по которым уточняют аллергический возбудитель (триггер) бронхоспазма, аллергены вызывают на коже покраснение и зудящие ощущения;
- кал берут для определения гельминтов, которые могут размножиться до инвазивного количества и вызвать аллергическую интоксикацию организма, что также может влиять на возникновение приступов.
С помощью специально разработанных аппаратов проводится инструментальная диагностика. На первом месте в аппаратной диагностики стоит пикфлуометрия. На пикфлоуметре, который являет собой трубочку с нанесенной шкалой, измеряется самая большая скорость потока воздуха при выдохе, сделанном с максимальным усилием (форсированный выдох). Такая пиковая скорость выдоха называется ПСВ. Этот тест доступен детям с четырех лет, также он применяется и для взрослых.
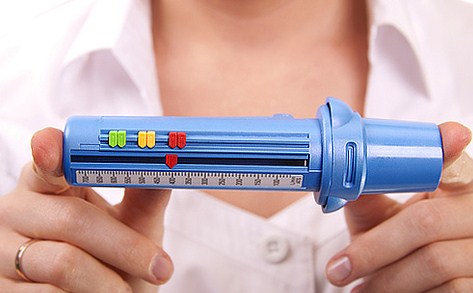
Измерительные процессы проводятся дважды в день, сутра и ближе к вечеру. Делаются три попытки, из которых выбирается та, которая сделана наиболее правильно. На трубку нанесена шкала с зеленой, желтой и красной зоной, которые обозначают степень проблемы. Но эта шкала не унифицирована, она подбираются путем индивидуальных двухнедельных исследований каждого больного. Если показатели в зеленой зоне, значит, что симптомы астмы под контролем, желтая зона — возможно обострение, при красной зоне нужно немедленно спешить человеку на помощь.
Больной должен зафиксировать лучшее значения ПСВ, и при дальнейшем использовании прибора при определении обструктивных изменений надобно соотносить с этим значениям другие показатели шкалы. Нужно правильно делать выдох форсированным способом, результаты записывать в дневник, чтобы с этими результатами ознакомить позже лечащего врача. Возможно, в вашем городе есть школа для больных астмой (где доктора рассказывают, как лечить это заболевание), поинтересуйтесь у доктора.

Спирограмма показывает форсированную жизненную емкость легких, сокращенно ФЖЕЛ, а также объем форсированного выдоха за одну секунду, сокращенно — ОФВ1, и так называемую пиковую скорость выдоха (ПСВ). Высчитывается индекс Тиффно, который составляет ОФВ1 поделить на ФЖЕЛ, у здоровых людей этот показатель выше 0,75.
Если при подозрениях на астму показатели спирографа в пределах нормы, делают медицинскую провокацию — дают больному метхолин или гистамин в виде ингаляций и сравнивают спирограмму с обычной обструкцией и под действием этих лекарств.
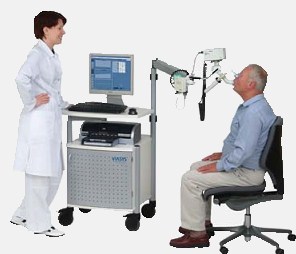
Но анализ дыхания может не дать четких результатов в случае, если заболевание являются профессиональным и приступ вызывает вещество, присутствующее только на работе. Чтобы диагностировать профессиональную астму, нужно кроме тестов дыхания изучить анализы и с помощью опроса выявить аллерген на рабочем месте пациента.
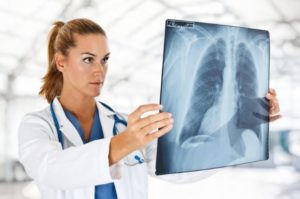
Если болезнь уже долго прогрессирует, развивается эмфизема, увеличение в объеме легких, которые на рентгенологической фотографии видимы как более прозрачные.
Томографию также назначают не во всех случаях, а только тогда, когда кашель и удушье не проходят длительное время, не смотря на лечение, и есть подозрения на наличие других болезней.
Диагностика астматических приступов у детей имеет особенности, поскольку они часто болеют респираторными и другими заболеваниями с похожими симптомами. Прежде всего у детей выясняют зависимость приступов от действий аллергенов, также возможную склонность к аллергии на генетическом уровне — есть ли близкие родственники с сильной аллергией на что-либо, это позволяет уточнить диагноз.

У детей исследуют внешнее дыхание с помощью приборов, предварительно дав бронходилататоры (препараты, расширяющие просвет в бронхах). Также сдают анализы, чтобы отследить наличие гельминтов и воспалительного процесса в организме, иногда проводят аллергологический тест. Но некоторые современные врачи отказываются от тестов на аллергены, резонно указывая на то, что в большинстве случаев аллергены вполне обычны и избежать их влияния довольно трудно.
У детей бронхиальная астма полностью излечима в большинстве случаев, однако для успешного лечения имеет большое значение своевременная диагностика бронхиальной астмы и правильное лечение, которое состоит не только в приеме медикаментов, но и в укреплении организма.
Люди пожилого возраста имеют множество заболеваний, которые могут хронически проходить долгие годы. Симптомы этих болезней могут накладываться на астматические, и клиническая картина становится нечеткой.

Кроме того, рекомендуется проводить функциональные методы выявления бронхиальной астмы, включающие ЭКГ, рентгенографию, пикфлоуметрию (это исследование нужно делать в течение 2 недель). Только после выполнения всех диагностических мероприятий назначается симптоматическое лечение бронхиальной астмы.
источник
 Эндоскопическая трансбронхиальная биопсия. Проводится во время процедуры бронхоскопии.
Эндоскопическая трансбронхиальная биопсия. Проводится во время процедуры бронхоскопии. Рак легкого. Рак легкого может развиваться из эпителия (эпидермоидный рак) и железистых клеток (аденокарцинома, железисто-плоскоклеточный рак). Он может быть дифференцированным, низкодифференцированным и недифференцированным. Морфологическая картина рака – это наличие клеток, отличающихся по строению от нормальных тканей, различных по форме и размеру, с нарушенным клеточным строением и большим количеством делений. Чем менее клетки похожи на соседнюю здоровую ткань, тем менее дифференцированный тип опухоли, и тем она более злокачественна.
Рак легкого. Рак легкого может развиваться из эпителия (эпидермоидный рак) и железистых клеток (аденокарцинома, железисто-плоскоклеточный рак). Он может быть дифференцированным, низкодифференцированным и недифференцированным. Морфологическая картина рака – это наличие клеток, отличающихся по строению от нормальных тканей, различных по форме и размеру, с нарушенным клеточным строением и большим количеством делений. Чем менее клетки похожи на соседнюю здоровую ткань, тем менее дифференцированный тип опухоли, и тем она более злокачественна.

 Прослушивание проходит через стетоскоп, стетофонендоскоп или фонендоскоп, причем последний наиболее подходит для изучения звуков, издаваемых грудной клеткой при астме. Если происходит обострение, свист и характерные хрипы слышны по всей легочной поверхности, но при ремиссии свистящий хрип слышен снизу от лопаток и то только при усиленном вдохе.
Прослушивание проходит через стетоскоп, стетофонендоскоп или фонендоскоп, причем последний наиболее подходит для изучения звуков, издаваемых грудной клеткой при астме. Если происходит обострение, свист и характерные хрипы слышны по всей легочной поверхности, но при ремиссии свистящий хрип слышен снизу от лопаток и то только при усиленном вдохе. если в анализе крови отсутствуют признаки воспалительных процессов и токсинов, выделяемых бактериями, то при наличии астматических симптомов доктору легче отличить астму от обычного бронхита или пневмонии;
если в анализе крови отсутствуют признаки воспалительных процессов и токсинов, выделяемых бактериями, то при наличии астматических симптомов доктору легче отличить астму от обычного бронхита или пневмонии;