| Признак | Бронхиальная астма | Сердечная астма |
| Анамнез | Легочная патология | Заболевание сердца |
| Одышка | Экспираторная | Смешанная |
| Мокрота | Вязкая, трудноотделяемая, «стекловидная», тонет в воде | Пенистая «розовая», плавает над водой |
| Цианоз | Диффузный теплый | Холодный акроцианоз |
| Хрипы | Сухие свистящие на всем протяжении | Влажные, крепитация внижних отделах легких |
Диагностические критерии:
Дифференциальный диагноз с бронхиальной астмой очень важен, так как при бронхиальной астме противопоказаны (опасны) наркотические анальгетики и показаны — адренергические препараты. При сердечной астме противоположность наркотические анальгетики применяются при оказании неотложной помощи.
При осмотре:
§ положение больного ортопноэ (сидя с опущенными ногами), при таком положении тела одышка уменьшается,
§ число дыханий достигает 30 и более в минуту,
§ одышка смешанного характера в покое,
§ кашель с выделением пенистой мокроты, иногда с розовым окрашиванием,
§ акроцианоз кончиков ушей, кончика носа, пальцев рук и ног.
Аускультативно:
§ выслушиваются влажные хрипы, симметрично расположенные с локализацией в нижних отделах легких. В последующем может развиться картина альвеолярного отека легких с резким нарастанием одышки.
При выслушивании сердца определяются изменения, характерные для основного заболевания:
§ митрального порока сердца (систолический шум на верхушке сердца),
§ инфаркта миокарда (глухие тоны сердца, снижение пульсового и систолического АД),
§ гипертонической болезни (акцент II тона над аортой, резкий подъем АД),
− отмечается тахикардия, при мерцательной аритмии дефицит пульса,
Оказание неотложной помощи при сердечной астме.
Цель:Уменьшение застоя и снижение давления в легочных сосудах, ликвидация гипоксии, понижение проницаемости легочных капилляров, нормализация артериального давления.
Ресурсы:тонометр, фонендоскоп, кислородный баллон, маска, марлевая салфетка, жгуты, стерильные:одноразовые шприцы,системы для в/в капельного введения лекарственных препаратов, ватные шарики, спирт этиловый 70%, резиновый жгут, перчатки, пинцет в дезрастворе, клеенчатый валик, лоток.
Лекарственные препараты:
· Натрия хлорида 0,9 % раствор 200 мл
Алгоритм действий.
1. Придать больному сидячее положение с опущенными ногами
2. Наложить жгуты на конечности.
3. Подать увлажненный кислород.
5. Дать таблетку нитроглицерина под язык
6. Ввести в/в 5000 ЕД гепарина на 10 мл 0,9 % раствора физиологического раствора
7. Ввести в/в или в/м 1 мл 1% раствора морфина.
8. При гипертоническом кризе ввести в/в 1 мл 0,01% р-р клофелина с
9. При бронхоспазме ввести в/в эуфиллин 2,4 % -10 мл струйно медленно.
Примечание:сердечные гликозиды при инфаркте миокарда противопоказаны,так как они,усиливая сократительную способность миокарда,увеличивают зону некроза.
ОСТРАЯ ЛЕВОЖЕЛУДОЧКОВАЯ НЕДОСТАТОЧНОСТЬ
ОТЕК ЛЕГКИХ
Острая левожелудочковая недостаточность и ее основные проявления — сердечная астма и отек легких — представляют собой патологическое состояние, обусловленное обильным пропотеванием жидкой части крови в интерстициальную ткань легких, а затем в альвеолы, что клинически проявляется тяжелым удушьем, цианозом и клокочущим дыханием. Отек легких (ОЛ): возникает более или менее внезапно, либо в результате нарастания тяжести ОА. Появление при ОЛ обильных мелко – и среднепузырчатых хрипов, распространяющихся на переднее-верхние отделы легких, указывает на развивающийся («2степень») ОЛ.
Появление пенистой, обычно розовой мокроты (примесь эритроцитов) является достоверным признаком ОЛ. Хрипы отчетливо слышны на расстоянии. Прочие объективные и субъективные признаки как при тяжелой СА.
Для 1 стадии ОЛ характерны тяжелое ортопноэ, холодный пот. Различают молниеносное (смерть в течение нескольких минут), острое (продолжительность приступа от О,6 до 2 — 3 ч) и затяжное (до суток и более) течение. Пенистую мокроту при ОЛ следует отличать от пенистой, окрашенной кровью, слюны, выделяемой при эпилептическом приступе и при истерии. «Клокочущее» дыхание у крайне тяжело (агонизирующих) больных не является специфическим признаком ОЛ.
Классификация:
По варианту течения различают следующие виды отека легких:
§ молниеносный– развивается бурно, в течение нескольких минут; всегда заканчиваясь летальным исходом
§ острый– нарастает быстро, до 4-х часов; даже при немедленно начатых реанимационных мероприятиях не всегда удается избежать летального исхода. Острый отек легких обычно развивается при инфаркте миокарда, ЧМТ, анафилаксии и т. д.
§ подострый– имеет волнообразное течение; симптомы развиваются постепенно, то нарастая, то стихая. Такой вариант течения отека легких наблюдается при эндогенной интоксикации различного генеза (уремии, печеночной недостаточности и др.)
§ затяжной– развивается в период от 12 часов до нескольких суток; может протекать стерто, без характерных клинических признаков. Затяжной отек легких встречается при хронических заболеваниях легких, хронической сердечной недостаточности
Появляется удушье, дыхание клокочущее, беспокоит кашель с отделением розовой пенистой мокроты. При перкуссии легких определяется притупление перкуторного звука в нижних отделах. Здесь же выслушиваются крепитация, мелкопузырчатые хрипы.
При прогрессировании альвеолярного отека хрипы выслушиваются более чем над 50% поверхности легких.
источник
Опросите больного бронхиальной астмой и выявите жалобы:
экспираторная одышка, характеризующаяся резко затрудненным выдохом, при этом вдох делается коротким, а выдох удлиненным; приступы удушья, возникающие в любое время суток, особенно ночью или ранним утром, в морозную погоду, на сильном ветру, в период цветения некоторых растений и протекающие от нескольких часов до 2-х и более дней (астматическое состояние), приступообразный кашель с отхождением скудного количества вязкой, стекловидной мокроты, возникающий после физической нагрузки, при вдыхании аллергенов, усиливающийся ночью или при пробуждении; появление эпизодов хрипов или чувство сдавления в грудной клетке при вышеназванных условиях.
Соберите анамнез у больного инфекционно-аллергической формой бронхиальной астмы:указания на перенесенные заболевания верхних дыхательных путей (риниты, гаймориты, ларингиты и т. д.), бронхиты и пневмонии; возникновение первых приступов удушья после них; простуда, которая «опускается в грудь» или продолжается более 10 дней. В последующие годы частота появления приступов удушья, их связь с холодной, сырой погодой, перенесенными острыми респираторными заболеваниями (грипп, бронхиты, пневмонии). Длительность приступного и меж-приступного периодов заболевания. Эффективность лечения и его результаты в амбулаторных, стационарных условиях. Использование медикаментозных средств, кортикостероидных препаратов. Наличие осложнений -формирование пневмосклероза, эмфиземы легких, присоединение дыхательной и легочно-сердечной недостаточности.
Соберите анамнез у больного атонической формой бронхиальной астмы:обострения болезни имеют сезонный характер, сопровождаются ринитом, конъюнктивитом; у больных бывает крапивница, отек Квинке, выявляется непереносимость некоторых пищевых продуктов (яйца, шоколад, апельсины и др.), лекарственных средств, пахучих веществ, отмечается наследственная предрасположенность к аллергическим заболеваниям.
Проведите общий осмотр больного.Оцените состояние больного (которое может быть тяжелым), положение в постели: во время приступа бронхиальной астмы больной занимает вынужденное положение, обычно сидя в постели, руками опираясь о колени или спинку стула. Больной громко дышит, часто, со свистом и шумом, рот открыт, ноздри раздуваются. При выдохе появляется набухание шейных вен, которое уменьшается при вдохе. Отмечается разлитой диффузный цианоз.
Выявите симптомы бронхиальной астмы у больного при исследовании органов дыхания:при осмотре грудная клетка эмфизематозной формы, во время приступа расширяется и занимает инспираторное положение (в положении максимального вдоха). В дыхании активно участвует вспомогательная мускулатура, мышцы плечевого пояса, спины, брюшной стенки. При пальпации — определяется ригидная грудная клетка, ослабление голосового дрожания во всех отделах из-за повышенной воздушности легочной ткани. При сравнительной перкуссии отмечается появление коробочного звука над всей поверхностью легких, при топографической перкуссии: смещение границ вверх и вниз, увеличение ширины полей Кренига, ограничение подвижности нижнего легочного края. При аускультации легких на фоне ослабленного дыхания выслушивается большое количество сухих свистящих хрипов, нередко слышимых даже на расстоянии. Бронхофония ослаблена над всей поверхностью легких.
Выявите симптомы бронхиальной астмы при исследовании сердечно-сосудистой системы:при осмотре верхушечный толчок не определяется, отмечается набухание шейных вен. При пальпации верхушечный толчок ослаблен, ограничен или не определяется. Границы относительной тупости сердца при перкуссии определяются с трудом, а абсолютной — не определяются из-за острого вздутия легких. При аускультации тоны сердца ослаблены (из-за наличия эмфиземы легких), акцент IIтона над легочной артерией, тахикардия.
При лабораторном исследованииу больного бронхиальной астмой в периферической крови характерно появление эозинофилии и умеренного лимфоцитоза. При исследовании мокроты — слизистая стекловидная, вязкая, при микроскопическом исследовании находят много эозинофилов, часто — спирали Куршмана и кристаллы Шарко-Лейдена.
Выявите симптомы бронхиальной астмы у больного при рентгенологическом исследовании грудной клетки:отмечается повышение прозрачности легочных полей и ограничение подвижности диафрагмы.
Оцените функцию внешнего дыхания:для бронхиальной астмы характерно, в первую очередь, снижение показателей бронхиальной проходимости (ОФВIтеста Тиффно). Бронхиальная обструкция носит обратимый характер. Наблюдается увеличение ОО и ОЕЛ.
Отдифференцируйте приступ бронхиальной астмы от приступа сердечной астмы(см. табл. 6) и бронхиальную астму от хронического обструктивного бронхита(см. табл. 7).
Не нашли то, что искали? Воспользуйтесь поиском:
источник
Симптомы таких болезней как сердечная и бронхиальная астма критически похожи и определиться с диагнозом трудно даже опытному врачу. Однако отличить приступ этих недугов – важнейшая задача, потому что эти разные болезни нуждаются в применении различных препаратов. Особенно это касается неотложной помощи.
Для ликвидации приступов БА категорически запрещено использовать наркотические анальгетики. Равносильным этому является использование адренергических медикаментов при приступе сердечной астмы (далее СА). Эти средства купируют приступ бронхиальной астмы, но не приносят абсолютно никакого результата при приступе сердечной. Чем быстрее врач определит отличие этих недугов и поставит правильный диагноз, тем успешнее будет лечение.
Краткое содержание статьи
Это болезнь не относится к самостоятельным, а лишь является последствием нарушений в работе сердца и сердечно-сосудистой системы в целом.
Среди причин можно выделить 8 основных заболеваний:
- Желудочковая тахикардия.
- Обширный инфаркт и прединфарктное состояние.
- Отрыв аневризмы.
- Ишемия и прочие нарушения кровотока миокарда.
- Гипертония с наличием кризов.
- Миокардит.
- Кардиомиопатия.
- Эндокардит.
Кроме дисфункций сердечно-сосудистой системы и сердца, в медицинской практике есть пациенты, у которых СА возникала в таких случаях:
- болезни почек;
- нерегулярные нагрузки на организм;
- инфицирование тяжелыми недугами (к примеру – пневмония);
- употребление наркотических и психотропных веществ;
- бронхиальная астма на запущенном этапе;
- нарушение психологического и эмоционального баланса;
- прединсультное состояние.
ВАЖНО! Если человек страдает ожирением и постоянными запорами, то он однозначно попадает в зону риска этого заболевания. Кроме того, беременные или родившие ребенка женщины в возрасте после 45 лет тоже могут приобрести СА.
Определить первопричину возникновения приступов сердечной астмы может исключительно специалист. Ведь возникать и проявляться этот недуг может абсолютно по-разному.
Если у больного выявлены нарушения в работе сердечно-сосудистой системы или обнаружены прочие серьезные заболевания, то особое внимание стоит уделить приступам сухого кашля. Ведь они присущи не только бронхиальной астме. Кроме того, нужно уделить внимание биохимическим процессам организма: их нарушения тоже сигнализируют о сердечной астме.
Приступ СА сопровождается тахикардией, слабым наполнением пульса и повышенным или пониженным давлением (см. базовый недуг). Причины сердечной недостаточности можно просмотреть при исследовании электрокардиограммы. Отличить сердечную астму от бронхиальной не составит труда в том случае, когда она проявляется типичными сигналами. Если приступы сопровождаются бронхоспазмом, то это затрудняет и запутывает отличие. Во избежание этого следует рассказать врачу о хронических недугах, аллергиях и патологиях легких.
Чтобы не допустить серьезных осложнений, нужно знать базовую симптоматику недуга, особенно если известно о сердечной недостаточности:
- Усиленное биение сердца с ощущением сдавливания в области груди.
- Нехватка кислорода и удушье.
- Одышка, психологическая неадекватность и учащенные вдохи ртом – все это присуще страху смерти.
- Облегчение состояния при принятии положения стоя или сидя.
- Обострение известных сердечных болезней.
Самыми распространенными причинами возникновения этого недуга являются инфекции дыхательных путей и вдыхание или употребление аллергенов. Среди аллергенов лидирующее место занимают:
- пыль бытовая;
- клещи пылевые;
- растительная пыльца;
- шерсть домашних питомцев;
- бытовая химия;
- пищевые продукты (шоколад, орехи и др.).
Наличие аллергенов или инфекций отягощают течение бронхиальной астмы, делают выход затрудненным, свистящим и хрипящим. В этом состоит одно из отличий бронхиального недуга от сердечного, ведь при приступе сердечной астмы пациент может свободно вдохнуть.
ВАЖНО! Это заболевание характерно для более молодого возраста, что обусловлено перенесением бронхитов, пневмоний и прочих серьезных болезней в детстве.
| Признаки | Бронхиальная астма | Сердечная астма |
|---|---|---|
| Анамнез | Хронические неспецифические заболевания легких, повторные пневмонии, аллергия | Болезни сердечно-сосудистой системы, приводящие к левожелудочковой сердечной недостаточности |
| Характер одышки | Экспираторная (затруднен выдох) | Смешанная |
| Вынужденное положение | Сидя или стоя с фиксированным плечевым поясом | Ортопноэ (вынужден сидеть) |
| Цианоз | Диффузный | Периферический |
| Тип грудной клетки | Эмфизематозная | Не изменена |
| Перкуссия легких (простукивание) | Коробочный звук | Притупление звука в нижних отделах легких |
| Аускультация легких (выслушивание) | Ослабленное везикулярное дыхание. Сухие свистящие хрипы | Ослабленное везикулярное дыхание. Влажные мелкопузырчатые не звонкие хрипы |
| Перкуссия сердца | Абсолютная тупость сердца отсутствует или уменьшена. Границы относительной сердечной тупости достоверно определить не удается | Абсолютная тупость сердца не изменена или увеличена. Левая граница относительной сердечной тупости смещена кнаружи |
| Аускультация сердца | Тоны сердца ослаблены, ритмичны | Тоны сердца ослаблены, тахикардия, часто ритм галопа аритмии |
| Мокрота | Слизистая, скудная, вязкая, стекловидная, содержит эозинофилы, спирали Куршмана, кристаллы Шарко-Лейдена, выделяется в конце приступа | Серозная, розовая, пенистая, жидкая (при альвеолярном отеке легкого), может содержать сидерофаги (“клетки сердечных пороков”) |
| ЭКГ | Отклонение электрической оси сердца вправо нагрузка на правое предсердие | Отклонение электрической оси влево, гипертрофия левого желудочка, признаки ишемии миокарда, аритмии |
♦ Приступы бронхиальной и сердечной астмы сопровождаются попаданием плазмы крови в легкие. Однако происхождение мокроты абсолютно разное: при приступе бронхиальной астмы мокрота попадает в легкие из-за сверхусилий работы правого желудочка сердца, а при сердечной – из-за недостаточного функционирования левого желудочка сердца.
Эти факты осложняют симптоматику заболеваний, однако болезни все равно нужно как можно раньше отличить друг от друга. Главные факторы для отличия недугов можно найти в анамнезе. Основное отличие заболеваний состоит в их первопричинах и возрастном цензе. Для бронхиальной – это бронхиты и воспаления легких в детском возрасте, а для сердечной – недуги сердечно-сосудистой системы в более зрелом возрасте.
♦ Второе отличие – это разный характер дыхания. В отличии от бронхиальной, где трудно выдохнуть, при СА наоборот трудно вдохнуть.
♦ Третье отличие заключается в различной локации хрипов при прослушивании. Влажные хрипы в нижних отделах легких присущи сердечному заболеванию, в то время как для приступов второго характерны сухие хрипы на выходе.
Только правильное отслеживание симптоматики и диагностирование болезни позволит избежать осложнений в течении недуга, а следовательно жизнь и здоровье больного будут в безопасности.
Честно говоря я не знала, что астма бывает бронхиальной и сердечной. Прочитав статью я так поняла, что их легко перепутать, а неуместное лечение может привести к летальному последствию. Тут говорится, что сердечная астма может проявляться при запущенном виде бронхиальной астмы. Задается вопрос, а как назначают терапию в данном обстоятельстве? Что нужно излечить первостепенно? Еще меня интересует одно, какое из этих заболеваний может передаватья генетически или формироваться еще в зародыше?
источник
Хронические неспецифические заболевания легких, повторные пневмонии, аллергия
Заболевания сердечно-сосудистой системы, приводящие к левожелудочковой сердечной недостаточности
Сидя или стоя с фиксированным плечевым поясом
Притупление в нижних отделах легких
Ослабленное везикулярное дыхание
Ослабленное везикулярное дыхание
Влажные мелкопузырчатые не звонкие хрипы
Абсолютная тупость сердца отсутствует или уменьшена
Границы относительной сердечной тупости достоверно определить не удается
Абсолютная тупость сердца не изменена или увеличена
Левая граница относительной сердечной тупости смещена кнаружи
Тоны сердца ослаблены, ритмичны
Тоны сердца ослаблены, тахикардия, часто ритм галопа аритмии
Слизистая, скудная, вязкая, стекловидная, содержит эозинофилы, спирали Куршмана, кристаллы Шарко-Лейдена, выделяется в конце приступа
Серозная, розовая, пенистая, жидкая (при альвеолярном отеке легкого), может содержать сидерофаги (“клетки сердечных пороков”)
Отклонение электрической оси сердца вправо нагрузка на правое предсердие
Отклонение электрической оси влево, гипертрофия левого желудочка, признаки ишемии миокарда, аритмии
Однако следует помнить, что при затянувшемся приступе сердечной астмы, вследствие присоединения застойного бронхита, она может приобретать некоторые черты бронхиальной астмы (экспираторный характер одышки, сухие свистящие хрипы).
Хронический обструктивный бронхит
Постоянный, разной интенсивности
Приступы экспираторной одышки
Постоянная без резких колебаний выраженности
Обратимость бронхиальной обструкции
Эозинофилия мокроты и крови
Опросите больного с эмфиземой легких и выявите жалобы: одышка, которая постепенно упорно прогрессирует и носит обычно экспираторный характер.
Соберите анамнез:часто встречающаяся так называемая вторичная эмфизема легких развивается на фоне хронического обструктивного бронхита, бронхиальной астмы. В этих случаях эмфизема диффузная. В происхождении довольно редкой первичной эмфиземы легких ведущее значение отводится генетическим факторам и, в частности, дефициту1-анти-трипсина, который при определенных условиях может привести к избыточному действию ферментов, в том числе эластазы (основным источником которой являются нейтрофилы). Это ведет к разрушению межальвеолярных перегородок и слиянию отдельных альвеол в более крупные эмфизематозные полости. Следует выяснить экзогенные факторы, способствующие развитию эмфиземы легких: курение, поллютанты окружающей среды, профессиональной вредности, повторяющиеся респираторные инфекционные заболевания. Среди поллютантов наибольшая доля отводится диоксидам серы и азота, а также озону и черному дыму. В анамнезе следует отразить год возникновения одышки, периоды ухудшения состояния, присоединения легочной и легочно-сердечной недостаточности, лечение и его результаты, причину настоящей госпитализации.
Выявите симптомы эмфиземы легких при общем осмотре: для больных эмфиземой легких характерноснижение массы тела, что связано с напряженной работой респираторных мышц, которая направлена на преодоление высокого сопротивления терминального отдела дыхательных путей.
Больные эмфиземой легких в начальных стадиях заболевания принимают вынужденное положениена животе с опущенными вниз головой и плечевым поясом, что приносит им облегчение, т.к. в таком положении достигается повышение внутрибрюшного давления, поднятие вверх диафрагмы и улучшение ее функции. Однако при выраженной эмфиземе легких и утомлении дыхательных мышц горизонтальное положение вызывает чрезмерно напряженную работу диафрагмы, поэтому они вынуждены спать в сидячем положении.
Температура телау больных эмфиземой легких нормальная или субнормальная (колебание в пределах 35,0 0 С-36,5 0 С), что объясняется замедлением периферического кровотока в венозной системе. Она редко повышается более, чем на 1 0 С у больных диффузной медленно прогрессирующей эмфиземой легких, даже при присоединении инфекции.
Цвет кожных покрововпри эмфиземе легких скорее розовый, чем синюшный. Мало выраженный цианоз обусловлен длительным сохранением газового состава крови, только в далеко зашедших случаях появляется цианоз, который обусловлен развитием гиперкании. При этом у больных можно выявить «вересковый язык» (голубой оттенок языка), который является клиническим показателем гиперкании при эмфиземе легких.
Проведите исследование органов дыхания:
Осмотр грудной клетки:для эмфиземы легких характернабочкообразная грудная клетка, объем которой увеличен как за счет увеличения межреберного промежутка, так и в связи с увеличением переднезаднего размера (расстояния между позвоночником и грудиной). Такая грудная клетка как бы постоянно находится в фазе глубокого вдоха. Ребра приближаются к горизонтальному положению, подвижность их ограничена, межреберные промежутки расширены и даже выбухают. Эпигастральный угол увеличивается и становится тупым, надключичные области расширяются, сглаживаются, иногда имеют подушкообразное выбухание. Плечевой пояс приподнимается, создавая впечатление укороченной шеи, наблюдается дискоординация дыхательных движений, появление признаков парадоксального дыхания (ребра на вдохе могут парадоксально втягиваться, что связано с тягой низко стоящей уплощенной диафрагмы).
Иногда наблюдается кифоз. Во время выдоха повышается внутригрудное давление, вследствие чегонабухают шейные вены, иногда выявляются расширенные вены в нижней части грудной клетки. В случае присоединения правожелудочковой сердечной недостаточности набухание вен не исчезает и на вдохе.
Одышка при эмфиземе легких имеет экспираторный характер, при этом одышка напоминаетпыхтение. Больные при небольшой физической нагрузке и даже в покое осуществляют выдох при сомкнутых губах, надувая щеки («пыхтят»). При этом повышается давление в бронхиальном дереве, что уменьшает экспираторный коллапс мелких бесхрящевых бронхов (обусловленный нарушением эластических свойств легочной ткани и возрастанием внутригрудного давления) и способствует увеличению объема вентиляции.
Пальпация грудной клетки. Она становится ригидной. Голосовое дрожание не изменено или ослаблено, что объясняется повышением воздушности легочной ткани, из-за чего она хуже проводит звуковые колебания на поверхность грудной клетки.
Перкуссия. При сравнительной перкуссии выявляется коробочный звук. При топографической перкуссии отмечается увеличение высоты стояния верхушек и расширение полей Кренига. Нижние границы легких опущены. Наблюдается резкое ограничение подвижности нижнего легочного края. Характерно уменьшение сердечной и печеночной тупости. Все изменения обусловлены повышением воздушности и увеличением объема легочной ткани при эмфиземе легких.
Аускультация. При эмфиземе легких выслушивается ослабленное везикулярное дыхание, в тяжелых случаях — резко ослабленное. Появление хрипов не характерно для эмфиземы легких. Лишь при проведении кашлевой пробы или на высоте форсированного выдоха может появляться скудное количество сухих свистящих хрипов.
Бронхофонияне изменена или ослаблена.
Выявите симптомы эмфиземы легких у больного при исследовании сердечно-сосудистой системы. При осмотре верхушечный и сердечный толчок не определяются. При пальпации — верхушечный толчок ослаблен, ограничен или не пальпируется. При перкуссии границы относительной тупости сердца определяются с трудом, а абсолютной — не определяются. При аускультации сердца — ослабление тонов, акцент II тона над легочной артерией, брадикардия, которая обусловлена ваготонией, выявляемой при эмфиземе легких уже в начальные периоды болезни, и только при присоединении правожелудочковой сердечной недостаточности возникает тахикардия.
Проведите исследование печени.Размеры абсолютной тупости печени при эмфиземе легких уменьшены в связи с повышением воздушности легких и увеличением их объема. Из-за низкого стояния диафрагмы печень может быть опущена и пальпируется на несколько сантиметров ниже реберной дуги, хотя размеры ее не изменены. Только при развитии правожелудочковой сердечной недостаточности наблюдается истинное увеличение печени, край ее при пальпации закруглен, болезненный, при надавливании на нее увеличивается набухание шейных вен (симптом Плеша).
Выявите симптомы эмфиземы легких у больного при рентгенологическом исследовании грудной клетки: отмечается повышение прозрачности легочных полей, низкое стояние купола диафрагмы, ограничение подвижности диафрагмы, расширение межреберных промежутков, ослабление легочного рисунка на периферии. Сердце, как правило, не увеличивается, а вследствие низкого стояния диафрагмы оно принимает каплевидную форму («капельное сердце»).
Оцените функцию внешнего дыхания: при эмфиземе легких наблюдается стойкое снижение скоростных показателей (ОФВ1, тест Тиффно), обструкция носит стойкий необратимый характер, отмечается увеличение общей емкости легких и остаточного объема, снижение ЖЕЛ и МВЛ, диффузионной способности легких.
источник

Проявления сердечной астмы – приступы удушья, чаще возникающие в ночное время во сне. Стоит обратить внимание на качество своего сна. Вы ощущаете нехватку воздуха во сне, а также вдруг возникающий страх смерти. Эти ощущения заставляют вас часто и глубоко дышать, возможно будет сопутствовать приступообразный сухой кашель.
Вам ничего не остается, как сесть в постели (принять вертикальное положение) и спустить ноги на пол, чтобы попытаться успокоиться. Возможно вам придется подойти к окну, чтобы ушло ощущение нехватки воздуха. Все эти действия предупреждают о возникновении проблем с сердцем. Если вы вдруг начинаете сталкиваться с этим, то следует обязательно проконсультироваться с врачом.
Астма представляет собой приступы удушья, при которых нормальное физиологическое дыхание становится тяжелым или невозможным. Это приводит к нарушению насыщения крови кислородом, транспорта и снабжение O2 тканями.
Существуют различные причины возникновения астмы. Но все они приводят к нарушению дыхания и кислородному голоданию.
Бронхиальная астма характеризуется быстрым развитием бронхоспазма. Это развивается вследствие действия на слизистую оболочку верхних и средних дыхательных путей различных аллергенов или раздражающих веществ.
При этом происходит быстрое сужение бронхов большого и малого калибра, сопровождающееся существенным отеком слизистого слоя, дыхательный акт резко нарушается, потребление воздуха и соответственно кислорода становится недостаточным. Является хронической патологией, но характеризуется острыми приступами удушья.
Сердечная астма – это патофизиологическое состояние, сопровождающееся регулярными приступами одышки и удушья различной интенсивности вследствие развития застойных процессов в малом круге кровообращения.
В результате воздействия патологического внешнего или внутреннего фактора, на фоне нарушения работы сердца, происходит резкое нарушение работы левых отделов сердца (предсердия и желудочка), но функциональная способность правых отделов при этом сохраняется.
В результате этого диссонанса (несоответствия) увеличивается давление в левом предсердии, и соответственно повышается гидростатическое и гидродинамическое давление в сосудах малого круга. При этом значительно увеличивается давление в микроциркуляторном русле легочной ткани (в капиллярах, артериях, венах, артериолах и венулах).
С дальнейшим постепенным повышением давления в левом предсердии активизируется компенсаторный механизм – рефлекс Китаева. Он характеризуется спазмом сосудов системы легочной артерии, как ответная реакция на интенсивное повышение давления в левых отделах сердца.
Пропотевающая субстанция содержит в своем составе плазму, большое количество белка и эритроцитов . Потоки воздуха в полости альвеол перемешиваются с транссудатом. Это проявляется пенистой мокротой нередко розового цвета (из-за обилия эритроцитов в жидкости).
Прогрессирование этого процесса приводит к гипоксемии (недостаток O2 в крови), гипоксии (кислородное голодание тканей организма), повышенным содержанием углекислого газа во взвеси крови (гиперкапния).
Основной причиной развития сердечной астмы является сердечная недостаточность, в частности левых отделов сердца.
Это заболевание происходит вследствие действия многих предрасполагающих факторов и перенесенных патологий органов сердечно-сосудистой системы:
- Диффузный кардиосклероз;
- Перенесенный инфаркт миокарда:
- ИБС ;
- Острые воспалительные процессы сердечной мышцы (миокардит);
- Патологическое расширение полостей сердца ( аневризма левого предсердия, желудочка);
- Приобретенные пороки сердечных клапанов (стеноз митрального, аортального клапана);
- Опухоли сердца;
- Наличие крупных тромбов в полостях сердца;
Также провоцирующими факторами являются:
- Стойкое и интенсивное повышение цифр артериального давления (гипертоническая болезнь). Повышенное кровяное давление только способствует пропотеванию (просачиванию) плазмы и форменных элементов в альвеолы;
- Гломерулонефрит и др. воспалительные заболевания почек. Эти патологии приводят к задержке воды в организме и увеличению объема циркулирующей крови. Это также негативно сказывается на сердечной деятельности и может привести к сердечной астме;
- Васкулиты, при которых наблюдается истончение и повреждение сосудистой стенки. Это ускоряет процессы транссудации при развитии сердечной астмы.
Симптоматика сердечной астмы схожа с проявлениями бронхиальной. Наиболее характерным симптомом является нарастающая одышка, 
- Физическая нагрузка;
- Нервное перенапряжение.
- В отличие от бронхиальной астмы ее возникновение не сопряжено с контактом аллергенов или других патогенных агентов.
Наиболее характерными проявлениями сердечной астмы являются:
- Постепенно развивается кашель. По началу, он является сухим, но с прогрессированием состояния появляется пенистая мокрота белого или розового цвета (в зависимости от наличия и концентрации эритроцитов в ней). Кашель становиться влажным с крупно- или мелкокалиберными хрипами. Если в начале развития сердечной астмы кашлевые акты единичные, то с нарастанием симптоматики они становятся более продолжительными, мучительными, возникают спонтанно приступами удушья;
- Бледность кожных покровов и акроцианоз. В результате недостаточного снабжения кислорода тканями кожные покровы и слизистые оболочки сначала становятся бледными, а затем приобретают синий оттенок (в частности в области носогубного треугольника).
- Изменение общего состояния. Появляется возбужденность, чувство страха смерти. Это является показателем нарушения кровоснабжения сердца и головного мозга;
- Соматические проявления: слабость, утомленность, появление холодного пота;
- Нередко наблюдается набухание шейных вен вследствие острой сердечной недостаточности.
Также перечисленные симптомы могут сопровождаться загрудинной болью тупого характера.

Во время опроса необходимо обратить внимание на имеющиеся хронические заболевания респираторной и сердечно-сосудистой систем. На то, с чем связываете возникновение приступа, какие были проявления до этого.
После этого специалист аускультативным методом (прослушивание при помощи фонендоскопа) оценит состояние легких, дыхательных трактов, сердца.
Со стороны респираторной системы будут прослушиваться хрипы во время кашля, дыхания. Это может сопровождаться отделением мокроты, в частности пенистого характера розового цвета ли с примесью крови.
При аускультации сердца могут быть приглушены его тоны (звуки, характеризующие качество деятельности миокарда), возможно появление шумов, патологических тонов (при врожденных патологиях клапанов).
Сердечная астма будет сопровождаться:
- значительной тахикардией (110-150 уд. в мин.),
- тахипное (22-30 вдохов в минуту),
- инспираторной одышкой (тяжелый вдох).
Также может потребоваться проведение рентгенографии органов грудной клетки, эхокардиографии с эффектом Доплера. Эти диагностические методы более наглядно покажут общее состояние сердца, объем сердечного выброса, что позволит более точно определить причину развития сердечной астмы.
источник
Несмотря на многие сходные проявления, сердечная астма и бронхиальная астма имеют отличительные признаки, позволяющие дифференцировать их друг от друга. Это важно для проведения правильной диагностики и назначения лечения, так как эти состояния в корне отличаются происхождением и требуют разных методов воздействия.
Оба вида проявляются приступами удушья, но вызываются они совершенно разными причинами. Сердечную форму нельзя считать самостоятельным заболеванием, так как она является следствием наличия у больного нескольких проблем с сердечно-сосудистой системой, приводящих к развитию сердечной недостаточности.
Бронхиальная астма – это отдельное заболевание, чаще всего аллергической природы, поражающее легкие и бронхи, но никак не связанное с сердечной деятельностью. В этом состоит основное отличие бронхиальной астмы от сердечной астмы. Для назначения лечения важно различать эти два состояния, так как воздействовать на них нужно различными методами и препаратами.
Грамотная диф. диагностика бронхиальной астмы и сердечной астмы помогает распознать картину заболевания и начать его лечение на самых ранних стадиях, задолго до развития осложнений.
Приступ сильного удушья, который возникает при различных кардиологических проблемах, принято называть сердечной астмой. Это состояние нужно вовремя распознавать, так как оно может сопровождать такое опасное для жизни больного заболевание, как инфаркт миокарда. Также приступ может развиться при разных типах пороков сердца, кардиосклерозе и других заболеваниях, сопровождающихся сердечной недостаточностью.
Сердечная форма астмы возникает как проявление недостаточности левого желудочка, вызванной застоем крови в малом круге кровообращения и отеком легких. Приступ развивается внезапно, начинаясь с одышки и переходя в сильный, надсадный кашель сухого типа, ощущением недостатка воздуха, страхом смерти и другими симптомами.
Больному нужна срочная помощь, добиться купирования приступа можно приемом нитроглицерина и других нитратов, а также иных препаратов по назначению врача. Так как причиной такого состояния может быть инфаркт, больному нужно вызвать скорую помощь и госпитализировать его.
Особенность бронхиальной астмы состоит в том, что это заболевание имеет воспалительную природу, поражает дыхательные пути и клеточные элементы. В основном эта болезнь имеет аллергическое или иммунологическое происхождение, сопровождается сильнейшими приступами удушья с характерными признаками.

При обследовании при подозрении на наличие такой астмы проводится бронхоальвеолярный лаваж. Это диагностический смыв нейтральным раствором легких и бронхов, исследование которого позволяет установить точную причину заболевания.
Отличие сердечной астмы от бронхиальной заключается в различной природе заболеваний и проявляется разными признаками:
-
Сердечная астма является следствием сердечной недостаточности, возникает при ишемической болезни, пороках, инфаркте миокарда, артериальной гипертензии. Развивается в основном в среднем и пожилом возрасте, сопровождается акроцианозом, то есть посинением максимально удаленных от сердца участков тела, отеками, при этом у больного холодные руки и ноги. При приступе больной предпочитает находиться в сидячем положении, ему не хватает воздуха, он издает влажные хрипы, словно внутри лопаются пузыри, у него выделяется обильная пенистая мокрота, которая указывает на ухудшение состояния. Если вовремя не принять меры, у пациента может развиться отек легких. Купировать приступ помогают нитраты, например, Нитроглицерин.
- Бронхиальная астма обычно начинается в раннем возрасте, может быть наследственным заболеванием, вызываться экологическими и профессиональными факторами. Она проявляется спазмом бронхов, при котором человек не может выдохнуть воздух. Состояние сопровождается свистящими хрипами, разлитым цианозом из-за нехватки кислорода, наличием малого количества прозрачной, стекловидной мокроты. Ее появление свидетельствует о завершении приступа. При нем больной старается находиться сидя или опираться на руки, его конечности остаются теплыми. Прием Нитроглицерина не улучшает состояния больного.Характерными отличиями при разных типах астмы является отхождение мокроты и тип удушья. При сердечной астме появление мокроты означает ухудшение состояния, а при бронхиальной – наоборот, завершение приступа с облегчением состояния больного. При сердечной форме больной никак не может вдохнуть воздух, а при бронхиальной – его выдохнуть.
Различия между заболеваниями очень важны, так как для лечения используются совершенно разные препараты и способы.
Дифференциальная диагностика сердечной и бронхиальной астмы предусматривает использование различных методов обследования. При подозрении на бронхиальное происхождение приступов применяются следующие способы обследования:
-
Спирометрия. Она позволяет оценить уровень обструкции и ее обратимости. При методике исследуется объем усиленного выдоха за секунду и форсированная жизненная емкость легких.
- Пикфлоуметрия помогает вычислить пиковую скорость выдоха, которая является на только способом диагностики, но и методом определения правильности назначенного лечения.
Кроме этих способов, больного опрашивают, узнают, имелись ли случаи заболевания в роду, осматривают, прослушивая легкие, отдают на анализ мокроту, сдают кровь, а также проводят различные аллергологические пробы.
Для выявления сердечной формы и ее дифференциации от других заболеваний со сходными признаками (астматического бронхита, стеноза гортани, уремической одышки, медиастинального синдрома, истерического припадка) применяются следующие методики:
- осмотр пациента;
- сбор анамнеза;
- ЭКГ;
- рентгенография области грудной клетки.
При сердечной астме присутствуют шумы при дыхании, но они все равно отличаются от звуков при бронхиальных проявлениях, позволяют уловить глухие тона сердца и разграничить проявления разных состояний.
После получения полноценных данных и выявления картины заболевания врач может поставить точный диагноз и начать правильное, целевое лечение. Так как сердечные приступы несут непосредственную опасность жизни пациента и могут быть проявлением инфаркта миокарда, при котором уровень выживаемости больных зависит от скорости госпитализации, человеку нужно обязательно вызывать «скорую помощь» для предотвращения ухудшения состояния.
Бронхиальная астма имеет хроническое течение и требует постоянного применения выписанных врачом препаратов, прохождения специализированного лечения для снижения частоты и тяжести приступов.
источник
В последние годы внимание исследователей всё больше привлекает проблема мульти- и коморбидности. Вероятность развития сочетанных заболеваний при увеличении продолжительности жизни повышается, что можно объяснить, как возрастными изменениями, так и отрицательными воздействиями окружающей среды и условий жизни в течение длительного времени.
Увеличение количества болезней с возрастом отражает, прежде всего, инволюционные процессы, а понятие коморбидности подразумевает детерминированную возможность их сочетанного течения, причём последнее изучено значительно меньше.
Имеется ряд общеизвестных сочетаний, таких как ишемическая болезнь сердца (ИБС) и сахарный диабет, артериальная гипертензия (АГ) и ИБС, АГ и ожирение. Но при этом всё чаще появляются указания на более редкие комбинации, например, язвенной болезни и ИБС, митрального стеноза и ревматоидного артрита, язвенной болезни и бронхиальной астмы (БА).
Изучение вариантов сочетанной патологии может способствовать более глубокому пониманию патогенеза болезней и разработке патогенетически обоснованной терапии. Это особенно важно по отношению к широко распространенным и социально значимым заболеваниям, к которым относятся в первую очередь заболевания сердечно-сосудистой системы (АГ, ИБС) и бронхолегочной системы (БА).
На возможность сочетания БА и АГ впервые в отечественной литературе указали Б.Г. Кушелевский и Т.Г. Ранева в 1961 г. Они рассматривали такое сочетание, как пример «конкурирующих заболеваний». Дальнейшие исследования показали, что распространенность артериальной гипертензии у пациентов с бронхообструкцией в среднем составляет 34,3 %.
Столь частое сочетание БА с АГ позволило Н.М. Мухарлямову выдвинуть гипотезу о симптоматической «пульмоногенной» гипертензии, признаками которой служат:
- повышение артериального давления (АД) у больных хроническими неспецифическими заболеваниями легких на фоне обострения болезни, в том числе у больных БА при приступах удушья;
- снижение АД по мере улучшения показателей функции внешнего дыхания на фоне применения противовоспалительных и бронхолитических (но не гипотензивных) препаратов;
- развитие АГ через несколько лет после начала заболевания легких, первоначально лабильной, с повышением АД только во время усиления обструкции, а затем — стабильной.
Ситуации, когда АГ предшествовала появлению БА и не имела связи с ухудшением бронхиальной проходимости, следовало расценивать как ГБ.
Изучая «пульмоногенную» АГ у больных бронхиальной астмой, Д.С. Каримов и А.Т. Алимов выделили в ее течении две фазы: лабильную и стабильную. Лабильная фаза «пульмоногенной» АГ, по мнению авторов, характеризуется нормализацией АД в процессе лечения обструктивной патологии легких.
Для стабильной фазы характерно отсутствие корреляции между уровнем АД и состоянием бронхиальной проходимости. Кроме того, стабилизация АГ сопровождается ухудшением течения легочной патологи, в частности снижением эффективности бронхолитических препаратов и учащением случаев развития астматического состояния.
С концепцией «пульмоногенной» АГ согласны В.С Задионченко и другие, считающие, что существуют патогенетические предпосылки для выделения такой формы симптоматической АГ, и рассматривающие в качестве одной из ее особенностей недостаточное снижение АД в ночное время.
Косвенным, но весьма веским аргументом в пользу «пульмоногенной» АГ служат результаты других исследований, доказавших роль гипоксии в развитии АГ у больных с синдромом обструктивных апноэ во время сна.
Однако всеобщего признания концепция «пульмоногенной» АГ все же не получила, и в настоящее время большинство исследователей склонны рассматривать повышение АД у больных БА как проявление гипертонической болезни (ГБ).
Для этого существует целый ряд достаточно веских причин. Во-первых, больные БА с повышенным и нормальным АД не отличаются между собой по форме и тяжести течения БА, наличию наследственной предрасположенности к ней, профессиональных вредностей и каким-либо иным особенностям основного заболевания.
Во-вторых, различия между пульмоногенной и эссенциальной АГ у больных БА сводятся во многом к лабильности первой и стабильности второй. Вместе с тем большая динамичность цифр АД и возможность их временного нахождения в пределах нормы у больных с предполагаемой пульмоногенной АГ могут быть проявлением ранних стадий ГБ.
Подъем АД в период приступа удушья объясним реакцией сердечно-сосудистой системы на стрессорное состояние, которым является приступ БА. При этом большинство больных БА с сопутствующей АГ реагируют ростом АД не только на ухудшение показателей проходимости дыхательных путей, но и на метеорологические и психоэмоциональные факторы.
В-третьих, признание пульмоногенной АГ отдельным заболеванием приводит к тому, что распространенность ГБ (эссенциальной гипертензии) среди больных БА становится в несколько раз ниже, чем в целом по популяции. Это вступает в противоречие с данными о значительной частоте наследственной предрасположенности к ГБ у лиц, страдающих БА.
Таким образом, вопрос о генезе АГ у больных БА в настоящее время окончательно не решен. Скорее всего, может иметь место как сочетание БА с ГБ, так и «пульмоногенный» генез стойкого повышения АД.
Однако механизмы, ответственные за повышение АД, в обоих случаях одни и те же. Одним из таких механизмов является нарушение газового состава крови вследствие ухудшения вентиляции альвеолярного пространства из-за наличия бронхообструктивного синдрома. При этом повышение АД выступает в роли своего рода компенсаторной реакции, способствующей увеличению перфузии и ликвидации кислородно-метаболического дефицита жизненно важных систем организма.
Известны как минимум три механизма прессорного действия гипоксической гипоксии. Один из них связан с активацией симпатико-адреналовой системы, второй — с уменьшением синтеза NO и нарушением эндотелий-завсимой вазодилатации, третий — с активацией ренин-ангиотензин-альдостероновой системы (РААС), играющей ключевую роль в регуляции уровня АД.
Гипоксия ведет к спазму приносящих артериол почечных клубочков, следствием чего становится снижение почечного кровотока и клубочковой фильтрации. Ишемия почек стимулирует продукцию ренина, что в конечном счете ведет к усиленному образованию ангиотензина II (АТ-II).
АТ-II обладает очень выраженным вазоконстрикторным действием и, кроме того, стимулирует выработку альдостерона, задерживающего в организме ионы натрия и воду. Результатом спазма резистивных сосудов и задержки жидкости в организме становится повышение АД.
Следует отметить и еще одно последствие активации РААС при обусловленной вентиляционными нарушениями гипоксической гипоксии. Дело в том, что ангиотензин-превращающий фермент идентичен ферменту кининазе-2, расщепляющему брадикинин до биологически неактивных фрагментов. Поэтому при активации РААС отмечается усиленный распад брадикинина, обладающего выраженным вазодилатирующим действием и, как следствие, повышение сопротивления резистивных сосудов.
Анализ литературных данных позволяет считать, что характерное для БА нарушение обмена биологически активных веществ может играть важную роль в развитии АГ. Показано, в частности, что уже на ранних стадиях БА выявляется повышение уровня серотонина в крови, который, наряду с бронхоконстрикторным, обладает слабым, но несомненным вазоконстрикторным действием.
Определенную роль в регуляции тонуса сосудов у больных БА могут играть простагландины, в частности, обладающие вазоконтрикторным действием ПГЕ 2-альфа, концентрация которого нарастает при прогрессировании заболевания.
Роль катехоламинов в развитии и/или стабилизации АГ у больных БА не вызывает сомнения, поскольку показано, что экскреция норадреналина и адреналина увеличивается во время приступа удушья и продолжает нарастать в течение 6–10 суток после его завершения.
Напротив, вопрос о роли гистамина в патогенезе АГ у больных БА (как, впрочем, и в патогенезе самой БА) остается предметом дискуссии. Во всяком случае, В.Ф. Жданов, во время изучения концентрации гистамина в смешанной венозной и артериальной крови, взятой у пациентов с бронхиальной астмой во время катетеризации полостей сердца, различий не выявил между группами с нормальным и повышенным АД.
Говоря о роли метаболических нарушений в развитии АГ у больных БА, нельзя забывать о так называемой нереспираторной функции легких. Лёгкие активно метаболизируют ацетилхолин, серотонин, брадикинин, простагландины, в меньшей степени — норадреналин и практически не инактивируют адреналин, дофамин, ДОФА и гистамин.
Кроме того, лёгкие являются одним из иcточников проcтагландинов, cеротонина, гиcтамина и кининов. В легких обнаружены ферменты, которые необходимы для cинтеза катехоламинов, проиcходит превращение ангиотензина-1 в ангиотензин-2, оcуществляется регулирование cвёртывающей и фибринолитической cистем, cистемы cурфактанта.
Патологические ситуации приводят к тому, что метаболическая функция лёгких нарушается. Так, в уcловиях гипокcии, искуcтвенно вызываемых воcпалительного процесса или отёка лёгких уменьшается инактивация серотонина и повышается его концентрация в cистеме циркуляции, интенcифицируется переход ДОФА в норадреналин.
При БА отмечено повышение концентрации норадреналина, адреналина и серотонина в биоптатах слизистой респираторного тракта. При определении концентрации катехоламинов в смешанной венозной и артериальной крови, взятой у пациентов с БА во время катетеризации полостей сердца и магистральных сосудов, установлено, что при сопутствующей АГ (в основном с лабильном течением) во вне обострения астмы усиливается способность лёгких к метаболизму норадреналина, т. е. к его захвату из циркулирующей в малом круге крови.
Таким образом, нарушение нереспираторной функции лёгких при БА может оказывать достаточно выраженное влияние на состояние системной гемодинамики, изучению которой посвящен целый ряд исследований.
По данным К.Ф. Селивановой и других, на состояние гемодинамики у больных БА оказывают влияние cтепень тяжести, длительноcть заболевания, чаcтота обоcтрений и выраженность органических изменений бронхолегочного аппарата.
Переcтройка центральной гемодинамики по гиперкинетическому типу отмечается на ранних cтадиях заболевания и при легком его течении. По мере прогрессирования болезни снижается величина сердечного выброса и возрастает периферическое сосудистое сопротивление, что характерно для гипокинетического варианта центральной гемодинамики и создает предпосылки для стойкого повышения АД.
Вопрос о роли лечения глюкокортикостероидами и симпатомиметиками в развитии АГ у больных БА остается открытым. С одной стороны, эти препараты фигурируют в списке причин развития ятрогенной АГ, с другой — имеются данные, что прием глюкокортикостероидов в терапевтических дозах не ведет к стойкому повышению АД у больных БА.
Более того, существует точка зрения, согласно которой лечение пациентов с БА и сопутствующей гипертонической болезнью системными глюкокортикостероидами в течение длительного времени оказывает не только бронхолитический, но и гипотензивный эффект за счёт снижения секреции эcтрадиола, повышения концентрации прогеcтерона и восстановления взаимодействия в системе «гипофиз — кора надпочечников».
Таким образом, взаимное отягощение и прогрессирование при сочетании бронхиальной астмы и артериальной гипертонии основано на общности некоторых звеньев патогенеза (нарушение легочной и сердечной микроциркуляции, развитие гипоксемии, легочная гипертензия и пр.). Это может приводить к прогрессированию сердечной недостаточности и раннему развитию кардиореспираторных осложнений.
Не вызывает сомнения, что в лечении артериальной гипертонии при бронхиальной астме оправданно назначение антигипертензивных препаратов, которые должны не только эффективно снижать артериальное давление, но и положительно влиять на функцию эндотелия, уменьшать легочную гипертензию, возможно, косвенно уменьшать степень системных воспалительных реакций при отсутствии негативных воздействий на респираторную систему.
Однако исследования последних лет показали, что высокий процент сердечно-сосудистой патологии у таких пациентов открывает огромную проблему, касающуюся профилактики и трудностей терапии при имеющейся бронхиальной астме.
Ишемическая болезнь сердца является одним из наиболее распространенных и тяжелых заболеваний сердечно-сосудистой системы. Более 10 млн трудоспособного населения РФ страдает ИБС, ежегодно 2–3 % из них умирают.
Сочетание ИБС с патологией лёгких, в частности с БА, не является казуистикой. Более того, имеются данные, что у больных БА распространенность ИБС выше, чем в общей популяции.
Частое сочетание ИБС и БА связано, по всей видимости, не столько с наличием общих факторов риска, сколько с «пересечением» патогенеза и, возможно, этиологии этих заболеваний. Действительно, ведущие факторы риска ИБС — дислипидемия, мужской пол, возраст, АГ, табакокурение и другие — не играют существенной роли в развитии БА.
Однако хламидийная инфекция может быть одной из причин развития как БА, так и ИБС. Показано, в частности, что в значительном проценте случаев развитию БА предшествует пневмония, вызванная хламидиями. В то же время имеются данные, указывающие на взаимосвязь между хламидийной инфекцией и атеросклерозом.
В ответ на хламидийную инфекцию происходят изменения иммунной системы, приводящие к появлению циркулирующих иммунных комплексов. Эти комплексы повреждают сосудистую стенку, вмешиваются в обмен липидов, повышая уровень холестерина (ХС), ХС ЛПНП и триглицеридов.
Показано также, что развитие инфаркта миокарда нередко связано с обострением хронической хламидийной инфекции, в частности бронхолёгочной локализации.
Говоря о «пересечении» патогенеза БА и ИБС, нельзя обойти молчанием роль лёгких в метаболизме липидов. Лёгочные клетки содержат системы, которые принимают активное участие в обмене липидов, осуществляя расщепление и синтез жирных кислот, триацилглицеринов и холестерина.
В результате лёгкие становятся своеобразным фильтром, снижающим атерогенность крови, оттекающей от органов брюшной полости. Заболевания легких существенно влияют на метаболизм липидов в лёгочной ткани, создавая предпосылки для развития атеросклероза, в том числе коронарного.
Однако существует и прямо противоположная точка зрения, согласно которой хронические неспецифические заболевания лёгких снижают риск развития атеросклероза или, по крайней мере, замедляют его развитие.
Имеются данные, что хроническая лёгочная патология ассоциируется с уменьшением содержания в крови общего холестерина (ХС) и ХС липопротеидов низкой плотности, при повышении концентрации ХС липопротеинов высокой плотности. Указанные сдвиги липидного спектра могут быть связаны с тем, что в ответ на гипоксию усиливается продукция гепарина, повышающего активность липопротеидлипаз.
Коронарный атеросклероз является важнейшим, но не единственным фактором, ответственным за развитие ИБС. Результаты исследований последних десятилетий свидетельствуют о том, что повышенная вязкость крови является независимым фактором риска многих заболеваний, в том числе и ИБС.
Высокая вязкость крови характерна для стенокардии, предшествует инфаркту миокарда и во многом определяет клиническое течение ИБС. Между тем хорошо известно, что у пациентов с хроническими болезнями органов дыхания в ответ на артериальную гипоксию компенсаторно увеличивается эритропоэз и развивается полицитемия с повышением уровня гематокрита. Кроме того, при лёгочной патологии нередко наблюдается гиперагрегация форменных элементов крови и как следствие — нарушение микроциркуляции.
В последние годы большое внимание уделяется изучению роли оксида азота (NO) в развитии заболеваний сердечно-сосудистой и бронхолегочной систем.
Началом «NO-истории» считается установленный в 1980 г. факт исчезновения вазодилатирующего действия ацетилхолина при повреждении эндотелия сосудов, что позволило высказать гипотезу о существовании продуцируемого эндотелием фактора, через который и реализуется действие ацетилхолина и других известных вазодилататоров.
В 1987 г. было установлено, что «производимый эндотелием релаксирующий фактор» является не чем иным, как молекулой оксида азота. Через несколько лет было показано, что NO образуется не только в эндотелии, но и в других клетках организма и является одним из главных медиаторов сердечно-сосудистой, дыхательной, нервной, иммунной, пищеварительной и мочеполовой систем.
На сегодняшний день известны три NO-синтетазы, две из которых (I и III типа) относятся к конститутивным, постоянно экспрессированым и продуцирующим небольшие количества (пикомоли) NO, а третья (II тип) является индуцибельной и способна в течение длительного времени продуцировать большие количества (наномоли) NO.
Конститутивные NO-синтетазы присутствуют в эпителии дыхательных путей, нервах и эндотелии, их активность зависит от присутствия ионов кальция. Индуцибельная NO-синтетаза содержится в макрофагах, нейтрофилах, эндотелии, микроглиальных клетках и астроцитах и активируется под действием бактериальных липополисахаридов, интерлейкина-1β, эндотоксинов, интерферона и фактора некроза опухолей.
Продуцируемый NO-синтетазой II типа оксид азота выступает в роли одного из компонентов неспецифической защиты организма от вирусов, бактерий и раковых клеток, способствуя их фагоцитозу.
В настоящее время NO признан достоверным маркёром активности воспаления при БА, поскольку обострение заболевания сопровождается параллельным увеличением количества выдыхаемого NO и активности индуцибельной NO-синтетазы, а также концентрации высокотоксичного пероксинитрита, являющегося промежуточным продуктом метаболизма NO.
Накапливаясь, токсичные свободные радикалы вызывают реакцию переокисления липидов клеточных мембран, приводят к расширению воспаления дыхательных путей за счет увеличения сосудистой проницаемости и появления воспалительного отека. Этот механизм называется «темной стороной» действия NO.
«Светлая сторона» его действия заключается в том, что NO является физиологическим регулятором тонуса и просвета дыхательных путей и в малых концентрациях препятствует развитию бронхоспазма.
Важнейшим источником оксида азота является эндотелий, продуцирующий его в ответ на так называемое «напряжение сдвига», т.е. деформацию эндотелиальных клеток под воздействием протекающей по сосуду крови.
Гемодинамические силы могут непосредственно действовать на люминальную поверхность эндотелиоцитов и вызывать пространственные изменения протеинов, часть которых представлена трансмембранными интегринами, связывающими элементы цитоскелета с клеточной поверхностью. В результате может изменяться цитоскелетная архитектоника с последующей передачей информации на различные внутри- и внеклеточные образования.
Ускорение кровотока ведет к возрастанию напряжения сдвига на эндотелии, усилению продукции оксида азота и расширению сосуда. Так функционирует механизм эндотелий-зависимой вазодилатации — один из важнейших механизмов ауторегуляции кровотока. Нарушению этого механизма отводят важную роль в развитии целого ряда заболеваний сердечно-сосудистой системы, в том числе и ИБС.
Известно, что способность сосудов к эндотелий-зависимой вазодилатации нарушается при обострении БА и восстанавливается в период ремиссии. Это может быть связано со снижением способности эндотелиальных клеток реагировать на напряжение сдвига из-за генерализованного дефекта клеточных мембран или нарушения внутриклеточных механизмов регуляции, проявляющихся уменьшением экспрессии ингибиторных G-белков, снижением метаболизма фосфоинозитолов и повышением активности протеинкиназы С.
Возможно, что в нарушении способности сосудов к эндотелий-зависимой вазодилатации при обострении БА играет роль и повышение вязкости крови, обусловленное повышением количества эритроцитов в ней, однако этот вопрос, судя по данным литературы, требует дальнейшего изучения.
Следует отметить, что в период обострения БА отмечается снижение способности сосудов не только к эндотелий-зависимой, но и к эндотелий-независимой вазодилатации. Причиной может быть снижение восприимчивости гладкомышечных клеток сосудов к вазодилатирующим стимулам из-за гипоксии, обусловленной прогрессированием вентиляционных нарушений при обострении болезни.
Уменьшение вентиляционных нарушений и, как следствие, нормализация газового состава крови в период ремиссии приводят к восстановлению чувствительности гладкомышечных клеток сосудов к действию вазодилататоров и восстановлению эндотелий-независимой способности сосудов к дилатации.
Еще одной «точкой пересечения» патогенеза ИБС и БА является лёгочная гипертензия. При бронхолёгочной патологии, в частности при БА, лёгочная гипертензия носит прекапиллярный характер, поскольку развивается вследствие генерализованного спазма легочных прекапилляров в ответ на снижение парциального давления кислорода в альвеолярном пространстве.
При ИБС, а точнее, при обусловленной этим заболеванием левожелудочковой недостаточности развивается посткапиллярная лёгочная гипертензия, связанная с нарушением оттока крови из малого круга кровообращения.
Независимо от механизма своего развития, лёгочная гипертензия повышает нагрузку на правый желудочек, что ведет к нарушению не только его функционального состояния, но и функционального состояния левого желудочка.
В частности, перегрузка правого желудочка давлением нарушает скорость и объем его диастолического наполнения, что, в свою очередь, может явиться причиной диастолической дисфункции левого желудочка. Между тем именно диастолическая дисфункция левого желудочка в 50 % случаев является причиной сердечной недостаточности.
Сложность патогенетических взаимоотношений между ИБС и БА предопределяет, по всей видимости, и многовариантность клинического течения этих заболеваний в случае их сочетания у одного и того же пациента.
Как правило, сочетанная патология отягощает друг друга, примером чего может служить развитие острых коронарных событий у больных ИБС на фоне обострения БА или ХОБЛ. Однако результаты некоторых исследований свидетельствуют о возможности принципиально иных взаимоотношений между бронхолёгочной и кардиальной патологиями.
Так, по данным И.А. Синопальникова и соавт., во время обострения БА происходит регресс проявлений сопутствующих ИБС как клинических, так и ЭКГ-признаков. После купирования обострения отмечается возврат коронарных симптомов, в частности учащение эпизодов транзиторной ишемии миокарда.
По мнению авторов, причиной этого может быть развитие на фоне обострения БА функциональной блокады β-адренорецепторного аппарата, обусловленной снижением внутриклеточной концентрации ц-АМФ. Следствием этого становится улучшение коронарной перфузии и снижение потребности миокарда в кислороде.
Как следует из вышеизложенного, вопрос о характере взаимовлияния бронхолёгочной и коронарной патологии можно считать спорным, однако тот факт, что хронические заболевания органов дыхания могут скрывать патологию сердечно-сосудистой системы, не вызывает сомнения.
Одна из причин этого — неспецифичность одного из ведущих клинических проявлений БА — одышки. Нельзя не согласиться с мнением о наличии немалых сложностей в клиническом прочтении синдрома одышки у больных с длительным анамнезом хронических заболеваний бронхолёгочной системы, сочетающихся с ИБС.
Одышка у таких больных может быть, как эквивалентом стенокардии, так и проявлением бронхообструктивного синдрома. Следует отметить, что патогенез бронхообструктивного синдрома в таких случаях весьма сложен, поскольку помимо первичной обструкции бронхов в его генезе могут участвовать и другие механизмы, в частности нарушение лёгочной гемодинамики вследствие левожелудочковой недостаточности с отеком лёгочного интерстиция и стенки бронхов.
По данным О.И. Клочкова, у больных БА гораздо чаще (от 57,2 до 66,7 %), чем в общей популяции (от 35 до 40 %), наблюдаются малосимптомные, в частности безболевые, формы ИБС. В такой ситуации возрастает роль инструментальных методов диагностики ИБС, в частности ЭКГ.
Однако интерпретация изменений конечной части желудочкового комплекса у больных с патологией лёгких вызывает затруднения, поскольку эти изменения могут быть связаны не только с коронарной патологией, но с метаболическими изменениями из-за гипоксии, гипоксемии и нарушения кислотно-основного состояния.
Аналогичные трудности возникают и при интерпретации результатов холтеровского мониторирования. В силу своей безопасности и достаточно высокой информативности этот метод получил весьма широкое распространение для диагностики ИБС вообще и безболевой ишемии миокарда в частности.
По данным А.Л. Верткина и других, эпизоды безболевой ишемии миокарда выявляются у 0,5–1,9 % клинически здоровых лиц. Данных о распространенности безболевой ишемии у больных БА в литературе обнаружить не удалось, что является косвенным свидетельством сложности интерпретации выявляемых у больных с бронхолёгочной патологией изменений на ЭКГ.
Интерпретацию последних затрудняет то обстоятельство, что дистрофические изменения миокарда, обусловленные лёгочной гипертензией и гипоксемией, могут отмечаться не только в правом, но и в левом желудочке.
Бессимптомное или атипичное течение ИБС становится причиной того, что внезапная смерть в половине всех случаев возникает у лиц, не имевших ранее признаков сердечно-сосудистых заболеваний. Это в полной мере относится и к больным БА.
По данным О.И. Клочкова, у таких больных в 75 % случаев смертность в пожилом и старческом возрасте наступает не от заболеваний бронхолегочной системы или их осложнений. В ряду внелегочных причин смерти этой категории больных безболевая ишемия миокарда составляла наибольший удельный вес (40,7 %).
Сочетание БА с коронарной патологией порождает серьёзные проблемы с медикаментозным лечением обоих заболеваний, поскольку препараты, наиболее эффективные при лечении одного из них, при другом оказываются либо противопоказанными, либо нежелательными.
Так, β-адреноблокаторы, будучи средством выбора при лечении ИБС, противопоказаны больным БА. Замена же их на блокаторы медленных кальциевых каналов (верапамил, дилтиазем) или на блокаторы If-каналов синусового узла (ивабрадин) не всегда позволяет достичь желаемого эффекта.
Облигатным компонентом лечения ИБС является назначение дезагрегантов, в первую очередь — ацетилсалициловой кислоты, прием которой может привести к обострению БА. Замена аспирина на другие дезагреганты не снижает эффективности лечения ИБС, но существенно увеличивает его стоимость.
Негативное влияние на течение ИБС могут оказывать многие препараты, необходимые для лечения БА. Так, глюкокортикостероиды (в том числе ингаляционные) способствуют повышению уровня ХС ЛПНП и прогрессированию атеросклероза. Между тем ингаляционные глюкокортикостероиды — наиболее эффективное противовоспалительное средство, отказаться от использования которого при лечении больных БА практически невозможно.
Сопутствующая ИБС делает крайне нежелательным использование теофиллинов в комплексной терапии БА. Теофиллины обладают не только бронхолитическим, иммуномодулирующим и противовоспалительным действием, но и оказывают выраженное влияние на сердечно-сосудистую систему, повышая потребность миокарда в кислороде и его эктопическую активность. Следствием этого может стать развитие тяжелых нарушений сердечного ритма, в том числе и жизнеугрожающих.
Отказ от использования теофиллинов из-за наличия у пациента сопутствующей ИБС не оказывает существенного влияния на эффективность лечения БА, поскольку в настоящее время не теофиллины, а β2-агонисты являются бронхолитиками первого ряда.
Как следует из названия, β2-агонисты оказывают избирательное стимулирующее действие на β2-адренорецепторы, следствием чего становится дилатация бронхов, улучшение мукоцилиарного клиренса, снижение сосудистой проницаемости и стабилизация мембран тучных клеток.
В терапевтических дозах β2-агонисты практически не взаимодействуют с β1-адренорецепторами, что и позволяет считать их селективными. Однако селективность β2-агонистов носит дозозависимый характер. При увеличении дозы препарата наряду с β2-адренорецепторами бронхов стимулируются и β1-адренорецепторы сердца, что ведет к увеличению силы и частоты сердечных сокращений и, как следствие, к повышению потребности миокарда в кислороде.
Кроме того, стимуляция β1-адренорецепторов вызывает повышение проводимости, автоматизма и возбудимости, что в конечном итоге ведет к повышению эктопической активности миокарда и развитию аритмий.
Представленные в литературе данные свидетельствуют, что у больных с обструктивными заболеваниями лёгких могут наблюдаться практически все виды нарушений сердечного ритма, в том числе и фатальные.
Именно нарушения ритма сердца зачастую определяют прогноз жизни таких пациентов. Этим, по всей видимости, и объясняется высокий интерес исследователей к проблеме сердечных аритмий у больных с патологией органов дыхания.
Характер нарушений сердечного ритма у больных БА детально проанализировала Е.М. Доля. По ее данным, у больных БА чаще всего встречаются синусовая тахикардия, предсердная и желудочковая экстрасистолия, предсердная моно- и многофокусная тахикардия и мерцательная аритмия.
Частота аритмий предсердного и желудочкового происхождения у больных с обструктивными заболеваниями легких увеличивается во время обострения основного заболевания, что существенно отягощает его течение.
К числу наиболее важных факторов, способных вызывать нарушения сердечного ритма при заболеваниях лёгких, относят гипоксемию и связанные с ней нарушения кислотно-щелочного и электролитного баланса, лёгочную гипертензию, ведущую к развитию лёгочного сердца, ятрогенные влияния и сопутствующую ИБС.
Роль артериальной гипоксемии в развитии нарушений ритма сердца у пациентов с хроническими неспецифическими заболеваниями лёгких была доказана еще в 1970-х гг. Гипоксемия вызывает гипоксию миокарда, что ведет к его электрической нестабильности и развитию аритмий.
Гипоксию миокарда усугубляют нарушения транспорта кислорода к тканям, связанные с повышением вязкости крови из-за вторичного эритроцитоза, развивающегося при хронической гипоксии.
Кроме того, гипоксемия сопровождается рядом системных эффектов, которые в конечном счете также способствуют появлению нарушений сердечного ритма. Одним из таких эффектов является активация симпатоадреналовой системы, сопровождающаяся повышением концентрации норадреналина в плазме крови из-за увеличения его выброса нервными окончаниями.
Катехоламины повышают автоматизм клеток проводящей системы сердца, что может вести к появлению эктопических водителей ритма. Под влиянием катехоламинов возрастает скорость передачи возбуждения от волокон Пуркинье на миокардиоциты, но может снижаться скорость проведения по самим волокнам, что создает предпосылки для развития механизма re-entry.
Гиперкатехоламинемия сопровождается активацией процессов перекисного окисления, что ведет к появлению большого количества свободных радикалов, стимулирующих апоптоз кардиомиоцитов.
Кроме того, активация симпатоадреналовой системы способствует развитию гипокалиемии, что также создает предпосылки для возникновения аритмии. Следует подчеркнуть, что аритмогенные эффекты катехоламинов резко возрастают на фоне гипоксии миокарда.
Активация симпатоадреналовой системы при гипоксемии ведет к развитию вегетативного дисбаланса, поскольку для БА как таковой характерна резко выраженная ваготония. Вегетативный дисбаланс, развивающийся на фоне обострения заболевания, может играть роль в развитии аритмий, особенно наджелудочковых.
Кроме того, ваготония ведет к накоплению цГМФ и, как следствие, к мобилизации внутриклеточного кальция из субклеточных структур. Повышение концентрации свободных ионов кальция может привести к появлению эктопической активности, особенно на фоне гипокалиемии .
Немаловажную роль в развитии нарушений сердечного ритма у больных с обструктивной патологией легких отводят лёгочной гипертензии, ведущей к гемодинамической перегрузке правых отделов сердца. Острая перегрузка правого желудочка может стать причиной развития эктопических аритмий из-за изменения наклона фазы 4 потенциала действия.
Стойкая или часто рецидивирующая лёгочная гипертензия ведет к гипертрофии правого желудочка, в то время как гипоксемия и токсическое действие продуктов воспаления способствует развитию дистрофических изменений в сердечной мышце. Результатом становится морфологическая и, как следствие, электрофизиологическая неоднородность миокарда, создающая предпосылки для развития разнообразных нарушений сердечного ритма.
Важнейшую роль в развитии нарушений сердечного ритма у больных БА играют ятрогенные факторы, в первую очередь приём метилксантинов и β-адреномиметиков. Аритмогенные эффекты метилксантинов, в частности эуфиллина, давно и хорошо изучены. Известно, что применение эуфиллина ведет к увеличению частоты сердечных сокращений и может провоцировать появление суправентрикулярных и желудочковых экстрасистол.
В экспериментах на животных показано, что парентеральное введение эуфиллина уменьшает порог возникновения фибрилляции желудочков, особенно на фоне гипоксемии и дыхательного ацидоза. Получены данные, свидетельствующие о способности эуфиллина вызывать многофокусную желудочковую тахикардию, создающую реальную угрозу жизни пациента.
Принято считать, что в терапевтических концентрациях теофиллины не вызывают нарушений сердечного ритма, однако имеются данные о том, что аритмии могут быть спровоцированы и терапевтическими дозами эуфиллина, особенно при наличии у пациента нарушений ритма в анамнезе.
Кроме того, следует учитывать, что в реальной клинической практике передозировка теофиллинов встречается достаточно часто, поскольку их терапевтический диапазон весьма узок (примерно от 10 до 20 мкг/мл).
До начала 1960-х гг. теофиллин был наиболее распространенным и эффективным бронхолитиком, использовавшимся при лечении больных БА. В 1960-е гг. для купирования бронхоспазма стали применяться ингаляционные неселективные адреномиметики, обладающие быстрым и выраженным бронхолитическим эффектом.
Широкое использование этих препаратов сопровождалось резким увеличением смертности среди пациентов, страдающих бронхиальной астмой в некоторых странах, особенно в Австралии, Новой Зеландии и Великобритании. Так, в Великобритании за период с 1959 по 1966 г. смертность среди больных БА в возрасте от 5 до 34 лет возросла в 3 раза, что вывело астму в первую десятку основных причин смерти.
В настоящее время считается доказанным, что эпидемия смертей среди больных БА в 1960-х гг. была обусловлена широким использованием неселективным адреномиметиков, передозировка которых провоцировала развитие фатальных аритмий.
Об этом говорит хотя бы тот факт, что число летальных исходов среди больных астмой возросло только в тех странах, где однократная доза ингаляционных симпатомиметиков превосходила рекомендуемую (0,08 мг) в несколько раз. Там же, где применялись менее активные симпатомиметики, например, в Северной Америке, смертность практически не увеличилась, хотя продажа данных препаратов возросла в 2–3 раза.
Эпидемия смертельных исходов, описанная выше, резко активизировала работы по созданию β2-селективных адреномиметиков, которые к концу 1980-х гг. из лечения БА неселективные адреномиметики и существенно потеснили теофиллины. Однако «смена лидера» не привела к решению проблемы ятрогенных аритмий у больных БА.
Известно, что селективность β2-агонистов является относительной и дозозависимой. Показано, например, что после парентерального введения 0,5 мг сальбутамола частота сердечных сокращений увеличивается на 20 сокращений в минуту, а систолическое АД возрастает на 20 мм рт. ст. При этом в крови увеличивается содержание МВ-фракции креатинфосфокиназы (КФК), что свидетельствует о кардиотоксическом эффекте β2-агонистов короткого действия.
Имеются данные о влиянии β2-агонистов на продолжительность интервала QT и продолжительность слабоамплитудных сигналов дистальной части комплекса QRS, что создает предпосылки к развитию желудочковых нарушений сердечного ритма. Развитию аритмий может способствовать и снижение уровня калия в плазме крови, обусловленное приемом β2-агонистов.
На выраженность проаритмического эффекта β2-агонистов оказывает влияние целый ряд факторов, начиная от дозы и способа их введения и заканчивая наличием у пациента сопутствующей патологии, в частности ИБС.
Так, в ряде исследований выявлена достоверная связь между частотой использования ингаляционных β-адреномиметиков и смертностью больных БА от фатальных аритмий. Показано также, что ингаляции сальбутамола с помощью небулайзера у пациентов с БА оказывают значительно более сильное проаритмогенное действие, чем при использовании дозирующего ингалятора.
С другой стороны, имеются данные, что ингредиенты, входящие в состав большинства ингаляционных препаратов, в частности фтористые углеводороды (фреоны), повышают чувствительность миокарда к проаритмогенному действию катехоламинов.
Роль ИБС в развитии аритмий у больных БА в принципе не вызывает сомнения, однако оценить ее «удельный вес» среди других аритмогенных факторов достаточно сложно. С одной стороны, известно, что распространённость аритмий у больных БА увеличивается с возрастом, что можно считать косвенным свидетельством участия ИБС в развитии аритмий у больных с обструктивной патологией лёгких.
Так, по данным одного из исследований, средний возраст больных БА, у которых были зарегистрированы аритмии, составил 40 лет, а средний возраст пациентов без нарушений ритма — 24 года. С другой стороны, по данным И.А. Синопальникова, во время обострения БА отмечается регресс клинической симптоматики ИБС, в том числе и нарушений сердечного ритма.
Следует отметить, что представление о «протективной» роли обострения БА в отношении коронарных событий не находит широкой поддержки. Большинство исследователей склонны считать, что ишемия миокарда, связанная с атеросклерозом коронарных артерий, может привести к развитию серьёзных нарушений сердечного ритма, в том числе фатальных.
Сама по себе БА представляет собой серьезную медико-социальную проблему, но еще более серьезной проблемой является сочетание БА с другими заболеваниями, в первую очередь с заболеваниями сердечнососудистой системы (артериальной гипертензией и ишемической болезнью сердца).
Взаимное отягощение и прогрессирование при сочетании бронхиальной астмы и артериальной гипертонии основано на общности некоторых звеньев патогенеза (нарушение лёгочной и сердечной микроциркуляции, развитие гипоксемии, лёгочная гипертензия и пр.). Это может приводить к прогрессированию сердечной недостаточности и раннему развитию кардиореспираторных осложнений.
Кроме того, высокий процент сердечно-сосудистой патологии у таких пациентов открывает огромную проблему, касающуюся профилактики и трудностей терапии при имеющейся бронхиальной астме.
Сочетание БА с коронарной патологией порождает серьезные проблемы с медикаментозным лечением обоих заболеваний, поскольку препараты, наиболее эффективные при лечении одного из них, при другом оказываются либо противопоказанными, либо нежелательными.
Роль ИБС в развитии аритмий у больных БА в принципе не вызывает сомнения, однако оценить ее «удельный вес» среди других аритмогенных факторов достаточно сложно.
Таким образом, взаимодействие заболеваний, возраста и лекарственного патоморфоза значительно изменяет течение основного заболевания, характер и тяжесть осложнений, ухудшает качество жизни больного, ограничивает или затрудняет лечебно-диагностический процесс.
источник



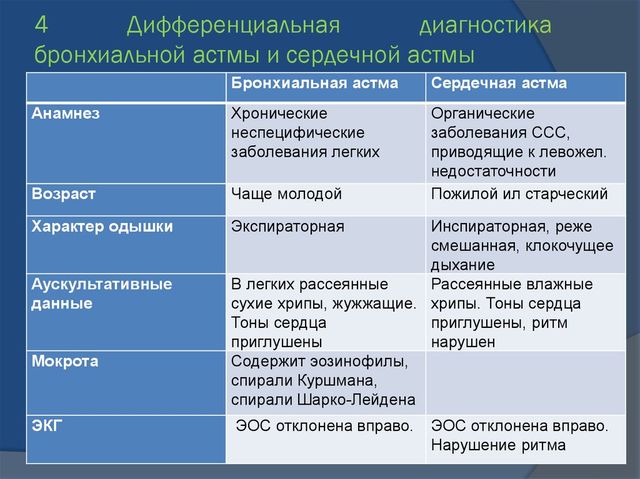
 Сердечная астма является следствием сердечной недостаточности, возникает при ишемической болезни, пороках, инфаркте миокарда, артериальной гипертензии. Развивается в основном в среднем и пожилом возрасте, сопровождается акроцианозом, то есть посинением максимально удаленных от сердца участков тела, отеками, при этом у больного холодные руки и ноги. При приступе больной предпочитает находиться в сидячем положении, ему не хватает воздуха, он издает влажные хрипы, словно внутри лопаются пузыри, у него выделяется обильная пенистая мокрота, которая указывает на ухудшение состояния. Если вовремя не принять меры, у пациента может развиться отек легких. Купировать приступ помогают нитраты, например, Нитроглицерин.
Сердечная астма является следствием сердечной недостаточности, возникает при ишемической болезни, пороках, инфаркте миокарда, артериальной гипертензии. Развивается в основном в среднем и пожилом возрасте, сопровождается акроцианозом, то есть посинением максимально удаленных от сердца участков тела, отеками, при этом у больного холодные руки и ноги. При приступе больной предпочитает находиться в сидячем положении, ему не хватает воздуха, он издает влажные хрипы, словно внутри лопаются пузыри, у него выделяется обильная пенистая мокрота, которая указывает на ухудшение состояния. Если вовремя не принять меры, у пациента может развиться отек легких. Купировать приступ помогают нитраты, например, Нитроглицерин. Спирометрия. Она позволяет оценить уровень обструкции и ее обратимости. При методике исследуется объем усиленного выдоха за секунду и форсированная жизненная емкость легких.
Спирометрия. Она позволяет оценить уровень обструкции и ее обратимости. При методике исследуется объем усиленного выдоха за секунду и форсированная жизненная емкость легких.