Иммунологическое бесплодие на нынешний момент изучено, пожалуй, в меньшей степени, чем любые другие факторы снижения фертильности. В его основе лежит наличие у одного или обоих супругов особых антител к половым клеткам. Речь идет об антиспермальных антителах (АсАт), которые могут препятствовать как самому процессу оплодотворения, так и развитию эмбриона на ранних стадиях. Иммунологический фактор выявляется в среднем у каждой десятой пары с идиопатическим бесплодием.
В организме человека присутствуют различные иммуноглобулины, которые подразделяют на 5 классов, каждый из которых имеет определенные биологические свойства. Примечательно, что у женщин специфические антитела обнаруживаются вдвое чаще, чем у мужчин.
Насколько сильно будет снижена репродуктивная функция, зависит от класса антиспермальных антител, их числа иместа прикрепления к половой клетке. Эти факторы могут сочетаться различным образом,провоцируя:
- нарушение процесса сперматогенеза, в результате которого развиваются олигозооспермия (снижение концентрации сперматозоидов), азооспермия (полное отсутствие половых клеток в эякуляте) и тератозооспермия (изменение нормальной морфологии клетки);
- снижение подвижности мужских половых гамет (астенозооспермия)или подавление их активности, которое происходит в результате агглютинации половых клеток, затруднения их передвижения по женским половым путям, а также обездвиживания под воздействием активированного комплимента;
- подавление взаимодействия сперматозоида и яйцеклетки на разных этапах (от момента проникновения мужской половой клетки через оболочку в цитоплазму ооцита до слияния пронуклеусов — ядер половых гамет);
- развитие трубно-перитонеального бесплодия, которое обусловлено наличием специфических антител в перитонеальной жидкости и фаллопиевых трубах, а также нарушением перистальтики органа;
- нарушение процесса имплантации эмбриона в стенку матки.
Среди антиспермальных антител выделяют:
- спермоиммобилизирующие, которые оказывают влияние на подвижность мужской половой клетки, отчасти или полностью обездвиживая ее;
- спермоагглютинирующие, которые становятся причиной склеивания сперматозоидов как друг с другом, так и с макрофагами, частицами других клеток, слизью, а также другими элементами;
- спермолизирующие, которые оказывают на мужские гаметы разрушающее воздействие.
Любые из этих АсАт могут стать причиной бесплодия.
Антитела могут прикрепляться к поверхности мужских половых клеток на разных участках. Исследования методом ИФА выявили следующую закономерность:
- антитела класса G обычно прикрепляются либо к хвосту половой гаметы, либо к ее головке;
- антитела класса А чаще всего обнаруживают в области хвоста, хотя они могут прикрепляться и к головке сперматозоида;
- антитела класса M, как правило, фиксируются в области хвоста.
Если фиксация АсАт в области хвоста оказывает влияние только на подвижность сперматозоида, то прикрепление к головке препятствует собственно процессу оплодотворения, подавляя способность мужской половой гаметы к пенетрации.
Если у женщин с равной долей вероятности могут выявляться все вышеуказанные классы антител, то у мужчин, как правило, обнаруживают только первые два.
Образование половых гамет у мальчиков впервые происходит только в пубертатном периоде, поэтому сперматозоиды должны восприниматься организмом как абсолютно чужеродные элементы, подлежащие уничтожению. Однако этого не происходит. Почему? Дело в том, что в норме сперма и клетки иммунитета никогда не пересекаются друг с другом, поскольку разделены специальным гематотекстикулярным барьером. Но иногда он может нарушаться в результате ИППП, длительного воспалительного процесса в органах малого таза, травм, хирургического вмешательства, варикоцеле, а также по ряду других причин. В этом случае сперматозоиды попадают в кровь и провоцируют аутоиммунную реакцию организма.
Для организма женщины мужские половые клетки являются чужими, однако в норме сперматозоиды на пути к яйцеклетке не встречаются с представителями иммунной системы, что и обеспечивает возможность продолжения рода. Однако в некоторых случаях эта система дает сбой. Если у женщины присутствуют ИППП, эндометриоз, гинекологические или аллергические заболевания, то велик риск того, что клетки иммунитета встретятся со сперматозоидами и постараются уничтожить чужаков.
Чтобы выявить иммунологический фактор бесплодия, врач должен назначить обследование, состоящее из нескольких этапов:
- анализ крови и эякулята на наличие АсАт (для мужчин);
- анализ крови на АсАт и оценка свойств шеечной слизи (для женщин);
- исследование на иммунологическую совместимость.
Факторы иммунологического бесплодия оцениваются на основе результатов таких исследований, как:
- посткоитальный тест, который позволяет оценить взаимодействие сперматозоидов и цервикальной слизи;
- пенетрационный тест, который дает возможность определить способность мужских половых клеток к проникновению в шеечную слизь;
- перекрестный пенетрационный тест, который осуществляется для того, чтобы выяснить, с чьей стороны (мужчины или женщины) присутствуют нарушения.
Лечение направлено на достижение беременности.
Если в основе иммунологического фактора бесплодия лежат нарушения со стороны мужчины, рекомендуются:
- ЭКО/ИКСИ. Этот метод предполагает введение сперматозоида непосредственно в цитоплазму женской половой клетки с помощью микроиглы;
- ПИКСИ — специальная методика, позволяющая отобрать только зрелые сперматозоиды.
Если в основе иммунологического фактора бесплодия лежат нарушения со стороны женщины, рекомендуются консервативные методы, такие как кондом-терапия (исключение незащищенных интимных контактов) или подавление выработки антиспермальных антител у супругов. При отсутствии положительного эффекта врач может предложить внутриматочную инсеминацию. Если достичь беременности по-прежнему не удается, назначают программу ЭКО/ИКСИ.
Сочетанное иммунологическое бесплодие предполагает применение вспомогательных репродуктивных технологий.
В рамках программы ЭКО рекомендуется проведение преимплантационной диагностики, которая позволяет исключить генетические заболевания у будущего ребенка.
Автор У.В. Лапай гинеколог-репродуктолог сети
Центров репродукции и генетики Нова Клиник
источник
Вашей семье уже несколько лет, все у вас в порядке, вот только ребенка никак не удается родить. Все анализы в норме у обоих, только вот в крови обнаружились некие злодеи, обозначенные непонятной аббревиатурой АСАТ — антиспермальные антитела. И из-за них и ничего не выходит с продолжением рода.
Впервые об антителах заговорили еще в конце 19 века. Тогда Э. Берингом и С. Кисато изучали влияние дифтерийной палочки на кроликов. Они нашли в крови животных вещества, которые были способны сопротивляться действию токсинов и выводить его из организма. Вскоре были обнаружены подобные тела, действовавшие подобным образом и на другие враждебные организму агенты. А в 1954 году немецкие ученые Рамк и Вильсон обнаружили подобные тела в половой сфере человека. С тех пор продолжается работа по их изучению и способах борьбы против их пагубного влияния. В конце прошлого столетия ВОЗ признал наличие этих тел в организме заболеванием.
Прежде всего, это молекулы иммунной системы. Говоря простым языком, все антитела распознают вредоносные клетки, атакуют их и выводят из организма. Но иногда в четкой системе происходит сбой, организм ошибается и воспринимает «свое» как «чужое».
Они способны «приклеиваться» к мужским половым клеткам, чем сильно снижают их подвижность. Это белки, которые вырабатываются в иммунной системе человека, неважно, мужчины или женщины. Их «задачей» является уничтожение сперматозоидов. Обнаружить такие тела можно в семенной жидкости, на поверхности самих сперматозоидов, в крови, в цервикальной жидкости. Среди всех видов мужского бесплодия этот вид составляет примерно 20% случаев. У женщин это также частый вид бесплодия. Чаще всего подобные антитела есть у обоих супругов — со спермой мужчины они попадают в организм женщины и там «закрепляются» в слизистой.
Если такие тела образуются в мужском организме, возникает аутоиммунное бесплодие, когда клетки собственного организма воспринимают другие свои же клетки как чужеродные и уничтожают их.
Если же такие тела образуются у женщины, диагностируется иммунологическая несовместимость партнеров. Несколько лет назад ВОЗ выделил эти диагнозы в отдельную группу заболеваний.
Другое название антител — иммуноглобулины. Они состоят из белковой и углеводной частей. Иммунная система использует их для распознавания чужеродных тел, которые попадают в организм, например вирусов или бактерий, различного вида паразитов либо грибов.
Антитела могут связываться только с определенного вида антигенами, по другому — клеточными стенками чужеродного тела.
Наличие этих тел фактически разрушает вещества, защищающие мембрану сперматозоидов, из-за чего те теряют подвижность и погибают. Антиспермальных антител существует несколько видов, каждый из них патологически воздействует на клетки-защитники. Так что иммунологическое бесплодие мужчин — это следствие комбинированного воздействия различных антиспермальных тел.
Антиспермальные антитела образуются в различных отделах репродуктивных органов мужчин и женщин, каждое из них направлено против определенной части сперматозоида — головки, хвоста, средней части, либо комбинированные. Они по разному воздействуют на репродукционные процессы. Бывает ситуация, когда в организме присутствует несколько видов антиспермальных антител.
Клетки спермы — последние, которые образуются в организме мужчины. Зачастую организм ошибается и воспринимает их как чужеродные. Начинают они образовываться в период полового созревания юноши, когда у него появляется сперма — это возраст около 12-13 лет. В это же время у мальчиков в организме появляются антигены семени, иммунная система воспринимает их как угрозу и должна уничтожать. Однако сперматозоиды надежно изолированы от кровеносного русла и в кровь могут попасть только в исключительных случаях, когда нарушается естественный барьер между кровотоком и семенными путями. Тогда-то в организме и включается механизм защиты. В нем запускается механизм уничтожения чужеродных для крови тел, начинают образовываться вещества, разрушающие сперматозоиды. Механизмов попадания в кровь спермы существует несколько.
- Блокировка семявыводящих путей — тогда сперматозоиды просто не могут выйти из канала;
- Повреждения и травмы малого таза
- Заболевания, перенесенные инфекции, в частности свинка.
- Крипторхизм, онкология
- Перенесенные оперативные вмешательства в области малого таза, брюшной полости или половых органов.
АСАТ в семенной жидкости негативно сказывается на выработке, подвижности, жизнеспособности сперматозоидов, при наличии этих тел также ухудшается их транспортировка. Кроме того, когда в сперме присутствуют антитела, в эякуляте существенно снижается количество сперматозоидов, изменяется вязкость, снижается кислотность семенной жидкости, в ней увеличивается количество лейкоцитов.
Все это сильно усложняет возможность оплодотворения яйцеклетки.
Также иногда случается, что антиспермальные антитела появляются в организме уже зрелого мужчины, даже в том случае, что у семейной пары уже имеются дети.
При попадании небольшого количества сперматозоидов либо их предшественников в кровь, в организме запускается система защиты. Молекулы иммунной системы начинают вырабатывать специфические тела, которые начинают «охотиться» за сперматозоидами, прикрепляются к ним, проникают внутрь его тела и разрушают его.
Частички разрушенных сперматозоидов попадают в лимфатическую систему, в ней образуются антитела, которые вновь попадают в кровь. Для крови это чужеродные тела, против которых в ней вырабатываются антитела, попадающие в сперму и разрушающие новые сперматозоиды. И так далее.
Когда даже здоровые сперматозоиды попадают в организм женщины, у которой есть антиспермальные антитела в цервикальной слизи, они тут же бывают ними атакованы. Антитела буквально обсыпают сперматозоиды, лишают их возможности двигаться. Затем проникают сквозь их мембраны и разрывают их изнутри.
Если такие антитела при анализах обнаруживают у женщины в шейке матки, это говорит о том, что они имеются у нее и в других репродуктивных органах — например, в полости самой матки, в трубах, в яичниках. Также они могут быть обнаружены в цервикальной слизи. Присутствие их в шейке матки делает невозможным дальнейшее продвижение сперматозоида естественным путем — они гибнут в течение нескольких часов.
- травмы и нарушения целостности слизистых оболочек;
- большое количество белых кровяных телец в сперме;
- механический способ переноса антител со спермой мужа;
- проникновение в организм «старых» сперматозоидов;
- если сперматозоиды попали в ЖКТ во время нетрадиционного секса — орального или анального. Если у мужчины в сперме имелись антиспермальные антитела, они при таком виде секса легко впитываются в слизистую женщины, после чего попадают в ее кровеносное русло. Дальше уже иммунная система самой женщины начинает бороться с чужеродными ей телами и у нее вырабатываются антитела;
- если в результате некорректно проведенной инсеменации сперма попала в брюшину — для женского организма это чужеродные тела, ее организму несвойственные. Иммунная система женщины начинает защищаться и старается удалить их;
- во время прошлых попыток забора ооцитов при гормональных всплесках во время проведения ЭКО — когда происходит сильнейшая гормональная атака, для того, чтобы у женщины при суперовуляции созрело большее количество яйцеклеток. При заборе ооцитов организм может отреагировать образованием в женском организме большого количества антител, которые попадают в лимфатическую систему.
- оперативные вмешательства на шейке матки, напр. коагуляция эрозии;
- неправильное использование оральных и химических контрацептивов — при этом может случиться сбой при их применении, организм ответит острой реакцией;
- при эндометриозе;
- как аллергическая реакция на сперму.
Иногда случается ситуация, когда у женщины имеется несовместимость именно со спермой мужа, тогда как другая семенная жидкость дает ей возможность забеременеть.
Эндометриоз — следует особо отметить, как причину женского бесплодия. Это воспалительное заболевание, и как и при любом воспалении организм посылает туда большое количество лейкоцитов, чтобы защитится от пагубного воздействия.
При этом состоянии клетки внутреннего строения матки сильно разрастаются, становятся рыхлыми, в них образовывается большое количество антител, которые при встрече со сперматозоидом разрушают его.
Эндометриоз может быть не только в области матки, но и во всех остальных отделах гинекосферы женщины. Но в любом случае, женские антитела будут уничтожать мужские половые клетки.
Когда сперматозоид под воздействием антител гибнет, его захватывают специальные клетки — макрофаги. Они поглощают его, и «разбирают» на более мелкие компоненты. В дальнейшем эти частички погибшего сперматозоида образуют на поверхности макрофага антигены.
Макрофаг попадает в кровоток, оттуда в лимфоузлы, в которых начинают формироваться несвойственные организму антиспермальные антитела. Эти тела с кровотоком распространяются по организму, попадают в слизистую, где задерживаются, атакуют попадающие туда сперматозоиды, и все повторяется по новому кругу. Получается так, что слизистая, вместо того, чтобы помочь сперматозоиду продвинуться к яйцеклетке, становится у него на пути непреодолимым препятствием.
Даже если беременность все же наступила, есть риск, что АСАТ будут отрицательно влиять на плод, что в конце концов приведет к его гибели.
Поэтому так важно, чтобы слизистая была здоровой — она не допустит контакта сперматозоидов с клетками крови, и такой патологический процесс не будет иметь места.
Так же сперматозоиды не могут полноценно попасть в цервикальную слизь. Существует такое явление, как «дрожание», или «кружение» сперматозоидов на одном месте. Это как раз и происходит со
Воздействие антиспермальных антител на процессы репродукции имеют широкий спектр, однако наиболее известны такие механизмы:
- нарушается функциональная активность сперматозоидов, резко снижается их подвижность
- невозможность проникновения сперматозоида в цервикальную слизь
- может стать причиной склеивания сперматозоидов между собой
- процесс взаимодействия сперматозоида с яйцеклеткой и того, как происходит процесс оплодотворения
- Негативное влияние на подготовку сперматозоида к капацитации и акросомальной реакции
- То, как происходит процесс имплементации оплодотворенной яйцеклетки в матку
- пагубное влияние АСАТ на процесс роста и развития зародыша
Зачастую большое количество АСАТ делает невозможным естественное зачатие. Тогда семейной паре предлагают воспользоваться процедурой ЭКО.
АСАТ пагубно влияют и на процесс репродукции — под воздействием антител сперматозоиды не в состоянии выделять фермент, разрушающий желтую оболочку яйцеклетки, через которую он мог бы проникнуть в нее. Этому естественному процессу мешают антитела, которые создают барьеры проникновения сперматозоида в яйцеклетку.
Иногда все же и при наличии повышенного уровня АСАТ у женщины наступает беременность. Но, как они влияют на малыша?
Существует риск, что они отрицательно будут влиять на развивающийся плод, нести угрозу его жизнеспособности.
Организм может воспринять его как «чужеродное» тело, начать отторгать его. Чаще всего беременность прекращается еще до установления факта ее наличия, реже это происходит через несколько неделей после начала.
Из-за АСАТ случаются и состояния «замершей беременности», когда плод перестает развиваться в матке, погибает в ней, но роды не наступают, а плод мумифицируется.
Так что женщина с высоким АСАТ во время беременности должна постоянно быть под наблюдением врача и принимать медикаменты, способствующие снижению уровня АСАТ. В каждом случае это будет свой план лечения, который назначается индивидуально.
Сегодня подобный анализ предписывают сдавать каждой паре, обратившейся к врачам по поводу бесплодия. Перед тем, как врач дает направление на анализ, проводится предварительное исследование общего состояния семейной пары.
Направления получают в том случае, если имеется:
- агглютинация (склеивание) сперматозоидов
- истинная, при которой они склеиваются между собой. Это делает невозможным их продвижение и является причиной бесплодия. При такой агглютинации антитела приклеиваются к основанию головки мужских половых клеток и не дают им двигаться. Бывают ситуации, когда между собой склеиваются сразу много сперматозоидов, либо комбинированная форма.
- ложной — при которой сперматозоиды склеиваются с другими клетками, находящимися в женском половом тракте или в семенной жидкости. Это в значительной степени снижает их способность передвигаться.
- также агрегация сперматозоидов;
- невысокая подвижность сперматозоидов — при этом можно заподозрить, что они обсеменены АСАТ;
- нежизнеспособность сперматозоидов — они могут быть повреждены АСАТ;
- малый объем спермы в цервикальной слизи;
- несколько неудачных попыток инсеминации или ЭКО в прошлом.
В случае с агглютинацией случается очень невысокое количество АСАТ и не сказывается на процессе оплодотворения.
Также направление получают и при невыясненных причинах бесплодия, так называемом «идиопатическом» бесплодии.
Его обязательно проводят каждой паре при сдаче анализов перед ЭКО.
Цервикальная слизь — это продукт, вырабатываемый шейкой матки. Это вязкая жидкость, может быть по цвету от совершенно прозрачной, до молочно-белой. Вырабатывается она железами шейки матки. Название получила от латинского наименования шейки матки — цервикс.
Уже научно доказано, что антиспермальные антитела блокируют проникновение сперматозоидов в цервикальную слизь и их дальнейшее продвижение к трубам. Когда сперматозоид достаточно близко подходит к слизи, в которой есть антитела, в слизи выделяются особые клетки — мицеллы, от которых сперматозоиды «отталкиваются» и не могут проникнуть дальше. В результате он останавливается еще на входе в шейку, где его уничтожают антитела. Это явление получило название блокады.
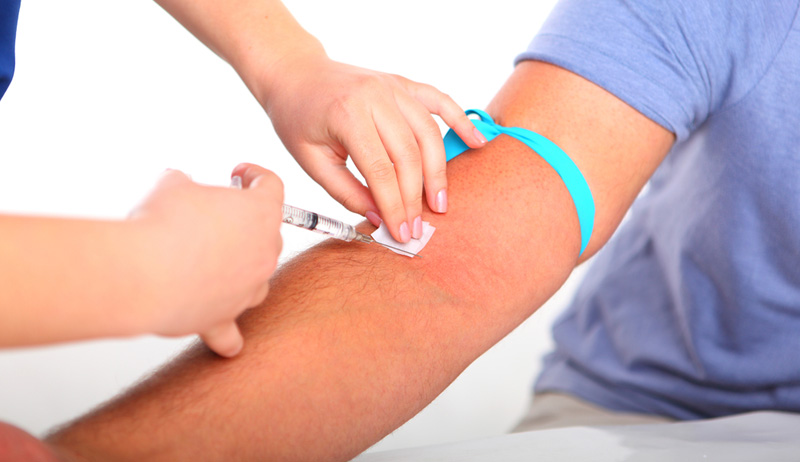
Для обследования надо сделать анализ крови из вены.
При заборе крови — проводится утром, натощак. Сутки до анализа остро рекомендуют воздержаться от курения и употребления даже легкого алкоголя, иначе результаты теста будут смазаны.
Бесплодные пары обязательно исследуют на наличие у них АСАТ. Обязательно обследуются оба супруга.
В дальнейшем у мужчин и женщин диагностика проводится по разному.
Основной анализ — это проверка семенной жидкости. Мужчина может предоставить ее и самостоятельно, либо при помощи пункции яичка. Ему делают спермограмму, которая определит количество антител в эякулляте, их морфологию и на какие части сперматозоидов они влияют.
Также определят и количество самих сперматозоидов, здоровых и поврежденных антителами.
Самыми «злостными» из всех являются антитела класса IgM, которые разрушают мембраму спермиев, что приводит к развитию тяжелой астенозооспермии.
Еще одно АСАТ — IgG. Оно увеличивает уровень лейкоцитов, снижает уровень рН, увеличивает время разжижения спермы. Кроме того, эти два антитела способны поглощать спермии на уровне придатка и уменьшать концентрацию сперматозоидов в эякулляте мужчины.
Еще одним часто встречающимся агресивным антиспермальным антителом является IgA, которое также вызывает патологическое состояние сперматозоидов.
Однако, такие грубые нарушения сперматогенеза случаются не так часто. Их выявляют примерно у каждого десятого мужчины с АСАТ.
Сейчас, по рекомендации ВОЗ, такой тест обязательно проводят при любом проведении спермограммы. Это позволяет уже на раннем этапе выявить возможные отклонения и вовремя начать лечение.
Основной женский анализ — посткоитальный тест. Это абсолютно безопасная и безвредная процедура, у нее нет противопоказаний.
Он проводится двумя способами — in vivo и in vitro.
Исследуется шейка матки в течение суток после полового акта за 1-2 дня перед овуляцией. «Отрицательным» (плохим) результат — если сперматозоиды в половых путях женщины неактивны, малоподвижны, либо имеется их большое количество погибших.
Этот анализ сложнее, его делают одновременно с обоими супругами. У мужчины берется сперма, у женщины слизь из матки. В лабораторных условиях исследуют их взаимодействие. «Отрицательный» результат — малоподвижность сперматозоидов и невысокая поступательная активность в слизи.
Такой анализ очень «капризный», зачастую дает не вполне точные результаты, поэтому его всегда проводят в комплексе с другими исследованиями. Иногда требуется повторное проведение такого теста, так как возможно совпадение какого-то воспаление в организме со сдачей анализа.
Существуют и другие, менее известные и популярные способы определения количества АСАТ в организме человека.
В случае же отрицательного результата подобные тесты станут обязательными для супругов до полного их излечения.
Однако следует принять во внимание и то, что зачастую отрицательный результат при проведении посткоитального теста является присутствие антиспермальных антител в сперме мужа, а не в шейке матки.
Существует также достаточно надежный по своим результатам MAR-тест. Он определяет количество сперматозоидов, которые связаны с антителами различных классов. Делают несколько таких тестов — прямой, когда проверяется связь с антителами классов IgG и IgA, и проверяющий наличие антиспермальных антител в биологических жидкостях. Например в спермоплазме, слизи шейки матки, в плазме крови. Это непрямой тест. Оба их надежны, они международно признанные стандарты диагностики АСАТ, применяются в лучших мировых клиниках и служат отличным средством определения причин бесплодия.
В идеале, в организме человека не должно содержаться АСАТ вообще, но такого практически не случается. Антиспермальные антитела есть у большинства людей, но их иммунная система блокирует их, и именно по этой причине они не наносят особого вреда здоровью человека.
Образуются они в крови еще во время внутриутробного развития человека.
Когда сдают анализ на антиспермальные антитела норма их, как у мужчин, так и у женщин, составляет 0-60 ед/мл. Если есть отклонения в пределах 55-60 ед от верхней границы нормы, врачи рекомендуют пройти повторное исследование в следующем цикле женщины. Возможно, был какой-то сбой в иммунной системе.
Если же АСАТ постоянно повышено, следует незамедлительно начать лечение, чтобы не терять времени для достижения беременности.
Прежде всего, это состояние излечимо, хотя и трудно. Особенно у женщин его не удается излечить полностью.
Основным этапом лечения является длительное применение барьерных способов контрацепции — не менее полугода. При снижении количества поступающей в женский организм семенной жидкости, уменьшается и количество вырабатываемых к ней антител. Для снижения вязкости цервикальной жидкости может назначаться Гуайфенезин.
Кроме того, паре могут предложить внутриматочную инсеминацию.
Мужчинам следует в это время укреплять свой иммунитет, вылечивать имеющиеся заболевания, искать и устранять причины, повлекшие АСАТ. Кроме того, врач пропишет и медикаментозное лечение обоим супругам, с целью снижения выработки таких антител.
Если снизить их уровень все равно не удается, семейной паре предложат технологии ИКСИ и ЭКО. Однако если проведенный тест покажет, что антиспермальные антитела повреждают головку сперматозоида, подобные технологи окажутся неэффективными.
Лечить это состояние все же необходимо. Такое комплексное лечение проводится для пар, желающих в дальнейшем родить ребенка.
источник

Появление АСАТ в семенной жидкости мужчины или шеечной слизи женщины может стать причиной иммунологического бесплодия.
В таком случае достижение беременности становится невозможным вследствие угнетения функции мужских половых клеток факторами иммунной системы.
В мужском организме антиспермальные антитела в норме не образуются. Этому препятствует гематотестикулярный барьер – физическая преграда, отделяющая яички от общей системы кровотока мужчины. Образован этот барьер преимущественно клетками Сертоли с их отростками.
Однако ряд патологических процессов в организме мужчины приводит к тому, что гематотестикулярный барьер нарушается. Чаще всего это происходит в области семявыносящих протоков. В результате факторы иммунитета, циркулирующие в крови, получают доступ к тканям яичек, где созревают сперматозоиды.
Возможные причины нарушения гематотестикулярного барьера:
- травмы мошонки;
- перенесенные хирургические вмешательства;
- воспалительные заболевания, в том числе венерические инфекции;
- варикоцеле.
Образование антител возможно из-за нарушения сперматогенеза, в результате чего сперматозоиды не приспосабливаются к новой среде после созревания. Это происходит вследствие варикоцеле, крипторхизма, воспалительной или эндокринной патологии. Наличие АСАТ в эякуляте мужчин – частая причина мужского бесплодия.
У женщин с бесплодием АСАТ обнаруживаются реже, чем у мужчин. В основном они наблюдаются в шеечной слизи, закрывающей вход в полость матки. Эти факторы местного иммунитета способны снизить шанс оплодотворения яйцеклетки, потому что препятствуют свободному прохождению сперматозоидов через цервикальный канал. Антиспермальные антитела у женщин:
- прикрепляются к мембранным антигенам сперматозоидов, снижая их подвижность;
- блокируют прохождение мужских половых клеток в полость матки;
- блокируют рецепторы на головке мужских половых клеток, которые ответственны за связывание с блестящей оболочкой яйцеклетки;
- вызывают гибель сперматозоидов.
Гораздо большее клиническое значение имеет определение АСАТ у мужчин, чем у женщин, так как обнаружение антиспермальных антител зачастую свидетельствует о снижении оплодотворяющей способности эякулята.

Иногда используется непрямой MAR-тест. В этом случае АСАТ определяются не в эякуляте мужчины, а в его крови. Его делают методом ИФА (иммуноферментного анализа).
Врачи «ВитроКлиник» отказались от определения АСАТ по шеечной слизи женщин, т.к. не доказана диагностическая значимость этого исследования в мировой практике.
Наиболее эффективным методом достижения беременности является использование вспомогательных репродуктивных технологий с целью преодоления бесплодия. Консервативные мероприятия при наличии АСАТ в женском или мужском организме не всегда оказываются эффективными. Искусственная инсеминация или ЭКО при АСАТ – лучший выход из этой ситуации.
Искусственная инсеминация – простой и доступный по цене метод решения проблемы мужского и женского иммунологического бесплодия. Если у пациентов обнаружены антиспермальные антитела, семенную жидкость, предварительно очищенную и концентрированную, можно ввести непосредственно в матку. Таким образом, сперматозоидам больше не нужно преодолевать цервикальный канал, и они легко попадают в маточные трубы для оплодотворения яйцеклетки.
В случае неэффективности инсеминации или большом показателе АСАТ в эякуляте лучшим решением будет ЭКО с ИКСИ. Метод предполагает выбор лучших сперматозоидов для оплодотворения женских яйцеклеток. В этом случае значительно повышается шанс наступления беременности и уменьшается риск невынашивания.
Проблема наличия антиспермальных антител в эякуляте или шеечной слизи в любом случае решаема. Вспомогательные репродуктивные технологии легко преодолевают эти трудности.
Для диагностики и лечения иммунологического бесплодия обращайтесь в «ВитроКлиник». Наши специалисты готовы вам помочь.
источник
Анализ крови на антиспермальные антитела (АСАТ) – лабораторное исследование, направленное на определение уровня специфических иммуноглобулинов к спермальным антигенам. Эти антитела снижают вероятность оплодотворения, могут рассматриваться как иммунологическая причина бесплодия. Анализ является дополнительным методом диагностики при бесплодии, назначается в комплексе со спермограммой, с тестами на антиспермальные антитела в сперме и антитела к овариальным антигенам. Показан для установления причин бесплодия. Исследование находит применение в гинекологии, урологии, репродуктологии. Кровь для анализа забирается из вены, определение в ней антиспермальных антител выполняется иммуноферментным методом. Значения нормы – от 0 до 54,99 МЕ/мл. Результаты подготавливаются в течение 5 рабочих дней.
Анализ крови на антиспермальные антитела (АСАТ) – лабораторное исследование, направленное на определение уровня специфических иммуноглобулинов к спермальным антигенам. Эти антитела снижают вероятность оплодотворения, могут рассматриваться как иммунологическая причина бесплодия. Анализ является дополнительным методом диагностики при бесплодии, назначается в комплексе со спермограммой, с тестами на антиспермальные антитела в сперме и антитела к овариальным антигенам. Показан для установления причин бесплодия. Исследование находит применение в гинекологии, урологии, репродуктологии. Кровь для анализа забирается из вены, определение в ней антиспермальных антител выполняется иммуноферментным методом. Значения нормы – от 0 до 54,99 МЕ/мл. Результаты подготавливаются в течение 5 рабочих дней.
Антиспермальные антитела – группа специфических иммуноглобулинов, которые взаимодействуют с антигенами сперматозоидов, препятствуя наступлению оплодотворения. Их производит иммунная система после контакта со спермой. У здоровых мужчин и женщин антитела к антигенам сперматозоидов не определяются ни в крови, ни в сперме. Их производству препятствует ряд защитных механизмов. В мужском организме воздействие иммунной системы на сперму ограничивается гематотестикулярным барьером – физическим барьером между кровеносными сосудами и семенными канальцами тестикул. Когда он нарушается, иммунная система запускает производство антител к сперме. Причиной могут стать травмы яичек, бактериальные и вирусные инфекции, рак яичек, операции. После связывания антиспермальных антител со сперматозоидами подвижность последних снижается, уменьшается способность проникать через слизь шейки матки.
В женском организме выработка антиспермальных антител может быть спровоцирована инфекциями и воспалениями в мочеполовой системе, аутоиммунными заболеваниями. Когда сперматозоиды приближаются к очагу воспаления, они воспринимаются клетками иммунной системы как чужеродные и уничтожаются. Фагоцитровавшие их макрофаги сохраняют на своей поверхности белковые фрагменты сперматозоидов – антигены. Циркулируя в крови, эти клетки провоцируют выработку АСАТ в женском организме. При половом контакте и после него антитела препятствуют продвижению сперматозоидов, при наступлении беременности нарушают синтез цитокинов, способствующих имплантации плодного яйца, формированию трофобласта и плаценты. Это приводит к выкидышу, гестозу, задержке внутриутробного развития.
Выраженность патологического эффекта антиспермальных антител зависит от титра и активности в отношении антигенов сперматозоидов. Их присутствие в крови не всегда приводит к бесплодию, но вероятность наступления беременности снижается на 40%. Обычно антиспермальные антитела рассматриваются как причина бесплодия, если другие нарушения исключены. Для проведения исследования кровь забирается из вены. Наиболее информативным методом распознавания антител является иммуноферментный анализ. Основные сферы применения исследования – репродуктология, гинекология и урология.
Анализ крови на антиспермальные антитела назначается при комплексном исследовании причин бесплодия, в частности при подозрении на нарушение иммунологической толерантности. Тест является дополнением к исследованию спермы. Он показан в случаях, когда по результатам спермограммы определено снижение подвижности, повышение агрегации и агглютинации сперматозоидов, а также когда выявлены отклонения в результатах посткоитального теста, смешанного антиглобулинового теста или теста латекс-агглютинации у женщин.
При обследовании мужчин более точные результаты теста на антиспермальные антитела могут быть получены в ходе анализа спермы. Исследование крови назначается как дополнительное в случаях отсутствия или дефицита сперматозоидов в эякуляте. К ограничениям анализа крови на АСАТ относится искажение результатов при поли- и моноклональных гаммапатиях, аутоиммунных заболеваниях, изменениях иммунного статуса, например, на фоне длительных инфекций.
При выполнении анализа на антиспермальные антитела в крови забор биоматериала выполняется из вены. Использование иммуноферментного метода предполагает соблюдение некоторых рекомендаций по подготовке к сдаче крови. Во-первых, за день до анализа необходимо исключить физические и психоэмоциональные нагрузки. Во-вторых, накануне запрещено употреблять алкоголь, желательно отказаться от жирной пищи. Кровь забирается на пустой желудок – с утра натощак или спустя 4 часа после приема пищи. За 30 минут до процедуры нужно отказаться от курения, следует провести это время в спокойной обстановке. Пациентам, принимающим лекарственные препараты, стоит обсудить их влияние на результат анализа с лечащим врачом. Процедура забора крови выполняется методом пункции. Биоматериал помещается в герметичную пробирку и доставляется в лабораторию.
Уровень антиспермальных антител определяется в сыворотке крови. Поэтому перед исследованием пробирку устанавливают в центрифугу, з полученной плазмы удаляют факторы свертывания, в частности фибриноген. Сыворотка подвергается иммуноферментному анализу. В общем виде его можно представить как двухэтапную процедуру. На первом этапе в образец вводятся антигены, которые образуют комплексы с АСАТ. Затем добавляется фермент, окрашивающий эти комплексы. Оптическая плотность измеряется с помощью фотометра, по полученным показателям рассчитывается концентрация антител в крови. Подготовка результатов занимает до 5 рабочих дней.
Абсолютной нормой считается отсутствие антиспермальных антител в крови. Референсные значения анализа – от 0 до 54,99 МЕ/мл. Они одинаковы для мужчин и женщин. При интерпретации результатов учитывается, что наличие антиспермальных антител в крови у супругов не обязательно будет сопровождаться бесплодием, однако вероятность зачатия снижается. Верно и обратное – нормальные результаты теста на АСАТ не исключают бесплодия. Это заболевание относится к мультифакторным, диагностика причин предполагает использование комплекса лабораторных и инструментальных методов. Согласно статистике, лишь около 20% необъясненного бесплодия вызвано иммунологическими причинами.
Основная причина повышенного уровня антиспермальных антител в крови – бесплодие аутоиммунного характера у мужчин и иммунологическая несовместимость с партнером у женщин. Заболевание провоцируется повреждением или операциями на яичках, опухолями яичек, инфекциями и воспалениями в органах репродуктивной системы. При повышенных показателях анализа пациенту может быть назначено дополнительное обследование на воспалительные заболевания мочеполовой системы. Если диагноз подтверждается, то через две недели после окончания курса лечения тест на АСАТ выполняется повторно. Причиной повышения уровня антиспермальных антител в крови может стать искажение результатов на фоне аутоиммунного заболевания, поликлональной или моноклональной гаммапатии, иммунодефицита. Поэтому перед анализом выполняется сбор анамнеза, при необходимости назначается исследование иммунного статуса.
Если антиспермальные антитела в крови отсутствуют или их уровень низкий, значит, причиной бесплодия является не иммунологический конфликт. В таких случаях врач принимает решение о необходимости дальнейшего обследования – диагностики хромосомных патологий, несовместимости по системам крови и т. д. У мужчин причиной снижения уровня антиспермальных антител в крови при изначально повышенных показателях является успешность проводимой терапии.
Анализ крови на антиспермальные антитела используется для диагностики иммунологических причин бесплодия. Он назначается в рамках комплексного обследования, включающего в себя спермограмму, MAR-тест или тест на антиовариальные антитела. При повышенных показателях у мужчин подтверждается диагноз бесплодия аутоиммунного характера, у женщин определяется иммунологическая несовместимость с партнером. С результатами анализа нужно обратиться за консультацией к лечащему врачу – репродуктологу, урологу, гинекологу. Специалист определит необходимость дальнейшего обследования, подберет адекватную терапию, решит вопрос о целесообразности применения вспомогательных репродуктивных технологий.
источник
Работа репродуктивной системы человека во многом зависит от его иммунитета: клетки защиты играют важную роль в процессах овуляции и имплантации, во взаимодействии яйцеклетки и сперматозоида, а также в последующем развитии беременности. Иммунный фактор является причиной так называемого необъяснимого бесплодия у 20-30% пар, и в большинстве случаев причиной его становятся антиспермальные антитела, присутствующие в организме одного или обоих супругов.
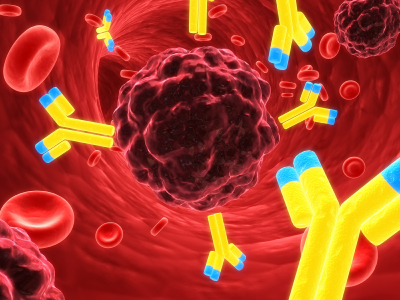
Антиспермальные антитела (или сокращенно АСАТ) — это вырабатываемые человеческой иммунной системой белки, негативно влияющие на сперматозоиды. По статистике, их обнаруживают в среднем в 15% случаев бесплодия у мужчин и в 32% случаев — у женщин.
АСАТ могут образовываться в разных отделах репродуктивного тракта мужчин и женщин, в разном количестве присутствовать в крови и разных секретах половой системы — в цервикальной слизи, эякуляте, фолликулярной или перитонеальной жидкости, воздействовать на разные части сперматозоида (головку, хвост, среднюю часть или комбинацию вариантов), и по-разному влиять на процессы репродукции.
Так, неблагоприятное действие АСАТ может состоять в:
- подавлении подвижности и снижении жизнеспособности сперматозоидов
- серьезных нарушениях сперматогенеза
- нарушении процесса проникновения мужских половых клеток в цервикальную слизь
- нарушении процесса оплодотворения и имплантации яйцеклетки
- подавлении роста и развития зародыша
Выработка организмом антиспермальных антител — это своего рода аллергия на сперму, причем появление этих белков у женщин говорит об иммунологической несовместимости супругов, а у мужчин — об аутоиммунном процессе, или борьбе мужского иммунитета с собственными клетками.
Иммунная система начинает формироваться еще во внутриутробном периоде, поэтому сперматозоиды, появляющиеся у мужчин лишь во время полового созревания, являются для нее «чужеродными». Однако умная природа заранее это предусмотрела и «разработала» определенные физиологические механизмы защиты половых клеток от иммунных:
-
гематотестикулярный барьер — это физический барьер из промежуточных клеток (так называемые клетки Сертоли) между сосудами и семенными канальцами, предотвращающий «встречу» иммунных клеток и сперматозоидов
- различные биологически активные вещества, вырабатываемые яичками и придаточными железами, тормозящие процесс активации иммунной системы,
- иммуноглобулин связывающий фактор, содержащийся в семенной жидкости, также препятствующий формированию иммунного ответа
Однако в некоторых случаях естественные механизмы нарушаются. И причинами этого могут стать:
- травмы и оперативные вмешательства на половых органах
- инфекционно-воспалительные процессы в семенных пузырьках, яичках, их придатках и простате (везикулит, простатит, орхоэпидидимит)
- анатомические изменения (крипторхизм, перекрут яичка, закупорка семявыносящих путей, паховая грыжа, варикоцеле)
Эти факторы способствуют проникновению в мужскую репродуктивную систему иммунных клеток, которые при встрече со сперматозоидами начинают активно «защищаться» и вырабатывать к ним антитела. АСАТ у мужчин могут формироваться в яичках, придатках яичек или в семявыносящих протоках.
В репродуктивной системе женщин, так же, как и в мужской, существуют природные механизмы, подавляющие иммунную «защиту» от сперматозоидов. Данные процессы в настоящее время плохо изучены, поэтому к ним предположительно относят:
- физиологическое снижение иммунитета в период овуляции
- блокирование местного иммунитета благодаря гибели сперматозоидов при прохождении их через половые пути
Однако наряду с подавляющими иммунитет факторами, существует ряд причин, активизирующими защитный ответ:
- инфекционно-воспалительные заболевания половых органов
- эндометриоз
- использование химических способов контрацепции
- большое количество лейкоцитов в сперме партнера
- попадание спермы в желудочно-кишечный тракт (оральные или анальные контакты)
- попадание сперматозоидов в брюшную полость (во время процедуры внутриматочной инсеминации)
- попадание «старых» сперматозоидов во влагалище при нерегулярных половых сношениях
- сперматозоиды с АСАТ
- лечение эрозии шейки матки при помощи коагуляции
- проведение в прошлом процедур ЭКО
- отягощенный аллергический анамнез
Иммунная реакция наиболее часто проявляется на уровне шейки матки, реже в этом принимают участие влагалище, эндометрий и маточные трубы. Это связано с наличием в цервикальном канале большого количества различных иммуноглобулинов, располагающих к развитию иммунологического бесплодия.
- исследование общего иммунного статуса (иммунограмма)
- анализ крови мужчин и женщин на АСАТ
- биологические пробы (посткоитальный тест, проба Курцрока–Миллера, перекрёстный пенетрационный тест, MAR-тест, изучение влагалищной слизи в зависимости от фазы менструального цикла и некоторые другие)
При выявлении антиспермальных антител лечение обычно направлено на снижение их титра с целью дальнейшего наступления беременности. Для этого могут применяться такие виды терапии:
- контрацептивная (длительное применение барьерной контрацепции для снижения титра АСАТ у женщин)
- плазмаферез
- искусственная инсеминация с предварительно обработанной от АСАТ спермой мужа
- ВРТ (наиболее успешный метод — ИКСИ в программе ЭКО)
Проблема иммунологического бесплодия, несмотря на многочисленные исследования и методы диагностики, до сих пор недостаточно изучена. Однако необходимо отметить, что выявление АСАТ у одного или даже у обоих супругов не позволяет исключить возможность самостоятельного наступления беременности, поскольку антитела снижают вероятность зачатия, но не во всех случаях этому препятствуют.
источник
Не все знают, что такое иммунология репродукции, и чем она занимается. Между тем, именно в этой области в последние годы были сделаны очень важные открытия, позволившие по-новому взглянуть на целый ряд нарушений репродуктивной функции и разработать новые эффективные методы лечения.
Предметом изучения иммунологии репродукции являются:
- нарушения иммунитета при гинекологических и андрологических заболеваниях, в том числе при хронических воспалительных процессах (снижение иммунитета как следствие и причина хронического течения воспалительных процессов);
- нарушения тканевого взаимодействия на всех этапах беременности, начиная с зачатия (взаимодействие сперматозоидов и яйцеклетки) и заканчивая родами и лактацией (беременность — это уникальный феномен дружественного сосуществования двух иммунологически разных организмов — матери и плода);
- аутоиммунные нарушения, приводящие к сбою в процессе созревания сперматозоидов и яйцеклетки, оплодотворения и развития беременности на всех сроках (например, повышенный уровень антиспермальных антител, антител к фосфолипидам, компонентам щитовидной железы);
- особенности течения беременности и родов при аутоиммунных заболеваниях (ревматизм, системная красная волчанка, бронхиальная астма);
- резус-конфликтная беременность;
- влияние иммунного статуса матери на формирование функциональных систем плода (пример: влияние антител к фактору роста нервов в крови матери на вероятность развития осложнений во время беременности) предрасположенности к нейро-психическим заболеваниям у детей);
- вопросы иммунокоррегирующего лечения при вирусных заболеваниях в акушерстве, гинекологии и андрологии;
- вопросы специфической и неспецифической профилактики развития инфекционных заболеваний в процессе подготовки к беременности и родам.
И это далеко не все. Нет ни одного процесса в организме, в котором так или иначе не участвовали бы иммунные факторы.
Антиспермальные антитела — это антитела к антигенам мембраны сперматозоидов
Впервые антиспермальные антитела в сыворотке бесплодных мужчин описали Rumke и Wilson в 1954 г.
Антиспермальные антитела обнаруживаются: в сыворотке крови, цервикальной слизи, семенной плазме, на поверхности сперматозоидов.
Чаще всего это антитела класса G, реже IgA и IgM.
Антиспермальные антитела обнаруживаются у здоровых мужчин (1-10%), у мужчин с бесплодием (15-22%), при этом в высоком титре всего у 6-7% и у бесплодных женщин.
Антиспермальные антитела в процессе сперматогенеза появляются на стадии сперматоцитов первого порядка, причем уровень их экспрессии увеличивается по мере развития сперматозоидов, они обладают свойством аутоантигенности, т.е. иммунологически чужеродны в собственном организме. У здоровых мужчин сперматозоиды, находящиеся в придатке яичка (эпидидимисе), подвергаются фагоцитозу, если не наступает эякуляция. Однако это не связано с появлением антиспермальных антител, что, возможно, обусловлено:
- иммунологической толерантностью, вызванной резорбцией сперматозоидов;
- блокадой образования антиспермальных антител другими антителами;
- индивидуальными особенностями антителообразования.
Образованию антиспермальных антител в разных отделах мужской репродуктивной системы препятствуют различные механизмы. Так, в яичке защиту сперматозоидов и клеток сперматогенеза осуществляет гематотестикулярный барьер (ГТБ), который изолирует клетки сперматогенеза от иммунокомпетентных клеток организма. Основу этого барьера составляют клетки Сертоли и их отростки. После выхода сперматозоида из яичка действует другой механизм защиты: способность сперматозоидов мимикрировать (приспосабливаться) к окружающей среде, т. е. сбрасывать с оболочки ранее сорбированные антигены и адсорбировать новые — из других сред, в том числе и из женского репродуктивного тракта. Эта способность сильнее выражена у жизнеспособных спермиев. Кроме того, в спермоплазме содержатся местные регуляторные факторы, препятствующие образованию антиспермальных антител и развитию клеточной антиспермальной сенсибилизации (например, иммуносупрессивный фактор спермоплазмы). Эти факторы секретируются в придаточных железах мужской репродуктивной системы.
Сбой механизмов защиты на любом уровне приводит к появлению антиспермальных антител. Так, повреждение ГТБ открывает для иммунной системы доступ к ткани яичка, являющейся носителем антигенов, к которым в организме не выработана иммунологическая толерантность. Чаще всего гематотестикулярный барьер повреждается в области сплетения и семявыносящих канальцев. Лимфоциты вызывают первичное повреждение, способствующее проникновению цитотоксических антител и комплемента. Деструкция в системе семявыносящих протоков ведет к вторичным иммунным поражениям в пределах семенных канальцев, вовлекающим клеточно-специфические антигены на всех стадиях сперматогенеза и появление антиспермальных антител. Это экспериментальная модель, которая имеет свои аналоги в клинике. Например, хирургические вмешательства, травмы мошонки, воспалительные заболевания мужской репродуктивной системы различной этиологии часто приводят к нарушению целостности ГТБ и развитию аутоиммунитета к антигенам сперматозоидов
Недостаточность механизма мимикрии приводит к контакту спермальных антигенов с иммунной системой и выработке антиспермальных антител как в мужском, так и женском организме. Нарушения процессов сперматогенеза (в яичке) или функционального созревания спермиев (в эпидидимисе), вызванные различными причинами (воспалительные заболевания, варикоцеле, крипторхизм, эндокринная патология) приводят к снижению жизнеспособности сперматозоидов и нарушению механизма мимикрии.
Половые органы женщины содержат большое количество иммунокомпетентных клеток. Естественное попадание спермы в половые пути женщины может вызвать иммунный ответ. Однако иммунологические процессы, происходящие в женском организме после попадания спермы, недостаточно изучены. Образованию антител в женском организме препятствуют различные механизмы, снижающие иммунный ответ. В период овуляции изменяется баланс Т-лимфоцитов: уровень Т-хелперов снижается, а Т-супрессоров повышается, а так же уменьшается концентрация иммуноглобулинов и С3 компонента системы комплемента. Важную роль в снижении иммунного ответа на сперматозоиды играют мужские механизмы защиты: мимикрия — сорбция и десоробция поверхностных антигенов при смене сред и иммуносупрессивный фактор спермоплазмы. Кроме того, предполагается, что в маточные трубы попадает только небольшое число генетически отобранных сперматозоидов, иммунологически отличающихся от большинства, остальные же погибают, блокируя местный иммунитет.
Нарушение фертильности сопровождается нарушением защитных механизмов и появлением антиспермальных антител. Выработку антиспермальных антител в женском организме стимулирует дополнительное воздействие других изоантигенов, получающих доступ в половые пути женщины, так иммунный ответ на антигены сперматозоидов может повышаться при воспалительных заболеваниях влагалища. Изоиммунный ответ на сперматозоиды может реализовываться через антитела или клеточно-опосредованные механизмы, каждый из которых оказывает чаще всего местный эффект.
Шейка матки является наиболее благоприятным и важным местом проявления местного иммунитета. Часто антиспермальные антитела обнаруживаются только в цервикальной жидкости и не определяются в сыворотке крови. Однако необходимо помнить, что гиперчувствительность замедленного типа к сперме и спермиммобилизирующие антитела могут встречаться и у здоровых женщин, имеющих регулярные половые сношения.
В литературе нет однозначного мнения о влиянии антиспермальных антител на качество эякулята. По мнению одних авторов — наличие антиспермальных антител не влияет на подвижность и другие морфологические характеристики качества спермы, другие считают, что антиспермальные антитела вызывают снижение скорости движения и жизнеспособности спермиев. Предполагается, что антиспермальные антитела могут нарушать функциональную целостность мембраны сперматозоидов. У мужчин с антиспермальными антителами часто наблюдается снижение показателей теста гипоосмотического набухания сперматозоидов, который сочетается со снижением оплодотворяющей способности эякулята. Сниженный тест гипоосмотического набухания сперматозоидов выявляется как у мужчин с нормальными, так и субнормальными показателями спермограммы. Антиспермальные антитела могут оказывать повреждающее действие на функцию предстательной железы, в частности на простасомы, органеллы, секретируемые ацинарными клетками предстательной железы. Антиспермальные антитела классов IgG и IgА цервикальной слизи и других жидкостей женского репродуктивного тракта препятствуют продвижению сперматозоидов и их пенетрации через цервикальную слизь, блокируют рецепторные участки на головке сперматозоида, ответственные за связывание с блестящей оболочкой яйцеклетки
Кроме того, антиспермальные антитела нарушают процесс капацитации сперматозоидов, воздействуют на акросомальную реакцию, блокируя экзоцитоз кортикальных гранул.
Всемирная Организация Здравоохранения рекомендует включать тест на определение антиспермальных антител в каждое исследование эякулята (спермограмму).
Отрицательный посткоитальный тест дает обоснованные указания на наличие антиспермальных антител либо в сперме, либо в цервикальной слизи.
Для супружеских пар с отрицательным посткоитальным тестом исследование антиспермальных антител является обязательным.
В настоящее время существует множество методик для определения антиспермальных антител. Наиболее простым и информативным является смешанный антиглобулиновый тест (MAR-test), рекомендованный ВОЗ для рутинного скрининга образцов семенной жидкости.
Его преимуществами являются простота определения, возможность выявления антиспермальных антител на подвижных сперматозоидах.
Тест выполняется на предметном стекле, на которое наносят одну каплю свежей спермы, одну каплю латексных частичек, покрытых IgА, затем одну каплю антисыворотки к человеческому IgG, перемешивают, смесь накрывают покровным стеклом и просматривают под микроскопом с увеличением 400х или 600х.
Если сперматозоиды не покрыты антителами, то они свободно плавают между частицами, если же сперматозоиды покрыты антителами, то они, перемещаясь, притягивают к себе частицы латекса и склеиваются с ними. Высчитывают % сперматозоидов, склеенных с латексными частицами, покрытыми IgG (это вполне исчерпывающее исследование, т. к. установлено, что IgА практически всегда появляются вместе с IgG).
Альтернативой этому тесту может служить определение антиспермальных антител методом латексной агглютинации. Этот тест не применим для выявления количества подвижных сперматозоидов, покрытых антиспермальными антителами, зато он информативен при низких показателях подвижности сперматозоидов, а также для выявления антиспермальных антител в цервикальной слизи.
Образцы для этого теста можно замораживать. Семенную жидкость или цервикальную слизь разводят буфером, центрифугируют, из надосадочной жидкости готовят разведения 1:100, 1:200 и т.д. На специальный планшет добавляют соответственные разведения образца и латексные частицы, затем оценивают появление агглютинации.
Если она появляется в разведении 1:100, тест считается положительным.
Для определения антиспермальных антител в сыворотке крови используются наборы на основе метода непрямого твердофазного иммуноферментного анализа.
Образцы разводят и помещают в микропланшет, ячейки которого покрыты смесью белков, способных взаимодействовать с антителами, антиспермальные антитела, находящиеся в образце связываются с этими белками и после определенной последовательности действий измеряется оптическая плотность содержимого ячеек, которая пропорциональна концентрации антиспермальных антител.
Нормальные значения: 0-60 Ед/мл; Промежуточные значения: 61-100 Ед/мл; Повышенные: более 100 Ед/мл.
Существуют и другие, менее распространенные методы определения антиспермальных антител: проточная цитометрия (определение антиспермальных антител и их концентрации на мембране сперматозоидов), радиоиммунный, иммунофлуоресценция и др.
Бесплодие, невынашивание, привычный выкидыш — эти печальные проблемы не всегда связаны с организмом женщины.
По статистике, 10 — 15 процентов всех беременностей оканчивается выкидышем. Вы можете о нем не знать — крошечный эмбрион погибает еще до наступления месячных. Та же картина с искусственным оплодотворением (ЭКО): заместительной гормонотерапией организм матери подготовился идеально, только расти, малыш! Однако показатели успешно развивающейся беременности по-прежнему топчутся на 10 — 15 процентах. В чем же дело?
Невынашивание, как и бесплодие, — не какая-то отдельная болезнь. Это следствие неполадок и в репродуктивной системе, и вообще в организме будущих матери и отца. Это симптом: нормальное развитие плода под угрозой, а потому жизнь его невозможна. Причин тут несколько.
Беременность — уникальное явление: девять месяцев сосуществуют два абсолютно разных организма — матери и плода. Ведь лишь наполовину ребенок наследует материнские клетки — остальные белки и гены отцовские, чужие. Взаимодействие двух организмов обеспечивают белки тканевой совместимости — это как бы маркеры на клетках, с помощью которых иммунная система женщины распознает своих и чужих.
Вне беременности иммунные клетки, циркулирующие в организме как разведчики, выслеживают на поверхности всех без исключения клеток белковый код — белки тканевой совместимости. И если обнаруживаются клетки с измененной структурой (это занесенные микробы или измененные клетки самого организма), организм немедленно выдает иммунный ответ — атипические клетки уничтожаются. Кстати, это ключевой момент в развитии онкозаболеваний, и вопросы повышения иммунитета у врачей-онкологов едва ли не на первом месте.
При беременности, если бы процесс был таким однозначным, плод неизбежно погибал бы — внутри «чужие» клетки! Но во время беременности плод и его клеточные структуры неразличимы для иммунной системы материнского организма. Иначе — существует биобарьер на пути клеток-бойцов за иммунологическое единообразие, и беременность развивается и оканчивается счастливо.
Однако современные исследования выявили — барьер этот мнимый: либо гуморальный иммунитет матери включается, и вырабатываются антитела на факторы плода, либо клеточный — клетки не довольны пришельцами, и иммунный ответ следует незамедлительно — отторжение (выкидыш).
Но все не так однозначно — так же, как функциям всех органов свойственны возбуждение и торможение, так и в иммунной системе может включаться и активное отторжение, и иммунологическая толерантность (совместимость). Она-то и позволяет сохранить трансплантат — именно так рассматривают будущего ребенка иммунологи. Эта дилемма иммунной системы определяет причины невынашивания, что выражается или в сбоях иммунной регуляции организма, или в нарушениях иммунологического взаимодействия между организмами матери и плода.
Лишь к концу 80-х годов ученые вплотную подошли к решению проблем невынашивания, и возникло новое направление на стыке акушерства, гинекологии и перинатологии — иммунология репродукции. И хотя теория накопила немало ценной информации, буквально рвущейся к практике, ввести в лечебный обиход новые знания пока сложно — тормозят дело буквальное отсутствие средств и организация обследования пациенток. По крайней мере, в нашей стране.
А между тем практическая помощь оказывается все успешнее. По всем группам иммунных нарушений. Например, аутоиммунные нарушения матери. При этом в организме женщины появляются антитела, похожие на антитела при таких заболеваниях, как ревматизм, заболевания почек и мышечной системы, аллергические реакции, системная красная волчанка. В организме возникают извращенные иммунные реакции, когда антитела (белки) направлены против собственных тканей. Провоцирует их активность плохая наследственность или тяжелые инфекции, и в таких случаях беременность под угрозой.
Однако специальный анализ крови может вовремя определить сбой, суть которого — нарушение кровообращения в мелких сосудах плаценты — оболочки зарождающейся жизни. Этот микротромбоз можно распознать и лечить на самых ранних сроках, и тогда беременность не прерывается и развивается по всем физиологическим законам до конца. Этот путь перспективен, что доказывает простое уравнение: чем выше уровень антител (по-научному они называются антифосфолипиды), тем вероятнее выкидыш — более 80 процентов. А при своевременном назначении специального лечения, направленного на снижение свертываемости крови, вероятность донашивания беременности составляет тоже 80 процентов!
Успех определяется воздействием не на причину, а следствие — разжижая кровь аспирином, мы восстанавливаем нормальное кровообращение между матерью и плодом. Кстати, раньше, лет десять назад аспирин применялся в неоправданно больших дозах, что нередко приводило к нарушениям питания мозга и нервной системы ребенка. Сегодня такие аномалии исключены — аспирин берется в дозах, в 10 — 15 раз меньших, чем стандартная норма. Для усиления аспиринового эффекта применяют гепарин — это естественное вещество редко вызывает аллергические реакции, не проходит через плаценту, так что какие-либо воздействия на плод невозможны, а эффект полезного аспирина удваивается.
Еще одна причина невынашивоемости — антитела, направленные на клеточные ядра. Опасность тут возрастает потому, что они легко проникают через плаценту и составляют угрозу для клеток плода. И такие нарушения можно диагностировать на ранних сроках и успешно лечить.
Гораздо сложнее бороться с аллоиммунными нарушениями — тут речь о взаимоотношениях матери и плода как части отцовского организма. Чтобы беременность успешно развивалась, она должна быть распознана и признана иммунной системой матери. Если же материнские клетки вяло, неохотно реагируют на вновь прибывших — это белки, унаследованные от отца, — реакция совместимости задерживается, и даже может пропустить сигнал отторжения — чужое! И снова несостоявшаяся беременность.
Самое печальное, что это стойкий механизм: выкидыши подряд в такой ситуации — частое явление. Но есть специальные тесты, позволяющие распознавать сходства и различия между организмом матери и плода. Если реакция на плод замедленная (это можно определить по уровню антител в крови), то специальным образом можно провести иммунизацию матери лимфоцитами отца.
HLA — human leucocyte antigens — антигены тканевой совместимости. (cиноним: MHC — major histocompatibility complex — главный комплекс гистосовместимости). На поверхности практически всех клеток организма представлены молекулы (белки), которые носят название антигенов главного комплекса гистосовместимости (HLA — антигены). Название HLA — антигены было дано в связи с тем, что эти молекулы наиболее полно представлены именно на поверхности лейкоцитов (клетки крови). Каждый человек обладает индивидуальным набором HLA — антигенов.
Молекулы HLA выполняют роль своеобразных «антенн» на поверхности клеток, позволяющих организму распознавать собственные и чужие клетки (бактерии, вирусы, раковые клетки и т.д.) и при необходимости запускать иммунный ответ, обеспечивающий выработку специфических антител и удаление чужеродного агента из организма. Синтез белков HLA — системы определяется генами главного комплекса гистосовместимости, которые расположены на коротком плече 6-й хромосомы. Выделяют два основных класса генов главного комплекса гистосовместимости:
- I класс включает гены локусов А, В, С;
- II класс — D-область (сублокусы DR, DP, DQ).
HLA антигены I класса представлены на поверхности практически всех клеток организма, в то время, как белки тканевой совместимости II класса выражены преимущественно на клетках иммунной системы, макрофагах, эпителиальных клетках.
Антигены тканевой совместимости участвуют в распознавании чужеродной ткани и формировании иммунного ответа. HLA — фенотип обязательно учитывается при подборе донора для процедуры трансплантации. Благоприятный прогноз пересадки органа выше при наибольшем сходстве донора и реципиента по антигенам тканевой совместимости. Доказана взаимосвязь между HLA-антигенами и предрасположенностью к ряду заболеваний. Так, практически у 85% больных анкилозирующим спондилитом и синдромом Рейтера выявлен HLA В27 антиген. Более, чем у 95% больных инсулинозависимым сахарным диабетом определяются HLA DR3, DR4 антигены.
При наследовании антигенов тканевой совместимости ребенок получает по одному гену каждого локуса от обоих родителей, т.е. половина антигенов тканевой совместимости наследуется от матери и половина от отца. Таким образом, ребенок является наполовину чужеродным для организма матери. Эта «чужеродность» является нормальным физиологическим явлением, запускающим иммунологические реакции, направленные на сохранение беременности. Формируется клон иммунных клеток, вырабатывающий специальные «защитные» (блокирующие) антитела.
Несовместимость супругов по HLA-антигенам и отличие зародыша от материнского организма является важным моментом, необходимым для сохранения и вынашивания беременности. При нормальном развитии беременности «блокирующие» антитела к отцовским антигенам появляются с самых ранних сроков беременности. Причем, самыми ранними являются антитела к антигенам II класса гистосовместимости.
Сходство супругов по антигенам тканевой совместимости приводит к «похожести» зародыша на организм матери, что становится причиной недостаточной антигенной стимуляции иммунной системы женщины, и необходимые для сохранения беременности реакции не запускаются. Беременность воспринимается, как чужеродные клетки. В таком случае происходит самопроизвольное прерывание беременности.
Для определения антигенов тканевой совместимости у супругов проводится HLA-типирование. Для проведения анализа берется кровь из вены, и из полученного образца выделяют лейкоциты (клетки крови, на поверхности которых наиболее широко представлены антигены тканевой совместимости). HLA-фенотип определяется методом цепной полимеразной реакции.
Вопрос о роли антиспермальных антител (АсАт) в бесплодии и репродуктивных потерях обсуждается в литературе с начала 80-х годов. В физиологических условиях АсАт не формируются, прежде всего благодаря существованию супрессорных (подавляющих их активность) механизмов как в сперме, так и в репродуктивном тракте женщины.
К нарушению физиологической супрессии антигенов спермы могут приводить воспалительные заболевания женского полового тракта, как клинически проявляющиеся, так и с бессимптомным течением. Показано, что у женщин с сексуально-трансмиссивными болезнями (болезни передающиеся половым путем) частота выявления АсАт выше, чем у здоровых женщин. Антиспермальные антитела у женщин могут быть обнаружены во всех отделах репродуктивной системы от влагалища до фолликулярной жидкости и в крови. При этом отмечено, что наличие циркулирующих в крови АсАт не всегда связано с наличием антител в репродуктивном тракте.
Повреждающие эффекты их многообразны и могут быть разделены на две группы:
- Эффекты, непосредственно оказывающие влияние на процесс оплодотворения, заключаются в подавлении миграции сперматозоидов через цервикальный канал (этим и объясняется цервикальный фактор), нарушении поступательно-прогрессивного движения сперматозоидов и их гибели в репродуктивном тракте женщины, блокировании прикрепления и проникновения сперматозоида в яйцеклетку и др.
- Эффекты, оказывающие негативное влияние уже после оплодотворения яйцеклетки сперматозоидом: нарушение дробления и нормального развития эмбрионов (зародыша), прямое отрицательное действие на жизнеспособность развивающегося эмбриона.
Для нейтрализации АсАт применяются разные методы. Одним из них является внутривенное введение гаммаглобулина, которое в последние годы широко используется за рубежом для коррекции различных аутоиммунных состояний. Однако высокая стоимость этого метода ограничивает его использование у нас в стране.
Альтернативным и доступным способом лечения является иммуноцитотерапия аллогенными лейкоцитами. В течение последних 20-ти лет иммуноцитотерапия успешно используется для профилактики и лечения привычных спонтанных абортов.
Качественное обследование может быть обеспечено в специализированных центрах, каковыми являются, в частности, центры планирования семьи и репродукции, которые есть в большинстве регионов России.
02.09.2008
к.м.н. Б. Каменецкий
врач акушер-гинеколог Российско-Финского Центра «АВА-ПЕТЕР»,
г.Санкт-Петербург.
Материал собран Софией
источник







 гематотестикулярный барьер — это физический барьер из промежуточных клеток (так называемые клетки Сертоли) между сосудами и семенными канальцами, предотвращающий «встречу» иммунных клеток и сперматозоидов
гематотестикулярный барьер — это физический барьер из промежуточных клеток (так называемые клетки Сертоли) между сосудами и семенными канальцами, предотвращающий «встречу» иммунных клеток и сперматозоидов