Еще один вид бесплодия это иммунологическое бесплодие. Такое бесплодие связано с выработкой, как у мужчин, так и у женщин, антиспермальных антител. Так иммунная система человека влияет на работу репродуктивной функции. Заболевание это никак не проявляется и не имеет симптомов, кроме отсутствия возможности зачать ребенка.
Иммунологическое бесплодие – это заболевание при котором у пары отсутствуют заболевания мочеполовой системы а забеременеть не получается. Точно установить причину патологии проблематично.
Еще недавно ученые были уверены, что такое бесплодие может быть только у женщины. Проявляется это заболевание у женщины так, иммунные клетки которые должны отвечать за овуляцию просто не воспринимают сперматозоиды определенного мужчины. Иммунитет женщины принимает сперматозоиды как инородный объект и отторгает их. Поэтому оплодотворение яйцеклетки не происходит.
На сегодняшний день, в результате исследований, удалось доказать, что и иммунитет мужчины способен вырабатывать антиспермальные антитела. Таким образом, яички мужчины могут просто не воспринимать женскую фолликулярную жидкость, и даже собственные биологические компоненты. Такой процесс называется аутоиммунизацией.
При аутоиммунизации у мужчины, в организме происходит сопротивление между собственными биологическими материалами и антителами. Иммунные клетки, которые находятся в яичках, производят антитела. Антитела воспринимают биологический материал как инородный объект. В результате сопротивления с собственными антителами сперматозоиды просто склеиваются между собой, значительно снижая качество спермы. Способность мужчины к оплодотворению, в этом случае, также существенно снижается.
Самым основным признаком иммунологического бесплодия является отсутствие наступления беременности при нормальном качестве спермы у мужчины и нормальной работы репродуктивных органов у женщины.
Главная причина такого бесплодия на сегодняшний день неизвестна. Врачи говорят о наследственности и индивидуальной особенности человека, как об основной причине иммунологического бесплодия.
Особенности иммунного фактора бесплодия:
- Аутоиммунизация.
- Антитела.
- Сильная чувствительность женской иммунной системы к сперме конкретного мужчины. В этом случае, женские антитела уничтожают сперматозоиды, воспринимая их, как инородный объект.
По статистике, чаще такое бесплодие встречается у мужчин при наличии заболеваний и травм органов мошонки. Например: орхит, водянка, травмы яичек, варикоцеле, застой спермы или киста семенного канатика.

Определить степень иммунологического бесплодия можно с помощью спермограммы с MAR тестом (анализа спермы). В анализе будут приведены показатели титра АСАТ и класса IgG, IgA, IgM. Также в анализе будет показан уровень возникновения иммунной реакции и места фиксации сперматозоидов. Подробнее о том, как сдавать и расшифровывать результаты этого анализа читайте в этой статье.
Видео из лаборатории о спермограмме с MAR тестом:
По причине иммунологического бесплодия от 6 до 22% пар не могут зачать ребенка. Если в течение года попыток забеременеть результата нет, то одной из возможных причин бесплодия может быть именно нарушения связанные с иммунитетом родителей, одного или двух. Бывает, что при таком бесплодии беременность наступает, но очень высока вероятность выкидыша на ранних сроках.

Одним из методов выявления этого заболевания является посткоитальный тест. Пред сдачей этого теста нужно чтобы мужчина уже прошел свое тестирование (спермограмму). Если по результатам спермограммы будет понятно, что мужчина здоров, то назначается посткоитальный тест.
Его сдает женщина на 14 день начала цикла менструации. Для теста на исследование берут цервикальную жидкость. Перед сдачей теста пара должна воздерживаться три дня от половой близости. Сам тест сдается спустя 10 часов после полового акта, но не дольше одних суток (24 часа). По результату исследований будет ясно, есть ли в фолликулярной слизи сперматозоиды. Если они присутствуют, будет определена их активность.

Помимо посткоитального теста иммунологическое бесплодие можно определить дополнительными исследованиями, которые в себя включают:
- метод латексной агглютинации;
- смешанный антиглобулиновый тест;
- с помощью иммуноферментного анализа;
- при помощи пенетрационного теста.
Также для установления диагноза и определения уровня АСАТ (антиспермальных антител) нужно дополнительно сдать фолликулярную жидкость и кровь.
Полезное и интересное видео:
В связи со сложностью определения точных причин такого бесплодия назначение лечения очень проблематично. Лечение включает в себя несколько способов: хирургическое вмешательство, иммуностимулирующие и андрогенные препараты.
Помимо вышеперечисленных способов лечения, дополнительно назначаются антибиотики, антигистаминные препараты и противовоспалительные средства. Чтобы исключить случайное зачатие в период действия сильнодействующих препаратов пара во время полового акта обязана использовать презерватив для контрацепции.
Время курса лечения иммунологического бесплодия составляет от полугода до 8 месяцев. В результате лечения чувствительность организма к спермальным антигенам снижается, вероятность зачатия увеличивается.
За три дня до овуляции женщине назначаются препараты для повышения уровня эстрогена. Иногда назначается курс гормональных препаратов а также кортикостероиды.
Иммунологическое бесплодие поддается лечению при помощи инсеминации (исскуственного ввода спермы в женский организм). ЭКО (экстракорпоральное оплодотворение) – это еще один действенный метод зачатия ребенка при иммунологическом бесплодии. В этом случае оплодотворение яйцеклетки происходит в специальной среде вне женского организма. После оплодотворения производится подсадка змбриона в полость матки.
Многие семейные пары пытаются лечить иммунологическое бесплодие способами и рецептами народной медицины. Обязательно проконсультируйтесь у врача, не стоит заниматься самолечением.
Если у семейной пары не получается зачать ребенка в течение года это серьезная проблема, возможно это иммунологическое бесплодие. Чтобы добиться появления ребенка на свет не стоит пускать ситуацию на самотек, нужно обязательно обратиться к врачу.
Не забывайте писать комментарии и ставить оценку статье звездочками. Спасибо за посещение сайта, надеемся мы смогли вам помочь.
источник
НЕСОВМЕСТИМОСТЬ ПОЛОВЫХ ПАРТНЕРОВ. ПОСТКОИТАЛЬНЫЙ ТЕСТ.
Бывают такие ситуации, когда в результате обследования у половых партнёров не выявлено никакой патологии, и зачатия не происходит. В таких случаях следует заподозрить несовместимость половых партнёров — иммунологическое бесплодие.
Этот термин определяет состояние, когда иммунная система организма женщины вырабатывает антитела к сперматозоидам, в следствии чего они теряют подвижность и гибнут.
Антитела к сперматозоидам (АсАт) могут вырабатываться, как у женщины, так и у мужчины. Если вам назначают исследование антиспермальных антител, уточните у врача – у кого из супругов подозревается наличие антиспермальных антител и в связи с чем. Просто так ни с того, ни с сего они не вырабатываются.
В случае, когда антиспермальные антитела (АсАт) вырабатываться у мужчины, к своим же сперматозоидам, то говорят об аутоиммунном бесплодии. В спермограмме будет низкий процент подвижных сперматозоидов, или они вообще будут отсутствовать. Такая ситуация является показанием к проведению MAR-Теста.
Если антиспермальные антитела (АсАт), вырабатываются у женщины, то говорят об иммунологической несовместимости супругов. Выявляется оно с помощью проведения посткоитального теста или его модификаций, пробы Шуварского или пробы Курцрока-Миллера. Смысл обследования, выяснить, как взаимодействует цервикальная слизь — секрет слизистой канала шейки матки, со сперматозоидами.
Качество и количество цервикальной слизи в течении менструального цикла не постоянно. В середине цикла, когда в яичнике созревает яйцеклетка и происходит овуляция, цервикальная слизь секретируется в большом количестве, имеет водянистую консистенцию, прозрачный вид и легко растягивается.
Повышение секреции связано с уровнем эстрогенов, в период овуляции он самый высокий. Такое состояние продолжается несколько дней, 2-3 дня до и 1-2 дня после овуляции. Женщины с эктопией шейки матки, в эти дни могут отмечать, характерного вида, слизистые выделения из влагалища.
Большое количество и водянистая консистенция цервикального секрета способствуют лёгкому продвижению сперматозоидов из влагалища в полость матки. В остальные дни менструального цикла, слизи в цервикальном канале мало, она густая и вязкая, что напротив, препятствует продвижению сперматозоидов. Эту особенность важно учитывать, так как несвоевременно проведённый посткоитальный тест может давать ложно отрицательный результат.
- Создаёт условия для лёгкого продвижения сперматозоидов из влагалища в матку.
- На основании подвижности и строения, осуществляет качественный отбор здоровых и выбраковка патологических форм сперматозоидов.
- Она является временным резервуаром сперматозоидов, обеспечивая период зачатия достаточным количеством качественных половых клеток.
- Цервикальная слизь является инкубатором для сперматозоидов, обеспечивает их питанием, делая их ещё более подвижными, защищает от «агрессивной» среды влагалища. Именно в цервикальной слизи сперматозоиды, как бы дозревают и подготавливаются к оплодотворению.
Можно сказать, что шейка матки в период овуляции, это своеобразный «спермадром«. Нарушения перечисленных функций возникают при воспалительных, инфекционных процессах в шейке матки и при иммунологической несовместимости супругов.
Посткоитальный тест, или тест на совместимость, требует строго соблюдения правил его проведения, т.к. достоверность результата зависит от очень многих факторов. Однократный отрицательный ПКТ не является достоверным признаком шеечного бесплодия, поскольку может быть следствием несоблюдения правил его выполнения. В классическом варианте — это исследование проводится спустя 9-24 ч. после полового акта (рекомендация ВОЗ).
Супружеская пара должна воздерживаться от половой близости 3-5 дней. Половой акт должен состоятся в наиболее вероятное время ожидаемой овуляции и быть не защищённым. Дату лучше высчитать вместе с гинекологом. Как перед, так и после полового акта, во время гигиенического туалета, женщина не должна пользоваться мылом и мыльными растворами. Так же запрещается использование влагалищных форм лекарственных препаратов и смазки для секса. После полового акта, женщине рекомендуется оставаться в лежачем положении с приподнятым тазовым концом (можно подложить под ягодицы подушку) в течении 30 минут, не следует принимать ванну.
Соблюдая все вышеперечисленные рекомендации, через 9-24ч., женщина приходит в клинику для проведения теста. Во время проведения обычного осмотра на гинекологическом кресле, врач, специальной пипеткой, собирает слизь из цервикального канала и изучает её под микроскопом. Оценивается количество и подвижность сперматозоидов в цервикальной слизи.
Результат посткоитального теста расценивается, как положительный — если в шеечной слизи обнаруживаются живые (подвижные) сперматозоиды, и отрицательный — если подвижные сперматозоиды не выявляются.
Можно избавиться от ряда правил если провести посткоитальный тест в искусственных условиях. Пробы Курцрока-Миллера и Кремера доступны для большинства лабораторий. В начале мужу проводится спермограмма, после чего сперма смешиваются с уже исследованной цервикальной слизью жены. Далее осуществляется динамическое наблюдение за сперматозоидами.
Гибель сперматозоидов, с высокой долей вероятности, говорит об иммунологическом бесплодии. В данном случае, фактором иммунологического бесплодия является наличие антиспермальных антител в шеечной слизи, т.е. у женщины.
Лечением иммунологического бесплодия занимаются доктора, прошедшие специализированное обучение.
АсАт повреждают сперматозоиды на всем пути движения их к яйцеклетке. Они нарушают дробление и нормальное развитие зародыша, а так же снижают жизнеспособность развивающегося эмбриона. Поскольку антиспермальные антитела обнаруживаются во всех отделах полового тракта, встаёт резонный вопрос о целесообразности такого метода лечения иммунологического бесплодия, как инсеминация.
Лечение иммунологической несовместимости направлено на снижение количества антиспермальных антител. Назначается барьерная контрацепция (презерватив) на 3-6 мес., так устраняется контакт женского организма со спермой мужа и, как следствие снижается выработка аниспермальных антител в организме женщины.
В общей схеме лечения используются препараты снижающие вязкость шеечной слизи (гуайфенезин), препараты подавляющие выработку АсАт, плазмофорез. При неэффективности консервативной терапии проводится ЭКО.
источник
Функционирование человеческого организма было бы невозможным без иммунной системы. Иммунитет защищает человека от мелких и крупных опасностей, порой не отличая настоящего врага от обычной клетки. Организм способен избавляться даже от собственных тканей, которые перестали выполнять свои функции. Один из ярких примеров – рак, который является клетками, что стали размножаться сверх меры. В этой статье рассмотрим понятие — иммунологическое бесплодие.
Иммунитет состоит из клеток, которые способны распознавать чужеродные элементы и уничтожать их. В процессе участвуют также антитела. Они возникают в организме после контакта с раздражителем, чтобы в будущем бороться с ним эффективнее. Антитела для каждого паразита индивидуальны. Некоторые распознают только конкретную болезнь, другие атакую все чужеродные объекты.
В иммунной системе еще есть антигены. Они отвечают за разделение родных и чужеродных клеток. Главный комплекс антигенов называют лейкоцитарным. Все клетки, имеющиеся на момент рождения, воспринимаются организмом родными, поэтому они не провоцируют защитную реакцию. Все отличные элементы будут чужеродными: паразиты, гельминты, собственные зараженные или аномально трансформированные ткани. Для мужчин чужеродными будут даже собственные половые клетки, так как они отделены от крови природным барьером, и контакт спермы с антителами будет губительным. Женский организм располагает функциями, которые позволяют ослабить воздействие антител на чужеродные половые клетки, но иногда эти функции выходят из стоя, иммунитет принимается уничтожать сперматозоиды, а порой и сам плод.
Некоторые клетки организма никогда не соединяются с иммунными, поэтому при внезапном контакте защита организма нападает на неизвестные, хоть и свои элементы. Так нейроны в головном мозге и сперматозоиды в яичках отделены от иммунитета. Существует разделение между тканями мозга и непосредственно кровью, как и тканями яичника. Это связано с тем, что некоторые белковые структуры отсутствуют при рождении, когда иммунитет запоминает родные клетки. Сперма начинает вырабатываться только в 11-13 лет, поэтому иммунитет будет ее атаковать. Во избежание этого спермиогенез происходит в сперматогенных канальцах, которые фильтруют кислород и необходимые вещества, но предотвращают контакт с кровью.
Иммунологическое бесплодие — состояние, при котором пара не имеет возможности зачать ребенка из-за агрессивного воздействия антиспермальных антител на сперматозоиды. Антитела являются иммуноглобулинами (белками), которые вырабатываются иммунной системой человека, и призваны атаковать чужеродные объекты.
Иммунологические факторы не позволяют зачать ребенка в среднем 10% бесплодных пар. Антиспермальные антитела, которые запускаю процесс уничтожения половых клеток, обнаруживаются у обоих полов (15% диагностирования у мужчин и 32% у женщин). Антитела могут содержаться в крови, а также другой среде (сперма, фолликулярная жидкость, цервикальная слизь и прочее).
Мужской организм способен вырабатывать антиспермальные антитела в крови или сперме для разрушения половых клеток. Женский организм производит антитела для уничтожения или парализации сперматозоидов. У женщин антитела находятся в крови и цервикальной слизи влагалища. Бывает, что антиспермальные антитела обнаруживали у обоих партнеров сразу.
Интенсивность воздействия определяется характеристиками антител: классом, количеством, плотностью покрытия половых клеток. Антитела могут нарушать процесс развития сперматозоидов, парализовать клетки в цервикальной слизи, предотвращать имплантацию оплодотворенной яйцеклетки в матке.
Классы антиспермальных антител:
- Ig, M – закрепляются за хвостик сперматозоида, приостанавливают его движение в цервикальной слизи (процесс оплодотворения остается неизменным);
- Ig, G – крепятся за головку клетки, что не влияет на подвижность, но мешает проникновению сперматозоида в женскую половую клетку (увеличивается количество лейкоцитов, снижается кислотность, сокращается время разжижения);
- Ig, A – изменяют морфологию клетки, успешно поддаются лечению (восстановление гематотестикулярного барьера между сосудами и семенными канальцами).
До полового созревания сперма не образуется, поэтому ее антигены не воспринимаются иммунитетом. Единственная причина, по которой иммунная система не уничтожает сперматозоиды, заключается в биологическом барьере. Сперма изолирована от клеток иммунитета, которые содержатся в крови. Защитой выступает гематотестикулярный барьер между кровеносными сосудами и семенными канальцами.
Барьер может повредиться при анатомических нарушениях вроде паховой грыжи, перекрута яичек, варикоцеле, недоразвитости или отсутствии семявыводящих путей. Также защита может пострадать от инфекций, которые передаются половым путем. Травмы и хирургическое вмешательство в органы малого таза и мошонки также повышают риск нарушения барьера. В группе риска мужчины с хроническими воспалениями мочеполовой системы.
Все эти факторы способны повредить гематотестикулярный барьер и высвободить сперму. При попадании в кровь она запустит защитный процесс.
Существует несколько видов антител, которые могут оказывать влияние на репродуктивную систему мужчины. Спермоиммобилизирующие могут частично или полностью прекратить активность половой клетки. Спермоагглютинирующие склеивают сперматозоиды с излишками (разрушенными клетками, слизью, частичками эпителия). Оба явления порождают иммунологическое бесплодие.
Не исключена возможность незначительного проникновения половых клеток за пределы барьера и попадания в кровь, но иммунологическая толерантность не дает запуститься защитным механизмам.
Повредить гематотестикулярный барьер может инфекция или травма (механическая или во время операции). Нарушение целостности барьера влечет за собой проникновение антител в генитальный тракт, что открывает доступ иммунной системе к сперме.
Появление антител связано с такими явлениями:
- варикоцеле (расширение вен семенного канала, из-за чего происходит перегрев яичек);
- онкологические заболевания;
- крипторхизм (яичка не опущены в мошонку);
- инфекции;
- хирургическое вмешательство.
Иммунная система у женщин контактирует с половой, однако это не мешает воспринимать сперму агрессивно. Природа построила половые органы женщины таким образом, чтобы сперматозоиды могли выжить в агрессивной среде и быть защищенными от иммунитета. Несмотря на то, что чужеродные сперматозоиды проникают в организм женщины при половом акте, иммунитет не уничтожает их (в здоровом организме). Дело в том, что среда влагалища защищает сперму от иммунных клеток.
В женском организме антитела возникают на фоне:
- повреждения слизистой;
- переизбытка лейкоцитов и лимфоцитов в семенной жидкости;
- попадания сперматозоидов, связанных в антителами;
- попытки ЭКО в анамнезе;
- попадания половых клеток в ЖКТ (при оральном или анальном сексе);
- нерегулярной половой жизни при высокой концентрации аномальных мужских половых клеток;
- неправильного строения половых путем, которое позволяет сперме попадать в брюшину;
- прижигания эрозий шейки матки в анамнезе.
Довольно долго медицина не знала, как именно антитела влияют на репродуктивную функцию человека и вызывают иммунологическое бесплодие. Сегодня ученые доказали факт следующих явлений:
- Антитела угнетают активные половые клетки. Прикрепляясь к сперматозоидам, антитела значительно их тормозят. Клетки не могут продвигаться как в мужском организме, так и в женском. Антиспермальные антитела склеивают половые клетки и парализуют их. Степень нарушений зависит от количества антител и их локализации на сперматозоиде. Считается, что при креплении к головке сперматозоид страдает больше всего.
- Сперматозоидам сложнее проникнуть в цервикальную слизь. Способность сперматозоидов проникать в среду влагалища определяет шансы на зачатие. При наличии антител половая клетка начинает, как называется в науке, «дрожать на месте». Данное явление можно заметить во время пробы Шуварского и Курцрока-Миллера. Антитела могут частично блокировать проникновение сперматозоидов в слизь или полностью.
- Нарушения при сперматогенезе.
- Нарушения при оплодотворении. Доказано, что антитела влияют на гаметы. Иммунные клетки блокируют проникновение сперматозоида в оболочку яйцеклетки. Природа явления до конца не изучена, но факт остается фактом – антитела препятствуют акросомальной реакции (преодоление мужской половой клеткой барьера женской).
- Проблемы с прикреплением оплодотворенной яйцеклетки в матке.
- Торможение роста и развития плода. Антиспермальные антитела влияют на состояние зародыша. Это является серьезной проблемой при лечении методами искусственного оплодотворения.
Иммунологическое бесплодие опасно тем, что развивается без симптомов у представителей обоих полов. При такой форме бесплодия мужчины способны заниматься сексом, у них сохраняется спермиогенез. У женщин отсутствуют физиологические факторы бесплодия (маточные, трубно-перитонеальные).
Поводом обратиться к врачам становится только отсутствие беременности больше года при регулярной половой жизни без средств контрацепции. При этом у женщины нормальный менструальный цикл, а мужчина не теряет эрекцию. Нередко при иммунологическом бесплодии беременность наступает, но плод не может закрепиться в матке и выходит с менструацией. Женщина даже не замечает, что зачатие произошло.
Иммунологическое бесплодие исследуют комплексно: у женщин (консультируется с гинекологом), у мужчин (с урологом-андрологом).
Этапы диагностики иммунологического бесплодия:
Для мужчины:
- Исследование крови.
- Спермограмма (уделить внимание антителам в сперме). При иммунологическом факторе бесплодия спермограмма покажет сокращение количества клеток, изменение их строения и формы, слабую активность и низкую стойкость.
Для женщины:
- Анализ цервикальной слизи.
- Исследование крови на предмет антиспермальных антител.
- Тест на совместимость шеечной слизи и половых клеток партнера (посткоитальный или проба Шуварского). Посткоитальный тест позволяет обнаружить антитела в цервикальной слизи после полового акта. Клетки, соединенные с антиспермальными антителами, отличаются специфическими движениями и низкой подвижности.
- MAR-тест (подсчет сперматозоидов покрытых антитела). Результаты MAR-теста говорят о количестве подвижных клеток, соединенных с антителами (бесплодие имеет место при 50% антител Ig, G).
- Проба Курцрока-Миллера (изучение способностей половых клеток проникать в слизь).
- Тест Буво-Пальмера (закрепление результата пробы Курцрока-Миллера).
- 1ВТ-тест. Исследование показывает расположение антител на половых клетках и вычисляет процент связанных сперматозоидов.
- Метод проточной цитофлуорометрии. С его помощью можно высчитать концентрацию антител на одной половой клетке.
При плохих результатах спермограммы и посткоитального теста рекомендовано пройти иммуноферментальный анализ (биохимическая реакция, которая позволяет выявить антитела в крови и подсчитать их количество). Иногда также проводят полимеразную цепную реакцию (выявление урогенитальных инфекций).
Во время исследований нужно прекратить прием лекарств (в особенности гормональных средств). Стоит наладить режим дня и правильное питание. Результаты анализов во многом зависят от настроения пациента.
Иммунологическое бесплодие у мужчин лечат при помощи вспомогательной репродуктивной медицины. Можно изучить сперматозоиды и выбрать подходящие для интрацитоплазматической инъекции в яйцеклетку или подобрать одну, но лучшую клетку для процедуры ЭКО.
Стратегия лечения иммунологического бесплодия у мужчин будет зависеть от причин такого состояния. Некоторым пациентам требуется хирургическое вмешательство, которое восстановит кровоток или устранит непроходимость. Также эффективна гормональная терапия. В любом случае лечение бесплодия будет длительным и сложным.
Лечение иммунологического бесплодия у женщин заключается в применении контрацептивов и препаратов для подавления антител у партнера. При отсутствии эффекта женщине также рекомендуется вспомогательная репродукция. Сначала проводят внутриматочную инсеминацию. Если беременность не наступает, обращаются к экстракорпоральному оплодотворению.
У женщин антитела возникают на фоне воспаления или инфекции. Лечение также будет зависеть от первопричины. Врач должен учесть степень нарушений и состояние здоровья женщины.
Лечение эндокринного бесплодия у женщин состоит из трех шагов:
- Коррекция иммунной системы, лечение основного нарушения и сопутствующих заболеваний. На этом этапе устраняется иммунный дефицит (кортикостероиды). Необходимо вылечить все инфекции и воспаления, нормализировать среду кишечника и влагалища (антигистаминные и антибактериальные средства). Полезными будут общее укрепление организма и психологическая помощь. Список иммуномодулирующих препаратов, которые допустимы в данном случае, ограничен. Эффективным считается введение партнерше лимфоцитов супруга или здорового донора.
- Подготовка перед беременность. Этот этап должен начаться хотя бы за месяц до зачатия. Гинеколог определяет лечение индивидуально для каждого пациента.
- Терапия во время беременности, сохранение плода. После оплодотворения нужно следить за гемостазом и проверять кровь на аутоантитела. Все отклонения должны быть скорректированы вовремя.
При наличии антител в цервикальной слизи нужно использовать контрацептивы, чтобы не допустить попадания сперматозоидов в половые пути. Курс барьерного лечения должен составлять 6-8 месяцев. При сочетании мужского и женского иммунологического бесплодия также рекомендуется вспомогательная репродуктивная медицина.
источник
В случаях, когда сданы все анализы, пройдено множество обследований и никакой патологии, препятствующей зачатию ребенка, не выявлено, врач заподозрит наличие у вас иммунологического бесплодия. Это значит, что ваш организм, а именно его иммунная система, производит антитела, которые ведут борьбу со сперматозоидами. В результате происходит потеря их подвижности и гибель. Антиспермальные антитела могут производиться как женским, так и мужским организмом. В сегодняшней статье речь пойдет о случае, когда женская иммунная система препятствует наступлению беременности.
Антиспермальные антитела (АсАт), вырабатывающиеся в женском организме, приводят к иммунологической несовместимости партнеров. Выявить такую несовместимость помогает посткоитальный тест (ПКТ). Также его называют пробой Шуварского-Симса-Хунера. Смысл тестирования заключается в выяснении взаимодействия цервикальной слизи в шейке матки со сперматозоидами.
Количество и качество шеечной слизи постоянно меняется на протяжении каждого месячного цикла. Благодаря свойствам цервикальной жидкости в период овуляции, сперматозоиды получают возможность легко транспортироваться из влагалища в маточную полость. Происходит это за счет секреции слизи в большом количестве и ее водянистой консистенции именно в течение 2-3 дней до овуляции и 1-2 дней после. В другие дни цикла цервикальная слизь наоборот препятствует проникновению сперматозоидов в матку, становясь густой, вязкой и присутствуя в шейке матки в небольших количествах. С данным свойством цервикальной жидкости и связаны сроки проведения посткоитального теста. Если пройти его не вовремя, то возможно получение ложноотрицательного результата.
Таким образом, в овуляционный период цервикальная слизь способствует:
- созданию условий для продвижения семенной жидкости в полость матки;
- осуществлению качественного отбора здоровых и выбраковки патологических форм спермиев;
- обеспечению периода зачатия качественными половыми клетками в достаточном количестве, благодаря выполнению функции временного резервуара сперматозоидов;
- обеспечению питания сперматозоидов, увеличивая их подвижность;
- защите мужских половых клеток от кислотной среды влагалища.
Если перечисленные функции нарушены, то существует вероятность наличия инфекционно-воспалительных процессов в шейке матки или иммунологического фактора бесплодия супругов.
Для пробы Шуварского-Симса-Хунера должны быть строго соблюдены правила его проведения. Достоверность результатов зависит от множества факторов. Отрицательный результат ПКТ полученный единожды, не будет говорить о подтверждении диагноза шеечного бесплодия, поэтому специалисты рекомендуют пройти данное обследование несколько раз. По рекомендациям ВОЗ исследование проводят спустя 9-24 часа после полового контакта.
Достоверность подтверждения признака иммунологической несовместимости партнеров предполагает соблюдение следующих правил:
- воздержание супружеской парой от половой близости в течение трех-пяти дней до ПКТ;
- незащищенный половой контакт супруги должны провести в период овуляции (дата высчитывается вместе с гинекологом);
- исключить применение мыла и мыльных растворов во время гигиенических процедур до и после полового контакта;
- запрещено использовать влагалищные формы лекарственных препаратов, лубрикантов и смазок для секса;
- по завершении полового акта женщине необходимо полежать еще в течение тридцати минут с приподнятым тазом (воспользуйтесь подушкой, подложив ее под ягодицы);
- не принимайте ванну после завершения полового акта, не спринцуйтесь, не вводите во влагалище тампоны.
Через 9 часов и не позднее суток женщине нужно придти на прием к гинекологу для проведения ПКТ. Врач специальной пипеткой соберет шеечную слизь, которую впоследствии будут изучать под микроскопом, оценивая подвижность и количество присутствующих в ней сперматозоидов.
Положительным будет расценен тест, в результате которого в цервикальной жидкости обнаружены живые и подвижные сперматозоиды в количестве 5-10 штук. Он будет свидетельствовать об отсутствии у пары иммунологической несовместимости.
Тест будет считаться сомнительным, если сперматозоидов в слизи окажется менее пяти штук, а также в случае маятникообразного движения половых клеток.
Отрицательным тест будет при отсутствии подвижных сперматозоидов в шеечной слизи, что расценивается как фактор наличия в ней АсАт и, как следствие – иммунологическое бесплодие. Не стоит забывать, что к данному результату могут привести факторы отсутствия эякуляции у мужчины или низкое качестве спермы, что исключается сдачей спермограммы.
Если два цикла подряд получен отрицательный результат ПКТ, то можно провести пробу Курцрока-Миллера, который является модификацией посткоитального теста. Проводится он в искусственных условиях, то есть обследованные сперматозоиды и цервикальная слизь смешиваются на предметном стекле. Далее происходит динамическое наблюдение за половыми клетками. Их гибель будет подтверждением иммунного фактора бесплодия. В данном случае также определяется уровень АсАт в крови и проводится MAR-тест.
Для начала врач проведет комплексную терапию, направленную на снижение уровня АсАт. Женщине будут назначены глюкокортикостероиды, подавляющие иммунитет, и запрет на контакт организма пациентки на протяжении нескольких месяцев со спермой.
Если консервативная терапия не принесет положительных результатов, то лечение будет проводиться с помощью методов ВРТ, к которым относятся процедуры ВМИ, ЭКО, ИКСИ. Выбор врача в плане подходящего метода лечения будет определяться отдельно в каждом индивидуальном случае.
источник
Иммунологическое бесплодие – гипериммунное состояние женского или мужского организма, сопровождающееся секрецией специфических антиспермальных антител. Иммунологическое бесплодие проявляется несостоятельностью зачатия и наступления беременности при регулярной половой жизни без контрацепции при отсутствии других женских и мужских факторов инфертильности. Диагностика иммунологического бесплодия включает исследование спермограммы, антиспермальных антител плазмы, проведение посткоитального теста, MAR-теста и других исследований. При иммунологическом бесплодии применяются кортикостероиды, методы иммунизации и вспомогательные репродуктивные технологии.
Иммунологическое бесплодие — наличие патологического антиспермального иммунитета, препятствующего процессу оплодотворения яйцеклетки и имплантации эмбриона. При иммунологическом бесплодии антитела к сперматозоидам – антиспермальные антитела (АСАТ) могут синтезироваться как женским, так и мужским организмом и присутствовать в цервикальной и внутриматочной слизи, сыворотке крови, семенной плазме, семявыводящих протоках. Иммунологический фактор оказывается причиной бесплодия у 5-20% семейных пар в возрасте до 40 лет, при этом АСАТ могут выявляться только у одного супруга или сразу у обоих. Изучением проблемы иммунологического бесплодия занимаются специалисты в области репродуктивной медицины (гинекологи — репродуктологи, андрологи).
В минимальном количестве АСАТ могут присутствовать у фертильных мужчин и женщин, но их фиксация на мембранах большинства сперматозоидов резко ухудшает прогноз на беременность. Это связано с нарушением качества и фертильности спермы — повреждением структуры и резким спадом подвижности сперматозоидов, снижением их способности проникать в цервикальную слизь, блокадой подготовительных стадий (капацитации и акросомальной реакции) и самого процесса оплодотворения яйцеклетки. При наличии АСАТ существенно снижается качество эмбрионов, нарушаются процессы их имплантации в матку, формирования плодных оболочек и развития, что приводит к гибели зародыша и прерыванию беременности на самых ранних сроках.
По своей антигенной структуре сперматозоиды являются чужеродными для женского и для мужского организма. В норме они защищены механизмами супрессии иммунного ответа: у мужчин — гемато-тестикулярным барьером (ГТБ) в яичке и его придатке, иммуносупрессивным фактором спермоплазмы и способностью сперматозоидов к мимикрии (к сорбции и десоробции поверхностных антигенов); у женщин — уменьшением уровня Т-хелперов, Ig и С3-компонента системы комплемента, повышением числа Т-супрессоров во время овуляции.
Под действием определенных неблагоприятных факторов нарушение защитных механизмов делает возможным контактирование спермальных антигенов с иммунной системой и приводит к развитию иммунологического бесплодия. Причинами выработки аутоантител на сперматозоиды и клетки сперматогенеза у мужчин могут выступать острые и тупые травмы мошонки и операции на яичках, инфекции и воспалительные процессы урогенитального тракта (гонорея, хламидиоз, герпес, ВПЧ, орхит, эпидидимит, простатит), врожденные или приобретенные дефекты половых органов (крипторхизм, перекрут яичка, варикоцеле, фуникулоцеле и др.), онкопатология.
Сбой внутриматочной иммунной толерантности и появление АСАТ у женщин в предимплантационный период могут быть спровоцированы инфекционно-воспалительными заболеваниями репродуктивного тракта, повышенным уровнем лейкоцитов в эякуляте партнера (при неспецифическом бактериальном простатите), контактом с иммуногенными сперматозоидами партнера, уже связанными с его аутоантителами.
Формированию АСАТ у женщин также могут способствовать попадание спермы в ЖКТ при оральном/анальном сексе, применение химических средств контрацепции, коагуляция эрозии шейки матки в анамнезе, нарушения при внутриматочной инсеминации, гормональный «удар» при попытке ЭКО, травма при заборе яйцеклеток. Опосредованно стимулировать выработку АСАТ в женском организме могут другие изоантигены, содержащиеся в эякуляте партнера — ферменты и внутриклеточные антигены сперматозоидов, HLA антигены; несовместимость в системах ABO, Rh-Hr, MNSs.
Степень поражения сперматозоидов зависит от класса (IgG, IgA, IgM) и титра АСАТ, места их фиксации, уровня возникновения иммунной реакции. АСАТ, соединяющиеся с хвостовой частью сперматозоидов, затрудняют их движение, а фиксирующиеся к головке — блокируют слияние с ооцитом.
Иммунологическое бесплодие внешне протекает бессимптомно, не имея видимых проявлений у обоих партнеров. У мужчин с аутоиммунным бесплодием обычно сохраняется активный сперматогенез, эректильная функция и полноценность полового акта. При гинекологическом обследовании женщины не обнаруживаются маточные, трубно-перитонеальные, эндокринные и иные факторы, препятствующие зачатию.
При этом у супружеской пары детородного возраста при условии нормального менструального цикла женщины и регулярной половой жизни без предохранения имеет место отсутствие беременности в течение года и более. При АСАТ у женщин из-за дефекта имплантации и нарушения развития эмбриона наблюдается его гибель и отторжение, прерывание беременности на очень ранних сроках, обычно до того, как женщина может ее обнаружить.
При бесплодии комплексное обследование необходимо пройти и женщине, и мужчине — у гинеколога и уролога-андролога соответственно. Иммунологический характер бесплодия диагностируют по результатам лабораторных исследований: анализа эякулята, специальных биологических проб — посткоитального теста (Шуварского– унера in vivo и Курцрока–Миллера in vitro), MAR-теста; 1ВТ-теста, ПЦМ. определения антиспермальных антител плазмы. На время проведения диагностических испытаний прием гормональных и других лекарственных препаратов прерывают.
Наличие мужского фактора иммунологического бесплодия можно предположить при нарушении спермограммы (резком падении количества, искажении формы, агглютинации и слабой активности сперматозоидов, низкой выживаемости спермы, полном отсутствии живых спермиев). Данные основного посткоитального теста помогают выявить АСАТ в цервикальной слизи по ее воздействию на подвижность и жизнеспособность сперматозоидов в содержимом шеечного канала. Для соединенных с АСАТ сперматозоидов характерна низкая мобильность и адинамия, маятникообразные движения и феномен «дрожания на месте».
Одновременно со спермограммой выполняется MAR-тест, определяющий количество АСАТ-позитивных подвижных сперматозоидов (при MAR IgG >50% очевиден диагноз «мужское иммунное бесплодие»). 1ВТ-тест устанавливают локализацию АСАТ на поверхности сперматозоида и процент АСАТ-связанных спермиев. Методом проточной цитофлуорометрии (ПЦМ) оценивают концентрацию АСАТ на одном сперматозоиде, спонтанную и индуцированную акросомальную реакцию. При выявлении отклонений в спермограмме и посткоитальном тесте показано проведение ИФА с целью определения спектра АСАТ в сыворотке крови. Дополнительно может проводиться ПЦР-исследование на урогенитальные инфекции (хламидии, микоплазмы, ВПГ, ВПЧ, и др.), определение аутоантител к фосфолипидам, ДНК, кардиолипину, тиреоидным гормонам, HLA-типирование. Иммунологическое бесплодие необходимо дифференцировать от женского и мужского бесплодия другого генеза.
При иммунологическом бесплодии проводят коррекцию иммунного статуса женщины длительными курсами или ударными дозами кортикостероидов, назначают антигистаминные и антибактериальные препараты. В случае аутоиммунных процессов (антифосфолипидный синдром) лечение дополняют низкими дозами аспирина или гепарина. Использование барьерного способа контрацепции (презервативов) в течение 6-8 месяцев с исключением контакта сперматозоидов с иммунными клетками половых органов женщины позволяет уменьшить сенсибилизацию ее организма. Подавление иммунитета повышает шансы зачатия в 50% случаев. Для нормализации иммунных механизмов в женском организме предлагается подкожное введение аллогенных лимфоцитов (мужа/донора) до зачатия или внутривенное введение γ-глобулина — смеси белков плазмы от разных доноров.
Устранение мужского компонента иммунологического бесплодия основано на лечении фоновой патологии, приведшей к образованию АСАТ, и может включать оперативные вмешательства, корригирующие аномалии репродуктивного тракта и кровообращения. Возможно назначение приема протеолитических ферментов, цитостатиков и кортикостероидов.
Основными в лечении иммунологического бесплодия выступают вспомогательные репродуктивные технологии, которые требуют тщательного обследования и подготовки супругов. При искусственной инсеминации осуществляется введение спермы мужа непосредственно в полость матки, минуя шеечный канал, в овуляторном периоде женщины. При наличии способных к оплодотворению, но не достигающих яйцеклетку сперматозоидов, применяется метод искусственного оплодотворения. При низком оплодотворяющем потенциале более высокая частота наступления беременности достигается методом ИКСИ — интрацитоплазматической инъекцией одного качественного сперматозоида в цитоплазму яйцеклетки с последующей подсадкой эмбрионов в полость матки.
Для выхода полноценной яйцеклетки проводится гормональная стимуляция суперовуляции. Получение сперматозоидов у мужчин производят путем эякуляции, забором из яичка (TESA, TESE, Micro-TESE) или придатка яичка (PESA, MESA). В тяжелых случаях мужского иммунологического бесплодия используется донорская сперма. Наличие высокого титра АСАТ в крови женщины является противопоказанием для инсеминации, ИКСИ и ЭКО и требует продолжительного лечения до нормализации их уровня. Перспективно при лечении иммунологического бесплодия использование более качественных морфологически селекционных или генетически здоровых и функционально активных сперматозоидов (ИМСИ и ПИКСИ) и предимплантационной выбраковки или обработки эмбрионов (ассистированный хэтчинг). Для повышения вероятности наступления беременности производится предимплантационная криоконсервация эмбрионов.
Иммунологическое бесплодие имеет достаточно специфический характер: АСАТ вырабатываются на сперматозоиды конкретного мужчины, и при смене партнера появляется возможность беременности. При полноценном лечении с использованием современных ВРТ иммунологическое бесплодие удается преодолеть в большинстве нетяжелых случаев. Вероятность беременности в естественном цикле в отсутствие лечения мужчины с MAR IgG > 50% составляет
источник
Причины появления АСАТ у мужчин
Образование антиспермальных тел (АСАТ) у мужчины начинается в момент образования спермы — на этапе полового созревания. Антигены спермы — «новички» в мужском организме и — по идее — должны вызывать защитную реакцию у иммунной системы. Так и было бы, если бы сперматозоиды попадали в кровь, но они находятся в некой «изоляции» и могут «вырваться» только в «экстренных случаях»:
анатомические нарушения (паховая грыжа, варикоцеле, обструкция семявыносяших путей, крипторхизм, перекрут яичка, агенезия семявыносящих протоков).инфекции, передающиеся половым путем;травмы и операции на органах малого таза, мошонки.хронические воспалительные заболевания (простатит, эпидидимит, орхит);
В перечисленных ситуациях биологический барьер между кровеносными сосудами и семенными канальцами разрушается, «новички» попадают в кровь — организм воспринимает незнакомые клетки как враждебные и защищается.
Действие АСАТ на репродуктивную функцию мужчины
Специалисты выделяют несколько видов мужских антиспермальных антител, в зависимости от их действия: спермоиммобилизирующие — частично или полностью обездвиживающие сперматозоиды; спермоагглютинирующие — «склеивающие» сперматозоиды друг с другом, эпителиальными клетками, макрофагами, фрагментами разрушенных клеток или комками слизи. Оба вида могут препятствовать оплодотворению и, в ряде случаев, приводят к бесплодию.
Причины появления АСАТ у женщин
Сперматозоиды — «чужаки» для организма женщины, и, по идее, должны вызывать защитную реакцию у иммунной системы. Но если бы так происходило — женщины не беременели бы вовсе. Защитная реакция не происходит, потому что клетки влагалища препятствуют проникновению «чужаков» в иммунную систему. Исключение могут составлять следующие случаи:
инфекции, передаваемые половым путём, хронические воспалительные заболевания половых органов, генитальныйэндометриоз, аллергические заболевания.
При перечисленных заболеваниях женский организм может начать бороться со сперматозоидами — возникает иммунологический фактор бесплодия.
Диагностика иммунологического фактора бесплодия
Подтверждение диагноза «иммунологический фактор бесплодия» включает несколько этапов: обследование мужчины — анализ крови и спермограмма на наличие антиспермальных антител в эякуляте; обследование женщины — исследование цервикальной слизи и анализ крови на антиспермальные антитела; обследование на совместимость партнеров:
посткоитальный тест, или проба Шуварского: определение совместимости сперматозоидов и шеечной слизи. MAR-тест: определение количества сперматозоидов, покрытых антиспермальными антителами. Если более 50% подвижных сперматозоидов покрыты АСАТ — диагностируется иммунологический фактор бесплодия. проба Курцрока—Миллера (пенетрационный тест): определение проникающей способности сперматозоидов.тестБуво—Пальмера (перекрестный пенетрационный тест): подтверждение пробы Курцрока—Миллера. Обследование предполагает исследование спермы будущего отца и спермы мужчины-донора.
Лечение иммунологического фактора бесплодия
Мужской иммунологический фактор бесплодия преодолевают с помощью вспомогательных репродуктивных технологий (ВРТ), в частности — ICSI-MAQS (микроскопический анализ качества сперматозоидов для интрацитоплазматической инъекции в яйцеклетку) или PICSI (физиологический выбор лучшего сперматозоида для интрацитоплазматической инъекции в яйцеклетку) в рамках программы экстракорпорального оплодотворения (ЭКО).
Женский иммунологический фактор бесплодия может быть излечен консервативным способом — рекомендуют кондом-терапию или медикаментозное лечение, направленное на подавление продукции АСАТ у партнеров. Если лечение неэффективно, целесообразнее планировать беременность с помощью вспомогательных репродуктивных технологий — программы внутриматочной инсеминации (ВМИ). При отсутствии эффекта от инсеминации рекомендуют ЭКО с применением ICSI-MAQS (микроскопический анализ качества сперматозоидов для интрацитоплазматической инъекции в яйцеклетку) или PICSI (физиологический выбор лучшего сперматозоида для интрацитоплазматической инъекции в яйцеклетку).
В случае сочетанного иммунологического бесплодия в паре также помогают вспомогательные репродуктивные технологии.
Иммунологическое бесплодие — наличие патологического антиспермального иммунитета, препятствующего процессу оплодотворения яйцеклетки и имплантации эмбриона. При иммунологическом бесплодии антитела к сперматозоидам – антиспермальные антитела (АСАТ) могут синтезироваться как женским, так и мужским организмом и присутствовать в цервикальной и внутриматочной слизи, сыворотке крови, семенной плазме, семявыводящих протоках. Иммунологический фактор оказывается причиной бесплодия у 5-20% семейных пар в возрасте до 40 лет, при этом АСАТ могут выявляться только у одного супруга или сразу у обоих. Изучением проблемы иммунологического бесплодия занимаются специалисты в области репродуктивной медицины (гинекологи — репродуктологи, андрологи).
В минимальном количестве АСАТ могут присутствовать у фертильных мужчин и женщин, но их фиксация на мембранах большинства сперматозоидов резко ухудшает прогноз на беременность. Это связано с нарушением качества и фертильности спермы — повреждением структуры и резким спадом подвижности сперматозоидов, снижением их способности проникать в цервикальную слизь, блокадой подготовительных стадий (капацитации и акросомальной реакции) и самого процесса оплодотворения яйцеклетки. При наличии АСАТ существенно снижается качество эмбрионов, нарушаются процессы их имплантации в матку, формирования плодных оболочек и развития, что приводит к гибели зародыша и прерыванию беременности на самых ранних сроках.
Причины иммунологического бесплодия
По своей антигенной структуре сперматозоиды являются чужеродными для женского и для мужского организма. В норме они защищены механизмами супрессии иммунного ответа: у мужчин — гемато-тестикулярным барьером (ГТБ) в яичке и его придатке, иммуносупрессивным фактором спермоплазмы и способностью сперматозоидов к мимикрии (к сорбции и десоробции поверхностных антигенов); у женщин — уменьшением уровня Т-хелперов, Ig и С3-компонента системы комплемента, повышением числа Т-супрессоров во время овуляции.
Под действием определенных неблагоприятных факторов нарушение защитных механизмов делает возможным контактированиеспермальных антигенов с иммунной системой и приводит к развитию иммунологического бесплодия. Причинами выработки аутоантител на сперматозоиды и клетки сперматогенеза у мужчин могут выступать острые и тупые травмы мошонки и операции на яичках, инфекции и воспалительные процессы урогенитального тракта (гонорея, хламидиоз, герпес, ВПЧ, орхит, эпидидимит, простатит), врожденные или приобретенные дефекты половых органов (крипторхизм, перекрут яичка, варикоцеле, фуникулоцеле и др.), онкопатология.
Сбой внутриматочной иммунной толерантности и появление АСАТ у женщин в предимплантационный период могут быть спровоцированы инфекционно-воспалительными заболеваниями репродуктивного тракта, повышенным уровнем лейкоцитов в эякуляте партнера (при неспецифическом бактериальном простатите), контактом с иммуногенными сперматозоидами партнера, уже связанными сегоаутоантителами.
Формированию АСАТ у женщин также могут способствовать попадание спермы в ЖКТ при оральном/анальном сексе, применение химических средств контрацепции, коагуляция эрозии шейки матки в анамнезе, нарушения при внутриматочной инсеминации, гормональный «удар» при попытке ЭКО, травма при заборе яйцеклеток. Опосредованно стимулировать выработку АСАТ в женском организме могут другие изоантигены, содержащиеся в эякуляте партнера — ферменты и внутриклеточные антигены сперматозоидов, HLA антигены; несовместимость в системах ABO, Rh-Hr, MNSs.
Степень поражения сперматозоидов зависит от класса (IgG, IgA, IgM) и титра АСАТ, места их фиксации, уровня возникновения иммунной реакции. АСАТ, соединяющиеся с хвостовой частью сперматозоидов, затрудняют их движение, а фиксирующиеся к головке — блокируют слияние с ооцитом.
Симптомы иммунологического бесплодия
Иммунологическое бесплодие внешне протекает бессимптомно, не имея видимых проявлений у обоих партнеров. У мужчин с аутоиммунным бесплодием обычно сохраняется активный сперматогенез, эректильная функция и полноценность полового акта. При гинекологическом обследовании женщины не обнаруживаются маточные, трубно-перитонеальные, эндокринные и иные факторы, препятствующие зачатию.
При этом у супружеской пары детородного возраста при условии нормального менструального цикла женщины и регулярной половой жизни без предохранения имеет место отсутствие беременности в течение года и более. При АСАТ у женщин из-за дефекта имплантации и нарушения развития эмбриона наблюдается его гибель и отторжение, прерывание беременности на очень ранних сроках, обычно до того, как женщина может ее обнаружить.
Диагностика иммунологического бесплодия
При бесплодии комплексное обследование необходимо пройти и женщине, и мужчине — у гинеколога и уролога-андролога соответственно. Иммунологический характер бесплодия диагностируют по результатам лабораторных исследований: анализа эякулята, специальных биологических проб — посткоитального теста (Шуварского–унераinvivo и Курцрока–Миллера invitro), MAR-теста; 1ВТ-теста, ПЦМ. определения антиспермальных антител плазмы. На время проведения диагностических испытаний прием гормональных и других лекарственных препаратов прерывают.
Наличие мужского фактора иммунологического бесплодия можно предположить при нарушении спермограммы(резком падении количества, искажении формы, агглютинации и слабой активности сперматозоидов, низкой выживаемости спермы, полном отсутствии живых спермиев). Данные основного посткоитального теста помогают выявить АСАТ в цервикальной слизи по ее воздействию на подвижность и жизнеспособность сперматозоидов в содержимом шеечного канала. Для соединенных с АСАТ сперматозоидов характерна низкая мобильность и адинамия, маятникообразные движения и феномен «дрожания на месте».
Одновременно со спермограммой выполняется MAR-тест, определяющий количество АСАТ-позитивных подвижных сперматозоидов (при MAR IgG>50% очевиден диагноз «мужское иммунное бесплодие»). 1ВТ-тест устанавливают локализацию АСАТ на поверхности сперматозоида и процент АСАТ-связанных спермиев. Методом проточнойцитофлуорометрии (ПЦМ) оценивают концентрацию АСАТ на одном сперматозоиде, спонтанную и индуцированную акросомальную реакцию. При выявлении отклонений в спермограмме и посткоитальном тесте показано проведение ИФА с целью определения спектра АСАТ в сыворотке крови. Дополнительно может проводиться ПЦР-исследование на урогенитальные инфекции (хламидии, микоплазмы, ВПГ, ВПЧ, и др.), определение аутоантител к фосфолипидам, ДНК, кардиолипину, тиреоидным гормонам, HLA-типирование. Иммунологическое бесплодие необходимо дифференцировать от женского и мужского бесплодиядругого генеза.
Лечение иммунологического бесплодия
При иммунологическом бесплодии проводят коррекцию иммунного статуса женщины длительными курсами или ударными дозами кортикостероидов, назначают антигистаминные и антибактериальные препараты. В случае аутоиммунных процессов (антифосфолипидный синдром) лечение дополняют низкими дозами аспирина илигепарина. Использование барьерного способа контрацепции (презервативов) в течение 6-8 месяцев с исключением контакта сперматозоидов с иммунными клетками половых органов женщины позволяет уменьшить сенсибилизацию ее организма. Подавление иммунитета повышает шансы зачатия в 50% случаев. Для нормализации иммунных механизмов в женском организме предлагается подкожное введение аллогенных лимфоцитов (мужа/донора) до зачатия или внутривенное введение γ-глобулина — смеси белков плазмы от разных доноров.
Устранение мужского компонента иммунологического бесплодия основано на лечении фоновой патологии, приведшей к образованию АСАТ, и может включать оперативные вмешательства, корригирующие аномалии репродуктивного тракта и кровообращения. Возможно назначение приема протеолитических ферментов, цитостатиков и кортикостероидов.
Основными в лечении иммунологического бесплодия выступают вспомогательные репродуктивные технологии, которые требуют тщательного обследования и подготовки супругов. При искусственнойинсеминацииосуществляется введение спермы мужа непосредственно в полость матки, минуя шеечный канал, в овуляторном периоде женщины. При наличии способных к оплодотворению, но не достигающих яйцеклетку сперматозоидов, применяется метод искусственного оплодотворения. При низком оплодотворяющем потенциале более высокая частота наступления беременности достигается методом ИКСИ — интрацитоплазматической инъекцией одного качественного сперматозоида в цитоплазму яйцеклетки с последующей подсадкой эмбрионов в полость матки.
Для выхода полноценной яйцеклетки проводится гормональная стимуляция суперовуляции. Получение сперматозоидов у мужчин производят путем эякуляции, забором из яичка (TESA, TESE, Micro-TESE) или придатка яичка (PESA, MESA). В тяжелых случаях мужского иммунологического бесплодия используется донорская сперма. Наличие высокого титра АСАТ в крови женщины является противопоказанием для инсеминации, ИКСИ и ЭКО и требует продолжительного лечения до нормализации их уровня. Перспективно при лечении иммунологического бесплодия использование более качественных морфологически селекционных или генетически здоровых и функционально активных сперматозоидов (ИМСИ и ПИКСИ) и предимплантационной выбраковки или обработки эмбрионов (ассистированныйхэтчинг). Для повышения вероятности наступления беременности производится предимплантационная криоконсервация эмбрионов.
Иммунологическое бесплодие имеет достаточно специфический характер: АСАТ вырабатываются на сперматозоиды конкретного мужчины, и при смене партнера появляется возможность беременности. При полноценном лечении с использованием современных ВРТ иммунологическое бесплодие удается преодолеть в большинстве нетяжелых случаев. Вероятность беременности в естественном цикле в отсутствие лечения мужчины с MAR IgG> 50% составляет
источник
В жизнедеятельности организма участвуют все системы и органы человека. Ответственность за защиту организма от чужеродных клеток берёт на себя иммунная система. Однако иногда в иммунной системе случаются сбои и она начинает активно защищать организм от сперматозоидов, воспринимая их как чужеродные клетки. Такая ситуация случается не только у женщин, но и у мужчин и может вызвать бесплодие. Что же такое иммунологическое бесплодие и как с ним бороться — будем разбираться.
Бывает так, что молодая пара как бы ни старалась — не может зачать ребёнка долгое время. В то же время и явные нарушения в работе мочеполовой системы у каждого из партнёров отсутствуют. В этом случае причиной ненаступления беременности может быть иммунологическое бесплодие.
Иммунологическое бесплодие — это нарушения в детородной функции обоих полов, связанное с работой в организме антиспермальных антител (АСАТ), повреждающих мужские половые клетки или уменьшающих их возможность активно двигаться. Из всех факторов нарушений фертильности у женщин и мужчин — на сбой в работе иммунной системы приходится от 15 до 20%. Однако частота нахождения АСАТ в крови и половых жидкостях женщины примерно в два раза выше, чем у мужчины. Хотя раньше вообще считалось, что антитела, недружественные спермиям, могут существовать только у женщины.
Антиспермальные антитела могут присутствовать в крови, слизистых выделениях влагалища, во внутрибрюшной жидкости женщины, в крови и сперме мужчины. При наличии иммунного бесплодия мужские половые клетки в организме того или другого пола расцениваются как негативные образования. На защиту организма встаёт иммунитет человека и начинают работать АСАТ, которые бывают трёх видов:
- IgM — прикрепляются к хвостику спермия, замедляя или останавливая её движение;
- IgA — изменяют морфологию половой клетки;
- IgG — присоединяются к голове сперматозоида, не позволяя ему внедриться в яйцеклетку;
Иммуноглобулины IgM, IgA и IgG в малых количествах могут находиться у любого человека, однако при бесплодии количество таких клеток значительно превышает норму.
Факторов, влияющих на иммунологическое бесплодия множество. Их подразделяют на мужские и женские.
Причины иммунного бесплодия у мужчины:
- воспалительные болезни мужских органов (эпидидимит, уретрит);
- инфекции, распространяющиеся через сексуальные контакты (сифилис, трихомониаз и другие);
- изменения морфологии половых органов мужчины (фимоз, перекрут яичка и другие);
- повреждения и хирургические операции мужских органов.
Причины иммунного бесплодия у женщины:
- инфекции, распространяющиеся через сексуальные контакты (трихомониаз, сифилис, хламидиоз и другие);
- воспалительные болезни женских органов (кольпит, цервицит);
- химические средства предохранения (свечи, кремы, гели);
- эндометриоз;
- безуспешное проведение экстракорпорального оплодотворения ранее;
- аллергии.
При каждом незащищенном сексуальном контакте во влагалище и матку женщины попадает огромное количество мужских половых клеток. Иммунная система женщины воспринимает спермии как инородные клетки и начинает атаку на них. В большинстве случаев защитные клетки воздействует только на слабые и неактивные сперматозоиды, в то время как большинство мужских клеток всё-таки остаются жизнеспособными и двигаются к своей цели. Кроме того, во время овуляции в половых органах женщины создаётся благоприятная среда для сперматозоидов (увеличивается количество цервикальной слизи, шейка матки высоко поднимается и приоткрывается — сокращая путь к матке) и срабатывает система иммуноподавления. При иммунологическом бесплодии система иммуноподавления не работает, а женские иммунные клетки активно и успешно борются со всеми сперматозоидами.
Допустить существование проблем с иммунной системой, мешающих завести ребенка, можно при наличии факторов риска, перечисленных выше, особенно если факторы риска находятся у обоих партнёров.
Однако единственным симптомом наличия большого количества АСАТ, является длительная невозможность зачатия ребёнка парами, с относительно здоровой половой системой обоих партнёров. Отсутствие беременности может наблюдаться в течение года и более половой жизни без применения каких-либо средств контрацепции. Иногда бесплодие может выражаться в случайных выкидышах на ранних сроках беременности.
Для диагностики этого заболевания необходимо привлечь обоих членов супружеской пары, мечтающих зачать ребёнка. Поставить диагноз иммунологическое бесплодие может только врач, после проведения нескольких видов исследований. Мужчины сдают кровь и сперму для проведения анализа на наличие АСАТ. Кроме того, обоих членов пары проверяются на наличие инфекций, передающиеся половым путём. Женщине необходимо сдать кровь и цервикальный мазок. Завершением исследования должен быть анализ совместимости партнёров. На время проведения диагностических исследований, приём гормональных или иных лекарственных средств следует отменить. 
Для проверки крови на наличие в ней антиспермальных антител привлекаются мужчина и женщина. Кровь сдается обычно рано утром на голодный желудок. Небольшой объем крови, взятый у пациента помещается в планшет, который покрыт белками, восприимчивыми к АСАТ. В течение нескольких минут иммуноглобулины IgG, IgA и IgM начинают взаимодействовать с белками и прикрепляются к ним. После этого замеряется количество антиспермальных антител в исследуемом образце.
Нормальным считается результат от 0 до 60 Ед/мл. Это значит, что антиспермальных антител в исследуемом образце нет или их количество незначительно и не может повлиять на способность к зачатию. Средним значением является результат от 61 до 100 Ед/мл. Повышенные показатели АСАТ в крови — более 101 Ед/мл.
Среднее и повышенное содержание иммуноглобулинов в крови может влиять на способность к зачатию. Точно интерпретировать результаты исследований сможет доктор, исходя из самочувствия пациента, его пола, возраста и анамнеза.
Для изучения биологического материала мужчины используется спермограмма. Спермограмма — анализ фертильности спермы, исходя из числа, размера, морфологии, активности спермиев и других признаков. Изучение спермы производят для определения плодовитости мужчины, а также перед проведением процедуры ЭКО и ИКСИ. Сперма собирается мужчиной самостоятельно в специальную лабораторную пробирку. Перед сдачей эякулята необходимо воздержаться от секса 2–3 дня. Исследование спермы подразумевает оценку физических показателей (запах, цвет, консистенция) и количества сперматозоидов в 1 мл спермы и в общем ее объеме. Кроме того оценивается активность мужских половых клеток, их форма, наличие склеивания спермиев друг с другом или другими компонентами спермы, наличие слизи и белых кровяных клеток (лейкоцитов), кислотно-щелочной баланс.
Показатели спермы, по которым можно говорить о её фертильности и присутствии в ней иммуноглобулинов:
- малоактивность или неподвижность спермиев;
- малое количество сперматозоидов;
- наличие патологических форм мужских половых клеток;
- наличие большого количества мертвых клеток;
- склеивание сперматозоидов друг с другом;
- большое количество лейкоцитов;
- маятникообразное движение клеток, вместо правильного движения «вперед».
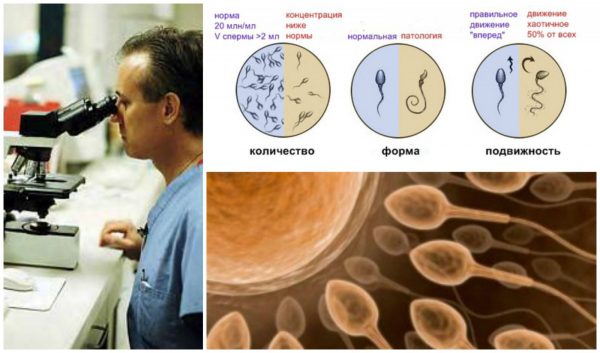
На изменение морфологии, то есть на появление патологических спермиев, оказывают влияние иммуноглобулины IgA, тем более в той ситуации когда их количество значительно превышено. АСАТ класса IgG и IgM увеличивают количество белых кровяных клеток в сперме, способствуя ее сгущению, кроме того, антитела в половой жидкости мужчины убивают спермии ещё в придатке яичка.
Для подтверждения женской «аллергической» реакции на эякулят партнёра существуют следующие тесты:
- проба Шуварского;
- тест Курцрока-Миллера.
Для исследования биологического материала женщины на наличие АСАТ проводят посткоитальный тест или пробу Шуварского. Посткоитальный тест проводится после обследования мужчины, а также после исключения других мочеполовых болезней женщины, возможных помешать наступлению беременности. Проба Шуварского производится во время предполагаемой овуляции — на 12–14 день менструального цикла. За 3–4 дня, до взятия пробы паре необходимо прекратить сексуальные отношения. Цервикальная слизь женщины отбирается обычно через 3–4 часа (но не более 24 часов) после полового акта.
Шеечная слизь женщины оценивается на содержание и активность в ней сперматозоидов. Результат теста оценивается:
- как положительный (то есть отсутствие беременностей не связано с наличием АСАТ в цервикальной слизи) при наличии в изучаемом материале не менее 15 подвижных мужских клеток;
- сомнительный — если сперматозоиды в слизи присутствуют, но их количество меньше 15, сперматозоиды неподвижны или их движения маятникообразные;
- плохой результат теста (несовместимость) — если в изучаемом материале обнаружено несколько обездвиженных спермиев;
- отрицательный результат — при отсутствии в предлагаемом материале сперматозоидов. Может говорить о неправильном проведении теста.
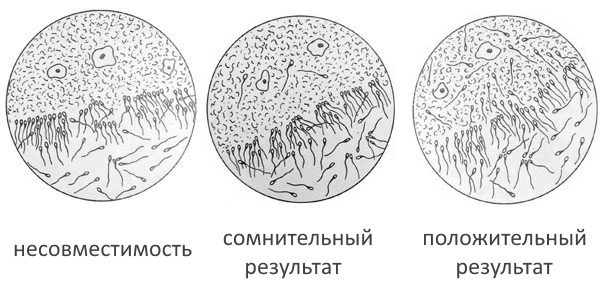
При сомнительном, плохом или отрицательном результате теста назначается повторное исследование через 2–3 месяца. Только после проведения минимум трёх проб Шуварского с получением плохого результата врач может поставить диагноз бесплодие.
Тест Курцрока-Миллера также проводится с целью изучения совместимости партнёров. Он очень похож на посткоитальный тест, также проводится после полового воздержания, во время овуляции у женщины. Однако в отличие от посткоитального теста при пробе Курцрока-Миллера, помимо оценки взаимодействия биоматериала супружеской пары, оценивается также и взаимодействие биоматериала каждого из членов пары с биоматериалом доноров, имеющих детей. Таким образом , в тесте Курцрока-Миллера используют два метода исследования:
- прямой — изучение взаимодействия биоматериала супругов;
- перекрёстный — взаимодействие биоматериала каждого члена пары с биоматериалом доноров.
При перекрёстном методе исследования в день анализа на исследование берётся шеечная слизь женщины и помещается между двух стёкол. Затем, к слизи дамы добавляют сперму её партнера и сперму донора, после чего на протяжении 5–7 часов биоматериалы взаимодействуют при температуре 37°С. Таким же образом на взаимодействие со слизью супруги и со слизью донора проверяется сперма мужа.
Итоги теста Курцрока-Миллера:
- Положительный (хороший) результат. В результате теста выявляется выживаемость и активность сперматозоидов мужа в шеечной жидкости его супруги. Вероятность наступления самостоятельной настоящей беременности у такой пары есть и она достаточно велика.
- Слабоположительный результат. В результате теста выявляется активность и целенаправленное движение «вперед» около половины спермиев. Вероятность естественного наступления беременности у данной семьи существует, но на зачатие может потребоваться длительный период. Иногда таким семьям могут назначить прием медикаментов, стимулирующих активность сперматозоидов.
- Отрицательный результат. Скорее всего означает иммунологическое бесплодие. По результатам теста выявляется, что спермии мужчины не могут проникать через шеечную жидкость его партнёрши. Шансы на самостоятельную беременность при отрицательном результате теста очень малы.
Терапия иммунноной бездетности является длительным процессом, так как связана с непростым механизмом — необходимостью снижения охранной функции собственной иммунной системы человека.
Лечение бездетности мужчин и женщин связано с применением антибиотиков, противоаллергенных средств и медикаментов против воспалений. Также, параллельно с приёмом медикаментозных веществ, супружеской паре необходимо предохраняться презервативами на протяжении 7–9 месяцев. Долговременное препятствие контакта женской половой системы со сперматозоидами позволяет уменьшить защитную функцию иммунной системы организма.
При отсутствии эффекта консервативного лечения с помощью медикаментов, паре, желающей иметь ребёнка, возможно будет прибегнуть к экстракорпоральному оплодотворению (ЭКО) или инъекции сперматозоидов в цитоплазму клетки (ИКСИ).
Для решения вопроса, связанного с бесплодием, мужчине прописывают курс приёма гормональных препаратов. Приём гормональных средств связан с необходимостью повышения уровня гормона тестостерона. Тестостерон является мужским половым гормоном, увеличивающим активность сперматозоидов, а значит и способность семенной жидкости к оплодотворению.
Также лечение иммунологического бесплодия мужчины может быть связано с хирургическим вмешательством, направленным на устранение патологии, послужившей образованию антиспермальных антител. Допустимо назначение приёма гормонов надпочечников или противоопухолевых препаратов.
Лечение женского бесплодия связывают в основном с подавлением чувствительности иммунной системы. Для этого назначают антигистаминные препараты, такие как Тавегил, Лоратадин, Зиртек. 
Также на иммунный статус воздействуют продолжительным приёмом гормонов надпочечников или приёмом антибактериальных средств.
В случае аутоиммунных процессов лечение могут дополнить аспирином. Для лечения от иммунной бездетности в кровь больного вводят противобактериальный и противовирусный препарат — гамма-глобулин. Этот метод является довольно дорогостоящим, поэтому не очень популярен. Наиболее дешевым средством терапии от иммуноглобулинов является введение в кровь женщины лимфоцитов супруга для иммунизации. Такие инъекции вводятся в кровь дамы от 3 до 6 месяцев. Также для уменьшения сопротивляемости иммунитета к сперматозоидам отлично подходит использование презервативов, которые исключают попадание мужской жидкости в женские половые органы. Применение таких методов защиты в течение 7–9 месяцев, позволит ослабить иммунную защиту организма женщины от спермиев. Такие методы лечения могут повысить шансы на беременность до 60%, в зависимости от сложности заболевания каждой конкретной пары. В случае если консервативные методы лечения не приводят к наступлению желанной беременности, паре рекомендуется проведение ИКСИ или ЭКО.
Наиболее новым и результативным средством избавления от бездетности является метод ИКСИ (интрацитоплазматическая инъекция сперматозоида). При применении метода ИКСИ, так же как и при ЭКО, оплодотворение происходит искусственным путём. Однако главное отличие интрацитоплазматической инъекции сперматозоида от экстракорпорального оплодотворения в том, что для ИКСИ отбирается только один сперматозоид, который вводится в яйцеклетку при помощи микроиглы.
Сперматозоид отбирают наиболее активный, полностью созревший, имеющий соответствующее норме строение и форму. Яйцеклетка также должна быть полностью созревшая и здоровая.
Оплодотворение проводят в день забора яйцеклетки. Опытный репродуктолог, используя специфические инструменты, вживляет мужскую половую клетку в цитоплазму яйцеклетки. После успешного оплодотворения эмбрион подсаживается в матку. Процедура ИКСИ является очень сложной и дорогой. Для её осуществления необходимо сложное оборудование, специальные комплекты реактивов, микроскопы, а также опытные врачи-репродуктологи — так как процесс оплодотворения является сложным, почти филигранным. В то же время эффективность этого метода очень высокая. Оплодотворение яйцеклетки наступает в более чем 85% случаев, а беременность в 45–65% случаев. Показатели эффективности метода ИКСИ пока не доходят до 100 %, так как бывают ситуации с повреждением яйцеклетки при проведении процедуры, наличием генетических отклонений спермия, женской клетки или не приживаемостью готового эмбриона в теле матки. 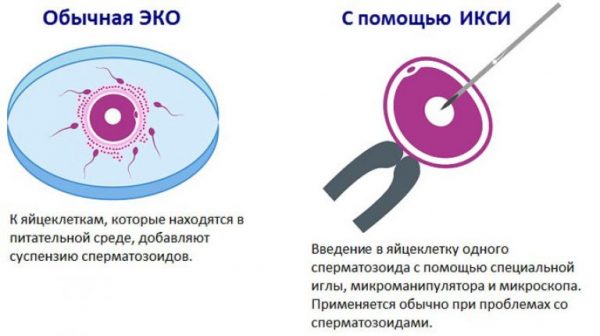
Ещё одним методом зачатия ребёнка является ЭКО.
При проведении ЭКО врачи берут от мужчины сперму со здоровыми активными сперматозоидами. У женщины отбирается одна яйцеклетка — при нормальном регулярном менструальном цикле. Если цикл женщины склонен к нарушениям из-за гормональных причин, врачи могут прибегнуть к стимуляции яичников и получению сразу нескольких зрелых фолликулов. Экстракорпоральное оплодотворение заключается в соединении в пробирке со специально подготовленными условиями нескольких яйцеклеток и сперматозоидов. После произошедшего оплодотворения готовые эмбрионы имплантируют в полость матки женщины.
После внедрения эмбрионов в матку, беременной следует пару дней принимать специальные препараты, ограничить физические нагрузки и исключить сильные эмоциональные переживания.
Эффективность ЭКО составляет от 30 до 50% и зависит от правильной работы врачей-эмбриологов, эмоционального настроя женщины и её физического состояния.
При наличии АСАТ у женщины эффективность ЭКО и ИКСИ значительно снижается, так как антиспермальные антитела могут мешать не только оплодотворению, но и имплантации эмбриона в матке, и всему течению беременности.
Использование методов ЭКО и ИКСИ возможно только в случае снижения активности или неподвижности сперматозоидов, но их сохранении возможности к оплодотворению. Если же, сперматозоиды неспособны самостоятельно оплодотворить яйцеклетку остаётся вариант лишь на использование спермы донора. Донором могут стать только здоровые мужчины в возрасте не более 35 лет, у ближайших родственниц по женской линии которых не было случаев самопроизвольных абортов или пороков внутриутробного развития ребенка.
Иммунологическое бесплодие не приговор. При не запущенности болезни и её лечении вероятность наступления беременности достигает 80%. Формы, длительность лечения и его успех зависит от течения болезни и индивидуальных особенностей человека. В тяжёлых случаях, шанс на зачатие ребёнка у пары остаётся при использовании процедуры ИКСИ или ЭКО.
источник

