В соответствии со статьей 37 Федерального закона от 21 ноября 2011 г. N 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» (Собрание законодательства Российской Федерации, 2011, N 48, ст. 6724; 2012, N 26, ст. 3442, 3446) приказываю:
Утвердить стандарт специализированной медицинской помощи при болезни Альцгеймера согласно приложению.
Зарегистрировано в Минюсте РФ 5 марта 2013 г.
Категория возрастная: взрослые
Стадия: деменция при болезни Альцгеймера
Осложнения: без осложнений
Вид медицинской помощи: специализированная медицинская помощь
Условия оказания медицинской помощи: стационарно
Форма оказания медицинской помощи: плановая
Средние сроки лечения (количество дней): 30
| Код по МКБ X Нозологические единицы | F00.0 | Деменция при болезни Альцгеймера с ранним началом (G30.0+) |
|---|---|---|
| F00.1 | Деменция при болезни Альцгеймера с поздним началом (G30.1+) | |
| F00.2 | Деменция при болезни Альцгеймера, атипичная или смешанного типа (G30.8+) (G30.1+) |
Наименование медицинской услуги
Усредненный показатель частоты предоставления*(2)
Усредненный показатель кратности применения
Прием (осмотр, консультация) врача-невролога первичный
Прием (осмотр, консультация) врача-психотерапевта первичный
Прием (осмотр, консультация) врача-психиатра первичный
Прием (осмотр, консультация) врача-психиатра повторный
Прием (осмотр, консультация) врача-терапевта первичный
Прием (осмотр, консультация) врача функциональной диагностики первичный
Прием (тестирование, консультация) медицинского психолога первичный
Лабораторные методы исследования
Исследование тиреотропина сыворотки крови
Исследование уровня фолиевой кислоты в сыворотке крови
Общий (клинический) анализ крови развернутый
Анализ крови биохимический общетерапевтический
Инструментальные методы исследования
Расшифровка, описание и интерпретация электрокардиографических данных
Магнитно-резонансная томография головного мозга
Компьютерная томография головы
Описание и интерпретация компьютерных томограмм
Описание и интерпретация магнитно-резонансных томограмм
Тестологическое психодиагностическое обследование
Наименование медицинской услуги
Усредненный показатель частоты предоставления
Усредненный показатель кратности применения
Прием (осмотр, консультация) и наблюдение врача-специалиста
Прием (осмотр, консультация) врача-невролога повторный
Прием (осмотр, консультация) врача-психиатра повторный
Прием (осмотр, консультация) врача-терапевта повторный
Наблюдение и уход за пациентом медицинскими работниками со средним (начальным) профессиональным образованием
Внутримышечное введение лекарственных препаратов
Внутривенное введение лекарственных препаратов
Лабораторные методы исследования
Общий (клинический) анализ крови развернутый
Инструментальные методы исследования
Расшифровка, описание и интерпретация электрокардиографических данных
Немедикаментозные методы профилактики, лечения и медицинской реабилитации
Семейное психологическое консультирование
Процедуры по адаптации к условиям микросреды
Процедуры по адаптации к условиям макросреды
Транскраниальная магнитная стимуляция
Воздействие излучением видимого диапазона через зрительный анализатор (цветоимпульсная терапия)
3. Перечень лекарственных препаратов для медицинского применения, зарегистрированных на территории Российской Федерации, с указанием средних суточных и курсовых доз
Наименование лекарственного препарата*(3)
Усредненный показатель частоты предоставления
Пиперидиновые производные фенотиазина
Диазепины, оксазепины и тиазепины
Другие антипсихотические средства
Другие психостимуляторы и ноотропные препараты
Другие препараты для лечения деменции
Наименование вида лечебного питания
Усредненный показатель частоты предоставления
Основной вариант стандартной диеты
*(1) — Международная статистическая классификация болезней и проблем, связанных со здоровьем, X пересмотра
*(2) — Вероятность предоставления медицинских услуг или назначения лекарственных препаратов для медицинского применения (медицинских изделий), включенных в стандарт медицинской помощи, которая может принимать значения от 0 до 1, где 1 означает, что данное мероприятие проводится 100% пациентов, соответствующих данной модели, а цифры менее 1 — указанному в стандарте медицинской помощи проценту пациентов, имеющих соответствующие медицинские показания
*(3) — Международное непатентованное или химическое наименование лекарственного препарата, а в случаях их отсутствия — торговое наименование лекарственного препарата
1. Лекарственные препараты для медицинского применения, зарегистрированные на территории Российской Федерации, назначаются в соответствии с инструкцией по применению лекарственного препарата для медицинского применения и фармакотерапевтической группой по анатомо-терапевтическо-химической классификации, рекомендованной Всемирной организацией здравоохранения, а также с учетом способа введения и применения лекарственного препарата.
2. Назначение и применение лекарственных препаратов для медицинского применения, медицинских изделий и специализированных продуктов лечебного питания, не входящих в стандарт медицинской помощи, допускаются в случае наличия медицинских показаний (индивидуальной непереносимости, по жизненным показаниям) по решению врачебной комиссии (часть 5 статьи 37) Федерального закона от 21.11.2011 N 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» (Собрание законодательства Российской Федерации, 28.11.2011, N 48, ст. 6724; 25.06.2012, N 26, ст. 3442)).
источник
Утверждающий документ:
Приказ Минздрава России от 20.12.2012 N 1228н
СПЕЦИАЛИЗИРОВАННОЙ МЕДИЦИНСКОЙ ПОМОЩИ
ПРИ БОЛЕЗНИ АЛЬЦГЕЙМЕРА
Категория возрастная: взрослые
Стадия: деменция при болезни Альцгеймера
Осложнения: без осложнений
Вид медицинской помощи: специализированная медицинская помощь
Условия оказания медицинской помощи: стационарно
Форма оказания медицинской помощи: плановая
Средние сроки лечения (количество дней): 30
Код по МКБ X F00.0 Деменция при болезни Альцгеймера с
Нозологические единицы ранним началом (G30.0+)
F00.1 Деменция при болезни Альцгеймера с
F00.2 Деменция при болезни Альцгеймера,
атипичная или смешанного типа (G30.8+)
1. Медицинские мероприятия для диагностики заболевания, состояния
Прием (осмотр, консультация) врача-специалиста
Наименование медицинской
услуги
Усредненный
показатель
частоты
предоставления
Усредненный
показатель
кратности
применения
Прием (осмотр,
консультация) врача-
невролога первичный
Прием (осмотр,
консультация) врача-
психотерапевта первичный
Прием (осмотр,
консультация) врача-
психиатра первичный
Прием (осмотр,
консультация) врача-
психиатра повторный
Прием (осмотр,
консультация) врача-
терапевта первичный
Прием (осмотр,
консультация) врача
функциональной диагностики
первичный
Прием (тестирование,
консультация) медицинского
психолога первичный
Вероятность предоставления медицинских услуг или назначения лекарственных препаратов для медицинского применения (медицинских изделий), включенных в стандарт медицинской помощи, которая может принимать значения от 0 до 1, где 1 означает, что данное мероприятие проводится 100% пациентов, соответствующих данной модели, а цифры менее 1 — указанному в стандарте медицинской помощи проценту пациентов, имеющих соответствующие медицинские показания.
Лабораторные методы исследования
Наименование медицинской
услуги
Усредненный
показатель
частоты
предоставления
Усредненный
показатель
кратности
применения
Исследование тиреотропина
сыворотки крови
Исследование уровня
фолиевой кислоты в
сыворотке крови
Общий (клинический) анализ
крови развернутый
Анализ крови биохимический
общетерапевтический
Инструментальные методы исследования
Наименование медицинской
услуги
Усредненный
показатель
частоты
предоставления
Усредненный
показатель
кратности
применения
Расшифровка, описание и
интерпретация
электрокардиографических
данных
Магнитно-резонансная
томография головного мозга
Компьютерная томография
головы
Описание и интерпретация
компьютерных томограмм
Описание и интерпретация
магнитно-резонансных
томограмм
Наименование медицинской
услуги
Усредненный
показатель
частоты
предоставления
Усредненный
показатель
кратности
применения
Тестологическое
психодиагностическое
обследование
2. Медицинские услуги для лечения заболевания, состояния и контроля за лечением
Прием (осмотр, консультация) и наблюдение врача-специалиста
Наименование медицинской
услуги
Усредненный
показатель
частоты
предоставления
Усредненный
показатель
кратности
применения
Прием (осмотр,
консультация) врача-
невролога повторный
Прием (осмотр,
консультация) врача-
психиатра повторный
Прием (осмотр,
консультация) врача-
терапевта повторный
Наблюдение и уход за пациентом медицинскими работниками со средним
(начальным) профессиональным образованием
Наименование медицинской
услуги
Усредненный
показатель
частоты
предоставления
Усредненный
показатель
кратности
применения
Внутримышечное введение
лекарственных препаратов
Внутривенное введение
лекарственных препаратов
Лабораторные методы исследования
Наименование медицинской
услуги
Усредненный
показатель
частоты
предоставления
Усредненный
показатель
кратности
применения
Общий (клинический) анализ
крови развернутый
Инструментальные методы исследования
Наименование медицинской
услуги
Усредненный
показатель
частоты
предоставления
Усредненный
показатель
кратности
применения
Расшифровка, описание и
интерпретация
электрокардиографических
данных
Немедикаментозные методы профилактики, лечения и медицинской реабилитации
Наименование медицинской
услуги
Усредненный
показатель
частоты
предоставления
Усредненный
показатель
кратности
применения
Семейное психологическое
консультирование
Процедуры по адаптации к
условиям микросреды
Процедуры по адаптации к
условиям макросреды
Транскраниальная магнитная
стимуляция
Воздействие излучением
видимого диапазона через
зрительный анализатор
(цветоимпульсная терапия)
3. Перечень лекарственных препаратов для медицинского применения, зарегистрированных на территории Российской Федерации, с указанием средних суточных и курсовых доз
Анатомо-
терапевтическо-
химическая
классификация
Наименование
лекарственного
препарата
Усредненный
показатель
частоты
предоставления
Пиперидиновые
производные
фенотиазина
Диазепины,
оксазепины и
тиазепины
Другие
антипсихотические
средства
Бензодиазепино-
подобные средства
Другие
психостимуляторы и
ноотропные препараты
Другие препараты для
лечения деменции
4. Виды лечебного питания, включая специализированные продукты лечебного питания
Наименование вида
лечебного питания
Усредненный показатель частоты
предоставления
Основной вариант
стандартной диеты
Международная статистическая классификация болезней и проблем, связанных со здоровьем, X пересмотра.
Международное непатентованное или химическое наименование лекарственного препарата, а в случаях их отсутствия — торговое наименование лекарственного препарата.
1. Лекарственные препараты для медицинского применения, зарегистрированные на территории Российской Федерации, назначаются в соответствии с инструкцией по применению лекарственного препарата для медицинского применения и фармакотерапевтической группой по анатомо-терапевтическо-химической классификации, рекомендованной Всемирной организацией здравоохранения, а также с учетом способа введения и применения лекарственного препарата.
2. Назначение и применение лекарственных препаратов для медицинского применения, медицинских изделий и специализированных продуктов лечебного питания, не входящих в стандарт медицинской помощи, допускаются в случае наличия медицинских показаний (индивидуальной непереносимости, по жизненным показаниям) по решению врачебной комиссии (часть 5 статьи 37 Федерального закона от 21.11.2011 N 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» (Собрание законодательства Российской Федерации, 28.11.2011, N 48, ст. 6724; 25.06.2012, N 26, ст. 3442)).
источник
Если у вас есть родственник или знакомый, страдающий болезнью Альцгеймера, то описанный здесь протокол, возможно, сможет помочь.
Представляем вашему вниманию перевод оригинальной статьи Дейла Бредесена, директора отдела нейродегенеративных заболеваний медицинского факультета Калифорнийского университета в Лос-Анджелесе (UCLA), автора «The End of Alzheimer’s: The First Program to Prevent and Reverse Cognitive Decline» (Конец болезни Альцгеймера: первая программа предотвращения и восстановления когнитивных функций).
В двух предыдущих исследованиях мы получили первые результаты восстановления когнитивных функций при болезни Альцгеймера и состояниях пред-деменции, таких как MCI (Mild Cognitive Impairment — Умеренное Когнитивное Нарушение) и SCI (Subjective Cognitive Impairment — Субъективное Когнитивное Нарушение). В общей сложности 19 пациентов показали устойчивое субъективное и объективное улучшение когнитивных функций.
Этого удалось достичь с помощью системного, персонализированного протокола лечения. Протокол включает выявление факторов, которые потенциально могут вносить вклад в развитие деменции, таких как воспаление, вызванное патогенными микроорганизмами или повышенной кишечной проницаемостью, снижение атрофической или гормональной поддержки, воздействие специфических токсинов и др.
Оценив индивидуальный профиль заболевания для каждого пациента, все потенциальные факторы, способствующие снижению когнитивных функций, подвергаются коррекции. Этот комплексный, персонализированный протокол лечения изначально назывался MEND (Metabolic Enhancement of Neurodegeneration — метаболическое укрепление при нейродегенеративных заболеваниях), а сейчас носит название ReCode (Reversal of Cognitive Decline — восстановление когнитивных функций).
Очевидный недостаток предыдущих исследований — небольшая выборка пациентов. Поэтому в настоящем исследовании мы описали 100 пациентов, получивших лечение у нескольких врачей, с документально подтвержденным восстановлением когнитивных функций. Это исследование может послужить основой для будущего рандомизированного контролируемого клинического испытания протокола.
Сегодня болезнь Альцгеймера является третьей основной причиной смерти в США [1-6], и разработка эффективного лечения и профилактики является важнейшей задачей здравоохранения. Тем не менее, все клинические испытания препаратов-кандидатов для лечения болезни Альцгеймера практически полностью провалились.
Причин такой череды неудач может быть несколько: (1) учитывая длительный пред-симптомный период, лечение обычно начинают на поздних стадиях патофизиологического процесса; (2) то, что называется болезнью Альцгеймера, не является единичным заболеванием, а скорее имеет несколько различных подтипов [3,4]; (3) так же, как и для других сложных хронических заболеваний, таких как сердечно-сосудистые заболевания, возможно существует множество потенциальных факторов, способствующих развитию болезни Альцгеймера, таких как воспаление, различные хронические инфекции, снижение выработки гормонов, инсулинорезистентность, сосудистая недостаточность, травма или воздействие определенных токсинов.
Следовательно, монотерапевтический, монофазный подход, вероятно, будет неоптимальным, а персонализированные, многофазные протоколы, основанные на генетике и биохимии каждого пациента в отдельности, могут быть предпочтительными. Данный протокол может также помочь тестированию монотерапевтических препаратов, если тестировать их фоне соответствующей терапии. (4)
Модель болезни Альцгеймера, на которой основаны лекарственные мишени (например, амилоид-β-пептид), может быть неточной или неполной моделью заболевания. Так, было показано, что пептид Aβ функционирует как антимикробный пептид [11]. Это наводит на мысль, что болезнь Альцгеймера может быть уменьшающей плотность синапсов (network-downsizing) защитной реакцией, на некоторые типы неблагоприятных факторов: патогены/воспаление, токсины, дефицит питательных веществ, гормонов или атрофических факторов [5].
Мы отстаиваем принципиально иной взгляд на болезнь Альцгеймера [1,2,5,7], в котором белок-предшественник амилоида APP (Amyloid Precursor Protein), функционирует как молекулярный переключатель благодаря своей активности в качестве интегрирующего рецептора зависимости [8-10], т.е. если он получает оптимальное количество атрофических факторов, APP расщепляется в альфа-сайте, что приводит к продукции двух синаптобластных пептидов, sAPPα и αCTF.
Напротив, в отсутствие оптимального количества атрофических факторов APP расщепляется в сайтах бета, гамма и каспазы, что приводит к продукции четырех синаптокластных пептидов, sAPPβ, Aβ, Jcasp и C31. В этой модели воспаление оказывает антитрофический эффект на APP, частично посредством индукции бета-секретазы BACE (Beta-site APP-cleaving enzyme) и гамма-секретазы ядерным фактором NF-κB. Точно так же токсины, такие как двухвалентные металлы (например, ртуть), оказывают антитрофический эффект на APP, поскольку они приводят к увеличению продукции токсин-связывающего пептида Aβ. Эта модель согласуется с открытием того факта, что пептид Aβ функционирует в качестве антимикробного пептида [11], что указывает на то, что болезнь Альцгеймера может являться защитной реакцией на некоторые типы неблагоприятных факторов: патогены/воспаление, токсины, дефицит питательных веществ, гормонов или атрофических факторов [5].
Такая модель предполагает, что развитие болезни Альцгеймера зависит от соотношения синаптокластической и синаптобластической активности [5]. Эта концепция подразумевает режим лечения, при котором для каждого пациента выявляется множество факторов синаптобластической и синаптокластической активности, после чего создается индивидуальная программа нацеленная на каждый фактор, увеличивая синаптобластическую и уменьшая синаптокластическую активность. Некоторые примеры: (1) выявление и лечение патогенных микроорганизмов, например, вирусы семейства Borrelia, Babesia или Herpes; (2) выявление и лечение повышенной кишечной пронициаемости, коррекция микробиома; (3) выявление инсулинорезистентности и повышенного гликирования, повышение чувствительности к инсулину и снижения гликирования; (4) выявление и коррекция неоптимальной питательной, гормональной или трофической поддержки (включая сосудистую); (5) выявление токсинов (металлотоксины и другие неорганические вещества, органические токсины или биотоксины), снижение воздействия токсинов и детоксикация. Поскольку каждый пациент имеет различную комбинацию многих факторов, подход к лечению является прицельным и персонализированным.
Ниже мы описываем 100 пациентов, которые получали терапию на основе этого системного, персонализированного подхода, и показали восстановление когнитивных функций.
68-летняя женщина начала замечать парафазические ошибки в своей речи, достаточно серьезные, чтобы это начали замечать окружающие. У нее развилась депрессия, и она получала лечение антидепрессантом. Она начала испытывать трудности с повседневной деятельностью, такой как покупки, готовка и работа за компьютером, общение с внучкой. Она перепутала минутную и часовую стрелку на часах. У нее были сложности с правописанием. Ее симптомы прогрессировали, и она начала забывать свое ежедневное расписание. Она была очень обеспокоенна, когда забыла забрать своих внуков в школе дважды за двухнедельный период.
У нее был установлен гетерозиготный генотип по ApoE (3/4). Имела амилоид, PET сканирование (флорбетапир) было положительным. На МРТ уменьшение объема гиппокампа до 14-го процентиля для ее возраста. Высокочувствительный С-реактивный белок (hs-CRP) составлял 1,1 мг/л, инсулин натощак 5,6 мМЕ/л, гемоглобин A1c 5,5%, гомоцистеин 8,4 micromol/L, витамин B12 471 пг/мл, свободный трийодтиронин (свободный Т3) 2,57 пг/мл, тиреостимулирующий гормон (TSH) 0,21 мМЕ/л, альбумин 3,7 г/дл, глобулин 2,7 г/дл, общий холестерин 130 мг/дл, триглицериды 29 мг/дл, сывороточный цинк 49 мкг/дл, фактор комплемента 4a ( C4a) 7990 нг/мл, трансформирующий фактор роста бета-1 (TGF-β1) 4460 пг/мл и матриксная металлопротеиназа-9 497 нг/мл.
Был поставлен диагноз «Умеренное когнитивное нарушение (MCI)», и она приняла участие в клиническом испытании анти-амилоидного антитела. Однако с каждым введением испытываемого препарата ее когнитивные функции ухудшались на 3-5 дней, а затем возвращались к исходному состоянию. После четырех сеансов лечения, она прекратила участие в исследовании.
Она начала лечение с помощью системного подхода, описанного здесь ранее [1]. Результаты теста на когнитивные способности MoCA увеличились с 24 до 30 в течение 17 месяцев и оставались стабильными в течение 18 месяцев. Объем гиппокампа увеличился с 14-го процентиля до 28-го. Симптомы заметно улучшились: сложности с правописанием ушли, ее речь улучшилась, а ее способность ходить по магазинам, готовить и работать за компьютером — все улучшилось и оставалось стабильным при дальнейшем наблюдении.
73-летняя женщина врач жаловалась на проблемы с памятью и подбором слов, которые начались около 20 лет назад, но усугубились за последний год, что привело к тому, что ее близкий друг описал ее память «катастрофической». Она не могла вспомнить недавние разговоры, пьесы, которые видела, или книги, которые читала, путала имена людей и домашних животных. Ей было трудно ориентироваться, даже трудно найти дорогу к столу в ресторане после посещения туалета.
Фтордезоксиглюкозо-позитронно-эмиссионная томография (FDG-PET) показала снижение утилизации глюкозы в теменной и височной области. МРТ выявила уменьшением объема гиппокампа (16-й процентиль по возрасту). Когнитивное тестирование поставило ее на 9-й процентиль для ее возраста. Генотип ApoE был 3/3, глюкоза натощак 90 мг/дл, гемоглобин A1c 5,3%, инсулин натощак 1,6 мМЕ/л, гомоцистеин 14,1 micromol/L, TSH 4,1 мМЕ/мл, свободный T3 2,6 пг/мл, обратный T3 22,6 нг/дл, витамин В12 202 пг/мл, витамин D 27,4 нг/мл, общий холестерин 226 мг/дл, ЛПНП 121 мг/дл, ЛПВП 92 мг/дл и ртуть 7 нг/мл.
Через 12 месяцев, в результате лечения с применением системного подхода, описанного ранее [1], тестирование ее когнитивных функций улучшилось с 9-го до 97-го процентиля. Ее близкий друг отметил, что ее память улучшилась с состояния «катастрофического» до «просто паршивого» и, наконец, до «нормального». Она остается на терапевтической программе и продолжает наблюдать улучшения.
62-летняя женщина страдала от снижения когнитивных функций, усталости, плохого сна и депрессии. Она потеряла способность запоминать имена, вести бухгалтерский учет, который делала ранее, вести свой бизнес.
Индекс массы тела составлял 24, с преобладанием абдоминального жира. МоСА был 20. Она была ApoE4 гетерозиготной (3/4). Уровень глюкозы в сыворотке натощак 101 мг/дл, гемоглобин A1c 6,1%, инсулин натощак 14 мМЕ/л, hs-CRP 1,7 мг/л, 25-гидроксихолекальциферол 24 нг/мл, TSH 2,4 мМЕ/л, свободный T3 2,9 пг/мл, обратный T3 19 нг/дл, эстрадиол Подписывайтесь на наш канал VIBER!
Хотя на этом не делался акцент в описанных здесь случаях, некоторые наблюдения все же были сделаны. Например, близкие пациентов отмечали, что они были «более вовлечены» и более отзывчивы на лечение именно в этом испытании. Распознавание лиц, навигация и память часто улучшались, тогда как вычисления и афазия улучшались реже. Для тех, у кого были выявлены специфические патогены или токсины, улучшение не происходило до тех пор, пока они не были устранены. Те пациенты, у которых наблюдался меньший упадок к началу лечения, отвечали с большей готовностью и полнее, чем те, кто находился на более поздней стадии болезни, что не удивительно. Тем не менее, были примеры улучшения даже с оценками MoCA, равными нулю.
Таким образом, таргетный, персонализированный подход к проблеме, который учитывает множество потенциальных факторов, способствующих снижению когнитивных функций у каждого пациента в отдельности, перспективен для лечения болезни Альцгеймера и его предвестников: MCI и SCI.
Улучшения, задокументированные у 100 пациентов, описанных здесь, могут послужить основой для проведения проспективного рандомизированного контролируемого клинического испытания, особенно с учетом отсутствия на сегодняшний день эффективного альтернативного лечения этого распространенного и тяжелого заболевания.
Мы благодарны многим врачам, которые анализируют и лечат пациентов с когнитивными нарушениями, используя этот комплексный протокол. Мы особенно благодарны доктору Мэри Кей Росс, Хилари Шафто и Маргарет Конгер за посещение некоторых пациентов, о которых здесь сообщалось, доктору Кристине Локкен, доктору Джонатану Канику и доктору Катаюну Шахроху Уолтерсу за нейропсихологическое тестирования некоторых пациентов, Аманде Уильямс и Cytoplan Ltd. за предоставление некоторых добавок для некоторых пациентов, Джеймсу и Филлис Истон за неоценимую поддержку в исследовании, а также Фонду Evanthea за поддержку в подготовке клинического испытания.опубликовано econet.ru.
Dale E Bredesen1, Kenneth Sharlin2, David Jenkins3, Miki Okuno3, Wes Youngberg4, Sharon Hausman Cohen5, Anne Stefani5, Ronald L Brown6, Seth Conger6, Craig Tanio7, Ann Hathaway8, Mikhail Kogan9, David Hagedorn10, Edwin Amos11, Amylee Amos12, Nathaniel Bergman13, Carol Diamond14, Jean Lawrence15, Ilene Naomi Rusk16, Patricia Henry16 and Mary Braud16
- 1. Department of Molecular and Medical Pharmacology, David Geffen School of Medicine, University of California, Los Angeles, Los Angeles, CA, USA
- 2. Sharlin Health and Neurology/Functional Medicine, Ozark, MO, USA
- 3. NeuroHub, Sydney, Australia
- 4. Youngberg Lifestyle Medicine Clinic, Temecula, CA, USA
- 5. Resilient Health, Austin, TX, USA
- 6. Carolina Healthspan Institute, Charlotte, NC, USA
- 7. Rezilir Health, Hollywood, FL, USA
- 8. Integrative Functional Medicine, San Rafael, CA, USA
- 9. GW Center for Integrative Medicine, George Washington University, Washington, DC, USA
- 10. Coastal Integrative Medicine, Jacksonville, NC, USA
- 11. Department of Neurology, University of California, Los Angeles, Los Angeles, CA, USA
- 12. Amos Institute, Los Angeles, CA, USA
- 13. Center for Functional Medicine, Cleveland Clinic, Cleveland, OH, USA
- 14. Mount Sinai Hospital, New York, NY, USA
- 15. Lawrence Health and Wellness, Toccoa, GA, USA
- 16. Brain and Behavior Clinic, Boulder, CO, USA
P.S. И помните, всего лишь изменяя свое сознание — мы вместе изменяем мир! © econet
Понравилась статья? Тогда поддержи нас, жми:
источник
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК — 2015
Название протокола:Деменция при болезни Альцгеймера
Деменция Альцгеймера – это первичная дегенеративная болезнь головного мозга неизвестной этиологии с характерныминейропатологическими и нейрохимическими проявлениями. Болезнь обычно начинается незаметно и медленно, но неуклонно прогрессирует в течение нескольких лет. [1]
Код протокола:
Коды МКБ-10:
F00.0* Деменция при болезни Альцгеймера с раннимначалом (до 65 лет).
F00.1* Деменция при болезни Альцгеймера с поздним началом (65 лет и старше).
F00.2* Деменция при болезни Альцгеймера, атипичная или смешанноготипа.
F00.9* Деменция при болезни Альцгеймеранеуточненная.
Сокращения, используемые в протоколе:
| АЛТ – | аланинаминотрансфераза |
| АСТ – | аспартатаминотрансфераза |
| ВВК – | военно-врачебная комиссия |
| В\м – | внутримышечно |
| В\в – | внутривенно |
| КТ – | компьютерная томография |
| ЛС– | лекарственные средства |
| МЗСР– | Министерство здравоохранения и социального развития |
| МНН– | международное непатентованное название (генерическое название) |
| МРТ– | магнитно-резонансная томография |
| МСЭК – | медико-социальная экспертная комиссия |
| ОАК– | общий анализ крови |
| ОАМ– | общий анализ мочи |
| ОКИ– | острые кишечные инфекции |
| ПЭТ – | позитронно-эмиссионная томография |
| РЭГ– | реоэнцефалография |
| РК – | Республика Казахстан |
| Р-р– | раствор |
| СИОЗС – | селективные ингибиторы обратного захвата серотонина |
| СПЭК – | судебно-психиатрическая экспертная комиссия |
| ЭКГ – | электрокардиограмма |
| ЭПО – | экспериментально-психологическое обследование |
| ЭЭГ – | электроэнцефалограмма |
| ЭхоЭГ – | эхоэлектроэнцефалограмма |
Дата разработки протокола: 2015 год.
Категория пациентов: взрослые.
Пользователи протокола: врачи-психиатры (психотерапевты).
Оценка на степень доказательности приводимых рекомендаций.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортных или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |
Диагностические критерии [1,8-10]:
Жалобы и анамнез:
Жалобы: ухудшение памяти,дезориентировка в собственной личности, утрата бытовых навыков.
Анамнез: постепенное интеллектуальное снижение.
Клинические признаки:
Требуется наличие обоих признаков:
Ухудшение памяти, наиболее заметное в области усвоения новой информации, хотя в более тяжелых случаях может нарушаться и воспроизведение ранее усвоенной информации. Расстройство касается как вербального, так и невербального материала. Снижение памяти должно подтверждаться объективно надежным анамнезом от информанта и, по возможности, дополняться данными нейропсихологического тестирования или количественной оценки когнитивных способностей. Уровни выраженности ухудшения памяти следует оценивать следующим образом (пороговое диагностическое значение имеет легкое нарушение памяти):
Легкое расстройство памяти. Повседневная деятельность затруднена, хотя все же возможно независимое проживание. Нарушено главным образом усвоение нового, материала. Например, могут отмечаться трудности в повседневной жизни в фиксации, хранении и воспроизведении, касающиеся местонахождения бытовых предметов, социальных договоренностей или информации, полученной от родственников.
Умеренное расстройство. Нарушение памяти представляет собой серьезное препятствие для повседневной жизни. Удерживается только очень хорошо усвоенный или очень знакомый материал. Новая информация удерживается лишь случайно или на очень короткое время. Больной не в состоянии вспомнить основные сведения о том, где он живет, что он недавно делал или как зовут его знакомых.
Тяжелое расстройство. Эта степень нарушения памяти характеризуется полной неспособностью усвоенной информации. Больной не в состоянии узнать даже близких родственников.
Снижение других когнитивных способностей характеризуется ослаблением критики и мышления, например, в планировании и организации, а также ухудшением общей обработки информации.
Подтверждение этому должно основываться, если возможно, на данных объективного анамнеза и по возможности дополняться нейропсихологическими тестами или количественными объективными оценками. Должно устанавливаться ухудшение по сравнению с предыдущим более высоким уровнем продуктивности.
Степень снижения должна оцениваться следующим образом (пороговое диагностическое значение имеет легкое нарушение):
Легкое нарушение. Снижение когнитивных способностей вызывает нарушение продуктивности в повседневной жизни, не обуславливая, однако зависимости больного от других. Невозможны более сложные повседневные задачи и формы досуга.
Умеренное нарушение. Снижение интеллектуальных способностей делает невозможным функционирование в повседневной жизни без посторонней помощи, включая покупки в магазинах и обращение с деньгами. В пределах дома может выполняться лишь простая работа. Интересы очень ограничены и поддерживаются плохо.
Тяжелое нарушение. Ухудшение характеризуется отсутствием или фактическим
отсутствием разумного мышления.
Общая тяжесть деменции лучше всего определяется уровнем нарушения памяти ИЛИ интеллекта, в зависимости от того, что более выражено (например, при легком расстройстве памяти и умеренном интеллектуальном нарушении деменция оценивается как деменция умеренной тяжести).
Снижение эмоционального контроля или мотивации, или изменение социального поведения, проявляющееся минимум одним из следующих признаков:
· эмоциональная лабильность;
· раздражительность;
· апатия;
· огрубение социального поведения;
Минимум одно из следующих требований:
· данные о прогрессировании;
· в дополнение к нарушению памяти должны отмечаться афазия (амнестическая или сенсорная), аграфия, алексия, акалькулия или апраксия (вовлечение височной, теменной и (или) лобной долей);
Отсутствие данных физического или специального обследования или данных из анамнеза о другой возможной причине деменции (например, о цереброваскулярном заболевании, заболевании, обусловленном БИЧ, болезни Паркинсона, болезни Гентингтона, гидроцефалии с нормальным внутричерепным давлением), системном заболевании (например, гипотиреоидизме, дефиците витамина В 12 или фолиевой кислоты, гиперкальциемии) или о злоупотреблении алкоголем или наркотиками.
Физикальное обследование: корковые нарушения при нейропсихологическом или неврологическом обследовании.
Диагностические исследования:
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне:
· экспериментально-психологическое обследование.
Дополнительные диагностические обследования, проводимые на амбулаторном уровне:
· ОАК;
· ОАМ;
· биохимический анализ крови (печеночные пробы);
· ЭКГ – проводятся с целью мониторинга изменений соматического состояния на фоне основной терапии;
· ЭЭГ – при эпилептических и эпилептиформных пароксизмах;
· ЭхоЭГ – при появлении симптомов угнетения сознания;
· РЭГ – при признаках нарушения кровообращения в головном мозге;
· КТ, МРТ – проводятся с целью уточнения области головного мозга, преимущественно вовлеченной в патологический процесс.
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию:согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
Основные (обязательные) диагностические обследования, проводимые в стационаре:
· ОАМ – не реже 1 раза в месяц;
· ОАК – не реже 1 раза в месяц;
· биохимический анализ крови (АЛТ, АСТ, билирубин (прямой и непрямой, уровень глюкозы в крови) – не реже 1 раза в месяц;
· ЭКГ – не реже 1 раза в месяц;
· ЭПО (для поступивших впервые в жизни или впервые в текущем году).ЭПО для иных категорий пациентов – по решению лечащего врача.
Дополнительные диагностические обследования, проводимыев стационаре:
· ЭЭГ – при эпилептических и эпилептиформных пароксизмах;
· ЭхоЭГ – при появлении симптомов угнетения сознания;
· РЭГ – при признаках нарушения кровообращения в головном мозге;
· КТ, МРТ – проводятся с целью уточнения области головного мозга, преимущественно вовлеченной в патологический процесс.
Инструментальное обследование: нарастание медленно-волновой активности (преимущественно ее q-диапазона, чаще низкой или средней амплитуды) и D-активности, а также редукция a-ритма в виде снижения его амплитуды и сглаженности региональных различий по сравнению с возрастной нормой. Выраженность b-активности, как правило, была снижена. Довольно часто (у трети больных) наблюдаются генерализованные билатерально-синхронные q- и D-волны, превышающие по амплитуде основную активность Наибольшей диагностической информативностью обладает такой признак, как нарастание медленно-волновой активности, степень его диагностической значимости колеблется от 68 до 91%.
Показания для консультации специалистов:
· консультация терапевта (педиатра) – исключение соматических заболеваний;
· консультация невропатолога – исключение текущих неврологических расстройств;
· консультация гинеколога (для женщин) – исключение гинекологических расстройств;
· консультации иных узких специалистов – сопутствующие соматические заболевания и\или патологические состояния.
Дифференциальный диагноз [8-10]:
источник
1 Рекомендовано Экспертным советом РГП на ПХВ «Республиканский центр развития здравоохранения» Министерства здравоохранения и социального развития Республики Казахстан от «15» сентября 2015 года Протокол 9 КЛИНИЧЕСКИЙ ПРОТОКОЛ ДИАГНОСТИКИ И ЛЕЧЕНИЯ I. ВВОДНАЯ ЧАСТЬ: ДЕМЕНЦИЯ ПРИ БОЛЕЗНИ АЛЬЦГЕЙМЕРА 1. Название протокола:деменция при болезни Альцгеймера. 2. Код протокола: 3. Коды МКБ-10: F00.0* Деменция при болезни Альцгеймера с раннимначалом (до 65 лет). F00.1* Деменция при болезни Альцгеймера с поздним началом (65 лет и старше). F00.2* Деменция при болезни Альцгеймера, атипичная или смешанноготипа. F00.9* Деменция при болезни Альцгеймеранеуточненная. 4. Сокращения, используемые в протоколе: АЛТ аланинаминотрансфераза АСТ аспартатаминотрансфераза ВВК военно-врачебная комиссия В\м внутримышечно В\в внутривенно КТ компьютерная томография ЛС лекарственные средства МЗСР Министерство здравоохранения и социального развития МНН международное непатентованное название (генерическое название) МРТ магнитно-резонансная томография МСЭК медико-социальная экспертная комиссия ОАК общий анализ крови ОАМ общий анализ мочи ОКИ острые кишечные инфекции ПЭТ позитронно-эмиссионная томография РЭГ реоэнцефалография РК Республика Казахстан Р-р раствор
2 СИОЗС СПЭК ЭКГ ЭПО ЭЭГ ЭхоЭГ селективные ингибиторы обратного захвата серотонина судебно-психиатрическая экспертная комиссия электрокардиограмма экспериментально-психологическое обследование электроэнцефалограмма эхоэлектроэнцефалограмма 5. Дата разработки протокола: 2015 год. 6. Категория пациентов: взрослые. 7. Пользователи протокола: врачи-психиатры (психотерапевты). II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ: Оценка на степень доказательности приводимых рекомендаций. Шкала уровня доказательности: А Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. В Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортных или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. С Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. D Описание серии случаев или неконтролируемое исследование или мнение экспертов. GPP Наилучшая фармацевтическая практика. 8. Определение: Деменция Альцгеймера это первичная дегенеративная болезнь головного мозга неизвестной этиологии с характерныминейропатологическими и нейрохимическими проявлениями. Болезнь обычно начинается незаметно и медленно, но неуклонно прогрессирует в течение нескольких лет. [1] 2
3 9. Клиническая классификация: нет. 10. Показания для госпитализации[2,3]: 10.1 Добровольная (экстренная и плановая) госпитализация: психопатологические расстройства психотического и\или непсихотического уровня с десоциализирующимипроявлениями, проявления которых не купируются в амбулаторных условиях или решение экспертных вопросов (МСЭК, ВВК, СПЭК) Принудительная госпитализация без решения суда наличие психопатологических расстройств и действий, обусловливающих: непосредственную опасность для себя и окружающих; беспомощность, то есть неспособность самостоятельно удовлетворять основные жизненные потребности, при отсутствии надлежащего ухода; существенный вред здоровью вследствие ухудшения психического состояния, если лицо будет оставлено без психиатрической помощи Принудительная госпитализация по определению суда, постановлению следственных органов и\или прокураторы. 11. Диагностические исследования: 11.1 Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне: экспериментально-психологическое обследование Дополнительные диагностические обследования, проводимые на амбулаторном уровне: ОАК; ОАМ; биохимический анализ крови (печеночные пробы); ЭКГ проводятся с целью мониторинга изменений соматического состояния на фоне основной терапии; ЭЭГ при эпилептических и эпилептиформных пароксизмах; ЭхоЭГ при появлении симптомов угнетения сознания; РЭГ при признаках нарушения кровообращения в головном мозге; КТ, МРТ проводятся с целью уточнения области головного мозга, преимущественно вовлеченной в патологический процесс Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию:согласно внутреннему 3
4 регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения Основные (обязательные) диагностические обследования, проводимые в стационаре: ОАМ не реже 1 раза в месяц; ОАК не реже 1 раза в месяц; биохимический анализ крови (АЛТ, АСТ, билирубин (прямой и непрямой, уровень глюкозы в крови) не реже 1 раза в месяц; ЭКГ не реже 1 раза в месяц; ЭПО (для поступивших впервые в жизни или впервые в текущем году).эпо для иных категорий пациентов по решению лечащего врача Дополнительные диагностические обследования, проводимыев стационаре: ЭЭГ при эпилептических и эпилептиформных пароксизмах; ЭхоЭГ при появлении симптомов угнетения сознания; РЭГ при признаках нарушения кровообращения в головном мозге; КТ, МРТ проводятся с целью уточнения области головного мозга, преимущественно вовлеченной в патологический процесс. 12. Диагностические критерии[1,8-10]: 12.1 Жалобы и анамнез: Жалобы: ухудшение памяти,дезориентировка в собственной личности, утрата бытовых навыков. Анамнез: постепенное интеллектуальное снижение. Клинические признаки: Требуется наличие обоих признаков: Ухудшение памяти, наиболее заметное в области усвоения новой информации, хотя в более тяжелых случаях может нарушаться и воспроизведение ранее усвоенной информации. Расстройство касается как вербального, так и невербального материала. Снижение памяти должно подтверждаться объективно надежным анамнезом от информанта и, по возможности, дополняться данными нейропсихологического тестирования или количественной оценки когнитивных способностей. Уровни выраженности ухудшения памяти следует оценивать следующим образом (пороговое диагностическое значение имеет легкое нарушение памяти): Легкое расстройство памяти. Повседневная деятельность затруднена, хотя все же возможно независимое проживание. Нарушено главным образом усвоение нового, материала. Например, могут отмечаться трудности в повседневной жизни в фиксации, хранении и воспроизведении, касающиеся местонахождения бытовых предметов, социальных договоренностей или информации, полученной от родственников. 4
5 Умеренное расстройство. Нарушение памяти представляет собой серьезное препятствие для повседневной жизни. Удерживается только очень хорошо усвоенный или очень знакомый материал. Новая информация удерживается лишь случайно или на очень короткое время. Больной не в состоянии вспомнить основные сведения о том, где он живет, что он недавно делал или как зовут его знакомых. Тяжелое расстройство. Эта степень нарушения памяти характеризуется полной неспособностью усвоенной информации. Больной не в состоянии узнать даже близких родственников. Снижение других когнитивных способностей характеризуется ослаблением критики и мышления, например, в планировании и организации, а также ухудшением общей обработки информации. Подтверждение этому должно основываться, если возможно, на данных объективного анамнеза и по возможности дополняться нейропсихологическими тестами или количественными объективными оценками. Должно устанавливаться ухудшение по сравнению с предыдущим более высоким уровнем продуктивности. Степень снижения должна оцениваться следующим образом (пороговое диагностическое значение имеет легкое нарушение): Легкое нарушение. Снижение когнитивных способностей вызывает нарушение продуктивности в повседневной жизни, не обуславливая, однако зависимости больного от других. Невозможны более сложные повседневные задачи и формы досуга. Умеренное нарушение. Снижение интеллектуальных способностей делает невозможным функционирование в повседневной жизни без посторонней помощи, включая покупки в магазинах и обращение с деньгами. В пределах дома может выполняться лишь простая работа. Интересы очень ограничены и поддерживаются плохо. Тяжелое нарушение. Ухудшение характеризуется отсутствием или фактическим отсутствием разумного мышления. Общая тяжесть деменции лучше всего определяется уровнем нарушения памяти ИЛИ интеллекта, в зависимости от того, что более выражено (например, при легком расстройстве памяти и умеренном интеллектуальном нарушении деменция оценивается как деменция умеренной тяжести). Снижение эмоционального контроля или мотивации,или изменение социального поведения, проявляющееся минимум одним из следующих признаков: эмоциональная лабильность; раздражительность; апатия; огрубение социального поведения; Минимум одно из следующих требований: 5
6 данные о прогрессировании; в дополнение к нарушению памяти должны отмечаться афазия (амнестическая или сенсорная), аграфия, алексия, акалькулия или апраксия (вовлечение височной, теменной и (или) лобной долей); Отсутствие данных физического или специального обследования или данных из анамнеза о другой возможной причине деменции (например, о цереброваскулярном заболевании, заболевании, обусловленном БИЧ, болезни Паркинсона, болезни Гентингтона, гидроцефалии с нормальным внутричерепным давлением), системном заболевании (например, гипотиреоидизме, дефиците витамина В 12 или фолиевой кислоты, гиперкальциемии) или о злоупотреблении алкоголем или наркотиками Физикальное обследование: корковые нарушения при нейропсихологическом или неврологическом обследовании Лабораторное обследование: специфических диагностических изменений нет Инструментальное обследование: нарастание медленно-волновой активности (преимущественно ее q-диапазона, чаще низкой или средней амплитуды) и D-активности, а также редукция a-ритма в виде снижения его амплитуды и сглаженности региональных различий по сравнению с возрастной нормой. Выраженность b-активности, как правило, была снижена. Довольно часто (у трети больных) наблюдаются генерализованные билатерально-синхронные q- и D-волны, превышающие по амплитуде основную активность Наибольшей диагностической информативностью обладает такой признак, как нарастание медленно-волновой активности, степень его диагностической значимости колеблется от 68 до 91% Показания для консультации специалистов: консультация терапевта (педиатра) исключение соматических заболеваний; консультация невропатолога исключение текущих неврологических расстройств; консультация гинеколога (для женщин) исключение гинекологических расстройств; консультации иных узких специалистов сопутствующие соматические заболевания и\или патологические состояния Дифференциальный диагноз [8-10]: Таблица 1 Дифференциальная диагностика. Параметры Деменция Легкое когнитивное расстройство Клиническая картина Тотальное снижение Клинически выраженные признаки когнитивного уровня, снижения интеллектуальной 6
7 Инструментальное обследование Анамнез снижение (отсутствие) продуктивности критики Наличие органических изменений головного мозга Данные за процессуальный характер расстройств с нарастанием когнитивного дефицита Часто указания на травму или иное повреждение головного мозга 13. Цели лечения: достижение медикаментозной ремиссии, стабилизация состояния пациента. 14. Тактика лечения [3-10, 12-20]: При оценке микросоциальных условий как удовлетворительных и\или нетяжелом уровне расстройства рекомендуется преимущественно амбулаторное лечение. В случае усложненной клинической картины (за счет коморбидных состояний) и\или неэффективности вмешательства на амбулаторном этапе решается вопрос о стационировании Немедикаментозное лечение: Комплаенс — терапия, различные виды психотерапии, трудотерапия. Режимы наблюдения (в зависимости от состояния пациента): общий режим наблюдения — круглосуточное наблюдение без ограничения передвижения в отделении. режим частичной госпитализации — возможность нахождения в отделении в дневное или ночное время с учетом необходимости его адаптации во внебольничных условиях. режим лечебных отпусков — возможность нахождения, по решению ВКК вне отделения от нескольких часов до нескольких суток, с целью постепенной адаптации к внебольничным условиям, решения бытовых и социальных вопросов, а также оценки достигнутого лечебного эффекта. усиленный режим наблюдения — круглосуточное наблюдение и ограничение передвижения за пределами отделения. строгий режим наблюдения — круглосуточное непрерывное наблюдение, постоянное сопровождение медицинским персоналом в отделении и за его пределами Медикаментозное лечение: Основные ЛС (таблицы 2 и 4): Холинергические препараты предназначены для блокирования обратного захвата ацетилхолинэстеразы (патогенетическое лечение) (донепезил, мемантин). Дополнительные ЛС (таблица 3 и 5): Малые нейролептики предназначены для коррекции поведенческих нарушений либо для терапии психотических расстройств в пожилом и старческом возрасте (хлорпротиксен, сульпирид) Нормотимические препараты предназначены для стабилизации настроения, 7
8 медикаментозного контроля нарушений биологических ритмов (вальпроевая кислота) Транквилизаторы препараты, предназначенные для купирования тревожных состояний Гипнотики препараты, нормализующие ритм сон-бодрствование (зопиклон) Медикаментозное лечение, оказываемое на амбулаторном уровне[4-7,9,12-21]: Таблица 2 Основные медикаменты. Рекомендуется монотерапия: одно из нижеперечисленных препаратов. МНН Терапевтический Курс лечения диапазон Донепезил (УД А) До 10мг\сутки От нескольких месяцев Мемантин (УД А) мг\сутки до нескольких лет Таблица 3 Дополнительные медикаменты. Препараты применяются исключительно как сопутствующая терапия при наличии в клинической картине коморбидных основным проявлениям заболевания состояний (тревоги, поведенческих расстройств, фазовых колебаний настроения) МНН Хлорпротиксен (УД С) Сульпирид (УД В) Вальпроевая кислота (УД В) Тофизопам (УД А) Зопиклон (УД А) Терапевтический диапазон мг\сутки До 600мг\сутки мг\сутки мг\сутки До 15 мг\сутки Курс лечения до исчезновения поведенческих нарушений До признаков стабилизации эмоционального фона До купирования тревожных проявлений 7-10 дней Медикаментозное лечение, оказываемое на стационарном уровне[4-7,9,12-21]: Таблица 4 Основные медикаменты: Рекомендуется монотерапия: одно из нижеперечисленных препаратов. МНН Терапевтический диапазон Курс лечения Донепезил (УД А) До 10мг\сутки На период Мемантин (УД А) мг\сутки 8 стационарного пребывания
9 Таблица 5 Дополнительные медикаменты: Препараты применяются исключительно как сопутствующая терапия при наличии в клинической картине коморбидных основным проявлениям заболевания состояний (тревоги, поведенческих расстройств, фазовых колебаний настроения) МНН Терапевтический Курс лечения Хлорпротиксен (УД С) диапазон мг\сутки До 600мг\сутки Сульпирид (УД В) Вальпроевая кислота (УД В) мг\сутки Тофизопам (УД А) 9 до исчезновения поведенческих нарушений До признаков стабилизации эмоционального фона мг\сутки До купирования тревожных проявлений Зопиклон (УД А) До 15 мг\сутки 7-10 дней 14.3 Другие виды лечения: нет Хирургическое лечение: нет Профилактические мероприятия [8-10]: Первичная профилактика нет. Вторичная профилактика обоснованное назначение психофармакопрепаратов. Третичная профилактика комплаенс-терапия, психосоциальная реабилитация, реализация психообразовательных программ для членов семей пациентов. Факторы риска ремиссия низкого качества, снижение количества социальных связей пациента Дальнейшее ведение (после стационара) формирование и укрепление комплаенса. 15. Индикаторы эффективности лечения: Устранение клинических симптомов Настроенность больного и\или его семьи на продолжение лечения на амбулаторном этапе Отсутствие негативной реакции на необходимость приема психотропных средств III. ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ВНЕДРЕНИЯ ПРОТОКОЛА: 16. Разработчики: 1) Джолдыгулов Г.А. кандидат медицинских наук, сотрудник
10 Республиканского научно-практического центра психиатрии, психотерапии и наркологии 2) Распопова Н.И. доктор медицинских наук, доцент кафедры психиатрии, психотерапии и наркологии РГП на ПХВ «Казахский национальный медицинский университет имени С.Д. Асфендиярова» 3) Нуркатов Е.М. кандидат медицинских наук, директор«медицинский центр проблем психического здоровья» (Астана) 4) Сатбаева Э.М. кандидат медицинских наук РГП на ПХВ «Казахский национальный медицинский университет им. С.Д. Асфендиярова», заведующая кафедрой фармакологии, клинический фармаколог. 17. Конфликта интересов нет. 18. Рецензент: 1) Толстикова А.Ю. доктор медицинских наук, профессор кафедры психиатрии, психотерапии и наркологии Казахского национального медицинского университета имени С.Д. Асфендиярова. 2) Семки А.В. доктор медицинских наук, профессор Федерального государственного бюджетного научного учреждения «Научно-исследовательского института психического здоровья», заместитель директора по научной и лечебной работе, РФ г. Томск. 19. Условия пересмотра протокола:пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности. 20. Список использованной литературы: 1. Международная Классификация болезней (10-й пересмотр). Классификация психических и поведенческих расстройств (Клинические описания и указания по диагностике). ВОЗ, Кодекс РК «О здоровье народа и системе здравоохранения»от 18 сентября 2009 г. 193-IV. 3. Приказ и.о. Министра Здравоохранения РК 15 от «Об утверждении положения о деятельности психиатрических организаций в РК». 4. Авруцкий Г.Я., Недува А.А. Лечение психически больных: Руководство для врачей. 2 издание, переработанное и дополненное. Москва «Медицина», Арана Дж., Розенбаум Дж. Руководство по психофармакотерапии.-4-е изд Мосолов С.Н. Основы психофармакотерапии. М. «Восток» 1996г- 288 с. 7. Яничак и соавт. Принципы и практика психофармакотерапии. Киев с. 8. Блейхер В.М., Крук И.В.. Толковый словарь психиатрических терминов. Воронеж НПО «МОДЭК», Руководство по психиатрии/под редакцией А.С.ТигановаТ1-2 Москва «Медицина»,
источник
Статья основана на положениях «Протокола ведения пациентов с болезнью Паркинсона», разработанного группой экспертов, в которую вошли ведущие отечественные специалисты по болезни Паркинсона (БП), и утвержденного Минздравсоцразвития РФ в 2005 г. Положения Протокола основаны на анализе в соответствии с принципами доказательной медицины контролируемых исследований, проведенных в нашей стране и за рубежом [1, 2, 4–7, 9–11, 13, 15], и в целом соответствуют недавно опубликованным рекомендациям по лечению БП Европейской федерации неврологических обществ [8] и Американской академии неврологии [12, 14, 16]. Текст Протокола опубликован в журнале «Проблемы стандартизации в здравоохранении» [3]. В Протоколе используется следующая шкала убедительности доказательств данных: А — доказательства убедительны (есть веские доказательства предлагаемому утверждению), B — относительная убедительность доказательств (есть достаточно доказательств в пользу того, чтобы рекомендовать данное предложение), C — достаточных доказательств нет (имеющиеся доказательства недостаточны для вынесения рекомендаций, но они могут быть даны с учетом иных обстоятельств).
Общие принципы. Поскольку на данный момент нейропротекторный потенциал ни одного средства при БП убедительно не доказан, лечение основывается главным образом на симптоматическом действии противопаркинсонических средств, которые принято назначать в том случае, когда хотя бы одно из проявлений заболевания приводит к ограничению жизнедеятельности пациента.
Лечение начинается с монотерапии. Если препарат оказался неэффективным (нет регресса симптоматики в течение месяца после достижения оптимальной дозы) или плохо переносится, его заменяют средством той же или другой фармакологической группы. При выборе препарата и его дозы следует стремиться не к полному устранению симптомов, а к существенному улучшению функций, позволяющему поддерживать бытовую и профессиональную активность. При частичном эффекте (недостаточное улучшение функций) к принимаемому препарату последовательно добавляют лекарственные средства иной фармакологической группы.
Принципы выбора противопаркинсонического препарата. Выбор препарата на начальном этапе лечения проводят с учетом возраста, выраженности двигательного дефекта, трудового статуса, состояния нейропсихологических функций, наличия сопутствующих соматических заболеваний, индивидуальной чувствительности пациента. Помимо достижения оптимального симптоматического контроля, выбор препарата определяется необходимостью отсрочить момент развития моторных флуктуаций и дискинезий (табл.).
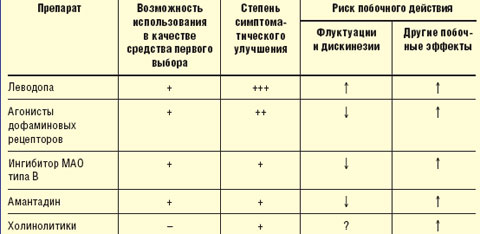 |
| Таблица Выбор препарата для начального лечения болезни Паркинсона |
У лиц моложе 50 лет при умеренной выраженности двигательных нарушений в отсутствие выраженных когнитивных нарушений назначают один из следующих препаратов: агонист дофаминовых рецепторов, ингибитор моноаминооксидазы (МАО) типа В (селегилин), амантадин, антихолинергические средства (тригексифенидил, бипериден).
Лечение предпочтительнее начинать с одного из агонистов дофаминовых рецепторов, которые хотя и не позволяют достичь того же уровня симптоматического контроля, как препараты леводопы, способны обеспечить поддержание уровня жизнедеятельности пациентов в течение длительного времени, отсрочить назначение леводопы и тем самым развитие осложнений долгосрочной терапии леводопой (уровень А). Индивидуальную эффективную дозу препаратов подбирают путем медленного титрования, стремясь получить адекватный эффект, необходимый для продолжения профессиональной деятельности, и избежать побочного действия (уровень С). Неэрголиновые агонисты (пирибедил, прамипексол) ввиду более благоприятного профиля побочных эффектов предпочтительнее, чем эрголиновые (бромокриптин).
Лечение пирибедилом начинают с дозы 50 мг 1 раз в день (днем или вечером — после основного приема пищи), в дальнейшем суточную дозу увеличивают на 50 мг 1–2 раза в неделю — до достижения необходимого эффекта, но не выше 250 мг/сут (50 мг 5 раз в день). Лечение прамипексолом начинают с дозы 0,125 мг 3 раза в день (после еды), затем еженедельно дозу последовательно увеличивают до 0,25 мг 3 раза в день, 0,5 мг 3 раза в день, при недостаточном эффекте — до 1 мг 3 раза в день и 1,5 мг 3 раза в день (максимальная доза — 4,5 мг/сут). Лечение бромокриптином начинают с дозы 2,5 мг 3 раза в день, в дальнейшем ее еженедельно последовательно увеличивают до 5 мг 3 раза в день, 7,5 мг 3 раза в день, 10 мг 3 раза в день, 10 мг 4 раза в день (максимальная доза — 40 мг/сут). При появлении тошноты в период титрования назначают домперидон. При неэффективности или плохой переносимости одного из агонистов дофаминовых рецепторов может быть испробован другой агонист дофаминовых рецепторов или препарат другой фармакологической группы (уровень С).
Антихолинергические средства показаны при наличии выраженного тремора покоя и сохранности нейропсихологических функций (уровень С). Хотя у этой категории лиц они могут применяться в качестве средств первого выбора, более целесообразно их добавление к агонисту дофаминовых рецепторов, если последний не обеспечивает достаточного подавления тремора. Лечение тригексифенидилом начинают с дозы 1 мг 2 раза в день, в дальнейшем дозу не чаще чем 1 раз в неделю последовательно увеличивают до 2 мг 2 раза в день, 2 мг 3 раза в день, 2 мг 4 раза в день (максимальная доза — 10 мг/сут). Лечение бипериденом начинают с дозы 1 мг 2 раза в день, в дальнейшем дозу не чаще чем 1 раз в неделю последовательно увеличивают до 2 мг 2 раза в день, 2 мг 3 раза в день, 2 мг 4 раза в день (максимальная доза — 10 мг/сут).
Лечение амантадином начинают с дозы 100 мг 2 раза в день, при недостаточном эффекте она может быть увеличена до 100 мг 3 раза в день, в дальнейшем — до 100 мг 4–5 раз в день (максимальная доза — 500 мг/сут). Лечение селегилином начинают с дозы 5 мг утром, через 1 нед ее увеличивают до 5 мг 2 раза в день.
Если указанные препараты и их комбинация в максимально переносимых дозах не обеспечивают адекватного состояния двигательных функций и социальной адаптации больных, назначают препарат, содержащий леводопу (стандартный препарат или препарат с замедленным высвобождением) в минимальной эффективной дозе (уровень А).
У лиц в возрасте 50–70 лет при умеренном двигательном дефекте и относительной сохранности нейропсихологических функций лечение начинают с одного из агонистов дофаминовых рецепторов. Если максимальные переносимые дозы одного из этих препаратов не обеспечивают достаточного функционального улучшения, к нему последовательно добавляют по указанным выше схемам один из следующих препаратов: селегилин, амантадин или холинолитик (при наличии тремора покоя). Больным после 65 лет тригексифенидил и другие антихолинергические средства не следует назначать из-за риска ухудшения познавательных функций и других побочных эффектов (уровень В). При недостаточной эффективности к комбинации из двух-трех указанных выше препаратов добавляют средство, содержащее леводопу, в минимальной эффективной дозе (200–400 мг/сут).
У лиц в возрасте 50–70 лет при выраженном двигательном дефекте, ограничивающем трудоспособность и/или возможность самообслуживания, а также при наличии выраженных когнитивных нарушений и необходимости получения быстрого эффекта, лечение начинают с препаратов, содержащих леводопу. Для лечения могут быть использованы как стандартные препараты, так и препараты с замедленным высвобождением. Если небольшие дозы леводопы (200–400 мг/сут) не обеспечивают необходимого улучшения, к ним последовательно добавляют по указанным выше схемам следующие препараты: агонист дофаминовых рецепторов, амантадин, селегилин.
У лиц старше 70 лет лечение следует начинать со средств, содержащих леводопу. Для лечения могут применяться как стандартные препараты, содержащие леводопу, так и препараты с замедленным высвобождением (уровень В).
Другие меры. Поскольку дофаминергические препараты у больных с глаукомой могут повысить внутриглазное давление, перед их назначением у всех пациентов старше 40 лет следует измерить внутриглазное давление. В дальнейшем его измерение проводят после подбора противопаркинсонической терапии (обычно на втором месяце лечения) либо при появлении жалоб на ухудшение зрения. Больным с запорами и другими проявлениями нарушения моторики желудочно-кишечного тракта показана диета с высоким содержанием пищевых волокон (уровень С); при снижении массы тела показана диета с повышенным содержанием белковых продуктов, а также продуктов, богатых витаминами и микроэлементами (уровень С); для подбора диеты назначается консультация врача-диетолога.
При ограничении подвижности и наличии скелетно-мышечных болей показано проведение лечебной физкультуры, включающей упражнение на растяжение мышц, поддержание гибкости и тренировку координации движений (уровень С), физиотерапии (уровень С), рефлексотерапии (уровень С); в связи с этим назначаются консультации врача лечебной физкультуры, физиотерапевта, рефлексотерапевта. Больному рекомендуется посильная двигательная активность с ежедневными занятиями лечебной гимнастикой, по показаниям — занятия с логопедом. В зависимости от тяжести двигательных расстройств больной может продолжать прежнюю работу, перейти на более легкую, изменить условия работы (неполный рабочий день). При стойкой утрате трудоспособности больному определяется группа инвалидности (вопросы трудоспособности определяются МСЭК).
Алгоритм лечения БП представлен на рисунке.
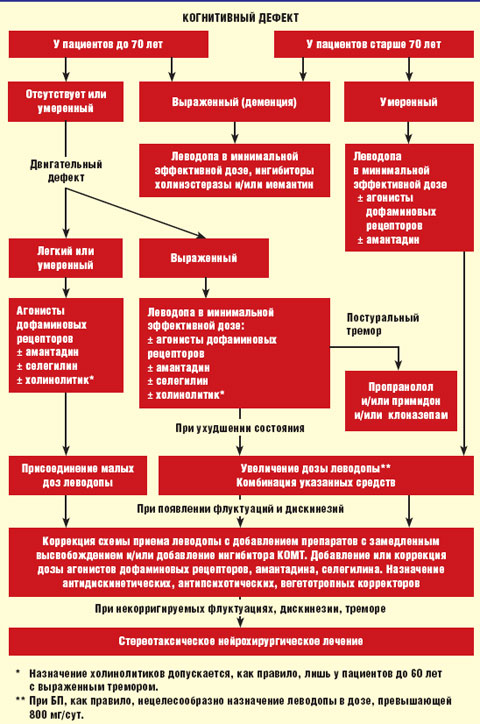 |
| Рисунок. Алгоритм лечения болезни Паркинсона |
Общие принципы лечения. Индивидуальную эффективную дозу препаратов подбирают путем медленного титрования, стремясь получить адекватный эффект, необходимый для продолжения профессиональной деятельности или поддержания повседневной активности, и избежать побочного действия. При необходимости для усиления эффекта противопаркинсонической терапии проводятся следующие мероприятия.
- Увеличение дозы принимаемого препарата — при необходимости до максимального рекомендуемого уровня.
- Замена препарата, не оказавшего терапевтического эффекта в максимальной дозе или вызвавшего неприемлемое побочное действие даже в минимальной терапевтической дозе, препаратом из той же или другой фармакологической группы. Замена препарата одной группы на препарат другой группы (например, холинолитика, амантадина или селегилина на агонист дофаминовых рецепторов) производится путем постепенной отмены принимавшегося ранее препарата с параллельным титрованием дозы вновь назначенного средства до получения эффекта. Во избежание рикошетного усиления симптоматики следует избегать внезапной отмены любого противопаркинсонического препарата, даже если он не оказывал видимого эффекта. Замена принимаемого препарата на иной препарат этой же группы (например, одного агониста дофаминовых рецепторов на другой либо препарата леводопы с одним ингибитором ДОФА-декарбоксилазы — например, карбидопой, на препарат леводопы с другим ингибитором ДОФА-декарбоксилазы (например, бенсеразидом — или наоборот).
- Добавление к ранее назначенному средству, оказавшему частичный эффект, препарата другой группы с переходом от монотерапии к комбинированной терапии (например, к агонисту дофаминовых рецепторов можно добавить малые дозы леводопы — или наоборот).
- Назначение дополнительных средств, воздействующих на отдельные симптомы (например, дрожание или депрессию).
Особенности лечения больных с тремором. При выраженном дрожательном гиперкинезе, нарушающем функции конечностей, особенно если он имеет постурально-кинетический компонент, к противопаркинсоническим средствам при отсутствии противопоказаний добавляют пропранолол (уровень В). Лечение пропранололом начинают с дозы 10 мг 3 раза в день. В дальнейшем дозу последовательно увеличивают не чаще чем 1 раз в неделю до 20 мг 3 раза в день, 40 мг 3 раза в день, 40 мг 4 раза в день (максимально до 320 мг/сут в 3–4 приема). При наличии противопоказаний к применению пропранолола (брадиаритмия, сахарный диабет, заболевания периферических сосудов), непереносимости или неэффективности препарата назначают примидон (уровень С). Первоначально препарат назначают в дозе 31,25 мг на ночь, затем дозу последовательно увеличивают 1 раз в 7–10 дней до 62,5 мг на ночь, 125 мг на ночь, 250 мг на ночь (максимально до 750 мг/сут в 2–4 приема или однократно на ночь).
Если пропранолол вызвал недостаточное улучшение, то к нему добавляют примидон в указанных дозах (уровень С). Клоназепам может быть добавлен к пропранололу или примидону при наличии выраженного кинетического компонента тремора (уровень С). Клоназепам первоначально назначают в дозе 0,5 мг на ночь, затем 1 раз в 7–10 дней дозу последовательно увеличивают до 0,5 мг 2 раза в день, 1 мг 2 раза в день, 2 мг 2 раза в день, пока не будет достигнуто существенное ослабление дрожания. При выраженном треморе может быть также использован клозапин в дозе 12,5–50 мг/сут (уровень В).
Особенности лечения больных с аффективными нарушениями. При наличии аффективных нарушений назначается консультация врача-психотерапевта для решения вопроса о целесообразности проведения аутогенной тренировки или других методов психотерапии. При наличии депрессии у больных без выраженных нарушений познавательных функций лечение следует начинать с одного из агонистов дофаминовых рецепторов (прамипексол, пирибедил), способных корригировать легкую депрессивную симптоматику, или их сочетания с малыми дозами леводопы (уровень В). При выраженной депрессивной симптоматике после консультации с психиатром показано назначение одного из следующих антидепрессантов: амитриптилин (25–150 мг на ночь), имипрамин (50–150 мг/сут), циталопрам (20–40 мг/сут), флуоксетин (20–40 мг/сут), сертралин (50–100 мг/сут), пароксетин (10–20 мг/сут), миртазапин (7,5–30 мг/сут), венлафаксин (75–225 мг/сут). После получения лечебного эффекта продолжительность назначения антидепрессанта в эффективной дозе должна быть не менее 6 мес (уровень С).
Продолжение читайте в следующем номере.
О. С. Левин, доктор медицинских наук, профессор
РМАПО, Центр экстрапирамидных заболеваний, Москва
источник