ПСВ — это при бронхиальной астме один из главных методов контроля за заболеванием, расшифровывается как «пиковая скорость выдоха» и измеряется пикфлоуметром. Это очень важный показатель, необходимый для полноценного мониторинга. Для получения картины заболевания в целом надо регулярно делать 2 основных исследования.
Спирометрия используется для взрослых и детей старше 5 лет и определяет ОФВ1 (объем форсированного выдоха за первую секунду) и ФЖЕЛ (форсированную жизненную емкость легких). Обычно проводится с применением бронхолитика быстрого действия. При проведении процедуры сначала измеряется ОФВ1 и ФЖЕЛ без применения лекарства, затем пациент вдыхает бронхолитик (например, Сальбутамол или Беротек) и примерно через 20-25 мин проводится повторная процедура спирометрии, которая позволяет узнать, насколько улучшились показатели ОФВ1 и ФЖЕЛ.
Эти показатели зависят от многих факторов, в том числе от возраста, пола и веса пациента, и могут разниться. По результатам спирометрии оценивают соотношение двух показателей (это называется индекс Тиффно — ИТ). В норме у взрослого человека ИТ должен превышать 0,80, а у детей — 0,90. Если есть понижение этого показателя, то можно говорить об обструкции, характерной для бронхитов или бронхиальной астмы.
Спирометрия проводится исключительно в больнице специалистом, перед началом врач подробно инструктирует пациента о том, как и когда надо дышать и выдыхать. Нос во время процедуры зажимается специальным зажимом, что может вызвать определенный дискомфорт у ребенка, потому перед тем, как вести его на спирометрию, родителям следует рассказать ребенку о том, что будет происходить в кабинете у врача, чтобы он не испугался, в противном случае процедура не сможет быть проведена. По окончании пациенту на руки выдается заключение с графиками.
Пикфлоуметрия — еще один метод обследования и контроля за течением бронхиальной астмы. В отличие от спирометрии, она может проводиться как в кабинете доктора, так и дома самостоятельно. Всем больным бронхиальной астмой врачи настоятельно рекомендуют приобрести пикфлоуметр и вести дневник пикфлоуметрии, чтобы регулярно замерять ПСВ.
ПСВ при бронхиальной астме необходимо знать для того, чтобы оценивать состояние больного и эффективность проводимой терапии.
Пикфлоуметр — небольшой портативный и относительно недорогой прибор, который можно приобрести в аптеке. У каждого больного бронхиальной астмой должен быть персональный прибор. Его необходимо содержать в чистоте и нежелательно давать в пользование другим людям.
Для того чтобы замерить ПСВ, следует полностью выдохнуть, затем сделать глубокий вдох и, плотно обхватив губами мундштук, резко выдохнуть в пикфлоуметр. При этом прибор держать надо ровно горизонтально, пальцами не перекрывая шкалы. После каждого замера указатель ставить на начальную отметку. Процедуру по возможности проводят стоя. Замеры следует делать утром и вечером до приема противоастматических препаратов, выдыхать — 3 раза, записывать наилучший результат в график пикфлоуметрии, который можно взять у врача или сделать самостоятельно, нарисовав систему координат на миллиметровой бумаге. Так можно будет отследить снижение ПСВ, что будет говорить о недейственной терапии.
При сильном понижении результата выдоха следует немедленно обратиться к врачу для лечения. На каждый прием пульмонолога больной должен приносить график пикфлоуметрии, чтобы специалист мог оценить ПСВ и понять, помогают или нет пациенту подобранные лекарственные препараты.
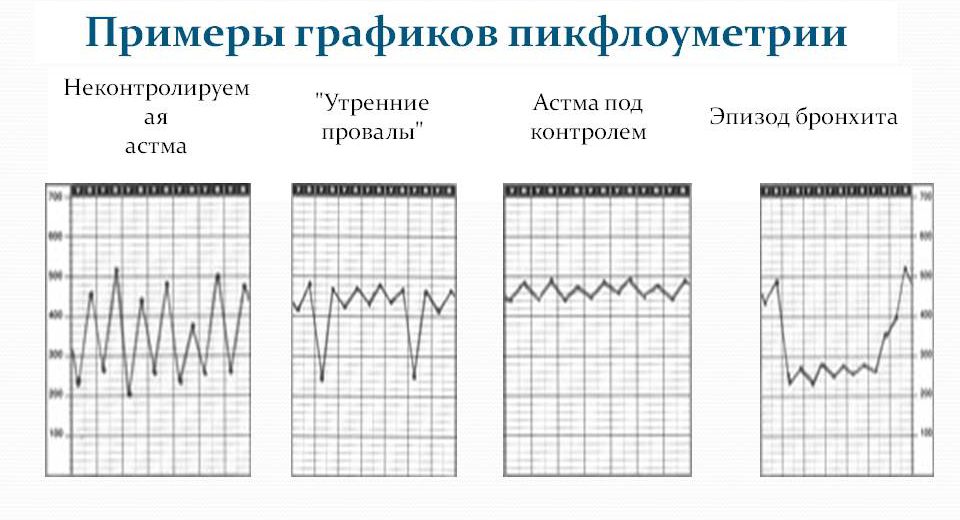
При правильном контроле за бронхиальной астмой график ПСВ близок к прямой линии, а вот если он резко скачет то вверх, то вниз, это уже может говорить о том, что терапия не помогает, контроль следует улучшить путем подбора других медикаментозных средств или увеличения дозы.
Для каждого пациента существует своя индивидуальная норма ПСВ, которую можно узнать у лечащего пульмонолога или рассчитать самостоятельно.
Для удобства врачей и пациентов была разработана систем трех цветовых зон результатов пикфлоуметрии.
Зеленая зона: лучший показатель ПСВ вне обострений следует умножить на 0,8 — это будет тем минимумом, являющимся нижней границей зеленой зоны. Если все значения выше этой цифры находятся в зеленой зоне, это значит, что терапия проходит успешно и поводов для беспокойства нет.
Желтая зона: здесь лучший показатель умножается на коэффициент 0,6, таким образом определяется нижняя граница желтой зоны. Если результаты пикфлоуметрии находятся в этой зоне, уже стоит прислушаться к организму: может появляться небольшая одышкаа, нарушения сна, затруднения в элементарных физических упражнениях. В этом случае необходимо обратиться к врачу, чтобы он либо назначил дополнительные медицинские препараты, либо увеличил дозу уже используемых. Не стоит игнорировать желтую зону — это может привести к развитию приступа и резкому и сильному обострению заболевания.
Красная зона — это все показатели, находящиеся после нижней границы желтой зоны. Это та зона, при которой появляется одышкаа и сильный кашель в состоянии покоя, становится очень трудно дышать, в груди появляется свист и сипы. Здесь, во-первых, необходим прием экстренных препаратов для быстрого купирования приступа, а во-вторых — срочное обращение к врачу для пересмотра лечебной терапии. Понижение показателей до этой зоны игнорировать ни в коем случае нельзя — это большая угроза для жизни.
Бронхиальная астма — заболевание, безусловно, тяжелое и неприятное, однако при правильном подходе к ее лечению как врача, так и самого пациента, она может протекать практически бессимптомно, не мешая человеку вести нормальную полноценную жизнь.
Роль пикфлоуметрии и самоконтроля при лечении этого заболевания очень важна, ведь таким образом человек может самостоятельно оценивать свое состояние и вовремя обращаться за врачебной помощью.
источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Как проводят диагностику астмы? Стадии болезни
Бронхиальная астма – это тяжелый недуг, который при неправильном лечении может привести к смертельному исходу. При подозрении на астму следует срочно посетить консультацию терапевта. Далее будут изложены способы определения этого заболевания, а также классификация заболевания, используемая современными врачами. Способы определения астмы направлены в первую очередь на выявление фактора, вызвавшего заболевание. Кроме этого врачам необходимо понять, насколько изменена работа органов дыхания. Классификация заболевания разработана исходя из сложности течения, а также степени изменения работы органов дыхательной системы.
Первая стадия диагностики: беседа и осмотр пациента
О наличии астмы могут говорить такие симптомы как кашель, особо донимающий в темное время суток, сиплое дыхание, припадки удушья, ощущение давления в груди. При астме эти признаки могут усиливаться после общения с домашними питомцами, контакте с цветами, бытовой химией, дымом, при волнении, тяжелых физических напряжениях, при попадании в слишком холодную или горячую атмосферу, а также в темное время суток. Также все признаки заболевания обостряются при любых недугах органов дыхания.
Нередко вместе с бронхиальной астмой у пациента обнаруживаются и иные недуги аллергического толка: экзема, атопический дерматит, алиментарная аллергия.
Во время обследования больного врач выявляет посинение носогубного треугольника, крапивницу или иные аллергические кожные проявления, поперечную морщину на носу, деформацию грудной клетки.
Вторая стадия: лабораторные исследования
Спирометрия – этот способ основан на определении величин, говорящих о состоянии органов дыхания. При бронхиальной астме диаметр дыхательных путей уменьшается, что не может не повлиять на работу органов дыхания. Так, в ходе спирометрии изучают два параметра: ОФВ1 или объем форсированного выдоха и ФЖЕЛ или форсированная жизненная емкость легких. У пациентов со здоровыми органами дыхания отношение этих двух величин друг к другу не менее восьмидесяти процентов. Если же оно менее восьмидесяти процентов – это говорит о наличии астмы.
Пикфлоуметрия – это обследование, которое определяет пиковую скорость выдоха. Данный способ является одним из основных при определении астмы. Для определения этого параметра применяют переносные пикфлоуметры, которые просты в использовании и невелики по размеру. Определение этого параметра нужно осуществлять после ночного сна, показатель следует фиксировать. Уменьшение ПСВ больше чем на двадцать процентов от физиологической нормы указывает на наличие бронхиальной астмы. Ежедневное фиксирование данного параметра дает возможность поставить диагноз, исправить погрешности в терапии, а также профилактировать осложнения недуга.
Тесты с физическими усилиями применяются в определении бронхиальной астмы. В период повышенных физических усилий у пациентов, страдающих этим заболеванием, уменьшаются основные параметры работы органов дыхания (ПСВ и ОФВ1).
Кожные аллергические пробы используются для выявления фактора, вызывающего аллергию при атопической форме заболевания. Обнаружение этого фактора дает возможность предотвратить приступы заболевания.
Существует такое понятие как «стадия предастмы» — это самые первые признаки появления заболевания. При выявлении явных признаков заболевания оно считается уже астмой. Но сегодня подобную формулировку применяют в единичных случаях. Здесь же она будет изложена, так как дает более четкую картину развития заболевания.
Согласно современной классификации заболевания, болезнь начинается с появления ее симптомов. Далее будет изложена данная классификация:
Первая фаза: интермиттирующая или переменная астма
- Приступы заболевания наблюдаются не чаще одного в семь суток,
- В темное время суток приступы бывают реже двух раз в четыре недели,
- Периоды обострения заболевания коротки,
- ОФВ1, а также ПСВ составляют восемьдесят процентов от физиологической нормы.
Вторая фаза: не тяжелая персистирующая или постоянная астма
- Признаки заболевания наблюдаются чаще, чем один раз в семь дней,
- Приступы ухудшают качество сна и работы пациента,
- В темное время суток приступы случаются чаще, чем два раза в четыре недели,
- ОФВ1 и ПСВ находятся на уровне восьмидесяти процентов от физиологической нормы.
Третья фаза: персистирующая астма средней тяжести
- Приступы наблюдаются каждый день, недуг обостряется регулярно,
- Достаточно часто наблюдаются и приступы в ночное время суток,
- Приступы очень сильно ухудшают качество сна, а также мешают работать пациенту,
- ОФВ1 и ПСВ находятся на уровне от шестидесяти до восьмидесяти процентов от физиологической нормы.
Четвертая фаза: сложная персистирующая астма
- Приступы наблюдаются каждый день, заболевание обостряется с небольшими промежутками,
- Приступы в темное время суток регулярны,
- Пациент не может вести нормальный образ жизни,
- ОФВ1 и ПСВ находятся на уровне шестьдесят или меньше процентов от нормы.
Автор: Пашков М.К. Координатор проекта по контенту.
источник
Бронхиальная астма – распространенное заболевание органов дыхательной системы хронического течения, требующее постоянного врачебного контроля. Только так можно отследить динамику болезни, предупредить осложнения и вовремя оказать помощь больным в случае приступа.
Но в повседневной жизни занятому на работе и в семье человеку не всегда удается регулярно посещать врача. С помощью пикфлоуметрии при бронхиальной астме пациент может самостоятельно мониторить свое состояние и при необходимости сразу же откорректировать дозу принимаемых лекарственных препаратов, предупредив обострение.
Пикфлоуметрия – популярный и доступный диагностический метод, позволяющий быстро определить при бронхиальной астме ПСВ — пиковую скорость выдоха. По этому показателю оценивают, насколько хорошо функционируют органы дыхания, есть ли спазм дыхательных путей.
Кроме того, эту методику используют для контроля эффективности назначенного лечения. Чтобы провести процедуру и сделать необходимые замеры, потребуется специальный прибор – пикфлоуметр. Для наглядности пикфлоуметрию можно сравнить с измерением артериального давления при гипертонии или же замером содержания глюкозы в крови при сахарном диабете.
Разобраться в устройстве и принципе действия прибора для измерения скорости дыхания совсем несложно, никаких особых навыков для этого не требуется.
Чаще всего пикфлоуметр представляет собой пластиковую трубку со шкалой, в которую пациент должен резко выдыхать. На шкале разными цветами выделено три зоны:
Однако существуют и электронные модели, где показатели выводятся на экран в цифровом виде. Отличаются они также производителем, стоимостью и дизайном исполнения. Но при этом колебания значений у разных приборов могут достигать 15%. По этой причине рекомендуется приобрести индивидуальный пикфлоуметр и применять только его.
Основной критерий, по которому различаются пикфлоуметры, – это возрастная категория. Для детей, так как они ниже ростом и имеют меньший вес, выпускаются приборы другого вида, чем для взрослых. Есть также универсальные устройства со сменными мундштуками, которые подходят и взрослым, и детям.
Не составит никакого труда сориентироваться в показаниях шкалы и самостоятельно определить, насколько стабильно состояние астматика. Особенно важно это, если бронхиальной астмой страдает ребенок, и регулярные замеры ПСВ нужно проводить ему.
Для бронхиальной астмы характерны спазмы бронхов и бронхиол, что затрудняет доступ воздуха в легкие и нарушает нормальную оксигенацию организма пациента. В результате развивается дыхательная недостаточность, что приводит к резкому ухудшению самочувствия больного.
Пиковая скорость выдоха, или ПСВ, – это показатель, который изменяется в зависимости ширины просвета в бронхах. Чем он больше, тем легче воздуху проходить по дыхательным путям и достигать легких, а значит, тем стабильнее состояние пациента. Потому процедура пикфлоуметрии при БА имеет огромное значение.
Основные цели пикфлоуметрии:
- Диагностика стадии заболевания и контроль эффективности проводимого лечения.
- Оценка гиперреактивности бронхов, нарастания воспалительного процесса, что позволяет установить степень нарушения их работы.
- Определение предрасположенности пациента к развитию бронхиальной астмы.
- Выявление причин заболевания. Пикфлоуметрию сначала проводят в условиях стационара или дома у больного, а затем на рабочем месте. Если на рабочем месте выявлено снижение ПСВ и сужение бронхов, значит, человек страдает профессиональной астмой (развитие болезни часто провоцирует вдыхание запыленного или загрязненного вредными веществами воздуха на протяжении длительного времени).
- Выяснение факторов, ставших толчком к развитию болезни и способных вызвать приступ бронхоспазма. С помощью пикфлоуметрии можно установить реакцию бронхов пациента на различные раздражители – пыльцу растений, бытовую пыль, химикаты и пр.
- Составление оптимальной схемы терапии. Посредством замера ПСВ выясняется, на какие медикаменты пациент реагирует лучше всего.
- Выявление особенностей динамики заболевания в разное время суток, в разных климатических условиях.
Благодаря пикфлоуметрии можно не только диагностировать бронхиальную астму и оценить ее степень тяжести, но и предотвратить развитие бронхоспазма, а также узнать, какими именно препаратами предпочтительней его лечить.
Основными показаниями к проведению пикфлоуметрии при подозрении на бронхиальную астму или уже поставленном диагнозе являются:
- Дифдиагностика патологий дыхательных путей, сопровождающихся спазмом бронхов.
- Мониторинг состояния при обострении бронхиальной астмы.
Существуют определенные правила проведения пикфлоуметрии при бронхиальной астме. Рекомендуется ознакомиться с ними и строго соблюдать, чтобы получить достоверный результат.
Врачи обычно дают пациентам памятку на консультации, чтобы они могли правильно проводить определение пиковой скорости выдоха в домашних условиях самостоятельно, без помощи медицинского работника.
Основные нюансы корректного проведения процедуры следующие:
- Для домашнего использования необходимо приобрести индивидуальный пикфлоуметр. Передавать его другим пациентам или брать у других категорически не рекомендуется.
- В сутки проводят не менее двух процедур, желательно утром, после пробуждения, и вечером, перед сном.
- Можно делать пикфлоуметрию и чаще, это совершенно безвредная и безболезненная процедура.
- Процедура заключается в резком трехкратном выдохе в трубку прибора. При этом выдыхать нужно на самом деле резко, между выдохами следует делать паузы продолжительностью в две-три минуты.
Если показания прибора резко изменяются и указывают на выраженные нарушения функционирования органов дыхательной системы, следует как можно быстрее обратиться к врачу за дополнительной консультацией. Скорее всего, требуется откорректировать схему приема медикаментозных препаратов.
Запомнить! Замер скорости выдоха не является принудительной процедурой, и только от пациента зависит, будет он выполнять ее регулярно или нет. Но следует понимать, что при таком непредсказуемом заболевании, как бронхиальная астма, пикфлоуметрия и ее результаты – единственная возможность самостоятельно выявить ухудшение состояния и вовремя внести корректировки в проводимую терапию.
Основные этапы проведения процедуры:
- Вынуть прибор из упаковки, продезинфицировать трубку или просто протереть, если прибор индивидуальный.
- Удобно сесть или встать, держать устройство параллельно полу и следить, чтобы ползунок оставался вначале шкалы совершенно неподвижным.
- Обхватить трубку губами и сделать резкий выдох. Язык не должен перекрывать вход в трубку. За одну процедуру делается три выдоха с небольшими интервалами.
- Очистить прибор с помощью воды и моющего средства для посуды, просушить.
- Внести полученные результаты в специальный дневник, он должен быть у каждого пациента.
- Сравнить новые результаты с предыдущими и при необходимости обратиться к доктору.
Проводят процедуру, как и было сказано выше, дважды в день. Никакой подготовки к ее выполнению не требуется. Достаточно просто несколько минут спокойно посидеть, расслабиться и успокоиться.
При бронхиальной астме у детей проводить измерения ПСВ должны родители или другие взрослые, ухаживающие за больным ребенком. Ребенок на момент проведения процедуры не должен быть голодным или сонным.
Дуть в трубку малышу предлагается так, как если бы он задувал свечи на торте. Перед замером пиковой скорости выдоха рекомендуется снять с ребенка тесную одежду и уговорить его спокойно посидеть полчаса.
Показатели пикфлоуметрии при бронхиальной астме у каждого пациента различны, так как у всех людей разная дыхательная активность. Норма у пациентов сильно отличается в зависимости от возраста, роста, пола и других индивидуальных особенностей.
Есть общепринятые стандарты, но это лишь ориентировочные показатели.
Чтобы определить, какова же норма ПСВ у конкретного пациента, его нужно обследовать на протяжении 21 дня в период ремиссии, когда его состояние стабильно и значительных нарушений дыхательных функций не отмечается. Затем составляется трехцветный график, который будет отображать минимальные и максимальные показатели. Именно по этому графику в дальнейшем пациент будет ориентироваться, все ли в порядке или нужно обратиться к врачу:
- Зеленая зона – оптимальные показатели для пациента, это означает, что он чувствует себя хорошо.
- Желтая зона – означает незначительное ухудшение состояние больного, при котором необходимо откорректировать дозировку принимаемых препаратов.
- Ползунок в красной зоне – состояние критическое, больному нужна срочная госпитализация.
Установленные общие нормальные показатели, по которым проводится расшифровка результатов измерений по пикфлоуметру, следующие:
- ПСВ выше 90% от нормы, высчитанной для пациента индивидуально, – состояние стабильное, не требующее корректировки лечения и консультации врача.
- ПСВ колеблется от 80% до 89% — изменять схему лечения пока нет необходимости, но пациент должен тщательно следить за своим состоянием.
- Показатель ПСВ колеблется от 50% до 79% от нормы – необходимо срочно откорректировать проводимую терапию.
- ПСВ ниже 50% от установленной нормы – больного нужно срочно госпитализировать, его состояние критическое.
Чтобы установить для зеленой зоны максимальное значение ПСВ при бронхиальной астме за время трехнедельного обследования пациента, наибольший показатель умножают на 0,8.
Чтобы получить цифровой эквивалент значения пиковой скорости для желтой зоны, означающей умеренное ухудшение состояния, наибольший результат умножают на 0,5. Все, что будет находиться ниже результатов желтой зоны, относится к красной, то есть к критической.
Для удобства можно скачать в интернете таблицы средних норм для мужчин, женщин и детей, распечатать их и сделать памятку. У женщин и детей цифры будут ниже, чем у мужчин, что вполне естественно, так как дыхательная активность у них от природы тоже ниже.
Обычно при покупке пикфлоуметра пациент сразу получает дневник, куда он будет вносить все данные ПСВ после утренних и вечерних замеров. В дневнике предусмотрен график пикфлоуметрии, рассчитанный на 4 недели.
В норме цифровые показатели должны быть примерно одинаковыми, а если соединить точки, которыми в графике отмечаются показатели ПСВ, то должна получиться почти ровная линия. У больного астмой график имеет вид кривой с зубцами разного размера.
Пикфлоуметрия – современный и доступный для каждого пациента способ самостоятельно контролировать свое состояние в домашних условиях.
С помощью этой процедуры можно минимизировать риск обострений, а также отследить динамику болезни и оценить эффективность проводимой терапии. Главное – правильно пользоваться прибором, делать все расчеты корректно и не забывать вносить их в дневник.
источник
Многие люди не знают, что такое астма, и часто путают это заболевание с аллергической реакцией. Современная медицина дает этому недугу следующее определение: астма это хроническая болезнь органов дыхания, которая может иметь различную этиологию. Она сопровождается характерной симптоматикой, которая позволяет специалистам заподозрить у пациента наличие патологии.
Астма – заболевание, характерной особенностью которого являются приступы удушья, кашля и одышки. Согласно данным статистики, которую ведут многие медицинские учреждения из разных стран мира, на сегодняшний день почти 10% населения земного шара страдает от этого недуга. Стремительное увеличение численности больных началось с середины 1980-х годов.
Специалисты такую динамику объясняют ухудшением экологической обстановки во всем мире. Люди вынуждены проживать в регионах, в которых воздух загрязнен нефтепродуктами и отходами тяжелой промышленности. Также повлияло на рост заболеваемости ухудшение качества пищи. Сегодня многие организации используют при выращивании скота, птицы, овощей и фруктов вредные добавки, которые ускоряют рост, но негативно отражаются на качестве и безопасности. Стоит отметить и малоподвижный образ жизни, который ведет большая часть населения.
Бронхиальная астма может развиваться у людей под воздействием разнообразных факторов, которые могут быть не только внешними, но и внутренними.
Современная медицина выделяет следующие причины развития патологии:
- Проживание в экологически неблагоприятном регионе. Данные статистики показывают, что среди людей, которые проживают по соседству с промышленными и перерабатывающими предприятиями, насчитывается большое количество астматиков. Высокий уровень заболеваемости этим недугом отмечается и в регионах с высокой влажностью и холодным климатом.
- Домашняя пыль. Если люди пренебрегают регулярной уборкой жилых помещений, то они автоматически включаются в группу риска заболеть астмой. Это обусловлено тем, что в пыли содержатся не только мельчайшие частички, но и большое количество патогенных микроорганизмов, которые могут выступать для людей в качестве аллергенов и провоцировать приступы астмы.
- Вредные привычки. В данном случае речь идет о курении. Люди, которые постоянно курят табачные изделия, а также различные ароматизированные смеси, чаще сталкиваются с заболеваниями органов дыхания.
- Систематический контакт с бытовой химией и использование косметических средств. В их составе присутствуют вредные для здоровья людей вещества, которые могут провоцировать развитие патологических реакций, в частности астмы.
- Вредные условия труда. Многие люди вынуждены трудиться на промышленных предприятиях, работать со строительными материалами и красками. Постоянный контакт с вредными испарениями провоцирует заболевания дыхательных путей.
- Перенесенные стрессы, постоянное психо-эмоциональное напряжение, депрессии и прочие нервные расстройства приводят к развитию серьезных патологий.
- Продолжительный прием медицинских препаратов может стать причиной развития астмы. Особенно вредны противовоспалительные нестероидные лекарства, а также Аспирин.
- Неправильное питание приводит к нарушению обменных процессов и развитию или обострению хронических заболеваний. Приступы астмы могут вызвать продукты, в составе которых присутствуют химические добавки и красители.
- Болезни дыхательных путей, такие как пневмония, трахеит, бронхит, и другие патологии, имеющие инфекционную этиологию, часто становятся причиной развития астмы.
В качестве внутренних причин, способных спровоцировать развитие астмы, специалисты рассматривают нарушения в работе таких систем:
Также учитывается и наследственная предрасположенность к бронхиальной астме. Результаты многочисленных исследований этой патологии показали, что у родителей, которые страдают от этого недуга, практически в 35% случаях рождаются дети, имеющие склонность к данному заболеванию. Такую форму астмы современная медицина классифицирует как аллергическую.
Каждый человек может заподозрить у себя развитие недуга по первичной симптоматике:
- Даже после незначительной физической нагрузки появляется одышка.
- Начинается кашель, который изначально бывает сухим, а спустя время у больных начинает отходить прозрачная мокрота.
- Пациент может без причины начать чихать.
- В груди появляется ощущение заложенности, сдавленности.
- Начинаются приступы удушья.
- На кожных покровах могут проявляться высыпания, характерные для крапивницы.
- У больных часто появляются хрипы при бронхиальной астме, которые сопровождаются характерным свистом.
- Дыхание становится поверхностным, при каждом выдохе ощущаются сложности. Чтобы сделать полный выдох человеку приходится садиться на кровать или на стул и крепко держаться за спинку.
Если человек заметит у себя такие признаки, то ему необходимо как можно быстрее обратиться в медицинское учреждение для консультации, комплексной диагностики и получения адекватной медикаментозной помощи.
Современная медицина определяет основную симптоматику, которая всегда сопровождает бронхиальную астму:
- Появляется общее недомогание, развивается слабость во всем теле.
- Нарушается сердечный ритм. У большинства больных развивается тахикардия. Во время приступов частота пульса увеличивается до 130 ударов в минуту.
- Начинаются приступы удушья.
- Появляется ощущение заложенности в груди.
- При продолжительных приступах возникают болевые ощущения в нижней части грудной клетки.
- Начинается головокружение, может развиваться сильная головная боль.
Если у человека наблюдается тяжелое течение недуга, то у него проявляется следующая симптоматика:
- Может увеличиться в размерах сердце.
- Кожные покровы изменяют привычный оттенок и приобретают синюшный цвет.
- Развивается акроцианоз.
- Появляются признаки эмфиземы легких. У пациента ослабевает дыхание, увеличивается в размерах грудная клетка.
- У больного появляется сонливость.
- Могут развиваться параллельные болезни, имеющие аллергическую этиологию.
Эта патология классифицируется следующим образом:
По этиологии
По степени тяжести
Особые формы
Экзогенная. Приступы случаются из-за проникновения в дыхательные пути аллергенов
Интермиттирующая. Появляются кратковременные приступы, частота которых не превышает 1 раза в неделю. ПСВ – менее 20%
Атопическая. Патология развивается на фоне плохой наследственности
Эндогенная. Эта форма патологии развивается под воздействием внутренних факторов. Например, перенесенный стресс, переохлаждение, инфекционное заболевание, сильные физические нагрузки
Лёгкая персистирующая. Приступы появляются гораздо чаще, до 1 раза в сутки. Если при бронхиальной астме ПСВ варьируются в диапазоне 20%-30%, то это свидетельствует о возрастающей реактивности бронхов
Рефлюкс-индуцированная. Недуг развивается на фоне проникновения в дыхательные пути содержимого желудка или из-за рефлюкса
Смешанного генеза. Спровоцировать развитие недуга могут как внешние, так и внутренние факторы
Персистирующая. Ежедневно случаются приступы, в том числе и ночные. ПСВ – 30% и более
Аспириновая. С этой формой патологии сталкиваются люди, которые длительное время принимают противовоспалительные нестероидные медикаменты или Аспирин
Тяжёлая персистирующая. Помимо ежедневных приступов появляется бессонница, ограничивается физическая активность. ПСВ – 30% и более
Физического усилия. С этой болезнью сталкиваются люди, которые предпочитают сильные физические нагрузки
Профессиональная. В группе риска находятся люди, которые работают в тяжелых условиях и вынуждены постоянно контактировать с химическими средами
Ночная. У пациентов наблюдаются приступы только в ночное время суток. Спровоцировать развитие этой формы патологии могут следующие факторы: воздействие аллергенов, переохлаждение, неправильное положение тела во время сна
Кашлевая. Патологию сопровождает только кашель, а другая симптоматика отсутствует. С такой формой астмы сталкиваются преимущественно дети, у которых приступы наблюдаются чаще всего в ночное время
Процесс диагностики бронхиальной астмы предусматривает широкий спектр мероприятий:
- Изначально врач-пульмонолог беседует с больным.
- Собирается анамнез заболевания.
- Проводится спирометрия.
- Делаются дыхательные пробы, при которых задействуются бронходилататоры.
- Проводится лабораторное исследование мокроты.
- Делается анализ крови.
- Выполняются различные пробы и тесты.
- Проводится рентгенография.
- Делается электрокардиограмма.
- При наличии показаний назначается компьютерная томография.
- Выполняется рН-метрия, суточная.
- Проводится тестирование больного, во время которого он должен в течение 8-ми минут бежать.
После получения результатов всех исследований специалист поставит пациенту точный диагноз и назначит эффективную схему лечения.
Чтобы защитить себя от развития этого недуга люди должны проводить профилактику:
- Специалисты настоятельно рекомендуют отказаться от пагубных привычек, особенно от курения. Если человек не имеет такого пристрастия, то он все равно может являться пассивным курильщиком, если будет вдыхать табачный дым. Именно поэтому следует избегать помещений, в которых накурено.
- При выборе района для постоянного места жительства необходимо узнать о том, на каком от него расстоянии расположены промышленные предприятия, свалки, стройки и автопарки.
- Каждый человек должен при трудоустройстве интересоваться, в каких условиях ему предстоит выполнять профессиональные обязанности. Если предстоит вредный труд, то работодатель обязан обеспечить его средствами индивидуальной защиты, а также качественным питанием, медицинским обслуживанием и санаторно-курортным отдыхом.
- В жилых помещениях люди должны регулярно проводить уборку, в частности влажную. Специалисты рекомендуют избавиться от всех пылесборников, коими являются напольные покрытия, натуральные перины и подушки и т. д.
- Климатическую технику необходимо регулярно чистить, чтобы в процессе ее работы в воздух не попадали частички осевшей на ее фильтрах пыли и плесени.
- Рекомендуется ежедневно проветривать жилые и рабочие помещения.
- Косметические средства следует использовать только те, в составе которых присутствуют растительные компоненты.
- Люди должны нормализовать свое питание, выработать распорядок дня и находить время для полноценного отдыха.
источник
Бронхиальная астма (БА) является гетерогенным заболеванием, как правило, характеризующимся хроническим воспалением дыхательных путей и наличием таких симптомов, как свистящее дыхание, одышка, чувство сжимания в грудной клетке и кашель, с переменной частотой и интенсивностью, связанных с различным по степени нарушением экспираторного потока воздуха через дыхательные пути. Ограничение потока воздуха вызвано: спазмом гладких мышц и отеком слизистой оболочки бронхов, формированием слизистых пробок, а с течением времени, также с перестройкой стенки бронха. БА с точки зрения этиологии делится на аллергическую (чаще всего начинается в детском возрасте, часто сопутствуют другие атопические заболевания, обычно эозинофилия индуцированной мокроты и хороший ответ на ингаляционные ГКС) и неаллергическую (обычно у взрослых лиц, часто худший ответ на ингаляционные ГКС). Кроме того, выделяют фенотипы БА:
2) с постоянной бронхиальной обструкцией;
3) сопровождающейся ожирением.
При аллергической астме связывание аллергена со специфическими антителами IgE на поверхности тучных клеток высвобождает медиаторы (в том числе гистамин, протеолитические энзимы, цистеиновые лейкотриены), которые вызывают бронхиальную обструкцию. В некоторых случаях спустя 6–8 часов после ранней фазы аллергической реакции наступает поздняя фаза, в которой тучные клетки, базофилы и другие клетки высвобождают цитокины и хемокины, многократно усиливающие приток воспалительных клеток, в частности, эозинофилов, в бронхи. Патомеханизм неаллергической астмы до конца не исследован, но гистопатологическая картина похожа на аллергическую астму. Повреждение эпителия бронхов стимулирует процессы репарации, результатом чего является перестройка стенки бронхов, которая приводит к тому, что в особенно тяжелых случаях обструкция становится необратимой.
Факторы, вызывающие приступы и обострения БА или провоцирующие их персистирование: аллергены, инфекции дыхательных путей (в основном вирусные), загрязнение воздуха (в том числе табачный дым, аэрозоли, используемые в домашнем хозяйстве, пары красок и т. д.), физическая нагрузка, сильные эмоции, изменения погоды, ЛС (β-блокаторы, НПВП), еда и пищевые добавки.
Факторы, повышающие риск обострений БА: неконтролируемые симптомы БА (в т. ч., чрезмерное потребление β 2 -агонистов короткого действия (ежемесячно >1 упаковки, содержащей 200 доз), неправильное использование ингаляционных ГКС (несоблюдение приема назначенного пациенту препарата, неправильная техника ингаляции), низкий ОФВ 1 (особенно
Факторы риска фиксации бронхиальной обструкции: неиспользование ингаляционных ГКС, воздействие табачного дыма или других вредных веществ (в том числе на рабочем месте), низкий исходный ОФВ 1 , хроническая чрезмерная продукция секрета в дыхательных путях, эозинофилия мокроты или крови.
КЛИНИЧЕСКАЯ КАРТИНА И ЕСТЕСТВЕННОЕ ТЕЧЕНИЕ наверх
1. Субъективные симптомы : пароксизмальная одышка, в основном экспираторная (иногда ощущаемая как сжимание в грудной клетке), которая проходит спонтанно или под влиянием лечения; свистящее дыхание; сухой, приступообразный кашель (сопровождающий одышку или как единственный симптом [так называемый кашлевой вариант астмы]; изолированный кашель у взрослых редко является симптомом БА). У больных с аллергической БА сопутствуют симптомы других аллергических заболеваний, наиболее часто аллергического ринита. Субъективные и объективные симптомы имеют изменчивый характер и могут не проявляться за исключением эпизодов приступов и обострений БА.
2. Объективные симптомы : диффузные, двусторонние свистящие хрипы (в основном экспираторные) и сухие хрипы, удлиненный выдох (иногда симптомы, которые выслушиваются только при форсированном выдохе); во время обострений работа вспомогательных мышц и тахикардия. При очень тяжелом обострении аускультативные симптомы могут не наблюдаться (так называемое «немое легкое»).
3. Естественное течение : БА может возникнуть в любом возрасте. Если она начинается в зрелом возрасте, то чаще является неаллергической и имеет более тяжелое течение. В течение БА происходят обострения, которые развиваются внезапно (в течение нескольких минут или часов) или постепенно (в течение нескольких часов или дней) и без применения лечения могут привести к смерти. Многолетняя неконтролируемая БА приводит к прогрессирующей, необратимой обструкции дыхательных путей.
Дополнительные методы исследования
1. Спирометрия: у большинства пациентов результат базовой спирометрии находится в пределах нормы. Для БА характерна обструкция, в особенности с изменчивой интенсивностью (существенные колебания между очередными исследованиями, или под влиянием лечения); при бронходилатационной пробе — существенное улучшение ОФВ 1 и/или ФЖЕЛ (≥200 мл и ≥12 % от должного) и часто даже устранение обструкции (при тяжелой БА или при БА с ремоделированием бронхов обструкция может быть необратимой), а также гиперреактивность бронхов при провокационной пробе с метахолином или гистамином. В особых случаях диагноз можно подтвердить с помощью специфических провокационных проб с аллергеном, ацетилсалициловой кислотой, присутствующими на рабочем месте факторами, физической нагрузкой.
2. Пиковая скорость выдоха (ПСВ): характерной является средняя (в течение 2 нед. измерений) суточная вариабельность ПСВ ([ПСВ макс – ПСВ мин ] / ПСВ средн ) >10 %; измерения используются для подтверждения диагноза, мониторинга заболевания (следует рассмотреть целесообразность у больных с тяжелой формой бронхиальной астмы или со слабым восприятием симптомов) и определения факторов, провоцирующих симптомы (напр. профессиональные факторы).
3. РГ грудной клетки: обычно в норме, при обострении могут присутствовать признаки гиперпневматизации легких (воздушные ловушки) и осложнения обострения (напр. пневмоторакс).
4. Пульсоксиметрия и газометрия артериальной крови: используйте с целью оценки тяжести и мониторинга течения обострений →см. ниже.
5. Исследования, определяющие IgE -опосредованную аллергию: кожные пробы, концентрация общего и специфического IgE — может определить сенсибилизирующий аллерген у пациента с аллергической астмой.
6. Исследование индуцированной мокроты на эозинофилию: в центрах, имеющих опыт, может использоваться для изменения лечения у пациентов с умеренной или тяжелой БА.
7. Исследование концентрации окиси азота в выдыхаемом воздухе ( FE NO ): в качестве дополнительного исследования при дифференциальной диагностике с ХОБЛ →табл. 3.8-1. У ранее не получавших лечение пациентов повышенный показатель (>50 ppb) коррелирует с хорошим ответом на лечение ингаляционными ГКС.
Для постановки диагноза БА (согласно GINA) требуется наличие симптомов заболевания, а также изменение выраженности бронхиальной обструкции при функциональных исследованиях →табл. 3.9-1. Необходимо оценивать степень тяжести заболевания.