Исследуем причины и симптомы, которыми проявляется болезнь Аддисона. Изучим также, как проводится диагностика и какие используются лекарства для лечения, позволяющие увеличить продолжительность нормальной жизни.
Болезнь Аддисона (Addison’s Disease) – это патология обмена веществ, при которой надпочечники производят гормоны в недостаточном количестве.
В этом состоянии секреция надпочечников не в состоянии обеспечить физиологические потребности организма, в результате чего появляется острая симптоматика, которая, если не лечить, может угрожать жизни больного.
Заболевание может поразить любого человека и в любом возрасте, но обычно возникает около 40 лет. Предполагается, что заболеваемость в мировом масштабе составляет 1 случай на каждые 100 000 человек.
Надпочечники, являющиеся эндокринными железами, размещены справа и слева от позвоночника на уровне последнего грудного позвонка, на верхней части обеих почек.
Каждый из 2 надпочечников состоит из двух различных частей. Внешняя часть, которая является истинной железой, выделяющей гормоны, и называемой корой надпочечников, и внутренней нервной ткани, называемой медуллярной областью.
Область коры надпочечников, в свою очередь, разделена на три отдельных слоя, продуцирующих гормоны:
- Минералокортикоиды: набор гормонов, принадлежащих к кортикостероидам (производные от деградации холестерина), функцией которых является регулировка баланса минеральных солей (натрия и калия, а, следовательно, водного баланса). Они производятся корой надпочечников, которая известна как клубочковая. Главный из этих гормонов – альдостерон, чья секреция увеличивается пропорционально увеличению в крови концентрации калия, который является регулятором артериального давления.
- Глюкокортикоиды: точнее кортизол и кортизон, которые ускоряют метаболические реакции и расщепляют жиры и белки в глюкозу внутри клетки. Стимуляция производства этих гормонов осуществляется посредством адренокортикотропного гормона (продуцируется гипофизом головного мозга).
- Андрогены и эстрогены. Андрогены выделяются в большом количестве, а эстрогены только в малых дозах. Всё это происходит как у женщин, так и у мужчин.
В медуллярной области синтезируются два нейротрансмиттера, которые имеют очень похожие химические свойства: адреналин и норадреналин.
- снижение производства альдостерона вызывает дисбаланс воды, натрия и калия в организме, что определяется изгнанием натрия и задержкой калий. Такое состояние может привести к гипотензии (снижению объема крови) и обезвоживанию;
- дефицит кортизола вызывает нарушения обмена веществ и проблемы гипогликемии, из-за чего организм ослабевает.
- снижение андрогенов может привести к снижению желания, выпадению волос и потери чувства благополучия всвязи с возникновением психических проблем.
Симптомы заболевания зависят от уровня концентрации гормонов коры надпочечников в крови. Снижение концентрации, в большинстве случаев, связано с разрушением клеток надпочечников. Разрушение, как правило, развивается медленно.
Таким образом, клиническая картина болезни Аддисона в начальной стадии отличается очень мягкой и неспецифической симптоматикой, которая медленно прогрессирует, по мере распространения разрушительных поражений железы.
Когда повреждение охватывает 90% секретирующих клеток, то развивается хроническая надпочечниковая недостаточность.
Резюмируя основные симптомы болезни Аддисона, следует отметить следующие:
- Астения. Снижение мышечной силы до такой степени, что трудно выполнять повседневные движения. Усталость присутствует даже в состоянии покоя или после абсолютно незначительного усилия.
- Гипотензия. Сопровождающаяся головокружением, а в тяжелых случаях даже обмороками и падениями. Пониженное давление крови, которое ещё больше уменьшается при переходе в вертикальное положение, является непосредственным результатом низкого уровня альдостерона. Это гормон блокирует экскрецию натрия с мочой. Низкий уровень концентрации альдостерона приводит к потере натрия и жидкости, в результате уменьшается объем крови и артериальное давление.
- Гипогликемия. Снижение уровня сахара в крови в результате низких уровней кортизола. Снижение концентрации последнего, на самом деле, снижает глюконеогенез, а именно производство глюкозы из белков и липидов, вызывая гипогликемию. Это усугубляется гипотонией и астенией.
- Обезвоживание. Обуславливается чрезмерным диурезом, вызванным потерей солей натрия с мочой. Сопровождается непреодолимой тягой к соленым продуктам.
- Потеря веса и анорексия. Это следствие гипогликемии и впечатляющие потери жидкости с мочой.
- Гиперпигментация кожи. Пигментация может отмечаться как на открытой солнцу коже, так и на скрытых участках тела, которые обычно не доступны для солнечных лучей: слизистые оболочки полости рта, десны, складки кожи, шрамы и др. Всё это происходит от того, что гипофиз стимулирует надпочечники к производству большего количества кортикотропина, который, в свою очередь, стимулирует производство меланина, отвечающего за пигментацию кожи.
- Желудочно-кишечные. То есть тошнота, рвота, диарея, спастические боли в животе.
- Боли в суставах и мышцах.
- Мигрень.
- Проблемы, связанные с настроением: раздражительность, чрезмерная тревожность, плохое настроение и меланхолия, а в тяжелых случаях депрессия. Все эти проблемы связаны с пониженной секрецией андрогенов, которые действуют на психику, обеспечивая ощущение общего благополучия.
- Потеря волос на теле. Симптом также связан с низким уровнем андрогенов.
В небольшом количестве случаев симптомы болезни, вместо хронической формы, развиваются быстро и внезапно, такое состояние называют острой надпочечниковой недостаточностью или кризис Аддисона. Эта ситуация требует немедленной медицинской помощи и правильного ухода за пациентом.
Симптоматология, которая характеризует кризис Аддисона, состоит в следующем:
- Резкие и мучительные боли, которые охватывают живот, спину, нижнюю часть или ноги.
- Лихорадка и спутанность сознания, проблемами в проведением осмысленных бесед.
- Рвота и понос с опасностью обезвоживания.
- Очень низкое артериальное давление.
- Потеря сознания и неспособность держаться на ногах.
- Очень низкий уровень глюкозы в крови.
- Очень низкий уровень натрия в крови.
- Высокий уровень калия в крови.
- Высокий уровень кальция в крови.
- Непроизвольные сокращения мышц.
Гормональная недостаточность, которая характерна для болезни Аддисона, может быть вызвана проблемами, возникающими как из надпочечников (первичная недостаточность надпочечников), так из других источников (вторичная недостаточность надпочечников).
В случае первичной надпочечниковой недостаточности сокращение уровня гормонов является следствием разрушения клеток железистой ткани, что, в свою очередь, может быть вызвано:
- Ошибка иммунной системы. Которая, по неизвестным причинам, распознает клетки коры надпочечников как чужеродные и разрушает их, приводя к развитию патологии.
- Гранулемы от туберкулеза. В данном случае гранулемы являются следствием воспалительного процесса, вызванного вирусной инфекцией.
- Грибковые инфекции или цитомегаловирусные инфекции. Они встречаются у пациентов, страдающих от иммуносупрессивных расстройств.
- Первичные или метастатические опухоли надпочечников (чаще всего лимфома или рак легких).
- Кровотечение из надпочечников. Примером такого заболевания является синдром Уотерхауса-Фридериксена. Это сильнейшее кровотечение в результате тяжелой бактериальной инфекции, вызванной, как правило, менингококками Neisseria meningitidis.
- Инфаркт надпочечника. Некроз соединительной ткани железы из-за недостаточного кровоснабжения.
- Генетические мутации, которые влияют на работу надпочечников. Они достаточно редки.
В случае вторичной надпочечниковой недостаточности надпочечники сохраняют работоспособность и эффективность, а низкий уровень гормонов является следствием:
- Проблем в работе гипофиза. Он несёт ответственность за секрецию адренокортикотропного гормона, который имеет задачу стимулировать кора надпочечников.
- Прекращение терапии кортикостероидами. Такая терапия часто осуществляется в случае пациентов, страдающих от астмы и ревматоидного артрита. Высокий уровень кортикостероидов уменьшает в крови уровень адренокортикотропного гормона. Уменьшение последнего приводит к резкому снижению стимуляции клеток надпочечников, отчего, в конечном итоге, происходит, своего рода, атрофия. Восстановления их нормальной работы может занять значительное время (порядка 6 месяцев). В этот период у пациента может случиться кризис Аддисона.
- Нарушение биосинтеза стероидов. Для производства кортизола надпочечники должны получать холестерин, который преобразуется с помощью соответствующих биохимических процессов. Поэтому в любой ситуации, когда прекращается поступление холестерина в надпочечники, развивается состояние дефицита кортизола. Такие ситуации, хотя и очень редко, случаются при синдроме Смита-Лемли-Опитц, синдроме абеталипопротеинемии и приёме некоторых лекарств (например, кетоконазол).
Первое предположение диагноза врач озвучивает на основе анамнестической истории пациента и детального анализа симптомов и признаков. Эта гипотеза затем проверяется рядом обследований и тестов.
Анализ крови, в котором должны отмечаться:
- Низкие уровни кортизола.
- Высокие уровни АКТГ.
- Низкий ответ кортизола на стимуляцию АКТГ.
- Наличие специфических антител к надпочечниковой системе.
- Уровень натрия ниже 130.
- Уровень калия более 5.
Измерение уровня глюкозы после введения инсулина. Пациенту вводят инсулин и через определенные интервалы времени оценивают уровень сахара и кортизола в крови. Если пациент здоров, уровень сахара в крови снижается, а уровень кортизола увеличивается.
Стимуляция надпочечников АКТГ. Пациенту вводят синтетический адренокортикотропный гормон, а затем измеряют концентрацию кортизола. Низкие уровни указывают на надпочечниковую недостаточность.
Компьютерная томография брюшной полости. Определяет размеры и любые аномалии желез.
Магнитно-резонансная томография турецкого седла (область черепа, где располагается гипофиз). Определяет возможные неисправности в гипофизе.
Независимо от причины, болезнь Аддисона может быть смертельно опасной, поэтому в организм необходимо поставлять те гормоны, которые надпочечники вырабатывают в недостаточном количестве.
Лечение болезни предусматривает введение:
- Кортикостероиды. В частности, флудрокортизон, чтобы компенсировать дефицит альдостерона и кортизона.
- Андрогены. Введение в достаточном количестве улучшает чувство благополучия, а, следовательно, улучшает качество жизни.
- Добавки натрия. Служат для уменьшения потери жидкости с мочой и увеличения артериального давления.
В случае кризиса Аддисона необходимо немедленное лечение, потому что это очень опасно для жизни пациента.
- Гидрокортизон.
- Инфузии физиологического раствора для увеличения объема крови.
- Введение глюкозы. Для повышения значений уровня сахара в крови.
Из-за опасности внезапного кризиса Аддисона, пациентам, страдающим от болезни, следует носить браслет экстренной медицинской помощи. Таким образом, медицинский персонал будет немедленно оповещен от тревоге.
Если правильно лечить болезнь Аддисона, то продолжительность жизни нормальная. Единственно возможная опасность может исходить от кризиса Аддисона. Поэтому больным рекомендуется носить информационный браслет, а также шприц для инъекций кортизола в экстренных случаях.
источник
Болезни, вызывающие бесплодие – это, прежде всего нарушения нормальной работы репродуктивной системы.
В случае, если каких-либо патологических изменений в организме не выявлено, и точную причину установить невозможно – то речь идет об идиопатическом бесплодии.
1) Эндокринные заболевания
При эндокринном бесплодии происходит нарушение гормональных механизмов, регулирующих менструальный цикл. Оно может иметь различные формы, однако существует один признак – отсутствие овуляции (созревание яйцеклетки и её выход в брюшную полость).
Часто причиной бесплодия являются заболевания щитовидной железы. Гиперфункция (когда повышается продукция гормонов щитовидной железы), так же, как и гипофункция (пониженная выработка гормонов щитовидной железы) влияют на способность забеременеть, т.к. это ведёт к подавлению функции яичников.
К эндокринным заболеваниям, которые приводят к бесплодию относятся:
- инсулинозависимый сахарный диабет;
- гиперкортицизм;
- опухоли гипоталамо-гипофизарной части головного мозга;
- последствия травм головного мозга;
- гиперпролактинемия;
- гиперандрогения (из-за нарушенной работы яичников или надпочечников);
- поликистоз яичников;
- диффузный токсический зоб;
- ожирение.

К ним относятся воспалительные заболевания матки (метрит, эндометрит), придатков матки (сальпингит, сальпингоофорит, гидросальпинкс), шейки матки (цервицит, эндоцерцивит), инфекции, передающиеся половым путем (хламидиоз, трихомониаз, гонорея, сифилис).
Все эти заболевания нарушают проходимость маточных труб, изменяют структуру эндометрия и в последствии приводят к бесплодию.
При непроходимости маточных труб сперматозоиды не могут оплодотворить яйцеклетку из-за препятствия на их пути. А на воспалённой слизистой невозможна имплантация эмбриона.
Кроме того, к бесплодию могут приводить опухолевые процессы в половых органах (миомы, кисты и кистомы яичников, полипы эндометрия).
Отдельно нужно отметить эндометриоз матки и яичников. Это заболевание, при котором ткань, подобная внутренней слизистой оболочке матки – эндометрию, обнаруживается в других органах и тканях: яичниках, маточных трубах, в шейке матки, во влагалище.
Процент наступления беременности после ЭКО у пациенток «ВитроКлиник» с диагнозом «Эндометриоз» — 47,9 %.
5) Осложнения после хирургических абортов
Инструментальные внутриматочные вмешательства могут вызвать стеноз (сужение) цервикального канала шейки матки, повредить внутренний слой матки (эндометрий). Он рубцуется, и это не позволяет оплодотворенной яйцеклетке нормально прикрепиться. И как следствие – отсутствие беременности или выкидыши на различных сроках.

- однорогая или двурогая матка;
- седловидная матка;
- перегородка во влагалище;
- аномалии развития маточных труб;
- недоразвитие яичников.
8) Избыточный (ожирение) или недостаточный вес
9) Наркотическая, алкогольная зависимость и табакокурение
Курение, злоупотребление алкоголем, приём наркотиков приводят к хронической интоксикации всего организма, что не может негативно не сказаться на работе всей репродуктивной системы.
Если вы хотите забеременеть, но у Вас не получается уже год или более, и имеется какое-либо заболевание или нарушение в работе репродуктивной системы, обратитесь к врачу репродуктологу – специалисту, занимающемуся проблемой бесплодия.
источник
Болезнь Аддисона в народе больше известна, как бронзовая болезнь, считается достаточно редким заболеванием эндокринной системы, которое сопровождается хронической недостаточностью коры надпочечников, как результат его одностороннего и двухстороннего поражения.
Если говорить о преобладающей клинической картине, то сущность болезни Аддисона заключается в следующем: это аутоиммунный процесс, то есть на организм нападают собственные иммунные клетки, разрушая некогда устоявшийся иммунитет и не только. Однако выделить также стоит и другие патогенные факторы:
- туберкулез надпочечников;
- сифилис;
- обширные грибковые поражения;
- кровотечение в надпочечниках;
- СПИД;
- адренолейкодистрофия;
- удаление надпочечников;
- саркоидоз;
- длительная медикаментозная терапия отдельных фармакологических групп.
Болезнь Аддисона прогрессирует стремительно, однако в острой форме преобладает недолго. Очень скоро она приобретает хронический характер и склонно к рецидивированию. В зависимости от степени поражения эндокринной системы выделяют первичную и вторичную недостаточность, где каждой присуща своя клиническая картина.
В первом случае виной патологического процесса становятся деструктивные процессы, прогрессирующие в результате разнообразных этиологических факторов, в частности туберкулез и аутоиммунная агрессия. А вот вторичная недостаточность прогрессирует на фоне нарушения гипоталамо-гипофизарной системы и повреждения синтеза адренокортикотропного гормона. В любом случае, данная патология требует немедленного лечения, иначе наблюдаются необратимые последствия для человеческого организма.
Не заметить болезнь Аддисона невозможно, поскольку пациент с характерным недугом начинает стремительно худеть, плохо себя чувствовать и ощущать постоянную усталость без причины. Кроме того, в данной клинической картине наблюдается устойчивый спад кровяного давления, а специальные препараты, направленные на его повышение, не способны стабилизировать общее состояние.
Среди других симптомов болезни Аддисона стоит выделить атрофию мышц и мышечную слабость, а также очевидное нарушение функций таких жизненно важных систем, как сердечно-сосудистая, дыхательная, пищеварительная и эндокринная. На фоне такой дисфункции прогрессирует повышенная пигментация кожи, а слизистые приобретают бронзовый оттенок. Вот отсюда и соответствующее название – бронзовая болезнь.
Болезнь Аддисона прогрессирует постепенно, а стартует с общего недомогания, который пациент ссылает на перемены погода и физическую усталость. Вскоре появляются первые проблемы с пищеварением, которые также негативно отражаются и на работе нервной системы. Так, больной испытывает приливы агрессии, которые чередуются с пассивностью и депрессивными состояниями. Затем кожа меняет свой цвет, а очевидные симптомы пигментации становятся поводом для обращения к специалисту за подробной консультацией.
Симптомы характерного недуга могут быть первичными и вторичными, но уже в запущенных клинических картинах пациент замечает, что начинает потреблять огромное количество соли. Это тревожный знак, который должен привлечь пристальное внимание к собственному здоровью. Если же случился криз, то он сопровождается такими симптомами, как гипотония, диарея, рвота, потеря сознания и боль в животе. Здесь уже не обойтись без медицинского вмешательства, а реанимационные меры должны последовать незамедлительно. В противном случае пациент может умереть.
Однако порой так происходит, что пациент не обращает внимания на проблему, считая, что в организме все в порядке. На самом деле это опасно для жизни, поскольку промедление в диагностике резко ухудшает общее состояние и может привести к неожиданному летальному исходу. Именно поэтому уже первые симптомы болезни Аддисона должны оговариваться в индивидуальном порядке с лечащим врачом.
Поставить окончательный диагноз без подробной диагностики очень сложно, поэтому в данной клинической картине врачи опираются на результаты лабораторных и клинических обследований. Однако акцент все же стоит делать на анализе, который позволяет судить о функции коры надпочечников.
Что же касается инструментального обследования, то требуется выполнение компьютерной томографии и рентгенографии, которые, в свою очередь, определяют характер заболевания и степень прогрессирующего патологического процесса. Когда клиническая картина будет окончательно ясна, самое время незамедлительно преступить к лечению болезни Аддисона.
Предупредить характерный недуг все же возможно, однако для этого требуется позаботиться обо всех мерах профилактики. Как таковой, схемы не предусмотрено, однако свою привычную жизнь все же стоит пересмотреть.
Первым делом требуется сесть на лечебную диету, полностью исключив из рациона жирную и вредную пищу. Кроме того, не стоит истощать организм вредными привычками и стрессами, а вот контроль работы эндокринной системы должен быть регулярным.
В тех клинических картинах, где появляются первые признаки болезни Аддисона, важно немедленно обратиться за консультацией специалиста, иначе патологический процесс будет только прогрессировать, нарушая привычное качество жизни пациента.
При заболевании Аддисона лечебный подход обязательно должен быть комплексным, а охватывать все аспекты жизни пациента. Что имеется ввиду?
Прежде всего, важно придерживаться лечебного рациона, а для этого индивидуально посетить диетолога. Пищу желательно обогатить протеинами и белками, а вот жиры должны быть исключительно растительного происхождения, углеводы — легкоусвояемыми углеводами, а витаминами и антиоксидантами обязательными. А вот продукты, богатые калием, лучше всего исключить из рациона, а для их компромиссной замены вспомнить о химическом составе поваренной соли.
В более запущенных клинических картинах эндокринолог назначает гормональную терапию, которая представлена длительным приемом глюкокортикоидови минералокортикоидов. Крайне важно дозировать такие лекарства, а способ применения и суточные дозы оговаривать строго в индивидуальном порядке. В случае прогрессирования аддисонических кризов необходима срочная госпитализация с выполнением реанимационных мер по стабилизации общего самочувствия пациента.
Задача врача – стабилизировать общее кровообращение, а для этих целей показано введение физиологического раствора и гидрокортизона. Когда же показатель кровяного давления стабилизируется, можно говорить о нормализации общего состояния. После того как самочувствие пациента зафиксируется на отметке «удовлетворительно», можно прекращать реанимационные меры и назначать симптоматическое лечение.
Поверхностное самолечение при болезни Аддисона может привести к ухудшению состояния и нарушению психики пациента, поэтому до таких ситуаций лучше не доводить. Также не исключается возникновение коллапса, а вывести пациента из этого состояния весьма проблематично. В целом, добиться окончательного выздоровления нереально, поскольку заболевание это – хроническое, а вот перевести его в спящее состояние вполне возможно.
источник
Принцип деятельности иммунной системы заключается в защите организма от микроогранизмов или других неблагоприятных факторов окружающей среды. В защите участвуют специфические лимфоциты Т и антитела.
В некоторых, пока малоизученных, ситуациях происходит сбой в системе опознавания и происходит аутоиммунная реакция: некоторые молекулы, клетки, ткани опознаются как «чужие» и становятся мишенью лимфоцитов Т и антител.
Подобные антииммунные нарушения встречаются у 5-7% населения и являются виновниками достаточно серьёзных патологий и бесплодия. Эти патологии разделяются на:
Систематические аутоиммунные заболевания , которые затрагивают молекулы, ткани, клетки. К ним относятся системная красная волчанка (lupus) и фосфолипидный синдром (они могут являться причиной бесплодия).
Специфическими аутоиммуные заболевания органов. Болезни Аддисона и аутоиммунные овариты.
Антитела антисперматозоидов вызывают мужское бесплодие.
Мужское аутоиммунное бесплодие
Яички защищены от иммунокомпетентных клеток и антител барьером. Если этот барьер разрушается (по причине трамвы или хирургического вмешательства), то организм быстро реагирует иммунной реакцией — сначала местным воспалительным процесом и затем выработкой антител антисперматозоидов.
В крови обнаруживаются антитела антисперматозоидов типа IgG, тогда как в спермической жидкости преобладают в основном — секреторные IgA. Эти антитела вызывают агглютинацию и блокируют подвижность сперматозоидов. Следствием этого является неспособность последних преодолеть цервикальную жидкость . Если же сперматозоидам всё-таки удалось преодолеть цервикальную жидкость, то антитела приклепляются к акросоме и препятствуют контакту сперматозоида с яйцеклеткой.
Попытки лечения этой патологии «промывкой» спермы не дали положительных результатов. В настоящее время, присутствие антител антисперматозоидов является показателем к лечению от бесплодия при помощи ИКСИ .
Женское аутоиммунное бесплодие
Существуют также множество причин иммунного характера, вызывающие бесплодие и у женщины. Некоторые аутоиммунные патологии затрагивают процессы от развития яйцеклетки до самой овуляции, и другие начинают своё негативное влияние уже после зачатия: или мешая развитию зародыша, или провоцируя самопроизвольные выкидыши.
Бесплодие, связанное со специфическими аутоиммунными заболеваниями огранов связано с ауто-иммунным оваритом, аутоиммунными гипофизитами, Базедовой болезнью.
Аутоиммунные овариты
Аутоиммунный оварит (очень редкое заболевание)является причиной возникновения ранней менопаузы (климакса). В анатомическом плане он характеризуется гипертрофией яичников со множеством кист внутри. В гистологическом плане — фолликулы пронизаны восспалительными клетками, в особенности лимфоцитами Т и макрофагами, а также плазмоцитами IgG.
Аутоиммунные гипофизиты
Эти патологии встречаются очень редко и чаще всего ассоциируются с болезнью Аддисона или с синдромом Турнера. При данном заболевании аутоантитела направлены против стероидных репродуктивных клеток.
Аутоиммунные тироидиты
Присутствие антител антитироглобулина и антитиропероксидаза могут стать причиной повторяющихся выкидышей.
Системная красная волчанка
Это серьёзное заболевание затрагивает одну женщину из 700 и в половом соотношении: 9 женщин на 1 мужчину. Причины возникновения этого заболевания ещё малоизучены и диагностируется по клиническим и биологическим показаниям.
И, тем не менее, есть основания предполагать, что внешние факторы, такие как некоторые медикаменты, вирусы, загорания на солнце, сильный стресс, могут стать факторами возникновения этого заболевания.
Клинические проявления волчанки достаточно разнообразны. Есть некоторые признаки, которые могут указать на начало развитие болезни: некоторые люди могут почувствать себя как при заболевании гриппом, усталость, мышечная боль и боль в суставах, высокая температура, отсутсвие аппетита. Эти симптомы могут длиться несколько месяцев и сопровождаться необъяснимой потерей или прибавкой веса. Появляется головная боль, начинают сильно выпадать волосы, наблюдается изменение цвета ногтей после пребывания на холоде или стойкое повышенное давление (гипертония).
Все эти симптомы говорят о начале заболевания. Специфические признаки болезни появятся позже.
*Нужно хотя бы 4 признака (необязательно единовременно, так как все
симптомы у человека проявляются редко) чтобы диагностировать заболевание:*
— артрит/полиартириты, боль в суставах рук и ног, челюсти, может
появиться покраснение, опухлость и чувство тепла на месте боли,
— кожный дерматит на носу и щеках,
— сильная чувствительность к солнцу,
— кожные корки красного цвета на лице, на голове, на ушах, на руках или
груди,
— небольшие ранки, в основном неболезненные, на слизистой носа или рта,
— боль в груди, которая увеличиавется при сильном дыхании или в лежачем
положении,
— прибавка в весе или опухлось на ногах,
— конвульсии или серьёзные ментальные сбои.
Протекание болезни может проходить иногда и малозаметно и только биологические анализы могут подтвердить диагноз.
В плане иммуннологии — выявляются антинуклерные антитела и антитела анти-АДН. И чаще всего выявляется ложно положительный анализ на сифилис присутствием антител анти-фосфолипидов.
Гематомологический анализ (гемостазиограмма) выявляет воспалительную анемию, реже — анемию, леукопению, лимфопению, тромбофению (наличие антипротромбиназов).
25% пациенток с волчанкой сталкиваются с проблемой повторяющихся выкидышей и возможно с преэклампсией. В основном эти выкидыши связаны с наличием в крови антител антифосфлипидов.
Самопроизвольные выкидыши и антитела антифософлипидов
Клинические признаки Фосфолипидного синдрома:
— тромбозы (артериальные, венозные, капилярные), ливедо, тромбопения…, — необьяснимые (без анатомической, генетической или гормональной причины) самопроизвольными выкидышами ( 3 раза или больше) или — смерть плода (1 раз или больше) после 10 недель без морфологических аномалий определяется при помощи УЗИ или гестатических анализов или — преждевременные роды (1 раз или больше) до 34 недели морфологичекси нормальным ребёнком, но сопровождающиеся пре-эклампсией или серьёзной плацентарной недостаточностью.
Биологические критерии:
— Наличие антител антикардиолипидов (АКЛ)- IgG и/или IgM > 20 U GPL/ml и бэта2-глюкопротеин I (b2GPI). Анализ взятый дважды с промежутком минимум в 6 недель и обнаруженны стандартным тестом ELISA. — Наличие в крови Циркулирующих Антикоагулянотов (ЦАК).
— Позитивный (ложно) анализ на сифилис.
Очень сильно завышенный уровень АКЛ и ЦАК указывает на серьёзные осложнения в беременности 2-го и 3-го триместра (смотрите выше).
Беременные женщины с фосфолипидным синдромом, не прошедшие лечение, рискуют потерять плод в 80-90% случаев в течение второго или третьего триместра.
80 % женщин, прошедших лечение, успешно рожают.
Лечение во время беременности зависит от показаний ваших анализов и тромбоэмболитических признаков. Лечение может быть следующим:
— Аспирин 100мг/в день,
— Аспирин + Гепарин,
— Аспирин + дозы антивооспалительного характера Преднизона, — Аспирин + дозы иммуннодепрессивного характера Преднизона, — или же внутривенные инъекции иммунноглобулина.
Предродовая терапия:
Прекращают Аспирин начиная с 32 недели беременности и переходят на
превентивные дозы Гепарина
*Послеродрвая терапия: *
— эффективные дозы Гепарина в течение 6 недель
— назначить/увеличить дозы кортикоидов в течение 6 месяцев.
Аутоиммуннет антияичников
Эта патология клинически характеризуется также бесплодием. В биологическом плане — наблюдается образование антител антияичников. Определяются эти тела в крови при помощи иммуннофлюорицентной техники и техники ELISA.
Эти тела были обнаружены у женщин с ранней менопаузой, с синдромом поликистозных яичников, а также при необьяснимом бесплодии. Возникновение этой патологии пока плохо изучено, но некоторые исследования позволили показать зависимость образования этих антител после многочисленных пункций яичников в протоколе ЭКО. Правильно подобранная иммуннодепрессивная терапия в протоколе ЭКО позволяет избежать возникновения этой патологии: Короткая кортикоидная терапия (Преднизон) после фолликулярной пункции.
Похожие статьи:
* Антитела к вирусу гепатита с
* Иммунологический фактор бесплодия
* Виды бесплодия
* Лечение иммунологического бесплодия
* Как лечить мужское бесплодие?
источник
Болезнь Аддисона, также известная как надпочечниковая недостаточность – это заболевание, при котором организм человека не вырабатывает достаточное количество гормонов надпочечников.
При аддисоновой болезни надпочечники производят мало кортизола, а также альдостерона. Болезнь Аддисона поражает людей любого возраста и пола.
Это заболевание может угрожать жизни больного.
Лечение болезни Аддисона основано не гормональной заместительной терапии, при которой больные получают необходимые дозы гормонов, которые не могут синтезировать сами.
Надпочечники, одни из важнейших желез нашего организма, располагаются прямо над почками человека в виде своеобразных «наростов». Это важное звено эндокринной системы, которое вырабатывает гормоны, сообщающие сложные команды всем клеткам организма.
Внутренняя часть надпочечников производит катехоламины, такие как адреналин. Адреналин влияет на тонус сосудов, уровень артериального давления, пульс, состояние нервной системы. Без этого гормона жизнь нашего организма была бы невозможна.
Наружный слой надпочечников, или кора, производит другую важную группу гормонов – кортикостероиды, которые подразделяются на глюкокортикоиды и минералокортикоиды. Эти гормоны играют ключевую роль в регуляции обмена веществ, воспалительных реакций и др..
Кора надпочечников способна производить мужские половые гормоны – андрогены.
1. Глюкокортикоиды. Кортизол влияет на способность организма преобразовывать пищу в энергию, играет роль в иммунном ответе и помогает нашему организму реагировать на стресс.
2. Минералокортикоиды. Эти гормоны, такие как альдостерон, поддерживают тонкое равновесие натрия и калия в организме, что очень важно для нормального давления и других жизненных функций.
3. Андрогены. Мужские половые гормоны в очень малом количестве продуцируются надпочечниками, как у женщин, так и у мужчин. Они вызывают развитие половых признаков, увеличение мышечной массы, усиление либидо у представителей обоих полов.
Первичная надпочечниковая недостаточность.
Если надпочечники не вырабатывают нужное количество гормонов из-за повреждения их коры, то врачи относят это заболевание к первичной надпочечниковой недостаточности. Поражение коры надпочечников может наблюдаться при аутоиммунных заболеваниях (когда иммунная система атакует собственные клетки).
1. Туберкулез.
2. Другие инфекции надпочечников.
3. Распространение рака на надпочечники.
4. Травма, кровотечение в железе.
Вторичная надпочечниковая недостаточность.
Надпочечниковая недостаточность может возникать из-за проблем в отдаленном участке тела – в гипофизе. Гипофиз вырабатывает адренокортикотропный гормон (АКТГ), который должен стимулировать кору надпочечников. Неадекватная выработка АКТГ может приводить к дефициту кортикостероидов, даже если кора надпочечников здорова. Врачи называют это состояние вторичной надпочечниковой недостаточностью.
Другой частой причиной вторичной недостаточности является внезапная отмена приема кортикостероидов, которые человек долгое время принимал для лечения какого-либо заболевания (астмы, артрита и др.) В этом случае организм «привыкает» к поступлению гормона извне, и оказывается попросту не готов возобновить собственную выработку при резкой отмене лекарства.
Симптомы этого заболевания обычно развиваются медленно, в течение нескольких месяцев.
1. Мышечная слабость и утомляемость.
2. Потеря веса и пониженный аппетит.
3. Потемнение кожи (гиперпигментация).
4. Низкое артериальное давление, вплоть до обмороков.
5. Боль в мышцах и суставах.
6. Стремление есть соль.
7. Низкий уровень сахара.
8. Тошнота и рвота.
9. Диарея (понос).
10. Раздражительность.
11. Депрессия.
Острая надпочечниковая недостаточность.
В некоторых случаях симптомы болезни Аддисона могут появляться внезапно.
При аддисоновом кризе, или острой надпочечниковой недостаточности, признаки включают:
1. Боль в нижней части спины, животе и ногах.
2. Тяжелая рвота и диарея, приводящая к дегидратации.
3. Пониженное артериальное давление.
4. Высокий уровень калия.
5. Потеря сознания.
Врач должен будет собрать медицинскую историю, расспросить больного о жалобах, которые могут указывать на болезнь Аддисона – похудание, нарушение настроения, тяга к соли и др.
Больному придется пройти ряд анализов:
В этом анализе ценными будут показатели концентрации натрия, калия, кортизола и АКТГ. Это даст врачу возможность связать жалобы больного с нарушением работы надпочечников. Анализ крови также может выявить антитела, ассоциируемые с аутоиммунным поражением желез.
2. Тест со стимуляцией АКТГ.
Этот тест предусматривает измерение уровня кортизола в крови после введения больному адренокортикотропного гормона гипофиза. Если причина болезни в поражении коры надпочечников, то ответ желез на АКТГ будет ограничен или будет отсутствовать вовсе.
3. Тест с инсулин-индуцированной гипогликемией.
Этот тест применяют, если подозревается вторичная недостаточность надпочечников (проблема с гипофизом). Тест предусматривает измерение уровня сахара и кортизола в крови после введения инсулина. У здоровых людей уровень сахара упадет, а уровень кортизола вырастет.
4. Визуализация надпочечников.
Врач может назначить компьютерную томографию живота, чтобы проверить размер надпочечников и найти аномалии, которые могли вызвать недостаточность. Также врач может назначить магнитно-резонансное сканирование гипофиза, если подозревается вторичная недостаточность надпочечников.
Заместительная гормональная терапия при болезни Аддисона включает:
1. Пероральный прием кортикостероидов. Врач может прописать больному флудрокортизон (Флоринеф), чтобы заменить альдостерон. Препараты гидрокортизон, преднизолон или кортизона ацетат могут использоваться для замены глюкокортикоидов.
2. Инъекции кортикостероидов. Если больной по каким-то причинам не переносит пероральные формы гормона (рвота, диспепсия), то большинство препаратов доступно в виде инъекций.
3. Андрогенная заместительная терапия. Для лечения дефицита андрогенов у женщин применяется дегидроэпиандростерон. Некоторые исследования предполагают, что такая терапия может улучшить общее самочувствие, повысить либидо и удовлетворение от секса.
Больным также рекомендуется обильное употребление натрия, особенно на фоне больших физических нагрузок, во время жары, а также при поносе.
Врач может предложить временное увеличение доз препаратов, в зависимости от конкретного случая. К таким случаям относят стрессовые для организма ситуации – болезни, инфекции, операции и др.
Лечение острой надпочечниковой недостаточности.
Это состояние представляет серьезную угрозу для жизни больного. Наиболее опасны понижение артериального давления, падение уровня сахара и гиперкалиемия (повышение концентрации калия в крови). При кризе больной нуждается в немедленной медицинской помощи и госпитализации.
Лечение включает внутривенное введение гидрокортизона, солевых растворов и глюкозы.
источник
Медицинский справочник болезней
Аддисонова Болезнь (Гипокортицизм). Причины, симптомы и лечение Аддисоновой болезни.
ГИПОКОРТИЦИЗМ — недостаточность коры надпочечников. Бывает первичным от повреждения надпочечников и вторичным от недостаточной секреции гипофизом АКТГ (адренокортикотропный гормон).
Первичный гипокортицизм может быть острым (Апоплексия надпочечниковая) и хроническим (Аддисонова болезнь).
Помимо того, может быть скрытая, стертая форма гипокортицизма не всегда распознается вследствие частичного повреждения коры надпочечников или наследственной недостаточности. Последняя выражается симптоматикой аддисоновой болезни, но в значительно менее выраженной степени.
Лечение этой формы не требует применения стероидных гормонов. Рекомендуется общеукрепляющая терапия, витамин С в больших дозах.
АДДИСОНОВА БОЛЕЗНЬ (Томасс Аддисон, 1855, Британия) — синонимы: хронический гипокортицизм, бронзовая болезнь.
Аддисонова болезнь характеризуется первичной хронической недостаточностью функции коры обоих надпочечников вследствие деструктивных или атрофических изменений в них.
Заболевание чаще встречается в возрасте 30—50 лет, преимущественно у мужчин, однако наблюдается и у детей. Легкие, стертые формы аддисоновой болезни встречаются относительно редко и называются аддисонизмом. Для развития аддисоновой болезни должно быть разрушено не менее 80—90% ткани надпочечников.
- Причиной Аддисоновой болезни в 50— 60% служит туберкулезное поражение надпочечников путем гематогенной диссеминации. Иммунологическое исследование обнаруживает в 40% случаев антитела к тканям коры надпочечников, циркулирующие в крови.
- В последние годы идиопатическая форма преобладает над туберкулезной.
При идиопатической форме надпочечники страдают меньше, чем при туберкулезной. Женщины идиопатической формой болеют в 2—3 раза чаще. Имеют определенное значение дистрофические изменения надпочечников вследствие перенесенных инфекций и интоксикаций: амилоидоз, травматические поражения, кровоизлияния, хирургическое удаление надпочечников или метастазирование в них опухолей из других органов — бронхов, молочной железы, нагноение надпочечников и др. В ряде случаев этиология остается невыясненной.
Идиопатическая форма часто сопровождается и другими аутоиммунными процессами, выражающимися в виде сахарного диабета, гипотиреоза, бронхиальной астмы, гипопаратиреоза, аменореи и др. При этой форме у ряда больных обнаружены антитела стероидопродуцирующих клеток яичек и яичников (синдром Шмидта).
Причиной сравнительно частого поражения надпочечников туберкулезом является высокое содержание в паренхиме стероидных гормонов, в частности, гидрокортизона, препятствующих образованию грануляционной ткани и заживлению процесса. Аддисонова болезнь может развиться вторично, на почве частичной недостаточности гипофиза: недостаточность АКТГ. В этих случаях речь идет о гипопитуитаризме.
В основе лежит тотальная недостаточность коры надпочечников. В результате недостаточного выделения кортизола, альдостерона в канальцах почек нарушается реабсорбция ионов натрия и хлора, приводящая к гипонатриемии и гипохлоремии. При этом в крови и в тканях повышается содержание ионов калия, что наряду с недостаточностью глюкокортикоидов служит причиной гипотонии, крайней слабости и адинамии.
В результате недостаточности глюкокортикоидов, в частности кортизола, развивается гипогликемия, лимфоцитоз и эозинофилия. При первичном поражении ткани коры надпочечников по закону обратной связи усиливается секреция АКТГ, что служит причиной меланодермии. Недостаточность глюкокортикоидов и минералокортикоидов, в частности ДОКСа, является причиной эрозивного гастрита и язвы желудка. В то же время снижение надпочечниковых андрогенов v мужчин ведет к импотенции.
Клиническая картина.
Больные жалуются на ухудшение аппетита, общую слабость, утомляемость, апатию, похудание, потемнение кожи, боли в животе, в тяжелых случаях появляется тошнота и рвота, запоры или поносы. Больные становятся рассеянными и забывчивыми, слабовольными, депрессивными. Иногда у них развиваются и психозы.
Меланодермия, как правило, выражена в местах естественной пигментации и усиливается при инсоляции (поясница, наружные половые органы, околососковые кружки, шея). Губы и слизистые окрашиваются в серо-аспидный цвет. Пигментация, борозд ладоней (симптом Аствацатурова) является ранним и достоверным признаком гипокортицизма.
С развитием заболевания пигментация усиливается, кожа и слизистые принимают темно-коричневую окраску, темнеют волосы. В ряде случаев, может наблюдаться очаговая депигментация в виде витилиго.
Аддисоновую болезнь следует дифференцировать от заболеваний, при которых имеет место расстройство пигментации.
Аддисонова болезнь может сочетаться с хроническим язвенным гастритом, язвой желудка или двенадцатиперстной кишки. Почечная недостаточность в виде азотемии наблюдается во время кризов. Завершение беременности нормальными родами возможно, если проводится соответствующее лечение.
Криз при Аддисоновой болезни наступает вследствие резкого обострения заболевания и может привести к тяжелому состоянию — коллапсу со смертельным исходом.
Причиной обострения Аддисоновой болезни могут быть различные экзогенные и эндогенные стрессовые факторы на фоне дефицита глюко- и минералакортикоидов: интеркурентная инфекция, психические и физические напряжения, голод, травмы и др. Нередко причиной кризов может быть прекращение лечения заместительными препаратами. Обычно критическое состояние развивается в течение нескольких дней.
При кульминации криза больные впадают в крайне тяжелое состояние с полной адинамией, резким падением кровяного давления, приводящим к анурии. Возникают сильные боли в животе, часто симулирующие перфорацию язвы желудка, сопровождающуюся кровавой рвотой, и наличием крови в стуле (синдром Бернара-Сертана).
Лабораторная диагностика.
Содержание СК бывает ниже 100 мг%, что обусловлено понижением гликонеогенеза, как проявления недостаточности глюкокортикоидов. Нагрузка глюкозой дает плоскую гликемическую кривую вследствие медленного всасывания сахара в желудочно-кишечном тракте. Наоборот, при внутривенной нагрузке кривая бывает нормальной. Больные Аддисоновой болезнью имеют повышенную чувствительность к инсулину.
Характерна гипонатриемия, гипохлоремия, гиперкалиемия, гипопротеинемия, высокая креатинурия.
В периферической крови: умеренная анемия, лимфоцитоз, эозинофилия; СОЭ, несмотря на анемию, не ускоряется из-за сгущения плазмы. Важное диагностическое значение имеет определение в крови содержания стероидных гормонов, а в моче — их метаболитов. В крови понижается содержание общего и свободного кортизола, альдостерона 11- и 17-кортикостероидов, а в суточной моче—17-КС, 17-ОКС и альдостерона.
Лечение этиологическое, заместительное и общеукрепляющее.
- Исходя из того, что основным в этиологии является туберкулезное поражение надпочечников, во всех установленных случаях туберкулеза необходимо проводить Противотуберкулезное лечение, что в отдельных случаях приводит к приблизительно хорошему результату.
- Заместительная терапия проводится Глюкокортикоидами и Минералокортикоидами. В начальном периоде больные нуждаются в больших количествах гормонов.
- Преимущество отдается естественным гормонам — кортизону, гидрокортизону и ДОКСА. Желательно сохранить естественное соотношение глюкокортикоидов и минералокортикоидов.
Кортизон назначается по 10—25 мг; ДОКСА по 5— 10 мг. - Из синтетических препаратов применяются преднизолон по 5-10 мг внутрь, дексаметазон — 2 мг внутрь, триамциналон — 8—16 мг. Количество стероидных гормонов устанавливается индивидуально, в соответствии с общим состоянием больного.
- Преимущество отдается естественным гормонам — кортизону, гидрокортизону и ДОКСА. Желательно сохранить естественное соотношение глюкокортикоидов и минералокортикоидов.
Больные Аддисоновой болезнью время от времени должны подвергаться стационарному обследованию для уточнения количества вводимых стероидных гормонов.
- При легком течении болезни заместительная терапия не назначается. В этих случаях дополнительно показано 10—15 г хлорида натрия и витамин С до 5 г в сутки, глицирам по 2—3 таблетки в день.
- При кризе аддисоновой болезни назначают внутривенно капельно 2—3 л изотонического раствора хлорида натрия с 5% раствором глюкозы , 100—300 мг кортизона или гидрокортизона или 100—200 мг преднизолона в день. При резком снижении артериального давления в указанный выше раствор добавляют 1 —3 мл 0,2% раствора норадреналина.
источник
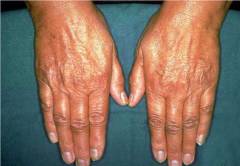
Повреждение коркового слоя надпочечников приводит к нарушению секреции ими стероидных гормонов, в первую очередь, альдостерона и кортизола, которые регулируют водно-солевой, белковый, углеводный, липидный обмены в организме. Они также участвуют в реализации стрессовых реакций, влияют на артериальное давление, общий объем циркулирующей крови.
При болезни Аддисона могут возникать различные симптомы, такие как повышенная утомляемость, общая слабость, головокружение, снижение трудоспособности, головная боль, чувство жажды, влечения к соленой пище, мышечная слабость, миалгия (боли в мышцах), мышечные судороги, боли в животе, тошнота, рвота, нарушение менструального цикла, низкое артериальное давление, гиперпигментация (потемнение кожи), витилиго, тахикардия (учащенное сердцебиение), боли в области сердца и др.
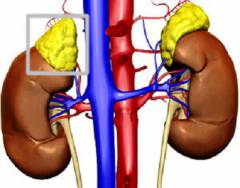
Левый надпочечник имеет полулунную форму, правый – треугольную. В каждом из них выделяют переднюю, заднюю и почечную поверхности. Задней своей поверхностью оба надпочечника прилежат к диафрагме. Почечная (нижняя) их поверхность соприкасается с верхним полюсом соответствующей почки. Правый надпочечник в ретроперитонеальном пространстве расположен чуть выше левого. Передней своей поверхностью он примыкает к нижней полой вене, печени и брюшине. Левый надпочечник спереди контактирует с поджелудочной железой, кардиальным отделом желудка и селезенкой. На переднемедиальной (передней внутренней боковой) поверхности каждого из надпочечников находятся так называемые ворота (hilum), через которые из них (из надпочечников) выходят центральные вены (в дальнейшем они называются надпочечниковыми венами).
Из каждого надпочечника выходит по одной центральной вене. Левая надпочечниковая вена затем впадает в левую почечную вену. Венозная кровь из правого надпочечника транспортируется через правую надпочечниковую вену сразу в нижнюю полую вену. В воротах надпочечников можно обнаружить и лимфатические сосуды, по которым лимфатическая жидкость попадает поясничные лимфатические узлы (nodi lymphatici lumbales), расположенные вокруг брюшной аорты и нижней полой вены.
Артериальная кровь проникает в надпочечники через ветви верхней, средней и нижней надпочечниковых артерий (a. suprarenalis superior, a. suprarenalis media, a. suprarenalis inferior). Верхняя надпочечниковая артерия является продолжением нижней диафрагмальной артерии. Средняя надпочечниковая артерия отходит от брюшной аорты. Нижняя надпочечниковая артерия служит ветвью почечной артерии. Все три надпочечниковые артерии под соединительнотканной капсулой, которая покрывает каждый из надпочечников, образуют густую артериальную сеть. От этой сети отходят мелкие сосудики (около 20 — 30), проникающие в толщу надпочечников через их переднюю и заднюю поверхности. Таким образом, артериальная кровь поступает к надпочечникам по многочисленным сосудам, тогда как венозная кровь удаляется из этих эндокринных желез только через один сосуд – центральную (надпочечниковую) вену.
Иннервация надпочечников осуществляется за счет ветвей, отходящих из солнечного, почечного и надпочечникового нервных сплетений, а также ветвей диафрагмального и блуждающего нервов.
Кнутри от соединительнотканной капсулы располагается корковое вещество (наружный слой) надпочечника, на долю которого приходится около 90% всей паренхимы (ткани) данного органа. Остальные 10% в надпочечнике занимает его мозговое вещество (внутренний слой надпочечника), которое находится под корковым веществом, непосредственно, в самой глубине железы. Корковое и мозговое вещество имеют различное строение, функции и эмбриональное происхождение. Корковое вещество (кора надпочечников) представлено рыхлой соединительной и железистой тканью. Этот слой на анатомических срезах имеет желтовато-коричневый цвет.
Наружный слой каждого из надпочечников принято делить на три зоны – клубочковую, пучковую и сетчатую. Клубочковая зона является самым внешним слоем коркового вещества и локализуется, непосредственно, под капсулой надпочечника. Сетчатая зона граничит с мозговым веществом надпочечника. Пучковая зона занимает срединное положение между клубочковой и сетчатой. В клубочковой зоне вырабатываются минералокортикоиды (альдостерон, дезоксикортикостерон, кортикостерон), в пучковой – глюкокортикостероиды (кортизол и кортизон), а в сетчатой – андрогены. Мозговое вещество надпочечников имеет буровато-красный цвет и не разделяется ни на какие зоны. В этой области в надпочечниках синтезируются катехоламины (адреналин и норадреналин).
Надпочечники являются жизненно необходимым органами и выполняют разнообразные функции посредством выработки ряда гормонов, обладающих специфическими свойствами. Как было уже сказано немного выше, в этих эндокринных железах вырабатываются минералокортикоиды (альдостерон, дезоксикортикостерон, кортикостерон), глюкокортикостероиды (кортизол и кортизон), андрогены и катехоламины (адреналин и норадреналин). Жизненно необходима для человека секреция надпочечниками альдостерона и кортизола. Альдостерон является единственным минералокортикоидом, который надпочечники выделяют в кровь. Этот стероидный гормон способствует задержке в организме натрия, хлоридов и воды и выделению калия вместе с мочой. Он способствует увеличению системного артериального давления, общего объема циркулирующей крови, влияет на ее кислотно-основное состояние и осмолярность. Альдостерон регулирует правильную работу потовых и желудочно-кишечных желез.
Кортизол, как и альдостерон, также относится к стероидным гормонам. Он оказывает разностороннее действие на обмен веществ (метаболизм) в органах и тканях организма. Кортизол стимулирует образование большого количества глюкозы и гликогена в печени и ингибирует (блокирует) утилизацию их в периферических тканях. Это способствует развитию гипергликемии (увеличению в крови уровня глюкозы). В жировой, лимфоидной, костной и мышечной ткани данный гормон стимулирует распад белков. В печени он, наоборот, активирует синтез новых протеинов. Кортизол регулирует и жировой обмен. В частности, он способствует распаду жиров в одних тканях (например, жировой) и липогенез (образование новых жиров) в других (туловище, лицо). Этот глюкокортикоид является главным гормоном стресса, который помогает организму приспособиться к действию различных стрессовых факторов (инфекциям, физическому перенапряжению, психическим или механическим травмам, хирургическим вмешательствам и др.).
Андрогены вырабатываются клетками сетчатой зоны коры надпочечников. Основными их представителями являются дегидроэпиандростерон, этиохоланолон, андростендиол и андростендион.
Тестостерон и эстрогены надпочечниками практически не вырабатываются. Андрогены, которые вырабатываются в больших количествах в надпочечниках, оказывают на ткани организма гораздо меньшее действие, чем это делают основные половые гормоны. Так, например, тестостерон по своей активности превосходит действие андростендиона в 10 раз. Андрогены отвечают за развитие вторичных половых признаков, таких как изменение голоса, оволосение на теле, развитие половых органов и др., регулируют обмен веществ, повышают либидо, то есть сексуальное влечение.
Катехоламины (адреналин и норадреналин), которые образуются в мозговом веществе надпочечников, отвечают за адаптацию организма к острым стрессовым воздействиям со стороны окружающей среды. Эти гормоны увеличивают частоту сердечных сокращений, регулируют артериальное давление. Также они участвуют в тканевом метаболизме (обмен веществ), посредством ингибирования выброса инсулина (гормон, который нормализует уровень глюкозы в крови) из поджелудочной железы, активации липолиза (расщепления жиров) в жировой ткани и распада гликогена в печени.
Вторичная надпочечниковая недостаточность является отдельным эндокринным заболеванием и не относится к болезни Аддисона, так как она появляется в результате нарушения секреции гипофизом адренокортикотропного гормона (АКТГ), который служит естественным стимулятором функционирования коры надпочечников. Этот гормон контролирует выработку и секрецию гормонов (в основном, глюкокортикостероидов и андрогенов) коры надпочечников. В условиях дефицита АКТГ пучковая (средняя) и сетчатая (внутренняя) зоны коры надпочечников подвергаются постепенной атрофии, что приводит к надпочечниковой недостаточности, но уже вторичной (так как первопричина заболевания не в самих надпочечниках).
При болезни Аддисона поражаются сразу все три зоны коры (коркового вещества) надпочечников – клубочковая, пучковая и сетчатая, поэтому, считается, что первичный гипокортицизм клинически протекает тяжелее, чем вторичный. Следует также отметить тот факт, что все симптомы, которые имеют место у пациента при болезни Аддисона, связаны только с деструкцией коры надпочечников, а не их мозгового вещества, возможное разрушение которого (в зависимости от причины первичного гипокортицизма) не играет никакой роли в механизме развития данной патологии. Как было уже сказано немного выше, болезнь Аддисона возникает в результате действия на кору надпочечников определенных повреждающих факторов. Ими могут быть различные микроорганизмы (бактерии, грибки, вирусы), аутоиммунные процессы, новообразования (опухолевое или метастатическое поражение надпочечников), генетические нарушения (например, адренолейкодистрофия), нарушение кровоснабжения коры надпочечников (ДВС-синдром, антифосфолипидный синдром).
Наиболее частыми причинами болезни Аддисона являются:
- аутоиммунное поражение тканей коры надпочечников;
- туберкулез;
- адреналэктомия;
- метастатическое поражение коры надпочечников;
- грибковые инфекции;
- ВИЧ-инфекция;
- адренолейкодистрофия;
- антифосфолипидный синдром;
- ДВС-синдром;
- синдром Уотерхауса-Фридериксена.
В подавляющем большинстве всех новых случаев (в 80 — 90%) болезнь Аддисона возникает в результате аутоиммунного разрушения коры надпочечников. Такое разрушение появляется вследствие нарушения нормального развития иммунной системы. Клетки иммунной системы (лимфоциты) у таких пациентов при контакте с тканью надпочечников (через кровь) начинают воспринимать ее как чужеродную. Из-за этого они активируются и инициируют деструкцию коры надпочечников. Важную роль в процессе аутоиммунной деструкции играют аутоантитела, которые секретируют в кровь лимфоциты.
Аутоантитела – это антитела (белковые, защитные молекулы), направленные против собственных тканей (в данном случае против тканей коры надпочечников), которые специфически связываются с различными структурами на клетках коры надпочечников и, тем самым, вызывают их гибель. Основными типами аутоантител, наблюдающихся в крови у больных с аутоиммунной болезнью Аддисона, являются антитела к ферментам надпочечникового стероидогенеза (процесса образования стероидных гормонов) – 21-гидроксилазе (P450c21), 17а-гидроксилазе (P450c17), ферменту отщепления боковой цепи (P450scc).
Адренолейкодистрофия (АЛД) – это наследственное заболевание, возникающее в результате делеции (удаления) определенного участка на длинном плече X-хромосомы. В этом участке локализуется ген ALD, который кодирует структуру фермента лигноцероил-КоА-синтетазы, участвующего в окислении длинноцепочечных жирных кислот (ДЖК) в клетках центральной нервной системы, надпочечников и в других тканях. При адренолейкодистрофии этот фермент не вырабатывается, в результате чего в нервной ткани и в коре надпочечников накапливается большое количество жира (ДЖК вместе с эфирами холестерина), что постепенно приводит к их дегенерации и отмиранию. Данная патология чаще всего регистрируется у мужчин (адренолейкодистрофия является X-сцепленным рецессивным заболеванием).
Существуют различные клинические варианты течения адренолейкодистрофии и не всегда при данной болезни могут серьезно поражаться ткани коры надпочечников. Например, у части таких пациентов преобладает неврологическая симптоматика (ювенильная форма адренолейкодистрофии), тогда как признаки болезни Аддисона могут долго отсутствовать (особенно в начале заболевания).
Помимо надпочечников и центральной нервной системы при адренолейкодистрофии нередко развивается первичный мужской гипогонадизм (недостаточность функции яичек), что может сказаться на репродуктивной способности мужчин. Адренолейкодистрофия является третьей по статистике причиной развития болезни Аддисона (после аутоиммунной деструкции коркового вещества надпочечников и туберкулеза надпочечников). Сопутствующая неврологическая симптоматика, встречающаяся при АЛД, делает прогноз болезни Аддисона менее благоприятной, по сравнению с другими причинами первичного гипокортицизма.
Антифосфолипидный синдром (АФС) является патологическим состоянием, характеризующимся нарушением свертываемости крови и появлением в различных сосудах тромбов. Причиной появления АФС служат антитела (белковые, защитные молекулы) к фосфолипидам клеточных мембран тромбоцитов, эндотелиоцитов (клеток, выстилающих внутреннюю поверхность сосудов). Считается, что возникновение таких антител в крови у пациентов связано с нарушением работы иммунной системы.
Антифосфолипидные антитела оказывают прямое повреждающее действие на эндотелий (внутреннюю стенку) сосудов, подавляют производство эндотелиоцитами специальных белков (простациклина, тромбомодулина, антитромбина III), обладающих антикоагулянтными (противосвертывающими) свойствами, вследствие чего они (антитела) способствуют развитию тромбозов. При антифосфолипидном синдроме, в очень редких случаях, может иметь место двусторонний тромбоз надпочечниковых вен, что может послужить причиной повреждения тканей коры надпочечников (из-за нарушения венозного оттока из тканей надпочечников) и развития болезни Аддисона.
Ткани коркового вещества надпочечников довольно часто поражаются при синдроме диссеминированного внутрисосудистого свертывания крови (ДВС-синдроме), который является одной из патологий системы гемостаза (система, контролирующая жидкое состояние крови и остановку кровотечений). На первых стадиях ДВС-синдрома в различных тканях и органах образуются многочисленные мелкие тромбы (гиперкоагуляция крови), что впоследствии (на более поздних стадиях данного синдрома) осложняется коагулопатией потребления (то есть истощением системы свертывания), сопровождающейся тяжелым нарушением свертывания крови и развитием геморрагического синдрома (в различных органах и тканях возникают спонтанные трудно останавливаемые кровотечения).
Причинами ДВС-синдрома могут служить разнообразные состояния, такие как тяжелые механические травмы, гемолитические анемии (снижение количества эритроцитов в крови на фоне их чрезмерного разрушения), лейкозы, опухоли, системные бактериальные, вирусные, грибковые инфекции, аутоиммунные заболевания, внутриутробная гибель плода, преждевременная отслойка плаценты, переливание несовместимой крови и др. При ДВС-синдроме в сосудах тканей коры надпочечников можно обнаружить многочисленные мелкие тромбы, которые служат непосредственной причиной расстройства микроциркуляции, нарушения кровоснабжения, гибели клеток клубочковой, пучковой и сетчатой зон и развития первичной надпочечниковой недостаточности (болезни Аддисона).
Синдром Уотерхауса-Фридериксена представляет собой патологию, возникающую в результате острого геморрагического инфаркта обоих надпочечников (то есть массивного кровоизлияния внутрь тканей надпочечников) и обычно наблюдающуюся при сепсисе (тяжелое, системное, воспалительное состояние, вызванное распространением инфекции по всему организму из первичного очага). При сепсисе нередко развивается ДВС-синдром, который, по сути, и служит непосредственной причиной кровоизлияния внутрь надпочечников. При таком внутреннем кровотечении ткани надпочечников быстро переполняются кровью. Кровоток в них резко замедляется, венозная кровь из надпочечников не удаляется, а новая артериальная кровь не поступает в достаточных количествах. Из-за этого клетки коры надпочечников быстро погибают. Развивается надпочечниковая недостаточность. Быстрое переполнение надпочечников кровью при синдроме Уотерхауса-Фридериксена спровоцировано не только нарушением свертываемости крови (причиной которого служит ДВС-синдром), но и особенностями кровоснабжения самих надпочечников.
Чаще всего синдром Уотерхауса-Фридериксена встречается при сепсисе, развивающимся на фоне менингококковой инфекции.

Отсутствие в организме кортизола делает его очень чувствительным к стрессовым для него факторам (например, инфекциям, физическому перенапряжению, механическим травмам и др.), при действии которых, собственно говоря, и происходит декомпенсация болезни Аддисона.
Кортизол является одним из гормонов, регулирующих углеводный обмен в организме. Он стимулирует образование глюкозы из других химических веществ (глюконеогенез), гликолиз (распад гликогена). Кроме того кортизол оказывает похожее с альдостероном действие на почки (то есть он способствует задержке в организме воды и натрия и удалению калия). Данный гормон также влияет на белковый и жировой обмен, усиливая распад белков и накопление жиров в периферических тканях. Кортизол хорошо взаимодействует с гормонами щитовидной железы и катехоламинами, то есть гормонами мозгового вещества надпочечников. Дефицит кортизола при болезни Аддисона приводит к нарушению углеводного, белкового, жирового обмена и снижению общей резистентности, то есть сопротивляемости организма стрессу.
При болезни Аддисона у пациентов часто наблюдается гиперпигментация кожных покровов (повышенное отложение в коже пигмента меланина). Она вызвана избытком в крови меланоцитостимулирующего гормона, который стимулирует меланоциты (пигментные клетки) кожи к производству меланина. Такой избыток возникает вследствие того, что при первичном гипокортицизме в гипофизе увеличивается концентрация общего для меланоцитостимулирующего и адренокортикотропного гормонов предшественника – проопиомеланокортина. Проопиомеланокортин не обладает гормональными свойствами. По химической структуре он является большой белковой молекулой, которая при расщеплении (определенными ферментами) разделяется на несколько пептидов-гормонов (адренокортикотропный, меланоцитостимулирующий, бета-липотропный гормоны и др.). Увеличенное содержание в крови меланоцитостимулирующего гормона постепенно вызывает потемнение кожи, поэтому болезнь Аддисона еще называют бронзовой болезнью.
При первичном гипокортицизме у пациентов наблюдается прогрессирующая потеря массы тела. Это связано с постоянными потерями организмом жидкости, присутствием у них анорексии (отсутствия аппетита) и истинным снижением количества мышечной массы. У них часто отмечается мышечная слабость, миалгия (боли в мышцах), мышечные судороги, тремор (непроизвольное дрожание пальцев рук), нарушение чувствительности конечностей. Мышечную симптоматику можно объяснить нарушениями водно-электролитного баланса (в частности, повышенным содержанием калия и кальция в крови), которые обычно отмечаются у таких больных.
Достаточно распространенной при болезни Аддисона является разнообразная гастроинтестинальная (желудочно-кишечная) симптоматика в виде тошноты, рвоты, запоров (иногда диареи), диффузных (распространенных) болей в животе. Больные постоянно испытывают влечение к соленой пище. Кроме этого их постоянно беспокоит чувство жажды, поэтому они часто пьют воду. Нередко такие пациенты долгое время наблюдаются у гастроэнтеролога в связи с тем, что у их выявляют различные заболевания желудочно-кишечной системы (например, язву желудка, двенадцатиперстной кишки, спастический колит, гастрит), а надпочечниковая недостаточность остается продолжительное время необнаруженной. Гастроинтестинальная симптоматика при болезни Аддисона, как правило, коррелирует со степенью анорексии (отсутствия аппетита) и снижения массы тела.
Одним из основных признаков болезни Аддисона служит гипотония (низкое артериальное давление). У большинства больных систолическое артериальное давление колеблется в пределах 110 – 90 мм.рт.ст., а диастолическое может падать ниже 70 мм.рт.ст. На начальных этапах болезни гипотония может иметь только ортостатический характер (то есть артериальное давление будет падать при смене положения тела с горизонтального на вертикальное). В дальнейшем артериальная гипотония начинает возникать при воздействии на организм практически любого для человека стрессового фактора. Кроме низкого артериального давления также может наблюдаться тахикардия (учащенное сердцебиение), боли в области сердца, одышка. Иногда артериальное давление может оставаться в пределах нормальных значений, в редких случаях оно может быть повышенным (особенно у пациентов с гипертонической болезнью). У женщин, страдающих болезнью Аддисона, порой нарушается менструальный цикл. Месячные либо исчезают полностью (то есть наступает аменорея), либо становятся нерегулярными. Это нередко серьезно сказывается на их репродуктивной функции и выливается в различные проблемы, связанные с беременностью. У мужчин при этом заболевании появляется импотенция (нарушение эрекции полового члена).
Гиперпигментация (потемнение кожи) при болезни Аддисона является одним из важнейших симптомов, характерных для данной патологии. Обычно существует четкая корреляция (зависимость) между давностью присутствия у пациента надпочечниковой недостаточности, ее тяжестью и интенсивностью окраски кожных покровов и слизистых оболочек, так как этот признак возникает у больных одним из первых. В большинстве случаев, сначала начинают темнеть открытые участки тела, которые постоянно контактируют с солнечным светом. Чаще всего ими являются кожа рук, лица и шеи. Кроме того наблюдается усиление пигментации (отложения меланина) в области тех участков тела, которые в норме имеют достаточно интенсивную темную окраску. Речь идет о коже мошонки, сосков, перианальной зоны (кожный покров вокруг ануса). Затем начинает темнеть кожа складок на ладонях (ладонных линий), а также тех участков, о которых постоянно трутся складки одежды (такое наблюдается в области воротника, пояса, локтевых сгибов и др.).
В некоторых случаях у части пациентов может темнеть слизистая оболочка десен, губ, щек, мягкого и твердого неба. В более поздних стадиях отмечается диффузная гиперпигментация кожи, которая может иметь различную выраженность. Кожный покров может приобретать дымчатый, бронзовый, бурый оттенок. Если болезнь Аддисона вызвана аутоиммунным разрушением коры надпочечников, то нередко на фоне пигментации на коже у пациентов может появляться витилиго (беспигментные, белые пятна). Витилиго может возникать практически в любом месте на теле и иметь различные размеры и очертания. Его достаточно легко обнаружить, так как кожа у таких больных гораздо темнее, чем сами пятна, что создает между ними четкий контраст. Очень редко при болезни Аддисона гиперпигментация кожи может отсутствовать или быть минимально выраженной (незаметной), такое состояние называется «белый аддисонизм». Поэтому отсутствие потемнения кожи еще не является доказательством того, что у данного пациента нет надпочечниковой недостаточности.
Кроме того, помимо лабораторных тестов для подтверждения первичного гипокортицизма назначают кратковременные и длительные диагностические пробы. Эти пробы являются стимуляционными. Пациенту вводят внутримышечно или внутривенно искусственно синтезированный адренокортикотропный гормон (АКТГ), который выпускается под коммерческим названием синактен, синактен-депо или цинк-кортикотропин. В норме, при попадании в организм, данные препараты должны простимулировать кору надпочечников, вследствие чего ее ткани начнут интенсивно выделять гормоны (кортизол), концентрацию которых и определяют в крови через 30 и 60 минут после введения препаратов. Если пациент болен болезнью Аддисона, то надпочечники не смогут адекватно отвечать на стимуляцию синактеном (или синактеном-депо, или цинк-кортикотропином), в результате чего уровень надпочечниковых гормонов в плазме крови останется неизменным.
После того как было осуществлено подтверждение присутствия у пациента болезни Аддисона, врачу важно установить ее этиологию. Поскольку в подавляющем большинстве случаев (в 80 — 90%) причиной этого эндокринного заболевания служит аутоиммунное поражение тканей коры надпочечников, то больному необходимо сдать кровь на иммунологическое исследование. С помощью него можно будет выявить антитела к ферментам надпочечникового стероидогенеза (процесса образования стероидных гормонов) – 21-гидроксилазе (P450c21), 17а-гидроксилазе (P450c17), ферменту отщепления боковой цепи (P450scc), являющихся маркерами (индикаторами) первичного аутоиммунного гипокортицизма. Если такие антитела не были обнаружены, то следующим диагностическим тестом, который должен быть назначен – это биохимическое исследование крови на содержание в ней длинноцепочечных жирных кислот (ДЖК).
Выявление ДЖК является важным диагностическим признаком адренолейкодистрофии, которая является третьей по статистике причиной развития болезни Аддисона. В случае отрицательного результата на наличие в крови ДЖК пациенту обычно назначают прохождение лучевых исследований (компьютерной томографии, магнитно-резонансной томографии), необходимых для визуализации структуры тканей коры надпочечников. Эти исследования, как правило, подтверждают наличие в надпочечниках метастазов рака или туберкулезного очага.
Диагностические мероприятия в отношении ДВС-синдрома, синдрома Уотерхауса-Фридериксена, антифосфолипидного синдрома, грибковых инфекций, ВИЧ-инфекции довольно сложно рассматривать, так как существует множество факторов, влияющих на выбор того или иного диагностического метода. Все зависит от конкретной ситуации. К тому же все эти патологии являются довольно редкими причинами болезни Аддисона, и заподозрить присутствие надпочечниковой недостаточности при них не всегда так просто.
| Название метода | Зачем проводиться данное исследование? |
| Анамнез | При сборе анамнеза врач расспрашивает пациента о беспокоящих его жалобах и об условиях, которые способствовали их появлению. Основными симптомами болезни Аддисона являются повышенная утомляемость, общая слабость, головокружение, головная боль, обморочные состояния, чувство беспокойства, тревоги, жажды, влечения к соленой пище, мышечная слабость, миалгия (боли в мышцах), мышечные судороги, боли в животе, тошнота, рвота, нарушение менструального цикла и др. |
| Внешний осмотр | При внешнем осмотре пациентов, страдающих болезнью Аддисона, можно выявить повышенную пигментацию кожных покровов, витилиго, снижение веса, артериальную гипотонию (пониженное артериальное давление), различные психические расстройства (нарушение памяти, снижение мотивации, потерю интереса к происходящим событиям, повышенную раздражительность, подавленность, депрессию и др.), тремор (непроизвольное дрожание пальцев рук), нарушение чувствительности конечностей. |
| Рентгенография и компьютерная томография | Компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) используются с целью выявления в надпочечниках метастазов, туберкулезных очагов. Рентгенография обычно назначается с целью выявления в легких туберкулезного процесса. КТ и МРТ головного и спинного мозга назначаются для подтверждения диагноза адренолейкодистрофии. |
| Магнитно-резонансная томография | |
| Общий анализ крови | При болезни Аддисона в общем анализе крови можно обнаружить анемию (снижение количества эритроцитов и гемоглобина), лимфоцитоз (увеличение количества лимфоцитов), нейтропению (снижение количества нейтрофилов), эозинофилию (увеличение количества эозинофилов), повышенное СОЭ (скорость оседания эритроцитов). |
| Биохимический анализ крови | Биохимическое исследование крови позволяет обнаружить гипогликемию (низкий уровень глюкозы), гипонатриемию (снижение уровня натрия), гипохлоремию (снижение уровня хлора), гиперкальциемию (повышенное содержание кальция), гиперкалиемию (повышенное содержание калия), сниженный уровень кортизола, альдостерона, повышенную концентрацию адренокортикотропного гормона (АКТГ), ренина. Если врач подозревает у пациента адренолейкодистрофию как причину развития болезни Аддисона, то он ему также может назначить анализ на содержание в крови длинноцепочечных жирных кислот (ДЖК). |
| Иммунологический анализ крови | Иммунологический анализ крови назначается для подтверждения аутоиммунного генеза (происхождения) надпочечниковой недостаточности. В таких случаях пациент должен пройти тестирование на содержание в крови антител к ферментам надпочечникового стероидогенеза (процесса образования стероидных гормонов) – 21-гидроксилазе (P450c21), 17а-гидроксилазе (P450c17), ферменту отщепления боковой цепи (P450scc). Такое исследование также может выявить антитела к вирусу иммунодефицита человека (ВИЧ) и системным грибковым инфекциям, которые могут быть одной из причин развития болезни Аддисона. Кроме того иммунологический анализ часто назначается при подозрении на антифосфолипидный синдром, при котором в плазме крови можно обнаружить антикардиолипиновые антитела, антитела к В-2-гликопротеину 1 и волчаночный антикоагулянт (ВА). |
| Общий и биохимический анализ мочи | В анализе мочи можно выявить увеличение ее суточного объема, гипостенурию (снижение относительной плотности мочи), повышенное содержание натрия, сниженное количество альдостерона, 17-оксикортикостероидов (общее содержание различных типов глюкокортикоидов, образующихся в коре надпочечников), а также 17-кетостероидов (андрогенов, синтезируемых корой надпочечников). |
| Диагностические пробы | Кратковременные (с синактеном) и длительные (с синактеном-депо или цинк-кортикотропином) диагностические пробы при болезни Аддисона выявляют существенное снижение секреции гормонов корой надпочечников при их стимуляции. |
| Биопсия ткани надпочечников | Биопсия (микрохирургическая операция, направленная на взятие кусочка ткани для цитологического исследования) ткани надпочечников производится крайне редко. В большинстве случаев, ее делают для уточнения характера поражения тканей коры надпочечников. |
| Общий анализ мокроты | Общий анализ мокроты назначается в тех случаях, когда у врача имеется подозрение на туберкулезное поражение коры надпочечников пациента. |
В качестве заместительных минералокортикоидов обычно назначается препарат кортинефф (или флудрокортизон). Его нужно пить по утрам (один раз в сутки). Суточная доза, как правило, подбирается индивидуально и всегда колеблется в пределах от 0,05 до 0,2 мг. Адекватность назначения кортинеффа должна постоянно находиться под клиническим и лабораторным контролем.
У пациентов, проходящих медикаментозное лечение с помощью данного гормонального препарата, должно быть нормальное артериальное давление, уровень калия, натрия и концентрации ренина (специфический фермент, вырабатывающийся почками) в плазме крови. Кроме того у них не должно быть выявлено признаков отечности (например, отеков на ногах, руках, лице), так как она будет свидетельствовать о задержке жидкости в организме, что будет служить косвенным признаком передозировки кортинеффа. Подбор дозировки этого препарата при беременности осуществляется с учетом уровня калия в крови и артериального давления. В таком случае дозировку, зачастую, приходится повышать, из-за того что в организме у беременной происходят определенные гормональные сдвиги.
Заместительные минералокортикоиды при болезни Аддисона обязательно стоит назначать в комплексе с синтетическими глюкокортикоидами. В зависимости от продолжительности своего действия последние делятся на три группы (короткого, среднего и длительного действия). Глюкокортикоиды короткого действия (гидрокортизон, кортизон) могут назначаться либо два (утром и после обеда), либо три (утром, после обеда и вечером) раза в сутки. Препараты средней продолжительности действия (преднизолон) обычно нужно употреблять два раза в сутки (утром и после обеда). Третью разновидность глюкокортикоидов (дексаметазон), которые имеют большую продолжительность действия и долго не выводятся из организма, рекомендуется выпивать по одному разу в сутки (утром или поздним вечером). Все виды гормональных лекарств следует использовать после приема пищи.
| Группа глюкокортикоидов | Название препарата | Время приема | Дозировка |
| Глюкокортикоиды короткого действия (трехразовая схема) | Гидрокортизон | Утром | 15 — 20 мг |
| После обеда | 5 – 10 мг | ||
| Вечером | 5 мг | ||
| Кортизон | Утром | 25 мг | |
| После обеда | 12,5 мг | ||
| Вечером | 6,25 мг | ||
| Глюкокортикоиды короткого действия (двухразовая схема) | Гидрокортизон | Утром | 20 мг |
| После обеда | 10 мг | ||
| Кортизон | Утром | 25 мг | |
| После обеда | 12,5 мг | ||
| Глюкокортикоиды средней продолжительности действия | Преднизолон | Утром | 5 мг |
| После обеда | 2,5 мг | ||
| Глюкокортикоиды длительного действия | Дексаметазон | Утром или поздним вечером | 0,5 мг |
Как и в случае с минералокортикоидами, за эффективностью лекарственной терапии синтетическими глюкокортикоидами (гидрокортизоном, преднизолоном, дексаметазоном, кортизоном) также необходимо пристально наблюдать. При правильном лечении у пациента должны пропасть основные признаки болезни Аддисона — общая слабость, повышенная утомляемость, хроническая усталость, периодические головные боли, головокружение, чувство голода, артериальная гипотензия (сниженное артериальное давление), гиперпигментация на коже, неврологические и психические расстройства (нарушение памяти, снижение мотивации, потеря интереса к происходящим событиям, повышенная раздражительность, подавленность, депрессия и др.) и др.
После начала лечения масса тела обычно начинает сразу же восстанавливаться, при этом чрезмерного набора веса не должно происходить (это будет признаком передозировки глюкокортикоидов). Гастроинтестинальная (желудочно-кишечная) симптоматика на фоне заместительной гормональной терапии минералокортикоидами и глюкокортикоидами также должна довольно быстро исчезнуть. Следует помнить, что гормональные средства, которые назначают при надпочечниковой недостаточности, имеют достаточное количество побочных эффектов и противопоказаний, поэтому необходимо строго придерживаться того курса лечения (и тех дозировок препаратов), которые назначит врач.
Если было установлено, что болезнь Аддисона была вызвана туберкулезной инфекцией, то пациенту необходимо назначить дополнительное лечение, которое должно включать антибиотики (рифампицин, стрептомицин, изониазид, этамбутол и др.). Антибактериальные средства при туберкулезе назначаются по специальным терапевтическим схемам и подбираются индивидуально. При грибковом поражении коры надпочечников назначают системные противогрибковые препараты (например, кетоконазол, флуконазол и др.). При антифосфолипидном синдроме дополнительно к гормональной терапии назначают антикоагулянты непрямого действия (варфарин, аценокумарол и др.) и антиагреганты (аспирин). Выбор тактики лечения при ДВС-синдроме и синдроме Уотерхауса-Фридериксена всегда зависит от их этиологии, степени тяжести и наличия осложнений. При метастатическом поражении коры надпочечников оперативное вмешательство, как правило, ничего полезного пациенту не даст, поэтому его лечат только с помощью заместительной гормональной терапии.
Минералокортикоиды и глюкокортикоиды не стоит принимать в таблетированной форме, если у пациента имеется желудочно-кишечное расстройство. В таких случаях лучше ввести препарат в виде инъекции (парентерально). Дело в том, что нарушения в желудочно-кишечной системе могут серьезно повлиять на всасывание гормональных препаратов в кровь, вследствие чего нормальный режим суточного дозирования будет испорчен. Если пациенту с болезнью Аддисона необходимо провести плановую операцию по какому-либо поводу (например, удалению аппендикса, желчного пузыря, грыжи и др.), то ему в дни перед оперативным вмешательством должен быть назначен курс инъекций гидрокортизона по 50 мг через каждые 8 часов. Непосредственно перед операцией ему необходимо вколоть 75 — 100 мг гидрокортизона внутримышечно. Во время операции ему следует капельно ввести 75 — 100 мг данного препарата, разбавленного в растворе глюкозы.
После оперативного вмешательства первые четверо суток больному нужно осуществлять инъекции гидрокортизона по 50 мг каждые 6 – 8 часов. На 5 – 6 сутки дозу гидрокортизона сокращают. В это время следует вводить по 50 мг 2 раза в день и употреблять в таблетированном виде преднизолон по 5 – 10 мг 2 – 3 раза в сутки. С 7 — 8 суток пациента переводят на обычную схему терапевтического лечения глюкокортикоидами, которые уже полностью следует принимать в виде таблеток. Дозировка минералокортикоидов подбирается индивидуально. Такая медикаментозная терапевтическая схема в дооперационный, операторный и послеоперационный периоды необходима, для того чтобы подготовить организм пациента к сильному стрессу, коим является оперативное вмешательство.

Пищевой рацион у них должен иметь высокую энергетическую ценность, что в скором времени (при правильно назначенном медикаментозном лечении) поможет им быстро набрать нормальный вес.
В сутки пациенты с болезнью Аддисона должны употреблять увеличенное количество белков (1,5 г/кг массы тела), углеводов (450 – 500 г/сут) и жиров (120 – 130 г/сут). Режим питания должен быть дробный. Принимать пищу стоит 4 – 5 раз в день мелкими порциями. В рацион обязательно должны быть включены продукты, стимулирующие аппетит и желудочно-кишечную секрецию (например, мясные бульоны, соусы, маринованные овощи, яйца и др.), которые довольно часто бывают нарушены у таких больных.
| Примеры продуктов, которые можно употреблять при болезни Аддисона | Примеры продуктов, которые не желательно потреблять при болезни Аддисона |
|
|
Если у пациента развился аддисонический криз, его необходимо сразу же госпитализировать. Лечение в таких ситуациях сводится к массивной регидратационной (то есть внутривенному вливанию больному жидкости), гормональной и этиотропной терапии. В качестве регидрационных растворов обычно используют раствор глюкозы. Гормональная терапия включает внутривенное введение пациенту больших доз гидрокортизона (100 мг) несколько раз в сутки. Далее дозу данного препарата постепенно уменьшают. При таких высоких дозировках гидрокортизона пациенту нет нужды еще назначать минералокортикоиды (кортинефф). Последние чаще всего начинают прописывать пациенту в тот момент, когда суточная дозировка глюкокортикоидов снижается ниже 100 мг/сут. При стабилизации состояния пациента его плавно переводят на препараты в таблетированной форме. Этиотропная терапия, назначаемая при аддисоническом кризе, требуется для устранения самой причины, которая могла его вызвать. В большинстве случаев, в качестве такой терапии используют антибиотики (в том случае, если аддисонический криз был вызван инфекционной болезнью).
У них постоянно имеется общая слабость, повышенная утомляемость, сниженная работоспособность. Им порой часто трудно подняться с постели по утрам.
У большинства пациенток можно наблюдать подавленное состояние, отсутствие инициативности, повышенную раздражительность, нарушение памяти, равнодушие к происходящему вокруг. Они нередко предъявляют жалобы на присутствие у них мышечной слабости, миалгии (болезненности в мышцах), тремора (непроизвольное дрожание пальцев рук), нарушения чувствительности кожи определенных участков на нижних и верхних конечностях. У женщин, страдающих этим недугом, иногда могут выявляться некоторые нарушения в динамике менструального цикла. Месячные, в некоторых случаях, могут просто не возникать (то есть у них наступает аменорея) или быть нерегулярными и несвоевременными, что порой отражается на репродуктивной функции и выливается в проблемы, связанные с зачатием ребенка.
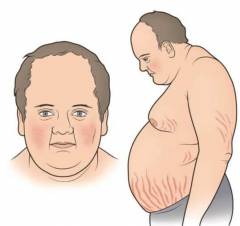
В условиях высокой концентрации в кровяном русле адренокортикотропного гормона надпочечники начинают более интенсивно функционировать, что сопровождается периодическим выбросом в кровь новых порций глюкокортикостероидов (кортизола). Одним из методов лечения болезни Иценко-Кушинга является двусторонняя адреналэктомия (удаление обоих надпочечников), после которой всегда развивается надпочечниковая недостаточность (болезнь Аддисона).
Адренокортикотропный гормон оказывает прямой стимулирующий эффект на клетки пучковой (где образуются глюкокортикостероиды) и сетчатой (где образуются андрогены) зон коры надпочечников. АКТГ практически не влияет на выработку надпочечниками минералокортикоидов (альдостерона).
При вторичном гипокортицизме гипофиз вырабатывает мало адренокортикотропного гормона (или вообще прекращает его производить), вследствие чего ткани надпочечников, зависящие от этого гормона, перестают нормально работать. Так развивается вторичная надпочечниковая недостаточность. Такая недостаточность отличается от болезни Аддисона не только по патогенезу (механизму происхождения заболевания), но и по клинической симптоматике, а также по некоторым лабораторным показателям. Эти отличия и используют врачи при дифференциальной диагностике этих двух патологий.
источник