Но у природы иногда свои планы. По статистике, у каждой пятой семьи в России возникают трудности с зачатием. Иногда это можно объяснить проблемы со здоровьем сердца, однако женский и мужской фактор, как причина бесплодия, сейчас составляют 50/50%, сочетание женского и мужского бесплодия встречается у 20 – 25% пар. К счастью, сейчас мы располагаем большими знаниями и технологиями в решении этой проблемы. В России сейчас выделена новая врачебная специальность – репродуктолог.
Здоровье населения 20 – 45 лет, или т.н. фертильного населения, сейчас, мягко скажем, неблагополучно. Это касается здоровья мужчин и женщин. Причина и в экологических особенностях промышленного края, и в наличии вредных привычек, и в тотальной эпидемии половых инфекций. До сих пор популярным методом контроля рождаемости у нас является аборт, а это — катастрофа для репродуктивного здоровья женщин. Следствием всего этого является не только бесплодие, но и невынашивание беременности, рождение слабых и больных детей. И все наши усилия по сохранению здоровья матери и ребенка оказываются запоздалыми и неэффективными. Поэтому паре, планирующей ребенка, нужно заранее обследоваться и подготовиться к беременности.
При отсутствии беременности в течение одного года регулярной половой жизни без контрацепции необходимость обратиться к врачу становится очевидной.
Если проанализировать основные причины, и отбросить те, что встречаются крайне редко, то фертильность пары, т.е. способность к зачатию, зависит от 5 факторов. Рассмотрим их.
Снижение качества спермы встречается почти у 50 % бесплодных пар. Виной тому неблагоприятная экология, курение, злоупотребление алкоголем, половые инфекции и связанное с ними воспаление мужской половой сферы. В подавляющем большинстве случаев мы сталкиваемся с нетяжелыми изменениями спермограммы, но и их достаточно, чтобы значительно снизить вероятность беременности. Снижается подвижность сперматозоидов, они склеиваются и не могут проникнуть и добраться до яйцеклетки. Диагностика нарушений проста: анализ спермограммы. Обследование проводится после 3 – 4 дневного воздержания от полового контакта. Обследование необходимо проводить 2 раза, так как показатели не стабильны, и можно ошибиться в диагнозе.
Воспаленная шейка матки может не пропустить сперматозоиды в полость матки, что делает беременность невозможной. Вообще – шейка матки – «замочная скважина», с которой начинается репродуктивное здоровье женщины. До беременности важно исследовать состояние шейки матки, восстановить ее.
По маточным трубам сперматозоиды проникают в брюшную полость женщины. В трубах происходит оплодотворение, по ним зародыш (по-научному – зигота), движется в полость матки. Если маточные трубы воспалены, если они вовлечены в спаечный процесс — они не проходимы для сперматозоидов. Иногда проходимость маточных труб утрачивается не полностью, а частично. Тогда оплодотворение происходит, но зародыш не может вовремя добраться по трубе до матки, и развивается внематочная беременность. Это серьезное осложнение.
Матка – «домик», где будет развиваться зародыш до самого рождения. Если условия в этом жилище недостаточно хорошие – беременность либо не наступит, либо будет протекать с осложнениями. Может быть потеря беременности, гибель плода. Чаще всего патология матки, вызывающая бесплодие – это воспалительный процесс. Поэтому важно в первую очередь исключить инфекции, передающиеся половым путем, полноценно пролечить воспаление матки и маточных труб.
Другая проблема со стороны матки – миома, эндометриоз, полипы матки.
Перед беременностью эти заболевания должны быть диагностированы, важно вовремя решить вопрос о необходимости хирургического лечения, гормональной коррекции.
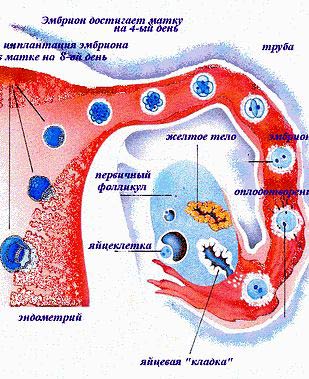
Это один из самых важных моментов. Всей сложной системой управляет головной мозг. Он регулирует работу гипофиза, надпочечников, щитовидной железы, яичников, и запускает менструальный цикл. Цикл начинается с первого дня менструации. В одном из яичников, в специальном пузырьке – фолликуле, растет женская половая клетка – яйцеклетка. На 14 – 15 день менструального цикла фолликул достигает размеров 20 мм, и яйцеклетка выбрасывается из яичника в брюшную полость. Это называется овуляцией. Две недели до овуляции называются первой фазой менструального цикла. Яйцеклетка попадает в маточную трубу, где встречается со сперматозоидом. Так происходит — Зачатие.
Участок в яичнике, откуда вышла яйцеклетка, превращается в желтое тело. Оно вырабатывает прогестерон – гормон, необходимый для развития зародыша. Желтое тело работает 2 недели, и погибает, если беременность не наступила. Эти 2 недели называются второй, или прогестероновой фазой цикла. Если беременности нет – приходит менструация. Если зачатие произошло – зародыш движется по трубе в матку и прикрепляется там с 4го по 8ой день от овуляции. Это называется имплантацией. Матка должна быть здорова и подготовлена к принятию зародыша. За это в большой степени отвечает прогестерон. Очевидно, что без полноценного овуляторного цикла наступление беременности невозможно.
Выбор метода лечения зависит от многих факторов: причины и тяжести бесплодия, состояния здоровья другого партнера, длительности бесплодия. В конечном счете, выбор метода — это осознанный выбор супружеской пары на основе рекомендаций врача. После тщательного анализа возможных причин бесплодия, лечение подбирается индивидуально и состоит из этапов:
1. Медикаментозный – лечение воспалительного процесса, восстановление иммунитета и кровообращения в тканях, устранение половых инфекций, коррекция хронических заболеваний.
Лечение лекарствами может быть успешным, в частности, когда бесплодие вызвано инфекцией и воспалением половых органов; в случае гормонального дисбаланса; когда бесплодие возникает на фоне различных заболеваний, лечение которых может восстановить утраченную фертильность.
Лечение воспаления и устранение ИППП играет ключевую роль, так как можно повлиять сразу на 4 первые фактора: качество спермы у мужчины, шейку матки, матку, маточные трубы. Этот этап колоссально важен. Он сам по себе позволит получить нормальную беременность у 60 — 70% пар. Он также подготовит будущую маму к вынашиванию здорового ребенка, защитит от осложнений.
Несмотря на широкие перспективы искусственного зачатия, ВОЗ настоятельно рекомендует отдавать приоритеты, при наличии возможности, самостоятельно наступившей беременности. 1 этап занимает, в среднем, от 1 до 6 месяцев.
2. Хирургический этап – коррекция спаечного процесса, удаление миомы, эндометриоза, полипов, и т.д. — у женщин; у мужчин: наличие варикоцеле требует оперативного вмешательства; при нарушенной проходимости семявыносящих протоков показана восстановительная операция с использованием микрохирургических методов.
Этот этап необходим лишь некоторым парам, и можно совместить по времени с 1 этапом.
После 1 и 2 этапов врач репродуктолог оценивает шансы пары на самостоятельную беременность. Решается вопрос о целесообразности так называемого режима ожидания – когда пара в течение нескольких месяцев пробует забеременеть самостоятельно.
Нередко бывает, что режим ожидания не рационален, так как за это время снова могут возникнуть устраненные на 1 и 2 этапе проблемы. Или точно известно, что шансы на самостоятельную беременность низки – непроходимые трубы, нет овуляции, плохое качество спермы.
Тогда необходимо приступить к 3 этапу.
3. Вспомогательные репродуктивные технологии (ВРТ) — методы, при которых отдельные или все этапы зачатия происходят вне тела человека. ВРТ не устраняют причины, приведшие к бесплодию, но в большинстве случаев приводят к рождению здорового ребенка. Этап применяется, когда пара физически готова к беременности, т.е. после 1 этапа, но беременность не получается или возможности для естественного зачатия нет. Из всех бесплодных пар эта группа составляет не более 20 – 30%.
К методам ВРТ относятся:
- Донорство.При некоторых типах мужского бесплодия (невозможность получить сперматозоиды мужа, риск передачи генетических аномалий, неуспешность или невозможность проведения другого лечения) используется сперма мужчины-донора из банка доноров спермы. Внутриматочная инсеминация спермой донора — метод, идентичный ВМИ спермой мужа, за исключением того, что сперма предоставляется донором. ЭКО с донорской спермой — ЭКО выполняется с использованием донорской спермы.
- Внутриматочная инсеминация. Здоровой подготовленной женщине в полость матки в дни овуляции вводят специально подготовленную сперму мужа или, при наличии показаний, донора. Процедура простая, не требует госпитализации и больших денежных затрат. Она позволяет в пробирке улучшить подвижность сперматозоидов, и устраняет шеечный фактор бесплодия.
- ЭКО и ПЭ (экстракорпоральное оплодотворение и перенос эмбрионов). Женщине заранее готовят яичники, и в них созревает не одна, как в природе, а до 15 – 20 яйцеклеток. Затем под наркозом все их извлекают из яичников тонкой иглой, и оплодотворяют в лаборатории. Получается от 5 до 15 эмбрионов. На 4 – 5 день 1 – 2 зародыша, которые к этому моменту состоят из нескольких клеток, тоненьким катетером безболезненно вводятся в полость матки. Остальные замораживаются, и готовы к введению в случае неудачи. Если для зародышей к этому времени в матке созданы подходящие условия, как правило, происходит имплантация, и развивается нормальный ребенок.
- ИКСИ.В случае выраженной патологии спермы, возможно искусственное введение сперматозоида непосредственно в яйцеклетку с помощью микроиглы. Даже при отсутствии сперматозоидов в эякуляте, есть возможность получить сперматозоиды из яичка и добиться долгожданной беременности.
Методы ВРТ способны помочь паре в самых безнадежных ситуациях. Вероятность зачатия после 1 ПЭ достигает 50 – 60 %. «Дети из пробирки» после рождения ничем не отличаются от обычных детей. От пары требуется терпеливо и настойчиво, шаг за шагом, двигаться к своей цели — рождению здорового малыша, а современная медицина может сделать их продвижение наиболее рациональным и коротким.
От пары требуется терпеливо и настойчиво, шаг за шагом, двигаться к своей цели — рождению здорового малыша, а современная медицина может сделать их продвижение наиболее рациональным и коротким.
Дементьева Т.Г., врач акушер, гинеколог-эндокринолог, репродуктолог.
источник
Примерно у 25% семейных пар беременность не наступает в течение одного года супружеской жизни.
Из них 15% лечатся по поводу бесплодия, но все же не менее 5 % семейных пар так и остаются бесплодными.
На долю мужского фактора, по статистике, приходится примерно 40% причин бесплодного брака и предполагается, что данный процент будет увеличиваться, поскольку в последние десятилетия у мужчин наблюдается необъяснимое прогрессивное снижение числа сперматозоидов в эякуляте (рис. 8.1).
Рис. 8.1. Уменьшение количества сперматозоидов у здоровых мужчин за 60 лет XX в.
Около 40% составляет женское бесплодие и 20% — смешанное бесплодие. Это означает, что примерно 6-8% женатых мужчин являются бесплодными.
Прогностические факторы при бесплодии:
• Длительность бесплодия.
• Первичное или вторичное бесплодие.
• Результаты анализа семенной жидкости (эякулята).
• Возраст и статус плодовитости пациента.
Диагноз мужского бесплодия ставится на основании данных анамнеза и данных спермограммы (показатели нормальной спермограммы приведены ниже). Во всех случаях необходимо одновременное обследование партнерши, так как, по данным ВОЗ, у одной из четырех пар. консультирующихся по поводу бесплодия в браке, имеются нарушения плодовитости обоих партнеров.
По имеющимся данным, в настоящее время обращаемость мужчин молодого и среднего возраста по поводу бесплодия в России составляет 47 на 100 000 человек мужского населения (Аполихин О. И., 2007). При этом примерно в 50% случаев причиной бесплодия являются урологические заболевания, которые достаточно эффективно лечатся. Речь идет о таких заболеваниях, как варикоцеле, заболевания, передающиеся половым путем (ЗППП) и инфекции придаточных половых желез (простатиты, везикулиты, эпидидимоорхиты). Инфекции сопровождаются повышением уровня антиспермальных антител, которые являются причиной иммунологического бесплодия.
Во всех случаях мужского бесплодия необходимо постараться найти его причину. Основные причины мужского бесплодия приведены в табл. 8.1. Достаточно часто найти причину не удается, тогда говорят об идиопатической бесплодии.
Таблица 8.1. Основные причины мужского бесплодия
Варикоцеле — варикозное расширение вен лозовидного сплетения мошонки (рис. 8.2).
Рис. 8.2. Механизм развития варикоцеле
Встречается в популяции мужчин молодого возраста примерно в 0.5-10% случаев, однако частота его выявления при бесплодии достигает 40%. Левостороннее идиопатическое варикоцеле встречается в 80% случаев, правостороннее и двустороннее — примерно в 10% случаев каждое.
Исследования влияния варикоцеле на репродуктивную функцию мужчин проводятся давно, и в настоящее время четко сформулированы диагностические критерии данной патологии и, самое главное, показания к оперативному лечению, которое включает около 120 предложенных в разные годы вариантов операции.
Не вызывает сомнения факт негативного влияния варикоцеле на сперматогенез (перегрев мошонки, гипоксия ткани яичка, нарушение гематотестикулярного барьера с индукцией выработки антиспермальных антител, астенозооспермия и т.д.), поэтому у мужчин с бесплодием и варикоцеле, при исключении других причин бесплодия, рекомендуется хирургическое лечение варикоцеле. Другими показаниями к оперативному лечению варикоцеле являются мошоночные боли и признаки атрофии яичка. Пациенты с неосложненным варикоцеле и отсутствием бесплодия должны находиться под динамическим наблюдением.
Оценку фертильности эякулята после оперативного лечения варикоцеле следует проводить не ранее, чем через 3 мес, (полный цикл законченного сперматогенеза). Улучшение показателей эякулята у большинства пациентов происходит, как правило, в течение 6-12 мес после операции. Но у ряда пациентов улучшения сперматогенеза после оперативного лечения не наступает. Ряд авторов рекомендует после варикоцелэктомии назначать сосудистые, венотонические и антиоксидантные препараты на срок не менее 3-6 мес, для более быстрого восстановления сперматогенного эпителия.
Еще одной распространенной причиной нарушения фертильности являются хронические инфекции придаточных половых желез (простатиты, везикулиты, эпидидимиты). Секрет семенных пузырьков обеспечивает до 60-70% объема жидкой части эякулята, а секрет простаты, соответственно, 30-40%. Нарушения физико-химических свойств семенной плазмы — среды обитания сперматозоидов, закономерно приводит к патозооспермии, чаще всего в виде астенозооспермии или индукции «ложных» антиспермальных антител, ассоциированных с инфекцией.
Интенсивное комплексное лечение инфекции половых желез способно привести к улучшению фертильности эякулята у бесплодного мужчины но необходимо помнить о токсическом действии антибиотиков, поэтому оценку эякулята следует проводить не ранее, чем через 3 месяца после их отмены.
Роль ЗППП в этиологии бесплодия у мужчин не вполне ясна. Однако доказанная способность некоторых возбудителей ЗППП (хламидии, трихомонады, гоннококки) вызывать иммобилизацию сперматозоидов делает необходимым этапом диагностики и лечения бесплодных мужчин выявление и санацию половых путей от данных возбудителей при их наличии. Кроме того, показано, что хламидии, трихомонады и гонококки вызывают воспаление простаты (рис. 8.4), а также острые и хронические эпидидимиты.
Рис. 8.4. Цитологический картина хронического простатита (лейкоцитарная инфильтрация и бактерии в секрете простаты)
Общеизвестна что длительный воспалительный процесс в придатках яичка вызывает нарушение дозревания и приобретения подвижности сперматозоидами, а также приводит к нарушению проходимости канала придатка яичка и, соответственно, может быть причиной обструктивных форм бесплодия.
Обследование на другие возбудители (кандиды, гарднереллы, микоплазмы, вирусные инфекции, вирус простого герпеса типов 1 и 2, цитомегаловирус и др.), особенно в отсутствие клинической картины уретрита нецелесообразно и не имеет клинического и практического значения.
Классификация причин мужского бесплодия (ВОЗ, 2006):
01 — психосексуальные расстройства.
02 — причин бесплодия не выявлено.
03 — изолированная патология семенной плазмы.
04 — ятрогенные причины.
05 — системные заболевания.
06 — врожденные аномалии.
07 — приобретенное повреждение яичка.
08 — варикоцеле.
09 — инфекции гениталий.
10 — иммунологический фактор
11 — эндокринные причины.
12 — идиопатическая олигозооспермия.
13 — идиопатическая астенозооспермия.
14 — идиопатическая тератозооспермия.
15 — обструктиная азооспермия.
16 — идиопатическая азооспермия.
Диагностика мужского бесплодия основана на комплексной оценке состояния мужской репродуктивной системы и проводится в определенной последовательности (рис. 8.5).
Рис. 8.5. Примерный алгоритм диагностических мероприятий при мужском бесплодии
Клинические методы обследования:
• Первичный опрос (сбор анамнеза и жалоб).
• Общее медицинское обследование.
• Урогенитальное обследование.
• Обследование терапевтом, генетиком, сексопатологом (по показаниям).
Лабораторно-диагностнческие методы обследования:
• Спермограмма — начальный и основной метод обследования.
• Исследования на ЗППП, в том числе на вирусы.
• Бактериологическое исследование эякулята (в случае лейкоспермии).
• Определение антиспермальных антител (MAR-тест, процент активно подвижных сперматозоидов покрытых антителами).
• Ультразвуковое исследование (УЗИ) органов малого таза.
• Гормональное обследование (тестостерон, лютеинизирующий гормон (ЛГ), фолликулостимулирующий гормон (ФСГ), пролактин, тиреотропный гормон (ТТГ), секс-стероид связывающий глобулин (СССГ)).
• Медико-генетическое исследование.
Биопсия яичка (показана только в случае азооспермии).
Урогенитальный статус исследуется путем осмотра и пальпации органов мошонки. При этом можно выявить варикоцеле, опухоли яичка и его придатка Определяют положение, размеры яичек по орхидометру Прадера и их консистенцию. В норме объем яичек у взрослого мужчины составляет не менее 15 мл. Маленькие (менее 4 мл) плотные яички характерны для синдрома Клайнфельтера.
Объем яичек напрямую коррелирует с фертильностью. поскольку до 80% их объема составляет именно герминогенная ткань, где вырабатываются сперматозоиды При осмотре обращают внимание на состояние и размеры полового члена, выявляют клинические признаки гормональных нарушений (микропенис, малый половой член, горизонтальная линия роста волос на лобке), а также изменения, которые могут явиться причиной нарушения выделения эякулята (гипоспадия, элиспадия), либо нарушать проведение полового акта (бляшки белочной оболочки при болезни Пейрони, фимоз).
Анализ семенной жидкости — важнейший метод оценки состояния сперматогенеза у мужчины. Он позволяет оценить фертильность (плодовитость). Если показатели спермограммы находятся в пределах нормативных достаточно ограничиться одним исследованием. При патоспермии анализ эякулята должен быть выполнен 2-3 раза с интервалом 4-12 нед. (72 дня) при условии полового воздержания не менее 3 дней и не более 7.
Способ получения спермы — мастурбация. Все манипуляции с образцом эякулята выполняются при температуре не ниже 20 и не выше 36 °С. Из полученных спермограмм оценивают лучший результат. При этом учитывают, что самым высоким дискриминационным показателем фертильности спермы является подвижность сперматозоидов.
Несмотря на длительную историю микроскопического изучения сперматозоидов (рис. 8.6), насчитывающую более трех веков, впервые методы количественного анализа были использованы в 1929 с, когда было показано, что пограничное количество сперматозоидов в 1 мл эякулята у здорового мужчины составляет 100 млн. в дальнейшем нижняя граница была снижена до 40 млн а в последние 10-15 лет — до 20 млн.
Рис. 8.6. Строение сперматозоида под элемронным микроскопом
В настоящее время приняты следующие нормативные показатели для оценки спермы (табл. 8.2).
Таблица 8.2. Нормальные значения параметров эякулята
При описании параметров эякулята используется специальная терминология (табл. 8.3).
Таблица 8.3. Терминология, используемая при описании параметров эякулята
Дальнейшая тактика обследования зависит от показателей спермограммы. На рис. 8.7-8.9 представлены алгоритмы обследования мужчин с различными отклонениями в спермограмме.
Рис. 8.7. Схема обследования и тактика ведения пациента с олигозооспермией при отсутствии гипогонадизма
Рис. 8.8. Алгоритм обследования мужчин с небольшим объемом эякулята (менее 1,5 мл) или азооспермией
Рис. 8.9. Алгоритм обследования больного только с одним измененным показателем спермограммы
В обеспечении репродуктивной функции участвует ряд гормонов мужской половой системы, их характеристика и физиологическое действие представлены в табл. 8.4.
Таблица 8.4. Характеристика и физиологическое действие гормонов мужской половой системы, участвующих в репродуктивной функции
Гормональные нарушения среди бесплодных мужчин встречаются чаще, чем в популяции в целом. Гормональное обследование включает определение в крови ФСГ. ЛГ и тестостерона, пролактина (табл. 8.5).
Таблица 8.5. Интерпретация результатов гормональных исследований при патологии эякулята
Определение ФСГ позволяет оценить не только тяжесть нарушения сперматогенеза, но и также провести дифференциальную диагностику между обструктивной (экскреторной) и необструктивной (секреторной) формами бесплодия» Нормальный уровень ФСГ является критерием сохранности сперматогенной функции яичек. Однако, по статистике» 29% мужчин с нормальным уровнем ФСГ имеют те или иные нарушения сперматогенеза.
При гипергонадотропном гипогонадизме (повышенный уровень ФСГ/ЛГ) медикаментозное лечение бесплодия неэффективно.
Наиболее часто причинами гипергонадотропного гипогонадизма являются:
• врожденные заболевания — синдром Клайнфельтера. анорхизм, криптохризм;
• приобретенные нарушения сперматогенеза, обусловленные перенесенными воспалительными и травматическими повреждениями яичка (орхит, перекрут яичка, кастрация), а также токсическими воздействиями (цитостатическая терапия).
Гипогондотропный гипогонадизм (пониженный уровень ФСГ/ЛГ).
Причинами данного заболевания могут быть:
• врожденные заболевания — нарушение секреции ФСГ и ЛГ (часто сочетается с аносмией — синдром Кальмана), изолированное нарушение секреции ЛГ (синдром Паскулиани, или фертильного евнуха), пангипопитуитаризм;
• приобретенные — поражения гипофиза или гипоталамуса любого генеза.
При гипогонадотропном гипогонадизме медицинское исследование должно включать магнитно-резонансную томографию (МРТ) или компьютерную томографию (КТ) головного мозга для исключения опухоли гипофиза.
Измерение концентрации тестостерона крови проводят всем мужчинам с бесплодием, даже при отсутствии клинических признаков гипогонадизма и нарушений сексуальной функции.
Целесообразность определения ЛГ крови заключается б выявлении характера гипогонадизма (соотношения ЛГ/андрогены), что будет указывать на резистентность клеток Лейдига и плохой прогноз в терапии бесплодия.
Уровень пролактина определяется у всех мужчин с бесплодием, поскольку гиперпролактинемия является частой причиной гипогонадизма. Определение уровня эстрадиола проводят только у мужчин с клиническими проявлениями гиперэстрогенемии для исключения эстрогенпродуцирующих опухолей яичек и надпочечников.
Микробиологическое исследование показано при лейкоцитурии, пейкоспермии и при ЗППП. Обычно выполняют четырехстаканную пробу Мирза-Стейми (Meares-Stamey). проводят бактериологические исследования эякулята, а также диагностику ЗППП методом полимеразной цепной реакции.
Урогечитальные инфекции сопровождаются образованием спермато-токсических свободных радикалов, которые ведут к снижению подвижности сперматозоидов. Гонорея и хламидиоз. кроме того, могут вызывать обструкцию семявыносящих путей.
Хромосомные отклонения нередко встречаются у мужчин с первичным бесплодием и олиго- и азооспермией. Не исключено, что часть случаев так называемого идиопатического бесплодия обусловлена генетическими дефектам и.
Самым распространенным генетическим нарушением является синдром Клайнфельтера. обусловленный наличием дополнительной Х-хромосомы (47,XXY). который выявляется примерно у 10% мужчин с азооспермией. Синдром Клайнфельтера сопровождается гипергонадотропным гипогонадизмом, развивающимся после периода полового созревания. Всем больным с подозрением на синдром Клайнфельтера показано генетическое обследование длл оценки кариотипа. У 5 % мужчин с первичным бесплодием могут выявляться делеции AZF-фактора (azoospermia factor).
Кариотипирование и генетическое обследование показано всем мужчинам с первичным бесплодием и содержанием менее 1 млн сперматозоидов в 1 мл эякулята.
При осуществлении интрацитоплазматической инъекции сперматозоида (ИКСИ) оба партнера должны пройти тест на обнаружение мутаций в гене CFTR (ген кодирует белок . регулятор мембранной проводимости, мутация в этом гене вызывает муковисцидоз).
В последнее время накапливается информация о влиянии активности андрогенного рецептора на сперматогенез. Чем активнее рецептор тем лучше показатели сперматогенеза (рис. 8.10).
Рис. 8.10. Влияние структуры андрогенного рецептора (количество CAG . повторов) на количество сперматозоидов
Практическое значение может иметь определение в эякуляте следующих показателей:
• Содержание цинка. лимонной кислоты и кислой фосфатазы. которые отражают секреторную функцию простаты В норме содержание цинка в эякуляте должно быть не менее 2.4 мкмоль/эякулят лимонной кислоты — не менее 52 мкмоль/эякулят, кислой фосфатазы — 200 ЕД/эякулят (Нишлаг Э., 2005).
• Содержание фруктозы — маркер функции семенных пузырьков. В норме уровень фруктозы в эякуляте составляет не менее 13 мкмоль/эякулят. В качестве показателя эндокринной активности фруктоза не имеет того значения, которое ей приписывалось ранее. При низком уровне фруктозы дальнейшую диагностику следует проводить с помощью трансректального ультразвукового исследования (ТРУЗИ) до и после эякуляции. Концентрация фруктозы в эякуляте — маркер не только функции семенных пузырьков, но и проходимости их протоков. Низкий уровень фруктозы (менее 13 мкмоль/эякулят) и рН эякулята менее 7.0, а также высокое содержание лимонной кислоты указывают на врожденное отсутствие семенных пузырьков.
• Маркерами функции придатков яичек служат а-глюкозидаза, L-карнитин и глицерофосфохолин. Уровень нейтральной а-глюкозидазы в норме составляет не менее 11 мЕД/ яэкулят (Нишлаг Э., 2005). Это высокоспецифичный и чувствительный показатель функции придатка яичка. Поскольку данный маркер определяется в эякуляте проще, дешевле и быстрее, чем другие, то именно его и рекомендуется исследовать в первую очередь (Cooper, 1990). Резко сниженное или неопределяемое количество нейтральной а-глюкозидазы на фоне нормального уровня ФСГ и нормального объема яичек указывает на то что причиной патоспермии (азооспермии) является двусторонняя обструкция придатков яичек или семявыносящих путей.
Для этого выявляют антиспермальные антитела класса IgG, IgA. IgM в сперме методами спермоагглютинации и спермоиммобилизации и/или в сыворотке крови. Эти методы трудоемки и имеют ряд недостатков.
В настоящее время наиболее распространенным методом выявления иммунологического бесплодия является MAR-тест — смешанная анти-глобулиновая реакция (mix antiglobulin reaction).
Агглютинация сперматозоидов в свежем эякуляте указывает на присутствие специфических антител к ним — антиспермальных антител. Не все антиспермальные антитела вызывают агглютинацию сперматозоидов: некоторые оказывают цитотоксический эффект и нарушают подвижность сперматозоидов.
Ряд авторов выделяют «истинные» антиспермальные антитела, возникающие в результате повреждения гематотестикулярного барьера под влиянием различных факторов (травма, воспаление, аутоиммунные процессы), и «ложные» антиспермальные антитела, обусловленные адгезией на поверхности сперматозоидов антигенов микроорганизмов, т.е. связанные с инфекционно-воспалительным и процессами в половой системе. В отличие от «истинных» антиспермальных антител, эти антитела успешно элиминируются из эякулята после курса антимикробной терапии простатита, везикулита или урогенитальной инфекции.
Сущность методики MAR-теста заключается в том, что свежую пробу эякулята и покрытые IgA или IgG латексные шарики или эритроциты барана смешивают с антисывороткой к IgA или IgG. Если на поверхности сперматозоида присутствуют соответствующие антитела, антисыворотка свяжет сперматозоиды с шариками или эритроцитами. Затем подсчитывают долю (в %) связанных сперматозоидов.
У здоровых мужчин агглютинация сперматозоидов в эякуляте отсутствует или антиспермальные антитела покрывают не более 10% сперматозоидов. При доле связанных сперматозоидов от 20 до 40% данные рассматриваются как недостоверные, что требует повторения теста. Если же антиспермальные антитела покрывают более 50% сперматозоидов, диагноз иммунологического бесплодия становится весьма вероятным (Abshagea 1998), Из-за вариабельности результатов теста его следует повторять 2-3 раза и дополнительно исследовать взаимодействие сперматозоидов с цервикальной слизью женщины (посткоитальная проба и проба Кремера).
Значение антиспермальных антител, определяемых в сыворотке крови, сомнительно и при обычном обследовании по поводу бесплодия их определение не имеет смысла (Нишлаг 2005).
Биопсия яичка как диагностическая манипуляция показана при азооспермии. Биопсия позволяет дифференцировать секреторные формы бесплодия (тяжелые нарушения сперматогенеза) от экскреторных форм (обструкция семявыносящих путей). Кроме того, при биопсии яичка можно получить генетический материал для проведения ИКСИ при различных вариантах дисгенезии яичек (гипоплазия, гипосперматогенез и т. д.).
Использование материала биопсии яичка для ИКСИ невозможно, если:
• отсутствуют семенные канальцы (тубулярный склероз):
• содержатся только клетки Сертоли (синдром «только клеток Сертоли». или синдром дель Кастильо).
Тактика лечения различных форм мужского бесплодия суммирована в табл. 8.6-8-8.
Таблица 8.6. Классификация мужского бесплодия, основанная на тактике лечения
Таблица 8.7. Алгоритмы лечения мужского бесплодия
Таблица 8.8. Медикаментозное лечение эндокринного бесплодия
Под мдиопатическим бесплодием подразумевают бесплодие неустановленной причины. Поскольку процент идиопатического бесплодия достаточно велик и составляет до 30% случаев в структуре бесплодия, то появилось и значительное количество методов его лечения.
Эффективность большинства существующих немедикаментозных и медикаментозных методов эмпирического лечения не доказана.
Немедикаментоэные методы и мероприятия:
• Замена плавок на трусы. Ношение плавок ведет к перегреванию яичек, что негативно влияет на сперматогенез. Однако все больше авторов в последнее время опровергают представление, что замена нижнего белья улучшает показатели эякулята и сперматогенеза.
• Изменение регулярности половых контактов. Половые контакты, а также любые другие формы половой жизни, сопровождающиеся семяизвержением, должны быть не чаще 1 раза в 4 дня, поскольку срок созревания сперматозоидов составляет 72 часа. При уменьшении данного времени увеличивается процент неподвижных сперматозоидов.
• Отказ от курения. Курение ведет к повышению окислительного стресса, которому сперматозоиды как короткоживущие клетки очень подвержены. Отказ от курения — простое конкретное действие, которое может повысить репродуктивную функцию мужчины Есть данные о повышении уровней пролактина и эстрадиола крови у курящих мужчин, и снижении как концентрации сперматозоидов, так и их подвижности, что способствует субфертильности. Курение усиливает негативное влияние варикоцеле на сперматогенез.
Злоупотреблением никотином считают выкуривание более 10 сигарет в день. Отказ от алкоголя. Не доказано, что умеренный прием алкоголя оказывает негативное влияние на сперматогенез. Избыточное потребление алкоголя нередко сопровождается гипогонадизмом и субфертильностью. Злоупотреблением условно считают прием более 60 г чистого алкоголя в день» что соответствует четырем двойным порциям виски или 2 л крепкого пива.
Стресс — доказанный фактор риска развития дисфункции гипоталамо-гипофизарно-гонадной системы, приводящий к дефициту тестостерона и снижению количества сперматозоидов в эякуляте. Физические упражнения. Умеренные регулярные физические нагрузки оказывают тонизирующее действие на половую систему мужчины в целом, но изнуряющая и длительная физическая активность может способствовать снижению фертильности.
Тепловые профессиональные и бытовые факторы оказывают негативное влияние на сперматогенез. Мужчинам с бесплодием рекомендуется избегать перегревания (посещение бань, саун, парных).
Кроме алкоголя и табака, токсическое влияние на сперматогенез оказывают наркотические препараты (марихуана, героин, кокаин), поскольку они ведут к гиперпролактинемии и андрогенному дефициту а также промышленные яды и химические препараты (свинец, этилена бромид, тяжелые металлы, пестициды и т.д.).
Медикаментозные методы лечения идиопатического бесплодия:
• Витамины. Определенные витамины и изменение характера питания могут улучшать качество спермы и повышать фертильность. Антиоксиданты усиливают подвижность сперматозоидов in vitro (Parinaud et aL 1997), однако в масштабном рандомизированном исследовании лечение мужчин с выраженной астенозооспермией высокими дозами витаминов Е и С не оказало влияния на подвижность сперматозоидов (Rolf et al., 1999). Сбалансированный комплекс витаминов и антиоксидантов, оказывающих положительное действие на сперматогенез, содержится в препарате Геримакс Премиум.
Избыток массы тела сопровождается повышением периферической конверсии тестостерона в эстрогены за счет усиления ароматизации, а гормон жировой ткани лептин оказывает угнетающее действие на синтез как тестостерона, так и ЛГ Поэтому пациентам с бесплодием следует придерживаться принципов рационального питания, а при наличии ожирения — добиться его ликвидации (цель: окружность талии — 94 см).
Антиоксиданты и антигипоксанты
Поскольку оксидативный стресс и повышение свободных радикалов оказывают негативное влияние на сперматогенез, антиоксиданты широко используются в лечении бесплодия. Цинк оказывает положительное действие на функцию простаты, а также на сперматогенез за счет повышения подвижности сперматозоидов. Цинк можно применять в качестве монопрепарата в виде препарата Цинкит длительностью не менее 3 месяцев. Селен улучшает подвижность сперматозоидов. Имеется комплексный препарат цинка и селена (Селцинк).
Низкие уровни фолиевой кислоты (витамин B9) в сыворотке сопровождаются малым количеством и малой подвижностью сперматозоидов. Но рандомизированных исследований на этот счет нет. Антигипоксантные эффекты описаны для полиненасыщенных жирных кислот (омега-три). растительных (ростки молодой пшеницы) и животных (рыбий жир, печень акулы) фитостеринов, солкосерила, актовегина, аскорбиновой кислоты, хотя объективных данных об эффективности указанных субстанций для повышения фертильных свойств эякулята с точки зрения доказательной медицины на сегодняшний день в многоцентровых контролируемых исследованиях либо не получено, либо явно недостаточно.
• Гепатопротекторы — группа препаратов, восстанавливающих и поддерживающих функциональное состояние печени. Роль печени в метаболизме половых гормонов объективно доказана. Именно с дисфункцией гепатоцитов можно связать андрогенный дефицит и гиперэстрогенемиюу мужчин вследствие нарушения синтеза СССГ или избыточного распада тестостерона с ароматизацией при гепатитах и циррозах (особенно, актуальной для российской действительности алкогольной этиологии).
Кроме того, печеночная недостаточность изолированно или в сочетании с почечной недостаточностью может быть причиной симптоматической гиперпролактинемии с формированием гиперпролактинемического гипогонадизма. Поэтому нормализация функции печени у пациентов с бесплодием, вероятно, обеспечивает более сбалансированное гормональное обеспечение сперматогенеза.
Данная группа препаратов довольно часто в литературе последних лет рекомендуется при лечении любых форм мужской инфертильности, правда, степень доказательности таких рекомендаций не превышает категории С или D, Определенные надежды связывают с препаратом адеметионин, выпускаемым под торговым названием «Гептрал», который восполняет дефицит адеметионина и стимулирует его выработку в организме, в первую очередь в печени и головном мозге.
Через комплекс биохимических реакций в печени препарат участвует в обмене таких необходимых для нормального функционирования половой системы мужчины биологически активных веществ, как таурин, спермин, спермидин, глутатион и некоторых других, входящих в структуру рибосом и обеспечивающих процессы микросомального окисления.
Кроме того, он обладает выраженным антидепрессивным эффектом, что является положительным моментом в лечении любых форм нарушения фертильности. которые практически в 100% случаев сопровождаются различной степенью выраженности депрессивно-невротическими реакциями, а назначение «классических» антидепрессантов не может быть рекомендовано у данной категории больных ввиду их негативного влияния на синтез и обмен тестостерона, а также их способность индуцировать лекарственную гиперпролактинемию. Вероятно, исследования ближайших лет смогут ответить на некоторые вопросы, касающиеся применения препарата при мужском бесплодии,
• Препараты ФСГ ЛГ и их сочетание существенно не увеличивают число сперматозоидов при идиопатическом бесплодии. По данным разных исследований, применение гонадотропинов не увеличивало частоту наступления беременностей. В то же время стоимость современных рекомбинантных препаратов ФСГ и ЛГ слишком высока, чтобы рекомендовать их для рутинной эмпирической терапии идиопатической патоспермии.
При импульсной терапии гонадолиберином уровни ЛГ и ФСГ возрастают, но данный препарат дорог, а его применение технически сложно для повседневной практики. Эффективность применения человеческого хорионического гонадотропина (чХГ) / макроглобулина (МГ) (а они применялись более 20 последних лет) для эмпирического лечения идиопатического бесплодия в последние годы ставится под сомнение и считается недоказанной.
Проспективное двойное слепое плацебо-контрояируемое исследование не показало положительного влияния терапии хорионическим гонадотропином (ХГ)/МГ при нормогонадотропной олигоастенотератоспермии ни на параметры эякулята, ни на вероятность наступления беременности (Knuth et al., 1987). Но имеются работы, в которых продемонстрировано двукратное повышение наступления беременности при инсеминации спермой мужа при подготовке чХГ по сравнению с теми пациентками, у которых подготовки не было.
Андрогены и ребаунд-эффект (эффект отмены тестостерона). Этот метод предусматривал полную блокаду сперматогенеза путем введения больших доз экзогенного тестостерона. После того, как наступает практически полная блокада сперматогенеза, тестостерон отменяют.
Предполагалось, что сперматогенез после отмены тестостероны должен улучшиться. Но физиологических предпосылок для этого метода нет, и в клинике этот метод давно не применяется. Это же относится и к современным пероральным препаратам тестостерона, эффект которых в настоящее время при лечении идиопатического бесплодия не доказан.
• Антиэстроген кломифена цитрат — препарат с антиэстрогенными свойствами, Кломифен блокирует обратную отрицательную связь эстрадиола в системе «гипоталамус— гипофиз», следствием чего является увеличение уровня ФСГ ЛГ и, соответственно, тестостерона. По данным неконтролируемых исследований, показатели спермограммы улучшаются у половины больных с идиопатическим бесплодием. Беременность у партнерш больных наступает в 30% случаев.
• Тамоксифен — препарате несколько меньшим эсгрогеноблокирующим эффектом, чем кломифен. Он препятствует секреции гонадоли-берина гипоталамусом по принципу обратной связи и таким образом повышает уровень ЛГ и ФСГ. Эффективность сопоставима с эффективностью кломифена. Рандомизированных плацебо-контролируемых исследований не проводили.
• Ингибиторы ароматазы (тестолактон — в России не зарегистрирован, анастрозол) подавляют активность ароматазы, трансформирующей тестостерон в эстрадиол. В неконтролируемом исследовании была показана некоторая эффективность этих препаратов (Clark et al., 1989).
• Пентоксифиллин — препарат из группы метилксантинов. Предполагалось, что его сосудорасширяющий эффект способен улучшить кровоснабжение яичка и косвенно сперматогенез. Но доказательств этой гипотезы пока не получено (Wang et aL 1983), В последнее время появляются данные о повышении эффективности экстракорпорального оплодотворения (ЭКО) при обработке сперматозоидов пентоксифиллином.
• а1-Адреноблокаторы улучшают микроциркуляции в яичке. Для теразозина показан эффект повышения объема эякулята и концентрации сперматозоидов, возможно за счет влияния на симпатическую систему в результате чего улучшаются условия транспорта и хранения сперматозоидов, но доказательная база работы довольно низка.
• Калликреины усиливают кровоснабжение яичка и стимулируют синтез простагландинов. В экспериментах улучшалась подвижность сперматозоидов, но на общее их содержание калликреины влияния не оказывали
• L-карнитин и аргинин. L-карнитин имеет большое значение для подвижности сперматозоидов. Эффективность этого препарата (в России выпускается 20% раствор «Элькар») исследуется в многоцентровых рандомизированных испытаниях.
Общие принципы терапии идиопатического бесплодия:
• Фармакотерапия идиолатической патоспермии у мужчин не дает обнадеживающих результатов.
• На сегодняшний день нет ни одного препарата с доказанным с точки зрения доказательной медицины влиянием на подвижность сперматозоидов, поэтому не существует патогенетического лечения астенозооспермии.
• Любой вид лечения мужского бесплодия должен считаться экспериментальным до тех пор, пока его эффективность не будет доказан контролируемыми клиническими исследованиями.
• Так как бесплодие не является опасным для жизни заболеванием нужно выбирать такие методы эмпирической терапии, которые не дают токсических и других тяжелых побочных эффектов.
• При консультировании пациентов перед проведением эмпирической терапии бесплодия необходимо давать реалистичные прогнозы в отношении потенциального успеха. Вряд ли эмпирическая терапия даст шанс мужчине с тяжелой олигозооспермией или азооспермией иметь детей путем естественного зачатия.
• Необходимо четко определить временные границы и пределы эмпирической терапии бесплодия, чтобы избежать «старения пары» и ненужной задержки лечения с помощью ВРТ.
• На фоне успешного применения и доступности методов ВРТ в Европе и США (но не в России!) фармакотерапия идиопатического мужского бесплодия уже не имеет большого значения. Особенно успешным при астеноопигозооспермии и даже азооспермии оказывается метод ИКСИ.
• Любое лечение мужского бесплодия должно сопровождаться оптимизацией женских половых функций.
• Цель получения беременности не может оправдать поспешного применения непроверенных средств для эмпирической терапии.
• Биологически активные добавки не должны применяться как самостоятельные средства лечения нарушения фертильности у мужчин.
Искусственное оплодотворение спермой донора или мужа (инсеминация). Этот метод предполагает введение отмытой спермы непосредственно в полость матки. Главное показание — иммунологический конфликт сперматозоидов с антителами цервикальной слизи. Кроме того, этот метод применяется при неудовлетворительных показателях спермограммы, при пороках развития мужской половой системы (например, гипоспадия), когда нарушен транспорт сперматозоидов.
Инсеминация может быть эффективным методом при содержании в образце спермы не менее 5 млн подвижных сперматозоидов. Эффективность этой методики зависит от состояния репродуктивной системы женщины. Частота беременностей после одного цикла лечения составляет 8-16%. При применении этой процедуры 3-4 раза частота наступления беременностей у супружеской пары достигает 30-35%. Оптимальные сроки искусственного осеменения определяют гинекологи на основании данных УЗИ о созревании яйцеклетки и по уровню ЛГ сыворотки крови.
Трансцереикальный перенос гамет (GIFT — gamete intrafallopian transfer) и зигот (ZIFT — zygote Intrafallopian transfer) в маточные трубы при их проходимости проводится в надежде, что беременность наступит у большего числа женщин, так как выбирается физиологическая зона имплантации. Считают, что этот метод не имеет каких-либо преимуществ перед ЭКО при мужском бесплодии. поскольку свойства имплантируемых сперматозоидов в процессе процедуры не улучшаются. Программа суррогатного материнства.
Экстракорпоральное оплодотворение впервые предложили в 1978 п для лечения обструктивных форм женского бесплодия. Теперь этот метод широко применяется и при мужском бесплодии. ЭКО — технически достаточно сложная процедура и включает в себя индукцию овуляции и забор яйцеклеток из яичников под контролем УЗИ с оплодотворением их 0.5-5 млн сперматозоидов в чашке Петри и последующей подсадкой оплодотворенных яйцеклеток в полость матки.
Методика является методом выбора при тяжелой патозооспермии. При неудачной попытке ЭКО повторная процедура является успешной у 10-18% супружеских пар, В целом эффективность ЭКО составляет 40%. По последним данным, у детей, родившихся с применением метода ЭКО, риск хромосомных аномалий в 4 раза выше, чем у детей, зачатых естественным путем.
Микроманипуляцонные методики требуют для своего проведения единственного жизнеспособного сперматозоида. Наиболее распространена методика ICSL или ИКСИ, при которой в яйцеклетку вводят один жизнеспособный сперматозоид, взятый из придатка яичка путем аспирации (MESA — microsurgical epididymal sperm aspiration) или через кожу мошонки (PESE — percutaneous epididymal sperm extraction), из яичка тонкой иглой (TESA — testicular sperm aspiration) или путем хирургической биопсии (TESE — testicular sperm extraction), а также из семявыносящего протока.
Недостаток ИКСИ — устранение фактора естественного отбора, который действует при естественном оплодотворении, из-за чего генетические дефекты с высокой вероятностью могут бьпь переданы потомству. Это сопряжено с целым рядом этических проблем, особенно при лечении мужчин с синдромом Клайнфельтера. Этот синдром может проявиться у внуков мужчин, страдающих бесплодием, излечимым благодаря современным методам искусственного оплодотворения.
источник
Что такое мужское бесплодие? Причины возникновения, диагностику и методы лечения разберем в статье доктора Рыжков А. И., андролога со стажем в 12 лет.
Под бесплодием понимают отсутствие зачатия в паре, живущей регулярной половой жизнью без использования контрацепции на протяжении более одного года. [1] С бесплодием ежегодно сталкиваются примерно 15% пар, планирующих зачатие. [2]
Причиной бесплодия могут быть нарушения репродуктивной функции у одного из партнёров (мужчины или женщины) или у обоих партнёров. Последнее наблюдается наиболее часто, так как нарушенная фертильность (способность иметь детей) одного из партнёров может компенсироваться сохранной фертильностью другого. [1]
О мужском факторе, или мужском бесплодии, говорят при наличии у мужчины изменений параметров спермы или механизма её доставки, препятствующих зачатию. Такая ситуация наблюдается у половины мужчин, обследованных по поводу бесплодия в браке. Причины мужского бесплодия достаточно многообразны и включают в себя медицинские факторы:
- Варикоцеле — это варикозное расширение вен мошонки, нарушающее кровоснабжение яичка. Самая распространенная обратимая причина мужского бесплодия. Точная причина, по которой варикоцеле вызывает бесплодие, неизвестна, вероятно, это связано с повышением температуры мошонки, приводящим к нарушению сперматогенеза и снижению качества спермы. Лечение варикоцеле позволяет улучшить параметры спермы, повысить шансы на естественное зачатие и зачатие в результате применения вспомогательных репродуктивных методов (ЭКО/ИКСИ).
- Инфекции репродуктивной системы, которые сопровождаются попаданием в сперму различных продуктов воспаления, нарушающих функционирование сперматозоидов, что приводит к ухудшению параметров спермы. К ним относятся: воспаление придатка яичка (эпидидимит) или самого яичка (орхит), предстательной железы (простатит) и некоторые инфекции, передающиеся половым путём, включая хламидийную инфекцию, гонорею, трихомониаз.
- Нарушения эякуляции. Чаще всего к бесплодию приводит ретроградная эякуляция — состояние, когда сперма во время оргазма не выходит через мочеиспускательный канал наружу, а движется в противоположную сторону и попадает в мочевой пузырь. К ретроградной эякуляции может приводить сахарный диабет, травмы позвоночника, приём некоторых лекарственных препаратов, а также операции на предстательной железе или мочевом пузыре. Гораздо реже встречается задержка эякуляции, когда мужчина во время полового акта не может достичь оргазма или достигает, но не во всех половых актах, и ему на это требуется значительное количество времени (иногда более часа).
- Иммунные факторы. Сперматозоиды, в отличие от остальных клеток организма, содержат половинный набор хромосом, поэтому иммунная система воспринимает их как чужеродные клетки. При контакте со сперматозоидами иммунная система вырабатывает специальные белки — антитела, которые фиксируются к сперматозоидам и нарушают их функционирование. В норме этого не происходит, так как яички устроены особым образом, и сперматозоиды в процессе созревания ограждены от взаимодействия с клетками иммунной системы специальной структурой — гематотестикулярным барьером. Но любое нарушение структуры яичка (травма, варикоцеле, нарушение проходимости семявыносящих путей) может приводить к повреждению гематотестикулярного барьера и образованию антиспермальных антител.
- Неопущенне яичек (крипторхизм). У некоторых мужчин одно или оба яичка при рождении не опущены в мошонку, а находятся в паховой области или брюшной полости. Вне мошонки яички не могут полноценно функционировать, так как для сперматогенеза необходима температура ниже температуры тела. Это приводит к необратимому нарушению сперматогенеза, которое сохраняется даже после хирургического опущения яичек в мошонку. Вероятность бесплодия значительно выше у мужчин с двусторонним крипторхизмом, чем с односторонним.
- Гормональные расстройства. Заболевания щитовидной железы (гипер- и гипотиреоз), заболевания надпочечников, низкий уровень тестостерона (мужской гипогонадизм) негативно влияют на сперматогенез. Самые тяжёлые нарушения сперматогенеза наблюдаются при дефиците основного гормона, стимулирующего сперматогенез — ФСГ (фолликулостимулирующий гормон), но такие состояния наблюдаются редко.
- Опухоли. Доброкачественные и злокачественные опухоли самого яичка и структур, регулирующих сперматогенез, например, гипофиза или гипоталамуса, часто сопровождаются тяжелыми нарушениями выработки сперматозоидов. Негативным образом на качестве спермы сказываются и методы, применяемые для лечения опухолей: химиотерапия, лучевая терапия, хирургическое вмешательство.
- Непроходимость семявыносящих путей. Семявыносящие пути, по которым движутся сперматозоиды, могут быть заблокированы на разном уровне: внутри яичка, в придатке яичка, семявыносящем протоке, на уровне предстательной железы или в уретре. Причины включают в себя повреждение во время операции (например, по поводу паховой грыжи), перенесённые инфекции, травмы или неправильное развитие в результате наследственных заболеваний.
- Хромосомные дефекты. Врожденные заболевания, например, синдром Клайнфелтера, при котором мужчины рождаются с двумя Х-хромосомами и одной Y-хромосомой (вместо одной Х и одной Y), приводят к неправильному развитию мужских репродуктивных органов. Другие генетические синдромы, связанные с бесплодием, включают муковисцидоз, синдром Кальмана и синдром Картагенера.
- Сексуальные проблемы. Они могут включать в себя проблемы с сохранением или поддержанием эрекции, достаточной для проведения полового акта (эректильная дисфункция), преждевременной эякуляцией, болезненным половым актом, анатомическими аномалиями (расположение наружного отверстия мочеиспускательного канала на нижней поверхности полового члена (гипоспадия), или психологические проблемы и проблемы межличностных отношений, препятствующие полноценной регулярной половой жизни.
- Приём лекарственных препаратов. Заместительная терапия тестостероном, длительное использование анаболических стероидов, лекарственные препараты для лечения рака (химиотерапия), противогрибковые препараты, препараты, используемые для лечения язвенной болезни, и некоторые другие лекарства могут снижать качество спермы.
- Перенесённые операции. Некоторые операции могут препятствовать попаданию сперматозоидов в эякулят. Это вазэктомия (пересечение семявыносящих протоков с целью контрацепции), операции по поводу паховой грыжи, операции на мошонке или яичках, операции на простате и большие операции на брюшной полости, проводимые при раке яичка и прямой кишки.
Причиной мужского бесплодия могут стать факторы внешней среды, такие как:
- Промышленные химикаты. Длительное воздействие бензола, толуола, ксилола, пестицидов, гербицидов, органических растворителей, малярных материалов и свинца негативно сказывается на качестве и количестве спермы.
- Тяжёлые металлы. Воздействие свинца или других тяжёлых металлов также может угнетать сперматогенез.
- Радиация или рентгеновское излучение. Воздействие радиации может значительно снизить количество сперматозоидов в сперме. Как правило, эффект обратимый, и через некоторое время параметры спермы восстанавливаются до нормальных значений. При высоких дозах облучения производство спермы может быть нарушено необратимо.
- Перегрев яичек. Повышение температуры мошонки негативно сказывается на сперматогенезе. Частое использование саун, бань может ухудшить качество спермы. Длительное пребывание в сидячем положении, тесное белье и одежда, работа с ноутбуком, лежащим на коленях, также может повысить температуру мошонки и негативно повлиять на производство спермы.
Образ жизни, вредные привычки и условия профессиональной деятельности также влияют на мужскую фертильность:
- Употребление наркотиков. Кокаин и марихуана обладают обратимым негативным эффектом на количественные и качественные параметры спермы.
- Чрезмерное употребление алкоголя. Злоупотребление алкоголем может снизить уровень тестостерона, вызвать эректильную дисфункцию и уменьшить производство спермы. Заболевания печени, вызванные чрезмерным употреблением алкоголя, также приводят к проблемам с фертильностью.
- Курение табака. У мужчин, которые курят, качество спермы существенно хуже, чем у некурящих мужчин. Пассивное курение тоже может влиять на мужскую фертильность.
- Эмоциональный стресс. Вырабатываемые во время стресса гормоны подавляют секрецию веществ, стимулирующих сперматогенез. Длительный и сильный стресс может приводить к существенным изменениям параметров спермы.
- Избыточный вес.Ожирение вносит дисбаланс в нормальный мужской гормональный статус, что приводит к снижению мужской фертильности.
- Профессиональная вредность. Мужчины некоторых профессий, например, водители или сварщики, имеют больший риск бесплодия по отношению к остальным мужчинам. [3]
У 30% мужчин с нарушением параметров спермы установить причину не удаётся, такую форму мужского бесплодия называют идиопатической (беспричинной).
Процесс создания сперматозоидов (сперматогенез) происходит в яичке. 90-95% объёма яичек представлено специальными трубочками — семенными канальцами, в которых происходит процесс создания сперматозоидов — сперматогенез. Процесс создания одного сперматозоида занимает около 70 дней.
Процесс создания сперматозоидов стимулируется фолликулостимулирующим гормоном (ФСГ), который вырабатывается в участке головного мозга — гипофизе. При отсутствии ФСГ сперматогенез не протекает, и сперматозоиды не образуются.
Сперматогенез — процесс достаточно деликатный. Множество факторов могут нарушать его нормальное течение (повышение температуры мошонки, приём лекарственных препаратов, рентгеновское излучение) и привести к созданию сперматозоидов с неправильной структурой (морфологией), слабой подвижностью и дефектным генетическим материалом, не способных к оплодотворению.
После выхода из яичка сперматозоиды попадают в длинную извилистую трубку, которая называется придаток яичка. В результате прохождения придатка яичка, которое занимает около недели, сперматозоиды улучшают свою подвижность, а также происходит изменение молекул на поверхности сперматозоида, необходимое для взаимодействия с яйцеклеткой.
На фоне воспалительных процессов в придатке яичка процесс созревания сперматозоидов может нарушаться, и они не смогут оплодотворить яйцеклетку. В отдельных случаях, в результате воспалительного процесса или после операций на придатке формируется препятствие прохождению сперматозоидов, в результате чего они не попадают в сперму.
После прохождения придатка яичка сперматозоиды могут храниться в теле мужчины на протяжении нескольких недель, сохраняя способность к оплодотворению. Но если сперма хранится слишком долго, сперматозоиды начинают деградировать и погибать.
Разрушающаяся сперма может повредить новые сперматозоиды, не давая им возможности покинуть придаток яичка. Мужчинам рекомендуется эякулировать каждые два или три дня, чтобы поддерживать качество спермы в оптимальном состоянии.
Во время эякуляции около 250 миллионов сперматозоидов начинают движение через семявыносящий проток и мочеиспускательный канал (уретру) наружу. Движение сперматозоидов обеспечивается сокращением мышц семявыносящего протока и уретры, которые сопровождаются приятными оргастическими ощущениями. Как правило, выброс спермы происходит в несколько порций. Большинство сперматозоидов содержатся в первой порции, во второй и третьей содержится преимущественно секрет дополнительных мужских половых желез — предстательной железы и семенных пузырьков.
Секрет добавочных половых желез (простаты и семенных пузырьков) необходим для обеспечения жизнедеятельности сперматозоидов после эякуляции. При воспалительном или ином патологическом процессе в простате или семенных пузырьках состав их секрета может изменяться, что нарушает функционирование сперматозоидов и снижает вероятность зачатия.
После попадания во влагалище сперматозоиды должны в течение нескольких минут его покинуть и переместиться в шейку матки. Дело в том, что среда влагалища является кислой, что необходимо для защиты женского организма от попадания бактерий и вирусов. Однако кислая среда быстро разрушает сперматозоиды, если сперматозоид находится в ней больше двух минут, он погибает. По статистике, лишь одному из 100 сперматозоидов удается покинуть влагалище и переместиться в шейку матки.
В связи с этим очень важно, чтобы сперматозоиды во время эякуляции попадали максимально близко к шейке матки, что невозможно при таких аномалиях, как гипоспадия (наружное отверстие уретры находится на нижней поверхности полового члена).
Шейка матки содержит специальную слизь, которая, с одной стороны, защищает сперматозоиды от агрессивной среды влагалища, с другой — может препятствовать их дальнейшему движению. Консистенция слизи зависит от гормонального статуса женщины, и большую часть времени она не проницаема даже для самых здоровых и подвижных сперматозоидов. За несколько дней до овуляции консистенция слизи меняется таким образом, что она становится способной пропустить сперматозоиды.
В отдельных случаях в слизи шейки матки могут содержаться антитела (белки, вырабатываемые иммунной системой для борьбы с чужеродными субстанциями, попавшими в организм) к сперматозоидам, которые не позволяют сперматозоидам пройти цервикальную слизь даже во время овуляции.
После прохождения шейки матки сперматозоид попадает в матку, и перед ним возникает дилемма — в какую маточную трубу двигаться дальше: правую или левую. Женщины имеют две маточные трубы (по одной с каждой стороны), но только в одну из них каждый месяц из яичника выходит яйцеклетка. В этой ситуации организм женщины приходит на помощь сперматозоиду. В период, близкий к овуляции, за счет гормональных воздействий мышцы матки на стороне овуляции начинают ритмично сокращаться, указывая сперматозоиду на правильное отверстие маточной трубы.
Следующий для сперматозоида этап — прохождение отверстия маточной трубы. Оно очень маленькое, диаметром лишь несколько головок сперматозоида, поэтому сперматозоиды, которые движутся хаотично, не смогут в него войти. Этот этап преодолевают только сперматозоиды с быстрым и прямолинейным движением.
Попав в маточную трубу, сперматозоиды оказываются в достаточно благоприятной среде, прикрепляются к стенкам трубы и ждут выхода яйцеклетки. В таком состоянии они могут находиться достаточно долго — около 48 часов.
Выход яйцелетки из яичника сопровождается повышением температуры в маточной трубе на 1-2 градуса, что служит сигналом для гиперактивации сперматозоидов. Они начинают интенсивные движения хвостом, открепляются от стенки и быстро движутся навстречу яйцеклетке. На этом этапе остаётся 6-8 сперматозоидов, и у них есть несколько часов, чтобы оплодотворить яйцеклетку, так как срок её жизни очень короток.
По сравнению со сперматозоидом, яйцеклетка — довольно большая клетка, самая крупная в человеческом теле. После выхода из яичника она окружена облаком клеток, называемых фолликулярными, через которые сперматозоиды должны проникнуть прежде, чем вступить в контакт с поверхностью яйцеклетки. Чтобы пройти через фолликулярные клетки, сперматозоиды должны использовать интенсивный стиль движения (гиперактивация), который они использовали, чтобы отделиться от стенок маточной трубы.
После прохождения фолликулярных клеток до яйцеклетки добирается 1–2 сперматозоида, которым необходимо попасть внутрь. Для этого у сперматозоида есть мешочек ферментов на самом верху головки, который лопается, как только сперматозоид вступает в контакт с внешней поверхностью яйцеклетки. Эти ферменты помогают растворить внешнюю мембрану яйцеклетки и в сочетании с мощными движениями хвоста помогают сперматозоиду проникнуть внутрь яйцеклетки. Как только сперматозоид попадает внутрь, мембрана яйцеклетки меняет свои химические свойства и становится полностью непроницаемой для остальных сперматозоидов. После слияния сперматозоида с яйцеклеткой образуется эмбрион, и начинается развитие беременности.
Если сперматозоид функционально незрелый и не содержит на своей поверхности необходимые сигнальные молекулы, он не сможет вступить в контакт с яйцеклеткой, и оплодотворение не произойдёт. Существует редкая аномалия — глобулозооспермия, когда сперматозоиды имеют не коническую, а круглую головку. Причиной этого является отсутствие мешочка с ферментами (акросомы), что также исключает проникновение сперматозоида внутрь яйцеклетки.
- Первичное — женщине/женщинам ни разу не удавалось забеременеть от данного мужчины.
- Вторичное — ранее были беременности, но на настоящий момент после года регулярной половой жизни без контрацепции зачатие не происходит.
Диагностика мужского бесплодия включает в себя следующие обязательные методы:
- Осмотр и с сбор анамнеза (истории заболевания). Врач проводит осмотр и пальпацию (прощупывание) органов репродуктивной системы, что позволяет диагностировать такие состояния, как варикоцеле, крипторхизм, аномалии развития мужских половых органов. С помощью опроса выявляют наличие у пациента наследственных состояний, хронических заболеваний, перенесённых травм и операций, особенности сексуальной жизни, которые могут повлиять на вероятность зачатия.
- Анализ спермы (спермограмма). Сперму для исследования мужчина сдаёт посредством мастурбации. Исследование требует от мужчины определенных ограничений — исключить тяжёлые физические нагрузки, употребление алкоголя, а также половое воздержание на протяжении 3-4 дней до исследования.
После сдачи образца сперма исследуется в лаборатории, оценивается общее количество сперматозоидов, количество сперматозоидов с неправильной формой (морфологией), а также скорость и характер движения сперматозоидов. Анализ спермы достаточно сложен, выполняется вручную и зависит от квалификации выполняющего его специалиста. Рекомендуется выполнять анализ спермы в специализированных лабораториях, расположенных при центрах лечения бесплодия.
Если анализ спермы не выявляет отклонений от нормы, то перед дальнейшим углубленным обследованием мужчины следует провести тщательное обследование женщины для исключения у неё факторов, препятствующих наступлению беременности.
При выявлении отклонений от нормы дальнейший план обследования составляется индивидуально в зависимости от результатов предыдущих исследований и может включать в себя следующие методы:
- Ультразвуковое исследование мошонки. Этот тест позволяет выявить варикоцеле, изменения структуры придатка и яичка, указывающие на наличие воспалительного процесса или нарушение проходимости семявыносящих путей.
- Допплерография сосудов мошонки — метод оценки кровотока по сосудам яичка, наиболее точный метод диагностики варикоцеле.
- Трансректальное ультразвуковое исследование — позволяет оценить структуру предстательной железы, что важно при диагностике инфекций добавочных мужских желез и обструкции семявыносящих путей.
- Мазки из уретры на урогенитальную инфекцию. Некоторые урогенитальные инфекции, например, хламидии, могут протекать скрыто, но при этом оказывать негативное влияние на параметры спермы.
- Бактериологическое исследование спермы. Исследование позволяет выявить наличие в сперме бактериальной инфекции. Обязательный метод исследования при подозрении на инфекцию добавочных мужских половых желез.
- Определение уровня гормонов крови. Используется при низком количестве сперматозоидов. Оценивают гормоны, влияющие на сперматогенез: фолликулостимулирующий гормон, лютеинизирующий гормон, тестостерон, эстрадиол. По особым показаниям определяют гормоны щитовидной железы и надпочечников.
- Генетические тесты. Обязательное исследование при отсутствии сперматозоидов в сперме или их крайне низкой концентрации. Исследование может включать анализ на делеции в Y-хромосоме (отсутствие определённых участков в Y-хромосоме), оценку кариотипа (количества хромосом), оценку мутаций в гене, ответственном за муковисцидоз (CFTR).
- Биохимическое исследование спермы. Позволяет оценить концентрацию в сперме веществ, секретируемых той или иной железой. Для придатка яичка это альфа-гликозидаза, для семенных пузырьков — фруктоза, для простаты — цинк и лимонная кислота. Отсутствие одного или нескольких этих веществ позволяет подтвердить диагноз обструкции семявыносящих путей и заподозрить её уровень.
- Биопсия яичек. Используется для оценки сохранности сперматогенеза в яичке при отсутствии сперматозоидов в сперме. В случае получения сперматозоидов в результате биопсии они должны быть подвергнуты криоконсервации, чтобы избежать повторных операций. Методики биопсии рассмотрены ниже.
- Оценка ДНК-фрагментации сперматозоидов. Метод позволяет оценить количество сперматозоидов, содержащих повреждённый генетический материал (ДНК с разрывами). Использование данного метода показано при потере беременности (выкидыш, замершая беременность) на ранних сроках, а также при отсутствии зачатия на фоне нормальных показателей спермограммы.
- HBA-тест. Тест позволяет оценить функциональную зрелость сперматозоидов по возможности связываться с гиалуроновой кислотой. Гиалуроновая кислота имитирует поверхность яйцеклетки, если сперматозоид не связывается с гиалуроновой кислотой, то он не сможет взаимодействовать с яйцеклеткой.
Тактика лечения мужского бесплодия зависит от причины, его вызвавшей.
Хирургическое лечение
- Варикоцеле — устранение этой причины мужского бесплодия возможно только посредством оперативного лечения. Наилучшие результаты в отношении частоты наступления беременности и уровня послеоперационных осложнений показывает микрохирургическая субингвинальная варикоцелэктомия. [4]
- Обструкция семявыносящих путей — в ряде случаев нарушенную проходимость семявыносящих путей можно восстановить хирургическим путем. Наилучшие результаты имеют операции: вазо-вазоаностомоз (соединяют между собой концы пересечённого семявыносящего протока).
При обструкции на уровне придатка яичка используют вазоэпидидимоанастомоз (соединение семявыносящего протока с протоком придатка яичка). Эффективность данного подхода составляет 60-87% и во многом зависит от опыта хирурга и времени, прошедшего с момента формирования обструкции. [5]
- Биопсия яичка — хирургическое извлечение сперматозоидов из яичка и придатка. Данный подход преимущественно используется при обструктивной и необструктивной азооспермии для получения сперматозоидов с целью их последующего использования в процедуре ЭКО/ИКСИ. Применяют следующие методы биопсии яичка:
Тонкоигольная биопсия яичка (TESA)
Через кожу в ткань яичка проводят тонкую иглу и выполняют аспирацию (всасывание) тестикулярной ткани, из которой в последующем извлекают сперматозоиды. Преимущество данной методики — в малой травматичности для пациента. Недостаток — низкая вероятность обнаружения сперматозоидов при необструктивной азооспермии (20-30%), что делает данную методику оправданной только при доказанной обструктивной азооспермии, когда вероятность наличия сперматозоидов приближается к 100%. [6]
Тонкоигольная биопсия яичка
Открытая биопсия яичка (TESE)
Производится небольшой разрез кожи мошонки — 1,5-2 см, выделяется яичко, рассекается его оболочка на небольшом протяжении. Из полученного отверстия забирается небольшой фрагмент ткани, разрезы зашивают, а полученный материал исследуют на наличие сперматозоидов. Средняя вероятность обнаружения сперматозоидов при необструктивной азооспермии для TESE составляет 40-50%. [6]
Микрохирургическая биопсия яичек (microTESE)
Методика отличается от TESE использованием операционного микроскопа с 15-20-кратным увеличением, что требует большего разреза на яичке, но позволят детально исследовать его ткань для обнаружения и извлечения расширенных семенных канальцев, которые наиболее вероятно содержат сперматозоиды. Представленный подход значительно повышает шансы на обнаружение сперматозоидов по сравнению с методиками случайной биопсии (TESA, TESE). Средняя вероятность получения сперматозоидов при необcтруктивной азооспермии для microTESE составляет 60-70%. [4]
Лекарственная терапия имеет несколько направлений:
- Антибактериальные препараты применяются у пациентов с инфекцией добавочных мужских половых желез.
- Препараты для коррекции сексуальной дисфункции используются при наличии у пациента эректильный дисфункции или преждевременной эякуляции.
- Гормональная терапия применяется, если причиной бесплодия являются нарушения уровня половых гормонов: низкий уровень ФСГ, тестостерона или высокий уровень пролактина.
- Антиоксидантная терапия используется в том числе при идиопатическом мужском бесплодии, так как оксидативый — наиболее частый фактор, приводящий к нарушению качества спермы.
Коррекция образа жизни — основной подход в коррекции идиопатического мужского бесплодия и важное дополнение в лечении установленной причины нарушения фертильности. Пациент получает индивидуальные рекомендации, исходя из особенностей его жизни:
- нормализация режима труда и отдыха (8 часов сна), избегать стрессовых ситуаций;
- увеличить количество в рационе продуктов, содержащих полиненасыщенные жирные кислоты (морская рыба, морепродукты);
- минимизировать потребление жареной пищи;
- потребление кофеина не более 100 мг/сутки (1 чашка кофе); [7]
- исключить потребление колы;
- минимизировать потребление алкоголя, [8] не более 5 единиц (1 единица — 10 грамм чистого спирта) в неделю;
- исключить курение/снизить количество сигарет, потребляемых в сутки; [9]
- повысить физическую активность (пробежки, умеренные физические нагрузки);
- исключить факторы, нагревающие мошонку (горячие ванны, сауны, бани, работа с ноутбуком, лежащим на коленях, не носить облегающее нижнее белье);
- регулярная половая жизнь — через 1-2 дня (3 раза в неделю), не использовать лубриканты (смазки), содержащие спермициды.
Вспомогательные репродуктивные технологии (ВРТ)
Применение данных методик показано, если наступление беременности без применения ВРТ невозможно (азооспермия, нарушения эякуляции), или бесплодие не поддаётся лечению на протяжении 12 месяцев с момента установления диагноза. Вспомогательные репродуктивные методы включают в себя следующие методики:
- Искусственная инсеминация спермой мужа (ИИСМ) — применяется при нарушении эякуляции (задержка эякуляции), нарушении проникновения сперматозоидов через цервикальную слизь и как первый этап вспомогательных репродуктивных технологий, предшествующий проведению ЭКО. Во время данной процедуры сперму мужа посредством катетера вводят непосредственно в матку женщины в период овуляции.
- Экстракорпоральное оплодотворение (ЭКО) — процедура, во время которой взаимодействие яйцеклетки и сперматозоида осуществляется не в организме женщины, а в специальном сосуде. При этом, если для мужчины это требует лишь сдачи спермы, процедура подготовки женщины к ЭКО значительно сложнее — проводится гормональная стимуляция, в результате которой в яичнике созревают несколько фолликулов, содержащих яйцеклетки. Для получения яйцеклеток фолликулы пунктируют иглой под ультразвуковым наведением. Взаимодействие сперматозоидов и яйцеклеток может привести к образованию эмбрионов. Эмбрионы некоторое время выдерживают в специальных условиях, отбирают 1-2 лучших и переносят в матку женщины. Оставшиеся эмбрионы можно подвергнуть криоконсервации и повторно перенести в матку при безуспешности первой процедуры. Беременность в результате одной процедуры ЭКО развивается примерно у 30% женщин. [10]
- Интрацитоплазматическая инъекция сперматозоидов (ИКСИ) — во время данной процедуры отбирают один сперматозоид и посредством иглы переносят его внутрь яйцеклетки. В остальном процедура аналогична ЭКО. Основные показания к использованию данного метода — низкое качество спермы (малое количество, низкая подвижность и большое количество сперматозоидов с ненормальной морфологией. Эффективность ИКСИ выше ЭКО — частота развития беременности 45%, но безопасность этого метода для потомства вызывает вопросы и окончательно не определена. [10]
Прогноз в отношении мужского бесплодия преимущественно благоприятный. Использование современных методов лечения, в том числе вспомогательных репродуктивных технологий, в большинстве случаев позволяет преодолеть мужской фактор и добиться наступления беременности. Неблагоприятный прогноз для мужчины в отношении возможности иметь детей, как правило, связан с полным отсутствием сперматозоидов не только в эякуляте, но и в яичке (по результатам биопсии или при наличии генетических факторов, исключающих сохранность сперматогенеза).
Далеко не все формы мужского бесплодия можно предотвратить посредством профилактики. Но соблюдение этих простых рекомендаций позволяет значительно снизить вероятность возникновения данного состояния:
- не курить, не употреблять наркотики;
- употреблять алкоголь в умеренных количествах, не систематически;
- активный, подвижный образ жизни (умеренные физические нагрузки)/поддержание нормальной массы тела; избегать факторов способствующих нагреву яичек (тесное белье, ноутбук на коленях);
- избегать сильных и продолжительных стрессов;
- минимизировать/исключить контакт с вредными веществами: пестициды, тяжёлые металлы и другие токсины.
источник








