

Невроз* — термин, который до сих пор не получил точного определения у специалистов. Так именуется некая группа состояний, возникающих вследствие длительного психоэмоционального напряжения.
Причины возникновения неврозов у пожилых людей.
С годами каждый человек в копилку своей жизни складывает не только позитивный опыт и мудрость. Порой туда попадают обиды, недовольство жизнью, чувство вины и одиночества, потеря близких и работы.
Все это бремя отягощается физической истощенностью и усталостью организма. Нередко причиной невроза становить гормональные нарушения и утрата динамики. Качество жизни снижается, а привычный образ жизни остается в прошлом…
Каждая из причин может являться причиной психического или нервного расстройства. Пожилому человеку тяжелее смотреть на жизнь с оптимизмом, присущим молодости. Он все чаще вздыхает о днях юности и тянется к общению с молодежью и детьми.

Основным симптомом является повышенная раздражительность, возбужденность, иногда переходящая в агрессию или напротив к замкнутости и апатии. Человек отстраняется от общения с другими людьми и даже с близкими. У него постоянные перепады настроения. Его мучает чувство тревоги, он видит опасность во всех проявлениях жизни. И самое главное, он теряет интерес к жизни и часто говорит о смерти.
На физиологическом уровне невроз выражается:
- в потере аппетита,
- нарушениях сна,
- чувствительности к климатическим изменениям,
- нарушениями краткосрочной памяти,
- он хуже видит и слышит…
Ароматерапия при неврологически заболеваниях.

Альцгеймера* – это нейродегенеративное заболевание, которое может развиваться десятками лет и характеризуется потерей памяти, изменениями в поведении, отказом двигательных функций.
Главную роль в процессах запоминания играет ацетилхолин, (вещество — нейрогормон, передающее информацию нервным окончаниям). С возрастом в мозге человека его становиться меньше. так возникает болезнь Альцгеймера. Болезнь в начале проявляется вялостью, беспричинной усталостью, склонностью к депрессии, раздражительностью. Основной проблемой является то, что в результате человек плохо запоминает информацию, его внимание постоянно рассеяно, он не узнает близких и трудно подбирает слова.
По мимо рекомендаций врачей специальных лекарственных препаратов, приема витаминов и правильного питания, нужно отметить пользу от эфирных масел.
Известно, что запахи обрабатываются в той же области мозга, которая отвечает и за память. Известный нейрофизиолог академик Наталья Петровна Бехтерева, советует при нарушении памяти и замедлении ассоциативных процессов в мозгу, наряду с основным лечением, непременно использовать Ароматерапию. Эфирные масла, по ее мнению, это эффективное и благотворное воздействие на сложные механизмы памяти.
…Оптимизируют мозговое кровообращение, улучшают память, концентрацию внимания и успокаивают длительные ингаляции и ванны с эфирными маслами, содержащими цинеол: эвкалипта и каяпута (в них цинеол находится в наибольших количествах — от 60 до 80%), найоли (50 — 65%), розмарина (30 — 45( о), лаванды, мяты перечной, ели. (Цинеол также содержится в эфирных маслах лавра, полыни цитварной, у шалфея лекарственного). Считают, что такой эффект этих ароматов может быть связан с тем, что монотерпен цинеол тормозит, предотвращает распад такого важного нейромедиатора как ацетил холин, участвующего в формировании памяти и процессах обучения; наибольшая его концентрация определяется в подкорковом образовании головного мозга гиппокампе, отвечающем именно за долговременную память…
Растительные нейростимуляторы, регуляторы нервной деятельности, помогающие при Болезни Альцгеймера: эвкалипт и каяпут (особенно), найоли, розмарин, лаванда, мята перечная и японская, ель.
К сведению, по мимо упомянут выше, можно добавить дополнительно список эфирных масел содержащих цинеол в разных количествах.
Это: базилик, масло бей, камфора, кардамон, имбирь, корица из коры, ладан, мирт, мускатный шалфей, пихта сибирская, полынь таврическая, розовое дерево, тысячелистник, чайное дерево.
Эти эфирные масла помогут оптимизировать мозговой поток и отодвинуть назад болезнь.
Применение заключается в следующем.
Один раз в день ставить аромалампу в комнате больного с ароматом эфирных масел. Масло может быть использовано -моно или в смеси с другими ароматами подробнее>>>
Для стимуляции процессов мозга, улучшения памяти помогают эфирные масла: розмарин и мята перечная (особенно), лаванда, кардамон, герань.
Лаванда — положительно влияет на гемодинамику головного мозга, уменьшает тоническое напряжение стенок сосудов и умеренно повышает их кровенаполнение. Это одно из самых эффективных и почитаемых масел в Геронтологии.
Герань — эйфорийный «лифтовый» аромат! Моментально улучшает настроение, активизирует умственный и физический потенциал, придает бодрости и сил, поселяет радость. Чем раньше вы начнете использовать эфирное масло герани в своей жизни, тем дольше продлиться ваш осознанный мир.
Способы применения:
- ингаляции (проводятся курсом в 10 дней, затем делается перерыв 5-7 дней и курс можно повторить)
- аромадиффузор- средство для распыления эфирного мала. Благодаря этому прибору масло зависает в воздухе на продолжительное время.
- аромалампа — 7-8 капель для помещения 12-15 кв.метров, подробнее>>>
Депрессия*- это психическое расстройство, характеризующееся снижением настроения, утратой способности радоваться, нарушениями мышления, отсутствием позитивного взгляда на жизнь, апатичностью, отсутствием динамики.
Рекомендации Ароматерапии:
Для пожилого престарелого человека можно использовать тонизирующие эфирные масла: нероли, базилик, майоран, роза болгарская и галльская, шалфей мускатный, ветиверия.
Способы применения:
- ингаляции (проводятся курсом в 10 дней, затем делается перерыв 5-7 дней и курс можно повторить)
- аромадиффузор- средство для распыления эфирного мала. Благодаря этому прибору масло зависает в воздухе на продолжительное время.
- аромалампа — 7-8 капель для помещения 12-15 кв.метров, подробнее>>>
- аромамассаж,
- аромаванны
В случаях, где депрессия сопровождается психическими отклонениями рекомендуется применять эфирное масло: лаванды, лимона, иланг-иланга, ладана.
Эти ароматы помогут затормозить нервную систему, окажут седативное влияние, снизят кровяное давление, успокоят нервное дыхание.
Для повышения концентрации внимания и повышения умственной деятельности рекомендуются эфирные масла: мята перечная, можжевельник (хвоя, ягоды), шалфей мускатный, ветивер, тимьян, ладан, иланг-иланг, гвоздика, пихта, ромашка римская, апельсин, мандарин, нероли, литсея кубеба, мирра, душица, сандал.
Сильные стимуляторы: базилик, розмарин, тимьян.
В момент стрессовой ситуации можно применить: масло ладана, сандала, кипариса, кедра атласского, амириса, мелиссы лимонной, иссопа, бергамота, мирры, можжевельника, герани.

Истерический невроз* — это реакция человека с ослабленной нервной системой на ситуацию, которую он не в состоянии перенести. Проявления истерии многообразны.
При возникновении истерии рекомендуется использовать эфирное масло ладана, лаванды, нероли, мирры, летсеи кубебы, душицы, майорана, пихты, сандала, ромашки римской.
Применение может быть одноразовым, а можно провести 10 дневный курс путем ингаляции или ароматизации комнаты больного. Эта мера позволит укрепить результат на более длительный срок.
♥ Навязчивые состояния.
Этот вид невроза возникает реактивно, без желания больного. Может выражаться в страхах, в чувстве вины, в комплексах неполноценности.
Причина возникновения — общая усталость, возраст, следы психической травмы в прошлом.
Рекомендуется использовать эфирное масло: ладана, мяты перечной и японской, нероли, мелиссы лимонной, иланг-иланга, лаванды, шалфея мускатного, пихты, полыни лимонной, мирры, мирта.

Это состояние чаще наблюдается у пожилых людей, обремененных гипертонической болезнью, атеросклерозом, функциональными заболеваниями центральной нервной системы с повышенной утомляемостью мозга, истощением его функций, стрессами, нарушением нормального соотношения между процессами возбуждения и торможения и т.п.
Рекомендуется использовать эфирное масло: лаванды, жасмина, мяты, эвкалипта, лимона, шалфея, кориандра.
Для стимуляции нервной системы: базилик, лимон, укроп из семени, можжевельник (ягоды, хвоя), мята, чеснок, розмарин, шалфей лекарственный, тимьян, чабрец.
Живите в сознании себя и окружающего вас мира!
источник
Использование эфирных масел (ЭО) и их компонентов давно известно в народной медицине и ароматерапии для лечения различных заболеваний, и в последнее время оно еще более возросло.
Эта обзорная статья была направлена на то, чтобы суммировать клинические исследования об эфирных маслах, протестированных против нейродегенеративных расстройств, таких как болезнь Альцгеймера (AD) и деменция. Влияние эфирных масел на патологические мишени Альцгеймера и деменции, включая амилоидное отложение (Аβ), нейрофибриллярные сплетения (НФТ), холинергическую гипофункцию, окислительный стресс и глутаматергические аномалии.
Кроме того, влияние эфирных масел на другие неврологические расстройства, включая тревогу, депрессию, когнитивную гипофункцию, эпилепсию и судороги, также было подробно исследовано и оценено.
В заключение, эфирные масла были эффективны в отношении нескольких патологических целей и улучшили когнитивные функции на животных моделях и людях. Таким образом, ЭО могут быть разработаны как мультипотентные агенты против неврологических расстройств с лучшей эффективностью, безопасностью и экономичностью.
Ключевые слова: эфирные масла, болезнь Альцгеймера, ингибиторы холинэстеразы, антиоксиданты, амилоид-β, NFT, деменция, BACE1, антивозрастные эфирные масла.
Эфирные масла (ЭО) представляют собой смесь очень сложных, встречающихся в природе летучих соединений, синтезируемых растениями в качестве вторичных метаболитов. ЭО могут содержать различные части растений: цветы, листья, семена, корневища, кора и, как правило, выделяются с помощью гидродистилляции, методов холодного прессования. Наиболее часто используемым лабораторным методом является паровая дистилляция, которая была разработана в средние века арабами.
В наши дни эфирные масела используются в традиционных лекарствах, альтернативных лекарствах, китайских лекарствах, ароматерапии, массажной терапии, а также в косметической, парфюмерной и пищевой промышленности. В Египте эфирные масела, извлеченные из ароматических растений, использовались для профилактики и лечения различных заболеваний. Вскоре после этого греки и римляне переняли египетскую практику использования эфирных масел в ароматерапии и для улучшения качества их жизни. Например, они использовали паровые бани, наполненные маслами жасмина, иланг-иланга и лаванды, для стимуляции центральной нервной системы (ЦНС) и психического расслабления (Ballard et al.; Keville and Green).
Естественно, эфирные масела играют жизненно важную роль в защите и размножении растений, выступая в качестве противомикробных средств, репеллента для травоядных животных и привлекательных агентов для насекомых, которые помогают в опылении. Благодаря своим природным свойствам эфирные масела широко используются в качестве антибактериальных, противогрибковых и инсектицидных средств.
Более глубокое понимание химии эфирных масел и способности проникновения через биологические мембраны сделали их важными инструментами лечения для терапии различных неврологических расстройств.
Почему эфиры так мощно работают?
Эфирные масла состоят из чрезвычайно сложных смесей соединений и содержат многочисленные компоненты в различных концентрациях (Рисунок 1). Основными компонентами эфирных масел являются ароматические соединения, терпены / терпеноиды и алифатические молекулы, особенно с низким молекулярным весом (Burt, 2007; Bakkali et al.; González-Burgos et al.).
Конкретные эфирные масла обычно имеют более высокие концентрации (20–95%) двух или трех компонентов, тогда как другие компоненты присутствуют в незначительных количествах.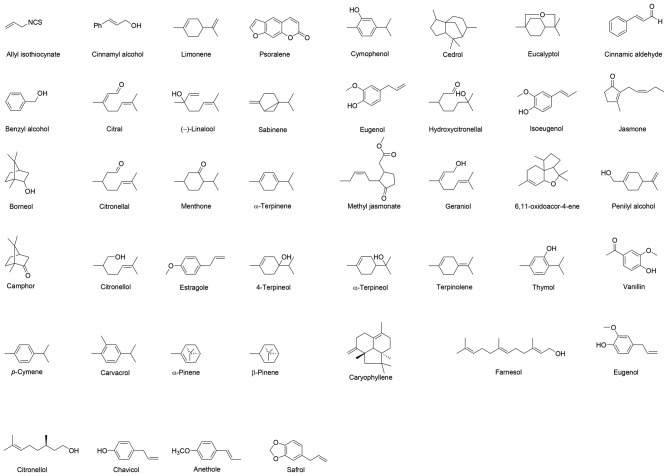
Например, линалол представляет 68% содержания EO Coriandrum sativum, тогда как альфа / бета-туион и камфора составляют 57% и 24% эфирного масла Artemisia Herba-alba.
Аналогично, составляющие со сравнительно более высокими концентрациями представляют собой D-лимонен (> 80%) в маслах кожуры цитрусовых, карвакрол и тимол (30 и 27%) в Origanum compactum.
Сходным образом, α-феландрен и лимонен (36 и 31%) в листьях эфирного масла Anethum graveolens, 1,8-цинеол (50%) в эфире Cinnamomum camphora, ментол и ментон (59 и 19%) в Mentha piperita являются основными компонентами.
Следовательно, для достижения эфирных масел с однородным химическим составом их необходимо извлекать из одной и той же части растения и собирать в одинаковых условиях выращивания (почва, вода, продукты питания, климат) и соблюдать наиболее эффективный сезон.
Большинство коммерциализированных эфирных масел химически охарактеризованы с помощью методов газовой хроматографии-масс-спектрометрии (ГХ-МС). Аналитические монографии, касающиеся качества эфирных масел, были опубликованы в Европейской фармакопее, ВОЗ, ИСО и Совете Европы (Smith et al).
Основные компоненты эфирного масла способствуют и определяют его биологические характеристики. Благодаря развитию современных аналитических методов, химический состав эфирного масла легко анализируется.
Потенциал ингибирования холинэстеразы.
Болезнь Альцгеймера (AD) является наиболее распространенным из нейродегенеративных нарушений, характеризующихся когнитивными дисфункциями, поведенческой турбулентностью, постепенной потерей памяти, дефицитом холинергической нейротрансмиссии, окислительным стрессом, накоплением амилоидных бляшек (амилоид-β, Aβ) и нейрофибриллярных клубков (NFT) в областях мозга (Nussbaum и Ellis).
Разработка основанных на механизме ингибиторов ферментов, вовлеченных в AD, является наиболее полезным вариантом в разработке лекарств против AD. В связи с этим ингибиторы ферментов ацетилхолинэстеразы (AChE) и бутирилхолинэстеразы (BChE), участвующих в деградации незаменимых нейротрансмиттеров ацетилхолина (ACh), представляют собой основные соединения, одобренные для клинического применения при симптоматическом лечении AD.
Среди одобренных в настоящее время препаратов против болезни Альцгеймера Ривастигмин, Такрин, Галантамин и Донепезил (4/5) являются ингибиторами AChE, тогда как 5-й мемантин является модификатором глутаматергической системы.
Эти ингибиторы холинэстеразы обратимо связываются с активными центрами ферментов AChE / BChE и таким образом ингибируют гидролитическую деградацию важного нейротрансмиттерного ACh, участвующего в нейротрансмиссии.
Следовательно, концентрация синаптического ACh увеличивается, что приводит к облегчению симптомов болезни Альцгеймера. Среди ингибиторов холинэстеразы Ривастигмин является периферическим ингибитором BChE и, следовательно, связан с периферическими холинергическими побочными эффектами (Birks and Grimley Evans).
Галантамин, другой холинэстераза на основе натурального продукта. Первоначально ингибитор был выделен из подснежника, принадлежащего к семейству Amaryllidaceae (Heinrich and Lee Teoh).
Сообщалось о нескольких исследованиях относительно потенциалов ингибирования холинэстеразы эфирными маслами. Недавно Ayaz et al сообщили об эффективности ингибирования ACh, BChE и свободных радикалов из эфирных масел на основе листьев и цветков Polygonum hydroropiper.
Они предоставили сравнительный анализ ГХ-МС и идентифицировали 141 и 122 соединения в маслах листьев и цветов соответственно. Оксид кариофилена (41,42%) был основным компонентом листового масла, тогда как декагидронафталин (38,29%) был основным компонентом цветочного масла. Эфирное масло листьев и цветов демонстрировали IC50 120 и 220 мкг / мл соответственно в анализах ингибирования AChE.
Принимая во внимание, что в анализах ингибирования BChE из эфирного масла листьев и цветов, то выявили IC50 130 и 225 мкг / мл соответственно. Те же самые эфирные масла продемонстрировали значительную антирадикальную активность с IC 50 20 и 200 мкг / мл соответственно в анализе поглощения свободных радикалов 1,1-дифенил-2-пикрилгидразила (DPPH).
Рассчитанные значения IC50 составляли 180 и 60 мкг / мл для листового масла и 45 и 50 мкг / мл для цветочного масла в анализах антирадикалов 2,2-азинобис-3-этилбензтиазолин-6-сульфоновой кислоты (ABTS) и H2O2 соответственно.
Авторы предположили, что, направленность более чем на один аспект заболевания предоставляет повышенную биодоступность, со временем они сделают эти эфиры более эффективными, чем доступные в настоящее время молекулы с одной мишенью для одного лекарства.
В другом исследовании Ahmad et al сообщили об антихолинэстеразных и антирадикальных потенциалах эфирных масел от Rumex hastatus D. Don.
ГХ-МС анализ эфирных масел выявил присутствие 123 соединений.
В анализе эфирных масел продемонстрировано зависимое от концентрации ингибирование AChE и BChE со значениями IC50 32,54 и 97,38 мкг / мл соответственно. Кроме того, в антиоксидантных анализах с использованием антирадикальных протоколов DPPH и ABTS эфирные масла показали высокую антиоксидантную эффективность со значениями IC50 3,71 и 6,29 мкг / мл соответственно (Ahmad).
Ученые сообщили об активности ингибирования AChE, BChE из цветочного масла Narcissus poeticus L., принадлежащего к семейству Amaryllidaceae.
Анализ ГХ-МС показал наличие трех основных соединений, включая бензилбензоат (19,0%), фенилэтиловый спирт (17,5%) и бензиловый спирт (11,0%), а также ряд минорных компонентов.
При концентрации 0,1 мг / мл наблюдалось ингибирование 39%. Исследовали потенциальную эффективность эфирного масла из Salvia leriifolia Benth., Семейства Lamiaceae, в лечении болезни Альцгеймера.
В GC-MS анализе камфора, цинеол, камфен и альфа-пинен были идентифицированы как основные компоненты с концентрациями 10,5, 8,6, 6,2 и 4,7% соответственно. Тестируемое эфирное масло проявляло высокие ингибирующие свойства BChE, антирадикалы DPPH и ингибировало выработку медиаторов воспаления.
Эфирное масло от Marlierea racemosa Vell. (Myrtaceae) было оценено против фермента AChE. Химический состав эфирного масла анализировали с помощью ГХ-МС, что свидетельствует о высокой концентрации спатуленола. Отмечено зависимое от концентрации (35–75%) и ингибирование AChE в зависимости от региона.
Пять эфирных масел: Cistus creticus, Cistus monspeliensis, Cistus salvifolius, Cistus villosus и Cistus libanotis из семейства Cistaceae были исследованы для антиоксидантных и холинэстеразных ингибиторных потенциалов.
Эфирные масла были охарактеризованы с помощью ГХ и ГХ-МС анализа. Результаты показали, что эфирное масло из C. monspeliensis продемонстрировало наиболее многообещающую активность в тесте на отбеливание β-каротина с IC50 54,7 мкг / мл.
В анализе FRAP C. libanotis был найден наиболее эффективным со значением 19,2 л MFe (II) / г. В анализах ингибирования холинэстеразы C. salvifolius проявлял ингибирующую активность в отношении AChE со значением IC50 58,1 мкг / мл. Принимая во внимание, что C. libanotis, C. creticus и C. salvifolius показали значительную ингибирующую активность в отношении BChE со значениями IC50 23,7, 29,1 и 34,2 мкг / мл соответственно.
Результаты исследования показали, что эфирные масла из видов Cistus могут развиваться как потенциальные нейропротекторы и агенты, модифицирующие болезнь Альцгеймера.
Познание — это сочетание двух жизненно важных компонентов: обучения и памяти. Обучение — это способность получать и обрабатывать новую информацию, тогда как под памятью подразумевается способность хранить эту информацию и использовать ее для будущих целей. При некоторых заболеваниях, таких как AD и деменция, когнитивные функции изменяются в зависимости от тяжести или стадии заболевания. Концепция познания и роль центральной холинергической передачи в приобретении когнитивных функций хорошо известна с начала шестидесятых годов. Несколько нейротрансмиттеров участвуют в приобретении обучения и памяти, но роль холинергической системы вызывает большее любопытство у неврологов (Hagan and Morris, 1988).
После первых в истории доказательств и сообщений о холинергическом участии в процессе познания Дойча появилось несколько новых областей неврологических исследований, включая поведенческую неврологию, старение, деменцию и поведенческую фармакологию. Следовательно, ухудшение холинергических нейронов, как было признано, связано с когнитивным дефицитом пациентов с AD. Кроме того, было признано, что антагонистический эффект неселективных антихолинергических агентов, таких как скополамин, усугубляет дефицит памяти, включая достижение, сохранение, консолидацию и восстановление памяти. Таким образом, повышение холинергического тонуса может потенциально регрессировать когнитивную гипофункцию. На основе этой стратегии было протестировано несколько препаратов, таких как предшественники АХ, никотиновые и мускариновые агонисты. Идея провалилась из-за ограниченных проблем эффективности, токсичности и биодоступности. Тем не менее, ингибиторы AChE и BChE оказались эффективными при лечении AD.
Сообщается, что препараты на основе натуральных продуктов, включая ЭО и чистые соединения, эффективны при многих заболеваниях. Сообщалось о нескольких исследованиях, касающихся психофизиологических особенностей запахов, хотя их когнитивные функции до сих пор не полностью выражены. Мы также обсудили несколько полезных аспектов ЭО при болезни Альцгеймера и деменции с использованием различных моделей памяти. В исследовании Shimizu et al. (2008, 2009) сообщили об эффекте ЭО от Eucalyptus globulus Labill. и Lavandula angustifolia Mill. на постоянное внимание в бдительности (условие быть внимательным в течение длительного периода времени).
В группах, обработанных лавандой ЭО, время реакции значительно сократилось по сравнению с контрольной группой. Результаты этого исследования показали, что субъекты, которых лечили лавандовым ЭО, поддерживали внимание во время длительных и неотложных упражнений. В хроническом исследовании та же группа сообщила, что седативные запахи, такие как лаванда, более полезны, чем стимуляция запахов в ситуациях тяжелых упражнений, в то время как чрезмерная настороженность может повредить бдительности. Кроме того, стимулирующие запахи были признаны более полезными в решении менее жестких задач, поскольку они держат субъектов в состоянии готовности.
Rosmarinus officinalis L. семейство Lamiaceae, является обычным домашним пряным растением и часто используется в диетических составах благодаря его сильным антирадикальным свойствам. Фармакологическое действие ЭО от R. officinalis, в том числе антибактериального, противогрибкового, противоопухолевого, антиоксидантного и гипогликемического, научно подтверждено в нескольких исследованиях (Faixova and Faix, 2008). Кроме того, розмарин ЭО, как сообщается, стимулирует нервную систему и, таким образом, улучшает память и способность к концентрации.
В исследовании наблюдалось улучшение производительности в задаче из-за обонятельного воздействия розмарина ЭО с увеличением общего качества памяти. Сообщалось, что комбинация ЭО из R. officinalis и M. piperita увеличивает память и уровень активности мышей и собак. Розмарин EO также обладает умеренной ингибирующей активностью по AChE и может синергически действовать с 2-пиненом и 1,8-цинеолом. Он также повышает двигательную активность, стимулирует энергию, стимулирует кору головного мозга, вызывает расслабление настроения и повышает бдительность (Hongratanaworakit, 2009). Все эти биологические свойства указывают на его потенциальное использование в лечении нейродегенеративных заболеваний, в том числе БА, старческого слабоумия, миастении.
Хорошо известно, что зрительный стимул может влиять на обонятельное восприятие, но об обратном случае известно меньше. В связи с этим Seo et al. (2010) исследовали влияние аромата на визуальную производительность и внимание. В проекте исследования, 60 здоровых добровольцев были представлены четырем ароматам, включая апельсин, кофе, лаванду и лакрицу, до и во время фотографического слайд-шоу, содержащего одну гармоничную и три разнородных картинки.
Система слежения за глазами использовалась для оценки уровня зрительного внимания с точки зрения количества и времени фиксации глаз после воздействия аромата. Хорошо известно, что пробанды чаще и дольше смотрят на объект, когда они чувствуют запах, по сравнению с ситуацией без аромата. Результаты показали, что аромат повышает внимание к последующему визуальному объекту по сравнению с ситуацией без вкуса.
Эффект стимулирования нервной системы EO от жасмина (Jasminum sambac L) был протестирован Hongratanaworakit (2010). Результаты показали, что ароматерапия жасмином усиливает вегетативно-опосредованную активность, включая насыщение крови кислородом, частоту дыхания и артериальное давление. Повышенное внимание и субъективное поведенческое возбуждение наблюдались у более энергичных и менее седативных лиц из группы ароматерапии.
Благодаря возможностям улучшения памяти Salvia lavandulifolia Vahl (испанский шалфей) Роббинс и Броян исследовали влияние ЭО этого растения на память (Robbins and Broughan, 2007). Шестьдесят добровольцев были разделены на три группы. Первая группа, названная «группой с отрицательным ожиданием», получила специальный совет, что S. lavandulifolia EO ухудшит их память. Вторая группа, получившая название «группа положительного ожидания», была обманута, полагая, что Э. S. lavandulifolia окажет положительное влияние на их память.
Третья группа, названная «контрольная группа», не была проинформирована о каких-либо преимуществах тестового ЭО в их памяти. После теста субъекты были проинформированы об участии во втором задании на память, которое было аналогично исходному. Основной целью этого исследования было проверить влияние ожиданий на фактический результат терапии. Как и ожидалось, члены первой группы имели меньший балл во втором тесте памяти по сравнению с первым тестом памяти. Аналогичным образом, согласно ожиданиям, вторая группа (положительное ожидание) представила улучшенные результаты во второй задаче памяти по сравнению с первой. Удивительно, но в противоположность пророчеству члены третьей группы (контрольной группы), у которых не было словесного плана, не запоминали увеличенное количество слов во втором задании на память. Результаты исследования еще раз подтвердили, что эффекты ароматерапии были частично основаны на психологических явлениях, особенно на ожиданиях, что особенно заметно в вопросах манипулирования ожиданиями (Robbins and Broughan, 2007).
Среди патологических аспектов Альцгеймера, образование мозговых бляшек, нагруженных β-амилоидным пептидом (Aβ), конгофильная (амилоидная) ангиопатия, дистрофический неврит, появление NFT в височной доле, потеря холинергических нейронов и белого вещества являются важными признаками (Haass и Selkoe, 2007). Aβ происходит от ферментативного гидролиза белка-предшественника амилоида, называемого APP (Figure (Figure 4) .4).
APP расщепляется ферментами α, β и γ-секретазой в последовательности этапов, что приводит к образованию Aβ17–42, катализируемого α- и γ-секретазой, и образованию нейротоксического Aβ1–42 посредством β- и γ-секретаз (De Strooper и др., 2010). Дисбаланс между генерацией и последующим удалением Aβ приводит к накоплению нейронов и может быть стартовым фактором в развитии AD. Следовательно, ингибирование бета-амилоидного расщепляющего фермента (BACE1) является обязательным выбором в управлении AD вследствие его роли в расщеплении домена Aβ на N-конце в APP.
ЭО и их активные компоненты были протестированы как потенциальные препараты против БА. Антиамилоидную эффективность этих ЭО оценивали с использованием клеточных линий и моделей на животных. Aβ участвует в образовании сенильных бляшек, важного патологического маркера AD, которые вызывают апоптоз в нейронах через окислительный или нитрозативный стресс. Ли и соавт. (2011) разработали исследование нейропротективных потенциалов и молекулярного механизма 6-гингерола, преобладающего и острого компонента имбирного ЭО, против опосредованной Аβ 25–35 гибели окислительных и нитрозативных клеток в клетках SH-SY5Y.
Предварительная обработка 6-гингеролом обеспечивала защиту от опосредованной Аβ 25–35 цитотоксичности и апоптотической гибели клеток. Защита клеток обеспечивалась путем ингибирования фрагментации ДНК, нарушения потенциала митохондриальной мембраны (ММР), активации каспазы-3 и увеличения соотношения Bax / Bcl-2. Сообщалось, что нейропротективный механизм 6-гингерола опосредован подавлением индуцированной Aβ25–35 внутриклеточной аккреции активных форм кислорода (ROS) и активных форм азота (RNS).
6-Гингерол также восстанавливает уровень антиоксиданта глутатиона иммунной системы, истощенного Aβ25–35. Кроме того, тестовый образец усиливал экспрессию мРНК и белков, ответственных за синтез ключевых ферментов, таких как c-глутамилцистеинлигаза, участвующих в биосинтезе глутатиона. Экспрессия вышеупомянутых ферментов опосредуется активацией фактора, связанного с NF-E2. Очевидно, что 6-гингерол, который 6-гингерол, может быть эффективным средством профилактики и лечения БА через усиление антиоксидантной способности иммунной системы.
В другом исследовании Jeon et al. (2011) исследовали ЭО от SuHeXiang Wan (SHXW), используемое в качестве традиционной медицины для лечения судорог, инфантильных конвульсий и инсульта для благотворного воздействия при АД и других нейродегенеративных расстройствах. Предварительная ингаляция SHXW EO оживила память о животных моделях AD, которым вводили Aβ1–42. EO также подавлял опосредованную Aβ1–42 N-концевую киназу c-jun (JNK), протеинкиназы (p38) и тау фосфорилирование в гиппокампе животных. SHXW EO скрывал Aβ-опосредованный апоптоз и продукцию ROS путем усиления экспрессии HO-1 и Nrf2 в клетках SH-SY5Y. Результаты этого исследования свидетельствуют о том, что SHXW EO является новой ингаляционной терапией для профилактики и лечения AD.
Чтобы научно обосновать благотворное влияние ЭО / компонентов, Azizi et al. (2012) исследовали влияние тимола и карвакрола на когнитивные функции с использованием животных моделей. В этом исследовании оба тестируемых образца улучшали когнитивные функции у животных, которым вводили Aβ25–35 и скополамин. В тесте Морриса с водным лабиринтом (MWM) задержка на спасение была увеличена, а записи в целевом квадранте были уменьшены. Aβ25–35 и вызванное скополамином ухудшение памяти были отменены после введения тимола и карвакрола.
Во время исследований токсичности оба образца были признаны безопасными даже при чрезвычайно высоких концентрациях. Результаты этого исследования предоставили важные доказательства эффективности и безопасности тимола и карвакрола при амилоид-индуцированных расстройствах, таких как AD и деменция. Анти-амилоидные, ингибирующие холинэстеразу, противовоспалительные и антиоксидантные потенциалы этих компонентов ЭО могут быть ответственны за благоприятные эффекты в когнитивной гипофункции.
Cioanca et al. (2014) протестировали ЭО из кориандра, Coriandrum sativum var. microcarpum за его потенциальные антидепрессантные, анксиолитические и антиоксидантные потенциалы в ингаляционной форме с использованием крысиной модели Aβ 1–42 у AD. Анксиолитический и антидепрессантоподобный эффект от вдыхаемого эфирного масла кориандра изучали с помощью моделей с повышенным уровнем лабиринта (EPM) и теста принудительного плавания (FSM).
Кроме того, антиоксидантную активность в гиппокампе оценивали с использованием специфической активности каталазы (CAT) и общего содержания восстановленного глутатиона (GSH). ЭО-лечение значительно улучшало двигательную активность, уменьшало время плавания и неподвижности у животных ФСМ, предварительно обработанных Aβ1–42. Кроме того, ингаляционная терапия ЭО увеличивала уровень глутатиона в гиппокампе на животных моделях и активность ферментов CAT, свидетельствующих о его антиоксидантном потенциале.
Текущее исследование предполагает, что многократные ингаляционные воздействия ЭО кориандра заметно улучшают тревожность, депрессию и снимают окислительный стресс при AD. В другом исследовании Majlessi et al. (2012) исследовали EO Zataria multiflora Boiss.
(Lamiaceae) для когнитивных и нейропротекторных эффектов на животных моделях AD. Результаты исследования показали, что зависимое от концентрации улучшение когнитивных способностей животных, на что указывают различные параметры, такие как увеличение латентного времени нахождения в пути, пройденное расстояние, угол курса, наблюдалось в предварительно обработанных группах Aβ25–35. ЭО был в высокой степени безопасен при проведении теста на острую токсичность даже при высоких концентрациях, чем тестируемая доза. Благоприятное воздействие ЭО объясняется наличием компонентов, эффективных при воспалении, окислительном стрессе и ингибиторов холинэстеразы.
Свободные радикалы генерируются во время аэробного дыхания, существенного аспекта живых существ. Эти свободные радикалы легко атакуют жирные кислоты, ДНК, белки, другие незаменимые молекулы и участвуют во множестве расстройств, включая AD, рак, старение, воспаление, болезнь Паркинсона, диабет, атеросклероз и заболевание печени.
Свободные радикалы, которые образуются в процессе окисления, нейтрализуются до нерадикальных форм ферментами, включая CAT и гидропероксидазу. Однако, когда образование свободных радикалов аномально велико или иммунная система истощена, тогда необходимо введение сторонников свободных радикалов (Halliwell, 1994; Ullah et al., 2016).
Кроме того, у пациентов с БА и старением головного мозга нарушение функции митохондрий приводит к чрезмерной выработке окисляющих свободных радикалов, что приводит к окислительному стрессу с последующим окислительным повреждением и патологическими нарушениями. Бета-амилоид (Aβ) является мощным возбудителем АФК и РНС. Эти реактивные виды быстро вызывают окислительное повреждение нервных, микроглиальных, цереброваскулярных клеток и тканей.
На рисунке приведены различные источники производства свободных радикалов с особым акцентом на Aβ как инициатор активных форм кислорода (ROS) и активных форм азота (RNS). После генерации свободные радикалы атакуют мембранные липиды, клеточные органеллы, что приводит к выработке митохондриальных токсинов гидроксиноненала (HNE) и малонового диальдегида. Окислительный стресс повреждает связанные с мембраной ионоселективные АТФазы и стимулирует приток кальция посредством стимуляции NMDA-рецепторов, комплекса мембранной атаки (MAC) и формирования ион-специфических пор Aβ с максимальным увеличением цитозольной и митохондриальной кальциевой нагрузки.
Клеточный амилоид направлен на цитохром с оксидазу, α-кетоглутарат и пируватдегидрогеназу и, таким образом, вызывает повреждение митохондриальной ДНК, вызывая ее фрагментацию. Продукты перекисного окисления липидов усиливают фосфорилирование и агрегацию тау-белков, которые впоследствии ингибируют комплекс I. Избыточные количества ROS и RNS продуцируются в комплексах I и III. Кроме того, митохондриальный мембранный потенциал (ММП) сминается и поры перехода проницаемости (ψm) открываются, что приводит к активации каспаз. Aβ также стимулирует выработку стресс-индуцированных протеинкиназ (p38) и c-jun N-терминальной киназы (JNK) в дополнение к p53, которые стимулируют апоптоз, приводящий к повреждению клеток.
Лаванда является важной традиционной медициной, повсеместно используемой в Азии, Европе, Риме, древней Греции, а также может быть найдена в древних еврейских текстах и Библии. Эфирное мало Лаванды используется в качестве альтернативного средства для лечения воспаления, головной боли, стресса и депрессии. Чтобы исследовать нейропротекторные эффекты лаванды, Hancianu et al. (2013) провели исследование, описывающее антиоксидантные и антиапоптотические потенциалы ЭО из лаванды (Lavandula angustifolia ssp.
Angustifolia Mill. И Lavandula hybrida Rev). Лаванда ЭО продемонстрировала значительный антиоксидантный и антиапоптотический потенциалы на моделях крыс со слабоумием, вызванных деменцией. Подострое ингаляционное воздействие ЭО значительно увеличивало уровень антиоксидантных ферментов иммунной системы, включая супероксиддисмутазу (СОД), глутатионпероксидазу и КАТ. Кроме того, общее количество GSH и перекисного окисления липидов снижалось в определенных гомогенатах тканей мозга.
Таким образом, защитные действия лавандового ЭО могут быть опосредованы сильной антиоксидантной активностью. Кроме того, прототипы расщепления ДНК не присутствовали в группах, обработанных ЭО, что указывает на антиапоптотический потенциал образцов. В целом, результаты исследования показывают, что сильная антиоксидантная и антиапоптотическая активность ЭО являются основными факторами, влияющими на нейропротекторное действие тестируемых образцов.
Последние достижения в неврологических исследованиях показали, что BACE1, также известный как секретаза, катализирует расщепление APP, приводящее к образованию β-амилоидных пептидов. Будучи амилоидогенными по природе, эти Aβ накапливаются в мозгу AD и вызывают воспалительные реакции с последующим высвобождением свободных радикалов, вызывающих повреждение нейронов (Nitsch, 1996; Asai et al., 2007; Vassar, 2014).
Антиоксидантные агенты могут быть полезны при химиотерапии AD, ослабляя воспалительные пути посредством удаления свободных радикалов (Kamal et al., 2015). В последнее время методы лечения на основе растений получили значительное внимание благодаря их сравнительной безопасности, эффективности и эффективности в отношении нескольких целей. Среди натуральных продуктов ЭО из ароматических и лекарственных растений представляют большой интерес благодаря их антиоксидантным, ингибиторным свойствам холинэстеразы, антиамилоидным свойствам и высокой доступности в мишени из-за липофильного характера. Таким образом, ЭО могут быть очень эффективными и альтернативными для лечения БА по сравнению с синтетическими препаратами, которые связаны с серьезными побочными эффектами (Brahmachari, 2013).
Сообщалось, что многочисленные ЭО обладают сильным антиоксидантным потенциалом и могут эффективно использоваться при расстройствах, вызванных свободными радикалами, включая неврологические заболевания и старение. Например, сообщается, что ЭО из тимьяна, гвоздики, эвкалипта, листьев корицы, можжевельника, базилика, ромашки, кориандра и тмина обладают значительным антиоксидантным потенциалом (Tomaino et al., 2005; El-Ghorab et al., 2008; Wei и Shibamoto 2010).
Сообщается, что Thymus spathulifolius обладает сильной антирадикальной активностью благодаря присутствию активных компонентов тимола и карвакрола в высоких концентрациях 36,5% и 29,8% соответственно (Tepe et al., 2004). Аналогичным образом, антиоксидантная способность египетского кукурузного шелка объясняется наличием высоких концентраций карвакрола (58,1%) и тимола (20,5%) (El-Ghorab et al., 2008). Поступление в пищу масла орегано, как сообщается, значительно задерживает окисление липидов на животных моделях (Botsoglou et al., 2004).
Сообщалось, что ЭО из Achillea millefolium удаляет гидроксильные свободные радикалы путем ингибирования перекисного окисления липидов в гомогенате тканей печени животных (Candan et al., 2003). В другом исследовании ЭО из Salvia multicaulis и Salvia cryptantha продемонстрировали более высокую антиоксидантную активность, чем стандартные препараты (Tepe et al., 2004).
Сообщается, что многие ароматические компоненты терпеноидов и терпеновых групп, такие как α-терпинен, β-терпинолен, 1,8-цинеол, β-терпинен, ментон, тимол, изоментон, линалоол и эвгенол, которые в избытке присутствуют в ЭО, ответственны за антиоксидантные потенциалы ( El-Massry and El-Ghorab, 2006; Wei and Shibamoto, 2010). Аналогично, было обнаружено, что ЭО из Thymus mastichina, Thymus caespititius и Thymus camphorates высокоэффективны против свободных радикалов благодаря наличию биоактивных компонентов линалоола и 1,8-цинеола.
Точно так же EO Melissa officinalis L., обогащенной ментоном, изоментоном, гераниалом и цитронеллалом, считается высокоэффективным антиоксидантным средством (Mimica-Dukic et al., 2004). Эти исследования подтверждают идею о том, что ЭО являются сильнодействующими антиоксидантами, которые являются биоразлагаемыми, липофильными, сравнительно безопасными и могут являться потенциальными заменителями синтетических лекарств в лечении нейродегенеративных расстройств (Янишлиева-Масларова и Хейнонен, 2001).
Несколько ЭО были протестированы для лечения возбуждения и других симптомов деменции в поисках более полезных препаратов в качестве нейролептиков, связанных с нежелательными побочными эффектами и ограниченной эффективностью. Например, Elliott et al. (2007) использовали EOs из Lavandula angustifolia Mill. и Melissa officinalis L., принадлежащей к Lamiaceae, для ведения возбуждения у лиц с тяжелой деменцией.
Седативный и успокаивающий эффект обоих ЭО уже установлен, что может способствовать консолидации памяти. В исследовании способности связывания рецептора оба масла интенсивно ингибировали связывание радиолигандов с мускариновыми рецепторами M1, 5HT2A, гистаминовыми H3 и сайтом канала рецептора GABAA. М. officinalis EO продемонстрировал широкую способность связываться с рецептором по сравнению с L. angustifolia EO и показал сродство к связыванию с 5HT1A и агонистическим сайтом связывания рецепторов GABAA.
Результаты этого исследования показали, что оба ЭО действуют как субстрат и взаимодействуют с несколькими рецепторами и могут эффективно использоваться для облегчения симптомов возбуждения. И наоборот, M. officinalis EO обладает способностью сокращать время социальной отмены и увеличивать время конструктивной деятельности пациентов с деменцией. В исследовании Huang et al. (2008) исследовали электрофизиологические свойства ЭО с акцентом на модуляцию ионных каналов.
Лаванда ЕО ингибирует связывание трет-бутилбициклофосфоротионата (TBPS) с каналом GABAA-рецепторов переднего мозга крысы. Однако никакого влияния на AMPA, NMDA, AMPA, холинергические и никотиновые рецепторы не наблюдалось. Е.О. L.angustifolia и M. officinalis в комбинации (50:50) ингибировали связывание флунитразепама. В электрофизиологическом задании L. angustifolia EO обратимо ингибировал GABA-опосредованный ток в культурах коры крыс и показал, что лавандовое масло обратимо, без ингибирующего действия на AMPA и NMDA-индуцированные токи.
Кроме того, M. officinalis EO ингибировал связывание TBPS с рецепторным каналом GABAA, однако никакого влияния на AMPA, NMDA, холинергические и никотиновые рецепторы не наблюдалось. Электрофизиологические тесты показали, что бальзамные ЭО могут обратимо ингибировать токи, опосредованные ГАМК. Однако не наблюдалось ингибирующего воздействия на токи, индуцированные AMPA и NMDA (Abuhamdah et al., 2008).
Влияние ЭО из L. angustifolia на поведение при агитации у пациентов с деменцией сообщалось Lin et al. (2007). Пожилые люди с AD, сосудистой деменцией или другими типами деменции были включены в исследование. Семьдесят пациентов были разделены на две группы: ароматическая группа поддерживала лавандовое ЭО в течение 3 недель с последующим введением ингаляции подсолнечника без запаха в течение 3 недель, тогда как вторая группа сделала диаметрально противоположное.
Клинический ответ оценивался с точки зрения китайской версии инвентаризации возбуждения Коэна-Мэнсфилда (CCMAI) и нейропсихиатрической описи (CNPI). Результаты исследования показали, что средний балл CCMAI и средний балл CNPI были значительно снижены после ароматерапии с лавандой. Кроме того, терапия лавандой хорошо переносилась в течение курса терапии, и наблюдалось значительное снижение поведения при возбуждении.
Следовательно, лавандовая ароматерапия может быть полезной альтернативой психотропным препаратам (Lin et al., 2007). Лимонен из EO лимона был протестирован Zhou et al. (2009) в модели деменции, вызванной скополамином, с применением теста пассивного избегания и теста в открытом поле. Лимонен и его метаболит периллиловый спирт показали значительное улучшение памяти. Уровень нейротрансмиттеров, особенно дофамина, был ниже у животных, получавших скополамин, но этот эффект был отменен терапией лимоненом или периллиловым спиртом до инъекции скополамина. Эти компоненты EO лимона также проявляют in vitro активность ингибирования холинэстеразы (Zhou et al., 2013).
Анксиолитические потенциалы эфирных масел.
Тревога — это состояние психологических и физиологических нарушений, проявляющихся когнитивными, эмоциональными, поведенческими и соматическими элементами. Все вместе эти факторы вызывают неприятные ощущения в сочетании с опасением, раздражением, беспокойством и беспокойством.
Начало тревоги внезапно и неожиданно без какого-либо стимулирующего стимула и, следовательно, является серьезным медицинским состоянием. Чтобы справиться с необычной ситуацией паники, организм подвержен некоторым симптомам, таким как напряжение, потливость, сердцебиение, боль в груди, расширение папиллярных узлов и одышка (O’Connor et al., 2000; Borkovec and Ruscio, 2001).
Современные анксиолитические средства, такие как бензодиазепины, связаны с многочисленными побочными эффектами, такими как лекарственная толерантность, злоупотребление и седация. Следовательно, ароматерапия с психоактивными ЭО может быть полезной альтернативной терапией для снятия тревоги (Woelk and Schläfke, 2010). Сообщалось, что некоторые растения обладают сильным анксиолитическим потенциалом.
Например, L. angustifolia Mill (лаванда), Citrus sinensis L. (апельсин), Santalum album RBr (сандаловое дерево), Rosa damascena Mill (роза), Citrus bergamia Risso. (бергамот), Salvia sclarea L. (шалфей шалфей), Anthemis nobilis L (ромашка романская) и виды пеларгонии являются сильными анксиолитическими агентами (Setzer, 2009; López et al., 2017). Химический состав и эффекты ЭО, составляющих Cananga odorata (иланг-иланг), были оценены исследователями на животных моделях с использованием инструментов поведенческой оценки (Gaydou et al., 1986; Zhang et al., 2016).
Кроме того, уровень нейротрансмиттеров и их метаболитов также оценивался после воздействия масла. C. odorata EO проявлял значительный анксиолитический эффект на животных моделях. Компоненты C. odorata, включая бензилбензоат, линалоол и бензиловый спирт, также показали анксиолитический эффект в модели тревоги на животных. Компоненты ЭО снижали уровни дофамина в стриатуме и увеличивали уровень 5-гидрокситриптамина (5-НТ) в гиппокампе экспериментальных животных.
Среди анксиолитических фитотерапий наиболее часто используется исследуемая лаванда ЭО и ее активный компонент линалоол. Аниолитическое действие линалоола было исследовано Cline et al. (2008) с использованием EPM и анализа сывороточных уровней катехоламинов и кортикостерона. Результаты исследования показали, что GABAA в озере линалоол опосредовал анксиолиз, но двигательная активность и двигательные функции были улучшены на животных моделях. В рандомизированном двойном слепом исследовании анксиолитические эффекты перорально вводимого лавандового ЭО были протестированы на 97 добровольцах с использованием нейтральных и вызывающих беспокойство кинопленок.
Влияние ЭО на настроение, тревогу, шкалу позитивных и негативных эффектов, частоту сердечных сокращений, характеристику состояния тревоги и гальваническую реакцию кожи измеряли после приема 100, 200 мкл капсул лаванды ЭО. Результаты показали, что 200 мкл лавандового ЭО уменьшали симптомы тревоги у людей, подвергшихся воздействию нейтральных пленок. Тем не менее, в вызывающих тревогу кинематографических группах лавандовый ЭО оказывал умеренное благотворное влияние. Это исследование делает вывод, что лавандовое ЭО эффективно при слабой и умеренной тревоге, но не эффективно при сильной тревоге (Bradley et al., 2009).
Фармакологически эффективная ароматерапия может быть лучшим выбором для снятия тревоги у пациентов, окаменевших от хирургических вмешательств или стоматологических процедур. В исследовании относительная эффективность лавандового ЭО и стандартных лекарств была проверена у пациентов с дооперационной тревожностью (Braden et al., 2009). Добровольцы (150 человек) были разделены на контрольную группу, получавшую стандартные лекарства, тестовую группу / группу аромата, поддерживающую ЭО (лаванда), и группу без аромата, получавшую стандартное лекарство плюс масло жожоба.
Симптомы тревоги оценивались при поступлении и переносе в операционную на этапах до и после терапии. В группах, обработанных лавандой ЭО, после переноса в операционные залы отмечалось значительное снижение симптомов тревоги, что свидетельствует о его потенциальной роли в снятии предоперационной тревоги. Другой препарат лаванды EO (капсулы Silexan) был протестирован Woelk and Schläfke (2010) в контролируемом клиническом испытании с использованием бензодиазепина в качестве стандартного препарата. Пациентов держали на тестовом препарате или лоразепаме в течение 6 недель.
Уровень тревожности объективно оценивали по шкале оценки тревожности Гамильтона (общий балл HAM-A) от исходного уровня до последней терапии. Результаты показали, что терапия на основе ЭО способна облегчить симптомы генерализованной тревоги и по эффективности аналогична стандартному препарату лоразепам.
В группах, получавших ЭО и ларазепам, соматическая, психическая тревожность и два промежуточных балла HAM-A были значительно снижены. Кроме того, под-баллы, включающие шкалу тревожности самооценки, клинические глобальные впечатления от степени тяжести, опросник состояния беспокойства Penn State и дневник сна, показали одинаковую положительную эффективность в обоих методах лечения.
Терапия на основе лаванды ЭО была лишена седативного эффекта, потенциального злоупотребления наркотиками и хорошо переносилась участниками. Таким образом, это может быть лучшей, безопасной, но эффективной альтернативой терапии бензодиазепинами при лечении генерализованной тревоги (Woelk and Schläfke, 2010).
Широдхара — аюрведическая масляная терапия, лечащаяся кунжутным маслом, — общеизвестное средство от тревоги и эффективное управление измененным состоянием сознания (ASC). Для оценки фармакофизиологических эффектов широдхары в композицию добавляли лавандовый ЭО. Добровольцы были разделены на три группы, а именно: обычная группа Широдхара (кунжутное масло), аромат-широдхара (0,3% лавандовый ЭО + кунжутное масло) и контрольная группа.
Масла наносились с помощью роботизированной системы капания масла. Были записаны различные параметры, включая частоту сердечных сокращений, беспокойство, температуру рук и ног и ASC. Сильные анксиолитические и ASC эффекты наблюдались в группе ароматов.
Значимость между анксиолиз-АСК и психологическим эффектом повышения температуры кожи ног была более очевидной в группе аромата Широдхара по сравнению с другими группами. Авторы пришли к выводу, что психофизиологические эффекты лаванды-широдхары были основаны на расслабляющем действии лавандового ЭО через обонятельные нервы, лучшем поглощении масел через кожу и физиологическом воздействии капли кунжутного масла на лоб, опосредованной соматоавтономным рефлексом через термосенсоры или датчики давления с использованием тройничного черепного нерва (Xu et al., 2008).
Масло нероли — еще одно традиционное анксиолитическое средство, полученное из цветов Citrus aurantium L (горький апельсин). Чтобы научно обосновать его анксиолитическое действие, Chen et al. (2008) исследовали нероли ЭО путем ингаляции на животных моделях.
Уровень тревожности оценивался с помощью FST и локомоторных заданий как в ароматических, так и в стандартных контрольных группах. Как терапия на основе ЭО, так и стандартное лекарственное средство (алпразолам) проявляли анксиолитическую активность в поведенческих тестах, хотя точный анксиолитический механизм не был объяснен. Это исследование обеспечило научную базу для потенциального использования масел нероли для лечения тревожных расстройств.
Другие EO, в том числе Citrus sinensis L. (аромат сладкого апельсина), Melaleuca alternifolia Maiden и Betche, Alpinia zerumbet (оболочка цветка) и Nigella sativa L. (черные семена) были детально исследованы с использованием моделей на животных. Эти ЭО проявляли значительную анксиолитическую активность (Murakami et al., 2009; Perveen et al., 2009; Faturi et al., 2010; Satou et al., 2010).
Составляющие ЭО также представляют большой интерес для научного сообщества, занимающегося неврологическими расстройствами. Например, влияние вдыхаемого линалоола на тревогу было исследовано Linck et al. (2009). Благоприятное воздействие линалоола оценивалось с точки зрения влияния на социальные взаимодействия, тревожность, агрессивное поведение и память.
Социальные взаимодействия были значительно улучшены, а агрессивное поведение было значительно снижено после лечения линалоолом. Высокий анксиолитический эффект наблюдался на обработанных животных моделях, на что указывало проведение большего количества времени в светлой области во время теста свет / темнота. Однако нежелательное влияние на память наблюдалось при высокой дозе, которая была связана с анксиолитическим и релаксантным действием линалоола. Аналогичным образом, положительные эффекты монотерпен фенолкарвакрол на поведенческие нарушения были проанализированы на животных моделях. Результаты подтвердили сильное анксиолитическое действие карвакола без влияния на двигательную активность подопытных животных (Melo et al., 2010).
Влияние ароматерапии на тревожность, вызванную раком, сообщается несколькими исследователями. Согласно литературным данным, 13,9-25% больных раком страдают от тревожных (около 70% непатологических) расстройств, которые сильно влияют на их образ жизни и химиотерапию (Mantovan et al., 2009).
Цитрусовые бергамия Risso EO обычно используются в качестве ароматерапии для лечения симптомов раковой боли, вызванного стрессом беспокойства и расстройств настроения. Анализируя нейрофармакологические эффекты ЭО от C. bergamia, итальянская исследовательская группа сообщила, что эти ЭО высвобождают экзоцит и несут опосредованный выброс аминокислот рядом с нейротрансмиттерами в гиппокампе млекопитающих.
Эти результаты подтверждают предположение, что эти ЭО мешают нормальной и патологической синаптической пластичности. Эти результаты и некоторые нейропротекторные эффекты ЭО от C. bergamia свидетельствуют о его использовании в альтернативной медицине при тревожных расстройствах (Imanishi et al., 2009; Bagetta et al., 2010). В нескольких других исследованиях также сообщалось о значении ароматерапии при тревожных расстройствах, вызванных раком (Hansen and Hansen, 2007; Chang, 2008; Imanishi et al., 2009).
Эпилепсия — это нейрональное расстройство, характеризующееся хронической и постоянной нейрональной активностью в результате снижения порога судорог в ЦНС (Thews et al., 1999). Одним из предлагаемых механизмов является чрезмерное высвобождение глутамата возбуждающего нейротрансмиттера, который после связывания с глутаматергическими нейронами вызывает чрезмерное высвобождение кальция в постсинаптических нейрональных клетках.
Другая теория объясняет расстройство с точки зрения мутаций, которые приводят к выработке неэффективного ингибирующего пептида, называемого ГАМК. Он затрагивает 50 миллионов человек во всем мире, и болезнь не может быть полностью ликвидирована. Эпилепсия имеет более 40 типов, классифицированных по возрасту, типу приступов, типу терапии и прогнозу. Около 30% пациентов имеют неконтролируемые судороги, несмотря на использование клинически доступных противоэпилептических препаратов (Mischel et al., 1995; Cendes, 2005).
Статус эпилепсии (SE) является наиболее опасным типом эпилепсии, характеризующимся постоянными и повторяющимися эпизодами судорог в течение более 30 минут, и связан с более высоким уровнем смертности.
Сообщалось о нескольких исследованиях терапевтической эффективности ЭО как альтернативы доступным в настоящее время лекарственным препаратам для лечения эпилепсии. Антиантиконвульсивная активность сафранала, монотерпенового альдегида и активного ароматического компонента Crocus sativus L. была исследована Pathan et al. (2009). Результаты показали, что сафранал проявлял дозозависимую антиконвульсивную активность в моделях SE, опосредованных пентилентетразолом (PTZ).
Предполагаемый противосудорожный механизм этого летучего компонента объясняется его агонистической активностью в отношении ГАМК-рецепторов. Таким образом, сафранал был предложен в качестве потенциальной будущей дополнительной терапии при лечении SE. Сообщается, что монотерпеноидный спиртовой компонент нескольких растительных ЭО, терпинен-4-ол, эффективен при судорогах (de Almeida et al., 2011). У животных, получавших терпинен-4-ол, отмечалось значительное снижение тонических судорог задних лап и спонтанной двигательной активности, тогда как период ожидания судорог был увеличен.
Эфир обыкновенной бытовой специи Ocimum basilicum L. и родственных видов были исследованы Oliveira et al., Благодаря уже зарегистрированным противосудорожным и депрессантным действиям ЦНС (Oliveira et al., 2009). Химический анализ выявил наличие психоактивных компонентов, 1,8-цинеола, гераниола и линалоола.
Эфир проявлял депрессантное действие на ЦНС через снижение спонтанной активности, атаксии, седации и птоза при всех испытанных дозах. Кроме того, ЭО показал значительное продление в период сна и уменьшил латентность сна. Эти ЭО увеличивали латентность эпизодов судорог как в тестах на PTZ, так и на пикротоксиновые припадки. Результаты этого исследования показали, что ЭО O. basilicum обладают противосудорожным и депрессантным потенциалом ЦНС, опосредованным через центральные ГАМКергические рецепторы.
Вахаб и др. (2009) сообщили о противосудорожной эффективности EO от Myristica fragrans Houtt. (мускатный орех) с использованием различных животных моделей судорог. Как правило, начало противосудорожного эффекта было быстрым, но длительность действия была короткой, тем не менее, он проявлял значительный противосудорожный эффект в модели заболевания MES. В моделях конвульсий, вызванных PTZ, дозозависимый противосудорожный эффект наблюдался даже после начала толчков.
Мускатный орех Е.О. задерживал начало опосредованных стрихнином судорог, не изменял двигательную активность даже при высоких концентрациях. В заключение, мускатный орех может быть эффективным средством при частичных и сильных приступах. Тем не менее, он не эффективен при миоклонических приступах и судорогах из-за отсутствия легкого потенцирующего эффекта клонических судорог.
В нейрофармакологическом исследовании Cymbopogon proximus EO El Tahir и Abdel-Kader (2008) обнаружили, что частичная или полная защита была предложена в моделях конвульсий, вызванных PTZ, стрихнином, пикротоксином и поражением электрическим током. Pimpinella anisum L. (анис) традиционно эффективен при эпилепсии, хотя механизм его антиэпилептической активности не совсем понятен.
В исследовании Janahmadi et al. (2008) оценивали противоэпилептический эффект ЭО в моделях судорог до и после ПТЗ. Результаты показали, что ЭО аниса вызывает гипервозбудимость нейронов за счет снижения после гиперполяризации улитки. Таким образом, анис ЭО должен быть осторожно использован у людей, страдающих эпилепсией (Janahmadi et al., 2008).
В текущей обзорной статье мы сосредоточились только на исследовательской работе, связанной с нашей темой, опубликованной в рецензируемых журналах. Исследователи из разных регионов изучали ЭО в попытке рационализировать их традиционное использование или найти альтернативные методы лечения для существующих лекарств и уменьшить побочные эффекты, связанные с использованием современных лекарств.
In vitro, in vivo и клинические исследования были проведены на ЭО и летучих составляющих, чтобы найти их эффективность и механизм действия. Завершая текущий обзор литературы, отмечается, что ЭО эффективны практически по всем известным в настоящее время патологическим мишеням БА.
Эфирные масла также обладают нейропротекторным, антивозрастным потенциалом и эффективны при деменции, эпилепсии, тревоге и других неврологических расстройствах. Что касается AD, важно, чтобы эфиры, которые эффективны на нескольких мишенях (мультипотентные агенты), нужно было разравнивать, чтобы найти более эффективные лекарства по сравнению с доступными в настоящее время лекарствами, которые имеют ограниченную эффективность и полезны только для облегчения симптомов.
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
источник
