Несмотря на распространенность болезни Альцгеймера, новые методы лечения этого заболевания появляются достаточно медленно. Методы лечения, доступные на текущий момент временно улучшают симптомы потери памяти и проблем с мышлением. Эти типы лечения болезни Альцгеймера улучшают работу химических веществ в мозге, которые переносят информацию от одной клетки мозга к другой. Тем не менее, эти методы лечения не останавливают основной процесс, приводящий к гибели клеток головного мозга. Чем больше мозговых клеток погибает, тем сильнее прогрессирует болезнь Альцгеймера. Новое в лечении этого заболевания мы рассмотрим ниже.
Эксперты надеются на то, что вскоре будут разработаны новые методы лечения болезни Альцгеймера, которые смогут остановить или существенно замедлить прогрессирование этого заболевания. Растущее понимание процесса, в результате которого происходит разрушение мозга приводит к возникновению потенциально эффективных методов лечения болезни Альцгеймера, способных препятствовать основным процессам развития этого заболевания.
Эффективность следующих вариантов лечения болезни Альцгеймера в настоящее время изучается.
Некоторые из новых методов лечения болезни Альцгеймера нацелены на развивающиеся микроскопические сгустки белка бета-амилоида (бляшки). Бляшки являются характерным признаком болезни Альцгеймера.
Вот стратегии последних лет, направленные на бета-амилоиды:
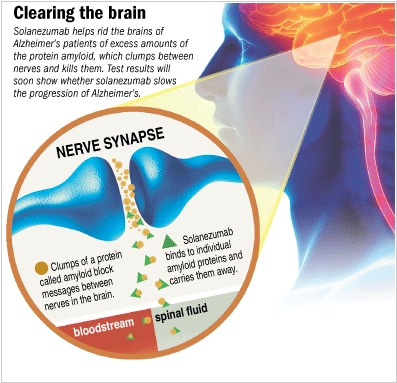
Некоторые препараты, известные как моноклональные антитела, могут предотвратить слипание бета-амилоидов и образование амилоидных бляшек, а также помочь организму очистить мозг от бета-амилоидов. Моноклональные антитела имитируют антитела человеческого организма, которые естественным образом вырабатываются в результате реакции вашей иммунной системы для подавления инородных организмов (в том числе и при вакцинации).
В результате недавних исследований, где изучалась эффективность моноклональных антител соланезумаба, были обнаружены возможные полезные эффекты в лечении людей, страдающих болезнью Альцгеймера начальной и средней стадии (подробно о стадиях болезни Альцгеймера читайте здесь – 7 стадий болезни Альцгеймера: признаки и симптомы). Препарат оказался более эффективным в лечении людей на ранней стадии развития этого заболевания. Самые последние исследования показали безопасность Соланезумаба. Дальнейшие исследования до сих пор проводятся.
Еще одним новым препаратом от болезни Альцгеймера является Адуканумаб. В предварительных исследованиях он показал обнадеживающие результаты. Однако действие этого препарата до конца не изучено и до сих пор ведутся дополнительные исследования.
Несколько лет назад исследователи узнали, что бета-амилоид взаимодействует с другим белком под названием Fyn. В сочетании с бета-амилоидом, Fyn чрезмерно активируется, что вызывает разрушение связей между нервными клетками (синапсы) в головном мозге.
Препарат Саракатиниб изначально разработан в качестве возможного лекарства от рака, в настоящее время проходит испытания эффективности при болезни Альцгеймера.
У мышей этот препарат выключал Fyn, что позволяло синапсам начинать работать снова, вследствие чего у животных в некоторой степени возвращалась память. Что касается эффективности Саракатиниба в лечении болезни Альцгеймера у людей, то сейчас полным ходом проводятся исследования.
Этот тип лечения позволяет уменьшить количество бета-амилоида, образованного в головном мозге. Исследования показали, что бета-амилоид получают из родительского белка в два этапа с помощью различных ферментов.
Несколько экспериментальных препаратов направлены на блокирование активности этих ферментов. Они известны под названием ингибиторы бета- и гамма-секретазы.
Жизненно важная транспортная система клеток мозга разрушается, когда тау-белок закручивается в микроскопические волокна, называемые нейрофибриллярными клубками, которые являются еще одной распространенной аномалией мозга при болезни Альцгеймера. Исследователи ищут способ предотвращения спутывания тау-белка и формирования клубков в головном мозге.
Ингибиторы агрегации тау-белка и тау-вакцины в настоящее время изучаются в клинических испытаниях.
Причиной болезни Альцгеймера может быть незначительное хроническое воспаление клеток мозга. Исследователи изучают способы лечения воспалительных процессов при болезни Альцгеймера.
Исследователи также изучают действие лекарственного средства от диабета под названием пиоглитазон (Актос), так как его применение может уменьшить образование бета-амилоида и воспаление в головном мозге.
Исследователи изучают влияние инсулина на мозг и функции его клеток, а также изменение инсулина в головном мозге, которые могут быть связаны с болезнью Альцгеймера. Они тестируют назальный спрей с инсулином, чтобы определить, помогает ли это средство замедлить прогрессирование болезни Альцгеймера.
Появляется все большее количество доказательств того, что здоровье головного мозга тесно связано со здоровьем сердца и кровеносных сосудов. Ученые полагают, что риск развития болезни Альцгеймера возрастет в результате развития многих заболеваний сердца или артерий. К ним относятся высокое кровяное давление (гипертония), болезни сердца, инсульт, диабет и высокий уровень холестерина.
Ряд исследований направлен на то, чтобы наилучшим образом отследить эту связь. Вот базовые стратегии в рамках исследования этой связи:
Исследователи изучают насколько лекарства, используемые для лечения сердечно-сосудистых заболеваний (таких как лекарства, снижающие кровяное давление) могут помочь людям с болезнью Альцгеймера или насколько они могут уменьшить риск развития этого заболевания.
Дополнительные проекты более внимательно присматриваются к тому, как связь между болезнью сердца и болезнью Альцгеймера происходит на молекулярном уровне, чтобы найти новые целевые препараты.
Исследователи изучили вопрос образа жизни, а именно на сколько сильно влияет здоровый образ жизни, способный предотвратить заболевания сердца и сосудов, на предотвращение развития болезни Альцгеймера или на способности отсрочить ее начало.
В одном исследовании женщинам с повышенным риском развития болезни Альцгеймера давали гормональные препараты на основе эстрогена по крайней мере в течение года в период перименопаузы или при возникновении ранней менопаузы, что способствовало предотвращению ухудшения мозговых функций и памяти у этих женщин.
Это открытие указывает на важность проведения некоторых профилактических мер в определенные периоды жизни людям, склонным к развитию болезни Альцгеймера. Различные открытия, связанные с гормональной терапией, различаются, в связи с чем необходимы дальнейшие исследования, прежде чем давать какие-либо рекомендации относительно профилактики этого заболевания.
Разработка новых лекарственных препаратов от болезни Альцгеймера очень медленный и трудоемкий процесс. Темп разработки новых методов лечения этого заболевания явно не на стороне людей, которые уже страдают от этого недуга и ждут новых вариантов лечения.
Чтобы помочь ускорить разработку новых лекарственных средств, Coalition Against Major Diseases (CAMD), альянс фармацевтических компаний, некоммерческих фондов и государственных советников, наладили первое в своем роде партнерство для обмена данными клинических испытаний относительно болезни Альцгеймера.
Исследователи предполагают, что совместное использование этих данных, относительно обследования более чем 4000 участников, позволит ускорить разработку более эффективных методов лечения.
источник
Для лечения Альцгеймера продолжают изобретать новые препараты. Это нейродегенеративное заболевание, которое приводит к потере памяти, способности ориентироваться в пространстве. Патология поражает преимущественно людей пожилого возраста. Прекратить разрушение головного мозга нельзя. С помощью препаратов можно лишь замедлить развитие патологического процесса.
Патология была описана немецким врачом Алоисом Альцгеймером. Он занимался изучением определенного вида слабоумия. В ходе исследований было выяснено, что развитию патологического процесса способствуют белковые соединения, которые откладываются в клетках и межклеточном пространстве и не пропускают нервные импульсы от клетки к клетке. Это приводит к дегенеративным изменениям и нарушениям функционирования органа.
После определения проблемы выявили гены, которые провоцируют развитие патологического процесса. Стало известно, что изменения в головном мозге провоцируются липопротеином и глуманатом. Если в организме в недостаточном количестве вырабатывается ацетилхолин, то нервные импульсы передаются неправильно.
Для устранения патологического процесса применяют определенные знания. В первую очередь, пользуются ингибиторами холинэстеразы, разрушающей ацетилхолин. Они также позволяют добиться сбоев в образовании бета-амилоида.
Но о точных причинах болезни известно мало что. Вся информация о болезни построена на предположениях. Поэтому с помощью терапевтических методик можно добиться только замедления развития деменции. Но поражение мозга будет дальше прогрессировать аж до смерти больного. До сих пор пытаются изобрести новый вариант развития патологии.
Новые методы лечения болезни Альцгеймера продолжают изобретать. Уже неоднократно доказано, что развитию заболевания способствуют сосудистые патологии. Часто люди страдают деменцией по сосудистому типу и болезнью Альцгеймера в одно и то же время.
Главной причиной атеросклеротического поражения является повышение уровня холестерина. Ученые выдвинули предположение о воздействии холестерина на формирование амилоида.
Холестерин способствует перемещению предшественников амилоида к клеточным мембранам, именуемым липидными плотниками, которые сообщены с плохими секторами альфа и бета.
Если получиться выявить средство для обнаружения препарата, препятствующего связи с холестерином, то предшественники не соединятся с липидными плотниками, растворятся альфа-секретазой, которая не образовывает амилоид.
Научные статьи о лечении болезни Альцгеймера говорят о том, что проводятся исследования по поводу влияния сосудистых патологий.
Существует предположение о взаимодействии бета-амилоида с фибриногеном. Этот процесс провоцирует тромбообразование, из-за чего нарушается питание клеток и они гибнут. На основе этой теории разработали новое лекарственное средство RU-505, который не дает амилоиду взаимодействовать с фибриногеном и формировать тромбы. Но при этом не происходит ухудшения работы системы свертывания крови.
Клинические испытания проводят на мышах, которые заражены болезнью Альцгеймера. Препарат использовали для лечения больных в течение трех месяцев. Он значительно улучшает когнитивные функции и замедляет течение патологии.
Лекарство обладает высокой токсичностью, поэтому, прежде чем использовать средство для лечения людей, следует добиться снижения токсичности препарата.
Новости в лечении болезни Альцгеймера сообщают, что некоторые ученые применяют для терапии болезни Бексаротен, который использовали для устранения рака кожного покрова. Изменения в мозге при болезни Альцгеймера этим препаратом лечили у крыс. Уже на протяжении недели наблюдалось снижение количества амилоидных бляшек в мозгу животных в несколько раз.
Для получения точной информации об эффективности средства, следует продолжать эксперимент. Есть необходимость в более тщательном изучении влияния Бексаротена на организм крыс. Только после этого можно будет начать испытывать средство на людях.
Существуют специальные программы, предназначены для тренировки памяти у людей, страдающих болезнью Альцгеймера. Этот вариант был создан специалистами израильской клиники. Они изобрели специальную систему, которая заключается в выполнении заданий разной сложности. Сначала пациенту говорят определить цвет, форму, размер, назвать буквы или животных, после чего приступают к более сложным заданиям.
В процессе выполнения заданий определенные отделы мозга, которые контролируют память и обучение, подвергают электростимуляции. Эта процедура отвечает за активизацию функциональной активности клеток головного мозга.
Новое в лечении болезни Альцгеймера пытались изобрести гарвардские ученые, которые использовали вышеописанную методику для терапии патологического процесса в мозге.
Удалось определить, что когнитивные функции под его влиянием значительно улучшились. Данную технологию уже подвергли сертификации и планируют в ближайшем будущем открывать различные центры в Европе, которые будут лечить больных в соответствии с этой методикой.
Поэтому считается, что лекарство от Альцгеймера найдено. Но полностью этот вариант еще не изучен.
Также считается, что развитию дегенеративных нарушений в мозге способствует нарушение глюкозного обмена в органе. Существует и другой источник для образования энергии, представлен в виде кетонов, образующихся из триглицеридов.
Образование кетонов происходит из жиров в процессе поста или голодания. Но они также содержатся в некоторых продуктах питания. Большое содержание триглицеридов обнаруживается в масле кокоса.
Статистика говорит, что люди, проживающие в тропических странах и регулярно употребляющие кокосы, редко страдают расстройствами нервной системы.
Поэтому кокосовое масло рекомендуют в качестве одного из средств для профилактики болезни Альцгеймера. Сейчас пытаются создавать лекарственные препараты, главным компонентом которых является масло из кокоса.
Также перспективным вариантом считают лечения болезни с помощью стволовых клеток. Но эта методика еще не изучена.
Патологический процесс приводит к серьезным нарушениям в головном мозге, поэтому все силы ученых направлены на изобретение новых вариантов в терапии болезни. Они пытаются найти средство, которое избавит человечество от этой страшной проблемы и позволит людям пожилого возраста нормально жить в старости.
источник
Болезнь Альцгеймера – это наиболее распространенная форма деменции у пожилых людей.
Это прогрессирующая и, в конечном счете, фатальная болезнь головного мозга. Болезнь Альцгеймера нарушает высшую нервную деятельность – память, мышление, поведение.
Современные исследователи до сих пор ищут ее причины, а также методы эффективного лечения и профилактики этой болезни.
Болезнь Альцгеймера – это распространенная проблема. В разных странах ею страдает один из нескольких десятков человек старше 60 лет. К примеру, в Австралии этот показатель составляет 1 из 25, или 4%. Болезнь поражает людей в основном случайно. Но есть и редкие генетические мутации, которые становятся причиной наследственной болезни Альцгеймера в семье.
Клетки мозга, или нейроны, передают сигналы друг другу через соединения, которые называются синапсами. При болезни Альцгеймера эти синапсы разрушаются и фактически исчезают в тех частях мозга, которые отвечают за мышление.
Исследования показывают, что у людей с болезнью Альцгеймера нервные клетки повреждены, а между ними накапливаются отложения, называемые амилоидными. Эти отложения почти полностью состоят из протеина, который называют бета-амилоидом, или «А-бета». Именно они и ответственны за повреждение мозга при болезни Альцгеймера.
Бета-амилоидный белок повреждает клетки несколькими путями:
• Нарушение нормальной передачи информации между мозговыми клетками, особенно в тех участках, которые отвечают за память и рассуждения.
• Преобразование кислорода в пероксид водорода, который затем окисляет и разрушает клетки мозга.
• Создание особого сигнала для мозговых клеток, который запускает их самоуничтожение.
Исследователи пытаются выяснить причину, по которой у одних людей начинает откладываться амилоидный протеин, а у других – нет. Они также пытаются найти способ нивелировать токсические эффекты этого протеина.
Доказанные факторы риска болезни Альцгеймера:
• Возраст. Риск развития этой болезни удваивается каждые 5 лет после 65-летнего рубежа. В возрасте 70-74 года риск составляет 3%, а в 90-94 года он уже достигает 30-35%.
• Наследственность. Болезнь Альцгеймера с ранним началом – это очень редкая форма болезни, которая возникает у людей в возрасте между 30 и 60 годами. В 1980-х годах исследователи установили, что эта форма болезни связана с дефектами в генах. Если один из родителей страдает этой болезнью, то риск для его детей составляет 50%.
• Генетические заболевания. Многие люди с синдромом Дауна заболевают болезнью Альцгеймера уже после 40 лет – гораздо раньше здоровых людей. Это связано с наличием у них лишней копии гена предшественника амилоида.
Предполагаемые факторы риска болезни Альцгеймера:
• Травма головы, особенно тяжелая травма.
• Размер головы. Люди с меньшим обхватом головы заболевают чаще.
• Сосудистые факторы риска. Курение, гипертензия, сахарный диабет повреждают мозговые сосуды, что, возможно, повышает риск болезни.
• Рацион питания. Есть предположение, что диета с высоким содержанием насыщенных жиров повышает риск болезни Альцгеймера.
Современные методы лечения фокусируются на следующих моментах:
• Увеличение эффективности работы поврежденных нейронов. Сейчас для этого применяют донепезила гидрохлорид (Aricept), мемантина гидрохлорид (Namenda). Они усиливают работу больных нервных клеток, но их эффекты кратковременны и не излечивают болезнь.
• Профилактика выработки бета-амилоидного протеина. Исследователи пока только ищут вещества, которые замедлят преобразование «родительской» молекулы в бета-амилоидный белок.
• Защита нейронов от действия пероксида водорода. Было установлено, что токоферол (витамин Е) дает улучшение нервных функций у некоторых больных. Сейчас ученые интенсивно изучают другие антиоксиданты. Некоторые исследователи изучают металлы, такие как цинк, железо и медь, которые нужны здоровому мозгу, но делают амилоидный белок токсичным.
• Замедление отложения бета-амилоидного белка в мозге. Предполагается, что этот белок становится опасным для клеток только тогда, когда накапливается в большом количестве. Если эти отложения можно будет расщепить, то болезнь будет побеждена.
Ученые годами изучают возможные факторы риска и способы, которые помогут избежать или отсрочить наступление болезни Альцгеймера.
Некоторые ученые предполагают связь между повышенным уровнем холестерина и болезнью Альцгеймера. Это привело к идее изучить, как влияет прием гипохолестеринемических препаратов на риск возникновения болезни.
Наиболее популярными препаратами этой группы давно являются статины. К разочарованию ученых, длительные исследования не выявили никакого влияния статинов на риск болезни Альцгеймера.
Другие исследователи выяснили, что высокий уровень аминокислоты гомоцистеина связан с риском болезни Альцгеймера. Высокий уровень гомоцистеина – это также фактор риска заболеваний сердца.
3. Высокое артериальное давление.
Предполагается, что существует связь между риском болезни Альцгеймера и гипертензией, а также другими факторами, предрасполагающими к инсульту – диабетом, возрастом. Эти факторы способствуют повреждению сосудов и ухудшают кровоснабжение мозга. В результате такого стресса отложение бета-амилоидного белка ускоряется.
Исследования показывают, что диабет ассоциируется с несколькими типами деменции, включая болезнь Альцгеймера и сосудистую деменцию. Сахарный диабет второго типа и болезнь Альцгеймера даже имеют общие характеристики. Например, при болезни Альцгеймера повреждающий амилоидный протеин откладывается в мозгу, а при сахарном диабете аналогичный процесс происходит в поджелудочной железе. Ученые изучают и другие связи между этими заболеваниями.
Установлено, что риск болезни Альцгеймера у женщин выше, чем у мужчин, даже с учетом большей продолжительности жизни у женщин. Ученые исследовали эффекты разных гормонов на мозг, включая эстрогены. Некоторые исследования показали, что женщины, которые длительно получали заместительную гормональную терапию (ЗГТ) эстрогенами, реже заболевали болезнью Альцгеймера. Другие исследования пошли еще дальше: оказалось, важен не столько уровень эстрогена в крови, сколько в головном мозге.
Стоит заметить, что еще одно исследование не обнаружило вообще никакого влияния эстрогенов на риск болезни. А в одном случае было признано, что комбинированные оральные контрацептивы (эстроген + гестаген) даже повышают этот риск. Вопрос остается открытым.
Поддержание постоянной активности мозга может уменьшать риск болезни Альцгеймера и отсрочивать появление симптомов. Считается, что постоянная активность помогает головному мозгу стать более гибким и лучше адаптироваться при поражении одних участков, компенсируя их за счет других.
Но этот вопрос также изучается, и пока рано давать конкретные рекомендации по профилактике болезни. В любом случае, умственная деятельность не повредит никому. Особенно, если речь идет о пожилом человеке, чьи умственные способности с годами снижаются и требуют постоянной тренировки.
Исследования на животных и на людях показывают улучшение как физических, так и психических функций при регулярных физических упражнениях. Лучше всего сказывается на работе мозга ходьба, бег, аэробика, особенно если упражнения выполняются на свежем воздухе.
В масштабных исследованиях было выявлено, что люди, занимающиеся такими упражнениями, показывают лучшие результаты в планировании, расчетах и принятии решений, чем люди, которые ведут малоактивный образ жизни.
8. Антиоксиданты и питание.
Сегодня продолжается интенсивное изучение роли питания и диетических добавок в профилактике болезни Альцгеймера:
• Антиоксиданты. Эти вещества могут защищать клетки от губительного влияния пероксида водорода. Витамин Е выглядит в этом плане многообещающим. Но высокие дозы витамина Е (порядка 1000 единиц в день) повышают риск инсульта.
• Жиры в пище. Длительное злоупотребление насыщенными жирами приводит к диабету, гипертензии, атеросклерозу. А эти заболевания традиционно ассоциируются с болезнью Альцгеймера.
• Витамины группы В. В группе риска болезни Альцгеймера находятся люди с дефицитом витамина В12 (цианокобаламина) и В9 (фолиевой кислоты). Дефицит любого из этих витаминов также повышает уровень гомоцистеина.
• Гинкго. Многочисленные пищевые добавки на основе гинкго двулопастного изучались в качестве антиоксидантов, но не показали ожидаемых эффектов при болезни Альцгеймера.
• Шалфей. Эта трава традиционно считается полезной для памяти. Он показал свойства, подобные ингибиторам холинэстеразы – по этому же принципу работает несколько запатентованных лекарств от болезни Альцгеймера.
• Алюминий. Пока нет свидетельств того, что воздействие алюминия на человека повышает риск болезни Альцгеймера, но исследования продолжаются.
Каждому человеку нужно помнить, что даже витамины и травы обладают серьезными побочными эффектами. Бесконтрольный их прием опасен для здоровья!
Невозможно вылечить деменцию. Не существует ни одного доказанного способа предотвратить деменцию, включая болезнь Альцгеймера. Но есть перспективные меры, которые считаются полезными для профилактики и замедления этой болезни, хотя они еще только изучаются.
• Избегание черепно-мозговых травм, в том числе при контактном спорте.
• Мониторинг уровня холестерина и гомоцистеина в крови.
• Постоянный контроль артериального давления.
• Ограничение содержания животных жиров в пище.
• Диета, богатая антиоксидантами из фруктов и овощей.
• Адекватное употребление витамина Е, но не более 400 единиц в сутки.
• Адекватное употребление витаминов В9 и В12, даже в виде пищевых добавок.
• Умеренный прием алкоголя или полный отказ от спиртного.
• Поддержание постоянной социальной и интеллектуальной активности.
• Регулярные физические упражнения.
• Полный отказ от курения.
источник
Разработки в области лечения болезни Альцгеймера ведутся во многих странах мира. Тяжелое, неизлечимое заболевание становится причиной инвалидности большого количества людей во всем мире. Болезнь Альцгеймера – это нейродегенеративное заболевание, которое приводит к деменции (слабоумию), инвалидности и быстрой смерти в течение нескольких лет. Продолжительность жизни больного в среднем составляет около 7 лет, очень редко встречаются случаи, когда пациент с болезнью Альцгеймера живет более 13 лет.
Клиника неврологии Юсуповской больницы специализируется на лечении болезни Альцгеймера. Профессора и врачи высшей категории проведут осмотр, назначат необходимую диагностику и по результатам обследований подберут оптимальную терапию.
Истинные причины развития заболевания не изучены до сих пор, но известны следующие факторы, влияющие на развитие патологии:
- наследственность. Мутация трех генов в организме человека приводит к развитию заболевания. Около 10% случаев заболевания болезнью Альцгеймера в молодом возрасте связано с мутацией в генах АРР, также большой фактор риска представляет унаследованная аллель Е4 (ген АРОЕ), вариация с геном RELN (болеют женщины);
- амилоидная гипотеза. Накопление амилоидных бляшек в тканях головного мозга приводит к гибели нейронов, к нейродегенеративным изменениям;
- гипотеза тау-белка. В результате формирования нейрофибриллярных клубков из тау-белка в нервных клетках нарушается биохимическая передача сигналов между нейронами – это приводит к гибели клеток.
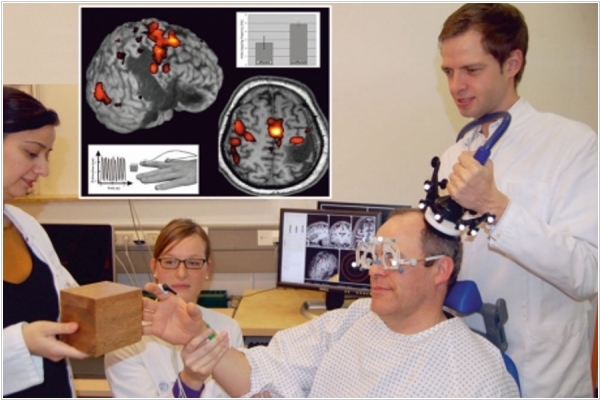
Новый метод борьбы с болезнью Альцгеймера исследуют в Австралии. С помощью высокочастотного ультразвука и газа (газ вводится микроскопическими пузырьками в кровь), проводят открытие гематоэнцефалического барьера в мозге, который препятствует поступлению в нервную ткань мозга находящихся в крови микроорганизмов, токсинов и факторов иммунной системы, воспринимающих ткани мозга как чужеродные. Открытие физиологического барьера происходит на короткое время, активизирует иммунные клетки мозга, которые поглощают амилоидные образования. Данный метод проходит апробацию на животных, клинические испытания на людях будут проводиться через несколько лет.
Исследователи из Китая научились превращать клетки соединительной ткани в клетки, похожие на нейроны. Биохимики использовали специальное химическое воздействие, которое полностью преобразовывало клетки. Исследователи смогли преобразовать больные нейроны в здоровые клетки.
Разработками вакцины против болезни Альцгеймера занимаются американские, шведские ученые. С помощью вакцины пытаются уничтожать образования из аномального белка. Американские ученые пошли дальше и решили воздействовать на токсины, которые вызывают разрушение сосудов мозга, а не на амилоидные бляшки. Опыты на мышах показали улучшение метаболизма в тканях головного мозга, снижение содержания окисленных жирных кислот, снизилось количество воспалительных процессов в мозге у стареющих мышей.
Научная конференция в Лондоне началась с представления нового метода лечения болезни Альцгеймера, Паркинсона, Хантингтона – метода генной терапии. Метод представлен как прививка вирусными частицами, которые встраиваются в поврежденные участки мозга. Модифицированные вирусные частицы – это носители здоровых генов, встроенных в фибробласты, созданные из клеток кожи участника. Ген производит белок, который стимулирует развитие и активность клеток мозга, поддерживает их жизнеспособность. Опыты с вирусными частицами показали позитивную динамику при введении их в определенные отделы мозга. Там наблюдался обширный рост нервных клеток, в отличие от других участков мозга, в которые не были введены вирусные частицы. Исследования находятся на второй стадии испытаний.
Американские компании Biogen и Eli Lilly заканчивают исследование современных препаратов для лечения болезни Альцгеймера – Адуканумаба и Соланезумаба. Действие Соланезумаба и Адуканумаба направлено на сокращение аномального белка, способствующего формированию амилоидных бляшек. Испытания на людях показали уменьшение содержания патологического белка в тканях головного мозга. Однако применение больших доз препарата Адуканумаба может привести к отеку мозга, у некоторых испытуемых препарат вызвал сильные головные боли. Работа над созданием новых методов и препаратов по борьбе с болезнью Альцгеймера продолжается.
Новый метод борьбы с болезнью Альцгеймера, который уже применяется для лечения больных – это лечение с помощью стволовых клеток. При введении молодых и здоровых стволовых клеток происходит активизация процесса восстановления в тканях головного мозга, регенерации нервных клеток, улучшение работы мозга.
В Юсуповской больнице применяют современные методы лечения болезни Альцгеймера, Специалисты больницы посещают международные симпозиумы и конференции, обмениваются опытом с коллегами из других стран. В клинике неврологии проводят современное лечение многих заболеваний, в том числе рассеянного склероза, болезни Паркинсона, болезни Альцгеймера, других расстройств. Чтобы пройти диагностику и лечение с помощью инновационной методики, запишитесь на консультацию к неврологу Юсуповской больницы по телефону.
источник
Профессор Рик Ливси открывает инкубатор в своей лаборатории в Кембридже и достает маленькую пластиковую чашу с шестью углублениями, заполненными розоватой жидкостью. В каждом углублении находится культура стволовых клеток, недавно выращенная из кожи пациента с болезнью Альцгеймера. Затем профессор извлекает похожую по форме чашу, где клетки созревали в течение 70 дней при температуре 37 градусов по Цельсию и преобразовались в нейроны. Видно, как они группируются вокруг образцов ткани мозга. В третьей чаше находятся специальные клетки под названием «микроглия» – передовая линия иммунной защиты в головном мозге. Считается, что они играют важную роль в патологии, связанной с болезнью Альцгеймера. Под микроскопом клетки микроглии похожи по форме на усики, стремящиеся к частичке ткани, инфицировавшей культуру. Профессор Ливси поясняет: «Очевидно, что микроглия притягивается к поврежденному участку. Однако пока не совсем ясно, что происходит с этими клетками при болезни Альцгеймера: проявляются ли они избыточную или, наоборот, недостаточную реакцию на повреждение в головном мозге».
Чтобы ответить на этот вопрос, в Кембриджском университете лаборатория под руководством профессора Ливси создала множественные клеточные культуры на основе биоматериалов, взятых у людей с наследственной болезнью Альцгеймера. Наблюдая за биохимическими процессами и поведением клеток, ученые рассчитывают в скором времени увидеть различия между этими клетками и здоровыми нейронами – это даст понимание фундаментальных процессов, происходящих при развитии деменции. После провальных испытаний препаратов от болезни Альцгеймера ученые обратили свои взоры на кардинально иные способы решения проблемы.
Пока же в мире насчитывается около 50 миллионов людей с деменцией, и эта цифра продолжает увеличиваться. Возможно, к 2030 году она достигнет 75 миллионов. Что касается расходов на лечение и уход за такими пациентами, то они достигают 1% от суммы всемирного ВВП: около одного триллиона долларов.
С тех пор как доктор Алоис Альцгеймер идентифицировал заболевание в 1906 году, ученые основательно изучили анатомические изменения при уменьшении объема головного мозга и развитии симптомов. В последние 30 лет молекулярные и генетические исследования позволили выявить, какие при этом протекают биологические процессы, при этом особое внимание уделялось отложениям из токсических протеинов, разрушающих нейроны. Однако доктор Ливси сетует: «При всех достижениях науки мы до сих пор не знаем основную причину развития болезни Альцгеймера. И даже нисколько не приблизились к разгадке».
Наиболее основательно учеными изучен процесс образования белка амилоида, он является основной мишенью большинства разрабатываемых фармацевтическими компаниями препаратов. Все начинается с белка – предшественника амилоида, присутствующего во всех здоровых клетках. Ученые до сих пор не могут определиться, в чем состоит его значение для организма. В головном мозге, пораженном патологическим процессом, ферменты расщепляют белок-предшественник амилоида на фрагменты под названием бета-амилоид, которые впоследствии откладываются в форме нерастворимых бляшек, характерных для болезни Альцгеймера.
Еще один процесс, свойственный этому нейродегенеративному заболеванию, — образование клубков тау-протеина – нерастворимых переплетений волокон внутри нейронов. Они являются деформированной формой тау-протеина, который в нормальном состоянии образует каналы в здоровых нервных клетках.
Последние двадцать лет нейробиологи фокусировали свое внимание на амилоиде, пытаясь создать средство, удаляющее из головного мозга амилоидные бляшки. Однако, как уже говорилось ранее, к ощутимым результатам это не привело. Теперь ученые переориентируются на принципиально новые методы, обращая внимание на роль иммунной системы и воспалительных процессов в головном мозге.
Впрочем, исследования, в которых амилоида выступает главной целью терапии, все еще доминируют. Джон Харди, профессор нейробиологии при Университетском колледже Лондона и первооткрыватель амилоидного генеза, настаивает на том, что амилоид – это первопричина, а не следствие заболевания. Последние исследования доказали, что отложения патологического белка амилоида начинают формироваться за 20-30 лет до проявления первых симптомов, а потом к нему присоединяется тау-протеин. По словам профессора Харди, лабораторные эксперименты длятся относительно недолго, поэтому ученым сложно было отследить начало развития патологического процесса, и лечение начиналось слишком поздно. Сейчас предпринимаются попытки назначать существующие препараты намного раньше, но и там необходимы дополнительные ресурсы.
Несмотря на отсутствие видимого прогресса, ученые не отказываются от борьбы с амилоидом. Клинические испытания препаратов, предназначенных для удаления амилоида, включая те, которые не прошли проверку у пациентов на поздних сроках болезни Альцгеймера – соланезумаб компании Эли Лилли и гантенерумаб компании Рош, – продолжаются, но уже на людях более молодого возраста, имеющих высокий риск развития заболевания из-за семейной истории и генетической предрасположенности. «У участников эксперимента нет симптомов заболевания, но благодаря позитрон-эмиссионной томографии обнаружены отложения бета-амилоида в головном мозге», — комментирует доктор Кэтрин Маммери, глава исследовательской группы. – «Участникам от 30 до 50 лет. Все они еще работают в полную силу. Здесь, конечно, возникает вопрос этического характера, ведь ни у кого из них нет симптомов, а нам приходится сообщать им об отложении амилоида в их головном мозге. Нам нужно очень тщательно подходить к вопросу отбора испытуемых в таких экспериментах».
Внимание к тау-протеину также не ослабевает. Швейцарская компания ИС Иммьюн разрабатывает средство от токсичного тау-протеина в трех направлениях: антитела, малые молекулы и вакцину, стимулирующую у пациента его собственную иммунную систему для борьбы с тау-протеином. «Мы хотим разработать вакцину против амилоида и тау, которую назначали бы человеку в сорок лет, чтобы предотвратить начало заболевания», — поясняет Андреа Пфайфер, глава компании. – «Мы стремимся к тому, чтобы врачи ставили пациентам индивидуально разработанные прививки».
Эпицентром всех новых подходов к исследованию болезни Альцгеймера стал Фонд исследования деменции в Лондоне, в который только один Билл Гейтс недавно инвестировал 50 миллионов долларов. Фонд – необычное коммерческое партнерство, образованное два года назад для вложения финансов в инновационные методы лечения. В партнерство входят правительство Великобритании, семь международных фармацевтических компаний и британский фонд исследований болезни Альцгеймера. Фонд поддерживает новые биотехнологии, финансируя 12 стартапов и проектов, ни один из которых не занимается разработкой молекул, воздействующих на амилоид, и только один занимается тау-протеином. В основном внимание уделяется иммунной системе как мощному оружию против деменции. (Кстати, сейчас аналогичный подход набирает обороты в лечении онкологического заболевания.) Так, Фонд инвестировал уже более 200 миллионов долларов в американскую фармацевтическую компанию АббВи, разрабатывающую противодементную иммунотерапию.
Различные исследования: от генетического анализа до работы с животными моделями и пациентами – дают основания считать основной причиной деменции неспособность иммунной системы головного мозга выводить токсичные вещества и патологические протеины. Но как ее укрепить – пока загадка. В головном мозге удалением нежелательных веществ занимаются две биологические системы. Одна, недавно обнаруженная, представляет собой ряд каналов, называемый глимфатической системой. Другая – микроглия, иммунные клетки головного мозга. Глимфатическую систему можно образно представить в виде дренажных каналов, а микроглию – дворником, собирающим мусор. Однако проблема с иммунной системой головного мозга состоит в том, что крайне сложно распознать, в чем заключается проблема: активна ли она чрезмерно или, наоборот, недостаточно.
Джим Салливан, глава отдела исследований в фармацевтической компании АббВи, считает, что иммунная система работает не в полную силу: «Представьте себе амилоидные бляшки, окруженные микроглией. Но бляшки при этом не исчезают. Это наводит на мысль о недостаточном функционировании иммунной системы. Именно поэтому выглядит обещающим направление по активизации глиальных клеток и предотвращению роста амилоидных отложений».
Разработка эффективной терапии должна сопровождаться усилением методов ранней диагностики деменции. Как правило, заболевание диагностируется слишком поздно. Обычно диагноз ставится после обращения пациента с жалобами на проблемы памяти. Однако болезнь начинается приблизительно за двадцать лет до появления данных симптомов. Конечно, есть позитрон-эмиссионная томография и анализ спинномозговой жидкости, обнаруживающие амилоидные отложения до появления симптомов. Однако высокая стоимость этих процедур тормозит их широкое распространение. Перспективным могло бы стать обнаружение маркеров болезни Альцгеймера в крови человека, и даже есть многообещающие начинания. Например, протеин под названием «кластерин». На данный момент идут клинические испытания, но, по словам заведующего лабораторией профессора Лавстоуна, еще далеко до массового внедрения анализа крови на выявление данного белка.
Заглядывая далеко в будущее, некоторые эксперты прогнозируют возможность трансплантации нервных стволовых клеток – похожих на те, которые выращивает в своей лаборатории профессор Ливси, – взамен погибших клеток у пациентов с деменцией. «Полагаю, в какой-то момент мы сможем остановить прогрессирование деменции, если захватим болезнь на раннем этапе», — с оптимизмом комментирует эту перспективу доктор Пфайфер. – «А затем нам понадобится терапия стволовыми клетками, чтобы болезнь повернула вспять».
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Наука и медицина не стоят на месте, поэтому постоянно появляются новые методики и направления в лечении нейродегенеративных патологий.
Рассмотрим новое в лечение болезни Альцгеймера:
- Препарат J147 – воздействует на токсины, которые разрушают нейронные связи в головном мозге и приводят к развитию деменции. Лекарство все еще находится на стадии активных испытаний, но уже есть положительные результаты. J147 улучшает когнитивные способности и метаболические процессы, уменьшает уровень жирных кислот в мозгу.
- Данная разработка основана на генной инженерии и предполагает доставку гена фактора роста нервов в нейроны мозга. Ген NGF стимулирует синтез белка, который поддерживает жизнеспособность нейронов, а также стимулирует их развитие и активность. Для доставки гена к месту назначения используется модифицированный вирус, который не оказывает негативного воздействия на организм. Данный метод проходит окончательную фазу испытаний.
- Еще одна разработка – это трансформация клеток соединительной ткани – фибробластов, в нейроны головного мозга. Для преобразования больных нейронов в здоровые, пациенту дают два препарата, взаимодействие которых обеспечивается химические реакции.
- Для борьбы с бета-амилоидными бляшками в головном мозге разработали нано лекарство. Действие препарата направлено на уничтожение соединений, которые нарушают коммуникацию между нейронами и способствуют их гибели. Также были разработаны нано частицы из полимера и золота, которые после попадания в организм соединяются с бета-амилоидными бляшками и останавливают их рост.
- Компьютерная система для выбора эффективного препарата. Суть данной разработки в том, что болезнь Альцгеймера имеет генетическое происхождение. Зная какие гены повреждены, и как на них влияют определенные лекарства, можно сформировать оптимальный препарат.
Все вышеперечисленные методики находится на этапе разработки или тестирования, но уже есть информация о их положительном эффекте.
С момента открытия стволовые клетки перевернули представление ученых о человеческом организме и стали причиной прорыва в области многих исследований. Они зарекомендовали себя при нейродегенеративных патологиях в качестве заместительной терапии. То есть метод лечения болезни Альцгеймера стволовыми клетками заключается в замещении измененных тканей здоровыми.
Клеточная терапия обладает такими свойствами:
- Активирует процессы регенерации.
- Способствует появлению новых кровеносных сосудов.
- Восстанавливает нервные клетки и утраченные функции головного мозга.
- Устраняет неврологические симптомы.
- Улучшает состояние памяти.
- Повышает когнитивные способности.
- Способствует восстановлению речи.
- Стабилизирует эмоциональный фон.
- Увеличивает мышечную силу и подвижность.
Методика лечения стволовыми клетками довольно проста. С помощью липосакции материал собирают из брюшного жира. Для активации клеток их подвергают фотовоздействию цветного спектра монохроматической частоты и через 2-3 часа возвращают в виде инъекции.
Данный метод лечения не нарушает моральные аспекты, поскольку лечение проводится стволовыми клетками пациента, а не животных или эмбрионов. Кроме деменции, клеточная терапия зарекомендовала себя при аутизме, болезни Паркинсона, инсульте, кардиомиопатии.
Лекарственные препараты с активным компонентом N-фенилантраниловая кислота – это фенаматы. Действующее вещество многокомпонентно, так как в его состав входит мефенамовая, меклофенамовая и этафенамовая кислоты. Особого внимания заслуживает мефенаминовая кислота.
Мефенамовая кислота – это нестероидное противовоспалительное средство. Обладает периферическим, центральным, анальгезирующим и жаропонижающим действием. Лечебный эффект при болезни Альцгеймера связан с противовоспалительными свойствами препарата, поскольку воспалительное поражение мозговых тканей имеет важное значение в патогенезе данного расстройства.
- Основное клиническое применение: уменьшение болей при ревматических заболеваниях. Лекарство быстро всасывается и трансформируется в два метаболита, которые поддерживают терапевтическую концентрацию в плазме крови в течение 1-8 часов. Около 50% препарата выводится с мочой в виде метаболитов, остальное количество с калом в виде неконъюгированного 3-карбонового метаболита. Активный компонент легко проникает через плацентарный барьер, может обнаруживаться в молоке во время лактации и в желчи.
- Побочные реакции: раздражение ЖКТ, диспепсические расстройства, кожные аллергические реакции, гемолитическая анемия, бронхоспазмы, повышение уровня мочевины в крови.
- Противопоказания: заболевания ЖКТ, прием антикоагулянтов, беременность и лактация.
- Взаимодействие с другими лекарственными препаратами: связывается с белками плазмы, оказывая потенцирующий эффект на активность антикоагулянтов из группы кумаринов. С особой осторожностью лекарство следует принимать с Варфарином.
Мефенамовая кислота выпускается в капсулах по 250 и 500 мг, также существует суспензия 10 мг/мл, используемая в педиатрической практике.

Болезнь Альцгеймера является самой распространенной формой деменции. Но несмотря на это, на сегодняшний день все еще не существует терапевтического метода или лекарства, которое бы остановило патологический процесс. Из-за этого постоянно разрабатываются новые препараты для лечения нейродегенеративной патологии.
Рассмотрим наиболее перспективные разработки:
Ее действие направлено не на профилактику заболевания, а на уничтожение прогрессирующей патологии. Вакцина содержит активные компоненты, которые после введения в организм активируют иммунную систему на выработку антител к морфологическому субстрату – бета-амилоиду. Благодаря этому болезнь замедляет развитие.
Разработка для устранения нейропатического болевого синдрома. Но в ходе исследований, было установлено что лекарство замедляет прогрессирование деменции. Механизм действия MDA7 основан на противовоспалительной активности в ЦНС и воздействии на каннабиоидные рецепторы в головном мозге. Проведенные эксперименты установили, что препарат способствует восстановлению познавательных процессов, синоптической пластичности и памяти.
Ингибирует фермент β-секретазы, расщепляющий белковые соединения. Блокирует биохимические процессы – амилоидный каскад, понижает концентрацию β-амилоида в спинномозговой жидкости. Согласно проведенным исследованиям, ежедневный прием препарата не просто замедляет альцгеймеровскую деменцию, а останавливает ее. Лекарство все еще проходит тестирование на пациентах с ранними формами болезни.
- 4. Противодиабетические препараты
- Росиглитазон – это лекарство, назначаемое при сахарном диабете второго типа. Но ученные доказали, что медикамент улучшает память, когнитивные функции и способность к обучению.
- Инсулин детимер – рекомбинантный инсулин и еще один потенциальный препарат от деменции. Повышает активность ферментов из группы митоген-активируемых протеинкиназ, которые отвечают за синаптическую передачу сигнала между нейронами головного мозга. Повышает когнитивные способности, улучшает память.
- 5. Лекарственный пластырь Экселон
Данный препарат представляет собой чрескожную форму ривастигмина. Пластырь наклеивают на 24 часа. За этот временной интервал в кровь поступает активный компонент, который борется с дегенеративными процессами. Особенность данного медикамента в том, что пластырь следует ежедневно наклеивать на новый участок тела, который не должен соприкасаться с одеждой.
источник
2019. Фен Жанг теперь умеет редактировать ДНК и РНК с точностью до буквы
Фен Жанг, один из трех ученых, которые изобрели знаменитую технологию редактирования ДНК — CRISPR, не сидит на лавке и не плюет семечки, вспоминая о прошлых заслугах. Недавно он основал собственный стартап Beam Therapeutics и сразу поднял $222 млн инвестиций. Что же так привлекло инвесторов? Оказывается, Жанг уже придумал CRISPR 2.0. Технология называется RESCUE и позволяет с высокой точностью заменять любое азотистое основание — аденин (A), гуанин (G), цитозин (C), тимин (T) — буквы генетического алфавита. По сравнению с первоначальной версией CRISPR — это как резинка и карандаш VS ножницы и клей (стандартный CRISPR может только вырезать целые куски ДНК молекулы и склеивать то, что осталось). Кроме того, RESCUE позволяет редактировать не только ДНК, но и РНК, что намного безопаснее — позволит перепрограммировать клетки лишь на время. В первую очередь Жанг хочет вылечить болезнь Альцгеймера. Говорит, там нужно исправить всего две буквы.
2019. Корейцы создали наноробота для доставки стволовых клеток в мозг
Доставить какой-либо препарат в мозг — это сложная задача, а доставить туда стволовые клетки — практически невозможная. Но корейскому профессору Hongsoo Choi и его молодой команде из Института DGIST это удалось. Более того, они научились доставлять стволовые клетки точно в тот участок мозга (крысы), в который требуется. Сделали они это при помощи наноробота, созданного 3х-мерной лазерной литографией. Наноробот может двигаться по кровеносным сосудам внутри организма под управлением внешнего магнитного поля и компьютерного томографа. Функции «Разгрузка» в нем нет — он разгружает груз стволовых клеток постепенно, главное его быстро доставить в нужное место. Зачем доставлять стволовые клетки в мозг? Для лечения нейродегенеративных заболеваний (типа болезни Альцгеймера) и омоложения мозга.
2019. Болезнь Альцгеймера пробуют лечить свето-звуковой стимуляцией мозга
Болезнь Альцгеймера пока не поддается лечению, но похоже, в конце туннеля появился свет и немного звука. Ученые из MIT выяснили, что если споймать мышку с болезнью Альцгеймера и ежедневно по 1 часу показывать ей мигающую лампочку на частоте 40Гц, которая сопровождается звуковыми сигналами, то мышка начинает гораздо лучше соображать. Пытливые ученые даже выяснили почему так происходит. Вернее, они подозревают, что такая стимуляция активирует глиальные клетки мозга, которые работают как макрофаги и начинают активнее поглощать амилоидные бляшки (те самые штучки, из-за которых и развивается болезнь Альцгеймера). Что хорошо в этом методе — то что он безопасный. Поэтому ученые уже начали эксперименты на людях.
2018. В Австралии разработали простой метод лечения деменции ультразвуком
Исследователи из австралийского университета Квинсленда, под руководством Юргена Гётца (на фото), разработали методику устранения амилоидных бляшек из мозга с помощью ультразвука. Считается, что именно эти бляшки вызывают болезнь Альцгеймера и другие формы деменции. Ультразвуковые волны активируют микроглиальные клетки, которые «переваривают» бляшки и таким образом удаляют их. Учёные успешно завершили испытания на мышах и готовы начать первую фазу испытаний на людях. Если метод окажется эффективным, то мы получим невероятно простой способ лечения деменции. Юрген Гётц говорит, что возможно в будущем у каждого будет личное небольшое ультразвуковые устройство, которое люди смогут использовать чуть ли не в превентивных целях.
2018. Ученые впервые восстановили память при болезни Альцгеймера
Одним из самых неприятных проявлений болезни Альцгеймера является постепенная утрата памяти из-за повреждения нейронных связей. Индийские биологи из Центра им. Джавахарлала Неру (JNCASR) во главе с профессором Тапасом Кунду (на фото) говорят, что им удалось споймать мышь с болезнью Альцгеймера и вернуть ей память. Они создали молекулу, которая в головном мозге активирует 2 фермента (ацетилтрансферазу гистона СВР и р300), которые отвечают за формирование нейронных связей. Потом доставили ее в мозг мыши (с помощью наночастиц) и повернули вспять процесс разрушения нейронных связей амилоидными бляшками.
2018. Ученые выяснили, как остановить развитие болезней Альцгеймера и Паркинсона
Британские ученые Сергей Каспаров и Аня Тешенбахер из Бристольского университета утверждают, что обнаружили способ, при помощи которого можно остановить прогрессирование болезней Альцгеймера и Паркинсона. В отличии от остальных терапевтических стратегий, нацеленных на нейроны, они придумали воздействовать на глиальные клетки — астроциты, которые поддерживают нейроны и разделяют их своими телами на группы. Исследователи установили, что астроциты отображают рецепторы для естественного соединения, которое называется просапозин. Когда просапозин воздействует на рецепторы, то тем самым задействует их защитный механизм, а также останавливает повреждения, вызывающие болезни Паркинсона и Альцгеймера. Ученые говорят, что теперь открыта дорога к созданию новых нейропротекторных препаратов.
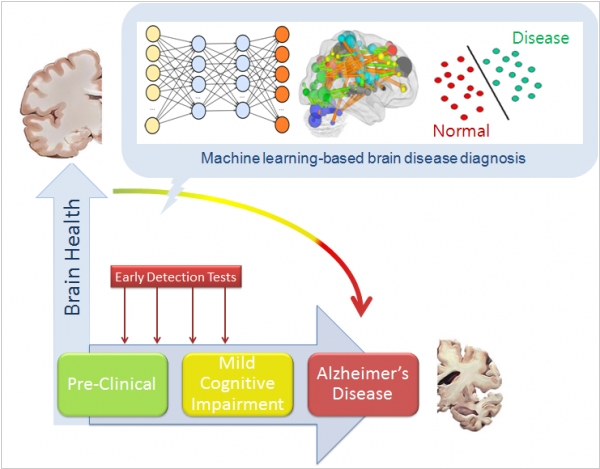
2017. Нейросеть диагностирует болезнь Альцгеймера на ранней стадии
Лечить болезнь Альцгеймера врачи пока не умеют, но диагностировав ее на ранней стадии, по крайней мере можно отсрочить ее воздействие. Ученые из университета Кейс Вестерн Резерв (США) создали нейросеть, которая предсказывет появление этого заболевания на ранней стадии. Система обрабатывает сканы МРТ, характеристики гиппокампа, метаболизма мозга, белковые и генетические особенности, умеренные когнитивные нарушения и другие параметры. Алгоритм отбирает параметры, которые лучшим образом разделяют больных и здоровых людей. А затем отбирает из переменных, указывающих на заболевание, те, что лучше других разделяют людей с умеренными когнитивными нарушениями и собственно болезнью Альцгеймера. Исследователи протестировали программу на 149 пациентах и утверждают, что их нейросеть превзошла другие методы диагностирования.
2016. Новый тест диагностирует болезнь Альцгеймера по анализу крови
Изменения в мозге, вызываемые болезнью Альцгеймера, начинаются как минимум за 10 лет до того, как проявляются первые симптомы. Поэтому лечить болезнь на ранней стадии — пока даже не пробовали. Однако исследователи Роуэнской университетской школы объявили, что создали схему анализа крови, которая позволяет определить Альцгеймера на ранней стадии и со 100% точностью. Они провели исследование и выделили 50 аутоиммунных биомаркеров, способных определить раннюю стадию Альцгеймера. С помощью белковых микрочипов этот набор биомаркеров способен определять людей, у которых начинается ранняя стадия Альцгеймера, со стопроцентной точностью. Помимо этого, тест способен выявить разницу между ранним Альцгеймером и более прогрессивной его формой с точностью до 98,7 процента, ранним Паркинсоном в 98 процентах случаев и рассеянного склероза и рака груди со 100-процентной точностью.
2015. Ученые научились замедлять старение мозга
Американские ученые Антонио Куррэис и Дэвид Шуберт из института биологии имени Джонаса Солка занимались разработкой технологии лечения болезни Альцгеймера. Обычно те, кто берется за эту болезнь, думают, как удалить из мозга амилоидные бляшки, которые разрушают нейронные связи. Но эта парочка решила воздействовать не на бляшки, а на токсины, разрушающие сосуды в мозге. Разрушение микрососудов в мозге обычно считают следствием болезни Альцгеймера, но что если это — ее первопричина? В общем, ученые синтезировали препарат J147 и испытали его на специальных быстро-стареющих мышах. В результате, принимавшие препарат мыши показали лучшие результаты в когнитивных тестах и тестах памяти, а также продемонстрировали лучшую координацию движений. Кроме того, состояние мозга этих мышей было гораздо лучшим, чем у тех, кто не подвергался действию препарата. Были отмечены лучшие показатели метаболизма, уменьшение количества воспалительных процессов и уменьшение содержания окисленных жирных кислот в мозгу.
2015. Verge Genomics собирается создать лекарство от болезни Альцгеймера не в лаборатории, а в компьютере
Болезнь Альцгеймера, как и многие другие нейродегенеративные болезни мозга, имеют генетическую природу. И фармацевтические гиганты, в надежде изобрести лекарство от этих болезней, тратят десятилетия и миллиарды долларов на лабораторные исследования того, как определенный препарат влияет на определенный ген. Стартап Verge Genomics хочет ускорить и удешевить этот процесс в тясячу раз. Они придумали компьютерную систему, которая похожа на поисковик Google. Подобно, как Google индексирует сайты в интернете и составляет их рейтинг релевантности каждому запросу, система Verge индексирует существующие лекарства и (по имеющейся информации) составляет их рейтинг релевантности каждому гену. Таким образом, даже не имея лаборатории, стартап может формировать оптимальный препарат, воздействующий на группу генов (а не на один ген, как у фарма-гигантов). А именно группы (комбинации) генов являются причиной болезни, заявляют в стартапе.
2015. Генная терапия дает надежду в лечении болезни Альцгеймера
Команда исследователей Калифорнийского университета Сан-Диего опубликовали результаты своих (10-летних) клинических испытаний технологии лечения болезни Альцгеймера, основанной на генной терапии. Технология предполагает доставку в нейроны мозга гена фактора роста нервов (NGF). Этот ген производит белок, поддерживающий жизнеспособность нейронов, стимулирующий их развитие и активность. Ген доставляли с помощью модифицированного вируса, а также в составе клеток соединительной ткани — фибропластов, созданных из клеток кожи участников. По заверению ученых, методика показал свою безопасность, и у всех без исключения пациентов был заметный положительный эффект от процедуры – в областях введения NGF наблюдался обширный рост нервных клеток, чего не было заметно в незатронутых медиками отделах мозга. В настоящий момент запущена II фаза испытаний – она покажет, насколько эффективно генная терапия может бороться с болезнью Альцгеймера, а также другими нейродегенеративными нарушениями.
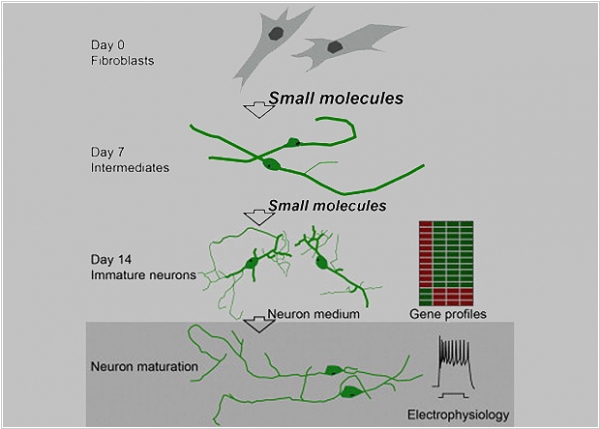
2015. Китайцы превратили клетки кожи в нейроны
Биохимики из Шанхайского института биологических наук превратили фибробласты (клетки соединительной ткани) в клетки, которые по своей морфологии, электрофизиологическим показателям и профилю экспрессии генов не отличается от обычных нейронов. Этого результата удалось добиться без встраивания в них каких-либо генетических конструкций, исключительно за счет двухэтапного воздействия несколькими, специально подобранными химическими «коктейлями». Ученые опробовали несколько тысяч химических соединений, прежде чем отобрать те, которые способны превращать один тип клеток в другой. Причем, как оказалось, ни одно соединение само по себе не способно приводить к трансформации, для этого требуется два «коктейля» химических стимулов. Ученые пошли дальше и сумели с помощью этой технологии преобразовать больные Альцгеймером нейроны в здоровые.
2015. Лекарство от болезни Альцгеймера может появиться в 2016 году
Фармацевтическая компания Eli Lilly начала последний этап клинических испытаний своего препарата, замедляющего развитие болезни Альцгеймера — Соланезумаба. Действие препарата направлено на сокращение количества деформированного белка бета-амилоида, из которого образуются амилоидные бляшки, вызывающие болезнь Альцгеймера. По результатам полуторогодичных клинических испытаний, скорость ухудшения высших мозговых функций у людей с ранней формой заболевания, получивших терапию соланезумабом, значительно замедлилась по сравнению с показателями пациентов из контрольной группы, получавшей плацебо. Ожидается, что в 2016 году будут получены результаты, которые позволят получить разрешение контролирующих органов на использование препарата. В настоящее время лекарств с доказанной эффективностью против болезни Альцгеймера не существует.
2015. Новый препарат Адуканумаб позволит замедлять развитие деменции и болезни Альцгеймера
Новый препарат Адуканумаб разработки американской компании Biogen показал убедительные результаты в терапии старческой деменции и болезни Альцгеймера. В клинических испытаниях приняли участие 166 добровольцев, им случайным образом были назначены различные дозы лекарства или плацебо. Первые положительные результаты от приема лекарства были выявлены спустя 26 недель — именно на данной стадии концентрация отложений начала изменяться. Несмотря на это, слишком высокие дозировки опасны для организма. Лекарство может вызвать отек мозга, особенно у тех, кто генетически предрасположен к болезни Альцгеймера. Стоит отметить, что лекарство от данного недуга — одно из самых ожидаемых во всем мире, так как в данный момент зафиксировано около 15 миллионов больных, у которых диагностируется болезнь Альцгеймера.
2014. Нанолекарства против болезни Альцгеймера
Болезнь Альцгеймера сопровождается образованием в мозге бета-амилоидных бляшек, которые нарушают коммуникации между нейронами и приводят к их гибели. Логика подсказывает, что справиться с этими бляшками могут нанолекарства. Они достаточно малы, чтобы преодолеть гематоэнцефалический барьер, попасть в мозг и растворить бляшки. Однако, к сожалению пока в этом направлении нет ни одного успешного проекта или стартапа. В 2008 году был создан европейский проект NAD, который ставит своей целью разработку нанотехнологии для лечения болезни Альцгеймера, но пока ничего значительного он не показал. Одна из последних научных работ в данном направлении принадлежит индийским ученым из Национального Центра исследования мозга. Они разработали наночастицы из золота и полимера, которые могут соединяться к бета-амелоидным бляшкам и прекращать их рост.
2014. Магнитная стимуляция восстанавливает когнитивные способности пациентов с болезнью Альцгеймера
Американские исследователи из Северо-Западного университета нашли способ возвращать память и восстанавливать умственные способности пациентов с болезнью Альцгеймера (по крайней мере, на 20%). Ученые предлагают стимулировать нейроны в гиппокампе и некоторых расположенных рядом областях мозга пациентов, страдающих от болезни Альцгеймера, с помощью транскраниальной магнитной стимуляции. В результате, наблюдается улучшение памяти и повышение способностей к обработке информации. До сих пор, без операции или применения лекарственных препаратов ничего похожего ученым не удавалось. Магнитная стимуляция позволяет добиться большей активности клеток мозга. Автор исследования Джоел Восс считает, что у методики есть все шансы стать распространенным способом борьбы с заболеванием, особенно учитывая его безопасность и тот факт, что этот способ воздействия на нейроны неинвазивный.
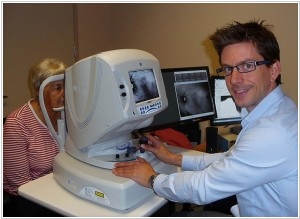
2014. Аппарат NeuroVision позволяет диагностировать болезнь Альцгеймера за 20 лет до появления симптомов
Хотя медики еще не научились лечить болезнь Альцгеймера, но возможность ее супер-ранней диагностики может привести к появлению новых методов ее лечения на ранних стадиях. Американская компания NeuroVision Imaging разработала технологию и аппарат для выявления болезни Альцгеймера посредством сканирования сетчатки глаза. Оказывается данная болезнь приводит к образованию амилоидных бляшек на сетчатке за долго до появления симптомов. Вот по наличию этих бляшек и осуществляют диагностику. Хотя пока аппарат еще находится в стадии клинических испытаний, разработчики заявляют чуть-ли не о 100% точности его работы.
2013. Американские стартапы разрабатывают технологии генной терапии
Если журнал Science назвал главным прорывом 2013 года в научной медицине иммунотерапию рака, то другой (не менее авторитетный журнал) Nature особо отметил технологию редактирования генома в живых клетках при помощи системы CRISPR, разработанную американским стартапом Editas Medicine. Конечно, генотерапия — круче иммунотерапии, потому что иммунотерапия борется с самим заболеванием, а генотерапия — с его источником — с ошибкой в ДНК. Так вот, новая технология CRISPR якобы позволяет намного дешевле и точнее доставлять редактор ДНК в нужные клетки и надежнее обрезать лишние (вредные) отрезки ДНК, чем существующая технология, использующая вирусы. В первую очередь Editas Medicine планирует использоваться свое генетическое лекарство для лечения нейропсихиатрических расстройств, таких как болезнь Хантингтона и шизофрения. Стартап привлек уже $43 млн инвестиций — а такие деньги на ветер не бросают. ***
2013. В Испании изобрели вакцину от болезни Альцгеймера
Испанская биотехнологическая компания Araclon Biotech, которая разрабатывает тест крови для ранней диагностики Болезни Альцгеймера, заявила о новом открытии — вакцине против болезни Альцгеймера, которая до сих пор считается неизлечимой. Лекарство основано на методе иммунотерапии. Согласно международным стандартам, лекарство прошло тестирования на животных, и они показали высокую эффективность новинки. Поэтому уже сразу после Рождества в Барселоне вакцину против болезни Альцгеймера протестирует первый пациент (т.е. стартуют клинические испытания на людях). Несмотря на довольно оптимистические прогнозы, научный директор компании Araclon Biotech, Мануэль Сараса (Manuel Sarasa) считает, что лучшее лекарство – это профилактика, так как полностью победить болезнь будет практически невозможно. По его словам, лишь к 2020 году учёные смогут окончательно ответить на вопрос, можно ли победить страшный недуг и его последствия.
2013. Clevermind — iPad приложение для противостояния болезни Альцгеймера
Clevermind — новое бесплатное приложение для iPad, предназначенное для тренировки ума престарелых людей и пациентов с болезнью Альцгеймера. Таким людям очень важно продолжать использовать мозг по назначению, чтобы замедлить деменцию, или даже восстановить умственные способности. Приложение вовлекает человека в различные умственные активности — социальные сети, новости, ежедневные задачи. Причем, в него встроен голосовой помощник, который организует взаимодействие в форме диалога.
2013. IT-звезды хотят решить медицинские проблемы. С помощью денег
Основатель Facebook Марк Цукерберг, основатель Google Сережа Брин, владелец Mail.ru Юрий Мильнер и председатель совета директоров Apple Арт Левинсон решили организовать премию Breakthrough Prize за научные достижения в сфере биомедицины. Ежегодно 5 ученых или команд, которые сделают наибольший вклад в усовершенствование лечения рака, болезни Паркинсона, Альцгеймера и других тяжелых заболеваний, будут получать по $3 млн. В этом году — акция. Приз неожиданно получили сразу 11 человек. Ну что ж, денежная стимуляция ученых — это конечно хорошо, но хотелось бы, чтобы компании этих техно-звезд тоже уделяли больше внимания медицине. Напомним, что Google практически единственный свой медицинский проект Google Health — закрыл. Хотя Google мог бы направить подконтрольный ему искусственный интеллект на решение медицинских проблем, как это делает IBM. Apple хоть и поставляет iPad для клиник, но никак не развивает огромный потенциал iPhone в качестве персонального медицинского гаджета. ***
2013. Америка поборется с Европой за мозг
Пару недель назад Еврокомиссия одобрила финансирование масштабного проекта по созданию модели головного мозга (в размере более 1 млрд евро). И США теперь ничего не остается, кроме как создать такой-же свой проект. Иначе лучшие американские умы побегут в Европу, туда где им предложат больше денег. А значит, Европа получит стратегическое преимущество в изучении мозга. Вы думаете, ну и что? Но представьте, если вдруг европейцы научатся лечить болезни Альцгеймера и Паркинсона в то время, как в США медики будут далеки от этого. Представьте, насколько велик этот рынок, и какие финансы сразу потекут в Европу. В общем, Барак Обама предложил выделить 3 млрд долларов на проект под названием Brain Activity Map (теперь дело за сенатом). Американцы уже хвастаются, что в отличии от европейского проекта, который ставит целю получить «статическую» карту мозга, их проект попробует изучить мозг в динамике, т.е. понять, как именно он работает.
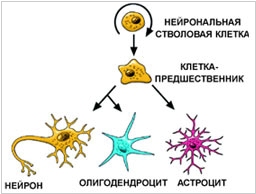
2012. Ученые научились превращать стволовые клетки в нейроны
Хотя большинство людей знает, что нервные клетки не восстанавливаются, на самом деле — они не только восстанавливаются, но уже и искусственно производятся. Разумеется, из стволовых клеток. Группа биологов из Имперского колледжа Лондона обнаружила, что гормон активин (управляющий менструальным циклом женщин и сперматогенезом мужчин) может превращать заготовки нейронов из эмбриональных стволовых клеток в нервные клетки. Ученые вырастили несколько зародышей мыши и извлекли из них стволовые клетки — предшественники нейронов. Потом добавили в них активин и через несколько дней стволовые клетки превратились во взрослые нейроны. Ученые на этом не остановились и вставили полученные нейроны в двигательную кору мозга мыши. Через месяц нервные клетки успешно интегрировались в мозг грызуна, исполняя роль вставочных нейронов, повреждение которых является одной из причин аутизма, шизофрении и эпилепсии. Биологи полагают, что кроме этих заболеваний, их методика восстановления нейронов поможет справиться и с болезями Альцгеймера и Паркинсона.
2011. Brainsway тестирует технологию магнитной стимуляции мозга для лечения Болезни Альцгеймера
Израильская компания Brainsway создала аппарат для лечения заболеваний головного мозга. Технология, на которой он основан, называется глубокой транскраниальной магнитной стимуляцией. Внешний вид устройства напоминает шлемы. В нем находится несколько электромагнитов, которыми управляет компьютер. Они излучают сигналы, направляемые в специальные зоны в головном мозге. Импульсы стимулируют мозговую деятельность и влияют на развитие болезни. Brainsway уже провела ряд успешных испытаний прибора для лечения депрессии, эпилепсии, синдрома расстройства внимания. Теперь очередь дошла до болезни Альцгеймера. В тестировании приняли участие 24 человека, при этом пациенты, прошедшие стимуляцию мозга через 8 недель показали ощутимое улучшение когнитивных способностей по сравнению с теми, которые не проходили данную процедуру. При этом отмечается полное отсутствие побочных эффектов.
источник