В современном мире болезнь Альцгеймера представляет серьезную проблему и занимает четвертое место среди смертельных недугов.
Впервые описал заболевание знаменитый немецкий психиатр Алоис Альцгеймер, в честь него и назвали болезнь.
Чаще всего недуг поражает пациентов старше 60 лет. Лечением болезни занимаются психиатры и неврологи.
Каковы симптомы болезни Альцгеймера, можно ли вылечить заболевание, как и чем лечить недуг в домашних условиях, в чем заключается лечение?

До сих пор не определена точная причина возникновения слабоумия. Общепризнанным является наследственный фактор.
Кроме этого, заболевание может возникнуть вследствие различных травм, воспалительных заболеваний мозга.
Недуг имеет органическую природу. Токсический белок (бета-амилод) откладывается между нейронами клеток головного мозга.
Появляются амилоидные бляшки, разрушающие связи между нейронами. В клетках образуются нейрофибрилляные клубочки, которые провоцируют полное отмирание клетки.
Еще один участник разрушающего процесса — липопротеин АроЕ.
К сожалению, на сегодняшний день не существует средств, способных вылечить деменцию полностью.
Есть препараты, которые разрушают нейрофибриллярные клубочки и препятствуют образованию бляшек. Однако, их эффективность слишком низкая.
Кроме того, генные мутации не позволяют остановить разрушительный процесс.
Поэтому лечение болезни Альцгеймера носит симптоматический характер, направлено на сохранение интеллектуальных навыков как можно дольше.
Терапия позволяет оттянуть наступление последней стадии болезни, сохранить человеку способность обслуживать себя самому.
О лечении болезни Альцгеймера расскажет видео:
Для успешного лечения заболевания проводится полная диагностика, чтобы определить стадию и распространение болезни.
Терапия включает в себя медикаментозное лечение и психологическую помощь.
Какой врач лечит болезнь Альцгеймера? Лечением занимаются неврологи и психиатры.
Кроме того, необходимо корректировать сопутствующие патологии (болезни сердца, щитовидки), от этого зависит положительный исход лечения.
Сложности этого метода в том, что организм пожилого пациента ослаблен и слишком восприимчив к лекарствам. Поэтому назначать препараты нужно с осторожностью, начиная с маленьких доз, постепенно корректируя схему лечения.
В психиатрии препараты для лечения болезни Альцгеймера делятся на следующие группы:
Ингибиторы холинэстеразы. Данная группа средств повышает уровень медиатора ацетилхолина, поэтому звмедляется патологический процесс в мозге. Это такие лекарства, как:
- Галантамин. Оказывает влияние на повышение внимания и памяти. Обладает довольно слабой токсичностью, хорошо переносится больными;
- Донепезил. Считается наиболее эффективным среди всех препаратов. Скорость ингибирования холинэстеразы повышается в 1000 раз быстрее, чем при использовании других лекарств;
- Ревастигмин. Применяется при сильно прогрессирующем течении болезни.
- Оланзапин;
- Клозепин;
- Рисперидон;
- однако, при острых психических состояниях (галлюцинации, бред) применяют Галоперидол.
Традиционно применяют Церебролизин и Актовегин. Эти средства улучшают мозговое кровообращение, способствуют снабжению клеток мозга кислородом.
Эффективность лечения достигается за счет длительного применения препаратов. Первые улучшения можно заметить по прошествии нескольких недель.
Среди новых методов лечения — применение стволовых клеток. Поврежденные клетки замещаются здоровыми, функции мозга восстанавливаются. Однако, этот метод является довольно дорогим и еще до конца не изученным.
Ингибиторы ацетилхолина (Донепезил), Мемантин и успокоительные при болезни Альцгеймера:
Применение народных методов оправдано в сочетании с медицинскими препаратами. Как моносредство они бесполезны.
Какими травами хорошо лечить болезнь Альцгеймера? На начальном этапе средства народной медицины могут слегка замедлить прогрессирование патологии:

Из витаминов принимают добавку — соевый лецитин. Он улучшает работу головного мозга.
Кроме того, полезно употреблять крепкий чай и кофе. Также хороший эффект дает постоянный прием Омега-3.
Важно! Доказано, что употребление трех чашек натурального кофе в день снижает риск деменции в несколько раз.
Кофе и болезнь Альцгеймера:
Как еще бороться с болезнью Альцгеймера? В настоящее время предпринимаются попытки найти эффективные и безопасные методы борьбы с недугом.

Однако, этот метод является спорным. Как самостоятельное средство его применять не рекомендуют, так как деменция является следствием органического поражения клеток, восстановить разрушительный процесс данному аппарату не под силу.
Применение психотерапевтических методик на начальном этапе значительно облегчает состояние больного и тормозит процесс развития болезни Альцгеймера.
Психологическая помощь оказывается в виде:
- арттерапии;
- лечения музыкой;
- обеспечения присутствия.
Выполнение различных умственных упражнений (решение задач, разучивание стихов, разгадывание кроссвордов, чтение книг).
Поможет ли логопед при болезни Альцгеймера? Да, при нарушении речи понадобится помощь логопеда.
Большое значение имеет психологическая поддержка близких. Важно хвалить больного за любые достижения, подбадривать.

Родственникам нужно смириться с тем, что близкий человек уже никогда не стане прежним. Нельзя раздражаться, обижаться на него.
Если больной уже не может самостоятельно себя обслуживать, это придется делать близким, либо прибегнуть к помощи сиделки.
Болезнь Альцгеймера — необратимый процесс. Она неизбежно будет прогрессировать. При отсутствии адекватного лечения деградация личности и смерть больного произойдет намного быстрее.
Излечима ли болезнь Альцгеймера? Полностью вылечить таких больных современная медицина не в состоянии.
Лечение направлено на продление начальной стадии, сохранение интеллектуальных навыков на как можно более долгий период.
Эффективная терапия сочетает в себе применение современных медицинских препаратов, средств народной медицины и методов психологической помощи.
Успех лечения зависит от правильно подобранных комплексных методик.
источник
д.м.н. Балашов А.М. Московский НИИ психиатрии Росздрава РФ
НПВС являются на сегодняшний день, вероятно, самыми применяемыми лекарствами, доступными населению. Они отпускаются из аптек как по назначению врача, так и без рецепта. Широкое распространение НПВС обусловлено их эффективностью в подавлении таких общепатологических феноменов, как воспалительные реакции или болевой синдром различного генеза.
Необходимо отметить, что вначале не существовало четких причин для исследования возможной терапевтической значимости НПВС при болезни Альцгеймера (БА), и исходные наблюдения были в определенной мере случайными.
Не задаваясь целью выявить возможную эффективность НПВС в терапии БА, авторы первых наблюдений, скрупулезно фиксировали анамнез и обратили внимание на низкую частоту встречаемости этой патологии у пациентов с ревматоидным артритом по сравнению с общепопуляционными показателями (Beard C.M. et al., 1991). Уже следующее наблюдение, опубликованное в научной литературе, более точно формулировало проблему, констатируя возможное положительное влияние НПВС при БА (Poza-Aldea J.J., Marti-Masso J.F., 1992), а вскоре читателям была представлена гипотеза о новом терапевтическом направлении (Schnabel J., 1993). Повторимся, первоначально клинические испытания с привлечением методологии доказательной медицины не проводились, и работы имели исключительно эмпирический характер (Aisen P.S., 1996). Рассмотрим их результаты более подробно.
Первое клиническое испытание НПВС у пациентов с БА было выполнено с использованием дизайна двойного слепого, плацебо контролируемого исследования. Индометацин назначали в суточной дозе 100–150 мг и регистрировали когнитивные функции в батарее тестов. В группе пациентов, леченых НПВС, с умеренной и средней степенью выраженности проявлений БА ухудшение когнитивных функций в течение полугодового наблюдения было выражено в 6 раз меньше, и различие с группой «плацебо» было статистически значимым (Rogers J. et el., 1993). К середине 90-х годов ХХ в. без существенного теоретического обоснования неоднократно предпринимались попытки изучения опыта клинического применения стероидных и нестероидных противовоспалительных препаратов (в т.ч., сравнительного характера) для купирования проявлений БА. Результаты полутора десятков неконтролируемых исследований суммированы в обзоре Breitner J.C. (1996), в котором сделано заключение о предпочтительности применения НПВС по сравнению с препаратами на основе глюкокортикоидных гормонов.
Дальнейшие работы имели преимущественно эпидемиологическую направленность: например, с применением катамнестических подходов было выполнено исследование на 1686 пациентах с БА, принимавших НПВС, при этом авторы не рассматривали особенности действия конкретных препаратов (Stewart W.F. et al., 1997). Оказалось, что протективный эффект НПВС зависел от длительности приема лекарств: совокупный относительный риск развития БА в группе лиц, принимавших НПВС в течение двух и более лет, оценивался величиной 0,4 по сравнению с 0,65 у тех, кто принимал НПВС менее 2 лет. На риск развития БА не влияли препараты на основе ацетамифена (парацетамола), в действии которого выражен обезболивающий компонент, а противовоспалительные свойства редуцированы. Весьма сходные данные получены при длительном исследовании, проведенном в Балтиморе (Baltimore Longitudinal Study of Aging); в результирующей работе приведены близкие цифры, а использование НПВС рассматривается в качестве предиктора относительно низкого риска развития БА (Zonderman A.B., 2005). Аналогичные результаты были опубликованы в 2002 г., при этом установлено, что, в отличие от НПВС, антагонисты гистаминовых Н2-рецепторов, также демонстрирующие противовоспалительную активность, не являются эффективными (Zandi P.P. et al., 2002).
В законченном в 2002 г. пилотном рандомизированном контролируемом испытании НПВС нимесулида исследовали его эффективность в качестве потенциального средства терапии БА (Aisen P.S. et al., 2002). Сорок пациентов, находившихся на лечении ингибиторами холинэстеразы, получали нимесулид (100 мг per os 2 раза в день) или плацебо в течение 12 нед при двойном слепом контроле. В течение последующих 12 нед НПВС назначали всем пациентам, а те, кто хорошо переносил препарат и чувствовал улучшение, были включены в следующую 2-летнюю фазу испытаний. По результатам исследования было сделано заключение, что, в противоположность длительному применению, кратковременная терапия нимесулидом не приводит к значительным изменениям скорости ухудшения показателей когнитивного дефицита, общего клинического состояния, жизненной активности, аффективного статуса или поведения. Вероятно, назначение нимесулида пациентам с БА должно осуществляться в течение длительного времени.
В популяционном исследовании, проведенном в Швеции, в котором принимали участие 702 пациента старше 80 лет с БА, изучали зависимость развития когнитивных нарушений от приема НПВС, назначаемых с целью профилактики после ишемического инсульта или продолжительных приступов стенокардии (Nilsson S.E. et al., 2003). Установлено, что прием высоких доз ацетилсалициловой кислоты статистически значимо уменьшает распространенность и прогрессирование когнитивных нарушений. Назначение низких доз ацетилсалициловой кислоты, а также парацетамола или D-пропоксифена приводило к сходным протективным реакциям, не достигавшим, однако, статистической значимости.
Весьма впечатляющее проспективное исследование было закончено в 2001 г. (Bas A. et al., 2001). Авторами представлены результаты продолжительного наблюдения за 6989 субъектами старше 55 лет, у которых на момент включения в программу не выявлялись признаки БА. Среди исследуемых были выделены четыре группы: 1-я — не употреблявшие НПВС и три группы употреблявших НПВС: 2-я — короткое время (менее 1 мес за весь период наблюдения); 3-я — промежуточное время (от 1 мес до 2 лет) и 4-я — более 2 лет. Факт употребления препаратов подтверждался документально выписками из аптек. В течение выполнения программы (средний срок наблюдения — 6,8 лет) БА сформировалась у 293 пациентов. Относительно общей популяции риск развития этой патологии составил 0,95 — в группе 2; 0,83 — в группе 3 и 0,20 — в группе 4;. при этом не была установлена зависимость этих показателей от возраста испытуемых. Из представленных данных следует строгий вывод о позитивном профилактическом влиянии НПВС на возникновение БА.
Необходимо отметить, что в литературе также представлены результаты клинических испытаний с негативным результатом; таковы исследования напроксена и селективного ингибитора ЦОГ-2 рофекоксиба (Aisen P.S. et al., 2003, Reines S.A. et al., 2004), диклофенака в комбинации с мизопростолом (Scharf S. et al., 1999).
В наиболее авторитетной и известной качественным мета-анализом кохрейновской базе данных суммированы и проанализарованы результаты всех плацебо контролируемых исследований ибупрофена при БА (Tabet N., Feldman H., 2003). Авторы делают вывод о целесообразности применения этого НПВС для коррекции когнитивных нарушений. Вместе с тем, аналогичный анализ, проведенный теми же авторами в отношении другого сходного препарата индометацина, привел к отрицательным рекомендациям (Tabet N., Feldman H., 2002).
Результаты приведенных клинических исследований спровоцировали научную дискуссию, развивающуюся до сегодняшнего дня в двух направлениях: выяснение патогенетической обоснованности использования НПВС при БА и уточнение терапевтической эффективности этих препаратов, в т.ч., их индивидуальной активности. Первому направлению, в основном, посвящены нижеследующие разделы настоящей публикации.
Однако прежде целесообразно охарактеризовать патогенетические механизмы формирования БА. Данные современных научных исследований позволяют полагать, что в патогенезе БА ведущую роль играют нарушения активности ацетилхолиновой системы, главным образом, в коре головного мозга и гиппокампе — областях, участвующих в формировании высших интеллектуальных функций и процессов памяти. Менее известной остается роль нейрохимических этиологических факторов, приводящих к дефициту функционирования холинергических нейронов. Сложность создания ясной патогенетической картины развития БА обусловлена обилием фактов, свидетельствующих о возможной вовлеченности в патологический процесс многочисленных функциональных компонентов нервной системы.
Предполагается, что в качестве причины повреждения ацетилхолиновых нейронов могут выступать хронические воспалительные реакции, оксидативный (гиперпродукция активных форм кислорода) и нитрозилактивный (вызванный образованием реакционноспособных молекул, содержащих азот) стресс (Prasad K.N. et al., 2002). Ранние стадии патологии обусловлены повреждением митохондрий и ингибированием протеасом, тогда как более поздние процессы визуализируются гистологически и характеризуются накоплением и отложением бета-амилоида (Аβ) и образованием сенильных бляшек. Как видно на схеме, помимо Аβ в процессе образования сенильных бляшек принимают участие клубки фибрилл, в свою очередь, формирующиеся из гиперфосфорилированного тау-белка (Hull M.H. et al., 2000).
Схема. Основные патогенетические звенья болезни Альцгеймера (адаптировано из NeuroRx.- 2005.- 2(4).- P. 612–626.)
В основе нарушений функционирования медиаторных систем, главным образом ацетилхолиновых, лежит дегенерация нейронов, в свою очередь, вызванная действием трех факторов: нарушение метаболизма амилоида, воспалительные реакции (которые зависят от амилоидного пути) и накопление извращенных клубочковых форм нейрофибрилл (что обусловлено нарушениями обмена нормального компонента фибрилл — тау-белка). Большинство исследователей главным пусковым патогенетическим механизмом БА полагают амилоид-зависимый путь.
Известно, что белок амилоид представляет собой нормальный компонент плазматических мембран клеток и может подвергаться деградации при помощи двух ферментов: α- и β-секретаз. В первом случае продуктом реакции является непатогенный полипептид — α-предшественник амилоидных пептидов (α-APPs), во втором — более короткий фрагмент — β-предшественник амилоидных пептидов (β-APPs). Остающаяся в мембране после действия β-секретазы часть молекулы может расщепляться далее ферментом γ-секретазой с образованием коротких растворимых пептидов: Аβ-42, Аβ-40 и т.д. (число означает количество аминокислотных остатков в структуре Аβ). Короткие молекулы Аβ способны к агрегации, запуская каскад процессов, приводящих к гибели клеток.
Таким образом, согласно современным представлениям о механизмах развития БА, что поиск потенциальных терапевтических средств следует проводить среди (Zimmermann M. et al., 2005):
— веществ, снижающих гибель нейронов (например, блокаторов NMDA-рецепторов);
— противовоспалительных препаратов нестероидной и, возможно, стероидной природы;
— соединений, активирующих ацетилхолиновую нейротрансмиссию (ингибиторы ацетилхолинэстеразы, активаторы ацетилхолиновых рецепторов);
— антиоксидантов, поскольку перекисные процессы являются одним из главных повреждающих механизмов при воспалении;
— активаторов α-секретазы для сдвига обмена амилоида в сторону α-пути и минимизации образования Аβ;
Из перечисленных групп препаратов к настоящему времени одобрены для клинического применения лишь ингибиторы ацетилхолинэстеразы, к которым в 2004 г. в США присоединился препарат мемантин, представляющий собой блокатор NMDA-рецепторов (Lleo A. et al., 2006). Представители остальных фармакологических групп пока используются только в исследовательских целях. Необходимо отметить, что эффективность фармакотерапии БА находится на очень низком уровне вне зависимости от применяемых препаратов (Frank B, Gupta S., 2005, Jelic V. et al., 2006). Однако вернемся к рассмотрению НПВС.
Противовоспалительное действие НПВС в ЦНС. Экспериментальное подтверждение возможности противовоспалительного действия препаратов основано на общих представлениях об основной мишени для НПВС — ЦОГ, доступность которой для субстрата (арахидоновой кислоты) уменьшается в присутствии этих лекарств (Vane J.R., Botting R.M., 1998).
В модельном исследовании, выполненном на препаратах крови людей 85-летнего возраста были получены данные, которые свидетельствовали об угнетении образования индометацином и ацетилсалициловой кислотой ПГЕ2. Снижение уровня ПГ приводило к уменьшению продукции ИЛ-6, усиленной после первичной стимуляции тромбином или липополисахардами (Bour A.M. et al., 2000).
В экспериментах на животных было установлено, что при введении индометацина на фоне стимуляции липополисахаридами наблюдается супрессия ИЛ-6-зависимой активации высвобождения ПГЕ2. Сдвиг биохимических параметров сопровождается поведенческими реакциями: индометацин в тесте активного избегания обращает амнезию, вызванную липополисахаридами (Ma T.C., Zhu X.Z., 1997). Ибупрофен при пероральном введении восстанавливает нарушенные когнитивные функции у экспериментальных животных. При прекращении приема НПВС эффект не сохраняется (Richardson R.L. et al., 2002).
В различных культурах клеток НПВС (ибупрофен, индометацин, сулиндак) ингибируют образование Аβ-42, максимально — на 80% (Weggen S. et al., 2001). Этот эффект, не связанный с ингибированием ЦОГ, специфичен по отношению именно к этому пептиду, поскольку уровень Аβ-38 увеличивается; вероятно, действие НПВС обусловлено влиянием на фермент гамма-секретазу. Помимо этого, НПВС демонстрируют уникальные свойства по отношению к биофизическим характеристикам Аβ. Они, с одной стороны, ингибируют агрегацию Аβ, в т.ч., вызванную Al 3+ , а с другой — предотвращают образование его складчатой бета-структуры (Thomas T. et al., 2001). Подобные эффекты не наблюдаются при применении других препаратов, использующихся для лечения БА.
Механизмы влияния НПВС на медиаторные системы. Считается, что влияние НПВС на нейромедиаторные и модуляторные системы головного мозга, в основном, опосредовано продуктами метаболизма липидов, изменяющегося вследствие их основного эффекта — ингибирования ЦОГ, имеющей отношение к метаболизму липидов, и в частности, к синтезу ПГ. В ранних исследованиях предполагалось, что эффективность НПВС в отношении того или иного патологического процесса подразумевает вовлеченность ПГ.
Например, с этих позиций рассматривались результаты о том, что индометацин в концентрациях, превышающих 100 мкМ, (но не ацетилсалициловая кислота) в экспериментах in vitro предотвращает дегенерацию нейронов в срезах мозжечка 7-дневных крыс после экспозиции с NMDA (Lehmann A., 1987). Другой представитель НПВС — кеторолак — предотвращает и блокирует электрическую активность нейронов, вызванную NMDA (Sotgiu M.L. et al., 1998).
Иная возможность реализации действия НПВС на рецепторы NMDA проиллюстрирована нейрохимическими исследованиями. При подкожном введении диклофенак обнаруживается в головном мозге и на этом фоне увеличивается концентрация кинуреиновой кислоты в ЦНС, главным образом, в среднем мозге и люмбо-сакральных отделах спинного мозга. Диклофенак опосредованно приводит к уменьшению активности системы возбуждающих аминокислот, что, с одной стороны, патогенетично по отношению к БА, а с другой — может служить объяснением одного из центральных механизмов обезболивающего действия НПВС (Edwards S.R. et al., 2000).
Таким образом, имеются как параклинические данные, так и результаты клинических наблюдений, свидетельствующие о патогенетически обоснованной эффективности НПВС при БА. Справедливости ради следует отметить, что подобно иным фармакотерапевтическим подходам к лечению БА, активность НПВС как препаратов, способствующих обратному развитию болезни, весьма незначительна. Доказанной представляется способность НПВС при длительном применении выражено снижать риск формирования этой патологии. Означает ли это, что адекватной является рекомендация длительного назначения НПВС с указанными целями? Однозначного ответа на этот вопрос пока нет.
Aisen P.S. Inflammation and Alzheimer disease// Mol. Chem. Neuropathol.- 1996.- 28.- P. 83–88.
Aisen P.S. The potential of anti-inflammatory drugs for the treatment of Alzheimer`s disease// Lancet. Neurol.- 2002.- 1.- P. 279–284.
Aisen P.S., Schafer K.A., Grundman M. et al. Effects of rofecoxib or naproxen vs placebo on Alzheimer`s disease progression: a randomized controlled trial// JAMA.- 2003.- 289.- P. 2819–2826.
Aisen P.S., Schmeidler J., Pasinetti G.M. Randomized pilot study of nimesulide treatment in Alzheimer`s disease// Neurology.- 2002.- 58.- P. 1050–1054.
Bas A., Ruitenberg A., Hofman A., Launer L.J., van Duijn C.M., Stijnen T., Breteler M.M.B, Stricker B.H.C. Nonsteroidal Antiinflammatory Drugs and the Risk of Alzheimer`s Disease// New England J. Med.- 2001.- Volume 345.- № 21.- P. 1515–1521.
Beard C.M., Kokman E., Kurland L.T. Rheumatoid arthritis and susceptibility to Alzheimer`s disease// Lancet.- 1991.- Jun. 8.- 337 (8754).- P. 1426.
Bour A.M., Westendorp R.G., Laterveer J.C. et al. Interaction of indomethacin with cytokine production in whole blood. Potential mechanism for a brain-protective effect// Exp. Gerontol.- 2000.- 35.- P. 1017–1024.
Breitner J.C. The role of anti-inflammatory drugs in the prevention and treatment of Alzheimer`s disease// Annu Rev. Med.- 1996.- 47.- P. 401–411.
Cutler N.R., Sramek J.J. Review of the next generation of Alzheimer`s disease therapeutics: challenges for drug development// Prog. Neuropsychopharmacol. Biol. Psychiatry.- 2001.- 25.- P. 27–57.
Edwards S.R., Mather L.E., Lin Y. et al. Glutamate and kynurenate in the rat central nervous system following treatments with tail ischaemia or diclofenac// J. Pharm. Pharmacol.- 2000.- 52.- P. 59–66.
Frank B., Gupta S. A review of antioxidants and Alzheimer`s disease// Ann. Clin. Psychiatry.- 2005.- Oct.-Dec.- 17(4).- P. 269–286.
Hoozemans J.J., Veerhuis R., Rozemuller A.J., Eikelenboom P. Non-steroidal antiinflammatory drugs and cyclooxygenase in Alzheimer`s disease// Curr. Drug Targets.- 2003.- 4.- P. 461–468.
Hull M.H., Fiebich B.L., Lieb K. Strategies to delay the onset of Alzheimer`s disease// EXS. 2000.- 89.- P. 211–225.
Jelic V., Kivipelto M., Winblad B.Clinical trials in mild cognitive impairment: lessons for the future// J. Neurol. Neurosurg. Psychiatry.- 2006.- Apr.- 77(4).- P. 429–438.
Lehmann A. Pharmacological protection against the toxicity of N-methyl-D-aspartate in immature rat cerebellar slices// Neuropharmacology.- 1987.- 26.- P. 1751–1761.
Lleo A., Greenberg S.M., Growdon J.H. Current pharmacotherapy for Alzheimer`s disease// Annu. Rev. Med.- 2006.- v. 57.- P. 513–533.
Ma T.C., Zhu X.Z. Suppression of lipopolysaccharide-induced impairment of active avoidance and interleukin-6-induced increase of prostaglandin E2 release in rats by indometacin// Arzneimittelforschung.- 1997.- 47.- P. 595–597.
Mackenzie I.R. Postmortem studies of the effect of anti-inflammatory drugs on Alzheimer-type pathology and associated inflammation// Neurobiol. Aging.- 2001.- 22.- P. 819–822.
Maillard M., Burnier M. Comparative cardiovascular safety of traditional nonsteroidal anti-inflammatory drugs// Expert Opin. Drug Saf.- 2006.- 5(1).- P. 83–94.
Nilsson S.E., Johansson B., Takkinen S. et al. Does aspirin protect against Alzheimer`s dementia? A study in a Swedish population-based sample aged >or = 80 years// Eur. J. Clin. Pharmacol.- 2003.- 59.- P. 313–319.
Poza-Aldea J.J., Marti-Masso J.F. Chronic NSAID consumption and Alzheimer`s disease// Neurologia.- 1992.- 7(2).- P. 85.
Prasad K.N., Cole W.C., Prasad K.C. Risk factors for Alzheimer`s disease: role of multiple antioxidants, non-steroidal anti-inflammatory and cholinergic agents alone or in combination in prevention and treatment// J. Am. Coll. Nutr.- 2002.- 21.- P. 506–522.
Reines S.A., Block G.A., Morris J.C. et al. Rofecoxib: no effect on Alzheimer`s disease in a 1-year, randomized, blinded, controlled study// Neurology.- 2004.- 62.- P. 66–71.
Richardson R.L., Kim E.M., Shephard R.A. et al. Behavioural and histopathological analyses of ibuprofen treatment on the effect of aggregated Abeta(1–42) injections in the rat// Brain. Res.- 2002.- 954.- P. 1–10.
Rogers J., Kirby L.C., Hempelman S.R. et al. Clinical trial of indomethacin in Alzheimer`s disease// Neurology.- 1993.- 43.- P. 1609–1611.
Scharf S., Mander A., Ugoni A. et al. A double-blind, placebo-controlled trial of diclofenac/misoprostol in Alzheimer`s disease// Neurology.- 1999.- 53.- P. 197–201.
Schnabel J. New Alzheimer`s therapy suggested// Science.- 1993.- 260 (5115).- P. 1719–1720.
Sotgiu M.L., Biella G., Formaglio F., Marchettini P. Central effect of ketorolac involving NMDA receptors activity// Brain. Res.- 1998.- 813.- P. 223–226.
Stewart W.F., Kawas C., Corrada M., Metter E.J. Risk of Alzheimer`s disease and duration of NSAID use// Neurology.- 1997.- 48.- P. 626–632.
Tabet N., Feldman H. Ibuprofen for Alzheimer`s disease// Cochrane Database Syst. Rev.- 2003.- 2.- CD004031.
Tabet N., Feldman H. Indomethacin for the treatment of Alzheimer`s disease patients// Cochrane Database Syst. Rev.- 2002.- 2.- CD003673.
Thomas T., Nadackal T.G., Thomas K. Aspirin and non-steroidal anti-inflammatory drugs inhibit amyloid-beta aggregation// Neuroreport.- 2001.- 12.- P. 3263–3267.
Vane J.R., Botting R.M. Mechanism of action of antiinflammatory drugs// Int. J. Tissue React.- 1998.- 20.- P. 3–15.
Weggen S., Eriksen J.L., Das P. et al. A subset of NSAIDs lower amyloidogenic Abeta42 independently of cyclooxygenase activity// Nature.- 2001.- 414.- P. 212–216.
Zandi P.P., Anthony J.C., Hayden K.M. et al. Reduced incidence of AD with NSAID but not H2 receptor antagonists: the Cache County Study// Neurology.- 2002.- 59.- P. 880–886.
Zimmermann M., Gardoni F., Di Luca M. Molecular rationale for the pharmacological treatment of Alzheimer`s disease// Drugs Aging.- 2005.- v. 22.- Suppl 1.- P. 27–37.
источник
В ревматологии НПВС наиболее часто используются по следующим показаниям:
- РА
- Артрит и серозит при СКВ
- Артрит при ССД
- Артрит при синдроме Шегрена
- Артрит и серозит при смешанном заболевании соединительной ткани
- Остеоартрит
- Анкилозирующий спондилит
- Синдром Рейтера
- Псориатический артрит
- Микрокристаллический артрит
- Бурсит, тендинит, теносиновит
- Артрит при васкулитах
- Ювенильный хронический артрит
Кроме того, НПВС часто используют для уменьшения выраженности менструальных спастических реакций; они способствуют более быстрому закрытию ductus arteriosus; НПВС нашли применение при воспалительных офтальмологических заболеваниях, шоке, периодонтите, спортивных травмах и лечении осложнений химиотерапии злокачественных новообразований. Имеются сообщение о антипролиферативном действии аспирина и НПВС на слизистую кишок, что позволило обсуждать потенциальную возможность их применения у больных со злокачественными новообразованиями толстой кишки (M. J. Thun и соавт., 1991; R. F. Logan и соавт., 1993).
По данным F. M. Giardello и соавт. (1993), сулиндак подавляет развитие аденоматозного полипоза кишечника. Недавно обнаружена клиническая эффективность индометацина при болезни Альцгеймера (J. Rogers и соавт., 1993). Особенно широко НПВС используются в лечении мигрени (K. M. A. Welch, 1993). Полагают, что они являются средством выбора у больных с умеренными или выраженными мигренозными атаками. Например, в двойном слепом контролируемом исследовании было показано, что напроксен достоверно уменьшает тяжесть и продолжительность головных болей и фотофобии, и что он более эффективен в этом отношении, чем эрготамин. Сходный эффект дает аспирин и другие НПВС.
Для достижения более выраженного действия в отношении тошноты и рвоты рекомендуется комбинировать НПВС с метоклопрамидом, который ускоряет абсорбцию препаратов. Для быстрого купирования мигренозных приступов рекомендуется использовать кеторолак, который можно вводить парентерально. Предполагается, что эффективность НПВС при мигрени связана с их способностью, ингибируя синтез ПГ, снижать интенсивность нейрогенного воспаления или, интерферируя с серотонином, уменьшать выраженность сосудистого спазма.
Несмотря на сходство химических свойств и основных фармакологических эффектов различных НПВС, у отдельных больных одним заболеванием (например РА) или при разных ревматических заболеваниях наблюдаются существенные колебания в «ответе» на тот или иной препарат (E. C. Huskisson и соавт., 1976). Действительно, на популяционном уровне достоверных различий между аспирином и другими НПВС при РА не выявлено (L. A. Heller и соавт., 1985), однако они становятся очевидными при анализе эффективности различных НПВС у отдельных больных (T. Pincus и соавт., 1989). Это диктует необходимость индивидуального подбора НПВС для каждого больного (Н. В. Бунчук, 1994).
Выбор НПВС является, как правило, эмпирическим и во многом основывается на личном опыте врача и прошлом опыте больного. Существует точка зрения о целесообразности в начале лечения использовать наименее токсичные препараты, к которым в первую очередь относятся производные пропионовой кислоты. Необходимо постепенно титровать дозу НПВС до эффективной, но не превышающей максимально допустимую, в течение 1-2 нед. и при отсутствии эффекта попытаться использовать другой или другие препараты. Назначение простых анальгетиков (парацетамола) позволяет уменьшить потребность в НПВС. Рекомендуемые дозы наиболее широко распространенных в клинической практике НПВС представлены в таблице.
источник
Медикаментозное лечение является основным приемом борьбы с дегенеративными процессами в тканях головного мозга при болезни Альцгеймера. Данная форма сенильной деменции неизлечима. Все действия медиков сводятся к замедлению прогрессирования патологии, купированию основных и сопутствующих симптомов, улучшению общего состояния больного. Более чем в 90% случаев недуг поражает людей старше 60-65 лет. В таком возрасте прием любых медикаментов представляет дополнительную угрозу для организма. Чтобы добиться максимального эффекта и минимизировать риски, подбором препаратов для лечения болезни Альцгеймера должен заниматься профессионал.

Лечение при синдроме Альцгеймера требует не только прямого воздействия на дегенеративные изменения в головном мозге. Патология сопровождается целым рядом органических расстройств, усугубляющих ситуацию. Со всем этим не может справиться одно лекарство, подход должен быть комплексным. Повышенное внимание уделяется коррекции явлений, угнетающих метаболизм во всем организме, которые приводят к снижению функциональности отделов ЦНС.
Обязательные моменты медикаментозного воздействия при синдроме Альцгеймера:
- борьба с нарушениями в работе сердца, сосудов, органов дыхания;
- снижение патологически повышенного уровня сахара, вредного холестерина, липидов в крови;
- нормализация гормонального фона при поражении желез внутренней секреции;
- повышение функциональности печени и почек;
- насыщение организма витаминами, минералами, полезными микроэлементами.
Результатом комплексного подхода становится нормализация питания нейронов, стимуляция восстановления их структуры. Все это приводит к более медленному увеличению площади атрофии, повышению работоспособности нервной ткани. В тяжелых случаях подход дополняется применением средств патогенетического действия, что приводит к угнетению симптомов болезни Альцгеймера, хоть и не избавлению от нее.
Дефицит нейромедиатора ацетилхолина способствует развитию и прогрессированию дегенеративных изменений в нервных тканях. При недостатке этого органического соединения атрофические процессы распространяются быстрее, усугубляя состояние больного. Подобные реакции становятся последствием сбоя выработки нейромедиатора или его ускоренным разрушением на фоне избытка ацетилхолинэстеразы. По этой причине в перечень основных лекарств при болезни Альцгеймера входят ингибиторы ацетилхолинэстеразы, а также препараты на основе мемантина.
С каждым годом в фармакологии появляются новые препараты такого профиля, что повышает шансы на подбор подходящего продукта для каждого пациента.
Сегодня наиболее активно применяются медикаменты селективного действия второго поколения.
В зависимости от типа основного вещества они блокируют ферменты, расщепляющие ацетилхолин, активируют рецепторы с целью повышения концентрации внимания. Обычно такие составы включают в схему лечения при стремительном прогрессировании патологии. Обилие лекарственных форм и типов препаратов позволяет подобрать продукт в соответствии с особенностями состояния больного.
Эффективность медикаментов в среднем составляет 70%, но важную роль при этом играет индивидуальная реакция на продукт. Для получения максимально выраженного результата подбором препаратов патогенетического действия для лечения болезни Альцгеймера должен заниматься врач. При этом учитывается не только переносимость состава, но и ответ организма в виде клинического улучшения. Для оценки терапевтического действия выбранного медикамента его надо принимать непрерывно не менее 3 месяцев в предельном переносимом объеме. В случае смены продукта на другой надо сделать перерыв от 3 до 7 дней в зависимости от типов лекарств.

Введение препаратов данной группы в схему терапии обычно означает их пожизненное использование. По этой причине важно подобрать удобную лекарственную форму состава. Это не всегда таблетки. Некоторые производители предлагают питьевые растворы и даже пластыри. В большинстве случаев в течение года после старта терапии держится выраженный лечебный эффект, затем прогрессирование дистрофии тканей возобновляется.
Использование ингибиторов ацетилхолинэстеразы проводится по таким правилам:
- назначать продукты может только специалист. Средства применяются лишь при условии постоянного внешнего контроля терапии медицинскими работниками или родственниками больного;
- любые побочные эффекты должны быть оценены лечащим врачом;
- прием таких составов одновременно с НПВС или медикаментами, снижающими частоту сердечных сокращений, запрещен;
- лекарства несовместимы со спиртными и тонизирующими напитками.
Прекращение применения медикаментов возможно только с разрешения врача. Обычно это делается на стадии тяжелой деменции, когда лекарства уже не помогают. В остальных случаях, отказываясь от препаратов, можно спровоцировать резкое прогрессирование дегенеративных процессов в головном мозге. Результатом станет заметное обострение клинической картины.
Принимать ингибиторы ацетилхолинэстеразы нужно пожизненно, поэтому наличие побочных реакций на такие препараты недопустимо. Избавиться от болезни Альцгеймера невозможно, но есть шанс ослабить выраженность симптомов, замедлить дегенеративные процессы. Аптеки предлагают самые разные медикаменты, среди которых всегда можно выбрать эффективный и не вызывающий негативных последствий.
Распространенные побочные реакции на прием ингибиторов ацетилхолинэстеразы:
- часто – тошнота и рвота, головокружение, ухудшение аппетита;
- редко – головные боли, дискомфорт в животе, тремор рук, обильное выделение пота, утомляемость, сонливость или повышенная возбудимость;
- единичные случаи – проблемы со сном, депрессивные расстройства, обмороки, галлюцинации, скачки АД, язвенные поражения слизистой органов пищеварения.
Обычно такие проявления становятся очевидны сразу после начала терапии. Иногда они возникают на фоне резкого повышения дозировки ранее переносимого препарата.

Перед началом приема препаратов для лечения деменции необходимо убедиться, что нет запретов или ограничений по их использованию. Абсолютными противопоказаниями называют непереносимость конкретных продуктов, тяжелые поражения печени и/или почек. Из-за особенностей действия составы не назначают при состояниях, когда стимуляция периферических холинэргических рецепторов по каким-то причинам представляет опасность.
Относительные запреты по использованию ингибиторов ацетилхолинэстеразы:
- хронические патологии респираторной системы с обструкцией дыхательных путей, бронхиальная астма;
- нарушение сердечного ритма;
- нестабильная стенокардия;
- прием препаратов, замедляющих сердечный ритм;
- обструкция мочевыводящих протоков, период восстановления после перенесенных хирургических вмешательствах на органах выделения;
- эпилепсия и/или гиперкинезы в анамнезе;
- непроходимость кишечника;
- язвенные поражения слизистой оболочки органов пищеварения;
- наркоз.
При язвенных поражениях слизистой оболочки органов пищеварения ингибиторы ацетилхолинэстеразы не применяют.
Возможность лечения болезни Альцгеймера ингибиторами ацетилхолинэстеразы при этих состояниях зависит от ряда моментов. Целесообразность проведения лекарственной терапии устанавливает врач.
Вылечить болезнь Альцгеймера нельзя даже при использовании самых эффективных и дорогих средств, запуске терапии на ранних стадиях патологии. Никакие подходы не позволяют добиться регресса дегенеративного процесса, полной остановки его распространения. Зато при правильном подходе к терапии есть шанс существенно замедлить развитие состояния, подарить пациенту 10-15 лет полноценной жизни.
Каждая из стадий болезни Альцгеймера требует проведения специфической терапии:
- преддеменция – достаточно применения антидепрессантов для нормализации психоэмоционального фона пациента. В зависимости от симптомов и в качестве альтернативной терапии врач назначает ноотропы, «Глицин», блокаторы кальциевых каналов, «Актовегин». Положительное влияние на мозг оказывает экстракт гинкго билоба;
- ранняя и средняя степени слабоумия – для борьбы с плохим настроением применяют нетипичные антидепрессанты, нейролептики. Патогенетическая терапия основывается на ингибиторах ацетилхолинэстеразы. Адекватной альтернативой могут выступать «Пирибедил», «Винпоцетин», «Пентоксифиллин»;
- тяжелая деменция – основным лекарственным препаратом становится «Мемантин».
Изменения в схему терапии должны вноситься лечащим врачом. Параллельный прием любых препаратов надо согласовывать с неврологом, чтобы не спровоцировать осложнений или побочных реакций, не снизить эффективность основного лечения.
Постепенная атрофия отделов головного мозга, которая развивается на фоне дегенеративных процессов, приводит к появлению ряда неприятных последствий. Если с ними не бороться отдельно, это приведет к снижению качества жизни пациента с болезнью Альцгеймера. Исследования показывают, что это нередко становится причиной снижения эффективности базовой медикаментозной терапии. Помимо антидепрессантов невролог может назначить больному еще ряд лекарственных средств в соответствии с особенностями его состояния.
Хороший эффект дает употребление «Глицина» и его многочисленных аналогов. Продукт стимулирует церебральное кровообращение, положительно сказывается на настроении пострадавшего.
«Карбамазепин» способен вернуть больному жажду жизни и интерес к любимым делам, избавить от апатии. При галлюцинациях или признаках бреда показаны нейролептики, транквилизаторы. Все перечисленные продукты следует принимать только в случае необходимости, а не с профилактическими целями. Из-за обилия противопоказаний и побочных эффектов при неадекватном использовании они могут нанести больше вреда, чем пользы.
Аптеки предлагают десятки препаратов, способных облегчить течение болезни Альцгеймера, влияя на саму причину дегенеративных процессов. Каждый из продуктов обладает своими особенностями и преимуществами, поэтому решение в пользу одного из них должен принимать врач. У большинства средств есть синонимы или аналоги, но даже их применение нельзя начинать без разрешения специалиста.
Уникальное средство, которое нормализует обмен глутамата и не допускает внутренней интоксикации нейронов. На сегодня является единственным продуктом, показывающим высокую эффективность на последней стадии болезни Альцгеймера. При комбинировании с ингибиторами ацетилхолинэстеразы результативность терапии многократно возрастает. Состав хорошо переносится пациентами, но запрещен к использованию при нарушении работы почек. На фоне эпилепсии терапия проводится с особой осторожностью. В силу специфики действия время приема лекарства должно подбираться индивидуально.
Медикамент представлен капсулами и раствором для приема внутрь, а также пластырями и пленками для трансдермального действия. Последняя лекарственная форма очень удобна в случаях, когда у родственников пациента нет возможности постоянно быть рядом. Дозировка подбирается индивидуально, может корректироваться по ходу терапии. При этом изменение режима дозирования должно меняться не чаще, чем раз в неделю.

Средство допускается к использованию при всех стадиях болезни Альцгеймера, а также других формах старческого слабоумия. Производитель предлагает лекарство в таблетках и растворе для приема внутрь. Состав обладает минимальным перечнем противопоказаний, редко вызывает негативную реакцию организма. Лечебные дозы подбирают индивидуально. Медикамент рекомендуется принимать в вечернее время. Изменение режима дозирования должно проводиться не чаще раза в месяц. У лекарства есть ряд более дешевых аналогов.
Продукт проявляет свою эффективность при борьбе с легкой и средней степенью болезни Альцгеймера. Нередко состав применяют для лечения хронических проблем с церебральным кровообращением. Прием средства не только купирует проявления дегенеративных процессов в головном мозге, но и повышает концентрацию внимания. Медикамент отличается минимальным уровнем токсичности, его разрешено давать даже беременным женщинам.
Список лекарств, используемых на фоне болезни Альцгеймера, нередко основывается на альтернативных продуктах. Обычно такие медикаменты применяют на более легких стадиях патологии, когда к патогенетическому лечению приступать еще рано. Они же могут быть введены в качестве замены неэффективным средствам или в случае их непереносимости.
Группы вспомогательных препаратов для лечения болезни Альцгеймера:
- составы, стимулирующие передачу импульсов между нейронами;
- продукты для нормализации кровообращения в головном мозге путем воздействия на самые мелкие сосуды, изменения состава и степени вязкости крови;
- экстракт гинкго билоба, оказывающий общее благоприятное воздействие на ткани головного мозга;
- ноотропы натурального и синтетического происхождения;
- медикаменты на основе пептидов, аминокислот;
- блокаторы кальциевых каналов, альфа-адреноблокаторы.
Традиционную терапию все чаще подкрепляют применением средств народной медицины. Для стимулирования работы мозга показано употребление напитков на основе пустырника, корня женьшеня.

Препараты, предназначенные для лечения болезни Альцгеймера, хоть и являются универсальными, могут быть использованы в разных схемах. Особенности тактики терапии зависят от возраста и пола пациента, степени поражения ЦНС, симптоматики, наличия усугубляющих ситуацию факторов, фоновых состояний.
источник
Нестероидные противовоспалительные препараты для наружного применения в лечении скелетно-мышечных болевых синдромов
Боль в спине, шее, суставах является ведущим симптомом при заболеваниях опорно-двигательного аппарата и относится к наиболее частой причине обращения к врачу. В лечении скелетно-мышечных болей наиболее часто применяются нестероидные противовоспалительные
Боль в спине, шее, суставах является ведущим симптомом при заболеваниях опорно-двигательного аппарата и относится к наиболее частой причине обращения к врачу. В лечении скелетно-мышечных болей наиболее часто применяются нестероидные противовоспалительные средства (НПВС). В практической деятельности врача, занимающегося лечением болевых синдромов, определяющим критерием выбора лекарственного средства является его анальгетическая эффективность, индивидуальная непереносимость, вероятность возникновения осложнений или побочных эффектов [1, 3].
Применение НПВС внутрь или парентерально часто сопровождается у пациентов развитием побочных эффектов и осложнений, в первую очередь со стороны желудочно-кишечного тракта, почек, центральной нервной системы. Возможность применять лекарственные средства местно (наружно) позволяет доставлять активное вещество максимально близко к источнику болевого ощущения, не вызывая системного воздействия, что значительно уменьшает риск развития побочных эффектов и осложнений.
В настоящее время арсенал препаратов для местного применения, содержащих НПВС, при заболеваниях опорно-двигательного аппарата достаточно широк, в том числе в связи с выпуском одних и тех же препаратов разными производителями под разными (патентованными) названиями.
Все НПВС для местного применения можно разделить на следующие группы по основному действующему лекарственному веществу, входящему в состав многокомпонентных или комбинированных препаратов [2].
1. Действующее вещество — диклофенак.
- Препараты монокомпонентного состава:
— Вольтарен Эмульгель.
— Дикловит.
— Диклак.
— Диклобене.
— Диклонат П гель.
— Диклоран.
— Диклофенак.
— Диклофенак-Акри.
— Мазь Ортофена. - Препараты комбинированного состава, содержащие диклофенак:
— Диклофенакол.
— Диклоран плюс.
2. Действующее вещество — ибупрофен.
- — Нурофен гель.
— Долгит.
— Долгит крем.
3. Действующее вещество — индометацин.
- Препараты монокомпонентного состава:
— Индометацин.
— Индометацин Софарма мазь.
— Индометацин-Акри. - Препараты комбинированного состава, содержащие индометацин:
— Индовазин.
4. Действующее вещество — кетопрофен.
- — Артрозилен.
— Быструмгель.
— Кетонал.
— Кетопрофен Врамед.
— Фастум.
— Феброфид.
— Флексен.
5. Действующее вещество — нимесулид.
6. Действующее вещество — пироксикам.
Основным механизмом действия препаратов монокомпонентного состава с действующим веществом диклофенаком является неселективное ингибирование активности циклооксигеназы (ЦОГ): ЦОГ-1 и ЦОГ-2, что приводит к нарушению метаболизма арахидоновой кислоты и подавлению синтеза простагландинов в очаге воспаления. При наружном применении данных препаратов возникают ослабление болей в месте их нанесения, уменьшение отечности и увеличение объема движений в пораженных суставах.
Показаниями для применения служат болевой синдром при воспалительных и дегенеративных заболеваниях суставов и позвоночника, ревматических поражениях мягких тканей, посттравматическом болевом синдроме, невралгии.
Побочные действия могут наблюдаться в виде местных кожных проявлений, при длительном применении препаратов возможны резорбтивное действие и развитие системных реакций (крапивница, бронхоспазм, ангионевротический отек).
Противопоказаниями для применения являются язвенная болезнь желудка и двенадцатиперстной кишки в стадии обострения, нарушение кроветворения, нарушение целостности кожных покровов, беременность, лактация, возраст до 6 лет, повышенная чувствительность к диклофенаку.
При сочетании диклофенака с ментолом в препарате Диклофенакол также дополнительно оказывается местное раздражающее и слабовыраженное анальгезирующее действие.
При сочетании диклофенака с метилсалицилатом, ментолом, льняным маслом в препарате Диклоран плюс противовоспалительное и анальгетическое действие диклофенака усиливается вторым препаратом из группы НПВС — метилсалицилатом, а также a-линоленовой кислотой, входящей в состав льняного масла; ментол оказывает местное раздражающее и слабовыраженное анальгезирующее действие.
Основным фармакологическим эффектом препаратов с действующим веществом ибупрофеном является местное анальгезирующее и противовоспалительное действие, механизм которого связан с торможением синтеза простагландинов за счет неселективного блокирования фермента ЦОГ.
Показаниями к применению являются миалгии, боли в спине, артриты, повреждения и растяжения связок, спортивные травмы, невралгии.
Побочные эффекты чаше всего отмечаются в виде небольшого покраснения кожи, жжения или покалывания. Системные реакции в виде аллергических реакций и бронхоспазма возникают чрезвычайно редко.
Противопоказанием к применению являются «аспириновая» астма, возраст до 12 лет, повышенная чувствительность к компонентам препарата. С осторожностью препарат применяют при сопутствующих заболеваниях печени и почек, желудочно-кишечного тракта, крапивнице, рините, беременности и лактации.
Основным фармакологическим эффектом препаратов монокомпонентного состава с действующим веществом индометацином является местное выраженное противовоспалительное и анальгетическое действие за счет неселективного блокирования фермента ЦОГ и подавления синтеза простагландинов. Показаниями к применению служат болевой синдром и местные воспалительные реакции при ревматоидных заболеваниях, острых скелетно-мышечных болях, подагре, невралгиях.
Побочные эффекты наблюдаются в виде местных кожных реакций (гиперемия, шелушение, крапивница и др.). Системные реакции в виде диспепсии, тошноты, головокружения, атаксии возможны при длительном, более 10 дней, применении либо при нанесении препарата на большой участок кожных покровов.
Препарат противопоказан при желудочно-кишечных заболеваниях, заболеваниях почек, центральной нервной системы, инфекционных заболеваниях, в период беременности и лактации, не назначается детям.
При сочетании индометацина с троксерутином в препарате Индовазин дополнительно оказывается местное противоотечное и ангиопротекторное действие.
Основным механизмом действия препаратов с действующим веществом кетопрофеном (производное пропионовой кислоты) является подавление активности ЦОГ-1 и ЦОГ-2, регулирующей синтез простагландинов. Противовоспалительная и анальгезирующая активность кетопрофена сходна с таковой индометацина и выше активности ибупрофена в 20 раз. Кетопрофен обладает антибрадикининовой активностью, стабилизирует лизосомальные мембраны, вызывает значительное торможение активности нейтрофилов у больных с ревматоидным артритом, подавляет агрегацию тромбоцитов.
Показаниями к применению являются острые и хронические воспалительные и дегенеративно-дистрофические заболевания опорно-двигательного аппарата, травмы.
Побочные действия наблюдаются в виде гиперемии кожи в месте нанесения препарата, фотосенсибилизации пурпуры. При длительном применении редко возможны системные реакции: боли в животе, рвота, астения, транзиторная дизурия.
Противопоказан к применению у пациентов с экземой, инфицированными ранами, у детей до 12 лет, при индивидуальной непереносимости препарата. С осторожностью возможно применение при беременности и в период лактации.
Основным механизмом действия препаратов с действующим веществом нимесулидом является селективное подавление активности ЦОГ-2, регулирующей синтез простагландинов. Нимесулид обратимо ингибирует синтез простагландина Е2 как в области воспаления, так и в восходящих путях ноцицептивой системы. Подавляет агрегацию тромбоцитов, высвобождение гистамина и фактора некроза опухоли a, обладает антиоксидантной активностью. Препарат хорошо переносится при длительной терапии. При местном применении вызывает уменьшение или исчезновение болей в месте нанесения геля, уменьшает отечность, утреннюю скованность суставов, способствует увеличению объема движений.
Показаниями к применению служат воспалительные заболевания с болевым синдромом умеренной интенсивности: заболевания опорно-двигательного аппарата, в том числе артриты, остеохондроз, остеоартроз, артралгии, миалгии, бурситы, травматические повреждения.
Побочные эффекты связаны с местными реакциями при нанесении геля — зуд, крапивница, шелушение, преходящее изменение цвета кожи — и не требуют отмены препарата.
Противопоказания: дерматозы, инфекции кожи в области применения геля, возраст до 2 лет, повышенная чувствительность к препарату, беременность и лактация.
Основным механизмом действия препаратов с действующим веществом пироксикамом является подавление синтеза простагландинов вследствие неселективного ингибирования ферментов ЦОГ-1 и ЦОГ-2. Применение препарата уменьшает отек, воспаление, мышечную и суставную боль, не вызывает сухости кожи.
Показаниями к применению является болевой синдром при спортивных травмах, анкилозирующем спондилоартрите, остеоартрозе, плечелопаточном периартрозе, тендините.
Побочные эффекты связаны с местными реакциями и проявляются в виде покраснения и шелушения, местного зуда, крапивницы.
Противопоказаниями для применения служат почечная недостаточность, возраст до 14 лет, беременность, индивидуальная непереносимость препарата.
- Гусев Е. И., Дробышева Н. А., Никифоров А. С. Лекарственные средства в неврологии. М., 1998.
- Справочник Видаль. Лекарственные препараты в России: Справочник. М.: АстраФармСервис, 2007.
- Лоуренс Д. Р., Бенитт П. Н. Клиническая фармакология: в 2 т./ пер. с англ. М.: Медицина, 1991.
Л. Е. Корнилова, кандидат медицинских наук
Е. Л. Соков, доктор медицинских наук, профессор
РУДН, Клиника лечения боли, ГКБ № 64, Москва
источник
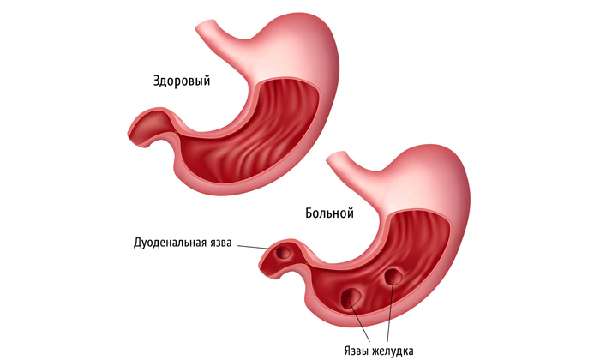 При язвенных поражениях слизистой оболочки органов пищеварения ингибиторы ацетилхолинэстеразы не применяют.
При язвенных поражениях слизистой оболочки органов пищеварения ингибиторы ацетилхолинэстеразы не применяют.