Церебролизин — эффективность при лечении болезни Альцгеймера (Результаты шестимесячного рандомизированного плацебо-контролируемого испытания эффективности церебролизина при болезни Альцгеймера)
Центр изучения старения, Монреаль, Канада
Б олезнь Альцгеймера (БА) является наиболее распространенной формой деменции в популяции лиц пожилого возраста. В период прогрессирующего течения заболевания больные утрачивают свою функциональную самостоятельность и становятся зависимыми от помощи, которую оказывают им либо родственники, либо профессионалы в области здравоохранения. В связи с увеличением во всем мире числа больных с этим заболеванием БА приобретает характер социально-экономического бремени, которое в будущем может стать еще более тяжелым по мере увеличения в популяции числа лиц пожилого возраста, так как старение является одним из важных факторов риска этой болезни.
Несмотря на проведение интенсивных исследований, этиопатогенез БА остается неясным. Современные принципы лечения базируются только на усилении холинергической нейропередачи, которая, по-видимому, главным образом и нарушается. В настоящее время единственными лекарственными препаратами, которые утверждены Управлением по контролю за качеством пищевых продуктов и лекарств в США и соответствующими органами большинства других стран для лечения основных симптомов БА, являются ингибиторы ацетилхолинэстеразы, увеличивающие концентрацию ацетилхолина в синаптической щели. Именно с помощью таких препаратов пытаются воздействовать на ключевые симптомы БА, к числу которых относятся утрата памяти, ориентации и инициативы. Установлено, что эти вещества дают согласующийся с лечением, но умеренный клинический положительный эффект. Более новые препараты этого класса, такие как донепезил и ривастигмин, не обладают тяжелым побочным действием (например, токсическим воздействием на печень). Однако, несмотря на умеренное симптоматическое действие, такие препараты не в состоянии в достаточной степени модифицировать прогрессирующее течение болезни.
Все это привлекает внимание исследователей именно к тем препаратам, которые в состоянии модифицировать патологический процесс. Такие фармацевтические препараты должны замедлить или даже приостановить прогрессирование нейродегенерации. Разработки, направленные на то, чтобы использовать для лечения БА нейротрофические субстанции, например NGF (фактор роста нервов), были затруднены в связи с их неспособностью проникать через гематоэнцефалический барьер, а также в связи с непереносимым побочным действием. Между тем пептидергический лекарственный препарат церебролизин, состоящий из аминокислот и биологически активных пептидов, проявляет экспериментально доказанную нейротрофическую активность, достаточно сходную с той, которая характерна для естественно возникающих нейротрофических соединений. При этом имеющийся клинический опыт подтвердил наличие у него благоприятного профиля безопасности.
Основываясь на данных клинического исследования церебролизина, проведенного в Германии (Ruther и соавт., 1994), в котором было показано, что лечение способствует улучшению когнитивной функции, общего функционирования и показателей активности повседневной жизни (при этом положительный эффект сохраняется в сроки до 6 мес после прекращения активного лечения), Канадская группа по изучению церебролизина приняла решение провести испытание, план которого предусматривает изучение потенциальных возможностей церебролизина в отношении модификации течения болезни. Это исследование спланировано как многоцентровое (с участием 14 клинических центров), двойное слепое, плацебо-контролируемое испытание с параллельными группами, предназначенное для оценки безопасности и эффективности церебролизина у больных с вероятной БА от легкой до умеренной тяжести. Главное отличие от всех других клинических испытаний, осуществленных до настоящего времени у больных с БА, заключалось в том, что в настоящем исследовании первичный подтверждающий статистический анализ планировалось провести через 2 мес после окончания периода активного лечения. Другими словами, цель этого проспективного испытания заключалась в том, чтобы определить, насколько продолжительным может оказаться эффект лечения церебролизином.
Больных лечили в течение 4 последовательных недель, при этом каждую неделю проводили 5 внутривенных инфузий (каждый больной получал 20 инфузий). В группе активного вмешательства доза церебролизина составляла 30 мл в 100 мл физиологического раствора, в группе плацебо вводили 130 мл физиологического раствора (0,9% NaCl). Клиническую оценку проводили до начала лечения, а затем — спустя 1, 3 и 6 мес. В течение 18 мес было рандомизировано всего 192 больных (97 в группу церебролизина и 95 в группу плацебо). В исследование были включены такие больные, которые отвечали критериям NINCDS-ADRDA, а рейтинг шкалы MMSE составлял 14-26. Основные критерии включения и исключения соответствовали хорошо известным методическим рекомендациям, предназначенным для тестирования антидементирующих лекарств.
Для оценки реакции на лечение в качестве первичных переменных использовались показатели CIBIC-плюс (современная версия клинического интервью, основанного на впечатлении о характере изменений) и ADAS-соg (шкала оценки БА — когнитивная часть). Положительной считалась такая реакция на лечение, которая составляла 4 по шкале CIBIC-плюс. По шкале ADAS-cog это соответствовало улучшению ? 4 пунктов по сравнению с исходной оценкой. Вторичные переменные эффективности включали MMSE (сокращенное исследование психического статуса), Корнельскую шкалу депрессии, шкалу оценки инвалидности, связанной с деменцией, шкалу сохранности самоподдержки при осуществлении физических функций (Physical Sell Maintenance Scale), шкалу активности повседневной жизни, шкалу оценки поведения при БА и рейтинговую шкалу клинических проявлений деменции. Первоначальному анализу для оценки эффективности была подвергнута популяция больных, имеющих намерение лечиться. Она включала всех рандомизированных больных, которые получили по крайней мере одну дозу исследуемого лекарства и которым была проведена по меньшей мере одна оценка эффективности до лечения, а также одна оценка после начала терапии. Популяция, соответствующая протоколу, включала всех больных, которые получили все 20 инфузий и у которых в соответствующие периоды времени были проведены все оценки эффективности лечения.
На исходном уровне между популяциями активного вмешательства и плацебо существовали два статистически значимых демографических различия. У больных группы, получавшей церебролизин, возраст был моложе, при этом деменция у них также проявлялась в более молодом возрасте. Что касается симптоматики самой деменции, то число больных, страдающих галлюцинациями, было значительно выше в группе церебролизина по сравнению с плацебо. В целом 79% получавших церебролизин и 84% получавших плацебо закончили весь курс лечения, т. е. получили все 20 инфузий.
Первоначальный анализ по состоянию на 3 мес показал отсутствие статистически значимых различий между группами церебролизина и плацебо по шкале ADAS-cog.
Обнаружено высокозначимое различие в общем рейтинге (CIBIC-плюс) между указанными группами. В группе церебролизина выявлено 76% положительных реакций. В группе плацебо — 57%. Таким образом, установлено высокозначимое различие (p
Так как различий между группами по шкале ADAS-cog выявлено не было, то возникал вопрос о том, какие параметры повлияли на возникновение значимого различия в рейтинге CIBIC-плюс. Хотя в популяции, имеющей намерение лечиться, не было обнаружено других значимых различий, существовала четкая тенденция в пользу благоприятного эффекта церебролизина в оценке инвалидности при деменции (DAD) и в рейтинге Корнельской шкалы депрессии. Это свидетельствует о том, что глобальный рейтинг зависел от улучшения показателей активности повседневной жизни и позитивного влияния на симптомы депрессии. Из-за того, что в группах церебролизина и плацебо число больных, страдающих галлюцинациями, было разным, третичный анализ был проведен только в той части соответствующей протоколу популяции, из которой такие больные были исключены. Анализ, проведенный с соблюдением этого требования, показал наличие исключительно высокого (30%) различия в пользу церебролизина при сравнении положительных реакций по шкале CIBIC-плюс. Было показано также значимое различие по шкале DAD.
Популяция для оценки безопасности включала всех рандомизированных больных, которые получили по меньшей мере одну дозу изучаемого лекарства и у которых проводилось по меньшей мере несколько оценок безопасности в период после начала лечения или имелась какая-либо информация о переносимости. Отмечено несколько побочных эффектов в обеих группах, но степень выраженности большинства таких событий была незначительной. В группе церебролизина не было событий, связанных с выраженным побочным действием. В группе плацебо у 2 больных возникло нарушение мозгового кровообращения. Испытание было преждевременно прекращено только у 1 больного, так как у него развилась непроходимость кишечника, которая, по мнению исследователей, вряд ли могла быть связана с изучаемым лекарством. Таким образом, можно сделать вывод, что в этом клиническом исследовании отсутствовали проблемы безопасности, связанные с лечением церебролизином. Между группами активного вмешательства и плацебо не было также существенных различий, касающихся изменений клинических лабораторных тестов или жизненно важных параметров.
Несмотря на то, что существенные различия, определяемые по шкале ADAS-cog, отсутствовали, следует подчеркнуть, что параллельно рейтингу CIBIC-плюс в популяции, соответствующей протоколу, у 80% больных, получавших церебролизин, отмечена положительная реакция на лечение. Это хорошо согласуется с результатами других клинических исследований церебролизина. Важно подчеркнуть также, что на общий рейтинг влияло улучшение способности больных к преодолению трудностей, возникающих в процессе повседневной жизни, что находило отражение в показателях шкалы инвалидности, связанной с деменцией. На исход исследования могло повлиять также неравномерное распределение больных по возрасту и срокам начала болезни, так как оба эти параметра влияют на темп прогрессирования. Необходимо принять в расчет, что продолжительность лечения (1 мес) была исключительно короткой, а число инфузий препарата — небольшим (20). Поэтому пропуск всего одной инфузии уже мог повлиять на терапевтический исход.
Можно сделать вывод, что по сравнению с другими лекарствами, применяемыми по аналогичным показаниям, церебролизин начинал действовать быстро, число положительных реакций было высоким, а терапевтическая эффективность сохранялась вдвое дольше, чем продолжительность активного лечения. Церебролизин, по-видимому, хорошо переносится и обладает потенциальной возможностью модифицировать патологический процесс при БА.
источник
Нет достоверных клинических данных о безопасности Церебролизина в период беременности и лактации, поэтому назначать препарат беременным и кормящим можно только в крайнем случае, когда польза от лечения превышает возможный риск. Препарат не следует назначать во время первого триместра беременности.
Для детей ограничения сводятся к стандартным педиатрическим – нужно тщательно контролировать дозу и следить за состоянием пациента.
Препарат разрешается применять во время вынашивания ребенка, если в этом имеется острая необходимость и польза превышает риски. Церебролизин может попадать в молоко матери при лактации (грудном вскармливании).
На период терапии лекарством кормление необходимо временно прекращать. Церебролизин при кормлении грудью назначается после тщательной оценки преобладания пользы для матери над возможными рисками.
Исследования на животных не выявили доказательств репродуктивной токсичности.
Однако данные о влиянии церебролизина на репродуктивную функцию человека отсутствуют. При беременности церебролизин может быть назначен только после тщательной оценки соотношения ожидаемой пользы для матери и потенциального риска для плода/ребенка. На время применения препарата в период лактации кормление грудью следует прекратить.
Церебролизин повышается эффективность антидепрессантов разных форм. В случае необходимости комбинации таких средств следует снижать дозировку антидепрессантов.
Важно! Препарат не рекомендуется соединять в одном шприце или флаконе с другими препаратами, даже несмотря на их нормальную совместимость.
Медикамент поступает в продажу исключительно в виде раствора для инъекций, в виде таблеток или других лекарственных форм он не производится. Стоимость зависит от объема лекарственного раствора и от количества ампул в упаковке. Примерная стоимость представлена в таблице (Табл. 1).
Таблица 1 – Примерная цена Церебролизина в розничной продаже в 2017 г.
| Объем лекарства в ампуле, мл. | Количество ампул в упаковке, шт. | Примерная стоимость, руб. |
|---|---|---|
| 2 | 10 | 1100 |
| 5 | 5 | 1050 |
| 10 | 5 | 1600 |
| 20 | 5 | 3100 |
Вводится лекарственное вещество путем внутримышечной или внутривенной инъекции. Максимальная разовая дозировка внутримышечной инъекции не должна превышать 5 мл, внутривенной –10 мл.
Церебролизин вступает во взаимодействие только с антидепрессантами – оба препарата усиливают действие друг друга. В таких случаях обычно достаточно уменьшить дозу антидепрессанта.
Назначение средства при всех показаниях к применению позволяет воздействовать как на симптоматику, так и на механизмы и причины указанных патологий.
Церебролизин вводится только в форме уколов внутримышечных или инфузий внутривенных взрослым и детям. Препарат в ампулах объемом от 1 до 5 мл требуется колоть внутримышечно, во флаконах 10-60 мл — вводить капельно.
Важно! Дозировка средства и продолжительность введения должна подбираться индивидуально для каждого пациента с обязательным учетом его состояния и формы патологического процесса.
Рекомендуемая длительность приема препарата — около одного месяца. Минимально число введений в неделю — 5, для лучшего эффекта лучше вводить средство ежедневно.
Способ применения для лечения острых заболеваний: вводить в форме медленных внутривенных капельных инфузий от 10 до 60 мл раствора, который предварительно разводят в 100-250 мл NaCl.
В периоды реабилитации после перенесенных патологий и для лечения депрессий рекомендуемая схема приема: внутривенно по 5-10 мл Церебролизина в сутки.
Курс лечения для детей (в том числе дети до года), как правило, составляет 1 месяц. Доза препарата составляет до 1 мл на 10 кг веса ребенка. Средняя терапевтическая доза — 1-2 мл внутримышечно. Инъекции выполняют каждый день. Рекомендуется проводить 2-3 курса лечения в течение года.
При нарушениях памяти и болезни Альцгеймера вводят внутривенно по 20-30 мл препарата. Количество введений — до 20.
Важно! Время введения препарата не имеет значения, его подбирают индивидуально — до обеда (утро), в обед или после обеда (вечер).
Что касается противопоказаний к применению, к ним можно отнести патологии почек и индивидуальная невосприимчивость компонентов, входящих в основу лекарственного средства. Запрещено также принимать средство при регулярных эпилептических припадках. С особой осторожностью препарат назначается больным, страдающим от диатеза аллергической формы.
Уколы предназначены для введения в мышцы или в кровоток. Дозировку должен назначить врач исходя из тяжести заболевания и общего состояния здоровья пациента.
- Острые состояния, в том числе осложнения после операции на мозге, инсульт, ЧМТ – 10-50 мл/день.
- Деменция, болезнь Альцгеймера – 5-30 мл/день.
- Депрессия различного генеза – 5-30 мл/день.
- Состояние после инсульта, травмы ЦНС – 5-50 мл/день.
- При необходимости назначения препарата детям – 0.1-0.2 мл/день на кг тела пациента.
При успехе от лечения врач может назначить дополнительный курс, обычно – с меньшей частотой введения (через день).
До 5 мл можно вводить в мышечные ткани, до 10 можно вводить Церебролизин внутривенно. Объемы выше нужно вводить только с помощью капельницы. Длительность введения зависит от объема.
Посмотрите небольшой фильм про препарат
Применение Церебролизина обосновано в психиатрии и неврологии при:
- деменции различного генеза;
- травмах ЦНС;
- инсульте и состоянии после него;
- цереброваскулярной недостаточности;
- депрессии, в том числе резистентной к антидепрессантам и эндогенной;
- слабоумии;
- СДВГ или задержке интеллектуального развития у детей.
Применение Церебролизина показано при следующих патологиях:
- Болезнь Альцгеймера;
- Недостаточность кровообращения головного мозга хронического течения;
- Повреждения головного мозга, вызванные травмами различной степени тяжести;
- Деградация умственной деятельности различного происхождения;
- Инсульт , вызванный недостаточностью кровоснабжения головного мозга;
- Недостаточность умственного развития у детей дошкольного возраста;
- Хроническое снижение настроения, обусловленное нарушениями деятельности нервной системы;
- Повышенная активность и недостаток внимания у детей.
Как указано в инструкции по применению раствор Церебролизин предназначен для парентерального введения. Объем для внутримышечного введения составляет 5 мл, для внутривенного – 10 мл.
Также допускается внутривенная медленная капельная инфузия объема раствора до 50 мл. Парентеральное применение препарата должно проводится с обязательным соблюдением правил асептики и антисептики, направленных на профилактику вторичного инфицирования пациента.
Режим применения и рекомендуемая терапевтическая дозировка раствора для парентерального введения Церебролизин определяются медицинскими показаниями:
- Депрессия, психоорганический синдром – 5-30 мл 1 раз в день.
- Острый ишемический инсульт, перенесенная черепно-мозговая травма, осложнения после проведенной нейрохирургической операции – 10-50 мл 1 раз в день.
- Болезнь Альцгеймера, деменция различного (в том числе сосудистого) происхождения – рекомендуемая терапевтическая дозировка варьирует от 5 до 30 мл 1 раз в день.
- Восстановительный период с наличием остаточных (резидуальных) неврологических явлений после инсульта, черепно-мозговой травмы – 5-50 мл 1 раз в день.
Для детей препарат используется в дозировке 0,1-0,2 мл на 1 кг массы тела ребенка. Средняя длительность курса терапии для детей и взрослых варьирует от 10 до 20 дней.
При необходимости могут проводится повторные курсы терапии препарата. После проведения курса основной терапии также может быть назначено поддерживающее лечение с введением раствора для инъекций Церебролизин 2-3 раза в неделю.
В большинстве случаев режим использования лекарственного средства, дозировка и длительность терапии устанавливаются врачом индивидуально.
Важно! Церебролизин с особой осторожностью назначают при беременности в первые три месяца.
Перед назначением средства врач обязательно должен оценить все риски и исключить наличие у пациентов состояний, которые производитель согласно аннотации (официальной инструкции) относит к противопоказаниям к применению.
У препарата всего 3 противопоказания – эпилептический статус, индивидуальная непереносимость (аллергия) и тяжелая почечная недостаточность.
Аллергический диатез, почечная недостаточность, эпилептический статус, беременность, гиперчувствительность к компонентам препрата.
Препарат полностью состоит из концентрированного Церебролизина, чуть больше 215 мг в одном миллилитре. Вспомогательные вещества: каустическая сода, вода.
Единственная форма выпуска лекарства – инъекция. Таблеток, мазей и прочих форм препарата в природе не существует. Раствор для инъекций представлен в разных объемах – от 1 до 20 мл в ампулах.
- за 10 ампул по 1 мл – от 590 рублей;
- за 10 ампул по 2 мл – от 1046 рублей;
- за 5 ампул по 5 мл – от 1025 рублей;
- за 5 ампул по 10 мл – от 1460 рублей;
- за 5 ампул по 20 мл – от 2900 рублей.
Сколько стоит Церебролизин в аптеках? Средняя цена находится на уровне 1 100 рублей.
Кирилл П.: этот препарат прекрасно помогает моей маме (80 лет) восстановиться после инсульта. Врач подбирает схемы лечения, вводит средство капельно. Эффект наступает очень быстро, практически не болит голова уже после 2-3 введений.
Ольга Х.: после нарушения кровотока в мозге для профилактики инсульта доктор, который меня лечит, назначил Церебролизин и принимать Церебрин (витамины, стоят дешевле). После 3 введений препарата я почувствовала себя намного лучше — ясность мыслей, отсутствие головных болей, головокружений, болей в шее. Очень довольна результатами лечения.
Богдан К.: доктор после инсульта назначил Церебролизин (чередовать с Кортексином), Актовегин и Мексидол (колоть). Отметил, чтобы не смешивали все средства в одном шприце. Хочу заметить, что чувствую себя хорошо на фоне лечения.
Мирон Павличенко, невролог: Своим пациентам часто назначаю Церебролизин или Кортексин (разница в составе). Эти два средства для меня характеризуются очень высокой эффективностью в лечении неврологических расстройств.
Яков Игнатуша, невролог: когда назначаю пациентам такие средства, как Церебролизат или Церебролизин, они часто интересуются отличиями между ними. Эти препараты являются аналогами по действию. Отличаются составом, в котором имеется похожий комплекс нейротропных белков. Оба средства являются эффективными.
Отзывы пациентов почти во всех случаях положительные. Врачи чаще всего назначают это лекарство в качестве поддерживающей терапии при болезнях, которые можно купировать, но нельзя полностью вылечить (травмы, Альцгеймер и так далее), и препарат справляется со своей задачей.
Больные отмечают улучшение памяти, у них «светлеет» настроение, повышаются когнитивные способности. Нередко лечение не заканчивается одним курсом, так как ввиду положительного эффекта врач назначает использование Церебролизина повторно.
Предлагаем ознакомиться с отзывами людей использовавших Церебролизин:
- Лена . Мне одно время назначали антидепрессанты, но они мне не помогали. Помимо вялости и нежелания что-либо делать, я заметила, что всё просто из рук валится, ни на чём сосредоточиться не могу. Мы с мамой пошли к врачу, он прописал Церебролизин внутримышечно. Через три недели я заметила, что стала лучше концентрироваться и соображать.
- Алина . Я в лечебных целях, из-за повышенного давления, болей в голове ставила церебролизин, а помимо головной боли у меня еще и бессонница была длительная. Проставила уколы, 14 штук, уже на фоне лечения, в середине курса стала спать как детеныш, сны такие стали сниться, утром чувствовать стала себя хорошо отдохнувшей. Головные боли сократились. бывают только если высокой давление поднимется, но врач сказала, что лечение надо проводить регулярно. Я не против)
- Елена . У меня хроническое нарушение мозгового и периферического кровообращения. С таким диагнозом я уже не один год живу. Периодически прохожу курсы лечения Церебролизином. Он эффективный, да, хотя надолго его эффект не сохраняется. Но временное улучшение налицо, это факт.
источник
Клинико-фармакологическая группа
Ноотропный препарат. Церебролизин включает низкомолекулярные нейропептиды, биологически активные, способные преодолевать гематоэнцефалический барьер и доставляться непосредственно к нервным структурам. Медикамент проявляет органоспецифическое мультимодальное влияние на мозг (одновременное проявление метаболической регуляции, функциональной нейромодуляции, нейропротекции и нейротрофической активности.
- Совокупность пептидов, извлеченных из свиного головного мозга
- Набор вспомогательных веществ – гидроксид натрия, вода дистиллированная.
Форма выпуска
Прозрачный водный раствор для инъекций, характерного янтарного цвета.
Ампулы из темного стекла с объемом 1, 2, 5, 10, 20 и 30 мл, в упаковке по 1, 5 и 10 ампул, ячейковые контурные упаковки, картонные пачки.
Условия и срок хранения
Церебролизин необходимо хранить при температуре не более 25°C, в месте, закрытом от детей и защищенном от света.
Срок годности Церебролизина в ампулах — 5 лет. Срок годности во флаконах — 4 года.
Фармакологическое действие
Метаболическая регуляция:
Церебролизин увеличивает интенсивность аэробного энергетического метаболизма головного мозга, позитивно влияет на внутриклеточный синтез белков в стареющем или развивающемся мозге.
Нейропротекция:
Церебролизин защищает нейроны от повреждающего влияния лактацидоза, предупреждает возникновение свободных радикалов, усиливает жизнеспособность нейронов, защищает их от гибели при гипоксии и ишемии, устраняет повреждения при нейротоксическом влиянии возбуждающих аминокислот.
Нейротрофическая активность:
Церебролизин — единственный ноотропный препарат, нейротрофическая активность которого доказана практически. Его действие аналогично влиянию естественных факторов нейронального роста (NGF), однако проявляющемуся в данном случае при периферическом введении.
Функциональная нейромодуляция:
Церебролизин положительно влияет при ослаблении когнитивных функций организма, повышает концентрацию внимания, стабилизирует процессы запоминания.
- болезнь Альцгеймера;
- синдром деменции различного генеза;
- ишемический мозговой инсульт;
- хроническая цереброваскулярная недостаточность;
- ЧМТ, травмы спинного мозга;
- осложнения после нейрохирургических операций и иные острые состояния;
- эндогенная депрессия в условиях неприятия антидепрессантов;
- болезнь Паркинсона;
- бессонница;
- боли в спине;
- вертебро-базилярная недостаточность:
- в нейропедии – при задержке умственного развития, гиперактивности, дефиците внимания;
Противопоказания
- эпилептический статус;
- острая почечная недостаточность;
- повышенная чувствительность к препарату.
Инструкция к применению
Церебролизин следует применять парентерально (внутривенно и внутримышечно). Внутримышечно – до 5 мл, внутривенно – до 10 мл. Использовать только прозрачный раствор препарата и только однократно.
Рекомендуемый курс лечения
Возможно однократное введение Церебролизина при дозе до 50 мл, предпочтительно проведение лечебного курса – ежедневные инъекции в течение 10-20 дней.
Дозировка и длительность применения определяются характером и тяжестью заболевания, и возрастом пациента.
- При острых состояниях (инсульт, ЧМТ, осложнения нейрохирургических операций) — от 10 до 50 мл.
- В резидуальном периоде инсульта, травмах головного и спинного мозга — от 5 до 50 мл.
- При психоорганическом синдроме и депрессиях — от 5 до 30 мл.
- При болезни Альцгеймера и синдроме деменции — от 5 до 30 мл.
- В нейропедиатрической практике — 0.1-0.2 мл/кг массы тела.
В целях повышения эффективности проводятся повторные курсы до тех пор, пока они положительно влияют на состояние пациента. После первого курса периодичность проведения инъекций может снижаться до 2-3 раз в неделю.
Передозировка
О случаях передозировки препаратом Церебролизин неизвестно.
Лекарственное взаимодействие (фармакосовместимость)
На практике подтверждена совместимость Церебролизина со стандартными инфузионными растворами (в течение 24 ч при комнатной температуре и обычном освещении): 0.9% раствор натрия хлорида, 5% раствор декстрозы (глюкозы), раствор Рингера.
Допустимо совместное применение препарата с витаминами и стимуляторами сердечного кровообращения. Но при этом препараты не рекомендуется смешивать в одном шприце с Церебролизином.
Не рекомендуется смешивать в одном растворе Церебролизин со сбалансированными растворами аминокислот.
Препарат несовместим с растворами, изменяющими рН среды (5.0-8.0) или включающими липиды.
Одновременное применение Церебролизина и антидепрессантов или ингибиторов МАО может вызывать их взаимное усиление. В этом случае рекомендуется снижать дозу антидепрессанта.
Побочные эффекты
Пищеварительная система
Редко – потеря аппетита, диспепсия, тошнота и рвота, диарея или запоры.
ЦНС и периферическая нервная система
Редко – предполагаемый эффект активации сопровождается возбуждением, агрессивным поведением, спутанностью сознания, бессонницей; в единичных случаях ( 115 Цепочка комментария
источник
Церебролизином пытаются и лечить последствия инсульта, и спасаться от «старческого маразма», и бороться с болезнью Альцгеймера, и улучшать внимание и память здоровых людей. От чего из этого списка он помогает и из какой неожиданной смеси веществ его производят, рассказывает Indicator.Ru.
Церебролизин назначают при повреждениях мозга при инсульте, чтобы улучшить когнитивные функции (как ноотроп), при деменции, черепно-мозговых травмах, болезни Альцгеймера, нейропедиатрии и даже при депрессии. Лекарство входит в группу «другие психостимуляторы и ноотропные препараты» российского списка «Жизненно необходимых и важнейших лекарственных препаратов», однако Формулярный комитет РАМН настаивает на том, чтобы исключить его из списка и признать неэффективным. Сайт препарата не предоставляет нам никаких аргументов в свою пользу — по состоянию на момент написания этой статьи он просто не работает.
Сайт российского Минздрава указывает только на два испытания, зарегистрированных Росздравнадзором (в 2006 и 2010 году), но никакой информации о результатах, пациентах и целях нет. Зарегистрированных Минздравом исследований тоже всего два, и из них одно приостановлено, хотя должно было быть завершено в июне 2017 года. Другое должно быть завершено в феврале прошлого года, но опубликованные результаты найти не удается.
Кто же прав и есть ли хотя бы одно показание, по которому действительно стоит принимать церебролизин? Давайте разберемся в этом вопросе подробнее.
Инсульт, деменция, болезнь Альцгеймера
По данным Всемирной организации здравоохранения (ВОЗ), инсульт занимает второе место среди причин смертности населения, уступая лишь ишемической болезни сердца, при которой нарушается кровоснабжение сердечной мышцы. Заболевание делится на два главных типа: ишемический инсульт (нарушение кровоснабжения мозга из-за закупорки или сужения артерий, его еще называют инфарктом мозга) и геморрагический инсульт (кровоизлияние в мозг или в полость между мягкой и паутинной мозговыми оболочками). Последний подтип называют субарахноидальным кровоизлиянием, «подпаутинным» в переводе с греческого.
При ишемическом инсульте важная задача врачей — восстановить поступление крови к областям мозга, так как без питания ткани будут отмирать. Если сосуд закупорен тромбом, его нужно убрать: растворить с помощью специальных лекарств или удалить хирургическим путем. При геморрагическом инсульте мозг, напротив, нужно спасти от излившейся в него крови. В обоих случаях счет идет на минуты (подробнее об этом в статье Джеффри Сэйвера), максимум на часы, ведь чем больше тканей мозга повредится, тем больше последствий инсульт принесет для пациента. А последствия эти очень серьезные: паралич различных частей тела, затрудненное глотание, невозможность выучивать новые движения, возможность потери больным речи или зрения. Если инсульт затрагивает центры контроля над жизненно важными процессами (например, над дыханием), человек может впасть в кому или даже умереть.
При черепно-мозговых травмах, как и при инсульте, все решает тяжесть случая и своевременная помощь врачей. Если травма серьезна, пациенту могут помочь в отделении реанимации, и главная задача здесь — сократить область поражения, потому что восстанавливать ткани и функции мозга будет намного сложнее. При благоприятном прогнозе реабилитация будет включать умеренную физическую активность, физиотерапию, но, как и после инсульта, нет никакой «волшебной таблетки» или инъекции, которая быстро поставит вас на ноги.
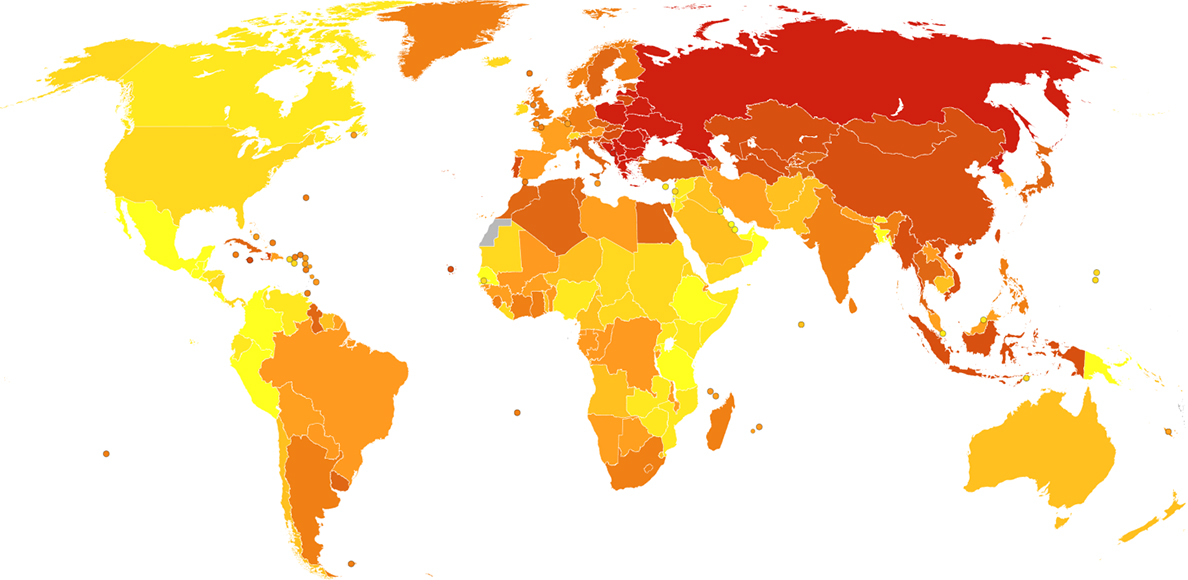
Еще одна рекомендация к применению Церебролизина — деменция, или старческое слабоумие. В 2015 году ею страдало 46 миллионов людей в мире, и эта цифра продолжает расти. Причиной деменции становятся самые разные заболевания, но более чем за половину случаев ответственность лежит на болезни Альцгеймера. Сама болезнь тоже не так проста: далеко не все случаи обусловлены генетической причиной (и только в 5% она установлена), остальные связаны либо с амилоидами (накоплением особых белковых комплексов внутри клетки), либо с нарушением работы тау-белка, либо с другими проблемами.
Сами амилоиды, кстати, тоже не так однозначны: хотя они стопорят работу клетки, некоторые ученые предлагают использовать их как лекарство (в случае, если клетку нужно усыпить, например, раковую). Вылечить или полностью остановить развитие болезни Альцгеймера с помощью существующих сегодня лекарств, к сожалению, невозможно. Известные на данный момент препараты либо дают слабый симптоматический или спорный эффект, либо обладают слишком опасными побочными эффектами, либо не помогают вовсе.
Из чего же из чего
В чем же польза Церебролизина? Может быть, при всех этих состояниях (и проблемах с памятью и вниманием у детей) он помогает стать немного умнее и более сконцентрированным, улучшая обмен веществ и питание головного мозга? Или просто содержит что-то полезное для этого органа? Ответ можно найти в составе лекарства.
Церебролизин состоит из смеси пептидов мозга свиней. Пептиды, которые меньше белков по размеру, по словам производителей Церебролизина, преодолевают гематоэнцефалический барьер (физиологический «фильтр», защищающий центральную нервную систему от циркулирующих в крови микроорганизмов и токсинов, и пропускающий питательные вещества и кислород). Этот препарат еще с 70-х продает австрийская фирма EVER Neuro Pharma, которая также выпускает пищевые добавки и лекарства от болезни Паркинсона.
Содержащиеся в мозге свиньи вещества могут быть полезны, но вот польза от самого Церебролизина видится неоднозначной. Например, хотя у пациентов с болезнью Альцгеймера при посмертном исследовании была обнаружена нехватка нейротрофического фактора мозга, белка, поддерживающего развитие нейронов, до конца его роль в заболевании не установлена. Впрочем, предполагается, что он защищает от пресловутых бета-амилоидов. Это же вещество задействовано и в механизмах долговременной памяти.
Другой белок мозга свиней и человека, который должен быть в составе Церебролизина, GDNF (Glial cell-derived neurotrophic factor — «глиальный нейротрофический фактор»), рассматривается как перспективное лекарство от болезни Паркинсона, но с переходом через гематоэнцефалический барьер, а значит, и с проникновением в мозг у него проблемы.
Ни точный состав Церебролизина, ни действие отдельных его компонентов не выяснено, поэтому трудно сказать, что он делает в организме. С тем же успехом в мозге свиньи могут быть белки, которые даже вредны человеку с перечисленными болезнями, даже если само животное было здорово.
Количество и соотношение разных веществ в препарате тоже под вопросом, так что подобрать дозировку правильно не представляется возможным. Единственным способом судить об эффекте Церебролизина становятся клинические исследования (хотя и странно, что препарат вообще дошел до них, если его состав вызывает столько повисающих в воздухе вопросов).
В списках (не) значился
Исследований Церебролизина так много, что в них можно потеряться. Поиск по базе данных медицинских научных статей PubMed выдает 389 работ, посвященных этому препарату. Если искать только двойные слепые контролируемые клинические испытания (постоянные читатели уже знают, что только они и могут служить подтверждением эффективности препарата с позиций доказательной медицины), мы найдем гораздо меньше — 34 статьи.
Многие из них просуммированы в таблице от Общества фармакоэкономических исследований (это российское отделение аналогичной международной организации). Там содержательно и на русском языке можно прочитать о количестве пациентов, результатах исследования и их методологическом уровне.
Основной проблемой клинических испытаний Церебролизина становится маленький размер выборки. Даже если исследования соответствуют критериям рандомизации, наличия контрольной группы и «двойного ослепления», количество участвующих в них пациентов очень мало (например, 60, 32 или 41).
Более масштабное исследование (точнее, даже цепочка из двух исследований) восстановления пациентов после инсульта показывает, что Церебролизин помогает быстрее улучшить двигательные функции. Эффект проявился на 90-й день.
Даже в тех случаях, где польза Церебролизина доказана, она все же неоднозначна: например, в испытании 2016 года, где поучаствовало в сумме 70 пациентов, эффект лекарства вместе со стандартной терапией слабо отличался от стандартной терапии. Наблюдался он только у пациентов с самым сильным поражением двигательных центров. Но в такой маленькой группе при наличии большого числа параметров можно выбрать параметр, который будет отражать корреляцию по простому совпадению, а не действительно существующую причинно-следственную связь. Многие исследования (например, это) профинансированы производителем. Конечно, это сразу не говорит о неэффективности лекарства, но делает выводы более сомнительными: компании выгодно, чтобы препарат работал. Что делать с таким обилием противоречивых данных?
На помощь здесь могут прийти обзоры большого количества научных статей. Наибольшим уважением в научной медицинской среде пользуются обзоры Кохрейновского сотрудничества, и вот почему.
Кохрейновских обзоров действия Церебролизина два. Первый из них был опубликован в 2013 году. Он касается сосудистой деменции. В обзор вошло шесть исследований, в которых поучаствовало в сумме 597 человек. Результаты его не очень вдохновляют. Авторы заключают, что, хотя Церебролизин «может оказывать положительный эффект на престарелых пациентов», у которых деменция проявляется слабо или средне, «доказательства все еще недостаточны», потому что исследований мало, а их длительность сильно отличается.
Другой обзор относительно свежий: он опубликован 21 апреля 2017 года, а резюме даже переведено на русский язык. Темой в этот раз стал острый ишемический инсульт. Авторы рассмотрели шесть исследований, в которых в сумме поучаствовало полторы тысячи пациентов, но все же не смогли однозначно порекомендовать препарат. Основная их претензия к испытаниям в пользу Церебролизина заключалась в том, что их чаще всего финансировали производители препарата. Также ученые нашли подтверждения тому, что препарат снижает риск смерти не лучше, чем плацебо, и что он может даже быть причиной «увеличения числа серьезных неблагоприятных событий при использовании Церебролизина у людей с острым ишемическим инсультом».
Есть и протокол Кохрейновского сотрудничества, касающийся того, как надо провести обзор статей, посвященных изучение болезни Альцгеймера. Подобный обзор был проведен, хотя и не Кохрейновский, но по сходным критериям. Он подчеркивает, что действие Церебролизина на когнитивные функции требует дополнительного изучения.
Indicator.Ru рекомендует: хорошо подумайте, стоит ли тратить на это деньги
Церебролизин — препарат с недоказанной эффективностью. Его действие либо показано на маленьких группах пациентов или в испытаниях, к дизайну которых есть претензии, либо опровергнуто. И даже в тех работах, где его эффект доказан, он все еще незначителен.
Лучший способ справиться с инсультом — либо не дать ему случиться (если это возможно), либо своевременно доставить пострадавшего к профессиональной бригаде врачей, которые сделают все необходимое, чтобы спасти как можно больше областей мозга от кровоизлияния или, наоборот, нехватки питания. Восстановить уже погибшие ткани мозга таблетки и инъекции не помогут. Реабилитация после инсульта или черепно-мозговой травмы, конечно, будет комплексной, и вам могут прописать много упражнений и лекарств. Не стоит, однако, надеяться, что Церебролизин — это чудо-лекарство, которое как-то серьезно повлияет на вероятность восстановления пациента. Платить ли за него, покупая ампулы за несколько тысяч рублей, или поесть жареных мозгов (с тем же успехом, но дешевле) — решать потребителю.
То же самое и с болезнью Альцгеймера, самой частой причиной старческой деменции: к сожалению, сейчас нет способов обратить ее вспять, и ученым нужно еще долго разбираться в хитросплетении причин и механизмов этой патологии. А пока большинство лекарств дает лишь слабый эффект. Данные в пользу Церебролизина все еще недостаточны, чтобы включать его в рекомендации. Известно, что активная умственная работа и изучение нескольких языков чаще всего помогают отдалить старение мозга.
Ноотропы, многочисленные «лекарства для улучшения внимания и памяти», которые студенты пачками скупают ближе к сессии, сами по себе спорны. Некоторые из них действительно улучшают кровоснабжение мозга или какие-то отдельные параметры его работы. Сделать же из посредственности гения на час они не смогут. К тому же ноотропы чаще всего разрабатывают для лечения каких-либо расстройств, а что они сделают со здоровым мозгом в долгосрочной перспективе, изучалось мало. Сам Церебролизин в этом качестве мало чем выделяется из остальных препаратов этой группы.
Если это лекарство после многих исследований докажет свою полезность, следовало бы понять, какие вещества и в каком количестве в нем содержатся, показать, что соотношение отдельных его компонентов соответствует самой подходящей их дозировке, и уже тогда его назначать.
Наши рекомендации нельзя приравнивать к назначению врача. Перед тем, как начать принимать тот или иной препарат, обязательно посоветуйтесь со специалистом.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
П отенциальная терапевтическая роль при деменциях нейротрофических факторов (фактор роста нервов, основной фактор роста фибробластов и др.) пептидов, обеспечивающих дифференциацию и функционирование нейронов, – довольно активно обсуждается в литературе [22,48,55,57,61]. Особый интерес к ним обусловлен тем, что эти вещества избирательно действуют на центральные холинергические нейроны [47]. В настоящее время существуют данные, свидетельствующие о роли дисфункции нейротрофических факторов при патогенетически различных заболеваниях центральной нервной системы. Поэтому теоретически обоснованным выглядит предположение об использовании подобных субстанций с целью затормозить прогрессирование патологического процесса – сосудистого и нейродегенеративного, стимулировать процессы восстановления, в том числе и связанные с формированием новых синапсов. Однако эти препараты не проникают через гематоэнцефалический барьер и поэтому не могут использоваться систематически, в единичных случаях они вводятся интравентрикулярно [55]. При этом на фоне их введения часто возникают побочные реакции (гипералгезия, значительное снижение веса).
Одним из эффективных лекарственных препаратов, обладающих нейротрофическими свойствами, является церебролизин. Этот препарат, состоящий из низкомолекулярных пептидов (25%) и свободных аминокислот (75%), используется для лечения деменций различного генеза и инсульта в нашей стране и за рубежом уже более 40 лет [1–4,7,17,32,36,46,51,63,64,75]. Препарат производится по стандартизированным биотехнологическим методикам с использованием ферментативного расщепления очищенных белков головного мозга свиней и не обладает аллергогенными или токсическими свойствами.
Следует отметить, что несмотря на большое число клинических исследований, свидетельствовавших об эффективности церебролизина, точные механизмы его действия не были известны. Ситуация кардинально изменилась в последние годы, когда появились новые данные, основанные на использовании современных лабораторных методов.
В целом ряде исследований была подтверждена нейротрофическая активность церебролизина, сходная с активностью естественных нейротрофических факторов [30,39,66,77]. Действие церебролизина по своему конечному эффекту и его выраженности напоминает действие фактора роста нервов [33,34,66]. L. Francis–Turner и соавт. [34] показали, что после перерезки бахромки свода (в эксперименте такое повреждение вызывает дегенерацию ацетилхолинергических нейронов в срединной перегородке) введение церебролизина сразу после повреждения уменьшает выраженность мнестических нарушений. Авторы провели сравнение эффективности естественно образующегося в организме фактора роста нервов, который вводился в желудочки головного мозга, и церебролизина, вводившегося интраперитонеально. Было отмечено, что церебролизин более значительно уменьшает обусловленные экспериментальным повреждением мнестические расстройства, чем фактор роста нервов. Кроме того, церебролизин ускорял процесс приобретения новых знаний, тогда как введение фактора роста нервов не влияло на способность к обучению [34]. Также было отмечено, что улучшение возникает после применения препарата в течение 4 недель, в то время как его применение в течение 2 недель дает только временный эффект. В последующей работе этих авторов [72] было показано, что церебролизин восстанавливает способность к обучению при назначении в существенно бoльшие сроки после экспериментального повреждения центральной нервной системы – спустя 4 месяца. Эффект препарата носил дозо–зависимый характер. Суммируя результаты прошлых работ и последнего исследования, V. Valouskova и L. Francis–Turner [72] сделали вывод о способности церебролизина препятствовать развитию мнестических расстройств, если применять его непосредственно после повреждения, и стимулировать восстановление способности к обучению даже в том случае, если он вводится спустя несколько месяцев после повреждения головного мозга.
Экспериментальные данные, полученные in vitro [41,42,44,45] и in vivo [21,53], свидетельствуют о нейропротективных свойствах этого препарата. Следует заметить, что эксперименты на животных имеют важное значение как для понимания патогенеза различных заболеваний, так и для оценки действия лекарственных препаратов. В частности, грызуны активно используются в качестве моделей процесса старения, поскольку у них нейробиологические основы старения сходны с нейрональными изменениями у людей [38]. На различных экспериментальных моделях было доказано положительное влияние церебролизина на способность к обучению и мнестические функции [33,34,41–45,56,72]. В частности, на крысах это продемонстрировали B. Hutter–Paier и соавт. [43], используя методику пассивного избегания. Эффект препарата носил дозо–зависимый характер, причем улучшение было более выраженным и более длительным у старых самок.
Одним из методов изучения способности обрабатывать пространственную информацию при старении у крыс является водный лабиринт. A. Gschanes и M.Windisch [38], используя эту методику, отметили уменьшение продолжительности латентного периода реакции выбора пути спасения под влиянием церебролизина, причем у самок это улучшение было более значительным. При исследовании двигательной активности, определяемой по скорости преодоления водной преграды, статистически значимое улучшение было только у самцов (у самок скорость плавания не изменилась).
Эксперименты на трансгенно измененных мышах, используемых для изучения процессов формирования b -амилоида при болезни Альцгеймера, показали способность церебролизина усиливать регенерацию синапсов и снижать уровень b -амилоида–42 [62]. Полученные данные позволили авторам сделать заключение о нейропротективном эффекте церебролизина на интрацеллюлярном уровне. Результаты этого исследования имеют принципиально важное значение, поскольку отложение b -амилоида является одним из ключевых моментов в патогенезе болезни Альцгеймера.
Было показано, что нейропротективный эффект церебролизина обусловлен антиапоптозными свойствами входящих в его состав пептидов и улучшением метаболизма нейронов под влиянием аминокислот [39,41,44]. В отличие от некроза, остро возникающего и пассивного процесса гибели клетки, характеризующегося ранним нарушением целостности клеточных мембран и увеличением объема клетки (что в конечном итоге приводит к гибели клетки), апоптоз является активным процессом [61]. Апоптоз, как форма программируемой гибели клетки, сопровождается гистологическими изменениями, такими как образование пузырьков в мембране клеток и конденсация хроматина. При апоптозе могут возникать характерные биохимические изменения, в частности, фрагментация межнуклеосомной ДНК.
В эксперименте было показано, что на фоне введения церебролизина уменьшается количество клеток с обусловленным апоптозом повреждением хроматина [39]. Один из механизмов антиапоптозной активности церебролизина связан с уменьшением повреждающего действия глутамата на нейроны [41]. Это обусловлено способностью пептидов, входящих в состав препарата, тормозить вызванный ишемией выброс глутамата, агонистически воздействуя на пресинаптические ГАМК–Б рецепторы.
Экспериментальное исследование, проведенное B.Hutter–Paier и соавт. [44], показало, что церебролизин обеспечивает защиту нейронов от отсроченной гибели, причем этот эффект носит дозо–зависимый характер. Полученные данные свидетельствуют о том, что одним из механизмов нейропротективного эффекта церебролизина является повышение пластичности нейронов, обусловленное предотвращением разрушения их цитоскелета. Таким образом, на клеточном уровне нейропротективный эффект церебролизина может быть связан с предотвращением повреждения дендритов.
M. Schwab и соавт. [67,68] на модели экспериментальной ишемии (окклюзия обеих сонных артерий у крыс) отметили, что после введения церебролизина показатели смертности у крыс в первые сутки после ишемии снижались с 31,7% до 17,6%. Это было связано с уменьшением цитотоксического отека и стабилизацией церебрального кровотока, преимущественно в задних отделах головного мозга. Введение церебролизина при ишемии также усиливало защитный эффект умеренной гипотермии (35°С). Кроме того, имеет значение еще один положительный эффект церебролизина – уменьшение образования в условиях ишемии/реперфузии свободных радикалов [70].
Следует заметить, что около 2% кислорода, используемого митохондриями, утилизируется неполностью. При этом образуются свободнорадикальные метаболиты О2, активно вступающие в химические реакции [12,31,37,59]. В норме избыточная продукция свободных радикалов компенсируется под влиянием ферментативных или неферментативных антиоксидантных систем, обеспечивающих поддержание гомеостаза.
В экспериментальной работе M.E. Gonzalez и соавт. [37] было показано, что церебролизин уменьшает выраженность оксидантного стресса, воздействуя на каталазу и супероксиддисмутазу. При этом летальность в группе получавших церебролизин экспериментальных животных (крыс) с повреждением септо–гиппокампального пути составила 18% по сравнению с 43% в контрольной группе. Отмеченные в экспериментальных исследованиях свойства церебролизина уменьшать неблагоприятные последствия ишемии находят и клиническое подтверждение [7,35].
На фоне действия церебролизина увеличивается уровень белка, ассоциированного с микротубулами–2 (англ. – microtubule associated protein–2, сокр. – MAP2) и снижается образование фосфорилированного тау–протеина [69,71]. Цитоскелетный белок MAP2 играет важную роль в жизнедеятельности нейронов. В основном этот белок локализован в дендритах, а его изменения являются одним из наиболее чувствительных и ранних индикаторов обусловленного ишемией повреждения клеток, поскольку предшествуют необратимым повреждениям нейронов. В эксперименте было показано, что добавление церебролизина, даже в небольшом количестве, к культуре клеток препятствует снижению уровня MAP2 в условиях ишемии [45,76]. Аналогичные данные были получены in vivo [69]. M. Schwab и соавт. [69] выявили, что наиболее значительно этот процесс выражен в области таламуса, гиппокампа и мезэнцефальных отделах. Авторы подчеркивают, что выявленный эффект церебролизина имеет важное значение в плане воздействия на ишемическую полутень, окружающую зону инфаркта головного мозга.
Церебролизин нормализует и нейротрансмиттерные нарушения. H. Xiong и соавт. [79,80] в эксперименте показали, что влияние препарата на структуры гиппокампа осуществляется путем непрямой (связанной с освобождением эндогенного агониста) стимуляции аденозиновых рецепторов. Аденозин является мощным тормозящим нейротрансмиттером, угнетающим выброс глутамата из пресинаптических терминалей. Конечным итогом этого процесса, также как и упоминавшееся выше воздействие церебролизина на ГАМК–ергическую систему, является торможение освобождения глутамата из пресинаптических терминалей и последующее уменьшение поступления ионов кальция в нейроны. Подобный механизм действия церебролизина может объяснить его способность замедлять прогрессирование нейродегенеративного процесса и воздействовать на эксайтотоксичность в условиях ишемии.
Учитывая значение ацетилхолинергических нарушений при болезни Альцгеймера, важным представляется отмеченное F. Akai и соавт. [21] нейротрофическое влияние церебролизина на холинергические нейроны гиппокампальной области. Авторы изучали эффект церебролизина на степень дегенерации денервированных в результате вмешательства холинергических нейронов медиальной перегородки у крыс и выявили достоверное увеличение времени жизнедеятельности клеток по сравнению с контрольной группой животных.
Экспериментальные данные дают основания для предположения о способности церебролизина увеличивать плотность синапсов и индуцировать нейрогенез в области гиппокампа [25,71,78]. При этом у экспериментальных животных отмечено существенное улучшение выполнения тестов, оценивающих мнестические функции и способность к обучению [71,78]. Эффект препарата характеризуется двухфазной модуляцией синаптической передачи – кратковременным ингибированием и последующим длительным усилением синаптической активности в области CA1 гиппокампа крыс [25], что связано с влиянием на пресинаптические аденозиновые рецепторы [79] и ГАМК–Б рецепторы [80]. M. Windisch и соавт. [78] отмечают, что улучшение выполнения тестов у экспериментальных животных коррелирует с достоверным повышением плотности синапсов в структурах гиппокампа (области CA1, CA3, зубчатая извилина) и энторинальной коре.
Одним из механизмов нейропротективного эффекта церебролизина является увеличение транспорта глюкозы через гематоэнцефалический барьер – из кровяного русла в паренхиму головного мозга, что было показано в целой серии работ, выполненных в США [26–30]. Глюкоза проникает через гематоэнцефалический барьер с помощью Na–независимого механизма, регулируемого геном–транспортером глюкозы GLUT1. Экспрессия гена – транспортера глюкозы GLUT1 в эндотелиальных клетках регулируется трофическими факторами. Имеются данные, что при болезни Альцгеймера уровень этого транспортного протеина снижается [54]. В работах, проведенных R.J. Boado [26,27,29], было выявлено, что церебролизин регулирует экспрессию гена–транспортера глюкозы GLUT1 на уровне посттранскрипционной стабилизации мРНК, а также специфично усиливает экспрессию этого гена в культуре клеток мозгового эпителия, увеличивая эффективность трансляции, причем это усиление носит дозо–зависимый характер. В последующей работе этого автора [30] было показано, что на фоне введения церебролизина в течение 7 дней у экспериментальных животных отмечается возрастание активности GLUT1, что сопровождается повышением транспорта глюкозы через гематоэнцефалический барьер. При этом отмечено достоверное снижение уровня гормонов, снижающих эту активность. В конечном итоге улучшается аэробный метаболизм [26–30,74]. Полученные данные объясняют положительный клинический эффект церебролизина не только при дегенеративных, но и при сосудистых заболеваниях головного мозга.
Доказательства эффективности церебролизина получены и по результатам клинических исследований. Следует заметить, что препарат обычно назначается в больших дозах – 20–30 мл/сут. внутривенно на изотоническом растворе натрия хлорида в течение 1 месяца ежедневно [9,16,20,63,64].
Улучшение когнитивных функций после терапии церебролизином было продемонстрировано в двойном слепом контролируемом исследовании, проведенном B.Kofler и соавт. [50]. Авторы применяли 20 мл препарата в течение 10 дней у пациентов как с сосудистой, так и первично–дегенеративной деменцией. Результаты завершенных в последнее время двойных слепых плацебо–контролируемых исследований, проведенных в Канаде [36,58], Южной Корее [23], а также в Германии [63–65], свидетельствуют о хорошей переносимости и статистически достоверном улучшении в состоянии пациентов с болезнью Альцгеймера после месячного курса лечения церебролизином в дозе 30 мл/сут. Положительный эффект проявлялся как в когнитивной сфере, так и в виде улучшения поведенческих характеристик больных. C.–Y.Bae и соавт. [23] отмечают, что по своей выраженности положительный эффект церебролизина сравним с эффектом центральных ингибиторов ацетилхолинэстеразы такрина, донепезила или метрифоната.
И.Ф.Рощина и соавт. [16] выявили у пациентов с болезнью Альцгеймера более выраженное улучшение состояния высших мозговых функций (в бoльшей мере – регуляторных, в меньший – операциональных) при терапии церебролизином и амиридином, чем только амиридином. Курс лечения церебролизином в этом исследовании проводился перед курсовой терапией амиридином.
E.Ruther и соавт. [63] в двойном слепом плацебо–контролируемом исследовании использовали церебролизин у 120 пациентов с болезнью Альцгеймера. Авторы выявили у обследованных больных улучшение когнитивных функций и активности в повседневной жизни, при этом сколь–либо значимых побочных явлений не было. Положительный эффект церебролизина сохранялся и после завершения курса терапии. Авторы, отмечая улучшение в состоянии больных через 3 месяца [64] и 6 месяцев [65] после завершения курса лечения, высказывают предположение о способности этого препарата замедлять прогрессирование болезни Альцгеймера. Механизмы подобного клинического эффекта могут быть связаны с экспериментально подтвержденным увеличением плотности синапсов в области гиппокампа и энторинальной коры [78].
Двойное слепое многоцентровое исследование, проведенное в Канаде [36], было специально направлено на оценку возможного влияния церебролизина на характер течения болезни Альцгеймера. Для этого эффект терапии оценивался не только непосредственно после окончания курса терапии, но также через 2 и 5 мес. Всего в исследование было включено 192 пациента с болезнью Альцгеймера (диагностика проводилась на основе критериев NINCDS–ADRDA), оценка по шкале MMSE составляла от 14 до 26 баллов. Проведенное исследование показало, что после курса терапии отмечается улучшение в состоянии больных, проявляющееся увеличением активности в повседневной жизни и уменьшением выраженности поведенческих расстройств. Полученные данные подтверждают способность церебролизина замедлять прогрессирование болезни Альцгеймера, поскольку даже после прекращения лечения состояние больных имело тенденцию к улучшению.
Ранее Н.В.Верещагин и соавт. [1], используя двойной слепой метод, изучали эффективность церебролизина у больных с мультиинфарктной деменцией. В исследование было включено 60 больных, которые получали 15 мл церебролизина на 100 мл физиологического раствора в течение 28 дней. После курса терапии у пациентов было отмечено улучшение абстрактного мышления и памяти по результатам теста Арнольда–Кольмана, положительная динамика ЭЭГ. G.F.Hebenstreit [40] в двойном слепом плацебо–контролируемом исследовании изучал эффект церебролизина в дозах 10 и 30 мл в течение 4 недель у 60 больных с сосудистой деменцией. Автор зафиксировал дозо–зависимое благоприятное влияние препарата на практическое мышление по результатом теста Арнольда–Кольмана. Была отмечена положительная динамика ЭЭГ. Кроме того, выявилось благоприятное влияние церебролизина на биохимические показатели: у пациентов, принимавших препарат, достоверно снизился уровень холестерина и триглицеридов.
После курса терапии церебролизином у пациентов как с сосудистой, так и с первично–дегенератичной патологией, параллельно улучшению когнитивных функций отмечается положительная динамика электроэнцефалографических параметров в виде уменьшения выраженности медленноволновой активности в дельта– и тета–диапазонах и усиления альфа–активности [13,20]. Для объективизации положительного влияния церебролизина у больных с мультиинфарктной деменцией О.И.Соловьев [18] применял компьютерное картирование ЭЭГ в контролируемом клиническом испытании. Было зафиксировано достоверное увеличение мощности ЭЭГ в широком частотном диапазоне (тета–, альфа–, бета–1 и бета–2). Помимо фоновой записи, проводилась функциональная проба, вызывающая легкую ишемию мозга, что позволило выявить повышение толерантности к ишемии у больных, получавших церебролизин, по сравнению с контрольной группой.
V.Lombardi и соавт. [52] провели изучение влияния однократного введения раствора церебролизина (30 мл) на когнитивные функции и биоэлектрическую активность головного мозга у здоровых пожилых. Было показано, что после введения церебролизина возрастает относительная мощность альфа–активности, причем этот эффект сохраняется до 6 часов после введения. Одновременно происходит генерализованное снижение медленноволновой дельта–активности. При этом обследованные лица достоверно лучше выполняли тесты, оценивающие память. Полученные данные свидетельствуют об активации даже после однократного введения церебролизина церебральных механизмов, связанных с мнестическими процессами и вниманием.
Ранее M.Funke и соавт. [35], используя гипервентиляцию в качестве модели церебральной ишемии (мозговой кровоток при этой пробе снижается до 50–60%, что в достаточной мере воспроизводит ситуацию при остром инсульте и, отчасти, при сосудистой деменции), показали, что церебролизин приводит к нарастанию мощности ЭЭГ, причем наиболее выраженные изменения были отмечены в теменных отделах. Этот эффект проявляется уже через 15 минут после инъекции препарата, достигает максимума через 2 часа и сохраняется в течение 8 часов после инфузии. Сразу после гипервентиляции и в первые четыре часа после нее в группе, получавшей плацебо, отмечено некоторое снижение кратковременной памяти, которое отсутствовало у лиц, получавших церебролизин. Основываясь на полученных данных, авторы подчеркивают, что электрофизиологические изменения, обусловленные введением церебролизина, отличаются от эффекта типичных ноотропных препаратов и соответствуют изменениям, характерным для нейропротекторов, обладающих антиглутаматергическими свойствами.
Церебролизин также используется при инсультах [3, 7,8,14,17,24,73]. K.Кlein [49] применял препарат у пациентов в остром периоде инсульта в дозе 20 мл на 500 мл раствора декстрана в течение 5 дней. Была отмечена положительная динамика общемозговой и очаговой неврологической симптоматики, повысились показатели выживаемости, улучшилось общее состояние больных. G.S.Barolin и соавт. [14,24,51] на большой группе больных с ишемическим инсультом показали, что чем раньше от начала инсульта вводится этот препарат, тем более благоприятно протекает реабилитационный период. D.Volc и соавт. [73] отметили наиболее существенное улучшение у больных более молодого возраста. Было показано, что у пациентов, получавших церебролизин, происходит более быстрое и существенное восстановление двигательных и когнитивных функций, они лучше справляются с необходимыми в повседневной жизни действиями.
Х. Димат [10] сообщает о благоприятном влиянии церебролизина на динамику неврологической симптоматики и параметры ЭЭГ у больных в остром периоде тяжелой черепно–мозговой травмы при применении препарата в дозе 60 мл внутривенно в течение 10 дней. Сходные данные ранее были получены F.Jelasic [46]. Имеются данные об эффективности церебролизина при тяжелой акинетической форме болезни Паркинсона. О.Шубрт [19] сообщает об удлинении «on»–периода и уменьшении побочных эффектов препаратов леводопы у таких больных после месячного курса терапии церебролизином. Кроме того, этот препарат также используется для коррекции побочных эффектов психотропных средств [15].
Еще одной сферой применения церебролизина является детская неврология. Препарат с успехом используется для лечения минимальной мозговой дисфункции [5], последствий закрытой черепно–мозговой травмы [11], ночного энуреза [6], гипоакузии [60].
В своем обзоре M.Windisch и соавт. [77] суммируют следующим образом механизмы действия церебролизина: нормализация функции нейронов, влияние на нейрональный окислительный метаболизм, активизация реакции спраутинга, нормализация нейротрансмиттерных нарушений и синаптической передачи. Под действием этого препарата, что подтверждается экспериментальными данными, происходит улучшение мнестических функций при различных типах повреждения. Пептиды, входящие в состав церебролизина, хорошо проникают через гематоэнцефалический барьер в фармакологически эффективных количествах, а их эффект обычно более выражен, чем эффект естественных нейротрофических факторов. Кроме воздействия на нейроны, препарат активирует микроглиальные элементы, уменьшает неблагоприятные эффекты факторов воспаления и воздействует на механизмы оксидантного стресса. Помимо этого, церебролизин улучшает транспорт глюкозы через гематоэнцефалический барьер. Таким образом, препарат обладает активным мультимодальным действием, направленным на целый ряд ключевых механизмов процесса нейродегенерации. Еще одним положительным свойством препарата является быстрое наступление положительного эффекта и его длительное сохранение после проведенного курса лечения.
1. Верещагин Н.В., Лебедева Н.В. Легкие формы мультиинфарктной деменции: эффективность церебролизина. //Сов. мед. –1991. –N.11. –С.6–8
2. Виленский Б.С. Инсульт. –СПб.: Медицинское информационное агентство, 1995. –288 с.
3. Виленский Б.С., Семенова Г.М., Широков Е.А. Применение церебролизина при ишемическом инсульте. //Журн. невролог. и психиатр. –1999. –Т.99, №.4. –С.65–69
4. Виндиш М. Церебролизин – новейшие результаты, подтверждающие разностороннее действие лекарства. //В кн.: Третий Международный Симпозиум по Церебролизину. –М., 1991. –С. 81–106
5. Громова О.А., Авдеенко Т.В., Бурцев Е.М. и соавт. Влияние церебролизина на оксидантный гомеостаз, содержание микроэлементов и электролитов у детей с минимальной мозговой дисфункцией. //Журн. невролог. и психиатр. –1998. –Т.98, №.1. –С.27–30
6. Грузман А.В., Левина И.Н. Эффект внутривенного введения церебролизина при резистентных формах ночного энуреза у детей. //Журн. невролог. и психиатр. –1998. –Т.98, №.11. –С.46
7. Гусев Е.И., Скворцова В.И. Ишемия головного мозга. –М.: Медицина, 2001.–328 с.
8. Гусев Е.И., Гехт А.Б., Гаптов В.Б., Тихопой Е.В. Реабилитация в неврологии. Учебн. пособие. –М., 2000. –52 с.
9. Дамулин И.В., Захаров В.В., Левин О.С., Елкин М.Н. Использование церебролизина в нейрогериатрической практике. /В сб.: Достижения в нейрогериатрии. Под ред. Н.Н.Яхно, И.В.Дамулина. –М.: ММА, 1995, Ч.1. – С.100–116
10. Димат Х. Церебролизин в терапии черепно–мозговой травмы. //В кн.: Третий Международный Симпозиум по Церебролизину. –М., 1991. –С.47–60
11. Заваденко Н.Н., Кемалов А.И., Петрухин А.С. и соавт. Лечение последствий закрытой черепно–мозговой травмы у детей: оценка эффективности церебролизина. //Невролог. журн. –2001. –Т.6, №.3. –С.38–42
12. Завалишин И.А., Захарова М.Н. Оксидантный стресс – общий механизм повреждения при заболеваниях нервной системы. //Ж. невролог. и психиатр. –1996. –Т.96, N.2. –С.111–114
13. Изнак А.Ф., Колыхалов И.В., Чаянов Н.В. и соавт. Влияние церебролизина на характеристики ЭЭГ при болезни Альцгеймера. /В сб.: Болезнь Альцгеймера: достижения в нейробиологии, диагностике и терапии. Тез. докл. –М., 1996. –С.46
14. Коппи С., Баролин Г.С. Применение церебролизина в терапии ишемического инсульта. //Журн. невролог. и психиатр. –1998. –Т.98, №.10. –С.30–33
15. Пантелеева Г.П., Бондарь В.В., Красникова Н.И., Раюшкин В.А. Церебролизин и магне В6 в терапии побочных эффектов психотропных средств. //Журн. невролог. и психиатр. –1999. –Т.99, №.1. –С.37–41
16. Рощина И.Ф., Колыхалов И.В., Селезнева Н.Д. и соавт. Влияние церебролизина на эффективность последующей терапии амиридином у больных с болезнью Альцгеймера (нейропсихологическое исследование). //Журн. невролог. и психиатр. –1999. –Т.99, №.12. –С.43–46
17. Скворцова В.И. Ишемический инсульт: патогенез ишемии, терапевтические подходы. //Невролог. журн. –2001. –Т.6, №.3. –С.4–9
18. Соловьев О.И. Нейротропное действие церебролизина по данным компьютеризированной топографии и визуального анализа ЭЭГ. //В кн.: Третий Международный Симпозиум по Церебролизину. –М., 1991. –С.61–70
19. Шубрт О. Опыт лечения церебролизином тяжелой акинетической формы болезни Паркинсона. //В кн.: Третий Международный Симпозиум по Церебролизину. –М., 1991. –С.71–80
20. Яхно Н.Н., Дамулин И.В., Захаров В.В. и соавт. Опыт применения высоких доз церебролизина при сосудистой деменции. //Тер. архив. –1996. –Т.68, №10. –С.65–69
21. Akai F., Hiruma S., Sato T. et al. Neurotrophic factor–like effect of FPF1070 on septal cholinergic neurons after transections of fimbria–fornix in the rat brain. //Histol. Histopathol. –1992. –Vol.7. –P.213–221
22. Appel S.H. Neuropeptides and Alzheimer’s disease. Potential role of neurotrophic factors. /In: Alzheimer’s Disease: Advances in Basic Research and Therapies. Editors: R.J.Wurtman et al. –Zurich, 1984. –P.275–291
23. Bae C.–Y., Cho C.–Y., Cho K. et al. A doudle–blind, placebo–controlled, multicenter study of Cerebrolysin in Alzheimer’s disease. //J. Am. Geriatr. Soc. –2000. –Vol.48. –P.1566–1571
24. Barolin G.S., Koppi S., Kapeller E. Old and new aspects of stroke treatment with emphasis on metabolically active medication and rehabilitative outcome. //EuroRehab. –1996. –N.3. –P.135–143
25. Baskys A., Wojtowicz M. Effects of brain tissue hydrolysate on synaptic transmission in the hippocampus. //Pharmac. Biochem. Behav. –1994. –Vol.49. –P.1105–1107
26. Boado R.J. Brain–derived peptides regulate the steady state levels and increase stability of the blood–brain barrier GLUT1 glucose transporter mRNA. //Neurosci. Lett. –1995. –Vol.197, N.3. –P.179–182
27. Boado R.J. Brain–derived peptides increase the expression of a blood–brain barrier GLUT1 glucose transporter reporter gene. //Neurosci. Lett. –1996. –Vol.220. –P.53–56
28. Boado R.J., Wu D., Pardridge W.M., Windisch M. In vivo administration of brain–derived peptides increases the transport of glucose from blood to brain. /In: XVI World Congress of Neurology. Buenos Aires, 1997. Abstracts. N. 2–07–06
29. Boado R.J. Molecular regulation of the blood–brain barrier GLUT1 glucose transporter by brain–derived factors. //J. Neural. Transm. –1998. –Vol.53 (Suppl.). –P.323–331
30. Boado R.J. In vivo upregulation of the blood–brain barrier GLUT1 glucose transporter by brain–derived peptides. //Europ. J. Neurol. –1999. –Vol.6, suppl.3. –P.37
31. Choi B.H. Oxidative stress and Alzheimer’s disease. //Neurobiol. Aging. –1995. –Vol.16. –P.675–678
32. Duma S., Mutz N. Wirsamkeit einer Peptid – Dextran – Kombination in der Behandlung von Schadel–Hirn–Verletzten. //Neuropsychiatrie. –1990. –B.4. –S.69–72
33. Francis–Turner L., Valouskova V. Nerve growth factor and nootropic drug Cerebrolysin but not fibroblast growth factor can reduce spatial memory impairment elicited by fimbria–fornix transection: short–term study. //Neurosci. Lett. –1996. –Vol.202. –P.193–196
34. Francis–Turner L., Valouskova V., Morky J. Long–term effect of NGF, b–FGF and Cerebrolysin on the spatial memory after fimbria–fornix lesion in rats. //J. Neural. Trasm. –1996. –Vol.47 (Suppl.). –P.277
35. Funke M., Fiehler J., Mewes I. et al. Dose–dependent effects of Cerebrolysin on EEG and short term memory of healthy volunteers during control and hyperventilation induced cerebral ischemia. //J. Neural. Transm. –1998. –Vol.53 (Suppl.). –P.385–398
36. Gauthier S. Results of a 6–month randomized placebo–controlled study with Cerebrolysin in Alzheimer’s disease. //Europ. J. Neurol. –1999. –Vol.6, suppl.3. –P.28
37. Gonzalez M.E., Francis L., Castellano O. Antioxidant systemic effect of short–term Cerebrolysin administration. //J. Neural. Transm. –1998. –Vol.53 (Suppl.). –P.333–341
38. Gschanes A., Windisch M. The influence of Cerebrolysin and E021 on spatial navigation of 24–month–old rats //J. Neural. Transm. –1998. –Vol.53 (Suppl.). –P.313–321
39. Hartbauer M., Hutter–Paier B., Skofitsch G., Windisch M. Antiapoptotic effects of the peptidergic drug Cerebrolysin on primary cultures of embryonic chick cortical neurons. //J. Neural. Transm. –2001. –Vol.108. –P.459–473
40. Hebenstreit G.F. Die Wirkung eines Aminosaure Peptide–Extraktes bei zerebralen Funktionsstorungen in der Gerontopsychiatriie. //Neuropsychiatrie. –1986. –B.1. –S.38–44
41. Hutter–Paier B., Grygar E., Windish M. Death of telencephalon neurons induced by glutamate is reduced by the peptide derivate Cerebrolysin. //J. Neural. Transm. –1996. –Vol.47 (Suppl.). –P.267–27
42. Hutter–Paier B., Fruhwirth M., Grygar E., Windisch M. Cerebrolysin protects neurons from ischemia–induced loss of microtubule–associated protein 2. //J. Neural. Transm. –1996. –Vol.47 (Suppl.). –P.276
43. Hutter–Paier B., Eggenreich U., Windisch M. Effects of two protein–free peptide derivates on passive avoidance behaviour of 24–month–old rats. //Arzneimittelforschung/Drug res. –1996. –Vol.46. –P.237–241
44. Hutter–Paier B., Steiner E., Windisch M. Cerebrolysin protects isolated cortical neurons from neurodegeneration after brief histotoxic hypoxia. //J. Neural. Transm. –1998. –Vol.53 (Suppl.). –P.351–361
45. Hutter–Paier B., Grygar E., Fruhwirth M. et al. Further evidence that Cerebrolysin protects cortical neurons from neurodegeneration in vitro. //J. Neural. Transm. –1998. –Vol.53 (Suppl.). –P.363–372
46. Jelasic F. Klinische Erfahrungen mit Cerebrolysin bei schweren hirnorganischen Prozessen. //Zeitschrift fur Allgemeinmedizin. –1976. –B.52. –S.1829–1831
47. Johannson B., Meyersson B. A physiological role of NGF in the brain? //Neuroendocrin. Lett. –1988. –Vol.10. –P.42–45
48. Khachaturian Z. Overview of drug treatment possibilities in Alzheimer’s disease. /In: Updating of Alzheimer’s Disease. Editors: M.Selmes et al. IIIrd Annual Meeting Alzheimer Europe. –Madrid: Alzheimer Espana, 1994. –P.98–102
49. Klein K. Erfahrungen mit einer rheologisch und metabilisch aktiven Wirkstoffkombination bei akuten zerebralen Ischamien. //Therapiewoche. –1985. –B.35. –S.2323–2330
50. Kofler B., Erhart C., Erhart P., Harrer G. A multidimensional approach in testing nootropic drug effects. //Arch. Gerontol. Geriatr. –1990. –Vol.10. –P.129–140
51. Koppi S., Barolin G.S. Hamodilutionstherapie mit nervenzellstoffwechsel–aktiver Therapie beim ischamischen Insult: ermutigende Resultate einer Vergleichsstudie. //Wien. Med. Wochenschr. –1996. –B.146, N.3. –S.41–48
52. Lombardi V., Ccabelos R., Perez P. et al. Cerebrolysin improves memory performance and the brain bioelectrical activity pattern in elderly humans. //Neurobiol. Aging. –2000. –Vol.21, N.1S. –P.S167
53. Masliah E., Armasolo F., Veinbergs I. et al. Cerebrolysin ameliorates performance deficits, and neuronal damage in apolipoprotein E–deficient mice. //Pharmacol. Biochem. Behav. –1999. –Vol.62. –P.239–245
54. Mooradian A.D., Chung H.C., Shan G.N. GLUT–1 expression in the cerebra of patients with Alzheimer’s disease. //Neurobiol. Aging. –1997. –Vol.18. –P.469–474
55. Orgogozo J.–M. Therapeutic Approaches in Alzheimer’s Disease. /In: Alzheimer’s Dementia. The 16th International Bayer Pharma Press Seminar. –Paris, 1997. –P.34–42
56. Paier B., Windisch M., Eggenreich U. Postnatal administration of two peptide solutions affect passive avoidance behaviour of young rats. //Behav. Brain Res. –1992. –Vol.51. –P.23–28
57. Palacios J.M., Mengod G., Probst A. Perspective of pharmacological treatment of dementia. /In: Cerebral Insufficiency: Trends in Research and Treatment. Vol.2. Edited by A.Carlson et al.. –Carnforth: The Parthenon Publishing Group, 1989. –P.93–110
58. Panisset M., Gauthier S., Moessler H., Windisch M. Treatment of Alzheimer’s disease: A randomized, double–blind, placebo–controlled trial with a neurotrophic agent. //Neurobiol. Aging. –2000. –Vol.21, N.1S. –P.S28
59. Prasad K.N., Cole W.C., Hovland A.R. et al. Multiple antioxidants in the prevention and treatment of neurodegenerative disease: analysis of biologic rationale. //Curr. Opin. Neurol. –1999. –Vol.12, N.6. –P.761–770
60. Pruszewicz A., Obrebowski A., Woznica B., Swidzinski P. Mozliwosci farmakologiczne leczenia niedosuchow odbiorczych u dzieci. // Otolaryngol. –1994. –Vol.48, N.1. –P.63–66
61. Reinprecht K., Hutter–Paier B., Crailsheim K., Windisch M. Influence of BDNF and FCS on viability and programmed cell death (PCD) of developing cortical chicken neurons in vitro. //J. Neural. Transm. –1998. –Vol.53 (Suppl.). –P.373–384
62. Rockenstein E., Mallory M., Mante M. et al. Effects of Cerebrolysin in human APP transgenic animal models of Alzheimer’s disease. //Neurobiol. Aging. –2000. –Vol.21, N.1S. –P.S168
63. Ruther E., Ritter R., Apecechea M. et al. Efficacy of peptidergic nootropic drug cerebrolysin in senile dementia of the Alzheimer’s type. //Pharmacopsychiat. –1994. –Vol.27. –P.32–40
64. Ruther E., Moessler H., Windisch M. The MAD–B Study: A randomized, double–blind, placebo–controlled trial with a Cerebrolysin in Alzheimer’s disease. //Neurobiol. Aging. –2000. –Vol.21, N.1S. –P.S28
65. Ruther E., Ritter R., Apecechea M. et al. Sustained improvements in patients with dementia of Alzheimer’s type (DAT) 6 months after termination of Cerebrolysin therapy. //J. Neural. Transm. –2000. –Vol.107. –P.815–829
66. Satou T., Imano M., Akai F. et al. Morphological observation of effects of Cerebrolysin on cultured neural cells. //Adv. Biosci. –1993. –Vol.87. –P.195–196
67. Schwab M., Schaller R., Bauer R., Zweiner U. Morphological effects of moderate forebrain ischemia combined with short–term hypoxia in rats – protective effects of Cerebrolysin. //Exp. Toxicol. Pathol. –1997. –Vol.49. –P.29–37
68. Schwab M., Bauer R., Zweiner U. Physiological effects and brain protection by hypothermia and Cerebrolysin after moderate forebrain ischemia in rats. //Exp. Toxicol. Pathol. –1997. –Vol.49. –P.105–116
69. Schwab M., Antonow–Schlorke I., Zweiner U., Bauer R. brain–derived peptides reduce the size of cerebral infarction and loss of MAP2 immunoreactivity after focal ischemia in rats. //J. Neural. Transm. –1998. –Vol.53 (Suppl.). –P.299–311
70. Sugita Y., Kondo T., Kanazawa A. et al. Protective effect of FPF 1070 (Cerebrolysin) on delayed neuronal death in the gerbil – detection of hydroxyl radicals with salicylic acid. //No To Shinkei. –1993. –Vol.45. –P.325–331
71. Tatebayashi Y., Lee M.H., Iqbal K., Grundke–Iqbal I. The peptidergic antidementia drug Cerebrolysin increases neurogenesis in the adult rat dentate gyrus and improves spatial learning and memory. //Neurobiol. Aging. –2000. –Vol.21, N.1S. –P.S42
72. Valouskova V., Francis–Turner L. Can Cerebrolysin influence chronic deterioration of spatial learning and memory? //J. Neural. Transm. –1998. –Vol.53 (Suppl.). –P.343–349
73. Volc D., Adler J., Goldsteiner H. et al. Therapeutic effects of Cerebrolysin in stroke patients during rehabilitation. //EuroRehab. –1998. –N.3–4. –P.21–28
74. Windisch M., Piswanger A. In vitro effects of peptide derivates and extracts from calf blood on the oxidative metabolism of brain, liver and heart muscle homogenates of the rat. //Drug Res. –1985. –Vol.35. –P.87–89
75. Windisch M., Albrecht E., Eggenreich U, Paier B. Neurotrophic effects of the nootropic drug cerebrolysin – a summary. //In: Third Int. Conference on Alzheimer’s Disease and Related Disorders. –Padova, 1992. –P.4–5
76. Windisch M., Fruhwirth M., Grygar E., Hutter–Paier B. Cerebrolysin normalizes MAP2 homeostasis after glutamate induced neuronal cell death. /In: XVI World Congress of Neurology. Buenos Aires, 1997. Abstracts. N.3–43–08
77. Windisch M., Gschanes A., Hutter–Paier B. Neurotrophic activities and therapeutic experience with brain derived peptide preparation. //J. Neural. Transm. –1998. –Vol.53 (Suppl.). –P.289–298
источник