Сегодня эндометриоз причисляется к наиболее распространенным заболеваниям женской половой сферы, вызывающих бесплодие. Он диагностируется примерно у 7% женщин, способных зачать и выносить ребенка. Часто среди бесплодных пациенток это заболевание может диагностироваться у каждой второй – четвертой. Эндометриоз и бесплодие, таким образом, тесно связаны между собой.
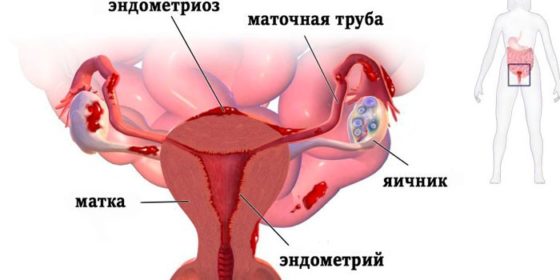
Эндометриоз матки – это гинекологическая патология, проявляющаяся в виде патологии клеток эндометрия, прорастание этой ткани в другие органы, нарушение функции матки, и в ряде случаев вызывающая бесплодие. Патологический процесс может охватывать ткань легкого, кишечник, мочевой пузырь. Измененные участки подвергаются всем трансформациям, происходящим в организме на протяжении менструального цикла. Болезнь характерна для женщин репродуктивного возраста. Наиболее часто встречается генитальная форма заболевания, что может приводить к бесплодию.
К наиболее распространенным причинам развития болезни относят такие факторы.
- Нарушения гормонального уровня. По мнению врачей, причина возникновения этого явления кроется в увеличении выработки эстрогенов. Вследствие гормонального дисбаланса у женщины нарушаются структуры слоя эндометрия.
- Ретроградная менструация. При этом состоянии менструальная ткань с яйцеклеткой вместо того, чтобы выйти через влагалище наружу, распространяется в маточную трубу. Затем она проникает в тазовую полость и начинает прорастать на внутренних органах. Маточная труба при этом воспаляется, ее ткань утолщается. Изолированное ее поражение встречается очень редко.
- Воспалительные заболевания матки.
- Пороки развития в яичниках, маточных трубах.
- Наличие воспалительных очагов на брюшине в результате распространения эндометриоидной ткани по сосудам.
- Неблагоприятная генетическая расположенность. При ее наличии в следующем поколении может отмечаться крайне неблагоприятное течение заболевания.
- Метаплазия, то есть стойкое превращение дифференцированных клеток одного типа такими же клетками другого типа.
- Нарушение работы иммунной системы.
- Неблагоприятная экологическая обстановка. Влияние загрязненного воздуха, воды, пищи при условии наличия в организме эндометриозных кист позволяет болезни прогрессировать далее, что в ряде случаев может являться причиной развития патологического разрастания слизистой матки.
Значительно повышают вероятность возникновения болезни такие факторы:
- воспалительные явления в области малого таза;
- опухолевые образования в матке;
- хирургические вмешательства, аборты, оперативные способы лечения эрозий шейки матки;
- роды с осложнениями;
- анемия;
- курение;
- злоупотребление алкоголем.
Эндометриоз может иметь разнообразную симптоматику: от практически бессимптомного протекания до развития характерных симптомов «острого живота». Наиболее распространенные симптомы болезни такие:
- болезненность внизу живота, области малого таза, пояснице разной интенсивности;
- усиление болей во время менструации;
- нарушение менструального цикла (у женщины появляются мажущие кровянистые выделения за несколько дней до и после месячных);
- увеличение продолжительности месячных;
- появление кровянистых выделений в межменструальный период;
- развитие бесплодия.
Если у женщины появились описанные симптомы, лечение эндометриоза и бесплодия должно осуществляться только после комплекса обследований. Диагностика бесплодия при эндометриозе является важнейшей мерой для определения репродуктивного здоровья женщины и оценки ее шансов стать матерью.
При диагностике проводятся такие обследования.
- Анализ на маркер СА-125. При рассматриваемом заболевании его уровень повышается.
- Влагалищное обследование. При этом виде диагностики обнаруживаются изменения эндометрия, бугристая поверхность увеличенной матки.
- УЗИ органов, находящихся в области малого таза. С его помощью можно увидеть эндометриоидные кисты яичников, наличие измененной ткани во внематочной области и предположить наличие разных форм аденомиоза.
- Кольпоскопия определяет локализацию, степень поражения матки. Врач обнаруживает кисты, участки эндометриозной ткани, которые визуализируются как объекты с измененным цветом, в зависимости от фазы цикла или как кровоточащие линейные зоны. После менструации из этих очагов может выделяться кровь.
- Магнито-резонансная томография позволяет обнаружить кисты яичника, поражения близлежащих органов.
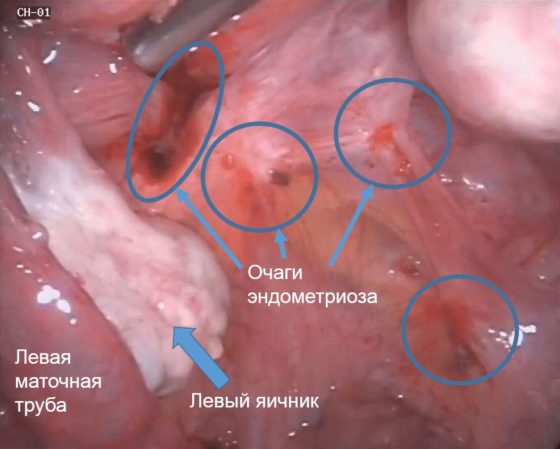
- Лапароскопия позволяет детально осмотреть брюшину, яичники, маточные трубы. На сегодня она является лучшим способом диагностики эндометриоза.
В значительном количестве случаев рассматриваемое заболевание способствует развитию бесплодия, так как патологически разросшийся внутренний слой матки может препятствовать нормальному выходу яйцеклетки. Это заболевание способствует выработке в больших количествах половых гормонов. В ряде случаев они способствуют появлению спаек.
Несмотря на нарушение нормального функционирования женской половой системы, забеременеть при эндометриозе возможно.
Причины бесплодия при эндометриозе состоят в том, что патологически увеличенная ткань яичников отрицательно влияет на работу яичников. Иногда она делает невозможным прикрепление плодного яйца к слизистой.
При тяжелом течении эндометриоза возникает спаечный процесс в органах малого таза. Из-за этого развивается непроходимость маточных труб, или трубное бесплодие. Из-за формирования эндометриозных кист яичники могут плотно прикрепляться к матке, что нарушает процесс образования яйцеклеток. Любые нарушения анатомии органов, расположенных в малом тазу, вызывают бесплодие.
Своевременное лечение эндометриоза повышает шансы на наступление беременности. Сегодняшние терапевтические методы эффективно устраняют воспалительные очаги и убирают спайки. Вероятность излечения бесплодия составляет более 50%.
Если эндометриоз поражает стенку матки, то по мере ее увеличения может случиться разрыв органа. Чтобы обнаружить опасность как можно раньше, женщине на протяжении всей беременности измеряют толщину стенки матки с помощью ультразвука. Во избежание потери ребенка на поздних сроках пациентке могут сделать кесарево сечение.
Выделение крови указывает на развитие патологического процесса во время беременности и служит показанием для проведения соответствующей терапии.
Если оплодотворение прошло успешно, это не означает, что можно расслабляться. У женщины существует высокая вероятность самопроизвольного прекращения беременности.
Иногда в организме женщины может случаться гормональный сбой. Из-за нарушения баланса гормонов в нем вырабатывается чрезмерное количество эстрогенов. При эндометриозе у женщин случается критическое уменьшение выработки прогестерона. При этом матка начинает сокращаться, что и приводит к выкидышу. Наибольшая угроза выкидыша бывает в первом триместре. По мере роста плаценты вероятность самопроизвольного аборта значительно снижается.
Целями лечения бесплодия являются удаление эндометриозных очагов, устранение болезненных ощущений, восстановление фертильности и недопущение рецидивов. Методы лечения заболевания выбираются в зависимости от стадии болезни, состоянии здоровья женщины.
Для угнетения гипоталамо-гипофизарных расстройств, если бесплодие связано с этим, назначают препараты половых гормонов. Это лечение является временным, и оно не может избавить пациентку от очагов заболевания. При наличии болевых ощущений выбор лекарственных средств зависит от возраста пациентки, выраженности нарушений менструального ритма, степени распространения патологических очагов, сопутствующих гинекологических и других хронических патологий.
Прием гормональных контрацептивов уместен как дополнительный метод комплексной терапии и для профилактики рецидивов. Наилучшие результаты можно получить после курса приема:
- Марвелона;
- Силеста;
- Регулона;
- Фемодена;
- Ярины и других средств.
Лекарствами выбора при медикаментозном лечении эндометриоза являются препараты Бусерелин, Трипторелин. Продолжительность приема составляет от 3 до 6 мес.
Показаниями для хирургического вмешательства являются:
- выраженные боли;
- разрыв кисты;
- назначение плановой операции по удалению маточных труб;
- бесплодие, спровоцированное эндометриозом.
При оперативном лечении бесплодия может осуществляться лапароскопия, лапаротомия, влагалищный доступ. Выбор метода лечения зависит от степени распространения и локализации патологических очагов. Иногда при наличии поверхностного поражения шейки матки возможно их удаление с помощью лазерного луча. При патологической менструации гистероскопия – осмотр полости матки делается обязательно, чтобы исключить развитие злокачественного процесса.
При глубоком расположении патологических очагов возможно удаление эндометриоза с помощью радиоволнового способа. Если диагностированы обширные формы заболевания, то перед операцией проводится медикаментозное лечение.
Различные методы терапии бесплодия при эндометриозе необходимы, потому что только в этом случае женщина сможет родить здорового ребенка. В качестве медикаментозного лечения прописываются оральные контрацептивы, содержащие необходимые для лечения гормоны.
При неэффективности гормональной терапии проводится хирургическая операция или решается вопрос о применении вспомогательных репродуктивных технологий.
При значительном снижении жизнеспособности яйцеклеток применяется экстракорпоральное оплодотворение. Женщинам, достигшим или перешагнувшим 40-летний рубеж, рекомендуется проведение интрацитоплазматической инъекции сперматозоида. При нормальной проходимости маточных труб применяется внутриматочная инсеминация.
Хотя эндометриоз в большинстве случаев осложняется бесплодием, женщине не стоит отчаиваться. Своевременное и эффективное лечение заболевания способствует излечению и рождению здорового малыша. Методы ЭКО значительно повышают шансы женщины стать матерью.
источник

Распространенность эндометриоза, как причины бесплодия, достигает 75%.
Этот диагноз гинекологи ставят довольно часто, однако женщины, как правило, так и остаются в неведенье – что именно у них обнаружено, почему это надо лечить и насколько опасно это состояние.
Для того чтобы понять, что такое эндометриоз, надо разобраться с тем, как происходит менструация и что такое эндометрий.
Полость матки изнутри выстлана слизистой оболочкой, которая называется эндометрий. Эта слизистая оболочка имеет сложную структуру, она состоит из двух слоев: первый – базальный, второй – функциональный.
Функциональный слой – это тот слой слизистой оболочки, который отторгается каждый месяц во время менструации (если беременность наступила, то именно в этот слой имплантируется оплодотворенная яйцеклетка).
Базальный слой – это слой, из которого каждый месяц вырастает новый функциональный слой. Каждый месяц под воздействием гормонов яичника в матке растет эндометрий, если беременность не наступила – эндометрий отторгается – это и есть менструация.
Практически у всех женщин менструальные выделения выходят не только наружу (через влагалище), но часть их также поступает по маточным трубам в брюшную полость.;
В норме, попавшие в брюшную полость менструальные выделения, быстро уничтожаются защитными клетками брюшной полости. Но кусочки отторгнувшегося эндометрия обладают способностью прикрепляться к различным тканям, имплантироваться в них и приживаться.
Таким образом, эндометриоз – это такое заболевание, когда слизистая оболочка полости матки (эндометрий) в виде отдельных очагов располагается вне полости матки, а в разных местах женского организма: чаще всего на брюшине (то, чем выстлана брюшная полость изнутри и чем покрыт кишечник).
Эти фрагменты эндометрия могут находиться на яичниках, маточных трубах, связках матки, кишечнике, а также могут приживаться в других местах вне брюшной полости. После того, как эти фрагменты эндометрия приживаются, они начинают существовать так же, как они это делали, находясь в полости матки – то есть под воздействием гормонов яичников эти очаги увеличиваются в размере, а потом часть их отторгается во время менструации.
При наличии эндометриоидных очагов на брюшине или стенке кишечника, которые хорошо иннервируются, могут возникать боли. Именно поэтому ведущим симптомом эндометриоза являются боли в животе во время менструации.
В клинической практике существуют случаи эндометриоза почек, мочеточников, мочевого пузыря, легких, кишечника.
Большинство исследователей считают, что причиной развития эндометриоза связано с изменением в гормональном фоне женщины, а именно изменения уровня эстрогенов. Теория увеличения уровня эстрогенов как причины развития эндометриоза лежит в основе большинства лечебных методик, которые применяются на сегодняшний день при эндометриозе.
Возможным доказательством этой теории является тот факт, что эндометриоз постепенно исчезает у женщин, которые вступают в период постменопаузы. Нет менструации – нет эндометриоза (если только женщина не получает заместительную гормональную терапию, на фоне которой эндометриоз может сохраняться).
Данная теория была выдвинута еще в 1920 году Джоном Сампсоном. Он сделал предположение, что менструальная ткань, которая представляет собой слущенную внутреннюю оболочку матки, вместо выхода через влагалище, попадает в маточные трубы (так называемый обратный, ретроградный отток) и выходит в полость таза, где она оседает на различных органах и начинает прорастать.
Однако, данная теория развития эндометриоза не объясняет, причины возникновения этой болезни у женщин, перенесших гистерэктомию, или перевязку маточных труб, а также почему эндометриоз может развиться и у мужчин, получающих лечение эстрогенами по поводу опухолевых заболеваний предстательной железы.
Ученые обнаружили, что у родственников первой степени больше риск развития эндометриоза. Кроме того, при наличии наследственной предрасположенности в следующем поколении отмечается более тяжелое течение эндометриоза.
Фрагменты эндометриоидной ткани могут распространяться по кровеносным и лимфатическим путям в другие области организма. Этот механизм объясняет то, как эндометриоз появляется в таких отдаленных областях, как легкие, головной мозг, кожа или глаза.
Метаплазия — это процесс превращения одной нормальной ткани в другой тип нормальной ткани. Есть предположение, что эндометриоидная ткань способна превращаться в другую ткань находясь вне матки.
У некоторых, больных эндометриозом женщин, отмечаются определенные нарушения работы иммунной системы.
Некоторые исследования показали, что определенные экологические факторы способны влиять на развитие эндометриоза, путем воздействия токсичных продуктов на продукцию половых гормонов и иммунную систему. Данная теория также остается спорной.

Иногда эти очаги сливаются и инфильтрируют ткани, особенно часто это бывает за маткой на ее связках. В этой области могут образовываться довольно большие массы эндометриоидной ткани (такое состояние называется «ретроцервикальный эндометриоз»).
Если ткань эндометрия попадает в яичник, то в нем могут образовываться эндометриоидные кисты, их еще называют «шоколадными кистами». Это доброкачественные кисты яичника. Их содержимым накапливается в процессе «миниатюрных менструаций» те очаги эндометриоза, которыми выстланы стенки кисты.
Эндометриоз характеризуется разнообразием клинической картины: от бессимптомного течения заболевания до такого синдрома, как «острый живот». К наиболее частым клиническим симптомам диагностики относятся:
- боли в нижних отделах живота и поясничной области различной интенсивности, усиление боли во время менструаций, полового акта;
- боль, отдающая в прямую кишку, нарушения менструации (появление мажущих коричневых выделений за 1-3 дня и в течение 1-7 дней после менструации);
- увеличение объема менструации и ее продолжительности;
- появление межменструальных кровянистых выделений.
Отдельным проявлением эндометриоза является бесплодие. Считается, что эндометриоз может приводить к бесплодию за счет двух механизмов:
Образование спаек, которые нарушают проходимость маточных труб. Спайки при эндометриозе образуются за счет того, что на месте очагов эндометриоза на брюшине фактически постоянно происходит воспалительный процесс, который стимулирует образование спаек. Спайки нарушают проходимость маточных труб, что приводит к бесплодию.
Кроме того, наличие эндометриоидных очагов на яичниках нарушает процесс созревания яйцеклетки, процесс ее выхода (овуляции), может изменяться качество яйцеклеток, на фоне этого нарушается оплодотворение и имплантация оплодотворенной яйцеклетки.
При эндометриозе в крови повышается его уровень. Но этот маркер специфичен и не отражает степень выраженности эндометриоза.
Ультразвуковое исследование органов малого таза
С помощью этого метода можно обнаружить наличие наружного эндометриоза, в частности эндометриоидных кист яичников, эндометриоидной ткани в позадиматочном пространстве при таком состоянии как ретроцервикальный эндометриоз, выявить ЭХО-признаки и предположить наличие диффузной и узловой форм аденомиоза ( аденомиоз- эндометриоз с локализацией в мышечном слое матки).
Информативный метод для определения диффузной формы аденомиоза. Позволяет увидеть слизистую оболочку полости матки, устья маточных труб и эндометриоидные ходы, которые выглядят как темно-красные точки на фоне бледно-розовой слизистой.
Магнитно-резонансная томография (МРТ)
МРТ имеет значительные преимущества по сравнению с УЗИ-исследованием для диагностики эндометриоза при наличии кист яичника или поражения соседних органов (кишечника, мочевого пузыря, прямокишечно-влагалищной перегородки). Но в связи с тем, что в большинстве случаев размеры гетеротопий на брюшине не превышают нескольких миллиметров в диаметре, этот метод не имеет высокой диагностической ценности для большинства больных.
На сегодняшний день «золотым стандартом» диагностики наружного генитального эндометриоза является лапароскопия, когда есть возможность подробно осмотреть висцеральную и париетальную брюшину, маточные трубы, яичники, пузырно-маточное и прямокишечно-маточное углубление, широкие связки.
Эндометриоз может предполагаться как одна из причин бесплодия в браке. Этот вопрос до сих пор остается открытым. Есть доказанные факты, указывающие на то, что после лапароскопической деструкции очагов эндометриоза наступает беременность, которая до этого не наступала. В настоящее время существует много мнений и тактик ведения пациентов.
В каждой конкретной клинической ситуации следует разбираться отдельно. Всегда очень важен индивидуальный подход к ведению пациента.
Если у пары есть другие, помимо эндометриоза причины, которые могут приводить к бесплодию – следует скорректировать их и постараться получить результат. Если результата не будет – планировать лапароскопию.
Существует два способа лечения: удаление очагов эндометриоза или временное выключение менструальной функции для того, чтобы очаги эндометриоза атрофировались. Часто эти два способа комбинируют.
Для полного выключения менструальной функции чаще всего используют препараты группы «агонисты ГнРГ». Назначают их обычно на курс от 3 до 6 месяцев. На их фоне у женщины пропадают менструации, и наступает состояние, похожее на менопаузу со всеми характерными симптомами: приливы, лабильность настроения и т. д., но это состояние обратимое, то есть после последней иньекции препарата через 1-2 месяца менструации восстанавливаются и состояние «менопаузы» проходит. За это время очаги эндометриоза, лишенные гормональных стимулов, подвергаются атрофии.
Так же в качестве медикаментозного лечения эндометриоза применяются препараты гестагенов диеногест. Диеногест, является производным нортестостерона, характеризуясь антиандрогенной активностью, оказывает мощный прогестагенный эффект in vivo. составляющей примерно одну треть от активности ципротерона ацетата.
Диеногест воздействует на эндометриоз путем подавления трофических эффектов эстрогенов в отношении нормально расположенного и эктопического эндометрия, вследствие снижения продукции эстрогенов в яичниках и уменьшения их концентрации в плазме.
При продолжительном применении вызывает атрофию эндометриоидных очагов.
Следует заметить, что медикаментозная терапия эндометриоза назначается врачом с учетом индивидуальной клинической ситуации пациентки и требует регулярного наблюдения со стороны лечащего врача.
Если нарушения, обусловленные эндометриозом, приводят к развитию бесплодия, то хирургическое лечение таких состояний обычно имеет хорошие результаты.
Для хирургического лечения эндометриоза используется лапароскопия.
Во время операции производится разрушение очагов эндометриоза с помощью различных энергий. Удаляются эндометриоидные кисты из яичников. Если эндометриоз привел к появлению спаек – спайки разрушаются, и проверяется проходимость маточных труб.
Эффект такой операции, к сожалению, длится не долго. Через некоторое время очаги эндометриоза появляются снова, вновь развиваются спайки. Если беременность планировалась – необходимо сразу после операции предпринимать попытки забеременеть. Важно помнить: чем больше прошло времени после операции, тем выше вероятность того, что эффект, достигнутый операцией, уже прошел, вероятнее всего вновь образовались спайки и появились новые очаги эндометриоза.
Если женщина не планировала беременность, то для того, чтобы эффект операции сохранился дольше сразу после операции пациенткам назначается курс медикаментозной терапии, после окончания курса основного лечения она может начать принимать контрацептивы для дальнейшей профилактики рецидивов.
Эндометриоз – одна из частых причин бесплодия. При этом заболевании можно самостоятельно забеременеть, если очаги имеют небольшие размеры. Поэтому на начальном этапе используется лишь консервативная терапия и выжидательная тактика. Если же беременность не наступает, может потребоваться хирургическое лечение и применение вспомогательных репродуктивных технологий.
Эндометриоз – это не только препятствие на пути к наступлению беременности, но ещё и повышенный риск ее прерывания на ранних сроках. Высокая частота выкидышей при этом заболевании связана главным образом с двумя факторами:
- Повышение сократительной активности миометрия, что вызвано усиленным образованием простагландинов F2α в очагах эндометриоза.
- Частой сопутствующей недостаточностью лютеиновой фазы.
В силу этих обстоятельств каждая женщина с эндометриозом должна наблюдаться у врача и получать медикаментозную поддержку, а не пускать свою беременность на самотёк. В противном случае она с высокой вероятностью может прерваться в первом триместре.
1. Факторы, которые ухудшают отток менструальных выделений во время менструации – способствуют развитию эндометриоза:
2. Профилактика внутриматочных вмешательств:
3. Хорошей профилактикой эндометриоза является прием гормональных контрацептивов в пролонгированном режиме (63+7), и регулярное посещение гинеколога раз в полгода.
источник
Бесплодие – наверно самый печальный диагноз для любой женщины, планирующей беременность. Невозможность завести собственного ребенка может подкосить даже самых сильных. Само по себе бесплодие не является заболеванием, так называют отсутствие беременности у женщины в течение года при активной половой жизни.
Всемирная Организация Здравоохранения (ВОЗ) выявила неутешительную статистику, по которой ясно, что около 8-10 % супружеских пар сталкиваются с проблемой бесплодия. Однако стоит понимать, что бесплодие подразделяется на несколько видов, оно может быть абсолютным или относительным (временным) на фоне каких-либо заболеваний. При относительном бесплодии стоит сосредоточиться на избавлении от первопричины, тогда беременность станет возможна. Понятие бесплодие относится именно к паре, поэтому проблема может быть как у женщины, так и у мужчины 1 .
Одной из самых часто встречающихся причин бесплодия является эндометриоз (разрастание ткани эндометрия), который обнаруживается у 7 % всех женщин. В группе женщин с бесплодием эндометриоз присутствует у каждой третьей женщины. Между бесплодием и эндометриозом существует тесная связь, которая порой может прятаться за другими заболеваниями репродуктивной системы женщины 1 .
Диагноз «эндометриоз» означает, что внутренний слой стенки матки (эндометрий) начал разрастаться и вышел за отведенное природой место. Эндометрий может врастать в саму матку или поражать всю репродуктивную систему женщины. Существует два основных типа развития – внутренний и наружный тип. В редких случаях эндометрий может начать расти не в половой системе, а, например, в брюшной полости 2 .
Эндометриоз достаточно загадочное заболевание, и не все врачи схожи во мнении из-за каких конкретно причин оно возникает. Самой вероятной причиной является сбой в гормональной системе женщины. Изменение в выработке определенных гормонов провоцирует рост эндометрия. Другие причины являются более редкими, и их можно расценивать, как факторы, способствующии развитию эндометриоза 2 :
- стресс;
- высокая физическая нагрузка;
- заболевания матки;
- хирургические вмешательства;
- инфекции и воспалительные процессы;
- ослабленная иммунная система;
- застой крови в матке;
- генетическая предрасположенность;
- аборты;
- заболевания внутренних органов, особенно печени;
- метаболический синдром и ожирение.
Логично, что разрастание эндометрия не ведет ни к чему хорошему. Поражаются внутренние и внешние органы половой системы, проявляется множество осложнений. Ввиду того, что основной причиной является нарушенный гормональный фон, начинает сбиваться нормальный менструальный цикл и процесс овуляции, что уже само по себе ведет к проблемам зачатия. Однако забеременеть все еще возможно, и зафиксировано множество случаев беременности при диагностированном эндометриозе 2 .
Чаще всего врачи говорят про абсолютное бесплодие, когда эндометриоз поражает яичники и маточные трубы. Подобный вид эндометриоза классифицируется как перитонеальный вид. Увеличенная ткань эндометрия в яичниках отрицательно влияет на функциональность органа, оплодотворенной яйцеклетке тяжело продвигаться по маточной трубе и еще тяжелей прикрепиться к стенке матки в дальнейшем. Также в маточных трубах из-за разросшейся ткани возможно образование спаек, что ведет к полной непроходимости. Нередко эндометриоз может вызывать развитие эндометриоидной кисты в яичнике, что опять ведет к бесплодию. Список достаточно обширный, стоит знать, что любое нарушение в работе репродуктивной системы может привести к бесплодию 3 .
Когда врач ставит диагноз бесплодие или возникают подозрения на бесплодие, первым делом, женщину проверяют на наличие эндометриоза. При его выявлении и своевременном лечении шансы забеременеть значительно возрастают. Главное — не упустить момент и помнить, что эндометриоз может вызвать абсолютное бесплодие.
источник
Детородные проблемы. Эндометриоз и бесплодие тесно взаимосвязаны: первое приводит к снижению фертильности, второе становится причиной возникновения эндометриоидной болезни.
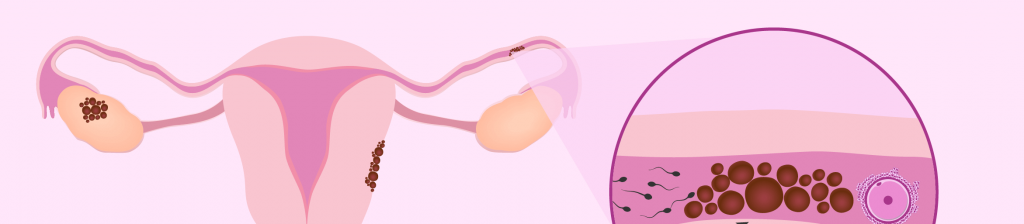
Одна из частых причин проблем с зачатием и вынашиванием плода. Эндометриоз и бесплодие – «сестры» по несчастью: связь между ними настолько тесная, что порой невозможно понять, что было первично. У женщины, обратившейся к врачу с жалобами на сложности с наступлением беременности, находят различные патологические состояния. Эндометриоидная болезнь, как эндокринные нарушения и маточные факторы, находятся в первых рядах причин бесплодного брака. Причем, оба варианта женских проблем могут формироваться параллельно из одних причинных факторов и на схожем эндокринном фоне.
Гинекологические заболевания всегда оказывают негативное влияние на детородную способность женщины. При обследовании выявляются следующие изменения в тканях:
- Утолщение стенок и воспалительная реакция в просвете с закупоркой маточных труб;
- Формирование множественных спаек в малом тазу, в том числе, и вокруг яичников;
- Снижение яичниковых функций (эндокринный дисбаланс);
- Изменение процессов овуляции за счет появления кист в яичниках.
Эндометриоз и бесплодие – это практически всегда трубно-перитонеальный фактор, являющийся основной причиной для невозможности зачатия.
Не получается забеременеть. Лечение не приносит желаемого результата. Психоэмоциональные и эндокринные причины провоцируют эндометриоидную болезнь. Выделяют следующие факторы:
- Нарушение баланса эстрогенов и гестагенов;
- Расстройство на уровне гипофизарных гормонов;
- Неадекватная ежемесячная овуляция;
- Гиперпластические процессы в эндометрии;
- Снижение местной иммунной защиты;
- Появление и рост миоматозных узлов в матке;
- Формирование кистозных полостей в яичниках (поликистоз или кистомы);
- Общие эндокринные нарушения, приводящие к проблемам в щитовидной железе и молочных железах.
Чем дольше нет желанной беременности, и чем агрессивнее лечение при бесплодии, тем выше вероятность возникновения генитального эндометриоза.
Оптимальный вариант избавления от обеих проблем. Эндометриоз и бесплодие можно излечить, если создать максимум условий для успешного зачатия. Если помочь женщине выносить и родить малыша. Лучший вариант лечения – желанная беременность, роды и длительное кормление грудью. Учитывая частое наличие трубно-перитонеальных спаек, единственный путь для наступления беременности – экстракорпоральное оплодотворение, перед которым надо выполнить:
- Хирургический этап терапии (лапароскопическое рассечение спаек);
- Лекарственная подготовка полости матки;
- Эндокринная коррекция на прегравидарном этапе.
Подсадка эмбриона должна сопровождаться сохраняющей терапией – необходимо точно и аккуратно выполнять назначения врача в 1 триместре беременности, чтобы обеспечить нормальную приживаемость плода. Следует помнить, что вынашивание беременности и родоразрешение могут осложняться проблемами у мамы и малыша.
Генитальный эндометриоз и бесплодие часто сопровождают друг друга, еще больше усложняя жизнь женщины. Лечение должно быть комплексным, а наступившая беременность и успешное вынашивание – оптимальные критерии выздоровления.
источник
В настоящее время эндометриоз признают одним из наиболее распространённых гинекологических заболеваний, связанным с бесплодием. Среди фертильных женщин эндометриоз диагностируют примерно у 6–7%, тогда как среди пациенток, страдающих бесплодием, его частота может достигать 20–48%.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ БЕСПЛОДИЯ ПРИ ЭНДОМЕТРИОЗЕ
К вероятным причинам инфертильности при эндометриозе можно отнести следующие:
- трубное бесплодие: органическое — при нарушении анатомии маточных труб, вызванном эндометриозным процессом; функциональное — изза воздействий на маточные трубы медиаторов воспаления и цитокинов, образующихся в очагах эндометриоидных гетеротопий, а также на фоне гормонального дисбаланса (постоянной относительной гиперэстрогении в сочетании с прогестероновой недостаточностью во 2й фазе цикла), сопровождающего эндометриоз;
- перитонеальное бесплодие — на фоне эндометриоза возникает при спаечном процессе в малом тазу под влиянием тех же причин (локальное воспаление в области эндометриоидных гетеротопий), что и органическое трубное бесплодие;
- эндокринное бесплодие (ановуляция, НЛФ, синдром лютеинизации неовулировавшего фолликула на фоне неадекватное функционирования оси «гипоталамус–гипофиз–яичники») — обусловливается сопровождающим эндометриоз дисбалансом женских половых стероидов (абсолютным или относительным повышением эстрогенов) и потенцированием образования пролактина, нарушающих гонадотропиновую регуляцию функции яичников;
- иммунные реакции, вызывающие угнетение процесса имплантации бластоцисты в эндометрий или поражение сперматозоидов активированными макрофагами.
Кроме того, бесплодию при эндометриозе в определённой степени способствует и нарушение половой функции изза выраженной диспареунии, затрудняющей регулярную половую жизнь и/или обеспечение полноценного полового акта.
У пациенток с эндометриозом при наступлении у них беременности отмечают тенденцию к повышению частоты выкидышей на ранних сроках. Нельзя исключить, что это может быть связано с активацией сократительной функции миометрия, индуцируемой простагландинами F2α, поскольку данные простагландины усиленно образуются в очагах воспаления в зоне эндометриоидных гетеротопий. Кроме того, поскольку эндометриозу достаточно часто сопутствует НЛФ (см. ниже), это также увеличивает риск ранних репродуктивных потерь и частоту вторичного бесплодия.
Наиболее очевидная причина бесплодия при эндометриозе маточных труб — прорастание гетеротопий в их просвет. При этом наблюдают диффузное утолщение стенок труб и сужение их просвета до полной окклюзии, также возникает деструкция ампулярного и истмикоампулярного отделов, что создаёт непреодолимое препятствие для прохождения мужских гамет на уровне маточных труб. Следует, однако, отметить, что изолированное поражение эндометриозом маточных труб встречают крайне редко и поэтому основной причиной анатомической непроходимости маточных труб оказывается их облитерация на фоне спаечного процесса в малом тазу. Спайки и сращения при перитонеальном бесплодии могут и не сопровождаться окклюзией маточных труб, обусловливая инфертильность другими причинами.
Полагают, что при перитонеальном бесплодии периовариальные спайки могут затруднять разрыв стенок преовуляторного фолликула и/или препятствовать пассажу яйцеклетки из яичника в ампулярный отдел маточной трубы.
Развитие связанного с ТПБ спаечного процесса при эндометриозе провоцирует воспалительная реакция брюшины, вызванная периодическими менструальноподобными кровоизлияниями в эндометриоидные гетеротопии и накоплением в тканях серозногеморрагического экссудата, способствующего отложению больших масс фибрина. При этом фибринолиз оказывается ослабленным изза наблюдаемого в условиях гипоксии торможения образования активатора плазминогена и снижения продукции плазмина. Постоянная гипоксия изза нарушений микроциркуляции, вызванной микротромбообразованием на фоне избыточного отложения фибрина, поддерживает угнетённое состояние фибринолитической системы и тем самым способствует дальнейшему накоплению фибрина и прогрессированию спаечного процесса, обусловливающего ТПБ.
В ряде случаев трубная непроходимость при эндометриозе может носить чисто функциональный характер. Известно, что физиологическая активность (характер тонуса и направленность мышечных сокращений) маточных труб коррелирует с циклической секрецией половых стероидов. В норме тонус и возбудимость труб в фолликулиновой фазе цикла резко повышены, тогда как в лютеиновую фазу они снижаются и при этом регистрируют проперистальтическую волну сокращения, продвигающую яйцеклетку от ампулы трубы к матке. Согласно наблюдениям разных исследователей, у каждой второй пациентки с эндометриозом и анатомически проходимыми трубами регистрируют дискоординированную сократительную деятельность труб. Причиной этого может быть нарушение баланса половых стероидов, заключающееся в типичной для эндометриоза абсолютной или относительной базальной гиперэстрогении, а также пиковых выбросах эстрадиола в лютеиновой фазе и дисбаланс в образовании простагландинов, оказывающих на маточные трубы как спастическое (F2α), так и расслабляющее воздействие (Е).
При эндометриозе относительно высокая базальная концентрация эстрадиола может быть связана с тем, что эндометриоидные имплантаты обладают (в отличие от нормального эндометрия) возросшей ароматазной активностью, недостаточно контролируемой ФСГзависимыми механизмами. Ароматаза — фермент, способствующий образованию эстрогенов из андрогенов — в основном эстрона из андростендиона и, в меньшей степени, эстрадиола из тестостерона. В норме активность ароматазы контролируют несколько механизмов, из которых в приложении к яичникам важнейшим служит регуляция, осуществляемая ФСГ. Поэтому у здоровых женщин репродуктивного возраста на фоне относительно низкого уровня ФСГ в ранней фоллиновой фазе цикла отмечают и относительно низкую концентрацию эстрадиола, обусловленную снижением ароматазной активности в яичниках.
У больных эндометриозом в ранней фолликулиновой фазе, несмотря на такие же, как у здоровых лиц, значения ФСГ, базальный уровень эстрадиола оказывается более высоким изза повышенной активности ароматазы в эндометриоидных имплантатах. Высокий уровень ароматазной активности в очагах эндометриоза может поддерживаться стимулирующим влиянием на этот фермент простагландинов Е, усиленно образующихся под влиянием некоторых цитокинов (ИЛ1β, фактор некроза опухолейα), интенсивно синтезирующихся в зоне воспаления в очагах эндометриоза. В свою очередь, локальное возрастание эстрадиола и эстрона, обусловливаемое повышенной ароматазной активностью, также способствует усиленному образованию простагландинов Е. Это обеспечивает самоподдержание процесса усиленной продукции эстрогенов в очагах эндометриоза и фактически делает его независимым от циклических колебаний ФСГ, служащих в норме основным активатором ароматазной активности в яичниках. И чем более обширна площадь и выраженней глубина эндометриозных поражений, тем в большей степени проявляют себя описываемые процессы.
Произошедшее в последние годы выяснение патологической значимости отклонений (повышения) активности ароматазы и вызываемой этим ферментом абсолютной и/или относительной гиперэстрогении у больных с эндометриозом обусловило обоснование использования ингибиторов ароматазы (анастрозол, летрозол) в качестве антиэстрогенных средств для терапии как самого эндометриоза, так и для восстановления естественной фертильности при этом заболевании. В России такие препараты ещё не получили распространения в клинической практике для лечения именно эндометриоза, хотя они уже достаточно долго используются как антиэстрогенные средства при терапии эстрогензависимых опухолей (анастрозол, летрозол).
Дисбаланс половых гормонов, вызывающих функциональное трубное бесплодие, может быть следствием нарушения уровня и секреции гонадотропинов. При эндометриозе разных локализаций можно наблюдать недостаточные пиковые подъёмы ЛГ, а также беспорядочные выбросы ЛГ и ФСГ в лютеиновую фазу, сопровождаемые нарушением нормальной динамики образования гормонов яичников с преобладанием продукции эстрогенов.
Помимо гиперэстрогении и дисбаланса гонадотропинов другой предпосылкой для дискоординированной деятельности маточных труб при эндометриозе служит нарушение продукции и соотношения между простагландинами Е и F2α, которое характеризуется относительным возрастанием спастических эффектов простагландинов F2α. Причиной этого становится сам воспалительный процесс, в условиях которого наблюдают усиление метаболизма арахидоновой кислоты и активацию образования простагландинов всех классов в постоянно меняющихся соотношениях, не соответствующих их нормативным значениях в физиологических условиях.
В некоторых случаях (по разным данным, от 3,5 до 37%) бесплодие при эндометриозе имеет явно ановуляторное происхождение или связано с НЛФ, что подтверждается при оценке овуляторной функции и/или измерении уровня прогестерона во 2й фазе цикла. Одной из вероятных причиной этого может становиться базальная гиперэстрогения, спровоцированная повышенной ароматазной активностью в эндометриоидных тканях. Относительно высокий уровень эстрогенов в 1й фазе цикла по принципу обратной связи обусловливает либо торможение продукции ФСГ (замедляется созревание фолликулов), либо способствует тенденции к преждевременному пику ЛГ (следствием этого становится лютеинизация неовулировавшего фолликула), либо сопровождается хаотичными колебаниями ФСГ и ЛГ (подобный дисбаланс гонадотропинов во 2й фазе цикла ведёт к НЛФ, характеризующейся задержкой трансформации эндометрия из пролиферативной фазы в секреторную на фоне относительной прогестероновой недостаточности).
Повышенный уровень эстрогенов при эндометриозе может провоцировать и гиперпролактинемию, наблюдаемую у отдельных больных. Связь гиперэстрогении с гиперпролактинемией находит подтверждение в экспериментальных наблюдениях, позволивших установить, что эстрогены способны усиливать секрецию пролактина, не только стимулируя пролактофоры в гипофизе, но и блокируя секрецию дофамина и его агонистов. В свою очередь, возникающая на фоне эндометриоза гиперпролактинемия может оказывать следующие эффекты.
- Под влиянием избытка пролактина тормозится влияние гонадотропинов на стероидогенез в яичниках за счёт конкурентного связывания пролактина с рецепторами к ФСГ и ЛГ. При эндометриозе в этом случае в большей степени будет ослабляться продукция прогестерона, так как уровень эстрогенов остаётся достаточно высоким за счёт их продолжающегося активного образования в эндометриоидных гетеротопиях под влиянием ароматазы. Данный механизм служит очевидной предпосылкой для НЛФ.
- Повышение уровня пролактина тормозит гонадотропинсекретирующую функцию гипофиза, блокируя спонтанный пик секреции ЛГ. Последствием таких изменений становится хроническая ановуляция.
- Избыток пролактина снижает чувствительность гипоталамуса к эстрогенам, что приводит к нарушению цирхорального ритма секреции гипоталамического ГнРГ, т.е. к гипоталамогипофизарной дисфункции, последствием которой может быть как хроническая ановуляция, так и НЛФ. В дополнение к описанным вероятным механизмам инфертильности при эндометриозе некоторые исследователи добавляют ещё и иммунную теорию. Согласно иммунологической концепции бесплодия при эндометриозе, на фоне этого заболевания можно отметить следующие иммунопатологические процессы.
- Продукты тканевой деградации, образующиеся при циклической трансформации эндометрия, не выводятся полностью из организма (в норме их выведение обеспечивает отторжение слизистой оболочки во время менструации), а фагоцитируются и резорбцируются тканевыми макрофагами, окружающими очаги эндометриоза. Это способствует индукции аутоиммунных реакций против тканей эндометрия, содержащих такие макрофаги. Последствием воздействия аутоантител может стать повреждение рецепторного аппарата эндометрия, обеспечивающего нидацию оплодотворённой яйцеклетки.
- В условиях воспаления локально образующиеся биологически активные вещества и цитокины активируют перитонеальные макрофаги, которые препятствуют реализации функции сперматозоидов за счёт их фагоцитоза и/или инактивации цитотоксическими медиаторами.
Современный подход к лечению бесплодия при наружном генитальном эндометриозе состоит в первоначальной попытке восстановления естественной фертильности с использованием средств (хирургических и/или гормональных), применяемых для лечения собственно самого эндометриоза и его осложнений (анемии, болевого синдрома). При этом также предусматривают устранение сопутствующей патологии, сопровождающей эндометриоз (например, овуляторных нарушений, перитонеальных спаек и др.). При сохраняющемся в течение 1–2 лет бесплодии на фоне такой терапии рекомендуют переходить к лечению с использованием ЭКО. Инфертильным пациенткам старше 38 лет процедуру ЭКО следует назначать сразу же, причём независимо от формы и тяжести эндометриозного процесса. Как безальтернативный метод преодоления бесплодия ЭКО исходно рекомендуют инфертильным пациенткам с аденомиозом, ретроцервикальным эндометриозом и перитонеальным эндометриозом IV степени (см. ниже).
При хирургическом лечении перитонеального эндометриоза выбор метода и доступа к гетеротопическим очагам зависит от локализации и распространённости патологического процесса. В основном для оперативных вмешательств используют лапароскопию, но при тяжёлых формах эндометриоза применяют и лапаротомический доступ.
При выявлении во время лапароскопической операции наружного генитального (перитонеального) эндометриоза I–II степени достаточно интраоперационной диатермогоагуляции очагов эндометриоза без последующей гормональной терапии. При наружном генитальном эндометриозе III степени после хирургической коррекции (лапароскопическим или лапаротомическим доступом) показано применение гормональной терапии на протяжении не более 3 мес и у пациенток не старше 38 лет. Гормональную терапию проводят агонистами ГнРГ или даназолом. Препараты агонистов ГнРГ используют в количестве не более 3 инъекций. Даназол назначают в дозе 40 мг/сут в непрерывном режиме не более 3 мес.
После выполненного хирургического лечения перитонеального эндометриоза возможно восстановление естественной фертильности в течение 1–2 лет. В этом периоде целесообразно проведение контролируемой индукции овуляции для повышения частоты овуляторных циклов. В случае отсутствия беременности в указанные сроки необходимо направить пациентку на программу ЭКО.
Диагностируемый при лапароскопии наружный генитальный эндометриоз IV степени служит показанием к безальтернативному использованию ЭКО, т.е. при такой выраженности эндометриозного процесса результаты хирургического лечения (его влияние на естественную фертильность) не прослеживают.
При наличии у пациентки с бесплодием эндометриоидных (шоколадных) кист яичников выполняют экономные операции, ставящие задачей удаление кистозных образований с минимальным повреждением здоровых тканей яичников. В настоящее время ведётся дискуссия о необходимости резекции яичников при небольших эндометриоидных кистах, поскольку такие операции малоэффективны для восстановления естественной фертильности и при этом неизбежно оказывают негативное влияние на фолликулярный резерв яичников. Последнее может стать существенной помехой для последующего успешного использования ЭКО, назначаемого пациенткам с эндометриозом после безуспешной попытки восстановления естественной фертильности.
При сочетании у больных бесплодием наружного (перитонеального) и внутреннего эндометриоза тактика ведения пациенток для достижения спонтанной беременности такова же, как и при наличии у них только наружного генитального эндометриоза. При неэффективности такого лечения пациенток направляют на ЭКО. При бесплодии, связанном только с аденомиозом, больным изначально рекомендуют ЭКО, поскольку при внутреннем эндометриозе восстановление естественной фертильности с помощью гормонального или эндохирургического лечения представляется бесперспективным.
Аналогичным образом ЭКО как безальтернативный способ преодоления бесплодия изначально рекомендуют и инфертильным пациенткам с ретроцервикальным эндометриозом. Лечение собственно самого ретроцервикального эндометриоза, ставящее задачей устранение болевого синдрома и нарушения функций смежных органов, представляется достаточно длительным и сложным и при этом фактически не влияющим на вероятность восстановления естественной фертильности. Поэтому гормональное и/или хирургическое лечение клинических проявлений ретроцервикального эндометриоза целесообразно начинать лишь после применения ЭКО.
При эндометриозе шейки матки при эктоцервикальном расположении гетеротопий лечение заключается в аппликации на них раствора солковагина©, электро или радиокоагуляции, лазерной вапоризации или криодеструкции поражённых участков. При эндоцервикальном эндометриозе можно применять радиокоагуляцию или лазерную вапоризацию очагов, конизацию шейки матки.
источник
Установлено, что 30-40% больных эндометриозом страдают бесплодием. С другой стороны у 6-25% бесплодных женщин выявляют эндометриоз. Риск бесплодия заметно выше при наружном, чем при внутреннем генитальном эндометриозе.
В.П. Баскаков с соавт. (1998) выделил следующие основные факторы, влияющие на репродуктивную функцию больных эндометриозом:
нарушение в гипоталамо-гипофизарно-яичниковой системе, приводящее к ановляции и/или недостаточности желтого тела;
синдром лютеинизации неовулировавшего фолликула;
повышение количества макрофагов в перитонеальной жидкости с усилением фагоцитоза сперматозоидов;
снижение и дискоординация сократительной активности маточных труб при сохраненной их проходимости;
задержка секреторной трансформации эндометрия;
нарушение цитоплазматического связывания прогестерона и усиление действия андрогенов на эндометрий, ухудшающее условия для нидации эмбриона;
иммунные нарушения с развитием аутоспермоиммунизации;
спаечный процесс в малом тазу и непроходимость маточных труб.
Следует заметить, что часть факторов, могут быть способствующими возникновению и развитию эндометриоза. К ним отнесятся: нарушение в гипоталамо-гипофизарно-яичниковой системе, приводящее к ановуляции и/или недостаточности желтого тела, синдром лютеинизации неовулировавшего фолликула, гиперпролактинемия и т.д. Повышение активности макрофагов приводит к пролиферации клеток эндометрия, попавших на брюшину.
Таким образом, бесплодие при эндометриозе не во всех случаях рассматривается как следствие этого заболевания. Оно может быть обусловлено сопутствующими и предшествующими эндометриозу патологическими состояниями репродуктивной и иммунной систем. Значит эндометриоз рассматривается не как непосредственная причина бесплодия, а как маркёр того, что данная женщина относится к группе высокого риска по нему.
Анамнез (типичные жалобы на боли во время менструации, постоянное боль ноющего характера внизу живота и в пояснице, нарушение менструального цикла по типу полименореи, семейный, сексуальный, длительное и безуспешное лечение «воспаления»)
При бимануальном исследовании: увеличение матки, неровная поверхность, плотная консистенция, болезненность при исследовании.
Гистеросальпингография с водорастворимым контрастом проводится на 5-7 день менструального цикла – наличие законтурных теней.
КТ и МРТ для определения границ поражения.
Эндометриоидные кисты: плотная капсула, размеры 10-12 см, гипоэхогенное содержимое с наличием мелкодисперсной взвеси.
Эндометриоз матки: в миометрии — участки повышенной эхогенности, неравномерность и зазубренность границ в мио- и эндометрии, округлые анэхогенные включениядо 5 мм в диаметре, при узловых формах – жидкостные полости до 30 мм в диаметре.
Кольпоскопия – для диагностики эндометриоза шейки матки.
Гистероскопия – идентифицируют эндометриоидные ходы, грубый рельеф стенок в виде хребтов и крипт. Гистероскопическая классификация степени распространенности эндометриоза (В.Г. Брусенко, 1977)
I стадия — рельеф стенок не изменен, эндометриоидные ходы в виде глазков темно-синего цвета кровоточащие. Стенки матки при выскабливании обычной плотности;
II – рельеф стенок матки неровный, имеет вид продольных или поперечных хребтов или разволокненной мышечной ткани, просматриваются эндометриоидные ходы. Стенки матки ригидные, полость матки плохо растяжима, при выскабливании стенки матки плотнее чем обычные;
III – на внутренней поверхности матки определяются выбухания различной велечины без четких контуров. На поверхности выбуханий иногра видны открытые или закрытые эндометриоидные ходы. При выскабливании неровная поверхность, ребристость, стенки матки плотные, характерен хруст.
источник
Наружный генитальный эндометриоз (НГЭ) встречается у 5–10% женщин репродуктивного возраста. Частота выявления этого заболевания при лапароскопии, в том числе проводимой с целью уточнения причины бесплодия, составляет 45–55%. Среди обращающихся в центры вспомогательных репродуктивных технологий для проведения ЭКО более 35 % пациенток имеют наружный генитальный эндометриоз. При выработке плана ведения больных бесплодием, ассоциированным с эндометриозом, следует учитывать возраст женщины, продолжительность бесплодия, наличие боли и стадию заболевания.
Несмотря на углубленные исследования проблемы бесплодия, обусловленного эндометриозом, сформированы отдельные гипотетические механизмы взаимосвязи этих состояний, к которым относят изменение нормальной анатомии тазовых органов, эндокринные нарушения, патологические гормональные и клеточно-опосредованные функции эндометрия, изменение функции париетальной и висцеральной брюшины, отсутствие овуляции, гиперэстрогения, хроническое воспаление и иммунные расстройства. При эндометриозе среди выявленных молекулярных механизмов бесплодия следует отметить многоуровневое негативное влияние эндометриоза на последовательные этапы формирования ооцитов, процессы оплодотворения, раннего эмбриогенеза и имплантации. Фолликулогенез при наличии наружного генитального эндометриоза характеризуется нарушениями стероидогенеза, синтеза простагландинов, присутствием повышенного количества иммунокомпетентных клеток (B-лимфоцитов, NK-клеток, измененным соотношением моноцитов − макрофагов).
Провоспалительные изменения фолликулярной жидкости оказывают влияние на оогенез, при этом фиксируют удлинение фолликулиновой фазы, уменьшение размера доминантного фолликула и активацию апоптоза клеток фолликула. На процесс оплодотворения может оказывать негативное влияние измененный состав перитонеальной жидкости, которая нарушает подвижность сперматозоидов, вызывает активацию апоптоза сперматозоидов, препятствует адекватной акросомальной реакции и прикреплению к яйцеклетке. В перитонеальной жидкости больных эндометриозом повышено содержание активированных макрофагов, ИЛ-1, туморонекротического фактора (ТНФ), протеаз, антиэндометриальных 17 аутоантител и лимфоцитов.
Эндометриоз оказывает особое негативное влияние на ранние этапы эмбриогенеза, при этом возможны аномалии дробления, ядерные и цитоплазматические нарушения, аномальный хетчинг, эпигенетическое репрограммирование эмбриона и функциональная незрелость. Нарушение восприимчивости эндометрия в условиях эндометриоза влияет на процесс имплантации и так называемое «эндометриальное бесплодие».
В последнее время уделяется особое внимание эпигенетическим механизмам бесплодия при эндометриозе: показано, что гиперметилирование HOXA10 и HOXA11 генов, ответственных за рост и пролиферацию de novo, децидуализацию эндометрия, приводит к резистентности к прогестерону в эутопическом эндометрии. Таким образом, эндометриоз приводит к альтерации функции ооцита, сперматозоида, эмбриона, эндометрия вследствие дефектного синтеза факторов роста, рецепторов, что приводит к нарушению трансдукции.
Прогрессирование эндометриоза ухудшает прогноз наступления беременности. Показания к проведению экстракорпорального оплодотворения (ЭКО) и переноса эмбриона (ПЭ) при эндометриозе − освобождение гамет и эмбрионов от негативного влияния провоспалительных агентов перитонеальной жидкости. Хирургическое лечение повышает частоту наступления беременности. Кроме того, в ходе лапароскопии подсчитывают ряд показателей индекса фертильности при эндометриозе (Endometriosis fertility index (EFI), предложенного G.D. Adamson. EFI является простым и надежным клиническим инструментом, фактически единственной изученной классификационной системой, имеющей прогностическое значение. С помощью него можно предсказать время наступления беременности у больных эндометриозом после хирургического лечения, использовать выжидательную тактику у пациенток с хорошим прогнозом и не тратить попусту время и сразу же переходить к процедурам вспомогательных репродуктивных технологий при неблагоприятном прогнозе.
Комбинированное лечебное воздействие хирургического вмешательства:
- эндоскопическая диагностика, биопсия, оперативное вмешательство с удалением пораженной ткани (кист яичников, лазеро-, крио- термодеструкция очагов эндометриоза, разделение спаек) с максимальным сохранением овариальной ткани (овариального резерва);
- медикаментозное воздействие с достижением антигонадотропного эффекта;
- контроль за эффективностью лечения.
Медикаментозное лечение бесплодия, связанного с эндометриозом:
- если больной эндометриозом показано ЭКО, аГнРГ в комбинации с возвратной гормональной терапией в течение 3–6 месяцев лечения перед его проведением, то это повышает частоту наступления беременности;
- если медикаментозное лечение бесплодия, связанного с эндометриозом в виде гормонального подавления, неэффективно, то его не следует предлагать пациентке.
Длительность медикаментозного лечения эндометриоза определяется:
особенностями клинической картины заболевания (характер болевого синдрома, выраженность нарушений менструального цикла, состояние репродуктивной функции);
конечной целью лечения (улучшение качества жизни и здоровья в целом, наступление беременности).
Кумулятивная частота наступления беременности, в течение первого года ожидаемого зачатия колеблется от 50 до 20% при I–II стадии НГЭ и снижается на 4% каждый последующий год. Отказ от выжидательной тактики и проведение внутриматочной инсеминации спермой мужа/донора значительно увеличивают частоту наступления беременности и родов, особенно при использовании гонадотропинов для стимуляции овуляции. Подавление функции яичников после хирургического лечения с целью восстановления репродуктивной функции при I–II стадии НГЭ неэффективно и может быть предложено только перед проведением процедур вспомогательных репродуктивных технологий.
Удаление или уничтожение (аблация) эндометриоидных очагов в сочетании с адгезиолизисом с целью улучшения фертильности при минимальной и умеренной степени эндометриоза более эффективны, чем диагностическая лапароскопия. Операция должна быть выполнена специализированной бригадой хирургов с учетом необходимости сохранения овариального резерва и оптимизации объема операции.
Показания к использованию ВРТ непосредственно после оперативного лечения эндометриоза:
- сочетание НГЭ с трубно-перитонеальным фактором;
- субфертильная сперма мужа;
- возраст женщины более 35 лет;
- безуспешность других методов лечения.
Риск рецидива не должен являться причиной отказа от использования методов ВРТ после хирургического лечения, так как даже при III–IV стадии заболевания рецидив наружного генитального эндометриоза сравнительно редко возникает после стимуляции суперовуляции в программе ЭКО.
При эндометриоидных кистах яичников важно рассмотреть желание пациентки сохранить фертильность, чтобы определить степень вмешательства и при необходимости сохранить яичники и их функцию. У пациенток, не заинтересованных в беременности, целесообразно начать терапию КОК (лучше в непрерывном режиме) после хирургического удаления эндометриодных кист яичников. Лапароскопическая цистэктомия у больных бесплодием при установленном диагнозе рекомендована при размере кист более 2 см с целью уточнения диагноза, уменьшения риска инфекции, улучшения доступа к созревающим фолликулам при ЭКО, исключения отрицательного воздействия содержимого кисты на процесс овуляции и оплодотворения, что очень важно, с целью исключения злокачественного процесса − при любых размерах образования. Важно учитывать высокую вероятность снижения овариального резерва после оперативного лечения кист яичников. Оперативное вмешательство на яичниках с доказанным гистологическим диагнозом в анамнезе – может служить основанием для назначения гормональной терапии без повторного хирургического вмешательства (при небольших размерах кист или эндометриозе брюшины). Необходимо полное обследование – онкомаркеры, УЗИ с доплерографией для соблюдения онкологической настороженности.
Преимущества использования аГнРГ в схемах стимуляции суперовуляции у больных генитальным эндометриозом:
- более синхронное созревание фолликулов;
- повышение показателей имплантации;
- более частое наступление беременности при проведении ЭКО и ПЭ.
При выполнении программы ЭКО и ПЭ у больных наружным генитальным эндометриозом предпочтение следует отдавать схемам стимуляции суперовуляции с использованием ежедневно вводимых препаратов а-ГнРГ.
Факторами, повышающими эффективность реализации программы ЭКО и ПЭ у пациенток с наружным генитальным эндометриозом, являются:
- двухэтапное комбинированное (хирургическое и медикаментозное) лечение заболевания до проведения программы ЭКО при III–IV стадии распространения;
- отказ от выжидательной тактики и проведение ЭКО и ПЭ непосредственно после завершения лечения женщинам с агрессивным рецидивирующим течением заболевания в возрасте старше 35 лет, со сниженными функциональными резервными возможностями яичников и при сочетании НГЭ с аденомиозом.
Таким образом, генитальный эндометриоз в зависимости от локализации и стадии распространения оказывает негативное влияние на активность процессов фолликуло-, оогенеза и раннего эмбриогенеза. Наличие наружного генитального эндометриоза III-IV стадии распространения, оперативное вмешательство на яичниках (при наличии кистозных форм в момент обследования), снижение их функциональных резервных возможностей и сочетание наружного генитального эндометриоза с аденомиозом любой стадии распространения значительно ухудшают эффективность реализации программы ЭКО и ПЭ. Следует помнить, что для больных эндометриозом тяжелой формы, у которых беременность наступила с использованием процедур вспомогательных репродуктивных технологий, характерны высокие акушерские риски: преждевременные роды, преэклампсия, замедление внутриутробного развития плода, предлежание плаценты. Получены убедительные клинические данные в пользу переноса одного, а не двух и более эмбрионов у таких женщин, поскольку многоплодная беременность существенно повышает риск невынашивания.
Хирургический этап лечения бесплодия при наличии эндометриоза заключается, прежде всего, в восстановлении нормальных анатомических взаимоотношений органов малого таза и удалении эндометриоидных кист яичников. Допустимо проведение только коагуляции очагов эндометриоза, расположенных вблизи мочеточника, сосудов и на стенках полых органов без их тотального иссечения. Это позволяет снизить риск развития тяжелых осложнений у пациенток, основной жалобой которых является бесплодие. Необходимо проведение тщательного сальпингоовариолизиса, гемостаза и проверки проходимости маточных труб. Целесообразно использовать противоспаечные барьеры для предотвращения развития трубно-перитонеального бесплодия. Нецелесообразно проведение повторных операций с целью восстановления естественной фертильности. Это неоправданно затягивает продолжительность лечения в целом и снижает эффективность ЭКО. При планировании ЭКО хирургическое лечение, предусматривающее удаление эндометриоидных кист и проведение сальпингэктомии при необратимых изменениях маточных труб, осуществляют в качестве подготовки. Спорным и не всегда оправданным является удаление обширного эндометриоидного позадишеечного инфильтрата или эндометриоза мочевого пузыря при отсутствии болевого симптома как этапа подготовки к ЭКО. Это значительно повышает риск развития послеоперационных осложнений, но при этом не оказывает существенного влияния на частоту наступления беременности. При хирургическом лечении необходимо использовать лапароскопический доступ, исключением могут быть только тяжелые формы эндометриоза либо экстрагенитальные заболевания, являющиеся противопоказанием к проведению лапароскопии. Важным компонентом хирургического лечения эндометриоза является предотвращение образования спаек путем минимизации травмирования тканей.
Основные принципы хирургического лечения с позиций доказательной медицины:
- Лапароскопия является предпочтительным хирургическим доступом («золотой стандарт») при лечении эндометриоза независимо от тяжести и степени распространения патологического процесса вследствие лучшей визуализации очагов благодаря их оптическому увеличению, минимальной травматизации тканей и более быстрой реабилитации пациенток, чем после лапаротомии.
- Лечебно-диагностическая лапароскопия с удалением очагов эндометриоза обеспечивает более значительное уменьшение интенсивности ассоциированных с эндометриозом болей по сравнению с диагностической лапароскопией.
- Эндометриомы яичников у женщин с тазовой болью должны быть удалены хирургическим путем при лапароскопии.
- У пациенток репродуктивного возраста при сохранении максимального объема непораженной ткани яичников принципиально важно полностью удалить капсулу кисты, что значительно снижает риск развития рецидивов в отличие от других методик (пункция, дренирование кисты, алкоголизация и уничтожение капсулы путем воздействия энергии различных видов).
- Очаги инфильтративного эндометриоза ректовагинальной перегородки, как правило, могут быть удалены лапароскопическим или комбинированным лапароскопически-влагалищным доступом, при необходимости в сочетании с одновременной резекцией пораженного участка стенки прямой кишки или в едином блоке с маткой (у женщин, незаинтересованных в беременности). При вовлечении в эндометриоидный инфильтрат толстой кишки в области ректовагинальной перегородки с характерными клиническими проявлениями (дисменорея, диспареуния, дисxезия) иногда следует выполнить резекцию кишки. Критериями для принятия решения о резекции кишки являются размер очага поражения более 2–3 см, степень вовлечения окружности кишки (более 1/3 окружности), глубина инвазии в мышечный слой 5 мм и более. При отсутствии показаний к резекции кишки возможно иссечение только эндометриоидного инфильтрата c использованием органосберегающей методики «shaving». Хирургическое лечение инфильтративных форм эндометриоза с вовлечением толстой кишки, мочевого пузыря и мочеточников необходимо проводить исключительно в специализированных экспертных лечебных центрах с применением мультидисциплинарного подхода (уровень доказательности IIIa). Выполнение резекции кишки или мочевого пузыря должен осуществлять хирург, имеющий сертификат о праве на проведение подобных операций (колоректальный хирург, уролог и т.д.).
- Радикальным методом лечения аденомиоза можно считать лишь тотальную гистерэктомию (экстирпация матки с придатками), которая может быть выполнена путем лапароскопии. При осуществлении гистерэктомии одновременно следует удалить все видимые эндометриоидные очаги, при этом билатеральная сальпингоофорэктомия может способствовать более эффективному купированию боли и уменьшению вероятности выполнения повторного оперативного вмешательства, однако вопрос об удалении яичников следует обсуждать с каждой пациенткой индивидуально.
источник